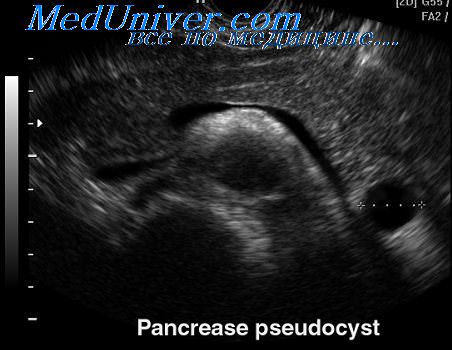
Псевдокиста поджелудочной железы что
Существует множество хирургических операций, используемых для лечения псевдокист поджелудочной железы. Выбор метода операции зависит от анатомических особенностей и имеющейся патологии, а также от общего состояния пациента. Необходимо учитывать и такие факторы, как размер и локализация псевдокисты, состояние ее стенки, ее взаимоотношения с желудком или двенадцатиперстной кишкой, наличие осложнений (быстрый рост с угрозой разрыва кисты или прорыв ее в брюшную полость, активное кровотечение, вызванное эрозией артерии или разрывом псевдоаневризмы, псевдоаневризма без кровотечения, массивное нагноение псевдокисты, возраст и общее состояние пациента и т. д.).
Формирование анастомоза между кистой и пищеварительным трактом желудком, гощей кишкой или двенадцатиперстной кишкой — используется наиболее часто и дает наилучшие результаты. Другие операции — наружное дренирование псевдокисты под контролем УЗИ или компьютерной томографии, марсупиализация, резекция поджелудочной железы, комбинация медикаментозной терапии и хирургического вмешательства (эмболизация кровоточащей артерии или ее окклюзия путем катетеризации артерии, выполняемой во время хирургического вмешательства, и т. д.) — используются реже. Все это придает особое значение полному дооперационному обследованию больных с псевдокистами поджелудочной железы, которое позволяет разработать наиболее подходящий план оперативного вмешательства в каждом отдельном случае.
Обязательным является рентгенологическое исследование грудной клетки из-за возможности левостороннего или двустороннего плеврального выпота. Необходимо выполнить также рентгенологическое исследование верхних отделов желудочно-кишечного тракта, чтобы определить взаимоотношения псевдокисты с желудком, двенадцатиперстной кишкой и кишечником. Ультразвуковое исследование важно не только для диагностики кисты, но и для наблюдения в динамике за изменением ее размеров, а также для оценки состояния стенки кисты и установления наличия желчных конкрементов или расширения желчных протоков. Если возможно, необходимо выполнить компьютерную томографию, чтобы получить еще более точные данные. В некоторых случаях, в дополнение к УЗИ, для выявления желчных камней можно выполнить холецистографию. Можно выполнить чрескожную чреспеченочную холангиографию. особенно при наличии расширения желчных протоков или желтухи. Полезной бывает также эндоскопическая ретроградная холангиопанкреатография, но ее выполняют с предельной осторожностью, т.к. она может привести к инфицированию желчных путей. Иногда при эндоскопической ретроградной холангиопанкреатографии удается законтрастировать проток поджелудочной железы и псевдокисту. Наличие сообщения между протоком поджелудочной железы и псевдокистой предполагается во всех случаях, но наглядно продемонстрировать его не всегда возможно, вероятно, из-за того, что это соединение действует подобно клапану.
Если псевдокиста осложняется активным кровотечением, очень важно выполнить селективную артериографию чревного ствола и верхней брыжеечной артерии, чтобы установить источник кровотечения и принять решение о наиболее адекватном оперативном вмешательстве с учетом анатомических особенностей. Некоторые авторы полагают, что всех пациентов с псевдокистами поджелудочной железы необходимо подвергать селективной ангиографии даже при отсутствии кровотечения, для того чтобы выявить псевдоаневризмы, которые могут кровоточить в послеоперационном периоде. Важно помнить, что для развития стенки псевдокисты требуется около шести недель: за это время она должна достаточно окрепнуть для удержания швов. Иногда стенка псевдокисты формируется раньше, но быть абсолютно уверенным в этом трудно; часто несостоятельность швов бывает вызвана незрелостью стенки псевдокисты. Чтобы определить степень зрелости стенки псевдокисты до операции, кроме клинической картины следует ориентироваться на данные компьютерной томографии, ультразвукового исследования, а также на уровень «остаточной амилазы» в крови.
30-40% псевдокист поджелудочной железы спонтанно разрешаются в течение 6 недель после их появления и поэтому не требуют оперативного лечения. По прошествии 6 недель кисты редко разрешаются спонтанно и более склонны к осложнениям.
Наружное дренирование псевдокисты поджелудочной железы
Наружное дренирование псевдокисты поджелудочной железы показано, когда киста быстро растет и существует угроза ее прорыва в брюшную полость. До тех пор пока стенка кисты не созрела, ее невозможно анастомозировать с пищеварительным трактом. Для наружного дренирования кисты производят срединный разрез между мечевидным отростком и пупком. Содержимое кисты аспирируют шприцем с иглой № 16. Производят бактериологическое и цитологическое исследование жидкости, определяют уровень ферментов.
Затем кисту пунктируют троакаром, все ее содержимое удаляют. В кисту помещают трубку для постоянного дренирования и, если возможно, закрепляют ее кисетным швом. Дренажную трубку выводят через небольшой разрез в брюшной стенке и присоединяют к системе для постоянного дренирования. Брюшную стенку ушивают послойно нерассасывающейся нитью. Если псевдокиста разорвалась до операции, вмешательство производят, как описано выше.
Наружное дренирование псевдокисты не является операцией выбора. Это только неотложное решение проблемы, которое может приводить к осложнениям, таким как формирование свищей, повреждения кожи в результате действия ферментов и частые рецидивы, ухудшающие течение заболевания и повышающие летальность.
Псевдокисты, которые увеличиваются до опасного размера, можно также пунктировать чрескожным доступом под контролем УЗИ или компьютерной томографии. Чрескожное дренирование должно выполняться в учреждениях, имеющих достаточный опыт проведения таких процедур. Показано, что у больных, которым выполнено чрескожное дренирование псевдокист, рецидивы возникают значительно чаще, чем у тех, которым выполнена хирургическая операция.
Ложная киста поджелудочной железы (K86.3)
Версия: Справочник заболеваний MedElement
Общая информация
Краткое описание
Период протекания
Образуется спустя 1-4 недель после начала острого панкреатита.
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
Общепринятая классификация отсутствует.
При описании используются следующие параметры:
1. Локализация:
— в головке пожелудочной железы (15%);
— в теле и хвосте (85%).
2. Число:
— единичная;
— множественные.
3. Размер:
— малые;
— большие ;
— гигантские.
4. Осложнения (см. соответствующем разделе).
Этиология и патогенез
Клиническая картина
Cимптомы, течение
Следует предполагать наличие псевдокист при наличии следующих проявлений:
Диагностика
1. Факт наличия диагноза панкреатита.
3. Компьютерная топография более чувствительна по сравнению с УЗИ. КТ позволяет проводить дифференциальную диагностику псевдокист. Кроме этого возможна пункция и дренирование псевдокист под контролем КТ.
4. Магнитно-резонансная томография. Данных о применении МРТ в диагностике псевдокист мало, но они позволяют отнести метод к необходимым в ряде случаев острого панкреатита. Преимущество МРТ по сравнению с МДКТ (мультидетекторной компьютерной томографией) при оценке перипанкреатических жидкостных скоплений является то, что твердые включения могут быть более легко оценены именно с помощью МРТ. Это может помочь отличить вызванные панкреатитом накопления жидкости от других кистозных поражений, а также выбрать методы дренирования, которые будет использоваться. Еще одним преимуществом МРТ является то, что при этой методике не используется ионизирующее излучение.
При контрастировании использование Т2-взвешенных последовательностей может быть очень полезным в оценке поджелудочной железы, а также при наличии жидкости внутри паренхимы поджелудочной железы (данный факт позволяет предположить некроз).
Таким образом, МРТ предлагает диагностические возможности похожие на МдКТ, но с лучшим изображением камней и системы поджелудочных и желчных протоков.
К недостаткам МРТ можно отнести ее недоступность.
Лабораторная диагностика
2. Лабораторной диагностике также подвергается жидкость, полученная при пункции псевдокисты. Определяются содержание белка, клеточных элементов (в т.ч. атипичных), проводится бакпосев.
Дифференциальный диагноз
Осложнения
3. Панкреатический асцит. Источник жидкости псевокиста в 70%, проток поджелудочной железы в 10-20%. Прилабораторном исследовании асцитической жидкости в ней обнаруживается большое количество амилазы и белка.
4. Свищи в основном являются следствием черезкожного дренирования псевдокисты. Как правило закрываются самостоятельно. При значительном отделяемом может понадобиться хирургическое вмешательство.
5. Обьструкция псевдокистой различных отделов ЖКТ, нижней полой вены, мочевых путей. Требуется экстренная операция.
Лечение
Медикаментозное
1. Назначение окреотида при образовании свища (вопрос остается дискутабельным).
2. Восполнение объема циркулирующей крови и внутрисосудистой жидкости при кровотечениях.
Хирургическое
1. Чрескожное дренирование через катетер.
Показания:
— пациенты низкой группы риска (шкалы APACHE, GLSGO);
— незрелость псевдокисты;
— инфицирование псевдокисты;
— предшествующая четкая визуализация анатомических особенностей протоков с применением эндоскопической ретроградной холангиопанкреатографии (ЭРХПГ) или магнитно-резонансной холангиопанкреатографии (МРХПГ).
2. Эндоскопическое дренирование.
Показания:
— псевдокисты небольшого размера;
— локализация псевдокисты в головке поджелудочной железы.
3. Хирургичекое дренирование.
Показания:
— неэффективность чрескожного и эндоскопического дренирования;
— множественные псевдокисты;
— гигантские псевдокисты;
— другие осложнения острого панкреатита;
— подозрение на опухоль.
Дренирование жидкостных образований, не оформившихся в кисту, обязательно не всегда. Подобные жидкостные скопления образуются более чем в половине случаев острого панкреатита с тяжестью выше средней. В большинстве случаев (65%) выпот рассасывается в течение 6 недель. Выпот, как правило, не связан с протоками поджелудочной железы, поэтому концентрация ферментов в нем относительно низкая.
Если образование (неоформленная псевдокиста) сохраняется более 6 недель и вызывает клинические проявления (боль, желтуху, температуру и прочие) следует подумать об осложнениях (обструкция, инфицирование) и выбирать тактику как при сформировавшейся псевдокисте.
Ложная киста поджелудочной железы
МКБ-10
Общие сведения
Ложная киста поджелудочной железы относится к опухолеподобным процессам. Данная патология представляет серьезную проблему в гастроэнтерологии, тесно связанную с увеличением заболеваемости населения острыми и хроническими панкреатитами, которые являются основной причиной формирования псевдокист. При алкогольном панкреатите ложные кисты поджелудочной железы образуются у 34-50% пациентов.
Псевдокисты склонны к нагноению, перфорации, малигнизации, образованию плохо поддающихся лечению внутренних и наружных свищей, чем обусловлена высокая летальность при данной патологии – до 53%. Клиническая картина псевдокисты часто маскируется под обострение основного заболевания, в ряде случаев ложные кисты являются интраоперационными находками. Несмотря на постоянное совершенствование методик лечения, в том числе микрохирургических, на сегодняшний день отсутствует единый лечебно-диагностический алгоритм и «золотой стандарт» лечения пациентов.
Причины ложной кисты поджелудочной железы
Наиболее часто формированию панкреатических псевдокист предшествует острый и хронический панкреатит, при этом острая форма сопровождается формированием полости в паренхиме железы в половине, а хроническая – в 80% случаев. В зоне повреждения паренхимы органа происходят деструктивные изменения, отграничение воспалительной массы с ее уплотнением и последующим разрастанием в строме соединительной ткани. Тканевой детрит постепенно уничтожается иммунными клетками, и на его месте остается полость без эпителиальной выстилки.
Иногда псевдокисты образуются при ограничении воспалительного процесса вследствие применения высоких дозировок ингибиторов панкреатических ферментов. Такие ложные кисты протекают на фоне хронического панкреатита. Редкой причиной формирования ложных кист поджелудочной железы является атеросклероз сосудов данного органа.
Классификация ложных кист поджелудочной железы
Панкреатические псевдокисты классифицируют по этиологии: возникающие после деструктивного панкреатита, посттравматические и другие. В зависимости от локализации различают псевдокисты головки, тела и хвоста панкреас.
Отдельно выделяют 4 стадии псевдокист, образующихся на месте очага деструкции паренхимы органа:
В практической гастроэнтерологии чаще используется следующая классификация псевдокист:
Симптомы ложной кисты поджелудочной железы
Ведущим симптомом панкреатической псевдокисты является боль. Ее характеристики зависят от размера, локализации, а также стадии формирования полости. Наиболее интенсивную боль испытывают пациенты в первом периоде «созревания» псевдокисты, когда происходят деструктивные процессы в паренхиме органа. Через некоторое время боль стихает, становится тупой. У некоторых пациентов остается только ощущение дискомфорта. В дальнейшем возможны повторные болевые приступы, которые связаны с гипертензией в протоках поджелудочной железы. Значительное усиление боли может свидетельствовать о развитии таких осложнений, как разрыв, нагноение, кровоизлияние в полость псевдокисты.
Локализация болевых ощущений зависит от расположения псевдокисты: при образовании в области головки панкреас боли возникают в правом подреберье, тела и хвоста – в эпигастрии и левом подреберье. Некоторых пациентов беспокоят постоянные боли, что может быть связано с давлением псевдокисты на солнечное сплетение. В таких случаях ощущения усиливаются при смене положения тела, физических нагрузках, давлении поясом одежды. Характерны также диспепсические жалобы: тошнота, рвота, ухудшение аппетита.
Диагностика ложной кисты поджелудочной железы
При проведении рентгенографии органов брюшной полости возможно обнаружение тени псевдокисты, а также смещения двенадцатиперстной кишки или желудка. Более информативна ультразвуковая диагностика. УЗИ поджелудочной железы позволяет визуализировать ложную кисту, оценить ее локализацию и размеры, в некоторой степени – связь с протоковой системой, а также наличие или отсутствие осложнений (нагноения, кровоизлияния в полость). В случае сдавления холедоха выявляется расширение желчных протоков, при портальной гипертензии – селезеночной и воротной вен. При малигнизации псевдокисты визуализируются неровные контуры ее стенки.
Эзофагогастродуоденоскопия проводится с целью выявления косвенных признаков воспалительного процесса в поджелудочной железе, сдавления желудка и двенадцатиперстной кишки: над участками сдавления определяются эрозии слизистой оболочки, может быть обнаружено варикозное расширение вен пищевода.
Важным методом диагностики панкреатических псевдокист является эндоскопическая ретроградная холангиопанкреатография (ЭРХПГ). Данный метод исследования позволяет оценить связь полости псевдокисты с протоковой системой, что играет определяющую роль в выборе лечебной тактики. Однако в связи с тем, что существует высокий риск инфицирования полости в ходе исследования, ЭРХПГ проводится исключительно перед хирургическим вмешательством для выбора метода лечения.
Для окончательной верификации диагноза, детальной оценки состояния ложной кисты поджелудочной железы и ее содержимого выполняются такие диагностические исследования, как МРТ поджелудочной железы, цитологическое исследование содержимого кисты. Дифференциальная диагностика проводится с ретенционными кистами, доброкачественными кистомами, злокачественными опухолями поджелудочной железы.
Лечение ложной кисты поджелудочной железы
Тактика лечения панкреатической псевдокисты зависит от стадии ее формирования, локализации, этиологии, а также связи с протоковым аппаратом. С целью уменьшения секреции в полость и купирования воспалительного процесса на всех этапах развития псевдокист назначается диетотерапия (стол №5 по Певзнеру), а также фармакотерапия, способствующая достижению «функционального покоя» поджелудочной железы (применяются блокаторы Н2-гистаминовых рецепторов, ингибиторы протонной помпы, холинолитики). В некоторых случаях (особенно при наличии хорошего сообщения псевдокисты с вирсунговым протоком) такого лечения достаточно для резорбции ложной кисты. Но даже при крупных псевдокистах, не связанных с протоками, на первом этапе именно консервативное лечение является ведущим, поскольку на фоне выраженных деструктивных процессов с большим количеством некротических масс хирургическое лечение может привести к осложнениям.
На данном этапе фармакотерапия комбинируется с ранним чрескожным пунктированием с установкой катетера. Катетер может находиться в полости псевдокисты до нескольких месяцев, что дает возможность выполнять промывание антисептическими растворами, аспирацию содержимого, а также пломбирование полости силиконовыми быстротвердеющими композициями. До формирования фиброзной капсулы псевдокисты применяется выжидательная тактика, которая обоснована и при бессимптомных ложных кистах поджелудочной железы. При этом активные методы применяются только при появлении клинических симптомов (сдавление соседних органов, боль).
Во втором и последующих периодах формирования псевдокисты ведущим методом лечения является дренирование. В настоящее время в клинической практике более часто применяются эндоскопические малоинвазивные методы, включающие цистогастростомию и цистодуоденостомию. В ходе данных вмешательств выполняется пункция стенки желудка или двенадцатиперстной кишки в области сдавления псевдокистой и установка стента, который может находиться в анастомозе несколько недель. Однако данные методы лечения имеют определенные недостатки: существует риск инфицирования псевдокисты с попаданием химуса в ее полость, раздражения слизистой пищеварительной трубки, кровотечения, а также рубцевания соустья, что приводит к рецидивам.
Хирургическое лечение показано при больших размерах ложных кист поджелудочной железы (более 6-7 сантиметров в диаметре), быстром их увеличении, длительно существующих полостях, большом количестве детрита в полости, а также при травматической этиологии. Также операция проводится при нагноении, перфорации, кровотечении, формировании свищей, неэффективности других методов лечения. Для лечения панкреатических псевдокист выполняется наружное дренирование (вскрытие псевдокисты с вшиванием в рану передней брюшной стенки), внутреннее дренирование (вскрытие кисты, ее ушивание и наложение анастомоза с желудком, двенадцатиперстной или тощей кишкой), удаление кисты (цистэктомия или резекция части панкреас с псевдокистой).
Прогноз и профилактика
Прогноз при ложных кистах поджелудочной железы зависит от причины их развития и выбора оптимального метода лечения в каждом конкретном случае. Послеоперационная летальность при данной патологии очень высокая – около 50%. В то же время рецидивы после различных видов лечения, в том числе эндоскопических, развиваются в 30% случаев. Существует высокий риск таких осложнений, как кровотечение, нагноение, перфорация псевдокисты, формирование свищей, малигнизация. Профилактика панкреатических псевдокист сводится к предупреждению панкреатитов (отказу от употребления алкоголя, рациональному питанию), травм брюшной полости.
Псевдокиста поджелудочной железы что
Полный текст статьи:
Этиология
ПК может возникнуть в 3 ситуациях:
Клиника
Большинство ПК ассимптоматичны, однако они могут иметь различные клинические проявления в зависимости от размеров и локализации.
Диагноз
Диагноз ПК обычно выставляется при КТ или УЗИ. При выполнении дренирования (обычно скорее с лечебной целью чем диагностической), значительное повышение уровня амилазы в содержимом ПК, в результате ее сообщения с протоковой системой ПЖ, характерно для ПК. Очень высокий уровень амилазы, обычно выше 1000 обнаруживается в жидкости полученной в результате лапароцентеза или торакоцентеза при панкреатическом асците или плеврите [4].
Вопросы требующие рассмотрения
При обнаружении сопровождающегося симптоматикой перипанкреатического скопления жидкости у пациента с острым или хроническим панкреатитом или травмой ПЖ клиницист должен обратить внимание на ряд вопросов, до момента принятия решения о дренировании.
Альтернативные диагнозы
Хотя высокий уровень амилазы в содержимом ПК в результате ее связи с панкреатическим потоком обычно указывает на воспалительную ПК, должен оставаться высокий уровень сомнения т.к. не один из тестов в отдельности не может исключить кистозную неоплазму. Много других незлокачественных заболеваний могут симулировать ПК, в результате этого, чрезвычайная внимательность необходима для избежания ошибок в диагностике [2,8].
Возможное наличие псевдоаневризмы
Мы полагаем, что аккуратно выполненная, болюсная, динамическая КТ с ранним выполнением снимков в артериальную фазу должна быть рутинным исследованием для всех пациентов рассматриваемых кандидатами для эндоскопического дренирования, для обнаружения псевдоаневризмы. Доплеровское сканирование брюшной полости может быть полезным, но имеет более низкую чувствительность. Ангиография является определяющим диагностическим тестом и все шире используется с целью эмболизации псевдоаневризм радиоконтрастной спиралью или пеной [12]. Среди первых 57 пациентов направленных для эндоскопического лечения псевдокисты в наше учреждение нам удалось диагностировать 5 псевдоаневризм до выполнения дренирования. Эти пациенты были пролечены путем мультидисциплинарного подхода, включая эмболизацию или резекцию [12]. Более недавно мы осторожно выполняли эндоскопическое дренирование после точной ангиографической эмболизации у пациентов которые не являлись хорошими кандидатами для хирургической резекции [13].
Роль консервативного лечения
Традиционное обучение в хирургии базируется на классическом исследовании, что ПК присутствующие более 6 недель редко разрешаются и при последующем наблюдении дают осложнения в 50 % случаев [14]. После 13 неделе никакого дальнейшего разрешения не наблюдалось и уровень осложнений резко возрастал. Оперативное вмешательство рекомендовалось после 6 недельного периода наблюдения для уверенности, что самостоятельное разрешение не произошло и для дачи времени созревания стенкам ПК позволяющее наложить прямую цисто-энтеростомию путем сшивания. Этот подход широко принят у хирургов и часто цитируется 17. Два других обзора, однако, рекомендуют более консервативный выжидательный подход у пациента с установленным отсутствием кистозной неоплазмы, псевдоанивризмы или с более чем минимальной симптоматикой. Ретроспективный обзор 68 пациентов с ПК пролеченных консервативно показало, что серьезные осложнения возникают в 9 % случаев, большинство из которых имеют место в первые 8 недель после установки диагноза [19]. Осложнения включали формирование псевдоаневризы у 3х, перфорацию в свободную брюшную полость у 2х и спонтанное формирование абсцесса у 1-го пациента. В дополнение к этому 1/3 пациентов подверглась плановой операции из-за боли связанной с увеличением кисты. Однако у 43 пациентов (63 %) наблюдалось либо спонтанное разрешение либо отсутствие симптомов и осложнений в средние сроки наблюдения в 51 месяц. Подобные наблюдения были отмечены в другом обследовании 75 пациентов [20]. Оперативное вмешательство предпринималось только по поводу тяжелой абдоминальной боли, осложнений или прогрессирующего увеличения размеров кисты. 52 % пациентов подверглись операциям по вышеназванным показаниям, оставшиеся пациенты велись консервативно. Среди пациентов последней группы у 60 % наблюдалось полное разрешение кисты в сроки до 1-го года и только у одного наблюдалось осложнения связанное с ПК. Другие пациенты этой группы симптомов не имели, а ПК либо сохранялась, либо постепенно уменьшалась в размерах. Невозможно предсказать на основе этиологии или КТ у каких пациентов произойдет полное разрешение ПК, но в общем ПК у больных в группе консервативного лечения были меньше в размерах, чем у пациентов требующих хирургического лечения. Подробного описания анатомии панкреатичекого протока, которое могло помочь в предсказании развития заболевания не приведено ни в одном из этих исследований [21].
Возможности дренирования
В прошлом, когда дренирование становилось необходимым в связи с осложнениями или некурабильными симптомами связанными с ПК хирургическое дренирование оставалось единственным способом лечения. В настоящее время имеются еще две возможности лечения которые достигли все возрастающей популярности: чрезкожное и эндоскопическое дренирование. Остающимся противоречием остается вопрос какой из этих методов должен быть предложен пациенту в качестве начального вида терапии. В настоящее время нет рандомизированных сравнительных исследований этих двух методов и врачи используют тот которым они лучше владеют. Недостатком чрезкожного дренирования является длительное нахождение катетера и возможное формирования наружного свища.
Внутреннее хирургическое дренирование. Большинство хирургов при возможности используют технику внутреннего дренирования, методика которой зависит от локализации псевдокисты:
Сообщаемый уровень осложнений внутреннего дренирования приблизительно 15 % со смертностью менее 5 %. Уровень послеоперационного рецидива около 10 % 23. При наличии обструкции главного панкреатического протока ниже уровня анастомоза некоторые хирурги предпочитают резекцию ПК, а не внутреннее дренирование в попытке минимизировать уровень рецидивов.
Наружное хирургическое дренирование может быть необходимым при невозможности создания внутреннего анастомоза. Наружные панкреатические свищи являются частым исходом подобного подхода [27].
Чрезкожное дренирование катетером. Чрезкожное дренирование катетером является таким же эффективным как хирургическое дренирование в дренировании и закрытии как стерильных так и инфицированных кист 30. Необходимо поддерживать проходимость катетера путем аккуратной ирригации. Катетер оставляется до тех пор пока уровень отделяемого снизится до 5-10 мл. в день. В одном исследовании включающим 52 пациента средний срок дренирования составил 42 дня [28]. Если такое снижение уровня отделяемого не происходит то назначение октреотида (50- 200 мг. подкожно, каждые 8 часов) может быть полезным. Контрольное КТ должно быть выполнено при уменьшении количества отделяемого для уверенности, что катетер не сместился из полости ПК. Основным осложнением этой процедуры является проникновение по катетеру инфекции, которое в одном исследовании происходила у половину пациентов [28]. Неизвестно должна ли обструкция главного панкреатического протока удерживать от выполнения чрезкожного дренирования.
Эндоскопический подход. Множественные сообщения подтверждают высокий уровень эффективности эндоскопической цисто-гастро (ЭЦГ) и цисто-дуоденностомии (ЭЦД). ЭЦД является процедурой выбора из-за ее более высокой безопасности, более легкого достижения перпендикулярного подхода к кисте во время дренирования и большей заинтересованности ДПК чем желудка в большинстве случаев ПК. Уровень разрешения ПК при эндоскопическом лечении варьирует от 65 до 89 %. Основными осложнениями эндоскопического дренирования являются кровотечение (которое по свое тяжести требует хирургического лечения в до 5 % случаев), ретроперитониальная перфорация, инфекция и не достижение разрешения ПК. Смертность связанная с этой процедурой практически отсутствует с уровнем рецидива в 6-18 %. Количество случаев перфорации или кровотечение может быть минимизировано путем обнаружения ПК до эндоскопической пункции. Мы предпочитаем обнаружение ПК путем эндоскопической пункции, хотя увеличение популярности эндоскопического УЗИ может сделать это методику приемлемой альтернативой.
Роль эндоскопического УЗИ
Наличие некроза поджелудочной железы
Мы считаем, что наиболее важным вопросом от которого зависит решение о применение эндоскопического, хирургического или рентгенологического дренирования это есть ли признаки ассоциированного с ПК, лежащего в ее основе некроза ПЖ, что определяется на КТ с дополнительным контрастированием. Присутствие плотных включений, дендрита, наличие некровоснабжаемых участков паренхимы ПЖ, может указывать, что может присутствовать значительное количество омертвевших тканей. Решение о применении трансмурального подхода зависит от того насколько организовавшимся выглядит некроз. Инфекционные осложнения часты при применении эндоскопического и рентгенологического дренирования в данных условиях [33]. Хотя большинство осложнений возникших при эндоскопическом дренировании могут быть пролечены эндоскопически опытным специалистом, не распознавание некроза, в следствии чего возникает неадекватное дренирование/промывание некротического очага может провести к серьезным инфекционным осложнениям вплоть до смерти. Таким образом, присутствие панкреатического некроза должно служить значительным поводом для сомнения в выполнении эндоскопического дренирования, хотя и не исключает его попыток. Хирургическое дренирование позволяет выполнить зондирование ПК для извлечения некротизированного дендрита и достижения полной эвакуации содержимого до наложения анастомоза. Эндоскопический подход с выполнением трансмуральной пункции позволяет проводить назогастральный лаваж, дилатацию отверстия с введением нескольких стентов и может быть альтернативой операции у тщательно отобранных пациентов в специальных центрах. Проблемы, которые могут возникнуть, проиллюстрированы в сообщении об 11 пациентах которым проводилось эндоскопическое дренирование по поводу такого типа кист (определенных как «организовавшийся некроз ПЖ») [34]. При использовании агрессивной эндоскопической техники успех был достигнут у 9 пациентов. Потребовались множественные процедуры с уровнем осложнений 50 %, хотя большинство из них было пролечено эндоскопически.
Присутствие панкреатического абсцесса
Ограниченное скопление гноя внутри или рядом с ПЖ традиционно описывалось как инфицированная псевдокиста, состояние требующее оперативного вскрытия и дренирования. Недавно эндоскопическое дренирование было использовано у группы пациентов с высокой степенью операционного риска в связи с наличием системных осложнений панкреатита [35]. Важными факторами являются адекватное дренирование, необходимость устранения обструкции оттоку и прилежное обучение и наблюдения пациента. Мы предпочитаем трансмуральный подход к дренированию абсцесса т.к. он позволяет в дальнейшем выполнить дренирование цистэнтеростомического канала, ввести назогастральный ирригационный катетер и множественные стенты для предупреждения сложностей связанных с недостаточной функцией катетера и остаточным содержимым.
Рекомендуемый подход
В настоящее время мы рекомендуем активную тактику у пациентов с ПК возникшими как осложнение хронического или острого панкреатита с наличием симптомов и длительности существования ПК минимум 4 недели. Мы выполняем РХПГ когда считаем, что пациент является кандидатом для попытки эндоскопического дренирования. Во время эндоскопии необходимо исключить портальную гипертензию и обструктивные нарушения эвакуации из желудка. РХПГ выполняется для обнаружения признаков сдавления билиарного древа, в особенности ели повышены печеночные показатели. Панкреатография необходима у всех пациентов для выявления лежащей в основе обструкции панкреатического протока. Неожидаемые стриктуры и конкременты панкреатического протока часто выявляются, может даже встретиться стриктура вызванная злокачественной опухолью. Т.к. эндоскопическое дренирование может быть выполнено как путем трансмуральной пункции так и чрезпапилярной установки стента, панкреатограмма очень важна для выбора между этими двумя возможностями. Эндоскопическое УЗИ может быть полезным в дифференциальной диагностике с кистозными поражениями ПЖ и дренировании ПК, хотя в рутинном порядке не используется. У пациентов с большими, упорными или увеличивающимися ПК часто обнаруживаются тяжелые повреждения панкреатического протока, что определяет необходимость и вид используемого лечения [10]. По нашему опыту обструкции панкреатического протока и его полные стриктуры часты в этой группе пациентов и они не разрешаются после разрешения псевдокист. В отличии от этого подтекание из периферических ветвей закрываются после эндоскопического лечения приводящего к разрешению кисты.