Что необходимо знать о мРНК-вакцинах: 5 позиций
В результате беспрецедентной скорости в разработке новых вакцин, миру были представлены первые клинически одобренные мРНК-вакцины
В результате беспрецедентной скорости в разработке новых вакцин, миру были представлены первые клинически одобренные мРНК-вакцины для борьбы с пандемией Covid-19 – одна из них произведена Pfizer и BioNTech, другая – компанией Moderna. Испытания показали эффективность этих вакцин на уровне не менее чем 94%.
1. Технология мРНК вакцин не так молода, как кажется
Классический механизм работы вакцин (например, против полиомиелита и гриппа) заключается в презентации иммунной системе инактивированных частиц вируса. Другие вакцины (например, против гепатита B) используют отдельно взятый белок, являющийся частью инфекционного агента, чтобы вызвать схожий иммунный ответ.
мРНК-вакцины работают по другому принципу, «обманывая» иммунную систему таким образом, что РНК (в основном матричная мРНК) кодирует белок, который продуцируется в клетке путем трансляции и представляется иммунной системе; он действует как антиген. Иммунная система учится избирательно бороться с клетками, экспрессирующими такие антигены, такими как клетки-хозяева, инфицированные вирусами, или опухолевые клетки.
Хотя вакцины от Pfizer/BioNTech и Moderna – первые препараты, одобренные в клинической практике, сама технология мРНК-вакцин существует относительно давно. Первые испытания в онкологии с использованием схожих технологий берут свое начало еще в 2011 году.
2. мРНК-вакцины не изменяют ДНК
Существуют абсолютно необоснованные опасения, что мРНК-вакцины способны изменять ДНК. На самом же деле мРНК не входит в ядро клетки, а после своего введения биодеградирует в течение нескольких дней. Именно поэтому для формирования полноценного иммунного ответа необходимо 2 инъекции препарата.
3. мРНК-вакцины имеют высокую специфичность
Вирус SARS-CoV-2 имеет достаточно сложную структуру и его различные части стимулируют иммунную систему на образование нейтрализующих антител, которые не всегда способны эффективно элиминировать инфекцию. мРНК-вакцины стимулируют иммунный ответ к спайк-белку вируса, являющегося только частью вирусной мембраны.
4. Разработчики и эксперты не «срезали углы» во время клинических испытаний
Испытания вакцин начались с доклинической фазы, проводимой на животных, а затем постепенно переходили на 1-ую, 2-ую и 3-ю фазы. Например, 3-я фаза вакцины от Pfizer/BioNTech включает более 40 000 человек, исследования эффективности и безопасности будут продлжаться следующие 2 года.
Основные проблемы, связанные с использованием вакцины, обычно возникают в первые 2 месяца. Тем не менее, не исключены редкие побочные эффекты на больших выборках в миллионы людей, поэтому за вакцинированными необходимо пристальное наблюдение, особенно с учетом инновационной природы технологии.
5. Вакцина запускает воспалительные реакции
Частично вакцина работает путем индуцирования локальных иммунных реакций, поэтому воспалительные признаки в месте инъекции и небольшой дискомфорт в первые дни – вполне нормальное явление.
3 типа вакцин от COVID-19: в чем их особенности
По состоянию на конец 2020 года в мире разрабатывалось более 200 вакцин-кандидатов для иммунной профилактики COVID-19. Из них по меньшей мере 52 вакцины-кандидата проходили испытания на людях.
Почему так много вакцин находится в разработке?
Как правило, множество кандидатов на вакцину будет оценено перед тем, как смогут установить, что какая-либо из них является одновременно безопасной и эффективной. Например, из всех вакцин, которые изучаются в лаборатории и на лабораторных животных, примерно 7 из 100 будут соответствовать критериями, позволяющий им дойти до клинических испытаний на людях. Из вакцин, которые проходят клинические испытания, только каждая пятая оказывается успешной. Наличие большого числа вакцин в процессе разработки увеличивает шансы на то, что будет создана одна или несколько успешных вакцин, которые докажут свою безопасность и эффективность для предполагаемых приоритетных групп населения.
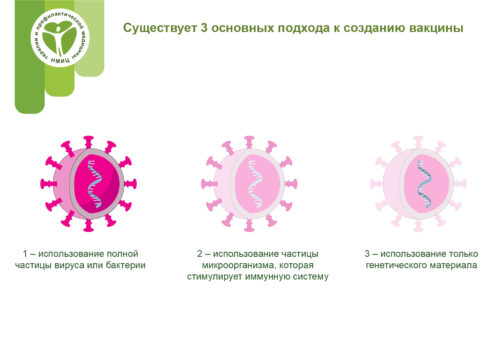
Разные типы вакцин
Существует три основных подхода к разработке вакцины. Их различия заключаются в том, используют ли они целый вирус или бактерию; только части микроба, которые запускают иммунную систему; или только генетический материал, который предоставляет инструкции для создания определенных белков, а не всего вируса.
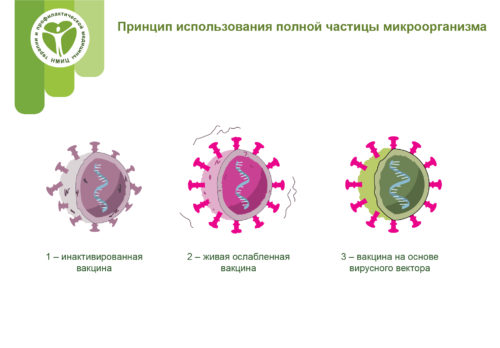
Принцип использования полной частицы микроорганизма
Инактивированные вакцины
Живые ослабленные вакцины
Живая ослабленная вакцина использует ослабленную живую вирусную частицу. Вакцина против кори, паротита и краснухи и вакцина против ветряной оспы и опоясывающего лишая являются примерами вакцины этого типа. Этот подход использует технологию, аналогичную инактивированной вакцине, и может быть изготовлен в больших масштабах. Однако подобные вакцины могут не подходить людям с ослабленной иммунной системой.
Векторные вакцины
Этот тип вакцины использует безопасный вирус для доставки определенных частиц (белков) интересующего микроорганизма, чтобы он мог вызвать иммунный ответ, не вызывая заболевания. Для этого «инструкции» по изготовлению определенных частей интересующего патогена вставляются в безопасный вирус. Затем безопасный вирус служит платформой или вектором для доставки белка в организм, а белок, в свою очередь, запускает иммунный ответ. Вакцина против Эболы является вакциной против вирусных переносчиков. Преимущество этого типа вакцин заключается в возможности быстрой разработки.
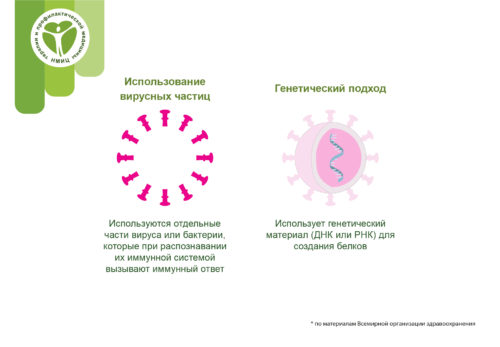
Подход использования вирусных частиц
Комментарий: используются отдельные части вируса или бактерии, которые при распознавании их иммунной системой вызывают иммунный ответ
Субъединичная вакцина – это вакцина, в которой используются только очень специфические части (субъединицы) вируса или бактерии, которые иммунная система должна распознать. Он не содержит всего микроба и не использует безопасный вирус в качестве переносчика. Субъединицами могут быть белки или сахара. Большинство вакцин в детском календаре вакцинации являются субъединичными вакцинами, защищающими людей от таких заболеваний, как коклюш, столбняк, дифтерия и менингококковый менингит.
Генетический подход (вакцина на основе нуклеиновых кислот)
В отличие от подходов к вакцинации, в которых используется ослабленный, убитый цельный микроорганизм или его части, вакцина на основе нуклеиновой кислоты использует участок генетического материала, который содержит инструкции для синтеза конкретных белков микроорганизма. ДНК и РНК являются «инструкциями», которые наши клетки используют для производства белков. В наших клетках ДНК сначала превращается в информационную РНК, которая затем используется в качестве основы для создания определенных белков.
Вакцина на основе нуклеиновых кислот доставляет нашим клеткам определенный набор инструкций в виде ДНК или матричной РНК, чтобы клетки вырабатывали определенный белок, на который должна отреагировать иммунная система. Подход с использованием нуклеиновых кислот является новым способом разработки вакцин. До пандемии COVID-19 ни одна из них еще не прошла полный процесс одобрения для использования на людях, хотя некоторые ДНК-вакцины, в том числе для конкретных видов рака, проходили испытания на людях. Из-за пандемии исследования в этой области продвигаются очень быстро, и некоторые вакцины против COVID-19 на основе матричной РНК получили разрешение на экстренное использование, что означает, что теперь их можно применять у людей вне клинических исследований.
Первая пошла: прототип одной из вакцин от COVID-19 создан в МГУ
Первый прототип вакцины от COVID-19 уже готов. Ученые МГУ им. М.В. Ломоносова впервые увидели под микроскопом созданные ими частицы, имитирующие строение коронавируса и при этом «работающие» как вакцина. Всего исследователи планируют «собрать» пять прототипов вакцины с различными комбинациями белков SARS-CoV-2 и, выбрав лучший, приступить к испытаниям препарата на животных.
Меньше чем за месяц
О том, что прототип вакцины от COVID-19, которая создается силами ученых университета, может быть готов за три месяца, декан биологического факультета МГУ им. М.В. Ломоносова Михаил Кирпичников заявил в разговоре с «Известиями» 18 марта.
Однако уже 15 апреля исследователи сообщили о первом успехе. Меньше чем за месяц им удалось получить ряд рекомбинантных белков, которые содержат эпитопы коронавируса — часть его антигенов, веществ, которые человеческий организм считает чужеродными и поэтому отдает сигнал для выработки иммунного ответа (антител).
Лаборатория химиков МГУ имени Ломоносова
Эти белки разместили и закрепили на специальной платформе — сферической частице, полученной из вируса табачной мозаики (патоген растений). По словам ученых, нужные белки успешно «сели» на платформу. Для того чтобы убедиться в стойкости прикрепления, их окрасили с помощью флуоресцентной метки.
— Под микроскопом мы увидели ту самую частицу, похожую на коронавирус, которая «по нимбу» светится зеленым светом, — это значит, что на ее поверхности размещены нужные белки SARS-CoV-2, — рассказала «Известиям» завкафедрой вирусологии биофака МГУ Ольга Карпова. — Мы впервые увидели частицу не на рисунке, а наяву.
Частица действительно внешне напоминает коронавирус. Это первый прототип вакцины, который, по словам эксперта, создавался в авральном режиме. Сотрудники лаборатории МГУ работали практически круглосуточно, без выходных.
От всех коронавирусов
Учеными также проделана и большая биоинформатическая работа. Она включала анализ геномов всех известных коронавирусов (в том числе MERS и SARS) с целью поиска «общих мест». В результате они были найдены в геномах не только коронавирусов, вызвавших эпидемии атипичных пневмоний в 2002 и 2013 годах, но и в SARS-CoV-2, и в других патогенах летучих мышей, которые имеют потенциал перехода на человека. Таким образом, вакцина будет защищать людей не только от существующих, но и от потенциальных будущих угроз.
В ближайшие месяцы планируется создать еще несколько прототипов вакцины — их частицы будут содержать другие комбинации белков SARS-CoV-2.
— Таких прототипов будет не больше пяти, — сообщила Ольга Карпова. — И потом мы перейдем к опытам на животных. Думаю, это будет в середине лета.
Как ранее рассказывали «Известия», искусственно сконструированные частицы, имитирующие коронавирус, уже испытаны на работоспособность. Учеными был проведен эксперимент, в ходе которого элементы поместили в искусственную среду, напоминающую кровеносную систему. Исследователи доказали, что нужные белки не «слетят» с поверхности шариков, то есть будут устойчиво и правильно работать, постепенно «отпуская» антигены в организме человека, вызывая иммунный ответ.
Что такое вакцина
Знаете ли вы, что такое прививка?
Вакцинация (прививка) – это введение в организм человека медицинских иммунобиологических препаратов для создания специфической невосприимчивости к инфекционным болезням.
Предлагаем разобрать каждую часть этого определения, чтобы понять, что же такое вакцина и как она работает.
Часть 1. Медицинский иммунобиологический препарат
Все вакцины — это медицинские иммунобиологические препараты, т.к. они вводятся под контролем врача и содержат обработанные по специальной технологии возбудители заболеваний (биологические), против которых планируется создать иммунитет (иммуно-).
Кроме возбудителей или их частей-антигенов, вакцины иногда содержат специальные разрешенные консерванты для сохранения стерильности вакцины при хранении, а также минимальное допустимое количество тех средств, которые использовались для выращивания и инактивации микроорганизмов. Например, следовые количества дрожжевых клеток, используемых в производстве вакцин против гепатита В, или следовые количества белка куриных яиц, которые в основном используются для производства вакцин против гриппа.
Стерильность препаратов обеспечивают консерванты, рекомендованные Всемирной организацией здравоохранения и международными организациями по контролю безопасности лекарственных средств. Эти вещества разрешены для введения в организм человека.
Полный состав вакцин указан в инструкциях по их применению. Если у человека имеется установленная тяжелая аллергическая реакция на какой-то из компонентов конкретной вакцины, то обычно это является противопоказанием к её введению.
Часть 2. Введение в организм
Для введения вакцины в организм используются разные методы, их выбор определяется механизмом формирования защитного иммунитета, а способ введения указан в инструкции по применению.
Кликните на каждый из способов введения, чтобы больше о нем узнать.
Внутримышечный путь введения вакцин
Наиболее часто встречающийся путь для введения вакцин. Хорошее кровоснабжение мышц гарантирует и максимальную скорость выработки иммунитета, и максимальную его интенсивность, поскольку большее число иммунных клеток имеет возможность «познакомиться» с вакцинными антигенами. Удаленность мышц от кожного покрова обеспечивает меньшее число побочных реакций, которые в случае внутримышечного введения обычно сводятся лишь к некоторому дискомфорту при активных движениях в мышцах в течение 1-2 дней после вакцинации.
Место введения: Вводить вакцины в ягодичную область не рекомендуется. Во-первых, иглы шприц-доз многих вакцин недостаточно длинны для того, чтобы достичь ягодичной мышцы, в то время, как известно, и у детей, и у взрослых кожно-жировой слой может иметь значительную толщину. Если вакцина вводится в ягодичную область, то она, возможно, будет введена подкожно. Следует также помнить о том, что любая инъекция в ягодичную область сопровождается определенным риском повреждения седалищного нерва у людей с нетипичным его прохождением в мышцах.
Предпочтительным местом введения вакцин у детей первых лет является передне-боковая поверхность бедра в средней его трети. Это объясняется тем, что мышечная масса в этом месте значительна, при том, что подкожно-жировой слой развит слабее, чем в ягодичной области (особенно у детей, которые еще не ходят).
У детей старше двух лет и взрослых предпочтительным местом введения вакцин является дельтовидная мышца (мышечное утолщение в верхней части плеча, над головкой плечевой кости), в связи с небольшой толщиной кожного покрова и достаточной мышечной массой для введения 0,5-1,0 мл вакцинного препарата. У детей первого года жизни это место обычно не используется в связи с недостаточным развитием мышечной массы.
Техника вакцинации: Обычно внутримышечная инъекция проводится перпендикулярно, то есть под углом 90 градусов к поверхности кожи.
Преимущества: хорошее всасывание вакцины и, как следствие, высокая иммуногенность и скорость выработки иммунитета. Меньшее число местных побочных реакций.
Недостатки: Субъективное восприятие детьми младшего возраста внутримышечных инъекций несколько хуже, чем при других способах вакцинации.
Пероральный (т.е. через рот)
Классическим примером пероральной вакцины является ОПВ – живая полиомиелитная вакцина. Обычно таким образом вводятся живые вакцины, защищающие от кишечных инфекций (полиомиелит, брюшной тиф).
Техника пероральной вакцинации: несколько капель вакцины закапываются в рот. Если вакцина имеет неприятный вкус, ее могут закапывать либо на кусочек сахара, либо печенья.
Преимущества такого пути введения вакцины очевидны: нет укола, простота метода, его быстрота.
Недостатками Недостатками перорального введения вакцин можно считать разлив вакцины, неточность дозировки вакцины (часть препарата может выводиться с калом, не сработав).
Внутрикожный и накожный
Классическим примером вакцины, предназначенной для внутрикожного введения, является БЦЖ. Примерами вакцин с внутрикожным введением также являются живая туляремийная вакцина и вакцина против натуральной оспы. Как правило, внутрикожно вводятся живые бактериальные вакцины, распространение микробов из которых по всему организму крайне нежелательно.
Техника: Традиционным местом для накожного введения вакцин является либо плечо (над дельтовидной мышцей), либо предплечье – середина между запястьем и локтевым сгибом. Для внутрикожного введения должны использоваться специальные шприцы со специальными, тонкими иглами. Иголочку вводят вверх срезом, практически параллельно поверхности кожи, оттягивая кожу вверх. При этом необходимо убедиться, что игла не проникла под кожу. О правильности введения будет свидетельствовать образование специфической «лимонной корочки» в месте введения – белесый оттенок кожи с характерными углублениями на месте выхода протоков кожных желез. Если «лимонная корочка» не образуется во время введения, значит вакцина вводится неверно.
Преимущества: Низкая антигенная нагрузка, относительная безболезненность.
Недостатки: Довольно сложная техника вакцинации, требующая специальной подготовки. Возможность неправильно ввести вакцину, что может привести к поствакцинальным осложнениям.
Подкожный путь введения вакцин
Довольно традиционный путь введения вакцин и других иммунобиологических препаратов на территории бывшего СССР, хорошо известный всем уколами «под лопатку». В целом этот путь подходит для живых и инактивированных вакцин, хотя предпочтительно использовать его именно для живых (корь-паротит-краснуха, желтая лихорадка и др.).
В связи с тем, что при подкожном введении может несколько снижаться иммуногенность и скорость выработки иммунного ответа, этот путь введения крайне нежелателен для введения вакцин против бешенства и вирусного гепатита В.
Подкожный путь введения вакцин желателен для пациентов с нарушениями свертывания крови – риск кровотечений у таких пациентов после подкожной инъекции значительно ниже, чем при внутримышечном введении.
Техника: Местом вакцинации могут быть как плечо (боковая поверхность середины между плечевым и локтевым суставами), так и передне-боковая поверхность средней трети бедра. Указательным и большим пальцами кожа берется в складку и, под небольшим углом, игла вводится под кожу. Если подкожный слой у пациента выражен значительно, формирование складки не критично.
Преимущества: Сравнительная простота техники, незначительно меньшая болезненность (что несущественно у детей) по сравнению с внутримышечной инъекцией. В отличие от внутрикожного введения, можно ввести больший объем вакцины или другого иммунобиологического препарата. Точность введенной дозы (по сравнению с внутрикожным и пероральным способом введения).
Недостатки: «Депонирование» вакцины и как следствие — меньшая скорость выработки иммунитета и его интенсивность при введении инактивированных вакцин. Большее число местных реакций — покраснений и уплотнений в месте введения.
Аэрозольный, интраназальный (т.е. через нос)
Считается, что подобный путь введения вакцин улучшает иммунитет во входных воротах воздушно-капельных инфекций (например, при гриппе) за счет создания иммунологического барьера на слизистых оболочках. В то же время, созданный таким образом иммунитет не является стойким, и в то же время общий (т.н. системный) иммунитет может оказаться недостаточным для борьбы с бактериями и вирусами, уже проникшими в организм через барьер на слизистых оболочках.
Техника аэрозольной вакцинации: несколько капель вакцины закапывают в нос либо распыляют в носовых ходах с помощью специального устройства.
Преимущества такого пути введения вакцины очевидны: как и для пероральной вакцинации, для аэрозольного введения не требуется укола; такая вакцинация создает отличный иммунитет на слизистых оболочках верхних дыхательных путей.
Недостатками интраназального введения вакцин можно считать существенный разлив вакцины, потери вакцины (часть препарата попадает в желудок).
Часть 3. Специфическая невосприимчивость
Вакцины защищают только от тех заболеваний, против которых они предназначены, в этом заключается специфика иммунитета. Возбудителей же инфекционных заболеваний множество: они делятся на различные типы и подтипы, для защиты от многих из них уже созданы или создаются специфичные вакцины с разными возможными спектрами защиты.
Так, например, современные вакцины против пневмококка (одного из возбудителей менингита и пневмонии) могут содержать по 10, 13 или 23 штамма. И хотя ученым известно около 100 подтипов пневмококка, вакцины включают самые часто встречающиеся у детей и взрослых, например, самый широкий на сегодня спектр защиты — из 23 серотипов.
Однако нужно иметь в виду, что привитой человек имеет вероятность встретиться с каким-то редким подтипом микроорганизма, который не входит в вакцину и может вызвать заболевание, так как вакцина не формирует защиту против этого редко встречающегося микроорганизма, не входящего в её состав.
Означает ли это, что прививка не нужна, раз не может защитить от всех болезней? НЕТ! Вакцина дает хорошую защиту от наиболее распространенных и опасных из них.
Календарь прививок, подскажет вам, против каких инфекций необходима вакцинация. А мобильное приложение «Беби-Гид» поможет не забыть о сроках детских прививок.
Что такое вакцины?
Этими принципами при создании вакцин пользуются и до сих пор. В их основе лежит очень важное свойство живого организма – «запоминать» возбудителей инфекции и вырабатывать при их первичном попадании в него особые вещества (антитела), индивидуальные для каждого вида возбудителя. В следующий раз при его попадании в организм, эти антитела быстро его «узнают» и обезвредят.
Вакцины готовят как из целых микроорганизмов и вирусов, так и из их токсинов (как правило, это продукты жизнедеятельности возбудителя) и отдельных структурных элементов бактериальных клеток и вирусов (антигенов). Основные типы вакцин: живые (ослабленные штаммы), убитые, анатоксины (обезвреженные токсины), химические анавакцины (одновременно содержат анатоксины и убитые вакцины). В зависимости от количества входящих антигенов вакцины подразделяют на моно-, ди- и поливакцины, содержащих соответственно один, два или несколько антигенов возбудителей. Вакцины широко применяют в профилактике и лечении инфекционных болезней. Их вводят подкожно, внутрикожно, внутримышечно, аэрозольно и др.
В наших аптеках «Живика» вы можете приобрести или заказать через Интернет (www.zhivika.ru) любую необходимую вакцину.
Распространенные вакцины, представленные в сети аптек «Живика»:
1. Вакцина Аваксим – профилактика вирусного гепатита А у детей в возрасте от 12 месяцев до 15 лет включительно. Вакцину вводят внутримышечно, в дельтовидную мышцу плеча в разовой дозе 0,5 мл двукратно с интервалом 6-18 месяцев.
2. Вакцина Альгавак М – активная профилактика вирусного гепатита А у детей в возрасте от 3 лет, подростков и взрослых.
4. Вакцина Превенар 13 – профилактика заболеваний, вызываемых Streptococcus pneumoniae серотипов 1, 3, 4, 5, 6А, 6В; 7F, 9V, 14, 18С, 19А, 19F и 23F (включая бактериемию, сепсис, менингит, пневмонию и острый средний отит) у детей в возрасте от 2 мес до 5 лет.
5. «Хаврикс®» (Великобритания) – инактивированная (убитая) вакцина для профилактики гепатита А. Клинические исследования показали, что у 99 % вакцинированных через 30 дней после введения первой дозы достигается стойкий иммунитет, а после ревакцинации с интервалом 6-12 месяцев он сохраняется до 25 лет и более.
Материал носит информационный характер. Лекарственные средства, биологические активные добавки и другие товары указаны в качестве примера их возможного использования и/или применения, что ни в коем случае не является рекомендацией к их применению. Перед применением лекарств, биологически-активных добавок и медицинской техники и других товаров обязательно проконсультируйтесь со специалистом.