Проницаемость биологических мембран
Полезное
Смотреть что такое «Проницаемость биологических мембран» в других словарях:
проницаемость биологических мембран — свойство биологических мембран пропускать различные вещества … Большой медицинский словарь
ПРОНИЦАЕМОСТЬ КЛЕТОК — свойство, определяющее способность клеток контролировать пропускание и удерживание веществ, растворенных в окружающей среде, а также способность отдавать в окружающую среду вещества, появляющиеся в клетке в процессе ее жизнедеятельности. П. к.… … Словарь ботанических терминов
ПРОНИЦАЕМОСТЬ ЦИТОПЛАЗМЫ — способность проникать через цитоплазматические мембраны в клетку и из нее различных метаболитов. Имеет важное значение для осморегуляции и поддержания постоянства состава клетки. П. ц. обусловлена особенностями строения биологических мембран … Словарь ботанических терминов
Проницаемость — – свойство биологических мембран, стенок сосудов пропускать различные вещества, воду, электролиты, метаболиты и др … Словарь терминов по физиологии сельскохозяйственных животных
Избирательная проницаемость — У этого термина существуют и другие значения, см. Мембрана Изображение клеточной мембраны. Маленькие голубые и белые шарики соответствуют гидрофильным «головкам» липидов, а присоединённые к ним линии гидрофобным «хвостам». На рисунке показаны… … Википедия
ИЗБИРАТЕЛЬНАЯ ПРОНИЦАЕМОСТЬ — способность биологических мембран пропускать сквозь себя одни вещества, не пропуская другие. И. п. обладают, в частности, плазма лемма и тонопласт клетки. И. п. обусловлена особенностями строения и структуры биомембран клетки, их способностью… … Словарь ботанических терминов
Медицина — I Медицина Медицина система научных знаний и практической деятельности, целями которой являются укрепление и сохранение здоровья, продление жизни людей, предупреждение и лечение болезней человека. Для выполнения этих задач М. изучает строение и… … Медицинская энциклопедия
Биофизика — биологическая физика, наука, изучающая физические и физико химические процессы, протекающие в живых организмах, а также ультраструктуру биологических систем на всех уровнях организации живой материи от субмолекулярного и молекулярного до… … Большая советская энциклопедия
Биологические мембраны — тонкие пограничные структуры молекулярных размеров, расположенные на поверхности клеток и субклеточных частиц, а также канальцев и пузырьков, пронизывающих протоплазму. Толщина Б. м. не превышает 100 Å. Важнейшая функция Б. м.… … Большая советская энциклопедия
Проницаемость мембраны в чем измеряется
• Клеточные мембраны разделяют различные по составу компартменты
• Липидный бислой биологических мембран обладает очень низкой проницаемостью для большинства биологических молекул и ионов
• Большинство веществ проходит через мембрану при участии транспортных белков
• Транспорт ионов и других метаболитов через мембрану контролирует электрические и метаболические функции клетки
Биологические мембраны представляют собой избирательно проницаемые барьеры, которые окружают клеточные компартменты. Плазматическая мембрана отделяет содержимое клетки от внешней среды, а в клетках эукариот специализированные компартменты отделены от цитозоля дополнительными мембранами.
Клеточные компартменты существенно различаются по составу мембран и внутренней-среды. В ходе эволюции клетки выработали механизм для поддержания и регулирования состава среды в каждом компартменте.
Поддержание определенной концентрации растворенных веществ по обеим сторонам мембраны является необходимым условием существования гомеостаза, который представляет собой способность клетки к поддержанию относительного постоянства состава внутренней среды, обеспечивающей протекание жизненно необходимых метаболических процессов.
В результате гомеостатической регуляции концентрации ионов в цитозоле по обеим сторонам мембраны создается относительное осмотическое давление, которое регулирует клеточный объем. Более того, быстро наступающие изменения в транспорте ионов через мембраны носят временный характер и используются клеткой как механизм адаптации к изменившимся обменным процессам и для обработки информации (например, сигналов стресса), а также для транспорта в клетку питательных веществ или удаления из нее продуктов обмена.
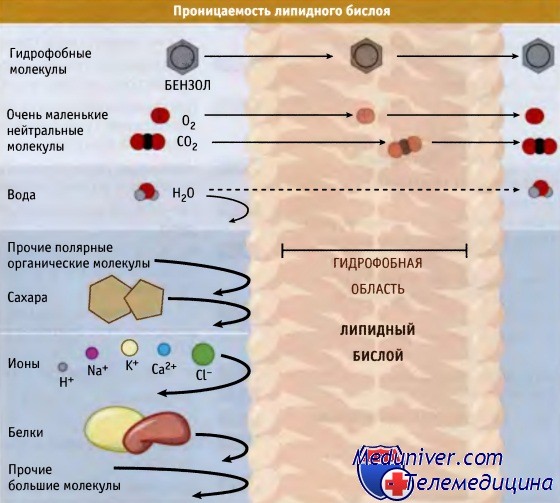
Поскольку внутренняя часть липидного бислоя обладает гидрофобными свойствами, она непроницаема для полярных, гидрофильных и крупных биологических молекул. Каким образом неорганические ионы, а также заряженные молекулы и водорастворимые соединения селективно проходят через клеточные мембраны?
Сейчас мы знаем, что транспорт ионов и метаболитов через мембраны клеточных компартментов происходит с участием мембранных белков. Транспортные белки локализованы в плазматической мембране, а также в мембранах внутриклеточных органелл, например эндоплазматического ретикулума, аппарата Гольджи, эндосом, лизосом и митохондрий. Для каждого типа мембран, так же как и для каждого типа клеток, характерен определенный набор транспортных белков.
Далее в отдельных статьях на сайте мы рассмотрим мембранные белки, которые принимают участие в транспорте ионов и небольших молекул, таких как глюкоза. Вначале мы остановимся на основных классах мембранных транспортных белков, а затем более подробно расскажем о строении и функции отдельных белков. Мы также обсудим вопросы совместного функционирования различных типов транспортных белков в клетке.
Большая часть статей на сайте посвящена транспорту ионов через мембрану. Клетка использует мембранные белки для поддержания определенной концентрации ионов во внутренней среде. Эта концентрация отличается от той, в которой они находятся во внеклеточной среде.
Различие в концентрации является причиной того, что в покоящихся клетках животных внутриклеточная среда заряжена отрицательно по отношению к внешней среде. Эти различия в концентрации и заряде создают электрохимический градиент, который клетка использует для запасания потенциальной энергии. Регуляция электрохимического градиента на мембране позволяет клетке осуществлять ряд основных функций, таких как выработка энергии, а также обрабатывать электрические сигналы поступающие в клетку и выходящие из нее.
В отдельных статьях на сайте также рассмотрены некоторые методы, позволяющие изучать мембраны. Поток заряженных частиц (ионный ток) через мембрану регистрируется электрофизиологическими методами. Этими методами можно исследовать как клетку целиком, так и фрагменты ее мембраны. Они также позволяют оценивать влияние различных воздействий, например изменение ионного состава, эффекты ингибиторов или активаторов транспорта.
Впервые ионные каналы были идентифицированы и выделены благодаря использованию природных токсинов (ядов), которые являются ингибиторами их функций. Эти токсины были также использованы в качестве инструмента для изучения функционирования каналов. Взаимосвязь между структурой и функцией каналов изучалась с использованием рекомбинантных транспортных белков, сайт-специфического мутагенеза, техники интеграции очищенных белков в искусственные мембраны и экспрессии транспортных белков в гетерологичных клетках.
Выяснение атомарной структуры части транспортных белков во многом способствовало пониманию их функционирования. Наряду с выяснением деталей мембранного связывания и транспорта метаболитов эти «фотографии» структуры помогают построить общие модели процессов трансмембранного транспорта.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Содержание материала
Проницаемость мембраны
Мембранный бислой разделяет две водные фазы. Так, плазматическая мембрана отделяет межклеточную (интерстициальную) жидкость от цитозоля, а мембраны лизосом, пероксисом, митохондрий и других мембранных внутриклеточных органелл их содержимое от цитозоля. [2] Биологическая мембрана — полупроницаемый барьер.
Полупроницаемая мембрана. Биологическую мембрану определяют как полупроницаемую, т.е. барьер, не проницаемый для воды, но проницаемый для растворённых в ней веществ (ионы и молекулы).
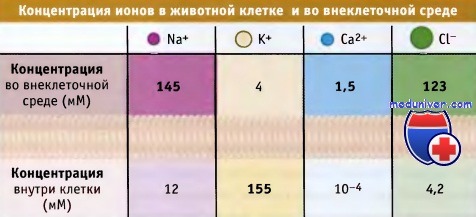
Физико-химические параметры межклеточной жидкости и цитозоля существенно различны (см. табл. 2-1), также различны параметры каждого мембранного внутриклеточного органоида и цитозоля. Наружная и внутренняя поверхности биологической мембраны полярны и гидрофильны, но неполярная сердцевина мембраны гидрофобна. Поэтому неполярные вещества могут проникать через липидный бислой. В то же время именно гидрофобный характер сердцевины биологической мембраны определяет принципиальную невозможность непосредственного проникновения через мембрану полярных веществ.
Неполярные вещества (например, водонерастворимые холестерол и его производные) свободно проникают через биологические мембраны. В частности, именно по этой причине рецепторы стероидных гормонов расположены внутри клетки.
Избирательная проницаемость — проницаемость биологической мембраны по отношению к конкретным химическим веществам) –– важна для поддержания клеточного гомеостаза. оптимального содержания в клетке ионов, воды, метаболитов и макромолекул. Перемещение конкретных веществ через биологическую мембрану называют трансмембранным транспортом (чрезмембранный транспорт).
[1] Гольджи Камилло (Golgi C.), итальянский гистолог (1843–1926). Разработал метод окрашивания ткани, основанный на импрегнации соединениями металлов. Метод был развит Рамон-и-Кахалем и его учениками, что позволило описать строение практически всех отделов нервной системы. За разработку этого метода Гольджи в 1906 г. был удостоен Нобелевской премии по медицине вместе с Сантъяго Рамон-и-Кахалем.
Лекция 3. Проницаемость и транспорт веществ в биологических мембранах
ПРОНИЦАЕМОСТЬ И ТРАНСПОРТ ВЕЩЕСТВ В БИОЛОГИЧЕСКИХ МЕМБРАНАХ
Проницаемость биологических мембран
Одна из важнейших функций биологической мембраны заключается в обеспечении обмена ионов и молекул между клеткой и окружающей средой. Способность биологических мембран пропускать через себя различные вещества называется проницаемостью. Изучение проницаемости клеток имеет большое значение, поскольку с данной функцией связаны практически все процессы жизнедеятельности клетки: метаболизм, генерация и проведение биопотенциалов, секреция, рецепция и т. д.
Любая клетка очень точно поддерживает свой химический, в том числе и ионный состав. Постоянство ионного состава называется ионным гомеостазом и поддерживается за счёт транспорта веществ.
Транспорт веществ в организме можно разделить на три категории:
— дальний транспорт – перенос веществ между органами, его протяжённость в растениях может достигать нескольких десятков метров;
— ближний транспорт – перенос между соседними клетками;
— мембранный транспорт – перенос веществ через мембрану.
По энергетическим затратам мембранный транспорт можно разделить на 2 важнейших класса: активный и пассивный.
Пассивный транспорт не связан прямо с затратой химической энергии; он осуществляется в результате диффузии веществ в сторону меньшего электрохимического потенциала (где концентрация веществ и заряд меньше). Активный транспорт происходит при затрате химической энергии АТФ или переносе электрона по дыхательной цепи.
Виды пассивного транспорта веществ в клетках и тканях: диффузия, осмос.
Диффузия — основной механизм пассивного транспорта веществ, обусловленный наличием концентрационного градиента. Различают несколько видов диффузии:
1) простая диффузия, диффундирующее вещество движется по градиенту через мембрану, не образуя комплекса или проникая через канал;
2) облегченная диффузия, осуществляемая с помощью переносчиков — белков или молекулярных комплексов.
Простая диффузия — это самопроизвольный физический процесс проникновения вещества из области высокой в область меньшей его концентрации в результате теплового хаотического (броуновского) движения молекул.
С помощью простой диффузии через мембрану переносятся растворимые в липидах вещества, в частности такие хорошо растворимые в липидах и важнейшие для метаболического обмена вещества как кислород и углекислый газ. Через липидную фазу мембран в клетку могут проникать также яды и лекарства.
Математическое обоснование процесса диффузии впервые дал А. Фик. Согласно первому закону Фика поток вещества (J) прямо пропорционален градиенту концентрации dC/dx:

где D – коэффициент диффузии, см2∙с-1. Коэффициент диффузии зависит от природы вещества, температуры и характеризует способность вещества к диффузии.
При исследовании проницаемости клеточной мембраны концентрационный градиент определить трудно, поэтому для описания диффузии вещества через нее пользуются более простым уравнением. Для его получения следует учесть три момента:
1) толщина мембраны постоянна, обозначим её как d;
2) концентрации вещества по обе стороны мембраны постоянны, Cin – концентрация вещества внутри клетки, Cout – концентрация вещества в окружающем клетку растворе;
В этом случае силой, которая двигает молекулы через мембрану, будет градиент концентрации вещества через мембрану, который выразится в формуле:
Учитывая это, формулу для потока вещества через мембрану можно записать в следующем виде:
Коэффициент проницаемости Р имеет размерность см/с и является количественной характеристикой способности конкретного вещества проникать через мембрану. Он аналогичен
коэффициенту диффузии (D), но зависит не только от природы вещества и температуры, но и от свойств мембраны.
Диффузия с участием переносчика, как и простая, происходит до тех пор, пока концентрация по обе стороны мембраны не станет одинаковой.
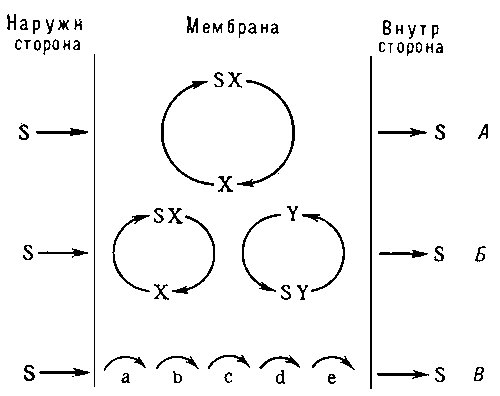
Разновидностью облегченной диффузии является так называемая обменная диффузия, при которой переносчик образует соединении с диффундирующим веществом и перемещается с ним от одной поверхности мембраны к другой, где молекула переносчика освобождается, ее место занимает другая молекула того же вещества и комплекс переносится обратно. При работе переносчиков в случае обменной диффузии концентрация веществ по обе стороны мембраны не изменяется. Существование обменной диффузии было доказано методом меченых атомов на эритроцитах, митохондриях и др.
Проникновение растворенных частиц, обладающих электрическим зарядом, через клеточную мембрану осуществляется по электрохимическому градиенту, а не по концентрационному.
Электрохимический потенциал – энергия, которую надо затратить для перемещения одного моля вещества из бесконечно удалённой точки пространства в данную точку с конкретными условиями.
Величина электрохимического потенциала описывается формулой:
где: 








Молекулы вещества всегда двигаются в сторону своего более низкого электрохимического потенциала.
Рассмотрим простую систему, представляющую собой два отсека, содержащие раствор соли (например, KCl) и разделённые мембраной, которая пропускает только катион, в нашем случае К+.
Растворы находятся в равновесии, это означает, что электрохимические потенциалы ионов в обоих отсеках одинаковы. Математически это будет выражаться уравнением:
Это уравнение, учитывая, что давления и моляльные объёмы вещества в обоих отсеках одинаковы, позволяет нам рассчитать разность электрических потенциалов между отсеками:
Это уравнение называется уравнением Нернста. Если учесть значения констант перед знаком логарифма, и вместо натуральных логарифмов использовать десятичные, то эту формулу можно записать в виде:
Таким образом, если два раствора разной концентрации разделены мембраной, которая обладает избирательной проницаемостью к компонентам раствора, то между этими растворами возникает разность электрических потенциалов. Если мембрана проницаема для одновалентного иона, то десятикратное изменение концентрации в одном из отсеков вызовет к увеличению разности потенциалов между ними на 59 милливольт.
В растворе помимо молекул растворённого вещества присутствуют и молекулы растворителя. Что будет, если мембрана между отсеками будет непроницаема для молекул растворённого вещества, но будет пропускать молекулы растворителя?
Рассмотрим простую модель – два отсека, разделённые мембраной, способной пропускать молекулы растворителя, например, воды и непроницаемой для молекул растворённых веществ. Для наглядности в первом отсеке концентрация растворённого вещества высокая, а во втором низкая. Выделим в каждом отсеке одинаковые объёмы.
Осмотическое давление раствора зависит от количества растворенных ионов и температуры. В соответствии с уравнением Вант-Гоффа осмотическое давление (π) раствора прямо пропорционально концентрации (С) растворенного вещества и абсолютной температуре раствора (T):
Выделяют первично-активный и вторично-активный транспорт.
Транспорт называется первично-активным, если он осуществляется белками-переносчиками (они ещё называются ионными насосами), источником энергии для которых служат АТР, пирофосфат или субстраты, окисляемые в электрон-транспортных цепях митохондрий, хлоропластов.
Вторично-активным (сопряженным) транспортом называют процесс переноса ионов через мембрану против градиента его концентрации за счет энергии электрохимического градиента других ионов. Сопряженный транспорт может осуществляться в режиме симпорта (оба иона переносятся через мембрану в одном направлении) или антипорта (ионы транспортируются в противоположных направлениях). Вторично-активный транспорт обеспечивает мембранный перенос моносахаридов, сахарозы, аминокислот, пептидов, анионов и ряда катионов. Для этой цели мембранные белки-переносчики чаще всего используют электрохимический градиент ионов водорода, создаваемый различными Н+-насосами.
Между пассивными и активными потоками в клетке существует взаимодействие, направленное на поддержание постоянства ионного состава клетки.
При блокировании энергетики клетки (пониженной температурой, ингибиторами, темнотой) интенсивность активного транспорта снижается, приток ионов из внешней среды уменьшается. Одновременно наблюдается возрастание электрического сопротивления мембраны в десятки раз. Это свидетельствует об уменьшении транспорта ионов по пассивным каналам, что предотвращает потерю ионов, находящихся в клетке.
ПРОНИЦАЕМОСТЬ
Проницаемость — способность клеток и тканей поглощать, выделять и транспортировать химические вещества, пропуская их через клеточные мембраны, стенки сосудов и клетки эпителия. Живые клетки и ткани находятся в состоянии непрерывного обмена химическими веществами с окружающей средой. Основным барьером (см. Барьерные функции) на пути движения веществ является клеточная мембрана. Поэтому исторически механизмы Проницаемости исследовались параллельно с изучением структуры и функции биологических мембран (см. Мембраны биологические).
Различают пассивную Проницаемость, активный транспорт веществ и особые случаи Проницаемости, связанные с фагоцитозом (см.) и пиноцитозом (см.).
В соответствии с мембранной теорией Проницаемости в основе пассивной Проницаемости лежат различные виды диффузии вещества через клеточные мембраны (см. Диффузия). Скорость диффузии вещества описывается уравнением Фика:
При исследовании Проницаемости клетки для растворенного вещества вместо градиента концентрации употребляют понятие разности концентраций диффундирующего вещества по обе стороны мембраны, а вместо коэффициента диффузии — коэффициент проницаемости (Р), зависящий также от толщины мембраны. Одним из возможных путей проникновения веществ в клетку является растворение их в липидах клеточных мембран, что подтверждается существованием прямой пропорциональной зависимости между коэффициентом проницаемости большого класса хим. соединений и коэффициентом распределения вещества в системе масло — вода. В то же время вода не подчиняется этой зависимости, скорость ее проникновения значительно выше и не пропорциональна коэффициенту распределения в системе масло — вода. Для воды и растворенных в ней низкомолекулярных веществ наиболее вероятным способом П. является прохождение через мембранные поры. Т. о., диффузия веществ через мембрану может происходить путем растворения этих веществ в липидах мембраны; путем прохождения молекул через полярные поры, образуемые полярными, заряженными группами липидов и белков, а также путем прохождения через незаряженные поры. Особыми видами являются облегченная и обменная диффузии, обеспечиваемые белками и жирорастворимыми веществами-переносчиками, которые способны связывать переносимое вещество по одну сторону мембраны, диффундировать с ним через мембрану и освобождать его по другую сторону мембраны. Скорость переноса вещества через мембрану в случае облегченной диффузии значительно выше, чем при простой диффузии. Роль специфических переносчиков ионов могут выполнять некоторые антибиотики (валиномицин, нигерицин, моненсин и ряд других), получившие название ионофорных (см. Ионофоры). Расшифрована молекулярная организация комплексов ионофорных антибиотиков с катионами. В случае валиномицина (рис. 1) показано, что после связывания с катионом калия молекула пептида изменяет конформацию, приобретая вид браслета с внутренним диаметром ок. 0,8 нм, в к-ром ион калия удерживается в результате ион-дипольных взаимодействий.
Распространенным видом пассивной П. клеточных мембран для полярных веществ является П. через поры. Хотя непосредственное наблюдение пор в липидном слое мембраны представляет трудную задачу, экспериментальные данные свидетельствуют об их реальном существовании. В пользу реального существования пор свидетельствуют также данные об осмотических свойствах клеток. Величина осмотического давления в растворах, окружающих клетку, может быть рассчитана по формуле:
где π — осмотическое давление; С — концентрация растворенного вещества; R — газовая константа; Т — абсолютная температура; σ — коэффициент отражения. Если скорость прохождения через мембрану молекулы растворенного вещества соизмерима со скоростью прохождения молекул воды, то величины сил будут близки к нулю (осмотическое изменение объема клетки отсутствует); если клеточная мембрана непроницаема для данного вещества, то величина σ стремится к 1 (осмотическое изменение объема клетки максимально). Скорость проникновения молекул через клеточную мембрану зависит от размеров молекулы и, таким образом, путем подбора молекул определенного размера и наблюдения за изменением объема клеток в растворе данного вещества можно определить размеры клеточных пор. Напр., мембрана аксона кальмара слабопроницаема для молекул глицерина, имеющих в радиусе ок. 0,3 нм, но проницаема для веществ с меньшими размерами молекул (табл.). Аналогичные эксперименты с другими клетками показали, что размеры пор в клеточных мембранах, в частности в мембранах эритроцитов, кишечной палочки, клеток эпителия кишечника и др., достаточно точно укладываются в пределах 0,6—0,8 нм.
| Название раствора неэлектролита | Радиус молекулы (в нм) | Коэффициент отражения (σ) |
| Метиловый спирт | 0,183 | 0,35 |
| Формамид | 0,196 | 0,44 |
| Этиловый спирт | 0,213 | 0,63 |
| Мочевина | 0,217 | 0,70 |
| Этиленгликоль | 0,224 | 0,72 |
| Глицерин | 0,277 | 0,96 |
Проникновение в клетки крупных макромолекул белка, нуклеиновых к-т. клеточных ферментов и целых клеток осуществляется по механизму фагоцитоза (захвата и поглощения клеткой крупных твердых частиц) и пиноцитоза (захвата и поглощения частью клеточной поверхности окружающей жидкости с растворенными в ней веществами).
П. клеточных мембран имеет больше значение для функционирования клеток и тканей.
Активный транспорт ионов и сопутствующее ему поглощение воды в клетках почечного эпителия происходит в проксимальных канальцах почки (см. Почки). Через почки взрослого человека ежедневно проходит до 1800 л крови. Белки при этом отфильтровываются и остаются в крови, 80% солей и воды, а также вся глюкоза поступают обратно в кровяное русло. Считается, что первопричиной этого процесса является трансцеллюлярный активный транспорт ионов натрия, обеспечиваемый Na+ K+-зависимой АТФ-азой, локализованной в клеточных мембранах базального эпителия. Если в русле почечного проксимального канальца концентрация ионов натрия составляет ок. 100 ммоль/л, то внутри клетки она не превышает 37 ммоль/л; вследствие этого пассивный поток ионов натрия направлен внутрь клетки. Пассивному проникновению катионов в цитоплазму способствует также наличие мембранного потенциала (внутренняя поверхность мембраны заряжена отрицательно). Т. о. внутрь клетки ионы натрия проникают пассивно в соответствии с концентрационным и электрическим градиентами (см. Градиент). Выход же ионов из клетки в плазму крови осуществляется против концентрационного и электрического градиентов. Установлено, что именно в базальной мембране и локализован натрий-калиевый насос, обеспечивающий удаление ионов натрия. Предполагается, что анионы хлора движутся вслед за ионами натрия по межклеточному пространству. В результате этого осмотическое давление плазмы крови возрастает, и вода из русла канальца начинает поступать в плазму крови, обеспечивая реабсорбцию соли и воды в почечных канальцах.
Для изучения пассивной и активной П. используются различные методы. Значительное распространение получил метод меченых атомов (см. Изотопы, Радиоактивные препараты, Радиоизотопное исследование). Для изучения ионной П. клеток используются изотопы 42 K, 22 Na и 24 Na, 45 Ca, 86 Rb, 137 Cs, 32 P и др.; для изучения П. воды — дейтериевая или тритиевая вода, а также вода, меченная по кислороду (18O); для изучения П. сахаров и аминокислот — соединения, меченные по углероду 14 C или сере 35 S; для изучения П. белков — иодированные препараты, меченные по 1 31 I.
Широко применяются при исследовании П. витальные красители. Сущность метода заключается в наблюдении под микроскопом скорости проникновения молекул красителя внутрь клетки. Для большинства витальных красителей (нейтральный красный, метиленовый синий, родамин и др.) наблюдения проводятся в видимой части спектра. Используются также флюоресцирующие соединения, и среди них флюоресцеин натрия, хлортетрациклин, мурексид и др. При исследовании мышц было показано, что П. молекул красителей зависит не только от свойств клеточной мембраны, но и от сорбирующей способности внутриклеточных структур, чаще всего белков и нуклеиновых к-т, с к-рыми красители связываются.
Для изучения П. воды и растворенных в ней веществ применяют осмотический метод. При этом с помощью микроскопа или измерения светорассеяния суспензии частиц наблюдают за изменением объема клеток в зависимости от тоничности окружающего р-ра. Если клетка находится в гипертоническом р-ре, то вода из нее переходит в раствор и клетка сжимается. Противоположный эффект наблюдается в гипотоническом р-ре.
Все чаще для изучения Проницаемости клеточных мембран применяют потенциометрические методы (см. Микроэлектродный метод исследования, Электропроводность биологических систем); широкий набор ионоспецифичных электродов позволяет исследовать кинетику транспорта многих неорганических ионов (калия, натрия, кальция, водорода и др.), а также некоторых органических ионов (ацетатов, салицилатов и др.). Все виды П. клеточных мембран в той или иной степени характерны для многоклеточных тканевых мембранных систем — стенок кровеносных сосудов, эпителия почек, слизистой оболочки кишечника и желудка. Вместе с тем для П. сосудов характерны некоторые особенности, проявляющиеся в нарушении сосудистой П. (см. ниже).
Содержание
Патологическая физиология сосудистой проницаемости
Термином «сосудистая проницаемость» пользовались для обозначения гистогематического и транскапиллярного обмена, распределения веществ между кровью и тканями, тканевой П., гемолимфатического перехода веществ и других процессов. Некоторые исследователи применяют этот термин для обозначения трофической функции капилляро-соединительнотканных структур. Неоднозначность использования термина было одной из причин противоречивости взглядов по ряду вопросов, особенно касающихся регуляции сосудистой П. В 70-х гг. 20 в. термин «сосудистая проницаемость» стали использовать гл. обр. для обозначения избирательной проницаемости, или барьернотранспортной функции, стенок кровеносных микрососудов. Имеется тенденция к отнесению к сосудистой П. также и П. стенок не только микрососудов (кровеносных и лимфатических), но и крупных сосудов (вплоть до аорты).
Изменения сосудистой П. наблюдаются гл. обр. в форме повышения избирательной П. для макромолекул и клеток крови. Типичным примером этого является экссудация (см.). Понижение сосудистой П. связывают в основном с белковым пропитыванием и последующим уплотнением сосудистых стенок, что наблюдается, напр., при гипертонической болезни (см.).
Существует мнение о возможности нарушения П. сосудистой стенки преимущественно в направлении интерстиция или из интерстиция в кровь. Однако преимущественное движение веществ в ту или другую сторону относительно сосудистой стенки еще не доказывает его связь с состоянием барьерно-транспортной функции сосудистой стенки.
Принципы изучения нарушений сосудистой проницаемости
Оценку состояния сосудистой П. необходимо проводить с учетом того, что сосудистая стенка обеспечивает разграничение и функциональную связь двух смежных сред (крови и внутритканевой среды), являющихся основными компонентами внутренней среды организма (см.). Обмен между этими смежными средами в целом осуществляется за счет микрогемоциркуляции (см. Микроциркуляция), а сосудистая стенка с ее барьерно-транспортной функцией выступает лишь в качестве основы органной специализации гистогематического обмена. Поэтому метод изучения состояния сосудистой П. можно считать адекватным только тогда, когда он позволяет оценивать качественные параметры гистогематического обмена с учетом их органоспецифичности и независимо от состояния органной микрогемоциркуляции и характера обменных процессов, формирующихся вне сосудистой стенки. С этой точки зрения наиболее адекватным из существующих методов является электронно-микроскопический метод изучения сосудистой П., позволяющий прямым способом наблюдать пути и механизмы проникновения веществ через сосудистую стенку. Особенно плодотворным оказалось сочетание электронной микроскопии с так наз. трассирующими индикаторами, или трейцерами, метящими пути своего движения через сосудистую стенку. В качестве таких индикаторов могут быть использованы любые нетоксические вещества, выявляемые с помощью электронной микроскопии или специальных приемов (гистохимически, радиоавтографически, иммуноцитохимически и др.). С этой целью применяют железосодержащий белок ферритин, различные ферменты с пероксидазной активностью, коллоидный уголь (очищенную черную тушь) и т. д.
Из непрямых методов изучения состояния барьерно-транспортной функции стенок кровеносных сосудов наиболее широкое распространение получила регистрация проникновения через сосудистую стенку естественных или искусственных индикаторов, слабо или вообще не проникающих через стенку в условиях нормы. При нарушении микрогемоциркуляции, что часто наблюдается при нарушении сосудистой П., эти методы могут быть малоинформативными, и тогда следует сочетать их с методами контроля состояния микрогемоциркуляции, напр. с помощью биомикроскопии или легкодиффундирующих индикаторов, гистогематический обмен которых не зависит от состояния сосудистой П. и тканевого метаболизма. Недостатком всех непрямых методов, основанных на регистрации накопления индикаторных веществ за пределами сосудистого русла, является необходимость учета массы факторов, способных существенно повлиять на уровень индикатора в изучаемом участке. Кроме того, эти методы довольно инерционны и не позволяют изучать кратковременные и обратимые изменения сосудистой П., особенно в сочетании с изменением микрогемоциркуляции. Эти трудности удается частично преодолеть с помощью метода меченых сосудов, основанного на определении проникновения в сосудистую стенку слабодиффундирующего индикатора, накапливающегося в стенке и окрашивающего ее. Окрашенные (меченые) участки выявляются с помощью светового микроскопа и являются доказательством нарушения П. эндотелия. В качестве индикатора может быть использован коллоидный уголь, образующий легко выявляемые темные скопления в местах грубого нарушения эндотелиального барьера. Изменения активности микровезикулярного транспорта этим методом не регистрируются и необходимо применять другие индикаторы, переносимые через эндотелий микровезикулами.
Возможности изучения нарушений сосудистой П. в условиях клиники более ограниченны, т. к. большинство методов, основанных на использовании микромолекулярных легко диффундирующих индикаторов (в т. ч. и радиоизотопов), не позволяют однозначно судить о состоянии барьерно-транспортной функции стенок кровеносных сосудов.
В клинической практике о состоянии регионарной сосудистой П. нередко судят по наличию внутритканевых или полостных скоплений свободной жидкости, богатой белком. Однако при оценке состояния сосудистой П., напр. в брюшной полости, может быть сделано ошибочное заключение, поскольку обменные микрососуды этих органов и тканей в норме характеризуются высокой П. для макромолекул благодаря прерывистости или пористости их эндотелия. Увеличение фильтрационного давления в таких случаях ведет к образованию богатого белком выпота. Особенно проницаемы для белковых молекул венозные синусы и синусоиды.
Следует отметить, что повышенный выход плазменных белков в ткань и развитие тканевого отека (см.) не всегда сопутствуют повышению сосудистой П. Микрососуды (капилляры и венулы), эндотелий которых в норме слабопроницаем для макромолекул, приобретают эндотелиальные дефекты; через эти дефекты легко выходят в подэндотелиальное пространство введенные в кровоток индикаторы — макромолекулы и микрочастицы. Однако признаки тканевого отека при этом отсутствуют — так наз. безотековая форма нарушения сосудистой проницаемости. Подобное явление наблюдается, напр., в мышцах животных при развитии в них нейродистрофического процесса, связанного с перерезкой двигательного нерва. Сходные изменения в тканях человека описаны, напр., при старении и сахарном диабете, когда образуются так наз. ацеллюлярные капилляры, т. е. обменные микрососуды с частично или полностью слущенными эндотелиальными клетками (признаки тканевого отека при этом также отсутствуют). Все эти факты говорят, с одной стороны, об относительности связи тканевых отеков с повышением сосудистой П., а с другой — о существовании внесосудистых механизмов, ответственных за распределение воды и веществ между кровью и тканями.
Факторы нарушения сосудистой проницаемости
Факторы нарушения сосудистой проницаемости условно делят на две группы: экзогенные и эндогенные. Экзогенные факторы нарушения сосудистой П. различной природы (физической, химической и др.) в свою очередь делятся на факторы, непосредственно влияющие на сосудистую стенку и ее барьерно-транспортную функцию напр., гистамин, введенный в сосудистое русло, различные токсины и т. п.), и факторы нарушения П. непрямого действия, эффект которых опосредуется через эндогенные факторы.
К уже известным эндогенным факторам нарушения сосудистой П. (гистамин, серотонин, кинины) стали относить большое число других, в частности простагландины (см.), причем последние не только повышают сосудистую П., но и усиливают действие других факторов; многие из эндогенных факторов продуцируются различными ферментными системами крови (системой фактора Хагемана, системой комплемента и др.).
Повышают сосудистую П. и иммунные комплексы. Из фактора, ответственного за «отсроченное» повышение сосудистой П. при развитии феномена Артюса, Йосинага (1966) выделил псевдоглобулин; Куроянаги (1974) открыл новый фактор П., обозначенный им как Ig-PF. По своим свойствам он существенно отличается от гистамина, кининов, анафилатоксина и калликреина, действует дольше, чем гистамин и брадикинин, угнетается витаминами K1 и K2.
Многие факторы нарушения сосудистой П. продуцируются лейкоцитами. Так, с поверхностью нейтрофилов связана протеаза, образующая из белков плазмы нейтральный пептидный медиатор, повышающий соудистую П. Белковый субстрат протеазы имеет мол. вес (массу) 90 000 и отличается от кининогена.
В лизосомах и специфических гранулах клеток крови содержатся катионные белки, способные нарушать сосудистую Проницаемость. Их действие опосредуется гистамином тучных клеток.
Различные эндогенные факторы нарушения сосудистой П. действуют в тканях одновременно или последовательно, вызывая в. сосудистой П. фазовые сдвиги. В связи с этим выделяют ранние, отсроченные и поздние изменения сосудистой П. Ранняя фаза — фаза действия гистамина (см.) и серотонина (см.). Вторая фаза развивается после периода мнимого благополучия, спустя 1—3 часа после первичного повреждения — замедленная, или отсроченная фаза; ее развитие обусловливается действием кининов (см.) или простагландинов. Развитие этих двух фаз зависит от уровня комплемента и угнетается антикомплементарной иммунной сывороткой. Через сутки после повреждения развивается третья фаза, связываемая с действием цито- и протеолитических ферментов, освобождающихся из лизосом лейкоцитов и лимфоцитов. В зависимости от природы первичного повреждающего агента количество фаз может быть разным. В раннюю фазу сосудистая П. нарушается гл. обр. на уровне венул, в последующие фазы процесс распространяется на капиллярное русло и артериолы.
Рецепция факторов проницаемости сосудистой стенкой. Эндогенные факторы нарушения П. представляют наиболее важную группу причин нарушения сосудистой П. Отдельные из них находятся в тканях в готовом виде (гистамин, серотонин) и под влиянием различных патогенных воздействий освобождаются из депо, в роли которых выступают тучные клетки и клетки крови (базофилы, тромбоциты). Другие факторы являются продуктом разных биохимических систем как в месте первичного повреждения, так и на расстоянии от него.
Вопросы происхождения факторов П. сами по себе важны для решения практических задач профилактики и лечения нарушений сосудистой П. Однако появление фактора П. еще не достаточно для нарушения сосудистой П. Для того чтобы фактор П. стал действительно фактором нарушения сосудистой П., он должен быть «замечен», т. е. рецептирован, сосудистой стенкой (если только он не обладает деструктурирующей способностью подобно цитолитическим агентам). Известно, напр., что гистамин, введенный в общий кровоток, нарушает сосудистую П. лишь в определенных органах и тканях, тогда как в других тканях (головной мозг, легочная ткань, эндоневрий и др.) он не эффективен. У лягушек введение в сосудистое русло серотонина и брадикинина вообще не вызывает нарушения сосудистой П. Однако причины неэффективности гистамина в обоих случаях различны.
По современным данным, эндотелий обменных микрососудов теплокровных животных и человека обладает чувствительностью к большому числу разнообразных агентов, т. е. характеризуется высокой рецепторной способностью. Что касается гистамина — одного из основных факторов П., вызывающего острое и значительное (хотя и кратковременное) нарушение сосудистой П., то экспериментальные данные говорят о наличии в эндотелии двух типов гистаминовых рецепторов H1 и H2, играющих разную роль в механизме действия гистамина. Именно стимуляция H1-рецепторов приводит к нарушению сосудистой П., характерному для действия гистамина.
При действии некоторых эндогенных факторов П., в частности гистамина, наблюдается тахифилаксия (см.) и повторное применение (через 30 мин.) агента уже не нарушает сосудистую П. Подобная временная нечувствительность эндотелия микрососудов не объясняется временной блокадой соответствующих рецепторов, хотя в некоторых случаях это и может быть. В случае с гистамином механизм тахифилаксии, по нек-рым сведениям, имеет внерецепторную локализацию. Это доказывается, в частности, фактом развития перекрестной тахифилаксии, когда применение гистамина ведет к развитию устойчивости эндотелия не только к самому гистамину, но и к солям лантана, действующим в обход рецепторов. Возникновение перекрестной тахифилаксии может быть одной из причин неэффективности отдельных факторов П., действующих одновременно или последовательно.
Ультраструктурные основы и эффекторные механизмы нарушения сосудистой проницаемости
Электронно-микроскопическими исследованиями выявлено, что морфол. основой повышения сосудистой П. является образование широких каналов в области межклеточных соединений в эндотелии (рис. 2). Такие каналы, или «течи», часто называют гистаминовыми щелями, т. к. их образование типично для действия на сосудистую стенку гистамина и впервые подробно изучено именно при его действии. Гистаминовые щели образуются гл. обр. в стенках венул тех органов и тканей, где отсутствуют малопроницаемые гистогематические барьеры типа гематоэнцефалического и др. Локальные расхождения межклеточных контактов обнаружены при нейрорегуляторных расстройствах, механических, термических, химических и других видах повреждений тканей, при действии различных биорегуляторов (серотонина, брадикинина, простагландинов Е1 и Е2 и т. д.). Нарушение межклеточных контактов возникает, хотя и с большим трудом, в капиллярах и артериолах и даже в более крупных сосудах. Легкость образования гистаминовых щелей прямо пропорциональна исходной структурной слабости межклеточных соединений, к-рая возрастает при переходе от артериол к капиллярам и от капилляров к венулам, достигая максимума на уровне посткапиллярных (перицитарных) венул.
Неэффективность гистамина в нарушении сосудистой П. некоторых органов хорошо объясняется именно с точки зрения развития плотных соединений в эндотелии микрососудов этих органов, напр. мозга.
В теоретическом и практическом отношении важен вопрос об эффекторных механизмах, лежащих в основе образования структурных дефектов типа гистаминовых щелей. Эти ультраструктурные сдвиги типичны именно для начальной фазы острого воспаления (см.), когда, по данным И. И. Мечникова (1891), повышение сосудистой П. биологически целесообразно, т. к. благодаря этому обеспечивается повышенный выход фагоцитов к очагу повреждения. Можно добавить, что повышенный выход плазмы в таких случаях также целесообразен, т. к. при этом в очаг доставляются антитела и средства неспецифической защиты. Т. о., повышение сосудистой П. в очаге воспаления можно рассматривать как специфическое состояние барьерно-транспортной функции стенок микро-сосудов, адекватное новым условиям существования ткани, а изменение сосудистой П. при воспалении и сходных ситуациях — не как нарушение, а как новое функциональное состояние, способствующее восстановлению нарушенного тканевого гомеостаза. Следует учитывать, что в некоторых органах (печень, селезенка, костный мозг), где в соответствии с особенностями органных функций существует непрерывный обменный поток клеток и макромолекул, межклеточные «течи» являются нормальными и постоянными образованиями, представляющими собой утрированные гистаминовые щели, но в отличие от истинных гистаминовых щелей способны к длительному существованию. Истинные гистаминовые щели образуются в первые же секунды после воздействия на эндотелий медиаторов острого воспаления и в большинстве своем через 10—15 мин. закрываются. Механизм образования гистаминовых щелей имеет защитный, филогенетически обусловленный характер и связан со стереотипной реакцией на клеточном уровне, запускаемой стимуляцией разных типов рецепторов.
Природа этой стереотипной реакции долго оставалась неизученной. И. И. Мечников считал, что повышение сосудистой П. при воспалении связано с сокращением эндотелиальных клеток. Однако позже было установлено, что эндотелиоциты в сосудах теплокровных не относятся к категории клеток, активно меняющих свою форму подобно мышечным. Роули (D. A. Rowley, 1964) высказал предположение, что расхождение эндотелиоцитов является следствием повышения внутрисосудистого давления и связанного с этим перерастяжения эндотелия. Прямые измерения доказали неприемлемость этой гипотезы в отношении венул и капилляров, однако для артериальных сосудов она имеет определенную ценность, т. к. при нарушении тонической активности мышечной оболочки высокое внутрисосудистое давление действительно способно вызвать перерастяжение эндотелия и повреждение межклеточных контактов. Но и в этом случае появление гистаминовых щелей в интиме не всегда связано с действием трансмурального давления. Робертсон и Кайраллах (A. L. Robertson, P. A. Khairallah, 1972) в опытах на изолированном сегменте брюшной аорты кролика показали, что широкие щели в эндотелии образуются под влиянием ангиотензина II в местах округления и укорочения эндотелиоцитов. Сходные морфол. сдвиги обнаружены и в эндотелии обменных микрососудов кожи при местном применении ангиотензина II, простагландина Е1 и сывороточных триглицеридов.
О. В. Алексеев и А. М. Чернух (1977) обнаружили у эндотелиоцитов обменных микрососудов способность, к быстрому увеличению содержания в цитоплазме микрофибриллярных структур, сходных по своим морфологическим признакам с актиновыми микронитями. Этот обратимый феномен (так наз. феномен оперативной структурализации микрофибриллярного аппарата) развивается под влиянием факторов, вызывающих образование широких межклеточных щелей. Обратимость феномена в случае применения гистамина затрудняет его выявление и хорошо объясняет кратковременность и обратимость существования гистаминовых щелей. С помощью цитохалазина-Б, блокирующего образование актиновых микрофибрилл, выявляется патогенетическое значение данного феномена в механизме образования межклеточных гистаминовых щелей. Эти факты говорят о наличии у эндотелиоцитов скрытой способности к сокращению, реализующейся в условиях, когда прежний уровень сосудистой П. оказывается неадекватным и требуется сравнительно быстрое и обратимое его изменение. Изменение сосудистой П. выступает, т. о., как особый акт биол. регуляции, обеспечивающий адаптацию барьерно-транспортной функции сосудистого эндотелия в соответствии с новыми местными потребностями, остро возникшими в связи с изменением условий жизнедеятельности ткани.
Наличие в тканях механизма изменения сосудистой П. можно отнести к так наз. факторам риска, т. к. срабатывание этого механизма в неадекватных условиях может стать причиной нарушения тканевого гомеостаза и органной функции, а не проявлением действия адаптационно-защитных механизмов. Основные пути нарушения сосудистой П. представлены на схеме. В основе изменения сосудистой П. лежат механизмы, не только приводящие к образованию межклеточных каналов (гистаминовых щелей), но и влияющие на активность клеточной поверхности (т. е. на микровезикуляцию и микровезикулярный транспорт, вакуолизацию и микропузыреобразование). Результатом может быть перфорация эндотелиоцитов с образованием более или менее обширных и долговременных трансцеллюлярных каналов.
Большое значение в механизмах нарушения сосудистой П. придается локальным изменениям поверхностного электрического заряда, особенно на мембранах, закрывающих поры в фенестрированных капиллярах (напр., почечных клубочков). По нек-рым данным, одно только изменение заряда может быть основой повышения выхода белков из клубочковых капилляров. Т. о. доказывается ограниченность теории пор, в соответствии с к-рой П. зависит лишь от размера и соотношения гипотетических крупных и мелких пор в стенках сосудов. В условиях патологии эффект повышения пористости эндотелия может достигаться разными путями: образованием межклеточных каналов типа гистаминовых щелей; усилением микровезикулярного и интравакуолярного транспорта; перфорацией эндотелиоцитов на основе усиления микровезикуляции, вакуолизации или микропузыреоб разования в эндотелии; микроочаговой деструкцией эндотелиоцитов; слущиванием эндотелиоцитов; изменением физ.-хим. свойств поверхности эндотелиоцитов и др. (см. Микроциркуляция]]). Этот же эффект может быть достигнут и за счет внестеночных механизмов, в частности за счет изменения связывательной способности макромолекул крови, с к-рыми взаимодействуют почти все известные индикаторы, используемые для оценки состояния сосудистой П. В условиях патологии чаще всего одновременно или последовательно действуют разные из перечисленных механизмов. Так, напр., гистамин повышает пористость сосудистой стенки за счет образования гистаминовых щелей в эндотелии венул, а также путем влияния на поверхность эндотелиоцитов и связанные с ее активностью транспортные процессы и ультраструктурные трансформации (образование трансцеллюлярных пор, фенестр, микроканальцев и др.). Необходимо учитывать, что при этом часто меняется толщина эндотелиоцитов и глубина межклеточных щелей, что может оказывать существенное влияние на проницаемость сосудистой стенки как диффузионного барьера. Совершенно не изучен вопрос о поведении в условиях патологии биохим. механизмов, препятствующих или, наоборот, способствующих проникновению через сосудистую стенку веществ, особенно биологически активных. Известно, напр., что эндотелиоциты мозговых капилляров в норме обладают ферментативной активностью, разрушающей серотонин и тем самым препятствующей его проникновению как из крови в мозг, так и в обратном направлении. Эндотелий легочных капилляров содержит кининазу II, локализуемую в микропиноцитозных везикулах и обеспечивающую разрушение брадикинина и одновременно превращение ангиотензина I в ангиотензин II (гипертензии). Т. о., эндотелий осуществляет своеобразный контроль баланса гуморальных биорегуляторов, активно влияет на гистогематический обмен этих агентов.
Этиопатогенетические основы профилактики и лечения нарушений сосудистой проницаемости
Направленное вмешательство осуществляется на трех уровнях (см. схему). Первый уровень — воздействие на процесс образования причинных (рецептируемых) факторов — практически не используется, хотя имеются отдельные медикаментозные средства, способные действовать именно на этом уровне. Напр., резерпин влияет на депонирование факторов нарушения П. в тучных клетках, представляющих собой основной источник медиаторов острого воспаления (гистамина и серотонина); антипростагландиновые средства угнетают синтез простагландинов — ацетилсалициловая кислота и др.
Второй уровень является основным в практике разработки средств профилактики и лечения нарушений сосудистой П. Он соответствует процессу рецепции причинного фактора. Используется значительное число антигистаминовых, антисеротониновых и антибрадикининовых препаратов, предупреждающих нарушения сосудистой П., вызываемые соответствующими медиаторами. Достоинством и в то же время недостатком данных препаратов, действующих путем блокады специфических рецепторов, является их высокая специфичность. Такая специфичность делает их неэффективными в условиях множественности этиол. факторов, действующих одновременно или последовательно, что обычно наблюдается в клин. практике. Важно и то, что исключение действия одного фактора или нескольких, определяющих развитие одной фазы нарушения сосудистой П., не исключает развитие последующих фаз. Эти недостатки могут быть преодолены путем вмешательства на третьем уровне.
Третий уровень — воздействие на внутриклеточные (субклеточные) эффекторные механизмы, через которые непосредственно реализуется действие факторов П., причем единые для действия различных патогенных агентов. Реальность и эффективность такого подхода удается продемонстрировать в эксперименте путем применения вещества (цитохалазина-Б), угнетающего феномен оперативной структурализации микрофибриллярного аппарата в эндотелиоцитах (образование актинового геля и актиновых микрофибрилл).
В клин. практике с целью нормализации повышенной сосудистой П. используют витамин P (см. Биофлавоноиды) и соли кальция. Однако эти препараты не могут рассматриваться как специфические лечебные средства при нарушении сосудистой Проницаемости, хотя они и оказывают общеукрепляющее влияние на гистогематические барьеры, мембраны и стенку сосудов в частности.
Для повышения сосудистой П. могут быть использованы различные эндогенные факторы П., напр. гистамин, или вещества, освобождающие их из тканевых депо.
Библиография: Алексеев О. В. Микроциркуляторный гомеостаз, в кн.: Гомеостаз, под ред. П. Д. Горизонтова, с. 278, М., 1976; Антонов В. Ф. Липиды и ионная проницаемость мембран, М., 1982; Биологические мембраны, под ред. Д. С. Парсонса, пер. с англ., М., 1978; Де Робертис Э., Новинский В. и Саэс Ф. Биология клетки, пер. с англ., М., 1967; Живая клетка, пер. с англ., под ред. Г. М. Франка, с. 130, М., 1962; Казначеев В.П. и Дзизинский А. А. Клиническая патология транскапиллярного обмена, М., 1975; Лайтфут Э. Явления переноса в живых системах, пер. с англ., М., 1977; Лакшминараянайах Н. Мембранные электроды, пер. с англ., Л., 1979; Лев А. А. Моделирование ионной избирательности клеточных мембран, Л., 1976; Овчинников Ю. А., Иванов В. Т. и Шкроб А. М. Мембранно-активные комплексоны, М., 1974; Структура и функция клетки, пер. с англ., под ред. Г. М. Франка, с. 173, М., 1964; Трошин А. С. Проблема клеточной проницаемости, М. — Л., 1956; Чернух А. М., Александров П. Н. и Алексеев О. В. Микроциркуляция, М., 1975; Di Rosa М., Giroud J. Р. а. Willoughby D. A. Studies of the mediators of the acute inflammatory response induced ln rats in different sites by carra-geenan and turpentine, J. Path., v. 104, p. 15, 1971; Majnо G. а. Pаlade G. E. Studies on inflammation, I. The effect of histamine and serotonin on vascu-lar permeability, an electron microscopic study, J. biophys. biochem. Cytol., v. 11, p. 571, 1961; Majnо G., Shea S. M. a. Leventhal M. Endothelial cont-raction induced by histamine-type mediators, J. Cell Biol., v. 42, p. 647, 1969: Shimamoto T. Contraction of endothelial cells as a key mechanism in athero-genesis and treatment of atherosclerosis with endothelial cell relaxants, в кн.: Atherosclerosis III, ed. by G. Schettler a. A. Weizel, p. 64, В.—N. Y., 1974.
B. Ф. Антонов; О. В. Алексеев (пат. физ.).