Признаки обструкции выходного тракта лж что это
Динамическая обструкция выходного отдела левого желудочка не всегда ассоциирована с ГКМП. Гипердинамическая систолическая функция ЛЖ, связанная с приемом лекарственных препаратов или С другими факторами, может стать причиной динамической обструкции ВОЛЖ, гемодинамически не отличимой от ГКМП с гипертрофией базального отдела МЖП. У пожилых больных с АГ при лечении вазодилататорами, диуретиками или дигоксином возможно развитие динамической обструкции, которая проявляется одышкой, болью в груди или гипотензией, нарастающей нa фоне лечения.
Это состояние называют гипертензивиой ГКМП, оно четко отличается от истинной ГКМП. Динамическая обструкция ВОЛЖ часто развивается в постоперационном периоде, когда снижен внутрисосудистый объем и назначены инотропные препараты. Пациенты со стенозом АК или ПМК особенно уязвимы в плане развития обструкции ВОЛЖ после протезирования ЛК или восстановительной операции на МК. Острая обструкция ВОЛЖ может появиться после острого передпеперегородочного ИМ, у некоторых больных с синдромом шаровидной верхушки, когда динамическую обструкцию выходного отдела левого желудочка (ВОЛЖ) вызывают передпесистолическое движение и ассоциация с MP.
Изолированный субаортальный стеноз может имитировать обструктивную ГКМП; однако в спектре скоростей на НВ ДЭхоКГ при субаортальном стенозе не бывает динамического позднего пика, он напоминает таковой при клапанном аортальном стенозе. Динамическая обструкция ВОЛЖ также может быть первым признаком амилоидоза сердца.
Апикальная гипертрофическая кардиомиопатия
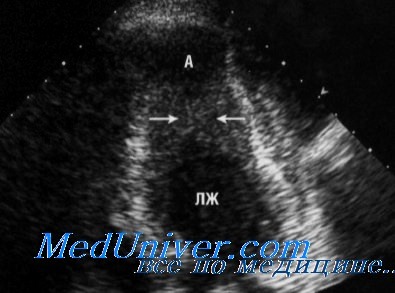
Апикальная гипертрофическая кардиомиопатия (ГКМП) может быть не диагностирована при двухмерной ЭхоКГ из парастернального доступа, поскольку этот вид гипертрофии ограничивается областью верхушки сердца. Апикальная ГКМП лучше всего визуализируется из апикальной позиции по короткой оси и апикальной четырехкамерной позиции при четком определении эндокардиальной поверхности. При этом определяются утолщение стенки ЛЖ в области верхушки и облитерация его полости в области верхушки во время систолы. Вследствие массивной апикальной ГКМП движение стенки в области эпикарда может напоминать дискинезию.
Апикальную ГКМП следует дифференцировать от облитерации полости АЖ в области верхушки, обусловленной гиперэозинофильным синдромом или аномальной трабекуляризацией верхушки при некомпактном миокарде. Введение в/в контраста хорошо помогает в визуализации малой полости в области верхушки с конфигурацией «туза», типичной для апикальной ГКМП. Это состояние обычно проявляется гигантскими зубцами Т в грудных отведениях.
Если медикаментозная терапия не способна облегчить симптоматику или обструкцию, следует обсудить целесообразность хирургической миоэктомии или алкогольной аблации. ЭхоКГ позволяет определить распространенность и локализацию гипертрофии и может помочь в проведении вмешательства. Аблация МЖП алкоголем — эффективный метод снижения обструкции ВОЛЖ у ряда больных при наличии показаний. Эта процедура приводит к развитию инфаркта в базальном отделе МЖП, что увеличивает площадь ВОЛЖ.
Поскольку эта часть миокарда кровоснабжается перегородочными перфорантными артериями, важно до аблании визуализировать область, которая должна быть инфарцирована. Для этих целей хорошо подходит миокардиальпая контрастная ЭхоКГ. Базальпый отдел МЖП атрофируется вследствие повреждения, индуцированного алкоголем, что приводит к снижению ДР в ВОЛЖ, который можно точно определить при НВ ДЭхоКГ. Хирургическая миоэктомия остается «золотым стандартом» для устранения обструкции ВОЛЖ. Этот метод предпочтителен при диффузной гипертрофии МЖП или аномалиях папиллярных мышц, усугубляющих обструкцию, а также у больных с другими показаниями к хирургическому вмешательству на сердце.
Гипертрофическая кардиомиопатия
Гипертрофическая кардиомиопатия – первичное изолированное поражение миокарда, характеризующееся гипертрофией желудочков (чаще левого) при уменьшенном или нормальном объеме их полостей. Клинически гипертрофическая кардиомиопатия проявляется сердечной недостаточностью, болью в грудной клетке, нарушениями ритма, синкопальными состояниями, внезапной смертью. Диагностика гипертрофической кардиомиопатии включает проведение ЭКГ, суточного ЭКГ-мониторирования, ЭхоКГ, рентгенологического исследования, МРТ, ПЭТ сердца. Лечение гипертрофической кардиомиопатии проводится b-адреноблокаторами, блокаторами кальциевых каналов, антикоагулянтами, антиаритмическими препаратами, ингибиторами АПФ; в ряде случаев прибегают к кардиохирургической операции (миотомии, миоэктомии, протезированию митрального клапана, двухкамерной электрокардиостимуляции, имплантации кардиовертер-дефибриллятора).
Общие сведения
В кардиологии различают первичные (идиопатические) кардиомиопатии (гипертрофическую, констриктивную, дилатационную, рестриктивную, аритмогенную дисплазию правого желудочка) и специфические вторичные кардиомиопатии (алкогольную, токсическую, метаболическую, климактерическую и ряд других).
Гипертрофическая кардиомиопатия – самостоятельное, не зависящее от других сердечно-сосудистых заболеваний, значительное утолщение миокарда левого (реже правого) желудочка, сопровождающееся уменьшением его полости, нарушением диастолической функции с развитием нарушений сердечного ритма и сердечной недостаточности.
Причины
Гипертрофическая кардиомиопатия – заболевание с аутосомно-доминантным типом наследования, поэтому обычно носит семейный характер, что не исключает, однако, возникновение спорадических форм.
В основе семейных случаев гипертрофической кардиомиопатии лежат передаваемые по наследству дефекты генов, кодирующих синтез сократительных белков миокарда (гена тяжелой цепи b-миозина, гена сердечного тропонина Т, гена а-тропомиозина, гена, кодирующего сердечную изоформу миозин-связывающего белка). Спонтанные мутации этих же генов, происходящие под воздействием неблагоприятных факторов среды, обусловливают развитие спорадических форм гипертрофической кардиомиопатии.
Гипертрофия миокарда левого желудочка при гипертрофической кардиомиопатии не связана с врожденными и приобретенными пороками сердца, ИБС, гипертонической болезнью и другими заболеваниями, которые обычно приводят к подобным изменениям.
Патогенез
При обструкции выходного отдела левого желудочка имеет место утолщение межжелудочковой перегородки и нарушение движения передней створки митрального клапана. В связи с этим в период изгнания возникает перепад давления между полостью левого желудочка и начальным отрезком аорты, что сопровождается повышением конечного диастолического давления в левом желудочке. Возникающая в этих условиях компенсаторная гиперфункция сопровождается гипертрофией, а затем и дилатацией левого предсердия, в случае же декомпенсации развивается легочная гипертензия.
В ряде случаев гипертрофической кардиомиопатии сопутствует ишемия миокарда, обусловленная снижением вазодилататорного резерва коронарных артерий, увеличением потребности гипертрофированного миокарда в кислороде, сдавлением во время систолы интрамуральных артерий, сопутствующим атеросклерозом венечных артерий и т. д.
Макроскопическими признаками гипертрофической кардиомиопатии служит утолщение стенок левого желудочка при нормальных или уменьшенных размерах его полости, гипертрофия межжелудочковой перегородки, дилатация левого предсердия. Микроскопическая картина гипертрофической кардиомиопатии характеризуется беспорядочным расположением кардиомиоцитов, замещением мышечной ткани на фиброзную, аномальным строением интрамуральных венечных артерий.
Классификация
В соответствии с локализацией гипертрофии выделяют гипертрофическую кардиомиопатию левого и правого желудочков. В свою очередь, гипертрофия левого желудочка может быть асимметричной и симметричной (концентрической). В большинстве случаев выявляется асимметричная гипертрофия межжелудочковой перегородки на всем протяжении или в ее базальных отделах. Реже встречается асимметричной гипертрофия верхушки сердца (апикальная гипертрофическая кардиомиопатия), задней или переднебоковой стенки. На долю симметричной гипертрофии приходится около 30 % случаев.
С учетом наличия градиента систолического давления в полости левого желудочка различают обструктивную и необструктивную гипертрофическую кардиомиопатию. Симметричная гипертрофия левого желудочка, как правило, представляет собой необструктивную форму гипертрофической кардиомиопатии.
Асимметричная гипертрофия может являться как необструктивной, так и обструктивной. Так, синонимом асимметричной гипертрофии межжелудочковой перегородки служит понятие «идиопатический гипертрофический субаортальный стеноз», гипертрофии средней части межжелудочковой перегородки (на уровне папиллярных мышц) – «мезовентрикулярная обструкция». Верхушечная гипертрофия левого желудочка, как правило, представлена необструктивным вариантом.
В зависимости от степени утолщения миокарда выделяют умеренную (15-20 мм), среднюю (21-25 мм) и выраженную (более 25 мм) гипертрофию.
На основании клинико-физиологической классификации выделяют IV стадии гипертрофической кардиомиопатии:
Симптомы гипертрофической кардиомиопатии
Длительное время течение гипертрофической кардиомиопатии остается бессимптомным, клиническая манифестация чаще происходит в возрасте 25–40 лет. С учетом преобладающих жалоб выделяют девять клинических форм гипертрофической кардиомиопатии: малосимптомную, вегетодистоническую, кардиалгическую, инфарктоподобную, аритмическую, декомпенсационную, псевдоклапанную, смешанную, молниеносную. Несмотря на то, что каждый клинический вариант характеризуется определенными признаками, всем формам гипертрофической кардиомиопатии присущи общие симптомы.
Необструктивная форма гипертрофической кардиомиопатии, не сопровождающаяся нарушением оттока крови из желудочка, обычно малосимптомна. В этом случае жалобы на одышку, перебои в работе сердца, неритмичный пульс могут отмечаться при выполнении физической нагрузки.
Диагностика
При диагностическом поиске обнаруживается систолический шум, высокий, скорый пульс, смещение верхушечного толчка. Инструментальные методы обследования при гипертрофической кардиомиопатии включают ЭхоКГ, ЭКГ, ФКГ, рентгенографию грудной клетки, холтеровское мониторирование, поликардиографию, ритмокардиографию. С помощью эхокардиографии выявляется гипертрофия МЖП, стенок миокарда желудочка, увеличение размеров левого предсердия, наличие обструкции ВТЛЖ, диастолическая дисфункция левого желудочка.
ЭКГ-признаки гипертрофической кардиомиопатии малоспецифичны и требуют дифференциальной диагностики с очаговыми изменениями миокарда, гипертонической болезнью, ИБС, аортальным стенозом и другими заболеваниями, осложняющимися гипертрофией левого желудочка. Для оценки тяжести гипертрофической кардиомиопатии, прогноза и выработки рекомендаций по лечению используются нагрузочные пробы (велоэргометрия, тредмил-тест).
Суточное мониторирование ЭКГ позволяет документировать пароксизмальные эпизоды желудочковой экстрасистолии и тахикардии, фибрилляции и трепетания предсердий. На фонокардиограмме регистрируется систолический шум различной степени выраженности, сохранность амплитуды I и II тонов. Сфигмография демонстрирует двухвершинную кривую каротидного пульса, характеризующуюся дополнительной волной на подъеме.
При рентгенологическом исследовании изменения контуров сердца (увеличение левых отделов сердца, расширение восходящей части аорты, выбухание ствола и расширение ветвей легочной артерии) обнаруживаются только в развернутой стадии гипертрофической кардиомиопатии. Для получения дополнительных данных за гипертрофическую кардиомиопатию прибегают к проведению зондирования левых отделов сердца, вентрикулографии, коронарографии, сканированию сердца с радиоизотопом таллия, МРТ, ПЭТ сердца. Окончательным подтверждающим методом служит генодиагностика.
Лечение гипертрофической кардиомиопатии
Пациентам с гипертрофической кардиомиопатией (особенно с обструктивной формой) рекомендуется ограничение физических нагрузок, которые могут спровоцировать увеличение градиента давления «левый желудочек-аорта», аритмии сердца и обмороки.
Прогноз гипертрофической кардиомиопатии
Течение гипертрофической кардиомиопатии вариабельно. Необструктивная форма гипертрофической кардиомиопатии протекает относительно стабильно, однако при длительном стаже заболевания все же развивается сердечная недостаточность. У 5–10% пациентов возможен самостоятельный регресс гипертрофии; у такого же процента больных отмечается переход гипертрофической кардиомиопатии в дилатационную; еще столько же пациентов сталкивается с осложнением в виде инфекционного эндокардита.
Лечение гипертрофической кардиомиопатии
Гипертрофическая кардиомиопатия (ГКМП) – это генетически обусловленное заболевание миокарда, проявляющееся комплексом специфических морфо-функциональных изменений
Лечение гипертрофической кардиомиопатии
Гипертрофическая кардиомиопатия (ГКМП) – это генетически обусловленное заболевание миокарда, проявляющееся комплексом специфических морфо-функциональных изменений и постепенно прогрессирующим течением с высоким риском развития жизнеугрожающих аритмий и внезапной смерти.
Типичными являются морфологические изменения: аномалия архитектоники сократительных элементов миокарда (гипертрофия и дезориентация мышечных волокон), развитие фибротических изменений мышцы сердца, патология мелких интрамиокардиальных сосудов.
При ГКМП происходит массивная гипертрофия миокарда левого (и реже правого желудочка), чаще асимметричного характера за счет утолщения межжелудочковой перегородки, часто с развитием обструкции выходного тракта левого желудочка (ЛЖ) при отсутствии каких-либо явных причин.
Общепризнанной является представление о преимущественно наследственной природе ГКМП. В связи с этим, широкое распространение получил термин «семейная гипертрофическая кардиомиопатия». К настоящему времени установлено, что более половины всех случаев заболевания являются наследуемыми, при этом основной тип наследования – аутосомно-доминантный. Оставшиеся приходятся на так называемую спорадическую форму; в этом случае у пациента нет родственников, болеющих ГКМП или имеющих гипертрофию миокарда. Считается, что большинство, если не все случаи спорадической ГКМП, также имеют генетическую причину, т. е. вызваны случайными мутациями.
Гипертрофическая кардиомиопатия – это генетически гетерогенное заболевание, причиной которого являются более 200 описанных мутаций нескольких генов, кодирующих белки миофибриллярного аппарата. К настоящему времени известны 10 белковых компонентов сердечного саркомера, выполняющих контрактильную, структурную или регуляторную функции, дефекты которых наблюдаются при ГКМП. Причем в каждом гене множество мутаций могут становиться причиной заболевания (полигенное мультиаллельное заболевание).
Наличие той или иной ассоциированной с ГКМП мутации признается «золотым» стандартом диагностики заболевания. При этом описанные генетические дефекты характеризуются разной степенью пенетрантности, выраженностью морфологических и клинических проявлений. Тяжесть клинической картины зависит от присутствия и степени гипертрофии.
Таким образом, ГКМП характеризуется крайней гетерогенностью вызывающих ее причин, морфологических, гемодинамических и клинических проявлений, разнообразием вариантов течения и прогноза, что существенно затрудняет выбор адекватных и наиболее эффективных лечебных подходов по контролю и коррекции имеющихся нарушений.
Возможны три гемодинамических варианта обструктивной ГКМП:
Cимптомы болезни разнообразны и малоспецифичны, связаны с гемодинамическими нарушениями (диастолическая дисфункция, динамическая обструкция путей оттока, митральная регургитация), ишемией миокарда, патологией вегетативной регуляции кровообращения и нарушением электрофизиологических процессов в сердце. Диапазон клинических проявлений крайне велик: от бессимптомных до неуклонно прогрессирующих и трудно поддающихся медикаментозному лечению форм, сопровождающихся тяжелой симптоматикой.
Повышение диастолического давления в левом желудочке из-за диастолической дисфункции, динамическая обструкция выносящего тракта левого желудочка проявляются одышкой в покое и при физической нагрузке, утомляемости, слабости. Нарастание давления в малом круге кровообращения сопровождается развитием острой левожелудочковой недостаточности (чаще в ночные часы – сердечная астма, альвеолярный отек легких).
Падение фракции выброса при физической нагрузке или нарушениях сердечного ритма сопровождается ухудшением кровообращения головного мозга. Преходящая ишемия мозговых структур проявляется кратковременной потерей сознания (обморок) или предобморочными состояниями (внезапная слабость, головокружение, потемнение в глазах, шум и «заложенность» в ушах).
Методы исследования:
ЭХО-КГ – основной метод диагностики ГКМП. Критериями диагностики ГКМП на основании данных ЭХО-КГ являются:
Если в покое обструкции выносящего тракта левого желудочка нет, ее можно спровоцировать медикаментозными (ингаляция амилнитрита, введение изопреналина, добутамина) или функциональными пробами (проба Вальсальвы, физическая нагрузка), которые уменьшают преднагрузку или повышают сократимость левого желудочка.
Катетеризация сердца и коронарная ангиография проводятся для оценки коронарного русла перед миоэктомией или операцией на митральном клапане, а также чтобы выяснить причину ишемии миокарда. При этом к характерным признакам ГКМП относят:
Сцинтиграфия миокарда и позитронно-эмиссионная томография
При гипертрофической кардиомиопатии сцинтиграфия миокарда имеет некоторые особенности, однако в целом ее значение в диагностике ишемии такое же, как и обычно. Стойкие дефекты накопления указывают на рубцовые изменения после инфаркта миокарда, обычно они сопровождаются снижением функции левого желудочка и плохой переносимостью физической нагрузки. Обратимые дефекты накопления указывают на ишемию, вызванную снижением коронарного резерва при нормальных артериях или коронарным атеросклерозом. Обратимые дефекты часто никак не проявляются, однако, по-видимому, они повышают риск внезапной смерти, особенно у молодых больных с гипертрофической кардиомиопатией. При изотопной вентрикулографии можно выявить замедленное наполнение левого желудочка и удлинение периода изоволюмического расслабления.
Позитронно-эмиссионная томография – более чувствительный метод, кроме того, она позволяет учесть и устранить помехи, связанные с затуханием сигнала. Позитронно-эмиссионная томография с фтордезоксиглюкозой подтверждает наличие субэндокарлиальной ишемии, вызванной снижением коронарного резерва.
Современные подходы к лечению ГКМП
По современным представлениям, лечебная стратегия определяется в процессе разделения больных на категории в зависимости от описанных выше вариантов течения и прогноза.
Все лица с ГКМП, включая носителей патологических мутаций без фенотипических проявлений болезни и пациентов с бессимптомным течением заболевания, нуждаются в динамическом наблюдении, в ходе которого оцениваются характер и выраженность морфологических и гемодинамических нарушений. Особое значение имеет выявление факторов, определяющих неблагоприятный прогноз и повышенный риск внезапной смерти (в частности, скрытых, прогностически значимых аритмий).
Общие мероприятия
Ограничение значительных физических нагрузок и запрещение занятий спортом, способных вызывать усугубление гипертрофии миокарда, повышение внутрижелудочкового градиента давления и риска внезапной смерти.
Медикаментозное лечение
До настоящего времени окончательно не решен вопрос о необходимости проведения активной медикаментозной терапии у наиболее многочисленной группы больных с бессимптомной или малосимптомной формами ГКМП и низкой вероятностью внезапной смерти. Противники активной тактики обращают внимание на то, что при благоприятном течении заболевания продолжительность жизни и показатели смертности не отличаются от таковых в общей популяции. Некоторые же авторы указывают на то, что использование в этой группе пациентов β-адреноблокаторов и антагонистов кальция (верапамил) может приводить к сдерживанию гемодинамических нарушений и клинической симптоматики. При этом никто не оспаривает тот факт, что выжидательная тактика в случаях бессимптомного или малосимптомного течения ГКМП возможна лишь при отсутствии признаков внутрижелудочковой обструкции, обмороков и серьезных нарушений сердечного ритма, отягощенной наследственности и случаев ВС у близких родственников.
Следует признать, что лечение ГКМП, генетически обусловленного заболевания, обычно распознаваемого на поздней стадии, пока может быть в большей степени симптоматическим и паллиативным. Тем не менее к основным задачам лечебных мероприятий относятся не только профилактика и коррекция основных клинических проявлений заболевания с улучшением качества жизни пациентов, но и положительное влияние на прогноз, предупреждение случаев ВС и прогрессирования заболевания.
Основу медикаментозной терапии ГКМП составляют препараты с отрицательным инотропным действием: β-адреноблокаторы и блокаторы кальциевых каналов. Для лечения весьма распространенных при этом заболевании нарушений сердечного ритма используются также дизопирамид (антиаритмический препарат IA класса) и амиодарон.
Предпочтение отдается β-блокаторам без внутренней симпатомиметической активности. Наибольший опыт накоплен по применению пропранолола (обзидан, анаприлин). Его назначают начиная с 20 мг 3-4 раза в день, с постепенным увеличением дозы под контролем пульса и артериального давления (АД) до максимально переносимой в большинстве случаев 120–240 мг/сут. Следует стремиться к применению возможно более высоких доз препарата, так как отсутствие эффекта терапии β-блокаторами, вероятно, связано с недостаточной дозировкой. При этом нельзя забывать о том, что повышение дозировок существенно увеличивает риск известных побочных эффектов.
Инвазивные методы лечения:
1. Чрезаортальная септальная миэктомия
2. Вальвулопластики или протезирования митрального клапана
В ряде случаев при наличии дополнительных показаний для уменьшения выраженности обструкции и митральной регургитации одномоментно выполняется операция вальвулопластики или протезирования митрального клапана низкопрофильным протезом. Улучшить отдаленные результаты миэктомии позволяет последующая длительная терапия верапамилом, обеспечивающая улучшение диастолической функции ЛЖ, что не достигается при хирургическом лечении.
3. Иссечения межжелудочковой перегородки
В настоящее время разработаны и успешно применяются отличные от классической миэктомии методики. В частности, в НЦССХ им. А. Н. Бакулева под руководством академика Л. А. Бокерия разработана оригинальная методика иссечения зоны гипертрофированной МЖП из конусной части правого желудочка. Этот способ хирургической коррекции обструктивной ГКМП является высокоэффективным и может стать методом выбора в случаях одновременной обструкции выходных отделов обоих желудочков, а также в случаях среднежелудочковой обструкции ЛЖ.
4. Транскатетерная септальная аблация
Другим альтернативным методом лечения рефракторной обструктивной ГКМП является транскатетерная алкогольная септальная аблация. Методика предполагает инфузию через баллонный катетер в перфорантную септальную ветвь 1–3 мл 95% спирта, вследствие чего возникает инфаркт гипертрофированного отдела МЖП, захватывающей от 3 до 10% массы миокарда ЛЖ (до 20% массы МЖП). Это приводит к значимому уменьшению выраженности обструкции выходного тракта и митральной недостаточности, объективной и субъективной симптоматике заболевания.
В Волынской больнице отработана методика выполнения транскатетерной септальной аблации при ГКМП. Доказан положительный результат данного вмешательства при относительно низком риске развития осложнений.
Признаки обструкции выходного тракта лж что это
Обструкция выносящего тракта левого желудочка (ЛЖ) является относительно редким явлением. Ее распространенность составляет 20-23 случая на 100 000 населения. При этом ежегодная первичная заболеваемость среди взрослого населения составляет 0,3-0,5 на 100 000 взрослого населения в год. Основными причинами возникновения данного феномена являются первичная гипертрофическая кардиомиопатия (ГКМП), а также длительное тяжелое течение артериальной гипертензии (АГ) [1].
Некоторые авторы под термином «обструкция выносящего тракта» понимают обструкцию ЛЖ на любом уровне (подаортальный, надаортальный и клапанный аортальный стеноз) [2]. В нашей статье речь пойдет именно про истинную обструкцию на уровне выносящего тракта левого желудочка (ВТЛЖ).
Своевременная диагностика явления обструкции ВТЛЖ затруднена в связи с отсутствием специфических жалоб и клинических проявлений. Обструкция ВТЛЖ характеризуется длительным бессимптомным течением вплоть до возникновения тяжелых фатальных осложнений и прогрессирования хронической сердечной недостаточности (в основном вследствие диастолической дисфункции левого желудочка) [3].
Применительно к ГКМП в рамках нового руководства по оценке риска сердечно-сосудистой смертности в данной группе больных выделяют следующие факторы риска внезапной сердечной смерти, к которым относятся:
— размер левого предсердия (парастернальная позиция);
— максимальная толщина стенки ЛЖ по данным эхокардиографии (Эхо-КГ);
— максимальный градиент в ВТЛЖ в покое и после маневра Вальсальвы;
— пароксизм неустойчивой желудочковой тахикардии (3 и более желудочковых комплекса с ЧСС более 120/мин.) по данным записей холтеровского мониторирования электрокардиографии (ХМ-ЭКГ);
— необъяснимые синкопальные состояния в анамнезе [5].
Следует особо отметить, что чем старше больной с ГКМП, тем меньше вероятность возникновения у него пароксизмов ВСС при отсутствии их в анамнезе. То есть длительность обструкции ВТЛЖ при прочих равных несет отрицательную предсказательную ценность как фактор риска ВСС.
Таким образом, в судьбе больного решающее значение имеет немедленное выявление обструкции ВТЛЖ с момента появления первых симптомов для успешного дальнейшего наблюдения с оказанием своевременной помощи, в том числе хирургической, или имплантации кардиовертера-дефибриллятора. При этом своевременное применение профилактических мероприятий, хирургической помощи закономерно улучшает прогноз пациентов.
Цель исследования: изучение клинической картины феномена обструкции ВТЛЖ с акцентом на первые его проявления на основе серии клинических наблюдений с целью раннего ее выявления.
Материал и методы исследования. Обследовано 28 пациентов с обструкцией ВТЛЖ. Все пациенты – больные, находившиеся на лечении в кардиологическом отделении № 1 ОГБУЗ «Белгородская областная клиническая больница Святителя Иоасафа» с 2016 по 2018 г. Возраст больных от 41 до 69 лет (средний возраст 55,4 9,01 года). В работу вошло 15 мужчин (54%), 13 женщин (46%).
Критерий включения пациентов в исследование: наличие обструкции ВТЛЖ. Критерии исключения: наличие умеренного и критического аортального стеноза.
Методы обследования больных: сбор жалоб и анамнеза с акцентом на первый симптом, послуживший поводом для обращения за медицинской помощью, объективное клиническое обследование, эхокардиографическое исследование с расчетом следующих параметров:
— градиент давления в ВТЛЖ;
— индекс массы миокарда левого желудочка (ИММЛЖ);
— толщина межжелудочковой перегородки;
В настоящее время при анализе феномена обструкции ВТЛЖ можно выделить пациентов с латентной (динамической) и фиксированной обструкцией. Отдельную группу составляют больные с фиксированной обструкцией с отчетливым динамическим компонентом, т.е. это те больные, которые имеют исходно значимую обструкцию с отчетливым приростом градиента давления в ВТЛЖ в ответ на физическую или фармакологическую нагрузку.
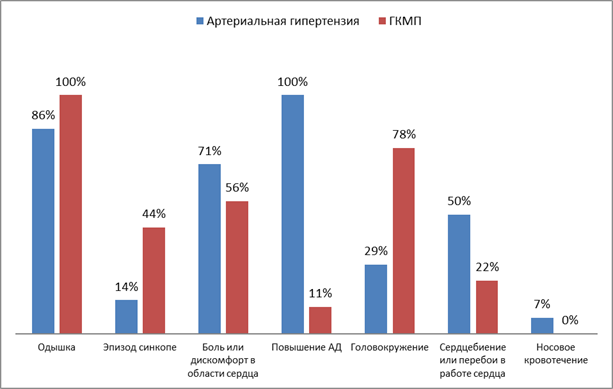
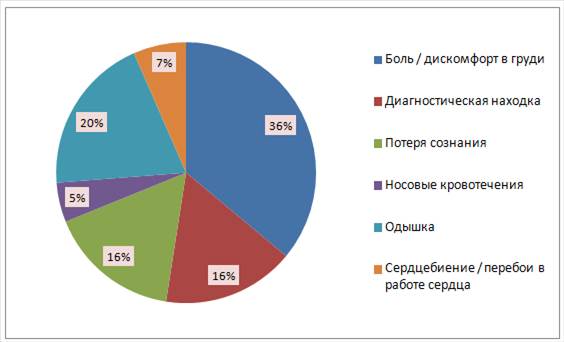
В ходе исследования проанализирована клиническая картина заболеваний, протекающих с обструкцией ВТЛЖ. Большинство больных при обследовании предъявляли жалобы на одышку, а также боли или дискомфорт в области сердца. Примерно половину больных беспокоили повышение артериального давления (АД), сердцебиение или перебои в работе сердца, а также головокружение. Реже встречались жалобы на эпизод синкопе или носовые кровотечения (рисунок 1).
Рис. 1. Дифференциальная диагностика заболеваний, приводящих к обструкции ВТЛЖ по клинической картине
При проведении исследования внимание было акцентировано на первом симптоме, послужившем поводом для обращения за медицинской помощью. 36% пациентов обратились в связи с болью или дискомфортом в области сердца, 20% больных обратились к врачу из-за одышки, у 16% пациентов заболевание впервые проявилось эпизодом синкопе. 7% обратились из-за проявлений нарушений ритма. Также у 16% больных обструкция ВТЛЖ была выявлена случайно при плановом обследовании. Наконец, 5% обратились в связи с носовыми кровотечениями (рисунок 2).
Рис. 2. Первый симптом, послуживший поводом для обращения за медицинской помощью
Была проведена дифференциальная диагностика заболеваний по первому симптому у пациентов с обструкцией ВТЛЖ. Предсказуемо выявлено, что у обратившихся за медицинской помощью в связи с эпизодом потери сознания диагностирована ГКМП. При этом синкопальные состояния чаще возникали внезапно у более молодых пациентов на фоне относительного благополучия в большинстве случаев после физической нагрузки или психоэмоционального напряжения. Тогда как с болью или дискомфортом в области сердца чаще обращались больные АГ.
Данное наблюдение объясняется длительной компенсацией сердечной недостаточности при ГКМП, а также более частым поражением сосудов атеросклерозом при АГ. В этом случае клиническая картина представляет собой сочетание АГ, симптомов обструкции ВТЛЖ и типичной стенокардии напряжения вследствие хронической ишемической болезни сердца.
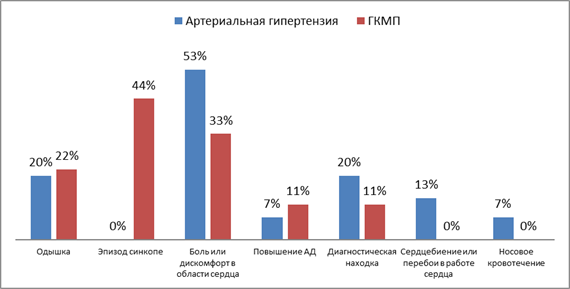
Одышка послужила поводом для обращения примерно в равном количестве случаев для пациентов с АГ и ГКМП (рисунок 3).
Рис. 3. Дифференциальная диагностика заболеваний, приводящих к обструкции ВТЛЖ по первому симптому
Вполне естественно, что жалобы, связанные с повышением АД, носовые кровотечения, головные боли являются патогномоничными для АГ. Отметим также, что обструкция ВТЛЖ в 2 раза чаще выявлялась при случайном обследовании у больных с АГ, что лишний раз подтверждает важность диагностики гипертрофии миокарда в этой группе больных.
Статистически проанализированы следующие параметры:
— градиент давления в ВТЛЖ;
— толщина межжелудочковой перегородки;
Поскольку выраженная гипертрофия миокарда ЛЖ является ведущим фактором риска аритмической смерти, данная корреляция может быть объяснена крайне неблагоприятным прогнозом течения феномена обструкции ВТЛЖ. Вероятнее всего, эта взаимосвязь отражает преждевременную гибель пациентов молодого возраста с крайне выраженной гипертрофией миокарда ЛЖ.
Обсуждение результатов. Несмотря на сравнительную редкость, диагностика феномена обструкции ВТЛЖ является крайне важным при определении прогноза жизни и лечебных мероприятий у конкретного пациента.
В нашей работе подчеркивается значение ангинозной боли, одышки и синкопе как возможных предвестников обструкции ВТЛЖ. Очевидно, что данным категориям пациентов по крайней мере однократно должно быть выполнено эхокардиографическое исследование. При сомнениях, соответствующей клинической и аускультативной картине (систолический шум на верхушке, в точках выслушивания аортального клапана или во всех точках аускультации) необходимо повторное проведение эхокардиографического исследования в экспертном центре. Значимость такого подхода трудно переоценить у больных с АГ.
Очевидно, что выводы нашего исследования наилучшим образом подтверждают значимость такого подхода, так как у 1/5 части пациентов с АГ обструкция ВТЛЖ была выявлена именно в результате рутинного эхокардиографического исследования.
К несомненным ограничениям нашего исследования относится ограниченность в возможности проведения генетической диагностики. Однако данные исследования в большинстве своем недоступны для врача в его повседневной деятельности, оставаясь в основном лишь частью специальных научных исследований в рамках изучения ГКМП. Таким образом, проведенный анализ вполне отражает особенности диагностики синдрома обструкции ВТЛЖ в реальной клинической практике.
1. Ведущими причинами феномена обструкции ВТЛЖ предсказуемо стали АГ и ГКМП.
2. Среди первых симптомов, приводящих к обращению пациента за медицинской помощью, преобладают боль или дискомфорт в области сердца и одышка. В рамках дифференциальной диагностики первым симптомом обструкции ВТЛЖ вследствие АГ стали боль или дискомфорт в области сердца, а при ГКМП – синкопальный эпизод.
3. Обратная корреляционная зависимость между возрастом пациента и ИММЛЖ убедительно свидетельствует о крайне неблагоприятной прогностической роли выраженной гипертрофии ЛЖ. Пациенты с экстремально высокими значениями массы миокарда подвержены высоким рискам ВСС.