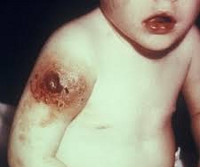
Гипогаммаглобулинемия, болезнь Брутона, аутосомная рецессивная агаммаглобулинемия швейцарского типа
Гипогаммаглобулинемия — это заболевание, возникающее в результате дефицита В-клеток (В-лимфоцитов) в сочетании с уменьшением размера антител — иммуноглобулинов.
Эти антитела не только определяют чужеродные антигены, но и генерируют генетический ответ, который приводит к уничтожению этих антигенов.
Уменьшение количества антител в организме связано с периодическими инфекциями, вызываемыми конкретными формами бактерий. В случае ответа B-лимфоцитов на нарушение качества клеточного иммунитета автоматически регулируется количество бактериальных, грибковых и вирусных инфекций.
Наиболее частые разновидности нарушений, связанных с В-клетками — это непосредственно гипогаммаглобулинемия, а также агаммаглобулинемия (сцепленная с Х-хромосомой, или агаммаглобулинемия Брутона), а также аутосомная рецессивная агаммаглобулинемия швейцарского типа.
Причины, симптомы и методы лечения гипогаммаглобулинемии
В организме существует два вида лимфоцитов. Т-лимфоциты отвечают за уничтожение болезнетворных организмов, В-лимфоциты производят антитела, «налипающие» на атакующие организм патогены, таким образом, Т-лимфоциты и другие защитные клетки накапливаются и атакуют чужеродные организмы.
Антитела – это ключевые белки, ответственные за обнаружение болезнетворных патогенов, понижение их уровня увеличивает восприимчивость к инфекциям. Критическое снижение количества антител вызывает гипогаммаглобулинемию.
Причины
Гипогаммаглобулинемия может быть первичной (то есть, врожденной) или вторичной (приобретенной), вызванной заболеваниями. Первичная форма заболевания может проявиться как при рождении, так и позднее — в более старшем возрасте, несмотря на то, что дефектный ген в организме присутствует с рождения. Большинство случаев гипогаммаглобулинемии развивается после 6-месячного возраста. Случаи заболевания, проявляющиеся на 3-м или 4-м десятилетии жизни, принято считать первичным иммунодефицитом. Их развитие, полагают медики, является результатом еще не установленных генных дефектов.
Симптомы
Большинство пациентов с гипогаммаглобулинемией страдают от рецидивирующих инфекций. Острота проявления симптомов зависит от семейной истории болезни, возраста начала болезни, имеющихся в организме инфекций, состава крови, состояния ЖКТ и опорного аппарата, а также от того, имеются ли у пациента аутоиммунные заболевания или болезни сосудов.
Симптомы гипогаммаглобулинемии:
Лечение
Лечение гипогаммаглобулинемии направлено на устранение основной причины недомогания, заболевание или инфекцию. Пациентам с нарушением функции Т-клеток, тяжелыми расстройствами В-клеток не назначают живые вакцины. Высокие дозы ВВИГ (внутривенного иммуноглобулина) или интератекального иммуноглобулина могут быть полезны пациентам с энтеровирусным менингоэнцефалитом. Показано применение полиэтиленгликоля при дефиците аденозиндезаминазы. Для лечения гранулематозных заболеваний применяют фактор некроза опухолей (ФНО). Успешным методом лечения является и генная терапия, наиболее эффективна она у детей с агаммаглобулинемией Брутона. У взрослых и детей старшего возраста эффективность такого метода лечения ниже.
Аутосомная рецессивная агаммаглобулинемия швейцарского типа
Тяжелый комбинированный иммунодефицит (SCID, ТКИД), или аутосомная рецессивная агаммаглобулинемия швейцарского типа, является наиболее серьезным расстройством из группы человеческих иммунодефицитов. В медицинских источниках и литературе данное заболевание известно также под названием алимфоцитоз. Это заболевание врожденного характера.
Развитие ТКИД сопровождается нарушениям работы гуморальной части иммунной системы человека. Клетки, которые должны производить иммунный ответ, не функционируют. Дети с данным заболеванием подвержены повторяющимся тяжелым инфекциям, задержке роста и ранней смерти.
ТКИД встречается у одного из пятисот тысяч новорожденных. Понятие «тяжелый комбинированный иммунодефицит» объединяет несколько заболеваний, в частности:
Гуморальная система состоит из В-клеток, которые являются единственными клетками в организме, производящими антитела. При ТКИД ни клеточная, ни гуморальная часть иммунной системы не функционирует так, как необходимо.
Причины и симптомы
SCID является наследственным заболеванием. Существует два типа неправильного развития иммунной системы плода. При первом типе генетического нарушения В- и Т-клетки являются дефектными. При втором типе только Т-клетки являются аномальными, но их недостаток влияет на функционирование лимфоцитов.
В течение первых нескольких месяцев жизни ребенок с ТКИД защищен антителами, попавшими в его организм из крови матери. Однако уже в возрасте трех месяцев ребенок с подобным нарушением начинает страдать от грибковой инфекции полости рта (молочницы), хронической диареи, отита и легочных инфекций, в том числе пневмоцистной пневмонии. Ребенок теряет вес, становится очень слабым, и, в конце концов, умирает от условно-патогенной инфекции.
Лечение аутосомной рецессивной агаммаглобулинемии
Тяжелый комбинированный иммунодефицит/агаммаглобулинемию можно лечить с помощью антибиотиков и иммунной сыворотки. Однако такие методы лечения не могут защитить больных, а лишь защищают от инфекций. Постоянная защита невозможна из-за привыкания к антибиотикам и уничтожения полезной микрофлоры ЖКТ. В настоящее время один из немногих эффективных методов лечения этого заболевания — это пересадка костного мозга.
Сцепленная с X-хромосомой агаммаглобулинемия Брутона с дефицитом гормона роста
Что такое агаммаглобулинемия Брутона?
Агаммаглобулинемия Брутона — это заболевание, относящееся к иммунодефицитам, впервые описанное в 1952 году. Огден Брутон обратил внимание на отсутствие иммуноглобулинов у мальчика с пневмонией и другими бактериальными инфекциями. Фактически именно этот тип иммунодефицита является первым официально описанным иммунодефицитом в истории медицины. Брутон был первым специалистом, обеспечившим больному специфическую иммунотерапию — с этой целью он вводил больному иммуноглобулины внутримышечно.
Состояние больного после лечения улучшилось, однако в дальнейшем, уже на четвертом десятилетии жизни, предрасположенность к болезни легких дала о себе знать.
В настоящее время данное заболевание формально называют болезнью Брутона, а фактическое название звучит как «сцепленная с Х-хромосомой агаммаглобулинемия».
Симптомы
Болезнь Брутона проявляется следующими симптомами:
Лечение
Основное лечение заключается во введении в организм больных иммуноглобулина (Ig). Агрессивное лечение бактериальных инфекций антибиотиками помогает предотвратить долгосрочные осложнения. Вирусные вакцины (например, против кори, эпидемического паротита, краснухи) таким больным противопоказаны, как и членам их семей, поскольку могут вызвать развитие инфекции, связанной с этими вакцинами.
Внутривенное введение иммуноглобулина приводит к улучшению клинической картины болезни и уменьшает прогресс серьезных инфекций, таких как пневмония и менингит.
Пациенты, получающие высокие дозы ВВИГ (400-500 мг/кг каждые 3-4 недели) и у которых уровень иммуноглобулина не опускается ниже 500 мг/дл, значительно реже болеют и попадают в больницу. При бронхоэктазах доза иммуноглобулина может быть выше (до 600 мг/кг). Больные менингитом нуждаются в 1000 мг/кг иммуноглобулина из-за гематоэнцефалического барьера.
Пациентам с хроническими инфекциями заболеваний верхних и нижних дыхательных путей и последующими структурными изменениями в этих органах необходимы антибиотики широкого спектра действия. Прием антибиотиков должен сопровождаться физиотерапией грудной клетки и хирургией носовых пазух (при хроническом синусите). Основным препаратом является триметоприм-сульфаметоксазол. Допустимо использование линезолида по отношению к пенициллинорезистентным пневмококкам.
Вспомогательные препараты это: ингаляционные кортикостероиды, антилейкотриеновые препараты, бронхорасширяющие средства.
Хроническая экзема лечится увлажняющими кремами и актуальными стероидами. Рекомендуемые пищевые добавки: поливитамины и минеральные добавки. Необходимо проведение печеночных проб и, при необходимости, соответствующее лечение гепатита С и аутоиммунного гепатита, а также точное определение этиологии диареи.
5 вариантов завтрака, которые помогут избавиться от жира на животе
Неправильные формы микропластика разрушают клетки человека и вызывают аллергию
Бег в районах с плохой экологией так же опасен, как и низкий уровень физической активности
Ученые: Из-за устойчивости к антибиотикам будет ежегодно погибать 10 млн человек
Деятельность, которая может спровоцировать инсульт в течение следующих 60 минут
Исследование: Человек эволюционировал и стал жить долго благодаря постоянной физической нагрузке
Агаммаглобулинемия – это наследственно обусловленное заболевание, при котором развивается тяжелый первичный иммунодефицит (дефект иммунной защиты организма) с выраженным снижением уровня гамма-глобулинов в крови. Проявляется болезнь обычно в первые месяцы и годы жизни ребенка, когда начинают развиваться повторные бактериальные инфекции: отит, синусит, пневмонии, пиодермии, менингит, сепсис. При обследовании в периферической крови и костном мозге практически отсутствуют сывороточные иммуноглобулины и B-клетки. Лечение агаммаглобулинемии заключается в пожизненной заместительной терапии.
МКБ-10
Общие сведения
Агаммаглобулинемия (наследственная гипогаммаглобулинемия, болезнь Брутона) – врожденный дефект гуморального иммунитета, обусловленный мутациями в геноме клеток, что приводит к недостаточности синтеза B-лимфоцитов. В результате нарушается образование иммуноглобулинов всех классов, и их содержание в крови резко снижается вплоть до полного отсутствия, развивается первичный иммунодефицит. Низкая реактивность иммунной системы приводит к развитию тяжелых повторных гнойно-воспалительных заболеваний ЛОР-органов, бронхов и легких, желудочно-кишечного тракта и мозговых оболочек. Болезнь Брутона встречается исключительно у мальчиков и наблюдается примерно у 1-5 человек из миллиона новорожденных, независимо от расы и этнической группы.
Причины
X-сцепленная форма наследственной агаммаглобулинемии возникает вследствие повреждения одного из генов X-хромосомы (расположен на Xq21.3-22.2). Этот ген ответственен за синтез фермента тирозинкиназы, участвующего в процессе образования и дифференцировки B-клеток. В результате мутаций этого гена и блокировки синтеза брутоновской тирозинкиназы нарушается формирование гуморального иммунитета. При агаммаглобулинемии молодые формы (пре-B-клетки) присутствуют в костном мозге, а их дальнейшая дифференцировка и поступление в кровеносное русло нарушена.
Классификация
Выделяют три формы наследственной агаммаглобулинемии:
Симптомы агаммаглобулинемии
Сниженная реактивность гуморального иммунитета при агаммаглобулинемиях приводит к развитию повторных гнойно-воспалительных заболеваний уже на первом году жизни ребенка (как правило, после прекращения грудного вскармливания – в 6-8 месяцев). При этом защитные антитела от матери в организм ребенка уже не поступают, а свои иммуноглобулины – не вырабатываются. К 3-4 летнему возрасту воспалительные процессы переходят в хроническую форму со склонностью к генерализации. Гнойная инфекция при агаммаглобулинемии может поражать различные органы и системы.
Со стороны ЛОР-органов нередки гнойные гаймориты, этмоидиты, отиты, причем гнойный отит чаще развивается на первом году жизни ребенка, а синуситы – в 3-5 лет. Из заболеваний бронхолегочной системы наблюдаются повторные бронхиты, пневмонии, абсцессы легкого. Часто встречается поражение желудочно-кишечного тракта с упорной диареей (поносами), вызванной хроническим инфекционным энтероколитом (основные возбудители – кампилобактерии, лямблии, ротавирус). На кожных покровах обнаруживается импетиго, микробная экзема, рецидивирующий фурункулез, абсцессы и флегмоны.
Нередким бывает поражение глаз (гнойные конъюнктивиты), полости рта (язвенные стоматиты, гингивиты), костно-мышечной системы (остеомиелиты, гнойные артриты). В целом клиническая картина агаммаглобулинемии характеризуется сочетанием общих симптомов, наблюдаемых при гнойной инфекции (высокая температура тела, озноб, боли в мышцах и головная боль, общая слабость, нарушение сна и аппетита и т. д.) и признаков поражения конкретного органа (кашель, одышка, затруднение носового дыхания, гнойное отделяемое, диарея и т. п.).
Осложнения
Любое инфекционное и соматическое заболевание у больного иммунодефицитом протекает тяжело, длительно и сопровождается осложнениями. Тяжелое течение агаммоглобулинемии может осложняться развитием менингита, вирусного энцефаломиелита, поствакцинального паралитического полиомиелита, сепсиса. На фоне заболевания повышена вероятность развития аутоиммунных и онкологических заболеваний. Гибель пациентов часто наступает от инфекционно-токсического шока.
Диагностика
При клиническом осмотре пациента врачом аллергологом-иммунологом выявляются признаки гнойно-воспалительного поражения того или иного органа (ткани) и симптомы, подтверждающие сниженную реактивность иммунной системы: гипоплазия миндалин, уменьшение периферических лимфатических узлов. Выражены и признаки отставания в физическом развитии ребенка.
Лабораторное исследование крови выявляет выраженное снижение уровня иммуноглобулинов в иммунограмме (IgA и IgM
Дифференциальная диагностика наследственной агаммаглобулинемии проводится с другими первичными и вторичными иммунодефицитными состояниями (генетическими нарушениями, ВИЧ и цитомегаловирусной инфекцией, врожденной краснухой и токсоплазмозом, злокачественными новообразованиями и системными нарушениями, иммунодефицитом вследствие интоксикации лекарственными препаратами и др.).
Лечение агаммаглобулинемии
Необходима пожизненная заместительная терапия антителосодержащими препаратами. Обычно используется введение внутривенного иммуноглобулина, а при его отсутствии – нативной плазмы от здоровых постоянных доноров. При впервые установленном диагнозе агаммаглобулинемии заместительное лечение проводится в режиме насыщения до достижения уровня иммуноглобулина IgG выше 400 мг/дл, после чего при отсутствии активного гнойно-воспалительного процесса в органах и тканях можно переходить к поддерживающей терапии с введением профилактических доз препаратов, содержащих иммуноглобулины.
Любой эпизод бактериальной гнойной инфекции, независимо от локализации воспалительного процесса, требует проведения адекватной антибактериальной терапии, которая выполняется одновременно с заместительным лечением. Чаще при агаммаглобулинемии используются антибактериальные средства из группы цефалоспоринов, аминогликозидов, макролидов, а также антибиотики пенициллинового ряда. Продолжительность лечения при этом в несколько раз превышает стандартную при данном заболевании.
Симптоматическое лечение проводится с учетом конкретного поражения того или иного органа (промывание околоносовых пазух носа антисептиками, выполнение вибрационного массажа грудной клетки и постурального дренажа при бронхитах и пневмониях и т. д.).
Прогноз
Если агаммаглобулинемия обнаружена в раннем возрасте до наступления тяжелых осложнений, и адекватная состоянию пациента заместительная терапия начата своевременно, возможно сохранение нормального образа жизни в течение многих лет. Однако в большинстве случаев диагностика наследственных нарушений гуморального иммунитета осуществляется слишком поздно, когда уже развились необратимые хронические гнойно-воспалительные заболевания органов и систем организма. В этом случае прогноз при агаммаглобулинемии неблагоприятный.
Болезнь Шегрена
Общая информация
Краткое описание
Общероссийская общественная организация Ассоциация ревматологов России
Федеральные клинические рекомендации по диагностике и лечению болезни Шегрена
М.35.0 Системная красная волчанка
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
* Оценочная шкала окраски глазного эпителия
Эпидемиология
Заболеваемость БШ колеблется от 4 до 250 случаев на 100000 населения. Пик заболеваемости приходится на 135-50 лет. Женщины страдают в 8-10 раз чаще мужчин. Смертность при БШ в 3 раза выше, чем в популяции.
Диагностика
Диагноз БШ устанавливается на основании жалоб, анамнестических данных, клинико-лабораторного и инструментального обследования пациента, при исключении других заболеваний.
Клинические признаки, повышающие вероятность диагноза БШ
Поражение секретирующих эпителиальных желёз (аутоиммунный эпителиит).
· Слюнные железы поражаются у всех больных по типу рецидивирующего паренхиматозного сиаладенита (чаще паротита), реже субмаксиллита в сочетании с сиалодохитом у четверти больных, или наблюдается постепенное увеличение околоушных/поднижнечелюстных слюнных желёз, крайне редко малых слюнных желёз слизистой полости рта.
· Различной степени тяжести сухой коньюнктивит/кератоконъюнктивит (снижение слёзовыделения по стимулированному тесту Ширмера 1 мм в диаметре характерно для паренхиматозного паротита)
· биопсию малых слюнных желёз нижней губы (обнаружение 100 и более клеток в поле зрения в среднем при просмотре не менее 4-х малых слюнных желёз является диагностичным).
· биопсию увеличенных околоушных/поднижнечелюстных слюнных желез (с целью диагностики MALT-лимфомы)
· сиалометрию (снижение стимулированной секреции слюны 1 мм
3) Очагово-диффузная лимфогистиоцитарная инфильтрация в биоптатах
малых слюнных желез ( ≥ 2 фокусов* в 4 мм²)
Дифференциальный диагноз
· Наиболее часто в ревматологической практике необходимо проводить дифференциальную диагностику между БШ и СШ в сочетании с РА, ССД, СКВ, аутоиммунным гепатитом, первичным билиарным циррозом печени.
· Помимо БШ сухость глаз и полости рта может быть следствием многих причин.
Сухость глаз
1) структурные нарушения слёзной плёнки
— дефицит водного слоя (сухой кератоконъюнктивит)
— дефицит муцина (гиповитаминоз А, пемфигус, химические ожоги, синдром Стивена-Джонса)
— дефицит жирового слоя (блефарит)
2) роговичная эпителиопатия (поражение V черепного нерва, ношение контактных линз)
3) дисфункция век
Дефицит слёз
1) Заболевания слёзных желёз
Первичные
— врождённая алакримия
— приобретенная алакримия
— первичное заболевание слёзных желёз
Вторичные
— саркоидоз
— ВИЧ
— реакция трансплантат против хозяина
— ксерофтальмия
2) Слёзная обструкция
— трахома
— офтальмологическая рубцовая пузырчатка
— синдром Стивена-Джонса
— ожоги
3) Рефлекторные нарушения
— нейропатический кератит
— контактные линзы
— паралич лицевого нерва
Сухость рта
— Лекарственные препараты (диуретики, антидепрессанты, нейролептики, транквилизаторы, седативные, антихолинергические, антигистаминные)
— Психогенные факторы (тревожное состояние, депрессия)
— Системные заболевания (саркоидоз, туберкулёз, амилоидоз, сахарный диабет, панкреатит, IgG4 склерозирующий сиалоаденит, лимфомы)
— Дегидратация
— Вирусные инфекции
— Аплазия или недоразвитие слюнных желёз (редко)
— Облучение
— Постменопауза
— Белковое голодание
Увеличение слюнных и/или слёзных желез, характерное для многих заболеваний, входящих в круг дифференциальной диагностики БШ, может быть одно- или двухсторонним.
Увеличение слёзных желез
Двухстороннее:
Бактериальный/вирусный дакриоаденит
Гранулематозные поражения (туберкулез, саркоидоз )
Лимфопролиферативные заболевания
Идиопатическое воспалительное заболевание орбиты
Доброкачественная лимфоидная гиперплазия (MALT-дакриоаденит)
IgG4-связанные заболевания (IgG4-связанный псевдотумор орбит и склерозирую-
щий дакриоаденит)
Гистиоцитозы (ювенильная ксантогранулёма, ретикулогистиоцитоз )
Одностороннее
Бактериальный/вирусный дакриоаденит
Лимфопролиферативные заболевания с поражением слёзных желёз
Первичные опухоли:
Эпителиальные (аденома, аденокарцинома)
Смешанные (ангиома, меланома)
Увеличение слюнных желез
Одностороннее
Бактериальные инфекции
Хронический сиаладенит
Сиалолитиаз
Первичные неоплазии (аденома, аденокарцинома, лимфома, смешанная опухоль слюнных желёз)
Двухстороннее
Бактериальные/вирусные инфекции (Эпштейн Барр, цитомегаловирус, коксаки, паромиксовирус, герпес, ВИЧ, вирус эпидемического паротита)
Гранулёматозные заболевания (туберкулез, саркоидоз)
AL-амилоидоз, мастоцитоз
Метаболические нарушения (гиперлипидемия, сахарный диабет, подагра, алкогольный цирроз печени)
Акромегалия
Анорексия, гипоменструальный синдром
IgG4-связанные склерозирующие сиалоадениты
Лимфоэпителиальный сиаладенит
Онкоцитарная гиперплазия слюнных желёз
Лимфомы
Лечение
Лечение проводится в зависимости от наличия железистых и внежелезистых проявлений, и иммуновоспалительной активности заболевания.
Цели лечения
· Достижение клинико-лабораторной ремиссии заболевания.
· Улучшение качества жизни больных.
· Предотвращение развития опасных для жизни проявлений заболевания (генерализованный язвенно-некротический васкулит, тяжёлые поражения центральной и периферической нервной системы, аутоиммунные цитопении, лимфопролиферативные заболевания).
Нефармакологические подходы к сухому синдрому (D)
1. Избегать ситуаций, усиливающих сухость слизистых оболочек: сухой или кондиционированный воздух, сигаретный дым, сильный ветер, длительная зрительная (особенно компьютерная), речевая или психоэмоциональная нагрузка.
2. Ограничить применение препаратов, усугубляющих сухость (диуретики, трициклические антидепрессанты, бета-блокаторы, антигистаминные), и определенных раздражающих веществ (кофе, алкоголь, никотин).
3. Частое употребление небольших количеств воды или не содержащей сахара жидкости облегчает симптомы сухости рта. Полезна вкусовая и механическая стимуляция саливации с использованием жевательной резинки и леденцов без сахара.
4. Скрупулезная гигиена полости рта, использование зубной пасты и ополаскивателей с фторидами, тщательный уход за зубными протезами, регулярное посещение стоматолога обязательно с профилактической целью относительно прогрессирующего кариеса и периодонтита.
5. Терапевтические контактные линзы могут служить дополнительной протекцией эпителия роговицы, однако, их ношение должно сопровождаться адекватным увлажнением и профилактической инстилляцией антибиотиков.
Применение точечной окклюзии входных отверстий носослезного канала: временной (силиконовые или коллагеновые пробки) или чаще перманентной (прижигание или хирургическое вмешательство).
Лечение железистых проявлений БШ.
1. Для лечения железистых проявлений используют локальную терапию сухого синдрома (увлажняющие заместители, иммуномодулирующие препараты), стимуляторы эндогенной секреции слюнных и слезных желез.
Для улучшения саливации и терапии сухого кератоконъюнктивита возможно применение препаратов системного действия (малые дозы ГК и лейкерана (C), ритуксимаб (РТМ) (А).
2. Для замещения объема слезы пациентам следует 3-4 и > раз в день использовать искусственные слезы, содержащие 0,1-0,4% гиалуронат натрия, 0,5-1% гидроксипропилметилцеллюлозу, 0,5-1% карбоксиметилцеллюлозу, 0,1-3% декстран 70. При необходимости интервал между закапыванием слез может быть сокращен до 1 часа. Препараты без консервантов позволяют избежать раздражения глаз. Для пролонгирования эффекта возможно использование препаратов искусственной слезы большей вязкости. Такие препараты лучше применять на ночь из-за возникновения эффекта помутнения зрения (В).
3. Глазные капли на основе сыворотки крови применимы для пациентов с непереносимостью искусственных слез или тяжелым, резистентным к лечению сухим кератоконъюнктивитом. Обязательно чередование с антибактериальными каплями (В).
4. Использование препаратов-заменителей слюны на основе муцина и карбоксиметилцеллюлозы восполняет её смазывающие и увлажняющие функции, особенно во время ночного сна (Oral balance гель, Biotene ополаскиватель, Salivart, Xialine). (В).
5. Учитывая высокую частоту развития кандидозной инфекции при наличии сухого синдрома, показано локальное и системное противогрибковое лечение (нистатин, клотримазол, флуконазол) (D) 22.
6. У пациентов со значительным увеличением околоушных, поднижнечелюстных слюнных и слёзных желёз, рецидивирующим характером паренхиматозного сиалоаденита противопоказана их рентгенотерапия ввиду значительного нарастания сухости и увеличения риска развития лимфом (С).
7. Офтальмологическая эмульсия Циклоспорина А (Restasis) рекомендуется для лечения сухого кератоконъюнктивита. Считается оптимальным назначение 0,05% глазных капель два раза в день в течение 6-12 мес. (В).
8. Локальное применение НПВП (0,1% индометацин, 0,1% диклофенак) уменьшает дискомфортные ощущения в глазах, однако, может провоцировать повреждения роговицы (С).
9. Приемлемым считается локальное применение ГК короткими курсами (до двух недель) при обострении сухого кератоконъюнктивита. (С). Потенциальные побочные эффекты, повышение внутриглазного давления, развитие катаракты, ограничивают длительность применения ГК. Для локального применения лучше подходят Лотепреднол (Lotemax) и Римексолон (Vexol), не обладающие типичными побочными эффектами.
10. Для стимуляции остаточной секреции слюнных и слезных желез системно применяются агонисты М1 и М3 мускариновых рецепторов: пилокарпин (Salagen) 5 мг 4 раза в день или цевимелин (Evoxac) 30 мг 3 раза в день. (А).
11. Диквафозол, агонист пуриновых P2Y2 рецепторов, стимулирует нежелезистую секрецию водного, муцинового и липидного компонента слезной пленки. Используется локально 2% раствор (В).
12. 2% офтальмологическая эмульсия ребамипида, повышающего количество муциноподобных веществ и слезной жидкости, улучшает повреждения роговицы и конъюнктивы (В). Пероральный прием ребамипида (Мукоген) по 100 мг 3 раза в день улучшает симптомы сухости рта (A).
13. Облегчение сухости верхних дыхательных путей (ринит, синусит, ларингит, бронхит) достигается при приеме бромгексина или ацетилцистеина в терапевтических дозах. (С).
14. При диспареунии, обусловленной недостаточной лубрикацией, помимо местного использование лубрикантов, в постменопаузальном периоде показано локальное и системное применение эстрогенов (D).
Лечение внежелезистых системных проявлений БШ.
Для лечения системных внежелезистых проявления БШ используются ГК, алкилирующие цитостатические (лейкеран, циклофосфан), биологические (ритуксимаб) препараты.
1. Больным с рецидивирующими сиаладенитами и минимальными системными проявлениями, такими как суставной синдром, назначают ГК в малых дозах (преднизолон 5 мг в день или через день) либо НПВП (С).
2. При значительном увеличении больших слюнных желёз (после исключения лимфомы), диффузной инфильтрации малых слюнных желёз, отсутствии признаков тяжёлых системных проявлений, умеренных и значительных сдвигах показателей лабораторной активности необходимо назначение малых доз ГК в сочетании с лейкераном 2-4 мг/сут в течение года, затем 6-14 мг/неделю в течение нескольких лет (С).
3. При лечении васкулита (криоглобулинемический гломерулонефрит, поражение периферической и центральной нервной системы, рецидивирующая пурпура и язвенно-некротическое поражение кожи) назначается циклофосфан. В комбинации с малыми дозами ГК циклофосфан в дозе 200 мг/неделю в течение 3 месяцев с последующим переходом на 400 мг/месяц применяется при не угрожающих жизни системных проявлениях заболевания (рецидивирующая криоглобулинемическая пурпура, смешанная моноклональная криоглобулинемия, сенсорно-моторная полинейропатия) (С).
4. Тяжелые системные проявления БШ, такие как криоглобулинемический и интерстициальный нефрит, язвенно-некротический васкулит, сенсорно-моторная нейропатия аксонально-демиелинизирующего и демиелинизирующего типа, мононеврит, полиневрит, энцефаломиелополирадикулоневрит, миозит, интерстициальный пневмонит, генерализованная лимфаденопатия, аутоиммунная гемолитическая анемия и тромбоцитопения, а также MALT-лимфома слюнных желез, требуют более высоких доз преднизолона (20-60 мг/сут) и цитостатических средств (лейкеран 6-10 мг/сут, циклофосфан 0,8-3,0 г/месяц) в сочетании с интенсивными методами терапии (С).
5. Длительный приём малых доз ГК в комбинации с лейкераном или циклофосфаном не только снижает частоту рецидивов паротита, приводит к нормализации размеров слюнных желёз, уменьшает показатели лабораторной активности, улучшает клиническую симптоматику и замедляет прогрессирование многих системных проявлений заболевания, но и достоверно повышает саливацию, уменьшает частоту развития лимфом и увеличивает выживаемость больных БШ (С).
6. Внутривенный иммуноглобулин применяется в лечении агранулоцитоза, аутоиммунной тромбоцитопении, гемолитической анемии при БШ, а также у отдельных больных с выраженной сенсорной нейропатией при резистентности к терапии (D).
Показания к проведению пульс-терапии (D):
· выпотной серозит
· тяжёлые лекарственные аллергические реакции
· аутоиммунная гемолитическая анемия и тромбоцитопения
· при наличии противопоказаний для проведения комбинированной пульс-терапии.
Пульс-терапия позволяет снизить дозу пероральных ГК и уменьшить частоту их побочных проявлений (D).
Показания к комбинированной пульс-терапии (D):
· острый криоглобулинемический гломерулонефрит, гломерулонефрит с быстро прогрессирующей почечной недостаточностью
· язвенно-некротический васкулит
· аутоиммунная панцитопения
· интерстициальный пневмонит
· мононеврит, полиневрит, энцефаломиелополирадикулоневрит, поперечный и восходящий миелит, цереброваскулит
После достижения клинического эффекта и нормализации иммуновоспалительной активности заболевания больные переводятся на поддерживающие дозы ГК и алкилирующих цитостатических препаратов (С).
Показания к проведению экстракорпоральной терапии (D):
Абсолютные
· язвенно-некротический васкулит
· криоглобулинемический гломерулонефрит
· энцефаломиелополирадикулоневрит, демиелинизирующая миелопатия, полиневрит
· ишемия верхних и нижних конечностей вследствие криоглобулинемического васкулита.
· синдром гипервязкости крови
Относительные
· гипергаммаглобулинемическая пурпура
· мононеврит
· лекарственный дерматит, отек Квинке, феномен Артюса
· интерстициальный пневмонит
· гемолитическая анемия, тромботическая тромбоцитопеническая пурпура
В случаях аллергических реакций, интерстициального нефрита с признаками хронической почечной недостаточности, при низких цифрах общего белка в сыворотке крови, тяжёлых офтальмологических проявлениях (буллёзно-нитчатый кератит, язвы роговицы) предпочтительно использование гемосорбции, криоафереза. При остальных системных проявлениях более эффективным является плазмаферез, криоаферез и двойная фильтрация плазмы. Последние два метода наиболее эффективны при смешанной моноклональной криоглобулинемии. Обычно процедуры проводятся с 2-5-дневным интервалом с введением после каждой процедуры 250-1000 мг метилпреднизолона и 200-1000 мг циклофосфана в зависимости от тяжести системных проявлений и иммуновоспалительной активности заболевания. Для больных с нормальным или низким общим белком сыворотки крови предпочтительно применять двойную фильтрацию плазмы, криоаферез с гепаринокриофракционированием плазменных белков. Всего проводится 3-5 процедур при наличии гипергаммаглобулинемической пурпуры и 5-8 процедур при криоглобулинемической пурпуре. При васкулите, обусловленном смешанной моноклональной криоглобулинемией, целесообразно использовать программный плазмаферез в течение года до достижения стойкой клинико-лабораторной ремиссии (D).
Применение генно-инженерных биологических препаратов
Применение анти-В клеточной терапии ритуксимабом (РТМ) позволяет контролировать системные внежелезистые проявления БШ и уменьшать функциональную железистую недостаточность. РТМ улучшает клиническое течение БШ без увеличения частоты побочных эффектов.
· РТМ назначается больным БШ с тяжелыми системными проявлениями (криоглобулинемический васкулит, гломерулонефрит, энцефаломиелополирадикулоневрит, интерстициальный пневмонит, аутоиммунная панцитопения), а также в случаях резистентности или недостаточной эффективности традиционного лечения ГК и цитостатическими препаратами. С целью усиления эффективности РТМ показана комбинированная терапия с циклофосфаном (D).
· У больных с небольшой длительностью БШ и сохраненной остаточной секрецией слюнных и слезных желез монотерапия РТМ приводит к увеличению саливации и улучшению офтальмологических проявлений (А).
· РТМ назначается при БШ, осложненной лимфомой низкой степени злокачественности MALT-типа: локализованной экстранодальной лимфомой слюнных, слезных желез или легких, без поражения костного мозга. Проводится как монотерапия РТМ, так и комбинированная терапия РТМ и циклофосфаном (D).
Профилактика
Первичная профилактика невозможна ввиду неясной этиологии заболевания. Вторичная профилактика направлена на предупреждение обострения, прогрессирования заболевания и своевременное выявление развивающихся лимфом. Она предусматривает раннюю диагностику и своевременно начатую адекватную терапию. Некоторые больные нуждаются в ограничении нагрузки на органы зрения, голосовые связки и исключении аллергизирующих факторов. Больным противопоказана вакцинация, лучевая терапия и нервные перегрузки. С большой осторожностью должны применяться электропроцедуры.
Обучение пациентов
Так как больные БШ имеют хроническое заболевание с неуклонной прогрессией на протяжении всей жизни, необходимо наладить тесный контакт с больными. Только при полном доверии пациента к врачу, он будет соблюдать рекомендуемую терапию. Необходимо научить пациента как можно раньше улавливать возможные побочные проявления назначаемых препаратов и знать основные признаки обострения заболевания.