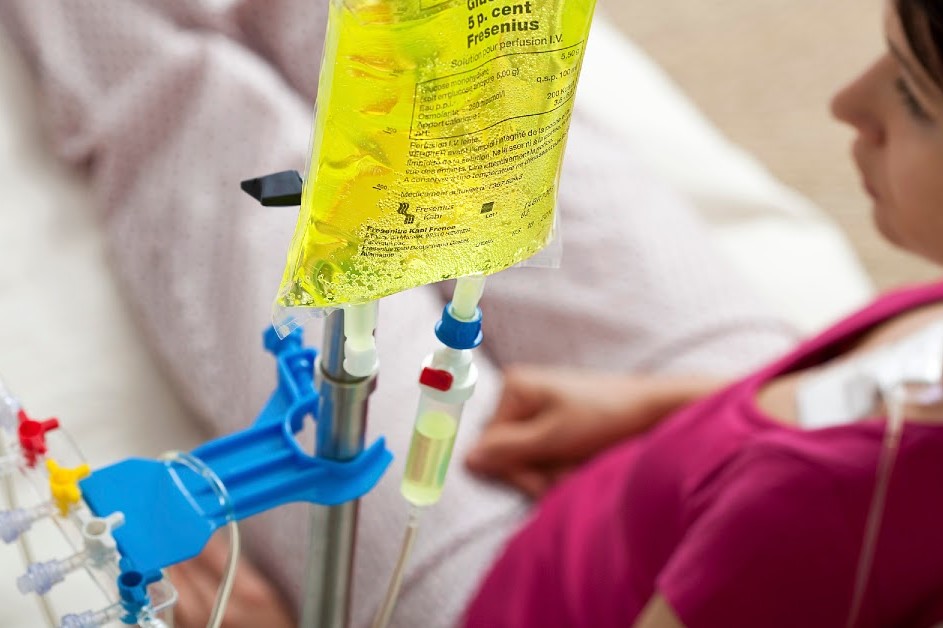
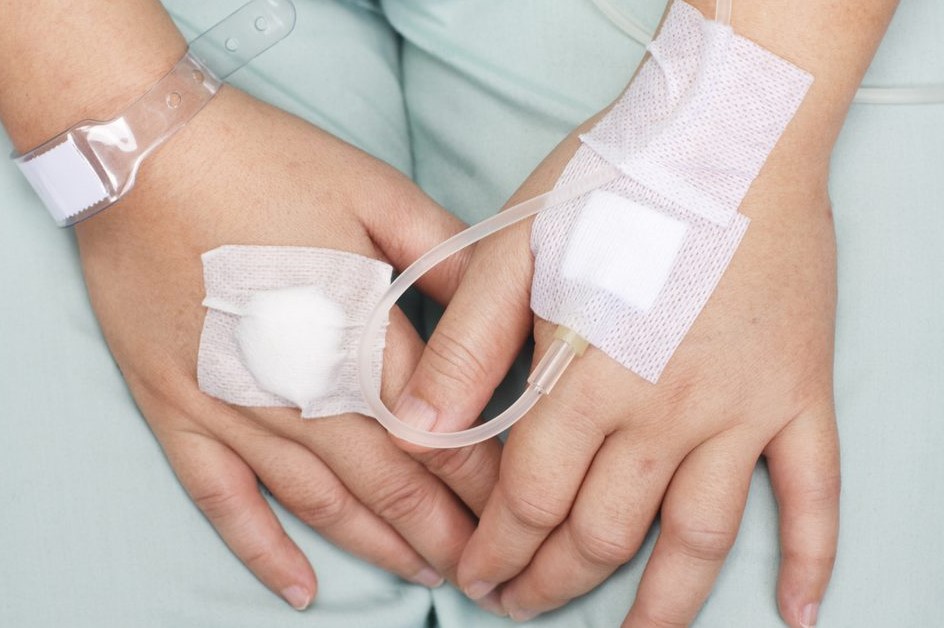
Противоопухолевое лечение и кожная токсичность
Что такое кожная токсичность?
Кожная токсичность – это кожные реакции, которые появляются более чем у 80% пациентов на фоне системной лекарственной противоопухолевой терапии. Эти реакции являются результатом токсического, угнетающего воздействия химиотерапии на растущие, быстроделящиеся клетки организма, в том числе клетки кожи, волос и ногтей. Так ранние реакции развиваются через 1-2 недели, отсроченные реакции через 3-5 недель и поздние реакции через 6 и более недель.
При химиотерапии кожа у пациента становится очень сухой, истончается, шелушится, трескается; может появляться кожный зуд. На лице, голове, туловище появляются акнеподобные (угревые) высыпания. На ладонях и подошвах кожа краснеет, грубеет, трескается, шелушится. На туловище и конечностях могут появляться высыпания в виде пятен и узелков. При попадании на кожу солнечных лучей могут возникать фотоаллергические реакции. Развивается выпадение волос, изменения ногтей и ногтевых валиков.
Типы кожной токсичности
К настоящему моменту описано более 30 различных вариантов кожной токсичности. Наиболее часто встречаются:
Химиотерапия, таргетная терапия и кожная токсичность
Для различных видов противоопухолевой терапии характерны свои особенности кожных реакций.
Так при химиотерапии (цитостатики) нарушаются процессы роста и механизмы деления всех клеток организма, а не только опухолевых. При этом происходит прямое цитотоксическое действие на клетки кожи и ее придатков, вследствие чего развиваются ладонно-подошвенный синдром, нарушение пигментации кожи, выпадение волос, изменение ногтей.
При таргетной терапии клетки кожи становятся «второй мишенью», помимо опухолевых клеток, так как несут на себе те же рецепторы, блокируемые препаратом. Например, препараты ингибиторы EGFR (эпидермального фактора роста) подавляют рост клеток кожи, волос и ногтей, вызывают выброс повреждающих тканевых ферментов и асептическое воспаление. В результате развиваются акнеподобные (угревые) высыпания, ксероз (сухость, истончение, шелушение) кожи, изменения волос и ногтей, поражение слизистых оболочек, ладонно-подошвенные кожные реакции, фотореакции (патологические кожные реакции на солнце).
Степень кожной токсичности
При оценке степени тяжести кожной токсичности учитывается площадь поражения, объективное ухудшение кожного процесса, выраженность субъективных ощущений пациента, нарушение его повседневной жизнедеятельности.
Так, например, по выраженности угревой (акнеподобной) сыпи выделяют 4 степени процесса:
I степень — площадь высыпаний менее 10%, возможен кожный зуд (болезненность);
II степень — площадь высыпаний 10-30%, кожный зуд (болезненность), негативное психологическое воздействие, ограничение активности;
III степень — площадь высыпаний более 30% кожный зуд (болезненность), негативное психологическое воздействие, ограничение самообслуживания, возможна локальная суперинфекция;
IV степень — площадь высыпаний любая связанная с распространенной суперинфекцией, требующей назначения внутривенной антибиотикотерапии, жизнеугрожающее состояние.
Таким образом, более тяжелые степени кожной токсичности требуют более активной терапии, снижения дозы химиопрепаратов, а при тяжелой III-IV степени приходится прерывать противоопухолевую терапию.
Первая помощь при кожной токсичности
Уже накануне противоопухолевой терапии врач-онколог назначает профилактическую терапию кожной токсичности, которая включает в себя:
Если на фоне профилактической терапии проявления кожной токсичности все-таки прогрессируют, необходимо сообщить об этом лечащему врачу и получить консультацию врача-дерматолога (дерматовенеролога), который назначит дополнительное лечение кожной токсичности.
Кроме того, пациенты с наличием хронических кожных заболеваний должны получить консультацию врача-дерматолога еще перед началом курса химиотерапии.
Чем опасно отсутствие лечения кожной токсичности?
При отсутствии лечения кожной токсичности возможно развитие распространенной суперинфекции, тяжелого жизнеугрожающего состояния и прерывание курса системной лекарственной противоопухолевой терапии.
Как правильно ухаживать за кожей во время химиотерапии?
Полностью избежать кожной токсичности невозможно, но при помощи следующих профилактических мероприятий можно уменьшить ее интенсивность:
Что делать, если возникает зуд?
Если пациент получает профилактическую терапию кожной токсичности: увлажняющие кремы-эмоленты утром, 1% гидрокортизоновый крем вечером, солнцезащитный крем и все-таки возникает зуд, — следует обратиться к лечащему врачу, либо на консультацию врача-дерматолога (дерматовенеролога).
Для облегчения зуда можно дополнительно нанести на зудящие области кремы-эмоленты. Внутрь можно принять 1 таблетку антигистаминного препарата 2-го поколения.
Что делать, если возникает сыпь?
Если пациент применяет профилактическую терапию кожной токсичности и при этом развивается сыпь, следует обратиться к лечащему врачу, который оценит степень тяжести, назначит дополнительное лечение, либо консультацию врача-дерматолога (дерматовенеролога).
Что делать, если поднялась температура?
Следует сообщить об этом лечащему врачу. При повышении температуры тела выше 38 гр. необходимо принять внутрь нестероидный противовоспалительный препарат.
Что делать, если есть сухость и шелушения?
Сухость и шелушение хорошо корректируются при помощи кремов-эмолентов, которые можно наносить 2 и более раз в сутки.
Что делать, если кожа меняет цвет?
Гиперпигментация кожи обычно развивается через 2–3 недели после окончания химиотерапии или на 10–12 неделе после начала курса лечения. Появляются окрашенные пятна на кончиках пальцев, локтевых суставах или ладонях, лице, вдоль используемых для инъекции вен.
Гиперпигментация дополнительного лечения не требует. После окончания курса противоопухолевой терапии она постепенно исчезнет. Специфической профилактики нет.
Как вести себя на солнце во время проведения курса химиотерапии?
Необходимо исключить пребывание на солнце. Рекомендовано ношение одежды с длинным рукавом, головной убор с широкими полями, солнцезащитные очки. Для верхней одежды предпочтение следует отдавать льняным тканям как более эффективным в отношении солнцезащиты, чем хлопчатобумажные. При этом окрашенные ткани обладают большим защитным эффектом по сравнению с белыми. Кроме того, нейлон, шерсть и полиэстер лучше защищают от ультрафиолетового облучения, чем хлопок.
Даже в холодные периоды года и при отсутствии солнца за 20 мин до выхода на улицу рекомендуется наносить на открытые участки кожи (лицо, кисти и др.) аптечные солнцезащитные кремы с максимальной комплексной защитой: SPF 50+/PPD 46.
Что при кожной токсичности категорически нельзя делать?
Нельзя заниматься самолечением кожной токсичности, в том числе народными средствами и самостоятельно снижать дозу, либо отменять противоопухолевые препараты.
Подошвенный синдром после химиотерапии чем лечить
Московский научно-практический Центр дерматовенерологии и косметологии Департамента здравоохранения, Москва
Московская медицинская академия им. И.М. Сеченова
Коррекция побочных эффектов противоопухолевой терапии cорафенибом
Журнал: Клиническая дерматология и венерология. 2015;14(3): 94-97
Круглова Л. С., Жукова О. В. Коррекция побочных эффектов противоопухолевой терапии cорафенибом. Клиническая дерматология и венерология. 2015;14(3):94-97.
Kruglova L S, Zhukova O V. Correction of side effects of anticancer sorafenib therapy. Klinicheskaya Dermatologiya i Venerologiya. 2015;14(3):94-97.
https://doi.org/10.17116/klinderma201514394-97
Московский научно-практический Центр дерматовенерологии и косметологии Департамента здравоохранения, Москва
Рассмотрены вопросы о побочных эффектах мультикиназного ингибитора сорафениба и их коррекции со стороны кожного покрова. Речь идет о ладонно-подошвенном синдроме, дерматите, ксерозе, зуде и алопеции. Авторы отмечают, что лечение побочных реакций порой представляет собой сложную задачу с необходимостью включать в него системную и наружную терапию. Среди профилактических мероприятий рассмотрены вопросы по уходу за кожей с использованием эмолентов, гипоаллергенных моющихся средств. Авторы обращают внимание на необходимость соблюдения режима труда и отдыха, ношение удобной обуви и хлопчатобумажной одежды. Информирование пациента и правильно подобранные профилактические средства способствуют снижению побочных действий противоопухолевого препарата и облегчают симптоматику со стороны кожного покрова.
Московский научно-практический Центр дерматовенерологии и косметологии Департамента здравоохранения, Москва
Московская медицинская академия им. И.М. Сеченова
Разработка и внедрение в клиническую практику мультикиназного ингибитора сорафениба открыло новые возможности в лечении ряда онкологических заболеваний. На сегодняшний день сорафениб (Нексавар) является одним из самых эффективных противоопухолевых препаратов направленного действия для лечения гепатоцеллюлярной карциномы, дифференцированного рака щитовидной железы, метастатического почечно-клеточного рака. По данным клинических исследований [1—3], включение сорафениба в комплекс терапевтических мероприятий у данной категории больных увеличивает медиану выживаемости и в ряде случаев позволяет добиться стойкого эффекта на протяжении нескольких лет. Cегодня применение сорафениба представляет собой единственный метод системной терапии, который в клинических исследованиях III фазы вызывал достоверное увеличение выживаемости в прогностически неблагоприятной группе больных с распространенным гепатоцеллюлярным раком [4].
Сорафениб относится к мультикиназным ингибиторам и способствует уменьшению пролиферации опухолевых клеток in vitro. Показано, что сорафениб подавляет многочисленные внутриклеточные киназы (с-CRAF, BRAF и мутантную BRAF) и киназы, расположенные на поверхности клетки (KIT, FLT-3, RET, VEGFR-l, VEGFR-2, VEGFR-3 и PDGFR-β). Полагают, что некоторые из этих киназ задействованы в сигнальных системах опухолевой клетки, в процессах ангиогенеза и апоптоза [5].
Как любой системный противоопухолевый препарат сорафениб может вызывать различные побочные реакции. Результаты клинических наблюдений и данные постмаркетинговых исследований показали, что применение сорафениба может сопровождаться следующими побочными эффектами из категории «не угрожающие жизни последствия»: артериальная гипертензия (41%), общая слабость (50%), снижение массы тела (47%), ладонно-подошвенная кожная реакция (ладонно-подошвенная эритродизестезия) (76%), кожная сыпь (50%), диарея (69%), гипокальциемия (19%). Следует отметить, что, по данным ряда авторов, некоторые нежелательные явления у пациентов с дифференцированным раком щитовидной железы регистрируются несколько чаще, чем в исследованиях препарата при почечно-клеточном или гепатоцеллюлярном раке. Отмеченные нежелательные явления включали ладонно-подошвенный синдром, диарею, алопецию, снижение массы тела, артериальную гипертензию, гипокальциемию и кератоакантому [6].
Применительно к кожным покровам наиболее встречаемыми побочными эффектами являются ладонно-подошвенный синдром, дерматит, алопеция, ксероз и зуд. Последние два, несмотря на частое упоминание в научных статьях, как отдельные негативные последствия рассматриваются редко. Данные состояния, безусловно, не могут приводить к летальному исходу, но в значительной степени причиняют дискомфорт и снижают качество жизни больных. Поэтому профилактические мероприятия и своевременная коррекция кожных проявлений побочных эффектов является важной задачей. Следует отметить, что информирование пациентов о возможных побочных эффектах может быть весьма полезным.
В ряде случаев развитие кожных побочных эффектов может потребовать коррекции дозы препарата. Как правило, это касается ладонно-подошвенного синдрома и дерматита, при этом основным критерием для снижения дозы является степень выраженности (II—III степень) или степень тяжести (тяжелая степень) проявлений кожной реакции. В дальнейшем при условии уменьшения выраженности кожных реакций до 0—I степени после не менее 28 дней лечения сниженной дозой препарата она может быть увеличена.
Ладонно-подошвенный синдром
При противоопухолевом лечении мультикиназными ингибиторами достаточно часто возникает ладонно-подошвенный синдром (ЛПС), что обусловлено экстравазацией препарата в ткани с последующим их повреждением. Он проявляется в виде эритемы, отека, болевых ощущений, гиперестезий, а в некоторых случаях (тяжелая степень течения) — в виде образования пузырных элементов, тотальной десквамации, глубоких трещин на ладонях и подошвах, что может приводить к ограничению при выполнении физических действий руками и ходьбе. Ладонно-подошвенный синдром обычно не превышает I—II степени тяжести (около 70% пациентов) и возникает, как правило, в первые 6 нед приема препарата [6]. Однако приблизительно у 20% пациентов ЛПС может достигать тяжелой степени: в этом случае рекомендовано снижение дозы сорафениба на фоне активного лечения ладонно-подошвенного синдрома.
Лечение ЛПС представляет достаточно сложную задачу, поскольку патологический процесс поддерживается приемом препарата. В тяжелых случаях может потребоваться назначение системных кортикостероидов в дозе 30—40 мг в преднизолоновом эквиваленте, диметилсульфоксида наружно для снижения экстравазации препарата, витамина В 6 (пиридоксин) и безрецептурных обезболивающих, таких как ацетаминофен, с целью купирования болевого симптома [7]. Возможно назначение амифостина (цитопротекторное вещество). Так, в патенте США № 6060083 раскрыто использование местного диметилсульфоксида для лечения ЛПС, в частности, когда осложнение было вызвано использованием другого противоопухолевого препарата — пегилированного липосомального доксорубицина.
Имеются данные об эффективности применения аллопуринола, который ингибирует ксантиноксидазу посредством блокирования продукции мочевой кислоты, обеспечивая таким образом защиту от опосредованного мочевой кислотой конечного повреждения органов в условиях, ассоциированных с повышенной ее продукцией. В исследованиях было обнаружено, что аллопуринол или его фармацевтически приемлемые соли при местном нанесении на ладони и ступни очень эффективны в лечении и предупреждении ладонно-подошвенной эритродизэстезии, индуцируемой химиотерапией фторпиримидином [8]. Таким образом, данный препарат может быть весьма полезен при ЛПС, обусловленном сорафенибом.
Наружное лечение включает использование препаратов ланолина и производных нефти с гидроксихинолинсульфатом в качестве антисептического компонента, эпителизирующих средств (декспантенол, метилурацил, актовегин, препараты серебра), противовоспалительных (топические глюкокортикостероиды), в том числе под окклюзию. Последние чаще рекомендуют назначать в виде композитных препаратов для предупреждения вторичного инфицирования.
К мерам профилактики и ослабления выраженности ладонно-подошвенного синдрома можно отнести следующие рекомендации: уходовые процедуры (охлаждающие ванночки с чередой, сборы трав эликосол или бруснивер), постоянное применение эмолентов с высоким содержанием мочевины (10—30%), охранительный режим (ношение удобной обуви, мягких хлопчатобумажных носков, ограничение излишних нагрузок на руки и ноги). В этом плане можно порекомендовать пациентам использовать специальные носки и повязки с мягким силиконом (разработанные для больных буллезным эпидермолизом), за счет которого они поддерживают влажную среду, предупреждают травматизацию кожи и способствуют заживлению уже образовавшихся пузырных элементов.
Дерматит
У 50% пациентов развивается дерматит как на ограниченных участках кожи (преимущественно лицо), так на всем кожном покрове. Элементы сыпи представлены эритемой, незначительной десквамацией, в редких случаях могут наблюдаться везикулы и папулы. При ограниченном процессе короткими курсами назначают кортикостероидные топические препараты, преимущественно сильного действия, но безопасные, например, гидрокортизон-17-бутират. Также используют эмоленты с противовоспалительным потенциалом. При дерматите важным является охранительный режим (ношение хлопчатобумажной одежды, мягкие гипоаллергенные моющие средства, фотозащита, ограничение физической нагрузки).
Ксероз
Ксероз (сухость) обусловлен нарушением барьерной функции кожи, при этом в ряде случаев он является неизменным симптомом побочных реакций противоопухолевых препаратов, в других ситуациях — следствием самого заболевания. Кожный барьер, обеспечивающий нормальный уровень увлажненности, включает кератиноциты, связанные между собой корнеодесмосомами, внеклеточные белковые и липидные структуры и внутриклеточный фактор естественного увлажнения кожи — NMF (natural moisturizing factor), состоящий из свободных аминокислот и их производных, которые образуются при распаде филаггрина. Нарушения в любой из этих структур неизбежно приводят к нарушению кожного барьера и избыточной трансэпидермальной потери воды.
При приеме мультикиназных ингибиторов ксероз возникает в первые недели приема, при этом степень выраженности имеет прямую корреляционную зависимость от длительности приема препарата, однако степень выраженности крайне редко бывает сильной.
На сегодняшний день арсенал топических препаратов, используемых для восстановления барьерной функции кожи, с различными механизмами действия, достаточно обширен. При этом число таких средств растет, что обусловливает определенные трудности в выборе наиболее оптимального из них, а значит, дерматологам необходимо уметь ориентироваться в этом многообразии, чтобы правильно подобрать нужный препарат для каждого конкретного случая.
По существу все дерматокосметологические средства разрабатываются специально для борьбы с проблемой ксероза кожи и в зависимости от механизма действия подразделяются на четыре основные группы:
— создающие окклюзию на поверхности (пассивное увлажнение);
— восполняющие дефицит веществ, которые входят в состав натурального увлажняющего фактора (активное увлажнение);
— стимулирующие синтез собственных факторов увлажнения (активное увлажнение);
— содержащие активные вещества, влияющие на окислительно-восстановительные процессы, например, антиоксиданты (опосредованное влияние на увлажненность кожи).
Безусловным преимуществом обладают наружные препараты, воздействующие сразу на несколько механизмов прогрессирования ксероза. При проведении противоопухолевой терапии, которая сама по себе является предиктором возникновения ксероза, увлажняющие топические препараты целесообразно назначать одновременно с основным лечением, в этом случае их применение можно рассматривать как профилактику. При возникшем ксерозе наиболее показаны препараты с мочевиной (2—10%), с прецерамидами, аллантоином, маслом ши (карите), льняным маслом, производные филаггрина и др.
Еще одним важным моментом в устранении ксероза можно считать правильное использование средств для душа. Больным необходимо рекомендовать такие гели и пены для ванн, которые также опосредованно обладают увлажняющим потенциалом и являются гипоаллергенными.
Относительно редко при применении сорафениба встречается зуд, который характеризуется внезапным началом, различной степенью интенсивности, не зависит от времени суток и плохо поддается лечению антигистаминными препаратами. Как правило, зуд у таких пациентов может быть обусловлен двумя причинами: ксерозом кожи и выделением субстанции Р в эпидермальных нервных окончаниях. В первом случае он хорошо купируется с помощью увлажняющих средств, во втором — целесообразно применение противозудных препаратов, топических ингибиторов кальциневрина, наружных кортикостероидов короткими курсами, антигистаминных препаратов (1-й и 2-й генерации). Рекомендуется протирать кожу 3—5% водным раствором уксуса, водно-спиртовыми растворами с 1% салициловой кислотой, анестезином, новокаином, ментолом, уротропино-тальковыми присыпками.
Алопеция
Повреждение аппарата волосяных фолликулов характерно практически для всех противоопухолевых препаратов. Прогноз зависит от длительности приема и дозы препарата, а также от индивидуальных особенностей организма пациента. При отсутствии необратимого повреждения волосяного фолликула прогноз достаточно благоприятный: после прекращения приема средства происходит восстановление роста волос. В период курсового лечения терапевтические мероприятия в отношении алопеции проводить нецелесообразно, можно лишь порекомендовать пациентам ношение париков.
Таким образом, побочные эффекты противоопухолевой терапии носят прогнозируемый и проходящий характер. Однако значительное отрицательное их влияние на повседневное функционирование и качество жизни пациентов, безусловно требует активных терапевтических мероприятий, начатых в как можно более ранние сроки. В ряде случаев предвестники возникновения кожных побочных эффектов, такие например, как ксероз, помогают предупредить развитие или снизить степень выраженности более тяжелых побочных эффектов.