Проведение нервного импульса
Полезное
Смотреть что такое «Проведение нервного импульса» в других словарях:
проведение возбуждения бездекрементное — (лат. decrementum уменьшение, от decresco уменьшаться, убывать) П. в. без существенного изменения величины нервного импульса … Большой медицинский словарь
проведение возбуждения декрементное — (лат. decrementum уменьшение от decresco уменьшаться, убывать) П. в., сопровождающееся уменьшением величины нервного импульса … Большой медицинский словарь
ПРОВЕДЕНИЕ — 1. Передача нервного импульса из одного места в другое. 2. Механическая передача звуковых волн через барабанную перепонку и слуховые косточки … Толковый словарь по психологии
Сальтаторное проведение — (лат. saltatorius, от salto скачу, прыгаю) скачкообразное проведение нервного импульса по мякотным (миелинизированным) нервам, оболочка которых обладает относительно высоким сопротивлением электрическому току. По длине нерва регулярно… … Большая советская энциклопедия
САЛЬТАТОРНОЕ ПРОВЕДЕНИЕ — (лат. saltatorius, от salto скачу, прыгаю), скачкообразное проведение нервного импульса от одного перехвата Ранвье к другому вдоль мякотного (миелинизированного) аксона. Для С. п. характерно сочетание электротонич. распространения по… … Биологический энциклопедический словарь
Незатухающее проведение — – термин, которым обозначают характеристику проведения нервного импульса по аксону, которое происходит в режиме «всё или ничего» … Энциклопедический словарь по психологии и педагогике
НЕЗАТУХАЮЩЕЕ ПРОВЕДЕНИЕ — Фраза, используемая для характерис ики проведения нервного импульса по аксону, которое происходит в режиме все или ничего … Толковый словарь по психологии
нервный импульс — волна возбуждения, распространяющаяся по нервному волокну, в ответ на раздражение нейронов. Обеспечивает передачу информации от рецепторов в центральную нервную систему и от неё к исполнительным органам (мышцам, железам). Проведение нервного… … Энциклопедический словарь
Нервные волокна — Нервные волокна отростки нейронов, покрытые глиальными оболочками. В различных отделах нервной системы оболочки нервных волокон значительно отличаются по своему строению, что лежит в основе деления всех волокон на миелиновые и безмиелиновые … Википедия
Потенциал действия — Потенциал действия волна возбуждения, перемещающаяся по мембране живой клетки в процессе передачи нервного сигнала. По сути своей представляет электрический разряд быстрое кратковременное изменение потенциала на небольшом участке… … Википедия
2_3 Потенциал действия и нервный импульс
Нервный импульс
Разбираясь в нервных импульсах, мы будем иметь в виду нервное возбуждение, бегущее (=распространяющееся) по мебране нейрона. Строго говоря, движущееся по нейронам и нервам возбуждение представляет собой нервные импульсы, а не потенциалы действия, хотя в физиологической литературе два этих понятия обычно используют как синонимы.
Можно сказать короче:
Потенциал действия – это резкое скачкообразное изменение мембранного потенциала с отрицательного на положительный и обратно.
Сравните два приведённых выше рисунка (покликайте по ним) и, как говорится, почувствуйте разницу!
Где рождаются нервные импульсы?
Как ни странно, не все студенты, изучившие физиологию возбуждения, могут ответить на этот вопрос. ((
Хотя ответ не сложен. Нервные импульсы рождаются на нейронах всего в нескольких местах:
1) аксонный холмик (это переход тела нейрона в аксон),
2) рецепторное окончание дендрита,
3) первый перехват Ранвье на дендрите (триггерная зона дендрита),
4) постсинаптическая мембрана возбуждающего синапса.
Места возникновения нервных импульсов:
Важно также учесть следующий факт. От аксонного холмика нервный импульс разбегается по всей мембране своего нейрона: как по аксону к пресинаптическоим окончаниям, так и по дендритам к постсинаптическим «начинаниям». Все локальные потенциалы при этом снимаются с мембраны нейрона и со всех его синапсов, т.к. они «перебиваются» потенциалом действия от пробегающего по всей мембране нервного импульса.
2. Рецепторное окончание чувствительного (афферентного) нейрона.
Если нейрон имеет рецепторное окончание, то на него может воздействовать адекватный раздражитель и порождать на этом окончании сначала рецепторный потенциал, затем генераторный потенциал, а потом и нервный импульс. Когда генераторный потенциал достигает КУД, то на этом окончании открываются потенциал-зависимые натриевые ионные каналы и рождается потенциал действия и нервный импульс. Нервный импульс бежит по дендриту к телу нейрона, а затем по его аксону к пресинаптическим окончаниям для передачи возбуждения на следующий нейрон. Так работают, к примеру, болевые рецепторы (ноцицепторы), являющиеся дендритными окончаниями болевых нейронов. Нервные импульсы в болевых нейронах вознимают именно на рецепторных окончаниях дендритов.
3. Первый перехват Ранвье на дендрите (триггерная зона дендрита).
4. Постсинаптическая мембрана возбуждающего синапса.
В редких случаях ВПСП на возбуждающем синапсе может быть настолько силён, что прямо там же достигает КУД и порождает нервный импульс. Но чаще это бывает возможно только в результате суммации нескольких ВПСП: или с нескольких соседних синапсов, сработавших одновременно (пространственная суммация), или за счёт того, что на данный синапс пришло несколько импульсов подряд (временная суммация).
Видео: Проведение нервного импульса по нервному волокну
Потенциал действия как нервный импульс
Ниже размещён материал, взятый из учебно-методического пособия автора данного сайта, на который вполне можно ссылаться в своём списке литературы:
Сазонов В.Ф. Понятие и виды торможения в физиологии центральной нервной системы: Учебно-методическое пособие. Ч. 1. Рязань: РГПУ, 2004. 80 с.
Все процессы мембранных изменений, происходящих в ходе распространяющегося возбуждения, достаточно хорошо изучены и описаны в научной и учебной литературе. Но не всегда это описание легко понять, поскольку в данном процессе задействовано слишком много компонентов (с точки зрения обычного студента, а не вундеркинда, конечно).
Для облегчения понимания мы предлагаем рассматривать единый электрохимический процесс распространяющегося динамичного возбуждения с трех сторон, на трех уровнях:
Электрические явления – развитие потенциала действия.
Химические явления – движение ионных потоков.
Структурные явления – поведение ионных каналов.
Три стороны процесса распространяющегося возбуждения
1. Потенциал действия (ПД)
Потенциал действия – это скачкообразное изменение постоянного мембранного потенциала с отрицательной поляризации на положительную и обратно.
Обычно мембранный потенциал в нейронах ЦНС изменяется от –70 мВ до +30 мВ, а затем вновь возвращается к исходному состоянию, т.е. к –70 мВ. Как видим, понятие потенциала действия характеризуется через электрические явления на мембране.
Кратко опишем электрические явления во время течения потенциала действия:
Восходящая ветвь графика:
потенциал покоя – исходное обычное поляризованное электроотрицательное состояние мембраны (–70 мВ);
нарастающий локальный потенциал – пропорциональная раздражителю деполяризация;
критический уровень деполяризации (–50 мВ) – резкое ускорение деполяризации (за счет самораскрытия натриевых каналов), с этой точки начинается спайк – высокоамплитудная часть потенциала действия;
самоусиливающаяся круто нарастающая деполяризация;
переход нулевой отметки (0 мВ) – смена полярности мембраны;
«овершут» – положительная поляризация (инверсия, или реверсия, заряда мембраны);
пик (+30 мВ) – вершина процесса изменения полярности мембраны, вершина потенциала действия.
Нисходящая ветвь графика:
реполяризация – восстановление прежней электроотрицательности мембраны;
переход нулевой отметки (0 мВ) – обратная смена полярности мембраны на прежнюю, отрицательную;
переход критического уровня деполяризации (–50 мВ) – прекращение фазы относительной рефрактерности (невозбудимости) и возврат возбудимости;
следовые процессы (следовая деполяризация или следовая гиперполяризация);
восстановление потенциала покоя – норма (–70 мВ).
Итак, сначала – деполяризация, затем – реполяризация. Сначала – утрата электроотрицательности, затем – восстановление электроотрицательности.
Образно можно сказать, что заряженные ионы – это и есть создатели электрических потенциалов в нервных клетках. Для многих людей звучит странно утверждение, что вода не проводит электрический ток. Но на самом деле это так. Сама по себе вода является диэлектриком, а не проводником. В воде электрический ток обеспечивают не электроны, как в металлических проводах, а заряженные ионы: положительные катионы и отрицательные анионы. В живых клетках основную «электрическую работу» выполняют катионы, так как они более подвижны. Электрические токи в клетках – это потоки ионов.
На химическом уровне мы, описывая распространяющееся возбуждение, должны рассмотреть, как изменяются характеристики ионных потоков, идущих через мембрану. Главное в этом процессе то, что при деполяризации резко усиливается поток ионов натрия внутрь клетки, а затем он внезапно прекращается на спайке потенциала действия. Входящий поток натрия как раз и вызывает деполяризацию, так как ионы натрия приносят с собой положительные заряды в клетку (чем и снижают электроотрицательность). Затем, после спайка, значительно нарастает выходящий наружу поток ионов калия, что вызывает реполяризацию. Ведь калий, как мы неоднократно говорили, выносит с собой из клетки положительные заряды. Отрицательные заряды остаются внутри клетки в большинстве, и за счет этого усиливается электроотрицательность. Это и есть восстановление поляризации за счет выходящего потока ионов калия. Заметим, что выходящий поток ионов калия возникает практически одновременно с появлением натриевого потока, но нарастает медленно и длится в 10 раз дольше. Несмотря на продолжительность калиевого потока самих ионов расходуется немного – всего одна миллионная доля от запаса калия в клетке (0,000001 часть).
Подведем итоги. Восходящая ветвь графика потенциала действия образуется за счет входа в клетку ионов натрия, а нисходящая – за счет выхода из клетки ионов калия.
Параллельно в открытием натриевых каналов с небольшим отставанием во времени идет нарастающее открытие калиевых каналов. Они медлительные по сравнению с натриевыми. Открытие дополнительных калиевых каналов усиливает выход положительных ионов калия из клетки. Выход калия противодействует «натриевой» деполяризации и вызывает восстановление полярности (восстановление электроотрицательности). Но натриевые каналы опережают калиевые, они срабатывают примерно в 10 раз быстрее. Поэтому входящий поток положительных ионов натрия в клетку опережает компенсирующий выход ионов калия. И поэтому деполяризация развивается опережающими темпами по сравнению с противодействующей ей поляризацией, вызванной утечкой ионов калия. Вот почему, пока натриевые каналы не закроются, восстановление поляризации не начнется.
Пожар как метафора распространяющегося возбуждения
Для того чтобы перейти к пониманию смысла динамичного процесса возбуждения, т.е. к пониманию его распространения вдоль мембраны, надо представить себе, что описанные нами выше процессы захватывают сначала ближайшие, а затем все новые, все более и более отдаленные участки мембраны, пока не пробегут по всей мембране полностью. Если вы видели «живую волну», которую устраивают болельщики на стадионе за счет вставания и приседания, то вам легко будет представить себе мембранную волну возбуждения, которая образуется за счет последовательного протекания в соседних участках трансмембранных ионных токов.
Когда мы искали образный пример, аналогию или метафору, которая может наглядно передать смысл распространяющегося возбуждения, то остановились на образе пожара. Действительно, распространяющееся возбуждение похоже на лесной пожар, когда горящие деревья остаются на месте, а фронт огня распространяется и уходит все дальше и дальше во все стороны от очага возгорания.
Как же в этой метафоре будет выглядеть явление торможения?
Ответ очевиден – торможение будет выглядеть как тушение пожара, как уменьшение горения и затухание огня. Но если огонь распространяется сам по себе, то тушение требует усилий. Из потушенного участка процесс тушения сам по себе не пойдет во все стороны.
Существует три варианта борьбы с пожаром: (1) либо надо ждать, когда все сгорит и огонь истощит все горючие запасы, (2) либо надо поливать водой горящие участки, чтобы они погасли, (3) либо надо поливать заранее ближайшие нетронутые огнем участки, чтобы они не загорелись.
Можно ли «погасить» волну распространяющегося возбуждения?
Вряд ли нервная клетка способна «погасить» этот начавшийся «пожар» возбуждения. Поэтому первый способ подходит только для искусственного вмешательства в работу нейронов (например, в лечебных целях). Но вот «залить водичкой» некоторые участки и поставить блок распространению возбуждения, оказывается, вполне возможно.
© Сазонов В.Ф. Понятие и виды торможения в физиологии центральной нервной системы: Учебно-методическое пособие. Ч. 1. Рязань: РГПУ, 2004. 80 с.
АВТОВОЛНЫ В АКТИВНО-ВОЗБУДИМЫХ СРЕДАХ (АВС)
Основные свойства волн, распространяющихся в активно-возбудимых средах (АВС)
Видео: Потенциал действия (Action potential)
НЕРВНЫЙ ИМПУЛЬС
Нервный импульс обеспечивает передачу информации от рецепторов к нервным центрам и от них к исполнительным органам — скелетной мускулатуре, гладким мышцам внутренних органов и сосудов, железам внутренней и внешней секреции и т. д.
Сложная информация о действующих на организм раздражениях кодируется в виде отдельных групп Нервных импульсов — рядов. Согласно закону «Все или ничего» (см.) амплитуда и длительность отдельных Нервных импульсов, проходящих по одному и тому же волокну, постоянны, а частота и количество Нервных импульсов в ряду зависят от интенсивности раздражения. Такой способ передачи информации является наиболее помехоустойчивым, т. е. в широких пределах не зависит от состояния проводящих волокон.
Распространение Нервных импульсов отождествляется с проведением потенциалов действия (см. Биоэлектрические потенциалы). Возникновение возбуждения может быть результатом раздражения (см.), напр, воздействие света на зрительный рецептор, звука на слуховой рецептор, или процессов, протекающих в тканях (спонтанное возникновение Н. и.). В этих случаях Н. и. обеспечивают согласованную работу органов при протекании какого-либо физиологического процесса (напр., в процессе дыхания Н. и. вызывают сокращение скелетных мышц и диафрагмы, результатом чего являются вдох и выдох, и т. д.).
В живых организмах передача информации может осуществляться и гуморальным путем, посредством выброса в русло крови гормонов, медиаторов и т. п. Однако преимущество информации, передаваемой при помощи Н. и., состоит в том, что она более целенаправленна, передается быстро и может быть точнее закодирована, чем сигналы, посылаемые гуморальной системой.
Факт, что нервные стволы являются путем, по к-рому передаются влияния от мозга к мышцам и в обратном направлении, был известен еще в эпоху античности. В средние века и вплоть до середины 17 в. считалось, что по нервам распространяется некая субстанция, подобная жидкости или пламени. Идея о электрической природе Н. и. возникла в 18 в. Первые исследования электрических явлений в живых тканях, связанных с возникновением и распространением возбуждения, были осуществлены Л. Гальвани. Г. Гельмгольц показал, что скорость распространения Н. и., к-рую ранее считали близкой к скорости света, имеет конечное значение и может быть точно измерена. Германн (L. Hermann) ввел в физиологию понятие потенциала действия. Объяснение механизма возникновения и проведения возбуждения стало возможным после создания С. Аррениусом теории электролитической диссоциации. В соответствии с этой теорией Бернштейн (J. Bernstein) предположил, что возникновение и проведение Н. и. обусловлено перемещением ионов между нервным волокном и окружающей средой. Англ. исследователи А. Ходжкин, Б. Катц и Э. Хаксли детально исследовали трансмембранные ионные токи, лежащие в основе развития потенциала действия. Позже стали интенсивно изучаться механизмы работы ионных каналов, по к-рым происходит обмен ионами между аксоном и окружающей средой, и механизмы, обеспечивающие способность нервных волокон проводить ряды Н. и. разного ритма и продолжительности.
Н. и. распространяется за счет местных токов, возникающих между возбужденным и невозбужденным участками нервного волокна. Ток, выходящий из волокна наружу в покоящемся участке, служит раздражителем. Наступающая после возбуждения в данном участке нервного волокна рефрактерность обусловливает поступательное движение Н. и.
Количественно соотношения разных фаз развития потенциала действия можно охарактеризовать, сопоставляя их по амплитуде и длительности во времени. Так, напр., для миелиновых нервных волокон группы А млекопитающих диаметр волокна находится в пределах 1—22 мк, скорость проведения — 5—120 м/сек, длительность и амплитуда высоковольтной части (пика, или спайка) — 0,4—0,5 мсек и 100—120 мв соответственно, следовой негативный потенциал — 12—20 мсек (3—5% от амплитуды спайка), следовой позитивный потенциал — 40—60 мсек (0,2% от амплитуды спайка).
Возможности передачи разнообразной информации расширяются за счет повышения скорости развития потенциала действия, скорости распространения, а также за счет повышения лабильности (см.) — т. е. способности возбудимого образования воспроизводить в единицу времени высокие ритмы возбуждения.
Возникновение Н. и. в нервных клетках (см.) или рецепторах (см.) связано с деполяризацией мембраны, т. е. со снижением величины электрического потенциала на мембране (потенциала покоя, или мембранного потенциала). Если величина мембранного потенциала снижается на 10—20% (пороговый критический уровень), то местный процесс переходит в распространяющийся — возникает потенциал действия (см. Возбуждение).
Конкретные особенности распространения Н. и. связаны со строением нервных волокон (см.). Сердцевина волокна (аксоплазма) обладает низким сопротивлением и, соответственно, хорошей проводимостью, а окружающая аксоплазму плазматическая мембрана — большим сопротивлением. Особенно велико электрическое сопротивление наружного слоя у миелинизированных волокон, у к-рых свободны от толстой миелиновой оболочки только перехваты Ранвье. В безмиелиновых волокнах Н. и. движется непрерывно, а в миелиновых — скачкообразно (сальтаторное проведение).
Различают декрементное и бездекрементное распространение волны возбуждения. Декрементное проведение, т. е. проведение возбуждения с угасанием, наблюдается в безмиелиновых волокнах. В таких волокнах скорость проведения Н. и. невелика и по мере отдаления от места раздражения раздражающее действие местных токов постепенно уменьшается вплоть до полного угасания. Декрементное проведение свойственно волокнам, иннервирующим внутренние органы, обладающие низкой функц, подвижностью. Без декрементное проведение характерно для миелиновых и тех безмиелиновых волокон, к-рые передают сигналы к органам, обладающим высокой реактивностью (напр., сердечной мышце). При бездекрементном проведении Н. и. проходит весь путь от места раздражения до места реализации информации без затухания.
Максимальная скорость проведения Н. и., зарегистрированная в быстропроводящих нервных волокнах млекопитающих, составляет 120 м/сек. Высокие скорости проведения импульса могут быть достигнуты за счет увеличения диаметра нервного волокна (у безмиелиновых волокон) или за счет повышения степени миелинизации. Распространение одиночного Н. и. само по себе не требует непосредственных энергетических затрат, т. к. при определенном уровне поляризации мембраны каждый участок нервного волокна находится в состоянии готовности к проведению и раздражающий стимул играет роль «спускового курка». Однако восстановление исходного состояния нервного волокна и поддержание его в готовности к проведению нового Н. и. связано с затратой энергии биохимических реакций, протекающих в нервном волокне. Процессы восстановления приобретают большое значение в случае проведения рядов Н. и. При проведении ритмического возбуждения (рядов импульсов) в нервных волокнах приблизительно вдвое возрастает теплопродукция и потребление кислорода, расходуются макроэргические фосфаты и повышается активность Na,K-АТФ-азы к-рую отождествляют с натриевым насосом. Изменение интенсивности протекания различных физ.-хим. и биохимических процессов зависит от характера ритмического возбуждения (продолжительность рядов импульсов и частота их следования) и физиологического состояния нерва. При проведении большого числа Н. и. в высоком ритме в нервных волокнах может накапливаться «метаболический долг» (это находит отражение в увеличении суммарных следовых потенциалов), и тогда процессы восстановления затягиваются. Но и в этих условиях способность нервных волокон проводить Н. и. долгое время остается неизменной.
Передача Н. и. с нервного волокна на мышечное или какой-либо другой эффектор осуществляется через синапсы (см.). У позвоночных животных в подавляющем большинстве случаев передача возбуждения на эффектор происходит при помощи выделения ацетилхолина (нервно-мышечные синапсы скелетной мускулатуры, синаптические соединения в сердце и др.). Для таких синапсов характерно строго одностороннее проведение импульса и наличие временной задержки передачи возбуждения.
В синапсах, в синаптической щели которых сопротивление электрическому току благодаря большой площади контактирующих поверхностей мало, происходит электрическая передача возбуждения. В них нет синаптической задержки проведения и возможно двустороннее проведение. Такие синапсы свойственны беспозвоночным животным.
Регистрация Н. и. нашла широкое применение в биол, исследованиях и клин, практике. Для регистрации используют шлейфные и чаще катодные осциллографы (см. Осциллография). При помощи микроэлектродной техники (см. Микроэлектродный метод исследования) регистрируют Н. и. в одиночных возбудимых образованиях — нейронах и аксонах. Возможности исследования механизма возникновения и распространения Н. и. значительно расширились после разработки метода фиксации потенциала. Этим методом были получены основные данные о ионных токах (см. Биоэлектрические потенциалы).
Нарушение проведения Н. и. происходит при повреждении нервных стволов, напр, при механических травмах, сдавливании в результате разрастания опухоли или при воспалительных процессах. Такие нарушения проведения Н. и. зачастую бывают необратимы. Следствием прекращения иннервации могут быть тяжелые функциональные и трофические расстройства (напр., атрофия скелетных мышц конечностей после прекращения поступления Н. и. вследствие необратимой травмы нервного ствола). Обратимое прекращение проведения Н. и. может быть вызвано специально, в терапевтических целях. Напр., с помощью анестезирующих средств блокируют импульсацию, идущую от болевых рецепторов в ц. н. с. Обратимое прекращение проведения Н. и. вызывает и новокаиновая блокада. Временное прекращение передачи Н. и. по нервным проводникам наблюдается и во время общего наркоза.
Библиография: Бpеже М. А. Электрическая активность нервной системы, пер. с англ., М., 1979; Жуков Е. К. Очерки по нервно-мышечной физиологии, Л., 1969; Коннели К. Восстановительные процессы и обмен веществ в нерве, в кн.: Совр, пробл. биофизики, пер. с англ., под ред. Г. М. Франка и А. Г. Пасынского, т. 2, с. 211, М., 1961; Костюк П. Г. Физиология центральной нервной системы, Киев, 1977; Латманизова Л. В. Очерк физиологии возбуждения, М., 1972; Общая физиология нервной системы, под ред. П. Г. Костюка, Л., 1979; Тасаки И. Нервное возбуждение, пер. с англ., М., 1971; Ходжкин А. Нервный импульс, пер. с англ., М., 1965; Ходоров Б. И. Общая физиология возбудимых мембран, М., 1975.
Мозг, общение нейронов и энергетическая эффективность
По всей видимости, в эволюции сформировались энергетически эффективные механизмы кодирования и передачи информации в мозге. Подпись: «Усердно пытаюсь минимизировать энергозатраты».
Автор
Редакторы
Статья на конкурс «био/мол/текст»: Клеточные процессы, обеспечивающие обмен информацией между нейронами, требуют много энергии. Высокое энергопотребление способствовало в ходе эволюции отбору наиболее эффективных механизмов кодирования и передачи информации. В этой статье вы узнаете о теоретическом подходе к изучению энергетики мозга, о его роли в исследованиях патологий, о том, какие нейроны более продвинуты, почему синапсам иногда выгодно не «срабатывать», а также, как они отбирают только нужную нейрону информацию.
Конкурс «био/мол/текст»-2017
Эта работа опубликована в номинации «Свободная тема» конкурса «био/мол/текст»-2017.

Генеральный спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.

Спонсором приза зрительских симпатий и партнером номинации «Биомедицина сегодня и завтра» выступила фирма «Инвитро».

Происхождение подхода
С середины ХХ века известно, что головной мозг потребляет значительную часть энергоресурсов всего организма: четверть всей глюкозы и ⅕ всего кислорода в случае высшего примата [1–5]. Это вдохновило Уильяма Леви и Роберта Бакстера из Массачусетского технологического института (США) на проведение теоретического анализа энергетической эффективности кодирования информации в биологических нейронных сетях (рис. 1) [6]. В основе исследования лежит следующая гипотеза. Поскольку энергопотребление мозга велико, ему выгодно иметь такие нейроны, которые работают наиболее эффективно — передают только полезную информацию и затрачивают при этом минимум энергии.
Это предположение оказалось справедливым: на простой модели нейронной сети авторы воспроизвели экспериментально измеренные значения некоторых параметров [6]. В частности, рассчитанная ими оптимальная частота генерации импульсов варьирует от 6 до 43 имп./с — почти так же, как и у нейронов основания гиппокампа. Их можно подразделить на две группы по частоте импульсации: медленные (
40 имп./с). При этом первая группа значительно превосходит по численности вторую [7]. Аналогичная картина наблюдается и в коре больших полушарий: медленных пирамидальных нейронов (
4—9 имп./с) в несколько раз больше, чем быстрых ингибиторных интернейронов (>100 имп./с) [8], [9]. Так, видимо, мозг «предпочитает» использовать поменьше быстрых и энергозатратных нейронов, чтобы те не израсходовали все ресурсы [6], [9–11].
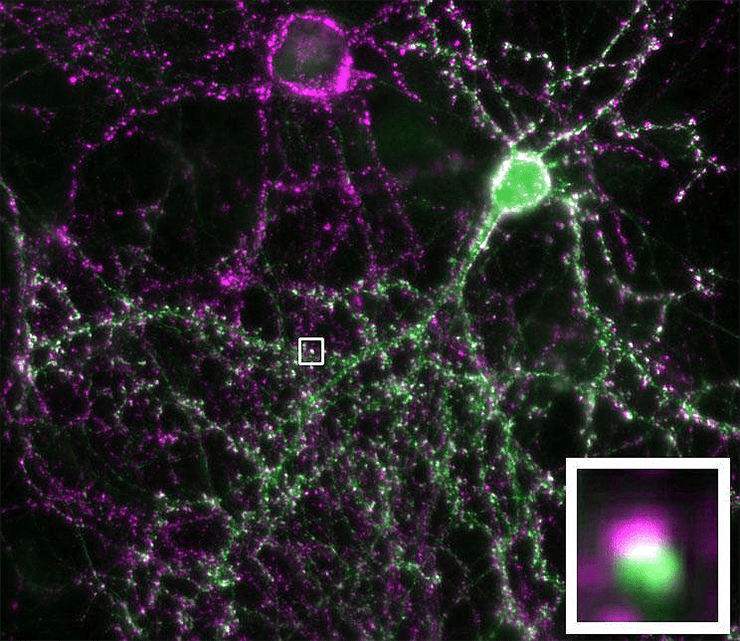
Рисунок 1. Представлены два нейрона. В одном из них фиолетовым цветом окрашен пресинаптический белок синаптофизин. Другой нейрон полностью окрашен зеленым флуоресцентным белком. Мелкие светлые крапинки — синаптические контакты между нейронами [12]. Во вставке одна «крапинка» представлена ближе.
Группы нейронов, связанных между собой синапсами, называются нейронными сетями [13], [14]. Например, в коре больших полушарий пирамидальные нейроны и интернейроны образуют обширные сети. Слаженная «концертная» работа этих клеток обусловливает наши высшие когнитивные и другие способности. Аналогичные сети, только из других типов нейронов, распределены по всему мозгу, определенным образом связаны между собой и организуют работу всего органа.
Что такое интернейроны?
Нейроны центральной нервной системы разделяются на активирующие (образуют активирующие синапсы) и тормозящие (образуют тормозящие синапсы). Последние в значительной степени представлены интернейронами, или промежуточными нейронами. В коре больших полушарий и гиппокампе они ответственны за формирование гамма-ритмов мозга [15], которые обеспечивают слаженную, синхронную работу других нейронов. Это крайне важно для моторных функций, восприятия сенсорной информации, формирования памяти [9], [11].
Интернейроны отличаются способностью генерировать значительно более высокочастотные сигналы, чем другие нейроны. Они также содержат больше митохондрий, главных органелл энергетического метаболизма, «фабрик» по производству АТФ. Последние к тому же содержат большое количество белков цитохром-с оксидазы и цитохрома-с, являющихся ключевыми для метаболизма. Так, интернейроны являются крайне важными и, в то же время, энергозатратными клетками [8], [9], [11], [16].
Работа Леви и Бакстера [6] развивает концепцию «экономии импульсов» Горация Барлоу из Университета Калифорнии (США), который, кстати, является потомком Чарльза Дарвина [17]. Согласно ей, при развитии организма нейроны стремятся работать только с наиболее полезной информацией, фильтруя «лишние» импульсы, ненужную и избыточную информацию. Однако эта концепция не дает удовлетворительных результатов, так как не учитывает метаболические затраты, связанные с нейрональной активностью [6]. Расширенный подход Леви и Бакстера, в котором внимание уделено обоим факторам, оказался более плодотворным [6], [18–20]. И энергозатраты нейронов, и потребность в кодировании только полезной информации являются важными факторами, направляющими эволюцию мозга [6], [21–24]. Поэтому, чтобы лучше разобраться в том, как устроен мозг, стоит рассматривать обе эти характеристики: сколько нейрон передает полезной информации и сколько энергии при этом тратит.
За последнее время этот подход нашел множество подтверждений [10], [22], [24–26]. Он позволил по-новому взглянуть на устройство мозга на самых разных уровнях организации — от молекулярно-биофизического [20], [26] до органного [23]. Он помогает понять, каковы компромиссы между выполняемой функцией нейрона и ее энергетической ценой и в какой степени они выражены.
Как же работает этот подход?
Положим, у нас есть модель нейрона, описывающая его электрофизиологические свойства: потенциал действия (ПД) и постсинаптические потенциалы (ПСП) (об этих терминах — ниже). Мы хотим понять, эффективно ли он работает, не тратит ли неоправданно много энергии. Для этого нужно вычислить значения параметров модели (например, плотность каналов в мембране, скорость их открывания и закрывания), при которых: (а) достигается максимум отношения полезной информации к энергозатратам и в то же время (б) сохраняются реалистичные характеристики передаваемых сигналов [6], [19].
Поиск оптимума
Эти «оптимальные» значения параметров затем нужно сравнить с измеренными экспериментально и определить, насколько они отличаются. Общая картина отличий укажет на степень оптимизации данного нейрона в целом: насколько реальные, измеренные экспериментально, значения параметров совпадают с рассчитанными. Чем слабее выражены отличия, тем нейрон более близок к оптимуму и работает энергетически более эффективно, оптимально. С другой стороны, сопоставление конкретных параметров покажет, в каком конкретно качестве этот нейрон близок к «идеалу».
Далее, в контексте энергетической эффективности нейронов рассмотрены два процесса, на которых основано кодирование и передача информации в мозге. Это нервный импульс, или потенциал действия, благодаря которому информация может быть отправлена «адресату» на определенное расстояние (от микрометров до полутора метров) и синаптическая передача, лежащая в основе собственно передачи сигнала от одного нейрона на другой.
Потенциал действия
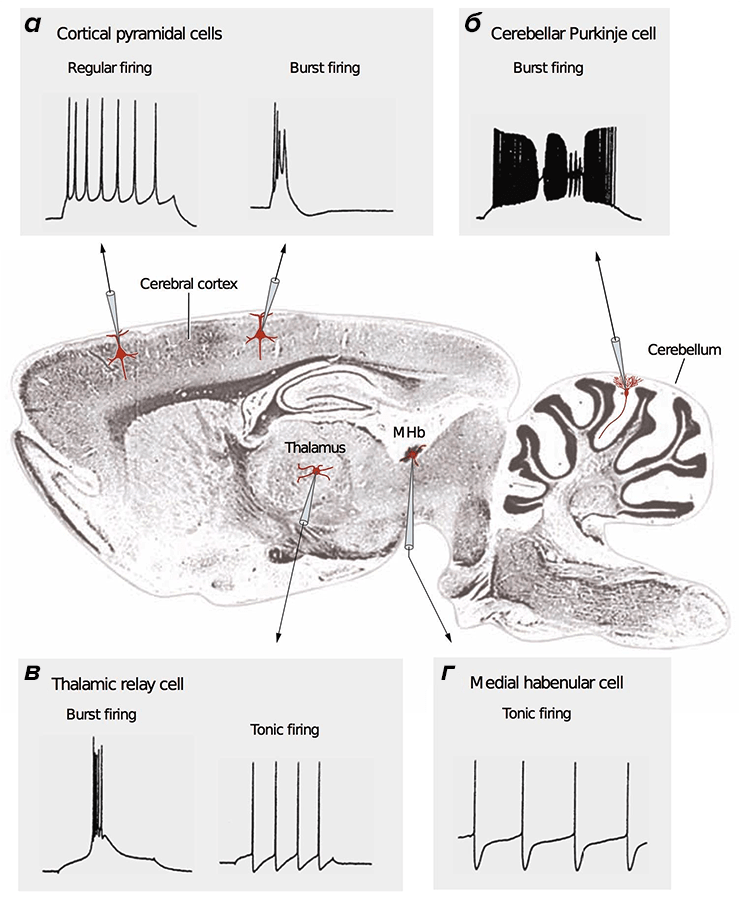
Потенциал действия (ПД) — сигнал, которые отправляют друг другу нейроны. ПД бывают разные: быстрые и медленные, малые и большие [28]. Зачастую они организованы в длинные последовательности (как буквы в слова), либо в короткие высокочастотные «пачки» (рис. 2).
Большое разнообразие сигналов обусловлено огромным количеством комбинаций разных типов ионных каналов, синаптических контактов, а также морфологией нейронов [28], [29]. Поскольку в основе сигнальных процессов нейрона лежат ионные токи, стоит ожидать, что разные ПД требуют различных энергозатрат [20], [27], [30].
Что такое потенциал действия?
ПД — это относительно сильное по амплитуде скачкообразное изменение мембранного потенциала.
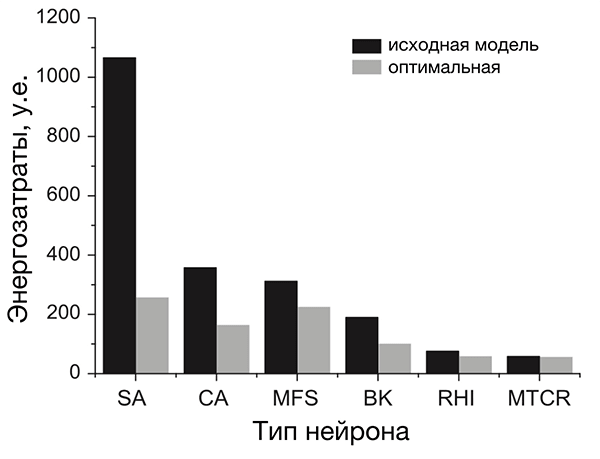
Анализ разных типов нейронов (рис. 4) показал, что нейроны беспозвоночных не очень энергоэффективны, а некоторые нейроны позвоночных почти совершенны [20]. По результатам этого исследования, наиболее энергоэффективными оказались интернейроны гиппокампа, участвующего в формировании памяти и эмоций, а также таламокортикальные релейные нейроны, несущие основной поток сенсорной информации от таламуса к коре больших полушарий.
Рисунок 4. Разные нейроны эффективны по-разному. На рисунке представлено сравнение энергозатрат разных типов нейронов. Энергозатраты рассчитаны в моделях как с исходными (реальными) значениями параметров (черные столбцы), так и с оптимальными, при которых с одной стороны нейрон выполняет положенную ему функцию, с другой — затрачивает при этом минимум энергии (серые столбцы). Самыми эффективными из представленных оказались два типа нейронов позвоночных: интернейроны гиппокампа (rat hippocampal interneuron, RHI) и таламокортикальные нейроны (mouse thalamocortical relay cell, MTCR), так как для них энергозатраты в исходной модели наиболее близки к энергозатратам оптимизированной. Напротив, нейроны беспозвоночных менее эффективны. Условные обозначения: SA (squid axon) — гигантский аксон кальмара; CA (crab axon) — аксон краба; MFS (mouse fast spiking cortical interneuron) — быстрый кортикальный интернейрон мыши; BK (honeybee mushroom body Kenyon cell) — грибовидная клетка Кеньона пчелы.
Почему они более эффективны? Потому что у них малó перекрывание Na- и К-токов. Во время генерации ПД всегда есть промежуток времени, когда эти токи присутствуют одновременно (рис. 3в). При этом переноса заряда практически не происходит, и изменение мембранного потенциала минимально. Но «платить» за эти токи в любом случае приходится, несмотря на их «бесполезность» в этот период. Поэтому его продолжительность определяет, сколько энергетических ресурсов растрачивается впустую. Чем он короче, тем более эффективно использование энергии [20], [26], [30], [43]. Чем длиннее — тем менее эффективно. Как раз в двух вышеупомянутых типах нейронов, благодаря быстрым ионным каналам, этот период очень короткий, а ПД — самые эффективные [20].
Кстати, интернейроны гораздо более активны, чем большинство других нейронов мозга. В то же время они крайне важны для слаженной, синхронной работы нейронов, с которыми образуют небольшие локальные сети [9], [16]. Вероятно, высокая энергетическая эффективность ПД интернейронов является некой адаптацией к их высокой активности и роли в координации работы других нейронов [20].
Синапс
Передача сигнала от одного нейрона к другому происходит в специальном контакте между нейронами, в синапсе [12]. Мы рассмотрим только химические синапсы (есть еще электрические), поскольку они весьма распространены в нервной системе и важны для регуляции клеточного метаболизма, доставки питательных веществ [5].
Чаще всего, химический синапс образован между окончанием аксона одного нейрона и дендритом другого. Его работа напоминает. «переброс» эстафетной палочки, роль которой и играет нейромедиатор — химический посредник передачи сигнала [12], [42], [44–48].
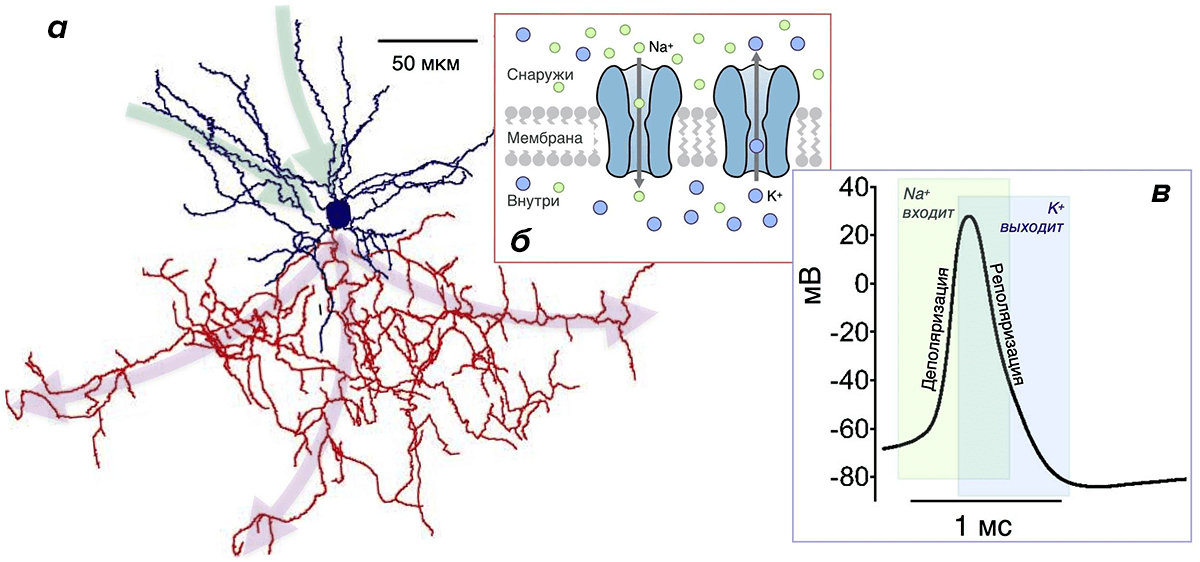
На пресинаптическом окончании аксона ПД вызывает выброс нейромедиатора во внеклеточную среду — к принимающему нейрону. Последний только этого и ждет с нетерпением: в мембране дендритов рецепторы — ионные каналы определенного типа — связывают нейромедиатор, открываются и пропускают через себя разные ионы. Это приводит к генерации маленького постсинаптического потенциала (ПСП) на мембране дендрита. Он напоминает ПД, но значительно меньше по амплитуде и происходит за счет открывания других каналов. Множество этих маленьких ПСП, каждый от своего синапса, «сбегаются» по мембране дендритов к телу нейрона (зеленые стрелки на рис. 3а) и достигают начального сегмента аксона, где вызывают открывание Na-каналов и «провоцируют» его на генерацию ПД.
Такие синапсы называются возбуждающими: они способствуют активации нейрона и генерации ПД. Существуют также и тормозящие синапсы. Они, наоборот, способствуют торможению и препятствуют генерации ПД. Часто на одном нейроне есть и те, и другие синапсы. Определенное соотношение между торможением и возбуждением важно для нормальной работы мозга, формирования мозговых ритмов, сопровождающих высшие когнитивные функции [49].
Как это ни странно, выброс нейромедиатора в синапсе может и не произойти вовсе — это процесс вероятностный [18], [19]. Нейроны так экономят энергию: синаптическая передача и так обусловливает около половины всех энергозатрат нейронов [25]. Если бы синапсы всегда срабатывали, вся энергия пошла бы на обеспечение их работы, и не осталось бы ресурсов для других процессов. Более того, именно низкая вероятность (20–40%) выброса нейромедиатора соответствует наибольшей энергетической эффективности синапсов. Отношение количества полезной информации к затрачиваемой энергии в этом случае максимально [18], [19]. Так, выходит, что «неудачи» играют важную роль в работе синапсов и, соответственно, всего мозга. А за передачу сигнала при иногда «не срабатывающих» синапсах можно не беспокоиться, так как между нейронами обычно много синапсов, и хоть один из них да сработает.
Еще одна особенность синаптической передачи состоит в разделении общего потока информации на отдельные компоненты по частоте модуляции приходящего сигнала (грубо говоря, частоте приходящих ПД) [50]. Это происходит благодаря комбинированию разных рецепторов на постсинаптической мембране [38], [50]. Некоторые рецепторы активируются очень быстро: например, AMPA-рецепторы (AMPA происходит от α-amino-3-hydroxy-5-methyl-4-isoxazolepropionic acid). Если на постсинаптическом нейроне представлены только такие рецепторы, он может четко воспринимать высокочастотный сигнал (такой, как, например, на рис. 2в). Ярчайший пример — нейроны слуховой системы, участвующие в определении местоположения источника звука и точном распознавании коротких звуков типа щелчка, широко представленных в речи [12], [38], [51]. NMDA-рецепторы (NMDA — от N—methyl-D—aspartate) более медлительны. Они позволяют нейронам отбирать сигналы более низкой частоты (рис. 2г), а также воспринимать высокочастотную серию ПД как нечто единое — так называемое интегрирование синаптических сигналов [14]. Есть еще более медленные метаботропные рецепторы, которые при связывании нейромедиатора, передают сигнал на цепочку внутриклеточных «вторичных посредников» для подстройки самых разных клеточных процессов. К примеру, широко распространены рецепторы, ассоциированные с G-белками. В зависимости от типа они, например, регулируют количество каналов в мембране или напрямую модулируют их работу [14].
Различные комбинации быстрых AMPA-, более медленных NMDA- и метаботропных рецепторов позволяют нейронам отбирать и использовать наиболее полезную для них информацию, важную для их функционирования [50]. А «бесполезная» информация отсеивается, она не «воспринимается» нейроном. В таком случае не приходится тратить энергию на обработку ненужной информации. В этом и состоит еще одна сторона оптимизации синаптической передачи между нейронами.
Что еще?
Энергетическая эффективность клеток мозга исследуется также и в отношении их морфологии [35], [52–54]. Исследования показывают, что ветвление дендритов и аксона не хаотично и тоже экономит энергию [52], [54]. Например, аксон ветвится так, чтобы суммарная длина пути, который проходит ПД, была наименьшей. В таком случае энергозатраты на проведение ПД вдоль аксона минимальны.
Снижение энергозатрат нейрона достигается также при определенном соотношении тормозящих и возбуждающих синапсов [55]. Это имеет прямое отношение, например, к ишемии (патологическому состоянию, вызванному нарушением кровотока в сосудах) головного мозга. При этой патологии, вероятнее всего, первыми выходят из строя наиболее метаболически активные нейроны [9], [16]. В коре они представлены ингибиторными интернейронами, образующими тормозящие синапсы на множестве других пирамидальных нейронов [9], [16], [49]. В результате гибели интернейронов, снижается торможение пирамидальных. Как следствие, возрастает общий уровень активности последних (чаще срабатывают активирующие синапсы, чаще генерируются ПД). За этим немедленно следует рост их энергопотребления, что в условиях ишемии может привести к гибели нейронов.
При изучении патологий внимание уделяют и синаптической передаче как наиболее энергозатратному процессу [19]. Например, при болезнях Паркинсона [56], Хантингтона [57], Альцгеймера [58–61] происходит нарушение работы или транспорта к синапсам митохондрий, играющих основную роль в синтезе АТФ [62], [63]. В случае болезни Паркинсона, это может быть связано с нарушением работы и гибелью высоко энергозатратных нейронов черной субстанции, важной для регуляции моторных функций, тонуса мышц. При болезни Хантингтона, мутантный белок хангтингтин нарушает механизмы доставки новых митохондрий к синапсам, что приводит к «энергетическому голоданию» последних, повышенной уязвимости нейронов и избыточной активации. Все это может вызвать дальнейшие нарушения работы нейронов с последующей атрофией полосатого тела и коры головного мозга. При болезни Альцгеймера нарушение работы митохондрий (параллельно со снижением количества синапсов) происходит из-за отложения амилоидных бляшек. Действие последних на митохондрии приводит к окислительному стрессу, а также к апоптозу — клеточной гибели нейронов.
Еще раз обо всем
В конце ХХ века зародился подход к изучению мозга, в котором одновременно рассматривают две важные характеристики: сколько нейрон (или нейронная сеть, или синапс) кодирует и передает полезной информации и сколько энергии при этом тратит [6], [18], [19]. Их соотношение является своего рода критерием энергетической эффективности нейронов, нейронных сетей и синапсов.
Использование этого критерия в вычислительной нейробиологии дало существенный прирост к знаниям относительно роли некоторых явлений, процессов [6], [18–20], [26], [30], [43], [55]. В частности, малая вероятность выброса нейромедиатора в синапсе [18], [19], определенный баланс между торможением и возбуждением нейрона [55], выделение только определенного рода приходящей информации благодаря определенной комбинации рецепторов [50] — все это способствует экономии ценных энергетических ресурсов.
Более того, само по себе определение энергозатрат сигнальных процессов (например, генерация, проведение ПД, синаптическая передача) позволяет выяснить, какой из них пострадает в первую очередь при патологическом нарушении доставки питательных веществ [10], [25], [56]. Так как больше всего энергии требуется для работы синапсов, именно они первыми выйдут из строя при таких патологиях, как ишемия, болезни Альцгеймера и Хантингтона [19], [25]. Схожим образом определение энергозатрат разных типов нейронов помогает выяснить, какой из них погибнет раньше других в случае патологии. Например, при той же ишемии, в первую очередь выйдут из строя интернейроны коры [9], [16]. Эти же нейроны из-за интенсивного метаболизма — наиболее уязвимые клетки и при старении, болезни Альцгеймера и шизофрении [16].
В общем, подход к определению энергетически эффективных механизмов работы мозга является мощным направлением для развития и фундаментальной нейронауки, и ее медицинских аспектов [5], [14], [16], [20], [26], [55], [64].
Благодарности
Искренне благодарен моим родителям Ольге Наталевич и Александру Жукову, сестрам Любе и Алене, моему научному руководителю Алексею Браже и замечательным друзьям по лаборатории Эвелине Никельшпарг и Ольге Слатинской за поддержку и вдохновение, ценные замечания, сделанные при прочтении статьи. Я также очень благодарен редактору статьи Анне Петренко и главреду «Биомолекулы» Антону Чугунову за пометки, предложения и замечания.