Протеолитические ферменты

Протеолитические ферменты играют важнейшую роль в переваривании белков пищи в желудке и кишечнике человека. Большинство протеолитических ферментов органов пищеварения продуцируется в виде проферментов. Физиологический смысл этого заключается в том, чтобы акт продукции фермента (профермента) был отделен от акта его активации — превращения в фермент и, таким образом, белки тканей, продуцирующих ферменты, не подвергались воздействию этих самых ферментов.
Классификация протеолитических ферментов
Экзопептидазами являются протеолитические ферменты карбоксипептидаза А и карбоксипептидаза В, также присутствующие в панкреатическом соке. К экзопептидазам относятся ферменты кишечного сока: аминопептидазы (аланин-аминопептидаза и лейцин-аминопептидаза) и дипептидазы (глицилглицин-дипептидаза, глициллейцин-дипептидаза, пролиназа и пролидаза).
Протеолитические ферменты в лекарствах
Протеолетические ферменты (протеазы) является активным компонентам во многих ферментных препаратах, применяемых для коррекции секреторной дисфункции желудка и нарушений процесса пищеварения в тонкой кишке.
Первый тип лекарств, содержащих протеолетические ферменты,— экстракты слизистой оболочки желудка, основным действующим веществом которых является пепсин. Он, а также другие содержащиеся в слизистой оболочки желудка пептидазы, расщепляют практически все природные белки. Эти лекарства используются преимущественно при гастрите с пониженной кислотностью и не рекомендуются при лечении заболеваний ЖКТ с повышенной кислотностью.
Второй тип содержащих протеолетические ферменты лекарств — комплексные препараты, содержащие основные ферменты поджелудочной железы домашних животных. Такие лекарства способствуют купированию клинических признаков внешнесекреторной недостаточности поджелудочной железы, к которым относят снижение аппетита, тошнота, урчание в животе, метеоризм, стеаторею, креаторею и амилорею. Самым популярным лекарством, содержащим комплекс панкреатических ферментов, включающим протеазы, является панкреатин. Кроме него, имеется множество других препаратов, содержащих протеолетические ферменты, ряд из них приведена в таблице (Саблин О.А., Бутенко Е.В.):
ПРОТЕОЛИТИ́ЧЕСКИЕ ФЕРМЕ́НТЫ
Том 27. Москва, 2015, стр. 625
Скопировать библиографическую ссылку:
ПРОТЕОЛИТИ́ЧЕСКИЕ ФЕРМЕ́НТЫ (протеазы), группа ферментов класса гидролаз, катализируют внутри- и внеклеточное расщепление (протеолиз) пептидных связей C(O) ─ NH в белках и пептидах живых организмов. Выделяют две подгруппы П. ф.: экзопептидазы (пептидазы), отщепляют аминокислоты с аминного ( аминопептидазы ) или карбоксильного ( карбоксипептидазы ) конца молекулы белка или пептида; эндопептидазы (протеиназы; этот термин иногда используется также как синоним термина «П. ф.»), гидролизуют преим. внутр. пептидные связи. Большинство изученных П. ф. синтезируются в виде неактивных предшественников – проферментов, или зимогенов. Их активация происходит путём ограниченного протеолиза – избирательного гидролиза определённых пептидных связей, протекающего либо автокаталитически, либо под действием др. протеиназ, и обычно сопровождается отщеплением пептидов. П. ф. разнообразны по физико-химич. свойствам. В зависимости от локализации П. ф. протеолиз происходит при разл. значениях pH. Напр., пепсин и гастриксины желудка – при pH 1,5–2, ферменты лизосом – при pH 4–5, П. ф. сыворотки крови, тонкого кишечника – при нейтральных или слабощелочных значениях. Некоторые П. ф. в качестве кофактора используют ионы металлов (в т. ч. коллагеназа, термолизин). П. ф. имеют разную субстратную специфичность, которая определяется в осн. особенностями боковых групп аминокислот. Так, напр., трипсин гидролизует связи, образованные карбоксильной группой осно́вных аминокислот – лизина и аргинина, а эластаза – аминокислот с небольшими боковыми цепями – аланина и серина. На расщепление пептидных связей влияет также их доступность при наличии пространственной структуры гидролизуемого субстрата. Ферменты с узкой субстратной специфичностью (напр., коллагеназа, калликреин) гидролизуют пептидные связи, образованные строго определёнными аминокислотными остатками, ферменты с широкой субстратной специфичностью (в т. ч. пепсин, папаин) – связи, образованные многими аминокислотами. В плазме крови и др. биологич. жидкостях, а также в разных клетках и тканях присутствуют белковые ингибиторы П. ф., которые могут блокировать активность отд. ферментов или групп ферментов. Благодаря им осуществляется регуляция активности П. ф. в физиологич. условиях, что предохраняет белки от неконтролируемого расщепления.
Протеолитические ферменты
Содержание
Протеолитические ферменты в спортивной медицине (обзор литературы) [ править | править код ]
Протеолитические ферменты на медицинском и фармацевтическом рынке [ править | править код ]
Наиболее часто встречаемые на рынке варианты комбинированных составов с протеазами приведены в таблице 1.
Таблица 1. Основные активные ингредиенты некоторых типовых комбинированных препаратов протеолитических ферментов на фармацевтическом рынке США и Европы [5]
Примечания: *1 μkat – количество фермента, которое превращает более 1 μM субстрата в секунду при стандартных условиях. Это соответствует 60 F.I.P – единиц. Ph. Eur.-ед протеиназы – протеиназные единицы действия по Европейской Фармакопее. Рутозид (рутин, кверцетин-3-О-рутинозид, софорин) — гликозид флавоноида кверцетина.
Как видно из таблицы 1, в большинстве случаев при формировании состава комбинированных протеолитических препаратов используются растительные протеазы цистеина – бромелайн (обязательный компонент) и папаин, а также протеазы серина животного происхождения – трипсин и химотрипсин. Некоторые составы включают панкреатин, амилазу, липазу и/или рутозид. Популярной формой выпуска являются кишечнорастворимые таблетки, покрытые оболочкой, для обеспечения наибольшей концентрации активных веществ в кишечнике (предотвращение распада таблетки в кислой среде желудка). Дозировки ферментов варьируют в диапазоне от 1 до 200 мг/таблетку. Количество протеаз в дозе на прием соответствует ферментной активности, описанной в F.I.P. (F.I.P.-units of the Federation Internationale Pharmaceutique). Одна F.I.P.-единица – количество фермента, которое способно конвертировать более 1 мкмол субстрата за 1 минуту при стандартных условиях.
Происхождение, химическая структура, классификация и свойства протеолитических ферментов [ править | править код ]
Растительные протеазы. [ править | править код ]
Протеазы дынного дерева [ править | править код ]
В соответствии с данными А.М.Пенджиева и А.Абдуллаева [2] «высушенный млечный сок (латекс) дынного дерева содержит ряд протеаз: Папаин – монотиоловая цистеиновая эндопротеаза. По характеру ферментативного действия ее называют «растительным пепсином». Но, в отличие от пепсина, папаин активен не только в кислых, но и в нейтральных и щелочных средах (диапазон рН 3–12, оптимум рН=5), что важно при часто встречающихся у спортсменов нарушениях кислотного состава желудка. Химопапаин – монотиоловая цистеиновая протеиназа. Благодаря субстратной специфичности похожа на папаин, но отличается от него электрофоретической подвижностью, стойкостью и растворимостью. Протеиназа IV – цистеиновая протеиназа, основная протеиназа латекса, составляет около 30 % присутствующего в нем белка. Проявляет высокую степень гомологии с протеиназой III папайи (81 %), химопапаином (70 %) и папаином (67 %). Очень близка к химопапаину по молекулярной массе и заряду молекулы. Карикаин – наиболее щелочная среди цистеиновых протеиназ латекса папайи. Подобно папаину, карикаин сначала продуцируется в форме неактивного зимогена прокарикаина, содержащего ингибиторный прорегион из 106 N-терминальных аминокислот. Активация фермента заключается в отщеплении прорегиона молекулы без ее последующих конформационных изменений. Протеиназа w (эндопептидаза А, пептидаза А) – монотиоловая цистеиновая протеиназа. Это полипептид, содержащий 216 аминокислотных остатков и 3 дисульфидные связи. Для проявления его ферментативной активности важно наличие свободного остатка цистеина в активном центре. Проявляет высокую степень гомологии с папаином (68,5 %). По специфичности ферментативного действия напоминает папаин, поскольку связывается с субстратом в участках локализации дисульфидных связей. Для стабилизации комплекса протеиназ папайи с практическими целями используются специальные полимеры, разработанные еще во времена существования СССР.
Протеазы ананаса [ править | править код ]
Протеазы животного происхождения [ править | править код ]
Фармакокинетика протеолитических ферментов [ править | править код ]
Абсорбция ПФ в желудочно-кишечном тракте и их биологическая активность [ править | править код ]
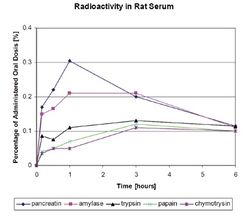
В обзорной работе G.Lorkowski [5] суммированы имеющиеся данные по абсорбции протеолитических ферментов в ЖКТ после их перорального приема, фармакокинетике ПФ и даны возможные объяснения механизмам этих процессов. Ранние исследования абсорбции протеаз у животных были выполнены путем перорального приема ферментных субстратов, меченых радиоактивными изотопами. Другим методом было количественное определение в плазме крови собственной эстеразной активности протеаз в отношении специфических субстратов, например, этилового эфира N-бензолил-L-аргинина (BAEE) как субстрата для трипсина, а этилового эфира N-ацетил-L-тирозина (ATEE) как субстрата для химотрипсина, а уровня гемоглобина – для оценки общей протеолитической активности. Экспериментальные исследования показали, что абсорбция протеолитических ферментов зависит от множества факторов, среди которых наиболее важным является размер молекулы. В серии экспериментальных работ J.Seifert и соавторов [15] [16] было показано, что после перорального приема (рис.1) меченых йодом-123 таких протеолитических ферментов как трипсин, химотрипсин, панкреатин и папаин, наблюдается постепенное нарастание концентрации протеолитических ферментов в крови, дифференцированное по времени и количественным параметрам в зависимости от конкретного протеолитического фермента. Прием панкреатина вызывал наибольший прирост концентрации фермента в сыворотке крови с максимумом в течение часа. В течение последующих 6-и часов происходило плавное снижение его концентрации. Для других протеолитических ферментов (трипсин, химотрипсин и папаин) максимальная концентрация в сыворотке крови достигалась только к 3-ему часу после перорального применения и была существенно ниже (в 3 и более раз) по сравнению с панкреатином. Характерно, что через 6 часов для всех ферментов уровень их концентрации в крови (в процентном соотношении с их введенной дозой на 1 г крови) был примерно одинаковым.
Детальные количественные характеристики изменений показателей ПФ в крови даны в таблице 2.
Таблица 2. Количественный анализ абсорбции ферментов в кишечнике крыс в сыворотку крови и лимфу (из J.Seifert и соавт., 1990).
Общий уровень абсорбции, (%) *
Общий уровень абсорбции (мг)
Низкомолекулярная часть (мг)
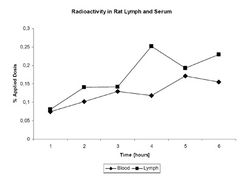
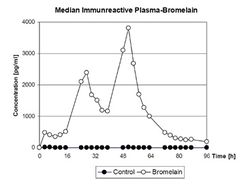
Абсорбция бромелаина при интрадуоденальном введении в экспериментах на крысах существенно отличалась от таковой других протеолитических ферментов. Как видно из рис.2, происходит медленное (по сравнению с другими ПФ) нарастание концентрации бромелаина в сыворотке крови и лимфе в течение 4 часов (максимум) и поддержание этих величин до 6-и часов наблюдения. В данной работе уровень абсорбции бромелаина определен в 50% от введенной дозы за 6 часов, при этом 80% составила высокомолекулярная фракция.
Фармакокинетика ПФ у человека [ править | править код ]
Таблица 4. Линейная зависимость максимальных уровней ПФ в плазме крови испытуемых в соответствии с перорально принимаемой суточной дозой ферментных препаратов [20] [21] [22]
Примечания: ДД – дневная доза (г); МКП – максимальная концентрация в плазме (нг/мл).
15 добровольцев получали кишечно-растворимые таблетки, каждая из которых содержала 200 мг бромелайна. Четверо испытуемых служили контролем (плацебо). В течение 1-го дня осуществлялось шесть приемов бромелаина: 3 таблетки в 8.00 утра (время «ноль» для исследования); в 11.00; 14.00; 17.00 и 20.00, а затем 5 таблеток в 23.00. Такой же режим соблюдался на 2-ой день. На 3-ий день осуществлялся только дин прием 3-х таблеток в 8.00. Стандартные приемы пищи производились в: 9.00; 12.00; 15.30 и 18.30. Образцы крови (12 мл) брались каждый раз перед приемом бромелаина. У большинства участников Смакс отмечалась через 48 часов и составляла в среднем 5 нг/мл, Т1/2 в плазме около 6 часов. AUC за период 3-51 часов составила 82,2 нг/час/мл.
В другой работе коллективом авторов из Института клинической фармакологии в Берлине (Германия) [20] [21] [22] (табл.4) выявлена четкая дозозависимость концентрации бромелаина, трипсина и папаина в плазме крови от введенной суточной дозы фермента, что еще раз подчеркивает, что протеолитические ферменты являются фармаконутриентами, т.е. сочетают способность влиять на нутритивные процессы подобно фармакологическим агентам.
Подводя итоги выполненным исследованиям фармакокинетики протеолитических ферментов, G.Lorkowski [5] в своем аналитическом обзоре делает следующее заключение: «Прием протеолитических ферментов обеспечивает усвоение организмом физиологически активных протеинов с высоким молекулярным весом. Фармакокинетические исследования показывают дозозависимое линейное нарастание концентрации протеаз в различных средах организма, варьирующее в достаточно широких индивидуальных пределах, медленную динамику абсорбции в кишечнике, быстрое и 100% связывание в организме с антипротеазными комплексами. Пероральный прием протеолитических ферментов увеличивает протеазную активность сыворотки крови с параллельным возрастанием концентрации в плазме крови соответствующих антипротеаз. Биологическая протеолитическая активность пероральных ПФ определяется взаимодействием с соответствующими рецепторами на поверхности клеток (протеаз-активируемые рецепторы) как в виде свободных протеаз, так и в комплексной форме с антипротеазами. Такой комплекс «протеаза-антипротеаза» вызывает возрастание плазменных концентраций антипротеаз и элиминацию самих комплексов и цитокинов. Эти механизмы реализуются при приеме внутрь протеолитических ферментов в виде кишечнорастворимых таблеток с содержанием растительных и животных протеаз, и обеспечивают стабилизацию и, возможно, улучшение физиологических и иммунологических процессов даже у здоровых лиц. Последнее обстоятельство приобретает особый смысл в спортивной медицине.
Протеолитические ферменты – катализаторы высвобождения аминокислот (АК) из протеинов [ править | править код ]
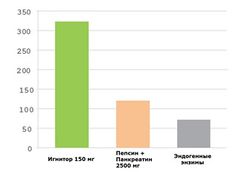
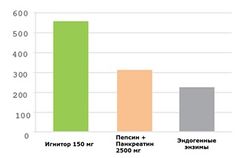
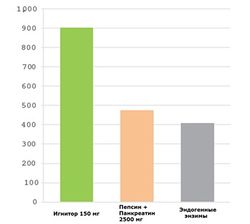
Сходным образом (рис.5), 150 мг Игнитора в 2 раза усиливает высвобождение лейцина из WPC по сравнению со смесью пепсина и панкреатина, и в 2,5 раза – по сравнению только с эндогенными ферментами. Почти такое же преимущество (рис.6) имел Игнитор и в плане высвобождения ВСАА в целом: в 2 раза активнее смеси пепсина и панкреатина, и в 2,25 раза – эндогенных ПФ.
Замена WPC на изолят (WPI) привела примерно к таким же результатам: 100 мг Игнитора высвобождало в 4 раза больше лейцина, в 3,25 раза больше ВСАА и в 2,25 раза больше глутамина по сравнению с эндогенными ПФ.
Таким образом, смесь протеаз различного происхождения при совместном приеме с whey-протеинами (WPC, WPI) увеличивает и оптимизирует во времени высвобождение из белков ВСАА и глутамина с последующей активацией mTOR, что определяет анаболическую эргогенную активность протеолитических ферментов (ПФ). Эргогенное действие ПФ носит опосредованный характер и проявляется при выборе оптимального соотношения общего количества и качества поступающего белка, собственной активности эндогенных ПФ и количества и протеолитических свойств экзогенных ПФ в составе препаратов и БАДов. Конечным эффектом оптимального приема пищевых добавок протеинов и ПФ в сочетании с силовыми тренировками является увеличение синтеза белка в скелетных мышцах, увеличение размеров мышечных волокон, повышение силы и мощности мышц.
Для повышения эффективности высвобождения ВСАА и глутамина из белка делают комбинированные формы WP и ПФ, в котором уже рассчитаны дозы ферментов, необходимые для оптимального расщепления протеинов (например, Isoject – сочетание изолята WP и Игнитора).
Протеолитические ферменты как фармаконутриенты для предупреждения и лечения EIMD и DOMS [ править | править код ]
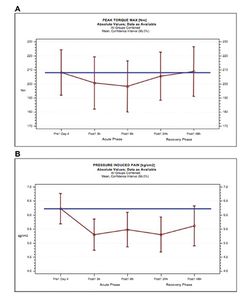
В более ранней работе P.C.Miller и соавторов [29] изучено влияние добавок ПФ на DOMS и функцию мышц у бегунов-мужчин (возраст 18-29 лет) в параллельных группах сравнения в холмистой местности (бег под уклон). Комбинированный БАД с протеолитическими и другими ферментами применялся в виде капсул. Каждая капсула содержала 325 мг ферментов поджелудочной железы, 75 мг трипсина, 50 мг папаина, 50 мг бромелаина, 10 мг амилазы, 10 мг липазы, 10 мг лизозима и 2 мг химотрипсина и принималась испытуемыми в течение 4-х дней по 2 капсулы 4 раза в день на пустой желудок за 30 минут до приема пищи в 200 мл воды. В контрольной группе участники получали плацебо в капсулах идентичного вида. Весьма важно, что данный вид бега вызывает достаточно ощутимые микроповреждения мышечных волокон и DOMS. Авторы работы показали, что пероральный прием протеаз редуцирует отсроченные мышечные боли, вызванные физическими нагрузками, что сопровождается ускорением восстановления и улучшением общего настроения и самочувствия у физически активных мужчин. При этом выявлена определенная закономерность: восстановление контрактильной способности мышц происходит быстрее при низкой и средней скоростях бега, чем при высокой скорости. Исследования P.C.Miller и соавторов [29] имеют вполне конкретную прикладную направленность. Лица, впервые начинающие тренировочный процесс без опыта физической подготовки, или пациенты, проходящие курс реабилитации после хирургического вмешательства, особенно при отсутствии консультаций специалиста по ОФП, имеют высокую вероятность развития DOMS. Последняя, в свою очередь, прерывает процесс восстановления или существенно его замедляет. Пищевые добавки ПФ – один из оптимальных способов лечения таких состояний, который снижает боли, ускоряет восстановление мышц. В результате возрастает объем и эффективность тренировочной работы, ускоряется восстановление после травм и операций.
Побочные эффекты перорального приема протеолитических ферментов [ править | править код ]
Грибковые протеазы – новое направление в создании ферментных фармаконутриентов для спортивной медицины [ править | править код ]
Развитие данного направления связано с выделением и изучением группы протеаз грибкового происхождения (Aspergillus niger и Aspergillus oryzae) в виде патентованной формулы Aminogen®. J.Oben и соавторы [33] провели исследование в двух группах здоровых мужчин (n=21, возраст 19-35 лет, ИМТ 20-24, физическая активность в рамках программы бодибилдинга). В течение первых 9 дней участники принимали (на фоне стандартизированной сбалансированной диеты в 2200 ккал/день, 40% углеводов, 25% белка и 35% жиров) 50 г концентрата WP (WPC), затем 50 г WPC с добавлением либо 2,5 г, либо 5 г Аминогена (Aminogen®, Triarco Industries,Wayne, NJ). WPC представлял собой порошок с содержанием 85% протеина, 6% жира, 3% неорганических веществ и 6% лактозы. На каждом этапе исследования (каждые 30-60 минут) брались образцы крови для оценки уровней аминокислот и С-реактивного белка в крови. Результаты показали, что в группах, получавших дополнительно грибковые протеазы, уровень всех аминокислот был через 4 часа после приема пищевых добавок достоверно выше, чем в контроле (увеличение площади под кривой AUC – «время-концентрация»). На фоне ферментов достоверно снижался С-реактивный белок по сравнению с контрольной группой, улучшался азотистый баланс. Авторы сделали заключение, что Аминоген усиливает переваривание белка в ЖКТ и скорость всасывания аминокислот (в 2,2-3,5 раза). Не прослеживалось достоверной связи между дозой ферментов и конечным результатом, что позволяет рассматривать дозу Аминогена 2,5 г как адекватную и достаточную. С практической точки зрения это означает, что грибковые протеазы, с одной стороны, повышают эффективность переваривания белка и всасывание аминокислот в среднем в 2,5 раза (растет уровень аминокислот в плазме крови), а с другой, организм получает возможность потребления дополнительного количества белка, который в обычных условиях не может быть переработан и усвоен собственными эндогенными протеазами (адекватный, т.е. усвояемый, однократный объем белка в обычных условиях – 15 г, на фоне ферментов – 30 г и более). В свою очередь, это приводит к снижению риска белковой перегрузки и вероятности диспептических явлений и желудочно-кишечного дискомфорта. Снижение уровней С-реактивного белка может вносить вклад в торможение процессов воспаления при физических нагрузках, уменьшение негативных последствий чрезмерного мышечного напряжения и ускорение восстановления в постнагрузочный период.
Исследования последних десяти лет позволили сформулировать концепцию полимодальности механизма действия протеолитических ферментов (ПФ) животного, растительного и комбинированного происхождения в спортивной медицине. Условно этот механизм складывается из двух взаимодополняющих частей: усиление и ускорение переваривания белка в ЖКТ и системное антипротеолитическое действие (снижение воспаления, уменьшение EIMD и DOMS. Основные положения этих направлений могут быть сформулированы следующим образом:
Применение ферментов позволяет использовать более приятные по органолептическим свойствам белковые смеси, содержащие нативные высококачественные протеины (например, WP, а не гидролизаты WPH). Такой подход (ферментирование белков «in vivo») является альтернативой промышленной ферментативной обработке белков до поступления в организм. При этом образование и абсорбция ВСАА (в частности, лейцина) в количественном плане идентичен эффективности уже ферментированных белков или добавок ВСАА в составе смесей.
В спорте высших достижений, где в подавляющем большинстве случаев имеет место относительная ферментная недостаточность, обусловленная большим объемом поступления белка (в составе диеты, функциональной пищи или добавок протеинов различного происхождения), задачей ферментных препаратов является адекватное переваривание дополнительных протеинов. Соответственно, расчет потребности в экзогенно вводимых ферментах осуществляется, исходя из имеющегося превышения возрастной нормы потребления белка, антропометрических показателей спортсмена и реальной физической нагрузки в процессе тренировок и соревнований, функционального состояния кислотообразующей и ферментообразующей функции ЖКТ.
Саблин О.А., Бутенко Е.В. Ферментные препараты в гастроэнтерологии // Consilium-Medicum. – 2004. – Том 6. – № 1. Гастроэнтерология.
Ферментные препараты в гастроэнтерологии.
Ферментные препараты – это группа фармакологических средств, способствующих улучшению процесса пищеварения. Нарушения процесса пищеварения различной степени выраженности встречаются практически при всех заболеваниях желудочно-кишечного тракта.
Причины нарушения пищеварения чрезвычайно многообразны и могут быть следующими:
– хроническом панкреатите, камнях поджелудочной железы;
– раке поджелудочной железы;
– свищах поджелудочной железы;
– язвенной болезни двенадцатиперстной кишки;
– синдроме раздраженного кишечника;
– состояниях после ваготомии и дренирующих операциях.
– дисбиозе тонкой кишки;
– состоянии после холецистэктомии.
– первичном билиарном циррозе;
– патологии терминального отдела тонкой кишки;
– дисбиозе тонкой кишки;
– дефиците дисахаридаз (врожденная, приобретенная лактазная или другая дисахаридазная недостаточность);
– нарушении внутриклеточного транспорта компонентов пищи в результате гибели энтероцитов (Болезнь Крона, глютеновая энтеропатия, саркоидоз, радиационный, ишемический и другие энтериты).
Практически все перечисленные состояния в той или иной степени являются показаниями к назначению ферментной терапии. При этом, несмотря на многообразие причин, вызывающих нарушение пищеварения, наиболее выраженные расстройства вызывают заболевания поджелудочной железы, которые сопровождаются первичной панкреатической недостаточностью. Она возникает при заболеваниях поджелудочной железы, сочетающихся с недостаточностью ее внешнесекреторной функции (хронический панкреатит, фиброз поджелудочной железы и т.д.).
В клинической практике чаще встречается вторичная или относительная недостаточность поджелудочной железы, как правило, вызываемая приемом необычной пищи, ее избыточным количеством или временными расстройствами функционирования поджелудочной железы. Панкреатическая недостаточность ограничивает усвоение пищи и может привести к нарушению процессов всасывания.
В некоторых случаях заместительная ферментная терапия показана здоровым лицам, при переедании, погрешностях в диете, для улучшения переваривания пищи.
Важным показанием к назначению ферментной терапии является подготовка больных к рентгенологическому и ультразвуковому исследованию органов брюшной полости, для уменьшения газообразования в кишечнике.
Заместительная ферментная терапия является основным направлением в терапии больных с синдромом нарушенного пищеварения, особенно при невозможности устранения причин его развития. В настоящее время в клинической практике имеется большое число ферментных препаратов, отличающихся комбинацией компонентов, энзимной активностью, способу производства и формам выпуска.
– устойчивость ферментов к действию хлористоводородной кислоты;
– быстрое высвобождение ферментов в двенадцатиперстной кишке;
– высвобождение ферментов в интервале 5–7 ед. рН;
Препараты, включающие панкреатические энзимы, используются для коррекции нарушений процесса пищеварения, а также для регуляции функций поджелудочной железы. Традиционно для этого используются комплексные препараты, содержащие основные ферменты поджелудочной железы домашних животных (прежде всего липазу, трипсин, химотрипсин и a-амилазу). Эти ферменты обеспечивают достаточный спектр пищеварительной активности (табл.1) и способствуют купированию клинических признаков внешнесекреторной недостаточности поджелудочной железы, к которым относят снижение аппетита, тошноту, урчание в животе, метеоризм, стеато-, креато- и амилорею.
Препараты отличаются по активности компонентов, что следует учитывать при их подборе у конкретного больного (табл. 2).
Входящая в комплекс амилаза разлагает крахмал и пектины до простых сахаров – сахарозы и мальтозы. Амилаза расщепляет преимущественно внеклеточные полисахариды (крахмал, гликоген) и практически не участвует в гидролизе растительной клетчатки.
Протеазы в ферментных препаратах представлены преимущественно химотрипсином и трипсином. Последний наряду с протеолитической активностью способен инактивировать холецистокинин-рилизинг-фактор, в результате чего снижаются содержание холецистокинина в крови и панкреатическая секреция по принципу обратной связи.
Кроме того, трипсин является важным фактором, регулирующим моторику кишки. Это осуществляется в результате взаимодействия с РАП-2-рецепторами энтероцитов.
Липаза участвует в гидролизе нейтрального жира в тонкой кишке.
Комбинированные препараты наряду с панкреатином содержат желчные кислоты, гемицеллюлазу, симетикон, растительные желчегонные (куркума) и др.
Введение в препарат желчных кислот существенно изменяет его действие на функцию пищеварительных желез и моторику желудочно-кишечного тракта. Препараты, содержащие желчные кислоты, увеличивают панкреатическую секрецию и холерез, стимулируют моторику кишечника и желчного пузыря. Желчные кислоты увеличивают осмотическое давление кишечного содержимого. В условиях микробной контаминации кишечника происходит их деконъюгация, что в некоторых случаях способствует активации цАМФ энтероцитов с последующим развитием осмотической и секреторной диареи.
Комбинированные препараты, содержащие компоненты желчи и гемицеллюлазу, создают оптимальные условия для быстрого и полного расщепления белков, жиров и углеводов в двенадцатиперстной и тощей кишках. Препараты назначают при недостаточной внешнесекреторной функции поджелудочной железы в сочетании с патологией печени, желчевыводящей системы, при нарушении жевательной функции, малоподвижном образе жизни, кратковременных погрешностях в еде.
Наличие в составе комбинированных препаратов наряду с ферментами поджелудочной железы компонентов желчи, пепсина и гидрохлоридов аминокислот (панзинорм форте) обеспечивает нормализацию процессов пищеварения у больных с гипоацидным или анацидным гастритом. У этих больных, как правило, страдают функции поджелудочной железы, желчеобразования и желчевыделения.
Гемицеллюлаза, входящая в состав некоторых препаратов (фестал), способствует расщеплению растительной клетчатки в просвете тонкой кишки, нормализации микрофлоры кишечника.
Многие ферментные препараты содержат симетикон или диметикон, которые уменьшают поверхностное натяжение пузырьков газа, вследствие чего они распадаются и поглощаются стенками желудка или кишечника.
Ферментные препараты растительного происхождения содержат папаин или грибковую амилазу, протеазу, липазу (пепфиз, ораза). Папаин и протеазы гидролизируют белки, грибковая амилаза – углеводы, липаза, соответственно, – жиры.
Кроме трех вышеуказанных групп существуют небольшие группы комбинированных ферментных препаратов растительного происхождения в сочетании с панкреатином, витаминами (вобэнзим) и дисахаридазами (тилактаза).
Форма выпуска препарата является важным фактором, определяющим эффективность лечения. Большинство ферментных препаратов выпускаются в виде драже или таблеток в кишечнорастворимых оболочках, что защищает ферменты от высвобождения в желудке и разрушения хлористоводородной кислотой желудочного сока. Размер большинства таблеток или драже составляет 5 мм и более. Тем не менее, известно, что из желудка одновременно с пищей могут эвакуироваться твердые частицы, диаметр которых составляет не более 2 мм. Более крупные частицы, в частности ферментные препараты в таблетках или драже, эвакуируются в межпищеварительный период, когда пищевой химус отсутствует в двенадцатиперстной кишке. В результате препараты не смешиваются с пищей и недостаточно активно участвуют в процессах пищеварения.
Для обеспечения быстрого и гомогенного смешивания ферментов с пищевым химусом были созданы ферментные препараты нового поколения в виде микротаблеток (панцитрат) и микросфер (креон, ликреаза), диаметр которых не превышает 2 мм. Препараты покрыты кишечнорастворимыми (энтеросолюбельными) оболочками и заключены в желатиновые капсулы. При попадании в желудок желатиновые капсулы быстро растворяются, микротаблетки смешиваются с пищей и постепенно поступают в двенадцатиперстную кишку. При рН дуоденального содержимого выше 5,5 оболочки растворяются, и ферменты начинают действовать на большой поверхности. При этом практически воспроизводятся физиологические процессы пищеварения, когда панкреатический сок выделяется порциями в ответ на периодическое поступление пищи из желудка.
Ацидин-пепсин – препарат, содержащий протеолитический фермент. Получают из слизистой оболочки желудка свиней. Таблетки по 0,5 и 0,25 г содержат 1 часть пепсина, 4 части ацидина (бетаина гидрохлорида). Назначаются при гипо- и анацидных гастритах по 0,5 г 3–4 раза в сутки во время еды. Таблетки предварительно растворяют в 1/2 стакана воды.
Вобэнзим – комбинированный препарат, содержащий высокоактивные ферменты растительного и животного происхождения. Кроме панкреатина содержит папаин (из растения Carica Papaya), бромелаин (из ананаса обыкновенного) и рутозид (группа витамина Р). Занимает особое место в ряду ферментных препаратов, так как наряду с выраженными ферментативными свойствами обладает противовоспалительным, противоотечным, фибринолитическим и вторично-анальгезирующим действием. Спектр применения очень широк. Используется при панкреатите, язвенном колите, болезни Крона, травмах, аутоиммунных онкологических, урологических, гинекологических заболеваниях. Дозу устанавливают индивидуально – от 5 до 10 драже 3 раза в сутки.
Дигестал – содержит панкреатин, экстракт желчи крупного рогатого скота и гемицеллюлазу. Препарат назначают по 1–2 драже 3 раза в день во время или после еды.
Креон – препарат, в желатиновой капсуле которого содержится большое количество панкреатина в устойчивых к соляной кислоте гранулах. Препарат характеризуется быстрым (в течение 4–5 мин) растворением желатиновых капсул в желудке, высвобождением и равномерным распределением устойчивых к желудочному соку гранул по всему химусу. Гранулы беспрепятственно проходят через пилорический сфинктер одновременно с химусом в двенадцатиперстную кишку, полностью защищают ферменты панкреатина при пассаже через кислую среду желудка и характеризуются быстрым высвобождением ферментов при поступлении препарата в двенадцатиперстную кишку.
Ликреаза – ферментный препарат на основе вытяжки, полученной путем измельчения, обезжиривания и высушивания свежей или замороженной поджелудочной железы свиньи. Капсулы содержат микросферы диаметром 1–1,2 мм, содержащие панкреатин, стабильны и не разрушаются в среде желудка с рН ниже 5,5. При диспепсических расстройствах назначают по 1–3 капсулы в сутки, при хроническом панкреатите – 3–6 капсул в сутки.
Мезим-форте – чаще назначают для коррекции кратковременных и незначительных дисфункций поджелудочной железы. Драже мезим-форте покрыты специальной глазурной оболочкой, защищающей компоненты препарата от агрессивного воздействия кислой среды желудка. Применяют по 1–3 драже 3 раза в день перед едой.
Меркэнзим – комбинированный препарат, который содержит 400 мг панкреатина, 75 Ед бромелаина и 30 мг бычьей желчи. Бромелаины представляют собой концентрированную смесь протеолитических ферментов, экстрагированных из свежих плодов ананаса и его ветвей. Препарат двухслойный. Наружный слой составляют бромелаины, которые высвобождаются в желудке и проявляют протеолитическое действие. Внутренний слой устойчив к соляной кислоте желудка, поступает в тонкую кишку, где высвобождаются панкреатин и желчь. Бромелаины остаются эффективными в широком диапазоне рН (3,0–8,0), поэтому препарат можно назначать независимо от количества соляной кислоты в желудке. Меркэнзим назначается по 1–2 таблетки 3 раза в день после еды.
Нигедаза – препарат в таблетках по 0,02 г, содержащий фермент липолитического действия. Получен из семян чернушки дамасской. Нигедаза вызывает гидролитическое расщепление жиров растительного и животного происхождения. Препарат активен в условиях повышенной и нормальной кислотности желудочного сока и наполовину активен в условиях пониженной кислотности желудочного сока. Препарат назначают внутрь по 1–2 таблетки 3 раза в день за 10–30 мин до еды. В связи с отсутствием в препарате протеолитических и амилолитических ферментов прием нигедазы целесообразно сочетать с приемом панкреатина.
Ораза – кислотоустойчивый комплекс протеолитических и амилолитических ферментов (из культуры гриба Aspergillus oryzae), состоящий из амилазы, мальтазы, протеазы, липазы. Препарат не разрушается в желудке, растворяется в кишечнике (при щелочном рН). Назначают по 1/2–1 чайной ложке гранул 3 раза в день во время или сразу после еды. Одна чайная ложка содержит 2 г гранул, что соответствует 0,2 г оразы.
Панзинорм форте – препарат, состоит из экстракта слизистой оболочки желудка, экстракта желчи, панкреатина, аминокислот. Экстракт слизистой оболочки желудка содержит пепсин и катепсин с высокой протеолитической активностью, а также пептиды, которые содействуют высвобождению гастрина, последующей стимуляции желез желудка и выделению хлористоводородной кислоты. Панзинорм является двухслойным препаратом. Наружный слой содержит пепсин, катепсин, аминокислоты. Этот слой растворяется в желудке. Внутренний слой является кислотоустойчивым, растворяется в кишечнике, содержит панкреатин и экстракт желчи. Панзинорм – один из немногих препаратов, который наряду с заместительным обладает стимулирующим пищеварение действием, что дает возможность применения препарата у больных с атрофическими формами гастритов, особенно в пожилом возрасте. Препарат принимают по 1–2 драже во время еды 3–4 раза в день.
Важно, что панзинорм изготовлен на говяжьем субстрате. Это дает возможность приема препарата пациентам с аллергией на свиной белок и лицам, не употребляющим в пищу свинину по религиозным мотивам.
Панзинорм форте-Н – отличительной особенностью препарата является оптимальное сочетание и высокое содержание ферментов поджелудочной железы, заключенных в таблетку, покрытую кислотоустойчивой оболочкой. Кроме того, препарат не содержит желчные кислоты, гидрохлориды аминокислот, говяжий белок, поэтому его могут принимать больные с обострением хронического панкреатита, тяжелой патологией гепатобилиарной системы, гиперацидными состояниями, больные диабетом, пациенты с аллергией на говяжий белок. Применяют по 1 таблетке во время еды.
Панкреатин – препарат поджелудочной железы крупного рогатого скота, содержащий ферменты. Суточная доза панкреатина составляет 5–10 г. Панкреатин принимают по 1 г 3–6 раз в день перед едой.
Панкурмен – комбинированный препарат, в 1 драже которого содержится панкреатин и экстракт куркумы (желчегонное средство). Принимают по 1–2 драже до еды 3 раза в день.
Панцитрат – препарат нового поколения с высоким содержанием панкреатина. Имеет фармакодинамику, сходную с креоном. Желатиновые капсулы содержат микротаблетки в специальной энтеросолюбильной оболочке, резистентной к желудочному соку, что гарантирует освобождение всех ферментов в кишечнике. Назначают по 1 капсуле 3 раза в день.
Пепфиз – содержит растительные ферменты (папаин, диастазу) и симетикон. В отличие от других ферментных препаратов пепфиз выпускается в виде шипучих растворимых таблеток с апельсиновым вкусом, которые при растворении в воде высвобождают цитрат натрия и калия. Они нейтрализуют соляную кислоту в желудке и уменьшают изжогу. Препарат применяется при синдроме похмелья, переедании, обильном употреблении пива, кофе, кваса, газосодержащих напитков, пищи, богатой углеводами, резкой перемене характера питания. Применяют по 1 таблетке 2–3 раза в день после еды.
Солизим – липолитический фермент, полученный из Perucillium solitum, гидролизует растительные и животные жиры, что приводит к купированию стеатореи, нормализации содержания общих липидов и липазной активности сыворотки крови.
Препарат принимают по 2 таблетки (40000 ЛЕ) 3 раза в день во время или сразу после еды.
Тилактаза – пищеварительный фермент представляющий собой лактазу, которая находится в щеточной кайме слизистой оболочки тощей кишки и проксимального отдела подвздошной кишки. Расщепляет лактозу на простые сахара. Назначают внутрь по 250–500 мг перед употреблением молока или молочных продуктов. Препарат можно добавлять в пищу, содержащую лактозу.
Фестал, энзистал, панзистал – комбинированные ферментные препараты, содержащие основные компоненты поджелудочной железы, желчи и гемицеллюлазу. Применяют по 1–3 драже во время еды 3 раза в день.
Одним из важных факторов, определяющих успех лечения, является правильный выбор ферментного препарата, его дозы и продолжительности лечения. При выборе препарата учитывают характер заболевания и механизмы, лежащие в основе нарушения пищеварения.
Выбор дозы ферментного препарата обусловлен тяжестью основного заболевания и степенью функциональных расстройств поврежденного органа. Так, применение среднеактивных панкреатических энзимов целесообразно при «пограничных» состояниях, когда имеются незначительные нарушения функций поджелудочной железы, сопровождающие различные заболевания верхних отделов пищеварительного тракта или встречающиеся при погрешностях в еде, переедании, алкогольных эксцессах.
При этом больные предъявляют субъективные жалобы на некоторое недомогание, изредка возникающую тошноту, тяжесть в животе после еды. Сходные симптомы возникают при переедании, приеме необычной, «незнакомой» пищи. Особенно часто это встречается у людей, находящихся на отдыхе вдалеке от обычных мест проживания. Новая диета, новый минеральный состав воды и продуктов вызывают нарушения процессов пищеварения. Через 20–30 мин после еды иногда может возникнуть кратковременная ноющая или давящая боль в околопупочной области. Кроме того, может отмечаться кратковременное расстройство стула в виде его размягчения (так называемая диарея путешественников), появляется флатуленция. Однако при объективном клиническом и лабораторном обследовании сколько-нибудь выраженных изменений, как правило, не определяется.
Назначение больших доз или высокоактивных ферментов целесообразно при заместительной терапии у больных хроническим панкреатитом. В этом случае дозы ферментов зависят от степени внешнесекреторной недостаточности, а также индивидуальных пищевых привычек и желания больного соблюдать диету. При легкой стеаторее, не сопровождающейся поносами и снижением массы тела, коррекция пищеварения достигается диетой с низким содержанием жира или приемом панцитрата 10000.
Таблица 1. Механизмы действия ферментов поджелудочной железы
Таблица 2. Характеристика основных ферментных препаратов
| Препарат | Форма выпуска | Состав | |||||||||||||
| ами- лаза (Ед FIР) | лип- аза (Ед FIP) | протеазы | желчь (г) | геми- целлю- лаза (г) | гидро- хло- риды амино- кис-лот (г) | холе-вая кис-лота (мг) | симе- тикон, димет- икон (мг) | экс- тракт куку- рмы | лак- таза | бетаи-на гидро- хло-рид | про- чие | ||||
| пепсин (Ед FIP) | трипсин (Ед FIP) | химо- трипсин (Ед FIP) | |||||||||||||
| Ацидин- пепсин | Таблетки | – | – | 0,1 г | – | – | – | – | – | – | – | – | 0,4 г | – | |
| Вобэнзим | Драже | Панкреатин 100 мг, папаин 60 мг, бромелаин 45 мг | 24 мг | 1 мг | Руто-зид 50 мг | ||||||||||
| Дигестал | Драже | 5000 | 6000 | 300 | 0,025 | 0,05 | – | – | – | – | – | – | – | ||
| Ипентал | Таблетки | Панкреатин 193 мг | |||||||||||||
8000
25000
форте
форте
10 000
зим
Бромелаин 75 Ед
тельная)
ковая)
ковая)
ковая)
офлат
летки в капсулах
таблетки в капсулах
ковая)
Крайне важно учитывать, что доза ферментных препаратов зависит от степени панкреатической недостаточности и от содержания в препарате липазы. При поступлении ферментов в тонкую кишку активность их резко падает и, уже за связкой Трейтца, остаются активными только 22% трипсина и 8% липазы. Следовательно, даже при умеренной панкреатической недостаточности возникает дефицит липазы.
При стеаторее, более 15 г жира в сутки, а также при наличии поносов и снижении массы тела, как правило, диета не дает существенного эффекта. Таким больным показано назначение капсул панцитрата или креона, содержащих 25000 липазы, при каждом приеме пищи. При этом можно расширить диету с включением преимущественно растительных жиров до 60–70 г/сут.
Тем не менее у части больных симптомы нарушения пищеварения сохраняются и при использовании высоких доз ферментов. Дальнейшее увеличение дозы, в большинстве случаев, не улучшает результаты лечения.
Основными причинами неэффективности ферментной терапии являются:
Активность ферментных препаратов в значительной степени зависит от таких факторов, как интрадуоденальный рН и моторика тонкой кишки, которые обеспечивают оптимальный по длительности контакт ферментов с пищевым химусом. При снижении рН в двенадцатиперстной кишке менее 4,0 происходит необратимая инактивация липазы, менее 3,5 – трипсина. При рН менее 5,0 наблюдается преципитация солей желчных кислот, что сопровождается нарушением эмульгирования жиров, уменьшением количества мицелл желчных и жирных кислот и снижением их всасывания.
Основными причинами закисления двенадцатиперстной кишки являются повышенная секреция хлористоводородной кислоты, снижение секреции бикарбонатов. В этих случаях вместе с ферментными препаратами для повышения интрадуоденального рН используют блокаторы Н2-гистаминовых рецепторов (ранитидин, фамотидин) или ингибиторы протонной помпы (омепразол, лансопразол, пантопразол, рабепразол). Дозы препаратов и продолжительность лечения определяют индивидуально в зависимости от ведущего механизма данного нарушения.
Расстройства моторики тонкой кишки также сопровождаются нарушением смешивания ферментных препаратов с пищевым химусом, что снижает их эффективность. Использование микротаблетированных и микросферических препаратов (панцитрат, креон, ликреаза), а также дополнительное назначение средств, нормализующих моторику кишечника (спазмолитики, прокинетики), позволяет существенно улучшить результаты лечения.
При дисбиозе тонкой кишки повысить эффективность ферментной терапии можно путем назначения эубиотиков для деконтаминации тонкой кишки.
Выбор комбинированных энзимных препаратов важен при сочетании заболеваний желчевыделительной системы и печени с нарушениями пищеварения. Тем не менее, нужно помнить, что использование препаратов с желчными кислотами может усилить интоксикацию при тяжелых хронических гепатитах и циррозах. При синдроме хронической диареи, в условиях вторичного нарушения всасывания желчных кислот в кишечнике, дополнительное их введение может усилить диарею. У больных с дуоденогастральным рефлюксом применение ферментных препаратов, содержащих в своем составе желчные кислоты (фестал, дигестал, панзистал и др.), нецелесообразно, поскольку в этих условиях желчные кислоты усиливают повреждающее действие рефлюкса на слизистую оболочку желудка.
В настоящее время установлено, что при обострении хронического панкреатита заместительная терапия ферментами способствует обратному торможению секреции железы, снижению гипертензии в протоках, в результате чего отмечается анальгезирующий эффект.
Важно учитывать, что при хроническом панкреатите ферментные препараты не должны снижать рН желудка, стимулировать панкреатическую секрецию и усиливать диарею. Препаратами выбора в таких случаях являются те, которые не содержат желчь и экстракты слизистой оболочки желудка (панзинорм форте-Н, панкреатин, сомилаза, солизим, трифермент, креон, панцитрат и др.).
Для коррекции креатореи требуются меньшие дозы препаратов, так как секреция панкреатических протеаз длительное время остается сохраненной даже при выраженных структурных изменениях поджелудочной железы. Кроме того, в принятых внутрь ферментных препаратах в первую очередь снижается активность липазы, а затем протеаз.
Ферментные препараты при хроническом панкреатите с внешнесекреторной недостаточностью назначают на очень длительное время, часто пожизненно. Дозы их могут быть снижены при соблюдении строгой диеты с ограничением жира и белка и должны увеличиваться при расширении диеты.
Эффективность лечения ферментными препаратами оценивается клинически и методами лабораторной диагностики. При этом наиболее информативны копрологическое исследование кала и тесты, основанные на определении экскреции жира с калом. Исследования проводятся по методу Ван де Камера (количественное определение жиров в кале), инфракрасной спектрофотометрией, радиоизотопными и другими методами.
В настоящее время для оценки внешнесекреторной недостаточности поджелудочной железы широкое распространение получил эластазный тест. В отличие от существующих неинвазивных тестов эластазный тест позволяет выявить эндокринную недостаточность поджелудочной железы уже на ранних стадиях заболевания. Эластаза в кале наиболее достоверно отражает экзокринную недостаточность поджелудочной железы, так как в отличие от остальных ферментов не инактивируется при транзите по кишечнику. Стандартный эластазный копрологический тест содержит моноклональные антитела к панкратической эластазе человека.
Побочные эффекты при применении ферментных препаратов встречаются крайне редко (менее 1%) и носят чаще всего дозазависимый характер.
В моче больных, применяющих высокие дозы панкреатических ферментов, может наблюдаться повышенное содержание мочевой кислоты. Гиперypикoзypия способствует преципитации мочевой кислоты в канальцевом аппарате почки, формирует условия для развития мочекаменной болезни. У больных муковисцидозом, длительно использующих высокие дозы панкреатических ферментов, возможно развитие интерстициального фиброза. При целиакии на фоне атрофии слизистой оболочки тонкой кишки в крови больных резко меняется обмен пуриновых оснований с накоплением высоких концентраций мочевой кислоты и увеличением ее экскреции. С осторожностью ферментные препараты применяют у больных подагрой.
В некоторых случаях больных, принимающих ферменты, может беспокоить диарея, запор, ощущения дискомфорта в области желудка, тошнота, раздражение перианальной области.
Основными противопоказаниями для назначения ферментных препаратов, содержащих компоненты желчи, являются острый и хронический панкреатиты, острые и тяжелые хронические заболевания печени, диарея, воспалительные заболевания кишечника, аллергические реакции в анамнезе на свинину или говядину.
Таким образом, терапию ферментными препаратами следует проводить дифференцированно с учетом механизма развития заболевания, лежащего в основе нарушения пищеварения. Наличие в распоряжении врача высокоактивных микротаблетированных и микрогранулированных препаратов позволяет значительно повысить эффективность лечения ферментами.
Ферментные препараты в гастроэнтерологии.
Саблин О.А., Бутенко Е.В.
Кафедра гастроэнтерологии ВМА им. С.М. Кирова, Санкт-Петербург.
Consilium-Medicum. 2004. Том 6, № 1. Гастроэнтерология.