ПРОЛИФЕРАЦИЯ
Пролиферация (лат. proles потомство + ferre носить, создавать) — новообразование клеток и внутриклеточных структур (митохондрий, эндоплазматической сети, рибосом и др.).
Пролиферация — явление широко распространенное в норме и патологии. Оно лежит в основе роста и дифференцировки тканей в процессе индивидуального развития, обеспечивает непрерывное обновление клеток и внутриклеточных структур, колебания функциональной активности органов, особенно при длительном их функциональном напряжении. Пролиферация. различных клеток иммунокомпетентной системы (лимфоцитов, плазматических клеток, макрофагов и др.) и их органелл является структурной основой иммуногенеза. При патологических процессах, сопровождающихся повреждением органов и тканей, с помощью Пролиферации ликвидируется образовавшийся дефект и нормализуется нарушенная функция. Пролиферация может возникать вследствие нарушений гормональных влияний и приводит к уродливому увеличению органа, напр, при акромегалии. В результате пролиферации клеток, утративших способность дифференцироваться в клетки того или иного органа, развивается опухоль. Пролиферация также лежит в основе метаплазии (см.).
Источником Пролиферации являются недифференцированные, так наз. стволовые клетки данной ткани, которые, периодически подвергаясь делению и последующей дифференцировке, постепенно превращаются в специфические клетки этой ткани, выполняющие характерную для нее функцию. Пролиферация клеток осуществляется путем их прямого или непрямого деления (см. Амитоз, Митоз). Новообразование ультраструктур клеток происходит посредством их деления, почкования и др.
Ряд органов и тканей (кроветворная, волокнистая соединительная, костная ткань, эпидермис, эпителий слизистых оболочек) обладает очень высокой способностью к Пролиферации клеток, другие — более умеренной (скелетная мышца, поджелудочная, слюнная железы и др.), третьи — совсем или почти лишены этой способности (ц. н. с., миокард). В последних репарация повреждения и нормализация функций после перенесенных болезней, а также длительное функциональное напряжение обеспечиваются гл. обр. за счет Пролиферации внутриклеточных структур в сохранившихся клетках, которые при этом увеличиваются в объеме, подвергаются гипертрофии. При этом гипертрофия органа может произойти как в результате Пролиферации клеток (см. Гиперплазия), так и только ультраструктур сохранившихся клеточных элементов.
Библиография: Давыдовский И. В. Общая патология человека, с. 376, М., 1969; Струков А. И. и Серов В. В. Патологическая анатомия, с. 99, М., 1979.
Пролиферация клеток это что такое
В развитии низших и высших позвоночных отчетливо прослеживается единая общебиологическая закономерность, выражающаяся в появлении зародышевых листков и обособлении основных зачатков органов и тканей. Процесс образования тканей из материала эмбриональных зачатков составляет суть учения о гистогенезах.
Эмбриональный гистогенез, по определению А.А. Клишова (1984), — это комплекс координированных во времени и пространстве процессов пролиферации, клеточного роста, миграции, межклеточных взаимодействий, дифференциации, детерминации, программированной гибели клеток и некоторых других. Все названные процессы в той или иной мере протекают в зародыше, начиная с самых ранних стадий его развития.
Пролиферация. Основной способ деления тканевых клеток — это митоз. По мере увеличения числа клеток возникают клеточные группы, или популяции, объединенные общностью локализации в составе зародышевых листков (эмбриональных зачатков) и обладающие сходными гистогенетическими потенциями. Клеточный цикл регулируется многочисленными вне- и внутриклеточными механизмами. К внеклеточным относятся влияния на клетку цитокинов, факторов роста, гормональных и нейрогенных стимулов. Роль внутриклеточных регуляторов играют специфические белки цитоплазмы. В течение каждого клеточного цикла существуют несколько критических точек, соответствующих переходу клетки из одного периода цикла в другой. При нарушении внутренней системы контроля клетка под влиянием собственных факторов регуляции элиминируется апоптозом, либо на некоторое время задерживается в одном из периодов цикла.
Метод радиографического анализа клеточных циклов в различных тканях выявил особенности соотношения клеточной репродукции и дифференцировки. Например, если в тканях (кроветворные ткани, эпидермис) имеется постоянный фонд пролиферирующих клеток, за счет которых обеспечивается непрерывное возникновение новых клеток взамен погибающих, то эти ткани относятся к обновляющимся. Другие ткани, например, некоторые соединительные, характеризуются тем, что в них увеличение количества клеток происходит параллельно с их дифференцировкой, клетки в этих тканях характеризуются низкой митотической активностью. Это растущие ткани. Наконец, нервная ткань характеризуется тем, что все основные процессы репродукции заканчиваются в период эмбрионального гистогенеза (когда формируется основной запас стволовых клеток, достаточный для последующего развития ткани). Поэтому она отнесена к стабильным (стационарным) тканям. Продолжительность жизни клеток в обновляющихся, растущих и стабильных тканях разная.
Наряду с обновлением клеточной популяции, в самих клетках постоянно наблюдается обновление внутриклеточных структур (внутриклеточная физиологическая регенерация).
Клеточный рост, миграция и межклеточные взаимодействия. Рост клеток проявляется в изменении их размеров и формы. При усилении функциональной активности и внутриклеточных биосинтезов наблюдается увеличение объема клетки. Если объем клетки превышает некую норму, то говорят о ее гипертрофии, и наоборот, при снижении функциональной активности происходит уменьшение объема клетки, а при переходе некоторых нормативных параметров возникает атрофия клетки. Рост клетки не беспределен и определяется оптимальным ядерно-цитоплазменным отношением.
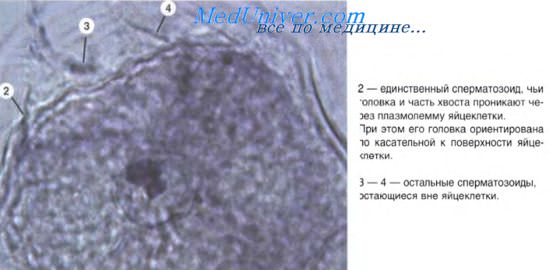
Важное значение для гистогенеза имеют процессы перемещения клеток. Миграция клеток наиболее характерна для периода гаструляции. Однако и в период гисто- и органогенеза происходят перемещения клеточных масс (например, смещения миобластов из миотомов в места закладки скелетных мышц; движение клеток из нервного гребня с образованием спинномозговых ганглиев и нервных сплетений, миграция гоноцитов и т. д.). Миграция осуществляется с помощью нескольких механизмов. Так, различают хемотаксис — движение клеток в направлении градиента концентрации какого-либо химического агента (перемещения спермиев к яйцеклетке, предшественников Т-лимфоцитов из костного мозга в закладку тимуса).
Гаптотаксис — механизм перемещения клеток по градиенту концентрации адгезионной молекулы (движение клеток протока пронефроса у амфибий по градиенту щелочной фосфатазы на поверхности мезодермы). Контактное ориентирование — когда в какой-либо преграде остается один канал для перемещения (описан у рыб при образовании плавников).
Контактное ингибирование — этот способ перемещения наблюдается у клеток нервного гребня. Суть способа заключается в том, что при образовании ламеллоподии одной клеткой и контакта ее с другой клеткой, ламеллоподия прекращает рост и постепенно исчезает, но в другой части мигрирующей клетки при этом формируется новая ламеллоподия.
В процессе миграции клеток важную роль играют межклеточные взаимодействия. Существует несколько механизмов такого взаимодействия (контактного и дистантного). Выделяется большая группа молекул клеточной адгезии (МКА). Так, кадгерины — это Са2+-зависимые МКА, отвечают за межклеточные контакты при образовании тканей, за формообразование и др. В молекуле кадгерина различают внеклеточный, трансмембранный и внутриклеточный домены. Например, внеклеточный домен ответственен за адгезию клеток с одинаковыми кадгеринами, а внутриклеточный — за форму клетки. Другой класс МКА — это иммуноглобулиновое суперсемейство Са2+-независимых МКА, обеспечивающих, например, адгезию аксонов к сарколемме мышечных волокон, или миграцию нейробластов вдоль радиальных глиоцитов в закладке коры большого мозга и др. Следующий класс МКА — это мембранные ферменты — гликозилтранферазы. Последние по типу «ключ-замок» соединяются с углеводными субстратами — гликозаминогликанами надмембранного комплекса клетки, осуществляя таким образом прочное сцепление клеток.
Кроме механизмов межклеточного взаимодействия, существуют механизмы взаимодействия клеток с субстратом. Они включают формирование рецепторов клетки к молекулам внеклеточного матрикса. К последним относят производные клеток, среди которых наиболее изученными адгезионными молекулами являются коллаген, фибронектин, ламинин, тенасцин и некоторые другие. Коллагены, среди которых различают несколько десятков типов, входят в состав межклеточного вещества рыхлой волокнистой соединительной ткани, базальной мембраны и пр. Фибронектин, секретируемый клетками, является связывающей молекулой между мигрирующей клеткой и межклеточным матриксом. Ламинин — компонент базальной мембраны, также связывает мигрирующие клетки с межклеточным матриксом (справедливо по отношению к эпителиоцитам и нейробластам).
Для осуществления связи мигрирующих клеток с межклеточным матриксом клетки формируют специфические рецепторы. К ним относятся, например, синдекан, который обеспечивает контакт эпителиоцита с базальной мембраной за счет сцепления с молекулами фибронектина и коллагена. Интегрины клеточных поверхностей связывают с внеклеточной стороны молекулы внеклеточного матрикса, а внутри клетки — белки цитоскелета (например, актиновые микрофиламенты). Так возникает связь внутри- и внеклеточных структур, что позволяет клетке использовать для перемещения собственный сократительный аппарат. Наконец, существует большая группа молекул, формирующих клеточные контакты, осуществляющие коммуникацию между клетками (щелевые контакты), механическую связь (десмосомы, плотные контакты).
Дистантные межклеточные взаимодействия осуществляются путем секреции гормонов и факторов роста (ФР). Последние — это вещества, оказывающие стимулирующее влияние на пролиферацию и дифференцировку клеток и тканей. К ним относятся, например, ФР, полученный из тромбоцитов и влияющий на переход клеток в фазу размножения (гладких миоцитов, фибробластов, глиоцитов); эпидермальный ФР — стимулирует пролиферацию эпителиоцитов, производных эктодермы; ФР фибробластов — стимулирует пролиферацию фибробластов. Особо выделяется большая группа пептидов (соматотропины, соматомедины, инсулин, лактоген), влияющих на развитие клеток плода.
Факторы, тормозящие пролиферацию и дифференцировку клеток, также принимают кооперативное участие в процессах развития клеток и тканей. К ним относятся, например, бета-интерферон и трансформирующий ФР. Последний, однако, в отношении разных клеточных типов действует по-разному: блокирует размножение многих типов эпителиоцитов, но стимулирует размножение соединительнотканных клеток.
— Вернуться в оглавление раздела «гистология»
Пролиферация клеток это что такое
Частота заболеваний щитовидной железы, особенно среди населения, проживающего на территориях с радиоактивным загрязнением, постоянно нарастает. Более трети населения мира страдают различными формами тиреоидной патологии. По данным исследователей, в ближайшие годы следует ожидать дальнейшего увеличения числа пациентов с этими заболеваниями. Рост тиреоидной патологии, особенно после Чернобыльской катастрофы, а также заметное влияние заболеваний щитовидной железы на здоровье, работоспособность и качество жизни определяют повышенный интерес исследователей к дальнейшему изучению структуры и функции этого органа в условиях патологии (Д.Е. Шилин, Н.М. Швора и соавт., 2003; О.К. Хмельницкий, Н.М. Хмельницкая и соавт., 2004; П.С. Ветшев, К.Е. Чилингариди, А.В. Золкин и соавт., 2006; Л.П. Чурилов и соавт., 2008; N.R. Gallegos-Flores и соавт., 2008; R.V. Aristarkhov и др., 2010).
Узловые образования – самая частая патология щитовидной железы. Распространенность узловых поражений щитовидной железы, по оценкам разных исследователей, составляет от 3 до 7 %. Заболеваемость узловым зобом прямо пропорциональна возрасту. Прирост заболеваемости составляет приблизительно 0,1 % в молодом возрасте и постепенно достигает 2 %. В группе лиц старше 35–40 лет распространенность узловых образований щитовидной железы достигает 46 %. За последние 20 лет наблюдается значительное изменение в структуре патологии щитовидной железы с возрастанием удельного веса больных с нетоксическим зобом (В.Э. Ванушко, Н.С. Кузнецов и соавт., 2005; Ю.В. Иванов, И.В. Кацков, 2006).
Узловой зоб – собирательное клиническое понятие, объединяющее все пальпируемые очаговые образования в щитовидной железе, имеющие различные морфологические характеристики. Наиболее частым заболеванием (около 90 %), протекающим с формированием узловых образований (узлов) щитовидной железы, является коллоидный, в разной степени пролиферирующий зоб, который по морфологии не относится к опухолям щитовидной железы. Термин «многоузловой зоб» целесообразно использовать при обнаружении в щитовидной железе 2 и более узловых образований (В. Семиков, 2002; В. Фадеев, 2002; Yushang Cui и др., 2002).
По мнению ряда авторов (И.И. Дедов, Г.А. Мельниченко, В.В. Фадеев и соавт., 2005), патологическое и прогностическое значение узлового зоба сводится к относительно небольшому риску того, что узловое образование является злокачественной опухолью щитовидной железы; относительно небольшому риску значительного увеличения щитовидной железы со сдавлением окружающих органов и/или формированием косметического дефекта; более существенному риску развития функциональной автономии щитовидной железы и тиреотоксикоза через многие годы после формирования узлового зоба.
Учитывая факт значительного распространения узлового зоба на территории Российской Федерации, наличия риска рецидива и малигнизации, возникает необходимость углубленного изучения пролиферативных процессов в щитовидной железе.
Цель исследования: определить характер и степень пролиферативной активности тиреоцитов при узловом зобе.
Задачи исследования:
1. Изучить патоморфологические изменения в щитовидной железе при узловом зобе.
2. Определить степень пролиферации тиреоцитов на основании показателей областей ядрышковых организаторов.
3. Выявить иммуногистохимические критерии пролиферативной активности тиреоцитов.
Материалы и методы исследования
Работа выполнена на операционном материале щитовидных желез в лаборатории кафедры патологической анатомии ГБОУ ВПО СтГМУ. Операционный материал получен у 213 больных во время операции на щитовидной железе в лечебных учреждениях г. Владикавказа.
Проводили макроскопическое и микроскопическое исследование материала. При макроскопическом исследовании определяли размеры, форму, цвет, консистенцию, состояние капсулы и вид на разрезе. Для гистологического исследования брали кусочки из всех узлов и подозрительных участков. Кусочки щитовидной железы фиксировали в 10 % растворе нейтрального формалина, проводили в спиртах по возрастающей крепости, заливали в парафин по стандартной методике. Из парафиновых блоков на санном микротоме готовили срезы толщиной 5–6 мкм. Депарафинироваванные срезы окрашивали гематоксилином и эозином, пикрофуксином по Ван Гизону, толуидиновым синим, по Маллори, проводили ШИК-реакцию.
С целью выявления областей ядрышковых организаторов срезы окрашивали азотнокислым серебром по методу D. Plofon, J. Crocker.
Для иммуногистохимического исследования кусочки щитовидной железы фиксировали в 10 % растворе забуференного формалина, готовили парафиновые блоки и делали серийные срезы с каждого блока толщиной 5 мкм. Иммуногистохимическое исследование проводили непрямым иммунопероксидазным методом с восстановлением антигенной специфичности.
Проведено морфометрическое исследование: измеряли площадь тиреоцитов в контрольной и основной группах.
Результаты исследования и их обсуждение
Из 213 случаев мужчины составили 30 случаев (14 %), женщины 183 случая (86 %). Соотношение мужчин и женщин составило 1:6, что соответствует данным литературных источников. По возрасту материал распределился следующим образом (таблица).
Распределение материала по возрастным группам
Узловой зоб наиболее часто встречается в возрастной группе от 30 до 50 лет. После 50 лет наблюдается постепенное снижение количества наблюдений.
Макроскопически узловой зоб представлен в виде одиночного, но чаще множественных узлов разной формы и размеров от 2–3 см в диаметре до 12–15 см. Чаще всего изменяется вся железа и представляет собой конгломерат узлов. Поверхность узлов гладкая, серовато-белого цвета, иногда дольчатая. На разрезе мягкой консистенции светло-коричневого цвета. Ткань узлов прозрачная, коллоидного вида. Почти все узлы инкапсулированы полностью или частично. Часто в узлах на разрезе обнаруживаются полости (кисты) разной величины и формы, одиночные или множественные.
При гистологическом описании зобноизмененных щитовидных желез обращали особое внимание на общий тип строения железы; распространение, диаметр и форму фолликулов; характер фолликулярного и интрафолликулярного эпителия; состояние коллоида, стромы и капсулы.
Узловой зоб характеризуются избыточным накоплением коллоида и растяжением фолликулов, что является основной причиной увеличения щитовидной железы. Это так называемый «стационарный» зоб. Однако в определенной части наблюдений увеличение железы происходит за счет пролиферации тиреоцитов, т.е. так называемый «пролиферирующий» зоб.
В 171 (80 %) случае из 213 исследований обнаружен пролиферирующий зоб. Пролиферирующие зобы чаще встречались у женщин. Выявлены следующие формы зобной пролиферации: пролиферация интрафолликулярного эпителия с образованием внутрифолликулярных сосочковых структур; пролиферация экстрафолликулярного эпителия с образованием подушечек Сандерсона; пролиферация малодифференцированных клеток с образованием узлов разного строения (трабекулярного, микрофолликулярного, папиллярного и др.).
Пролиферация интрафолликулярного эпителия в узловых (многоузловых) коллоидных зобах происходит путем деления фолликулярных клеток (тироцитов) с последующим увеличением размеров фолликулов. В увеличенных фолликулах образуются складки и сосочки разной величины и формы, которые вдаются в полость фолликулов. В пролиферирующих зобах число складок и сосочков увеличивается. Сосочки состоят из эпителиальных клеток, бывают разной формы и величины. В узловых зобах сосочковая пролиферация эпителия носит очаговый характер. Интрафолликулярная пролиферация наиболее выражена в многоузловых зобах.
Экстрафолликулярная пролиферация характеризуется образованием эпителиальных почек, которые оттесняют базальную мембрану, формируются крупные подушечки Сандерсона. В дальнейшем в подушечках Сандерсона образуются мелкие вторичные фолликулы. Во вторичных фолликулах начинается синтез тиреоглобулина, накапливается коллоид и образуются микрофолликулы.
Пролиферативные процессы в узловых зобах бывают разной степени выраженности, что проявляется увеличением количества и размеров сандерсоновых подушек.
В многоузловом зобе чаще всего узлы имеют разное строение, что придает щитовидной железе своеобразный полиморфный вид. Некоторые узлы значительно отличаются от остальных узлов и приобретают структуры, построенные в виде трабекул, сосочков или фетальных фолликулов. В данном случае отмечается пролиферация малодифференцированных клеток с образованием узлов-регенератов.
Встречаются узлы, образованные тяжами из мелких тироцитов с круглым гиперхромным ядром. Тяжи разделены тонкими прослойками соединительной ткани.
Описанные узлы чаще всего хорошо инкапсулированы, имеют равномерно выраженную соединительнотканную строму. Образование таких обособленных и четко инкапсулированных узлов происходит, по-видимому, вследствие пролиферации эпителиальных клеток эмбрионального зачатка. Эмбриональные клетки являются предшественниками тиреоцитов. Подобная пролиферация свидетельствует о высокой пролиферативной активности в железе. Изредка встречаются скопления эпителиальных тяжей без капсулы в толще многоузлового зоба.
Встречаются узлы, состоящие из малодифференцированных мелких фолликул, выстланных кубическим эпителием, которые похожи на гистологическую структуру щитовидной железы в фетальном (плодном) периоде. В большинстве микрофолликулов коллоид отсутствует, небольшая часть фолликулов заполнена жидким эозинофильным коллоидом.
В описанных узлах строма образована рыхлой волокнистой соединительной тканью, в центре таких узлов определяется отек и гиалиноз. По периферии узла определяются мелкие фолликулы, выстланные низким призматическим эпителием.
В пролиферирующих зобах встречаются узлы папиллярного строения. Они образованы крупными фолликулами, содержащими коллоид и наличием сосочковых структур. Сосочки образованы эпителиальными клетками кубической или призматической формы с базально расположенными ядрами. Строма сосочков образована соединительной тканью с наличием капилляров.
Таким образом, пролиферирующий зоб характеризуется выраженной интрафолликулярной и экстрафолликулярной пролиферацией эпителия, пролиферацией малодифференцированных клеток с образованием узлов-регенератов трабекулярного (эмбрионального), фетального (микрофолликулярного) и папиллярного строения. Гистологическое строение пролиферирующего зоба – это узловой или многоузловой зоб.
Полученные результаты позволили выявить 3 степени пролиферации в узловых образованиях щитовидной железы:
Первая степень зобной пролиферации не является фактором риска рецидива зоба после оперативного вмешательства на щитовидной железе.
Вторая степень зобной пролиферации служит фактором риска рецидива зоба. Признаков возможной малигнизации при данной степени пролиферации не выявлено.
Третья степень пролиферации служит достоверным признаком рецидива зоба и возможной малигнизации узлов-регенератов. Эту стадию, на наш взгляд, можно рассматривать как предраковую и оценивать как дисплазию III степени.
Выводы
Результаты исследования операционного материала щитовидных желез показали, что узловой (многоузловой) зоб является наиболее частой формой эндемического зоба в йоддефицитном регионе Северной Осетии – Алании. В 70 % случаев в узловом зобе обнаружены пролиферативные процессы, которые характеризуются пролиферацией фолликулярного эпителия, экстрафолликулярного эпителия, а также формированием узлов-регенератов в виде долек трабекулярного, микрофолликулярного (фетального) и папиллярного строения. Площадь ядер тиреоцитов в очагах пролиферации увеличивается от 26,3 до 78,3 мкм2. Параметры областей ядрышковых организаторов в очагах пролиферации составили 3,5 ± 0,05 экспрессия протеина Ki-67 повысилась от 15 до 35 %. Оценивая в совокупности перечисленные показатели, мы выделили 3 степени пролиферации тиреоидного эпителия. Третья степень пролиферации является наиболее тяжелой. Полученные данные указывают на высокую вероятность рецидива узлового зоба.
Рецензенты:
Коробкеев А.А., д.м.н., профессор, зав. кафедрой нормальной анатомии, ГБОУ ВПО «Ставропольский государственный медицинский университет» Министерства здравоохранения РФ, г. Ставрополь;
Бондарь Т.П., д.м.н., профессор, директор Института живых систем, зав. кафедрой медицинской биохимии, клинической лабораторной диагностики и фармации, ФГАОУ ВПО «Северо-Кавказский федеральный университет», г. Ставрополь.
Атипическая гиперплазия эндометрия
При атипической гиперплазии внутренний слой матки — эндометрий —разрастается, что ведет к увеличению его толщины и объема. При этом морфология клеток изменяется, появляются атипичные — клетки, изменившие свои свойства. Вид и особенности таких клеток становятся нехарактерными тем, из которых они появились. Заболевание может развиваться у женщин любой возрастной категории, но вероятность ее появления выше в постменопаузе.
Это гинекологическое заболевание относится к предраковым состояниям, если адекватное лечение отсутствует, то болезнь в 40% переходит в злокачественную форму. Появление эндометрия с атипической железистой гиперплазией может означать начало преобразования в аденокарциному — злокачественное заболевание. Появление атипичных клеток в функциональном слое слизистой характерно для начального этапа атипической гиперплазии эндометрия матки, их обнаружение в базальном слое и строме — признак начинающегося рака эндометрия.
Как появляется заболевание
Развитие заболевания тесно связано с уровнем гормонов в организме. У здоровой женщины функциональный слой эндометрия увеличивается в 1-й половине цикла. Когда зачатия не наступает, происходит его отторжение, затем он естественным путем удаляется из матки. При гормональных отклонениях этот процесс нарушен, происходит активное деление клеток, однако своевременного отторжения и выведения частиц эндометрия нет. Наблюдается его утолщение и разрастание. Патологические очаги могут появляться на отдельных участках или же избыточное разрастание будет равномерным. Когда все же происходит отторжение эндометрия, появляется обильное кровотечение.
Гиперплазия — прогрессирующее заболевание, со временем свойства эндометрия изменяются, что способствует появлению нехарактерных клеток, развивается атипическая гиперплазия эндометрия. Однако существуют факторы, увеличивающие вероятность появления заболевания:
К группе риска относятся женщины с лишним весом. Сахарный диабет, гипертония также увеличивают риск развития заболевания.
Симптомы
Основным признаком атипической гиперплазии эндометрия является кровотечение. Более продолжительные, чем менструация, нередко продолжающиеся около 3-х недель, кровотечения могут быть цикличными (чаще у женщин репродуктивного возраста) или ацикличными. Не отделившиеся частицы эндометрия могут стать причиной межменструальных выделений. Нередко кровотечения возникают после задержки; после незначительной — выделения носят умеренный характер, после длительной — они становятся обильными. У четверти пациенток возникают ановуляторные кровотечения — нерегулярные, большей продолжительности и кровопотери.
Отсутствие лечения приводит к осложнениям. В результате длительных и обильных кровотечений развивается анемия. К наиболее тяжелым последствиям атипической гиперплазии эндометрия относится переход болезни в рак.
Однако заболевание не всегда сопровождается характерными признаками, при бессимптомном течении женщина может долго и безуспешно пытаться забеременеть. Гиперплазия эндометрия в таком случае впервые диагностируется, когда женщина обращается к врачу по поводу бесплодия.
Диагностика
Чтобы своевременно обнаружить болезнь даже при бессимптомном течении, важно регулярно проходить гинекологическое обследование даже при отсутствии каких-либо жалоб. В настоящее время существуют различные методики, позволяющие безошибочно диагностировать заболевание даже на ранней стадии. Сюда входят:
Для уточнения диагноза также может быть рекомендовано проведение МРТ, назначено обследование у эндокринолога, что важно для пациенток, входящих в группу риска. Комплексное обследование позволяет обнаружить не только атипическую гиперплазию эндометрия, но и диагностировать другие заболевания: как половой сферы (миому, кисты яичников и т.п.), так и другие отклонения (сахарный диабет, гипертонию и др.).
Лечение
Выбор тактики лечения при атипической гиперплазии эндометрия зависит от возраста пациентки, тяжести состояния, наличия сопутствующих заболеваний, осложнений, а также желания женщины сохранить функцию репродукции. Лечение может быть консервативным или хирургическим.
При консервативной терапии назначаются гормональные препараты, направленные на подавление разрастания эндометрия, нормализацию цикла, восстановление гормонального баланса. При наличии кровотечений показано выскабливание эндометрия во время гистероскопии.
Хирургическое лечение — какие существуют варианты
Операция при атипической гиперплазии эндометрия назначается, если:
Не так давно единственным методом лечения было удаление матки. Я выполняю радикальную операцию в том случае, если патоморфологически подтвержден рак эндометрия, в остальных ситуациях возможно проведение органосохраняющего вмешательства.
Одним из эффективных методов является гистерорезектоскопия, рекомендованная женщинам репродуктивного возраста или в пременопаузальном периоде. Процедура относится к малотравматичным и выполняется с использованием эндоскопического оборудования, оснащенного видеокамерой. Возможность визуализации позволяет проводить манипуляции максимально бережно и с высокой точностью, без риска развития осложнений. Длительность процедуры — около получаса, период восстановления занимает не более 14 дней.
Однако для проведения гистерорезектоскопии, как и при любом хирургическом вмешательстве, имеются противопоказания:
При лечении гиперплазии неплохо зарекомендовала себя малоинвазивная процедура — абляция — трансцервикальная деструкция эндометрия. Во время ее проведения можно удалить базальный и функциональный слой эндометрия, а также часть миометрия на глубину 3-5 мм. Абляция может быть проведена с помощью лазерной или электрохирургической методики, но в любом случае процедура выполняется с использованием гистероскопического оборудования, поэтому является безопасной и эффективной.
При наступлении менопаузы женщине рекомендована гистерэктомия — удаление матки. Если патологические изменения в яичниках отсутствуют, то операция проводится без удаления придатков. В случае, если имеется аденомиоз или подтвержден злокачественный процесс в матке, то гистерэктомия проводится с удалением придатков. Органуносящая операция также показана пациенткам в постменопаузе при рецидиве после гормонального лечения.
Мною проведено более 4000 гинекологических операций, в том числе по поводу гиперплазии эндометрия. К каждой пациентке я подбираю тактику лечения, учитывая целый ряд деталей: возраст и наличие других болезней, желание сохранить матку как орган и проведенное ранее лечение. Если существует возможность, я всегда стремлюсь провести малотравматичную органосохраняющую операцию, после которой женщина сможет быстро вернуться к привычному образу жизни. После такой операции восстановление занимает не более двух недель, а госпитализация не превышает трех дней.
Сегодня возможность сохранить матку имеется даже у пациенток с сопутствующими гинекологическими заболеваниями (например, с миомой, кистами, полипами). Однако проведение органосохраняющей операции окажется невозможным, если процесс перейдет в злокачественный. Чтобы избежать подобного, следует регулярно проходить осмотры. В нашей клинике даже полное обследование займет минимум времени.