Контрацептивные и лечебные свойства прогестагенов
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Среди многочисленных методов предупреждения нежелательной беременности наиболее эффективным считается гормональная контрацепция. Комбинированные оральные контрацептивы (КОК) последнего поколения, в состав которых входят синтетические аналоги эстрогенов и гестагенов, приобретают все большую популярность среди женщин и обладают хорошей клинической эффективностью. Несмотря на снижение концентрации эстрогенов в современных КОК, причиной отказа от использования этих препаратов у большинства женщин являются такие осложнения, как тошнота, головные боли, болезненность молочных желез. С эстрогенами, входящими в состав КОК, связаны побочные дозозависимые эффекты: венозные тромбэмболии, инфаркт миокарда и инсульт, особенно у женщин с наличием факторов риска развития сердечно–сосудистых заболеваний.
На сегодняшний день КОК – не единственные противозачаточные препараты: значительное число различных по составу контрацептивов, синтезированных в последние годы, позволяет учитывать жизненные ситуации, возрастные группы, наличие гинекологических и экстрагенитальных заболеваний.
Параллельно с созданием КОК были разработаны препараты для контрацепции, содержащие только прогестагены, и цель их создания заключалась в исключении влияния на организм женщины эстрогенного компонента. Существует несколько видов прогестагенных контрацептивов (ПК), которые различаются по методу назначения и длительности применения. К этим препаратам относятся:
• таблетированные формы (мини–пили, Чарозетта)
• инъекционные препараты (Депо–провера)
• подкожные импланты (Норплант, Импланон)
• внутриматочные контрацептивы (Мирена).
Впервые контрацептивный эффект орального прогестагена норэтинодрела при назначении его в течение 20 дней с последующей меструальноподобной реакцией на его отмену был описан еще в 50–е годы ХХ века. Однако в клинической практике ПК, содержащие прогестагены первого и второго поколения – норэтистерон (НЭ) и левоноргестрел (ЛНГ), появились почти 20 лет спустя. Эти контрацептивы, к сожалению, не стали полноценной заменой КОК, т.к. не вызывали стойкого и полноценного подавления овуляции. Это отражалось на контрацептивной эффективности препаратов, которая обеспечивалась преимущественно влиянием прогестагенов на цервикальную слизь. Снижение перистальтики маточных труб на фоне приема мини–пили некоторые авторы расценивали, как фактор риска возникновения внематочной беременности. К негативным эффектам этой группы контрацептивов относятся: дозозависимый андрогенный эффект и ациклические кровянистые выделения в течение первых месяцев приема препаратов, возникающие в результате особенностей влияния препаратов на эндометрий.
В связи с этим при создании нового поколения ПК учитывались такие требования, как стойкое подавление овуляции и надежная контрацепция минимальными дозами прогестагенов, при минимальных побочных реакциях и осложнениях.
Дезогестрел (ДЗГ) является высокоселективным прогестагеном последнего поколения с низкой андрогенной активностью. При пероральном приеме ДЗГ быстро абсорбируется, метаболизируясь в печени и стенке кишечника. В процессе превращения образуется активный метаболит – 3–кето–дезогестрел (этоногестрел), который обладает бо’?льшим сродством к рецепторам прогестерона и ме’ньшим – к рецепторам андрогенов, чем прогестагены первого и второго поколения. Дозы ДЗГ 60 мкг в сутки уже достаточно для 100%–го подавления овуляции. В дозах, использующихся для контрацепции, ДЗГ лишен андрогенных побочных эффектов.
В клинической практике используется препарат, содержащий 75 мкг ДЗГ, известный под названием Чарозетта.
Контрацептивный эффект Чарозетты обусловлен:
• подавлением секреции гонадотропных и стероидных гормонов, что вызывает подавление овуляции. Сравнительная оценка контрацептивной эффективности Чарозетты и мини–пили, содержащего 30 мкг ЛНГ, выявила, что подавление овуляции наблюдалось в 97% циклов при использовании Чарозетты и в 34–50% циклов при использовании ЛНГ [Rice C. и соавт. 1996, 1999]. В другом клиническом исследовании подавление овуляции наблюдалось в 99% циклов [Korver T. и соавт. 2005];
• повышением вязкости цервикальной слизи, что препятствует проникновению сперматозоидов в полость матки;
• гистологическими изменениями эндометрия, препятствующими имплантации оплодотворенной яйцеклетки. По данным исследования Rice и соавт. (1999), у 30% женщин, принимающих Чарозетту, эндометрий находится в неактивной фазе или в фазе слабой пролиферации, а у 40–50% – в секреторной фазе.
Таким образом, у женщин, принимавших Чарозетту, отмечена выраженная степень подавления овуляции. Кроме того, в сравнительных клинических исследованиях доказано, что частота внематочной беременности при приеме Чарозетты не превышает аналогичные показатели в популяции [Korver T. и соавт. 1998].
Показателем эффективности методов контрацепции является индекс Перля: частота наступления беременности у 100 женщин в течение 1 года. Контрацептивная эффективность Чарозетты была изучена в многоцентровом сравнительном клиническом исследовании, в котором приняло участие 1320 женщин. На протяжении 12 месяцев женщины принимали Чарозетту (n=989) или мини–пили, содержащий 30 мкг ЛНГ (n=331). 30% женщин в обеих группах кормили грудью. В результате исследования установлено, что индекс Перля для Чарозетты составил 0,41, для мини–пили – 1,55. После исключения беременностей, которые наступили при несоблюдении правил приема препаратов, этот индекс составил соответственно: 0,14 и 1,17. Таким образом, выявлена более высокая контрацептивная активность Чарозетты, сравнимая с клинической эффективностью КОК (0,15–0,54).
Приемлемость препаратов, как правило, оценивается особенностями изменения менструального цикла, характером и степенью выраженности побочных эффектов и влиянием на изменение массы тела на фоне их приема.
Частота и особенности побочных эффектов не являются специфичными для Чарозетты и практически равны эффекту плацебо. Наиболее частыми побочными эффектами при приеме Чарозетты являются головная боль (6,8%), болезненность молочных желез (3,7%) и тошнота (3,3%), что у большинства женщин не является причиной отказа от данного вида контрацепции.
В течение первых циклов приема препарата ациклические маточные кровотечения на фоне Чарозетты могут наблюдаться чаще, чем при приеме КОК. В исследовании В.Н. Прилепской и соавт. (2004), изучавших характер кровянистых выделений на фоне Чарозетты, использована методика ВОЗ «стандартного временного интервала», который равен 90 дням. Показано, что в первом стандартном интервале (1–90 дней) редкие кровянистые выделения (1–2 эпизода) отмечались у 35% женщин, 3–5 эпизодов – у 52%. Это считается нормальным, т.к. за период в 90 дней у женщины бывает 3–5 менструаций. Частые кровянистые выделения диагностированы только у 9% женщин, аменорея – у 4% и длительные, более 14 дней, кровянистые выделения – у 14% пациенток. По мере продолжения приема препарата кровянистые выделения становятся более редкими и менее обильными. По данным Korver T. и его коллег (1998), аменорея наблюдалась у 20% женщин к 9–12 месяцу использования препарата. В случае аменореи на фоне приема прогестагенной контрацепции менструация не вызывается.
Изучение особенностей обмена веществ на фоне Чарозетты позволило сделать вывод о минимальном, клинически незначимом влиянии препарата на липидный спектр: незначительное снижение липопротеидов высокой плотности, общего холестерина, триглицеридов и липопротеина А при нормальном содержании липопротеидов низкой плотности [Barkfeldt J. и соавт. 1999]. Однако данные изменения не оказывают существенного влияния на риск развития сердечно–сосудистой патологии. Не было выявлено клинически значимых отклонений от нормы в углеводном обмене [Kivela А. и соавт., 2001]. При изучении системы гемостаза отмечена тенденция к уменьшению свертывающей и повышению фибринолитической активности показателей крови [Winkler U. и соавт., 1998]. Также Чарозетта не оказывает отрицательного влияния на артериальное давление и другие физиологические показатели организма женщин [Korver T. и соавт., 1998, Barkfeldt J. и соавт., 1999, Kivela А. и соавт., 2001].
Известно, что применение эстроген–гестагенных препаратов у лактирующих женщин противопоказано, т.к. эстрогены уменьшают количество молока и негативно влияют на его состав. При приеме Чарозетты не меняются количество и состав молока, а также отсутствует отрицательное влияние на рост и развитие ребенка [Bjarnadottir R. и соавт., 2001]. В связи с этими данными Чарозетта, как и другие прогестагенные контрацептивы, рекомендуется к применению уже через 6 недель после родов у лактирующих женщин.
Учитывая особенности влияния Чарозетты основные функциональные системы организма и высокую контрацептивную активность, приоритетными показаниями к назначению препарата являются:
• группы женщин, у которых имеются противопоказания для назначения КОК и женщины с экстрагенитальной патологией (пороки сердца, сахарный диабет, мигрень и др.)
• курящие женщины старше 35 лет
• женщины в период лактации.
Количество противопоказаний значительно меньше, чем для эстроген–гестагенных препаратов. К ним относятся:
• подозрение на беременность
• тяжелые заболевания печени с нарушением ее функции
• тромбоэмболия в настоящее время илив анамнезе
• прогестаген–зависимые опухоли
• вагинальные кровотечения неуточненного генеза.
Чарозетта назначается в непрерывном режиме с 1 дня менструального цикла по 1 таблетке в сутки в одно и то же время без перерыва на менструацию. Начать прием препарата можно и со 2 по 5–й день цикла, но в этом случае необзодимо использовать дополнительную контрацепцию в течение первых 7 дней использовании препарата. После аборта прием Чарозетты начинается непосредственно в день прерывания беременности в непрерывном режиме.
Если прием препарата задержан менее чем на 12 часов, это не влияет на контрацептивный эффект Чарозетты. Если пропуск в приеме таблетки более 12 часов, то требуются дополнительные методы предохранения от беременности.
В ряде исследований изучена возможность применения Чарозетты в комплексном лечении дисменореи и мигрени, связанной с менструальным циклом. Терапия, как правило, проводится совместно с неврологами–вегетологами.
Показана возможность применения Чарозетты у женщин с генитальным эндометриозом. В тех случаях, когда женщина не нуждается в беременности после комплексной терапии эндометриоза (лапароскопическая коррекция и последующая медикаментозная терапия агонистами гонадолиберина или данолом), целесообразно рекомендовать контрацепцию Чарозеттой, поскольку она применяется в непрерывном режиме и обеспечивает дополнительные лечебные эффекты.
Описан благоприятный эффект Чарозетты у женщин с предменструальным синдромом и фиброзно–кистозной болезнью молочных желез. Терапевтический эффект у этих женщин связывают с длительным подавлением овуляции и эстрогенных влияний, а также циклических колебаний стероидных гормонов.
Анализ данных отечественной и зарубежной литературы свидетельствует о высокой контрацептивной эффективности препарата Чарозетта, которая сравнима с эффективностью КОК. Высокая приемлемость, отсутствие отрицательного влияния на организм в целом и побочных эффектов, связанных с применением эстрогенов, расширяет возможности использования данного препарата не только с контрацептивной, но и с лечебной целью.
Менопаузальная гормонотерапия (МГТ)

Почему же процент женщин, принимающих МГТ, остается невысоким?
Крупное американское исследование WHI (Women’s Health Initiative, 2002 г.) вызвало драматический период в судьбе менопаузальной гормонзаместительной терапии, что способствовало резкому сокращению МГТ в большинстве стран мира, появлению страхов и сомнений в отношении пользы и рисков.
Преждевременное завершение части исследования по менопаузальной гормонзаместительной терапии (МГТ) привлекло к себе всеобщее внимание. Как женщины, так и врачи чувствовали себя обманутыми, так как терапия, которая до этого считалась полезной для здоровья в долгосрочной перспективе, теперь оказалась опасной. Отличающийся от фактического изложения пресс-релиз предварительной работы прогремел в СМИ за неделю до того, как сама статья стала доступна для большинства читателей. Сообщалось, что исследование было остановлено в связи с повышенным риском развития рака молочной железы, связанным с заместительной гормональной терапией. На самом деле, в скорректированном анализе связь МГТ и рака молочной железы не была статистически значима!
Последующий углубленный анализ результатов WHI показал, что МГТ характеризуется благоприятным профилем пользы/риска у более молодых женщин, которые начинают терапию в близкие к менопаузе сроки. Эти результаты характеризовались сходным защитным воздействием терапии в отношении ИБС и снижения общей смертности, которые были продемонстрированы ранее в крупномасштабных наблюдательных исследованиях с участием относительно молодых женщин. После WHI широкое распространение получила так называемая временная гипотеза или гипотеза «окна терапевтических возможностей», согласно которой существует различное влияние МГТ на атеросклероз и связанные с ним клинические события в зависимости от возраста женщины и времени начала использования МГТ по отношению к моменту наступления менопаузы.
Основными недостатки данного исследования являлись:
Что же происходит с женским организмом в 45-55 лет?
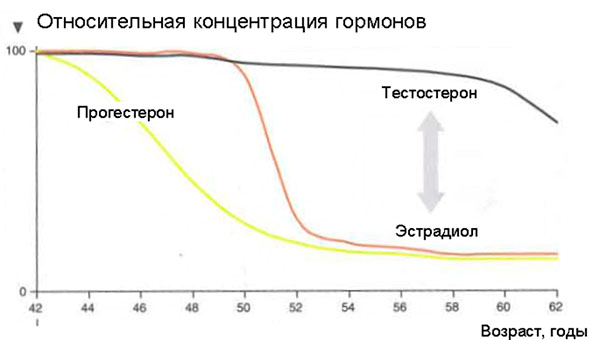
Что будет если МГТ не проводить?
А зачем нужно так «рисковать» и принимать «страшные» гормональные препараты при наступлении менопаузы? Ведь это естественный процесс, может, пусть все идет, как заведено природой? — Но тогда мы неизбежно столкнемся с заболеваниями, которые также предопределены природой.
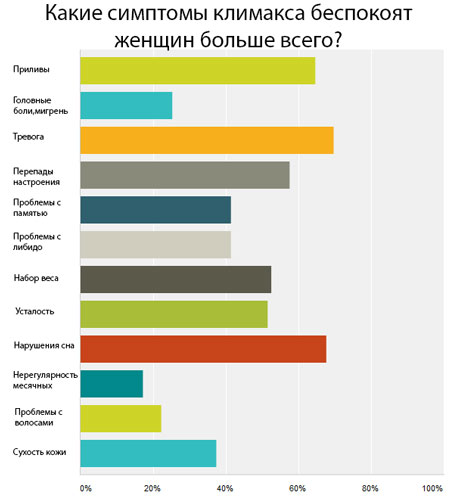
Сначала появляются ранние симптомы:
Через некоторое время появятся и поздние нарушения, связанные с длительным дефицитом половых гормонов:
Какое обследование проводится перед МГТ
Перед назначением менопаузальной гормональной терапии необходимо обследование (впрочем, которое необходимо проводить хотя бы раз в год и без терапии всем сознательным женщинам старше 45 лет).
Дополнительные обследования (при соответствующих данных анамнеза):
Когда пора начинать менопаузальную гормональную терапию?
Но проблема в том, что диапазон нормы ФСГ огромен, и для каждой женщины уровень свой. В идеале нужно сдать анализы крови на гормоны в период максимального расцвета – с 19 до 23 лет. Это и будет вашей индивидуальной идеальной нормой. А начиная с 45 лет ежегодно сверять с ней результаты. Но даже если вы впервые слышите о ФСГ – лучше поздно, чем никогда: в 30, 35, 40 лет имеет смысл выяснить свой гормональный статус, чтобы ближе к критическому возрасту было, на что ориентироваться.
Как самостоятельно понять, что пришло время МГТ?
Уровень эстрогенов снизился, если:
Препаратов огромное количество, какие из них наиболее безопасны?
Действует принцип «минимальности» и «натуральности»!
Для менопаузальной гормональной терапии применяются различные препараты, которые могут быть разделены на несколько групп:
«Натуральные» эстрогены – это препараты эстрогенов, которые по химической структуре идентичны эстрадиолу, синтезируемому в организме женщин. Благодаря современным технологиям создан синтетический эстрадиол, но по своей химической структуре он идентичен натуральному Эстрадиол–17b.
На сегодняшний день таким критериям более всего соответствует препарат Фемостон. Препараты линейки фемостона имеют различные дозировки, что укладывается в один из основных постулатов современной концепции МГТ – использование наименьшей возможной дозировки, которая сохраняет эффективность.
Препараты для двухфазной терапии – когда еще есть месячные
Фемостон 1/10 и Фемостон 2/10
В состав Фемостона 1/10 входят 28 таблеток. 14 белых, содержащих 1 мг Эстрадиола, и 14 серых, содержащих 1 мг Эстрадиола и 10 мг Дидрогестерона.
Состав Фемостона 2/10 отличается только количеством Эстрадиола
Препараты для монофазной терапии – когда месячные отсутствуют
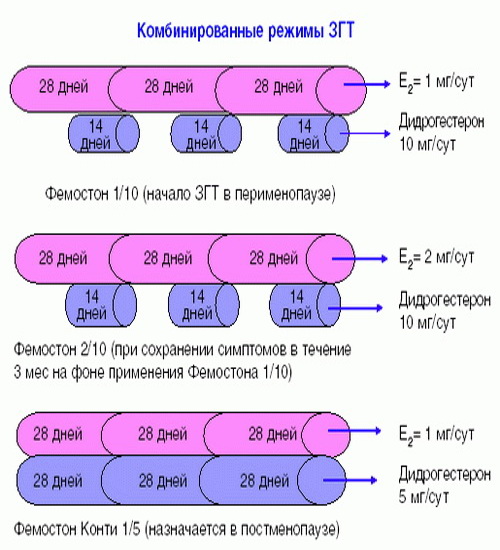
В состав Фемостона конти 1/5 входят 28 таблеток, содержащих 1 мг Эстрадиола и 5 мг Дидрогестерона.
В состав Фемостона мини 0,5/2,5 входят 28 таблеток, содержащих 0,5 мг Эстрадиола и 2,5 мг Дидрогестерона.
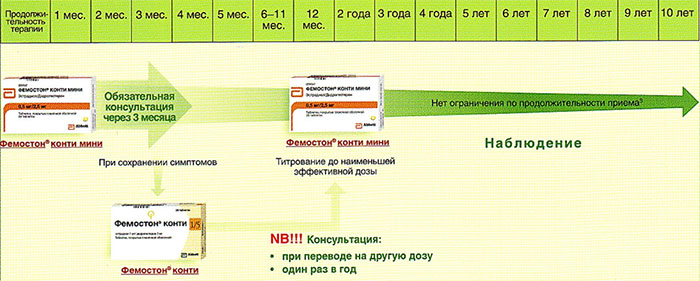
Ниже представлена более подробная схема первоначального назначения препаратов фемостон в пременопаузе (то есть до прекращения менструаций, но при наличии характерных климактерических симптомов). Пациенткам, у которых менструации не прекратились, рекомендуют начинать лечение в первый день менструального цикла. Пациенткам с нерегулярным менструальным циклом целесообразно начинать лечение после 10-14 дней монотерапии прогестагеном («химический кюретаж»).
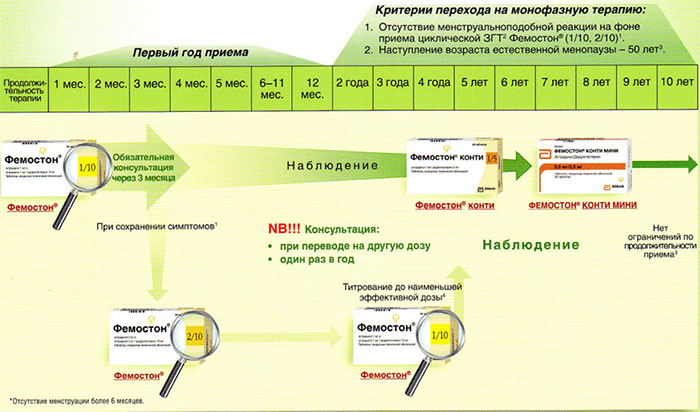
Далее Вашему вниманию представлен алгоритм первоначального назначения препарата фемостон в постменопаузе (то есть когда уже прошел год и более после последней менструации).
Какой способ применения препаратов лучше?
Трансдермальное (накожное) нанесение позволяет избежать первой стадии печеночного метаболизма, благодаря чему колебания концентрации эстрадиола в плазме крови при применении накожных препаратов незначительны. Метаболизм и выведение эстрадиола при трансдермальном введении подобен метаболизму натуральных эстрогенов.
Большинству пациентов желательно использовать оптимальную и наиболее безопасную на сегодняшний день схему: Дивигель накожно + Утрожестан интравагинально.

Схема приема для женщин, у которых сохранена менструальная функция, назначается врачом. Обычно средство прописывают циклом с первого дня после окончания менструации (5 день цикла) в течение 25 дней, после овуляции (c 16 по 25 день цикла) нужно добавлять препараты гестагенов.
Утрожестан – содержит прогестерон микронизированный, существует в двух формах — 100 и 200 мг.
При МГТ в постменопаузе в непрерывном режиме препарат Утрожестан применяется в дозе 100 мг с первого дня приема эстрогенов.
При болях в молочной железе можно добавить прожестожель ежедневно по 1 дозе на каждую молочную железу 2-4 недели.
Противопоказаниями для заместительной гормонотерапии являются:
Нужен ли женщинам тестостерон?
Согласно рекомендациям Международного общества по менопаузе (International Menopause Society (IMS)) основное показание для применения тестостерона – лечение уменьшенного сексуального влечения, которое заставляет данную женщину испытывать значительные страдания. До рассмотрения вопроса о проведении терапии тестостероном необходимо решить вопросы, связанные с другими причинами нарушенного сексуального желания и/или возбуждения. К ним относятся диспареуния, депрессия, побочные эффекты лекарственных препаратов, проблемы взаимоотношений и другие проблемы со здоровьем, влияющие на женщину или ее партнера.
В настоящее время возможно применение трансдермальных препартов. На отечественном фармацевтическом рынке существует только один вариант – Андрогель, но его применение у женщин является «off-label», то есть не разрешено инструкцией. Обычно назначается 1/5 пакета в день (то есть 1 г геля/10 мг тестостерона).
Еще более перспективным может стать интравагинальная форма тестостерона, которая также может оказывать благоприятное действие при лечении вульвовагинальной атрофии.
Ключевые положения по применению препаратов тестостерона
Самые частые заблуждения:
А как же рак молочной железы, ведь это самая главная причина смерти у женщин?
В этом утверждении много заблуждений. На самом деле рак молочной железы – причина смертности в 4% случаев. Ведущая причина преждевременной смерти – сердечно-сосудистые заболевания (50%), которые запускает инсулинорезистентность. А она возникает на фоне гормональных нарушений.
Гормоны вызывают побочные эффекты и от них толстеют?
Новые низкодозированные и высокоселективные препараты направлены четко на мишень. Врачи на протяжении многих лет наблюдали за тысячами женщин, которые получали МГТ? Сегодня уже есть уникальные гестагены, метаболически нейтральные, они не приводят к ожирению и вместе с тем не понижают тестостерон, если у женщины нет его избытка. Выработаны и новые схемы лечения. Иногда при применении таблеток с эстрогенами, где-то в 10% случаев, бывают головные боли и боль в венах. В этом случае они заменяются на трансдермальные формы в виде геля.
Зачем мне принимать гормоны, если у меня нет приливов и отличное самочувствие?
Вместе с падением уровня гормонов возникает риск развития возрастных болезней: повышается артериальное давление, возникает ожирение, увеличивается риск развития сахарного диабета второго типа, подагры, остеопороза и онкологических заболеваний.
Вместо таблеток лучше принимать травы и различные фитоэстрогены?
Эффективность данных препаратов по устранению вазомоторных симптомов составляет 30%, что равно эффективности плацебо. При этом данная группа препаратов никаким образом не оказывает профилактического действия на возрастные заболевания (сердечно-сосудистые, онкологические заболевания, остеопороз, ожирение и сахарный диабет).
Средства заместительной гормонотерапии (часть II)
Препараты различают в зависимости от содержания компонентов на эстроген–гестагенные, эстроген–андрогенные, эстроген–антиандрогенные. Эстроген–гестагенные препараты, в свою очередь, подразделяются на монофазные, двухфазные и трехфазные.
Преферанская Нина Германовна
Доцент кафедры фармакологии фармацевтического факультета Первого МГМУ им. И.М. Сеченова, к.фарм.н.
Часть II. Комбинированные гормональные эстрогенные препараты
МОНОФАЗНЫЕ ЭСТРОГЕН–ГЕСТАГЕННЫЕ ПРЕПАРАТЫ
Содержат одинаковое количество эстрогенов и гестагенов во всех таблетках, блистер (28 тб.) рассчитан 28 дней, в остальные дни цикла — перерыв.
К монофазным препаратам относятся:
Фемостон, Фемостон 1/10, Фемостон 1/5 Конти (тб., покр. обол. пленочной) – 1 мг эстрадиол + 5 мг дидрогестерон;
Клиогест, Паузогест — 2 мг эстрадиола гемигидрата + 1 мг норэтистерона ацетата в 1 тб.;
Анжелик — 1 мг эстрадиола гемигидрата + 2 мг дроспиренона в 1 тб.;
Климодиен — 2 мг эстрадиола валерата + 2 мг диеногеста в 1 тб.;
Индивина — 1 мг (2 мг) эстрадиола валерата + 25 мг (5 мг) медроксипрогестерона ацетата в 1 тб.
ДВУХФАЗНЫЕ ЭСТРОГЕН–ГЕСТАГЕННЫЕ ПРЕПАРАТЫ
Содержат разное количество таблеток двух цветов в блистере. В первую фазу таблетки содержат эстроген, а во вторую фазу помимо эстрогена добавлен гестагенный препарат.
К двухфазным эстроген-гестагеным препаратам относят:
Фемостон (блистер 28 тб.) — 1 мг (2 мг) 17β-эстрадиол (14 тб.) + 1 мг (2 мг) 17β-эстрадиол + 10 мг дидрогестерон (14 тб.);
Климонорм (блистер 21 тб.) — 2 мг эстрадиола валерата (9 тб.) + 0,15 мг левоноргестрела (12 тб.);
Дивина (блистер 21 тб.) — 2 мг эстрадиола валерата (11 тб.) + 10 мг медроксипрогестерон ацетат (10 тб.);
Цикло–Прогинова (блистер 21 тб.) — 1 мг (2 мг) эстрадиола валерата (9 тб.) + 1 мг (2 мг) эстрадиола валерата + 0,5 мг норгестрела (12 тб.).
ТРЕХФАЗНЫЕ ЭСТРОГЕН–ГЕСТАГЕННЫЕ ПРЕПАРАТЫ
Рассчитаны на три фазы менструального цикла, поэтому блистер в виде календарного диска или пластины содержит три разных по составу и цвету таблетки, в составе которых меняется количество эстрогена и во вторую серию таблеток добавлен гестаген.
Трисеквенс — 2 мг эстрадиола гемигидрата (12 тб.) + 1 мг норэтистерона ацетат (10 тб.) + 1 мг эстрадиола гемигидрата (6 тб.).
Обращаю внимание! Добавление гестагена в препараты ЗГТ особенно важно, т.к. они предотвращают развитие побочных эффектов, вызванных длительным применением эстрогенов, таких как гиперплазия эндометрия или рак эндометрия. Добавление гестагенного компонента позволяет усилить некоторые эффекты эстрадиола, в частности на сердечно-сосудистую и костную системы организма. От гестагенного компонента зависит переносимость препарата и частота побочных эффектов.
Используемые в настоящее время в ЗГТ гестагены помимо прогестагенного эффекта обладают эстрогенными и андрогенными свойствами – норэтистерона ацетат и тиболон; антиэстрогенными свойствами обладают прогестерон и дидрогестерон; антиандрогенными – медроксипрогестерона ацетат и диеногест.
Гестагены взаимодействуют с прогестероновыми рецепторами и оказывают специфические гестагенные эффекты. Наличие и выраженность того или иного эффекта при применении ЗГТ зависит от входящих в комбинированный препарат компонентов. Наиболее часто в качестве гестагена используют медроксипрогестерона ацетат, который входит в состав препаратов Дивина, Индивина.
Препараты Клиогест, Трисеквенс, Паузогест содержат синтетический гестаген — норэтистерона ацетат, который подобно прогестерону проникает в цитоплазму клетки, связывается с цитозольными рецепторами, образуя комплекс. Далее попадает в ядро и за счет прямого связывания с ядерными прогестиновыми рецепторами вызывает инициацию транскрипции и увеличение белкового синтеза. Служит для снижения повышенной стимуляции и пролиферации эндометрия, возникающих под воздействием эстрогена. При совместном применении с эстрадиолом влияет на липидный обмен, повышая концентрации антиатерогенных липопротеинов и снижая общий холестерин крови и триглицеридов. Применение норэтистерона ацетата обеспечивает предсказуемый контроль кровотечений у большинства женщин. Усиливает защитное действие эстрогенов на костную ткань, что сопровождается достоверным увеличением минерализации костей и ингибированием костной резорбции при его применении.
К препаратам, содержащим аналог природного прогестерона — дидрогестерон, относят Дюфастон и Фемостон, которые эффективны, начиная с ранних симптомов менопаузы. Они хорошо зарекомендовали себя при климактерических расстройствах в период менопаузы. Дюфастон не обладает эстрогенной активностью, его используют у женщин с расстройствами, обусловленными естественной или хирургической менопаузой, и показан во всех случаях недостаточности лютеиновой фазы.
Дроспиренон, входящий в состав противоклимактерического препарата Анжелик, является производным спиронолактона, калий-сберегающего диуретического средства, обладает гестагенным, антиадрогенным, антигонадотропным и антиминералокортикоидным действием. Препарат применяется при преждевременном истощении яичников, при климактерических расстройствах в постменопаузе и в целях профилактики постменопаузного остеопороза.
Диеногест — новый «гибридный» гестаген, входящий в состав препарата Климодиен, оказывает трансформирующее влияние на эндометрий, обладает умеренным антигонадотропным эффектом, антиандрогенной активностью и, что не менее важно, антипролиферативной активностью на раковые клетки молочной железы. Также оказывает минимальное влияние на метаболические процессы, т.к. имеет короткий период полувыведения и в организме не кумулирует.
При пероральном приеме имеет высокую биодоступность, не связывается с транспортными глобулинами крови и циркулирует в крови в виде свободной фракции, что позволяет применять препарат малыми дозами. Антигонадотропный эффект связан с заметным увеличением элиминации с мочой эстрогенов и уменьшением выведения гонадотропинов. Климодиен начинают применять не ранее чем через один год после наступления менопаузы, когда системная терапия вместе с эстрогенами приводит к уменьшению физиологической инволюции кожи при старении, оказывает протективное действие на сердечно-сосудистую систему, понижает уровень общего холестерина в крови, предупреждает потерю костной массы, улучшает настроение.
Климен относят к препаратам, содержащим эстроген–антиандроген (2 мг эстрадиола валерата (11 драже белого цвета) + 2 мг эстрадиола валерата + 1 мг ципротерона ацетата (10 драже розового цвета). Обладая антиандрогенной активностью, некоторые прогестины устраняют юношескую себорею, появление вторичных мужских половых признаков, умеренную вирилизацию (появление на лице волосяного пушка, усов и роста волос на подбородке). Ципротерона ацетат блокирует андрогенновые рецепторы в клетках-мишенях, уменьшает уровень андрогенов в крови, угнетает секрецию гипофизом гонадотропного гормона и тормозит овуляцию. Способствует исчезновению угревой сыпи, уменьшает повышенное салоотделение на волосистой части головы и коже лица, устраняет выпадение волос. Восполняет в организме женщины дефицит половых гормонов; устраняет симптоматику климактерических расстройств, гиперплазии эндометрия, понижает уровень холестерина ЛПНП в сыворотке крови. Его применяют для профилактики постменопаузного остеопороза; при эстрогенной недостаточности (овариоэктомия по поводу незлокачественных новообразований), нарушениях менструального цикла — первичная и вторичная аменорея и др.
Тиболон (в блистере 28 тб.) относится к препаратам, содержащим синтетические эстрогены, выпускается под ТН «Ледибон» и «Ливиал» и используется при климактерическом синдроме. 1 тб. содержит 2,5 мг тиболона. Препарат нивелирует климактерические изменения гипоталамо-гипофизарной системы, подавляет секрецию гонадотропинов ФСГ и ЛГ, а у фертильных женщин ингибирует овуляцию. Восстанавливает слизистую оболочку влагалища, предотвращает потерю костной массы, подавляет менопаузные расстройства, такие как приливы, повышенная потливость, головные боли, положительно влияет на либидо и настроение. Применяется для устранения симптомов менопаузы (естественной и после хирургических операций).
Важно! При применении данного препарата наблюдаются побочные эффекты: головная боль, головокружение, отек голеней, диспептические расстройства, влагалищное кровотечение, изменение показателей функции печени, себорейный дерматоз, усиление роста волос на лице, возможно снижение уровней общего и свободного тироксина и тироксинсвязывающего глобулина. Прием следует прекратить при появлении признаков тромбоэмболии, изменении лабораторных показателей функции печени, развитии холестатической желтухи.
Абсолютными противопоказаниями приема препаратов ЗГТ являются: геморрагический или ишемический инсульт, инфаркт миокарда, сердечная недостаточность, тяжелая форма гипертонии, тромбоэмболия, тромбофлебит, сахарный диабет, хронические заболевания печени и почек, новообразования половых органов и молочных желез (рак шейки и тела матки, миома матки, рак яичников, рак молочной железы), склонность к маточным кровотечениям и др. Курение повышает риск осложнений со стороны сердечно-сосудистой системы и снижает эффективность ЗГТ.