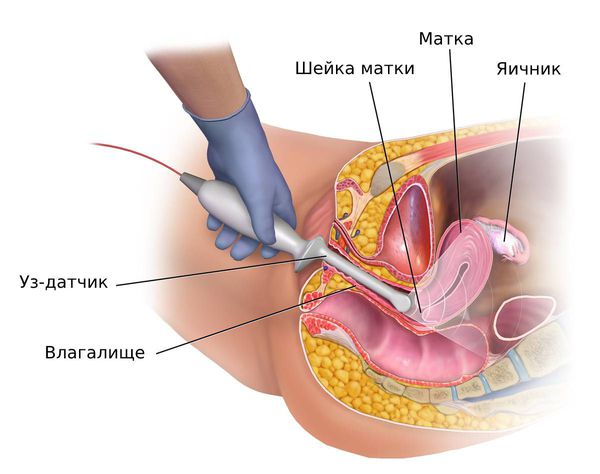
ПРОЛИФЕРАЦИЯ
Пролиферация (лат. proles потомство + ferre носить, создавать) — новообразование клеток и внутриклеточных структур (митохондрий, эндоплазматической сети, рибосом и др.).
Пролиферация — явление широко распространенное в норме и патологии. Оно лежит в основе роста и дифференцировки тканей в процессе индивидуального развития, обеспечивает непрерывное обновление клеток и внутриклеточных структур, колебания функциональной активности органов, особенно при длительном их функциональном напряжении. Пролиферация. различных клеток иммунокомпетентной системы (лимфоцитов, плазматических клеток, макрофагов и др.) и их органелл является структурной основой иммуногенеза. При патологических процессах, сопровождающихся повреждением органов и тканей, с помощью Пролиферации ликвидируется образовавшийся дефект и нормализуется нарушенная функция. Пролиферация может возникать вследствие нарушений гормональных влияний и приводит к уродливому увеличению органа, напр, при акромегалии. В результате пролиферации клеток, утративших способность дифференцироваться в клетки того или иного органа, развивается опухоль. Пролиферация также лежит в основе метаплазии (см.).
Источником Пролиферации являются недифференцированные, так наз. стволовые клетки данной ткани, которые, периодически подвергаясь делению и последующей дифференцировке, постепенно превращаются в специфические клетки этой ткани, выполняющие характерную для нее функцию. Пролиферация клеток осуществляется путем их прямого или непрямого деления (см. Амитоз, Митоз). Новообразование ультраструктур клеток происходит посредством их деления, почкования и др.
Ряд органов и тканей (кроветворная, волокнистая соединительная, костная ткань, эпидермис, эпителий слизистых оболочек) обладает очень высокой способностью к Пролиферации клеток, другие — более умеренной (скелетная мышца, поджелудочная, слюнная железы и др.), третьи — совсем или почти лишены этой способности (ц. н. с., миокард). В последних репарация повреждения и нормализация функций после перенесенных болезней, а также длительное функциональное напряжение обеспечиваются гл. обр. за счет Пролиферации внутриклеточных структур в сохранившихся клетках, которые при этом увеличиваются в объеме, подвергаются гипертрофии. При этом гипертрофия органа может произойти как в результате Пролиферации клеток (см. Гиперплазия), так и только ультраструктур сохранившихся клеточных элементов.
Библиография: Давыдовский И. В. Общая патология человека, с. 376, М., 1969; Струков А. И. и Серов В. В. Патологическая анатомия, с. 99, М., 1979.
Признаки пролиферации что это
Пролиферативная активность клеток отражает интенсивность роста опухолей. В статье приведены данные изучения уровня пролиферации клеток базалиомы — наиболее частой злокачественной опухоли кожи. Исследование проводили иммуногистохимическим методом с маркером пролиферации Ki67. По характеру пролиферации базалиома представляла гетерогенную группу. Солидный, аденоидный, поверхностный мультицентрический тип базалиомы отличались низкой пролиферативной активностью с преимущественным распределением клеток, экспрессирующих Ki67, по периферии комплексов. Высокую пролиферативную активность выявляли в инфильтративном, склерозирующем и микронодулярном типе при равномерном распределении пролиферирующих клеток.
Пролиферативная активность клеток отражает интенсивность роста опухолей. В статье приведены данные изучения уровня пролиферации клеток базалиомы — наиболее частой злокачественной опухоли кожи. Исследование проводили иммуногистохимическим методом с маркером пролиферации Ki67. По характеру пролиферации базалиома представляла гетерогенную группу. Солидный, аденоидный, поверхностный мультицентрический тип базалиомы отличались низкой пролиферативной активностью с преимущественным распределением клеток, экспрессирующих Ki67, по периферии комплексов. Высокую пролиферативную активность выявляли в инфильтративном, склерозирующем и микронодулярном типе при равномерном распределении пролиферирующих клеток.
В структуре злокачественных эпителиальных опухолей кожи первое место занимает базалиома, на долю которой приходится от 75 до 94% [1, 2]. В подавляющем большинстве случаев регистрируются солитарные опухоли, локализующиеся на открытых участках кожи, подверженных инсоляции. Опухоль отличается медленным течением и относительно благоприятным прогнозом. Однако в ряде случав она может значительно увеличиваться в размере, характеризуясь выраженным экзофитным ростом, либо приобретать инвазивные черты, проникая в окружающие и подлежащие ткани, приводя к их разрушению. Подобный рост опухоли обычно ассоциируется с определенными морфологическими типами, которые рассматривают как агрессивные [3].
Показателем интенсивности роста ткани является пролиферативная активность клеток. Она относительно спокойна в доброкачественных процессах и резко возрастает в злокачественных опухолях. Аналогичные тенденции присущи и эпителиальным опухолям кожи. Так, пролиферативная активность клеток базальноклеточного рака кожи выше, чем в очагах лейкоплакии [4], а при раке in situ индекс пролиферации превосходит таковой при предраковом актиническом кератозе [4,5]. Плоскоклеточный рак кожи отличается высоким уровнем пролиферации, который следует за снижением степени его дифференцировки [6, 7, 8].
Предыдущие исследования показали, что по характеру пролиферативной активности клеток базалиома представляет гетерогенную группу. Наиболее интенсивный рост имела язвенная форма, тогда как нодулярная и поверхностная характеризовались умеренными и низкими показателями [9]. Высокий уровень пролиферации отмечали в микронодулярном, метатипическом типе базалиомы и типе морфеа [10, 12]. Также отмечали повышение индекса Ki67 в инфильтративном и метатипическом типе по сравнению с нодулярным и поверхностным [11, 13]. В то же время единого мнения о связи уровня пролиферации с гистологическим типом базалиомы до сих пор нет, так как другие исследования свидетельствовали, что индекс Ki67 в нодулярном и поверхностном мультицентрическом типе базальноклеточного рака значительно превосходил аналогичный показатель в склерозированном и типе морфеа [14, 15]. Учитывая противоречивые данные, представляется интересным и актуальным продолжить изучение пролиферативной активности клеток в различных морфологических типах базалиомы, что позволит более детально понимать маркеры и предикторы агрессивного течения опухоли.
Материалы и методы
В работе исследования использовали 36 биоптатов кожи больных базальноклеточным раком кожи. Биопсию кожи размером 0,5 х 0,5 см проводили под местной анестезией 2% раствором новокаина, биоптаты фиксировали в 10% растворе формалина, забуфференом по Лилли при рН-7,4. Материал заливали в парафин по обычной методике. Серийные срезы толщиной 3–5 мкм депарафинировали по стандартной схеме, затем окрашивали гематоксилином и эозином. Иммуногистохимическое исследование проводили в соответствии со стандартным протоколом. Парафиновые срезы наносили на стекла с адгезивным покрытием, депарафинировали по стандартному протоколу. Срезы, погруженные в цитратный буфер, инкубировали в микроволновой печи при мощности 690 Вт два раза по пять минут. Двадцать минут при комнатной температуре, срезы охлаждали, подсушивали и наносили первичные антитела. Для определения уровня пролиферации использовали моноклональные антитела к протеину Ki67 (DAKO), разведение 1:200. Использовались соответствующие позитивные и негативные контроли – иммунные и неиммунные сыворотки. Срезы промывали в буфере, подсушивали, затем на них наносили EnVision (anti-mouse и anti-rabbit, фирмы DAKO, Дания) на 30–40 минут. Для визуализации реакции наносили DAB+ (3, 3 ґ– диаминобензидин), что позволяло получать специфическую коричневую окраску. Затем срезы докрашивали гематоксилином Майера. Определение уровня пролиферации оценивалась с помощью индекса, который вычислялся как среднее от числа меченных ядер на 100 учтенных ядер (при учете 500–1000 опухолевых клеток). Подсчет меченных ядер проводился в репрезентативных полях зрения с относительно равномерным распределением опухолевых клеток, сверху вниз и слева направо. Клетки на периферии срезов, где чаще всего наблюдается фоновое окрашивание, не учитывались.
Среди 36 базалиом пять имели поверхностный мультицентрический тип строения, четыре – поверхностный мультицентрический в сочетании с солидным, семь – солидный, два – аденоидный, два – солидно-аденоидный, пять – инфильтративный, три – микронодулярный. В восьми случаях отмечали различные варианты сочетания солидного, инфильтративного, микронодулярного, склерозирующего строения.
Индекс пролиферации Ki67 в поверхностном мультицентрическом типе и при сочетании его с солидным компонентом варьировал от 14,9 до 31,1%. Средний индекс составлял 22,2%. Пролиферирующие клетки в шести случаях располагались преимущественно по периферии клеточных комплексов, в трех – равномерно по клеточным комплексам. При солидных опухолях средний индекс составил 26,5%, он варьировал от 14,5 до 38,2% (рис.1). Периферическое распределение наблюдали в четырех случаях, равномерное – в трех. При аденоидном строении пролиферирующие клетки распределялись равномерно, индекс пролиферации составлял 22,6 и 31,3%. В случаях, когда имелось сочетание солидного и аденоидного компонентов, индекс пролиферации составлял 36,8 и 19,2%, В первом случае клетки распределялись равномерно, во втором – равномерно в аденоидном компоненте и по периферии – в солидном. В опухолях инфильтративного, микронодулярного строения и при их сочетании клетки, экспрессирующие маркер Ki67, диффузно регистрировались по всем клеточным комплексам. В инфильтративном типе минимальное и максимальное значение индекса было 27,6 и 47,8% (среднее значение – 35,4%) (рис.2). Микронодулярные базалиомы имели средний индекс Ki67 26,9%. В случаях инфильтративно-склерозирующего строения индекс имел значение 40,2 и 31,6%, пролиферирующие клетки равномерно распределялись в комплексах (рис.3). При сочетании инфильтративного, солидного и микронодулярного строения преимущественно отмечали равномерное распределение пролиферирующих клеток, и средний индекс составлял 36,5% (значения варьировали от 22,1 до 50,4%). Солидное строение в сочетании с инфильтративным склерозирующим имели опухли с индексом Ki67 26,7 и 35,3%, в солидном компоненте пролиферирующие клетки располагались преимущественно по периферии комплексов, инфильтративном склерозирующем – равномерно.
При анализе пролиферативной активности клеток мы сгруппировали опухоли в зависимости от характера течения и роста. В группу неинвазивного роста мы включили опухоли, имеющие поверхностный мультицентрический, солидный, аденоидный, сочетание поверхностного мультицентрического и солидного компонентов. В группу с инвазивным ростом нами были включены опухоли инфильтративные, микронодулярные, инфильтративно склерозирующие, а также опухоли сложного строения (инфильтративный + микронодулярный + солидный и солидый + инфильтративный склерозирующий).
Средний индекс пролиферации неагрессивных типов составил 24,77 ± 7, 47 с доверительным интервалом 95% 21,27–28,26 (табл. 1). Средний индекс Ki67 агрессивных типов составлял 33,53 ± 8,94 с доверительным интервалом 95% 28,77–38,29 (табл. 1). Различия в уровне пролиферации между агрессивными и неагрессивными типами носили статистически значимый характер (р = 0,003). Анализ характера распределения пролиферирующих клеток в опухолевых комплексах показал, что в неагрессивных типах периферическое распределение клеток наблюдалось в 50% случаев, равномерное – в 45%, в 5% случаев ряд комплексов в опухоли имели один тип распределения, другие комплексы – иной тип распределения (табл.2). В агрессивных типах 81,25% случаев имели равномерное распределение пролиферирующих клеток, сочетание двух типов распределения – 18,75% (табл. 2). Периферическое распределение пролиферирующих клеток в агрессивных типах не встречалось. При сравнении распределения клеток между агрессивными и неагрессивными типами опухоли было показано, что различия носят статистически достоверный характер (р = 0,003).
Таблица 1. Индекс пролиферации Ki67 в агрессивных и неагрессивных морфологических типах базалиомы
Цитологическая диагностика заболеваний шейки матки
Цитологическое исследование мазков из шейки матки позволяет оценить состояние слизистой оболочки, наличие или отсутствие признаков патологических процессов (реактивных, предопухолевых, опухолей). При выявлении другими лабораторными методами инфекционного агента (вирус папилломы человека, бактериальные и паразитарные инфекции), цитологический метод позволяет оценить реакцию организма на инфекционный агент, наличие или отсутствие признаков повреждения, пролиферации, метаплазии или трансформации эпителия. Возможно также при исследовании мазка определить причину изменений эпителия (наличие воспаления с ориентировочным или уверенным определением патогенной микробиоты (микрофлоры), патологических процессов, связанных с гормональным, лекарственным, механическим, лучевым воздействием на организм женщины и шейку матки, состояний, чреватых опасностью возникновения дисплазии и рака шейки матки, а при их развитии установить правильный диагноз. В связи с этим цитологическое исследование применяют как при скрининге (мазки с визуально нормальной шейки матки), так и при наличии видимых при гинекологическом осмотре изменений слизистой оболочки.
Получение материала
Рак шейки матки чаще всего развивается в зоне трансформации, ему предшествуют фоновые процессы и внутриэпителиальные поражения (дисплазия эпителия), которые могут располагаться на небольших участках, поэтому важно, чтобы материал был получен со всей поверхности шейки матки, особенно из зоны стыка плоского и цилиндрического эпителия. Число измененных клеток в мазке бывает различным, и если их мало, то увеличивается вероятность, что патологические изменения могут быть пропущены при просмотре препарата. Для эффективного цитологического исследования необходимо учитывать:
Материал из шейки матки должен брать врач-гинеколог или (при скрининге, профилактическом осмотре) хорошо обученная медицинская сестра (акушерка).
Важно, чтобы в мазок попадал материал из зоны трансформации, так как около 90% опухолей исходит из зоны стыка плоского и цилиндрического эпителия и зоны трансформации и только 10% из цилиндрического эпителия цервикального канала.
С диагностической целью материал получают раздельно из эктоцервикса (влагалищной порции шейки матки) и эндоцервикса (цервикального канала) с помощью шпателя и специальной щетки (типа Cytobrush). При проведении профилактического осмотра используют Cervex-Brush, различные модификации шпателя Эйра и другие приспособления для получения материала одновременно из влагалищной части шейки матки, зоны стыка (трансформации) и цервикального канала.
Перед получением материала шейку матки обнажают в “зеркалах”, дополнительных манипуляций не проводят (шейку не смазывают, слизь не удаляют; если слизи много – ее аккуратно снимают ватным тампоном, не надавливая на шейку матки.). Щетку (шпатель Эйра) вводят в наружный зев шейки матки, осторожно направляя центральную часть приспособления по оси цервикального канала. Далее ее наконечник поворачивают на 360° (по часовой стрелке), достигая тем самым получения достаточного числа клеток из эктоцервикса и из зоны трансформации. Введение инструмента выполняют очень бережно, стараясь не повредить шейку матки. Затем щетку (шпатель) выводят из канала.
Приготовление препаратов
Перенос образца на предметное стекло (традиционный мазок) должен происходить быстро, без подсушивания и потери прилипших к инструменту слизи и клеток. Обязательно перенести на стекло материал с обеих сторон шпателя или щетки.
Если предполагается приготовление тонкослойного препарата с помощью метода жидкостной цитологии, головку щетки отсоединяют от ручки и помещают в контейнер со стабилизирующим раствором.
Фиксация мазков выполняется в зависимости от предполагаемого метода окрашивания.
Окрашивание по Папаниколау и гематоксилин-эозином наиболее информативны в оценке изменений эпителия шейки матки; любая модификация метода Романовского несколько уступает этим методам, однако при наличии опыта позволяет правильно оценить и характер патологических процессов в эпителии и микрофлору.
Клеточный состав мазков представлен слущенными клетками, находящимися на поверхности эпителиального пласта. При адекватном получении материала с поверхности слизистой оболочки шейки матки и из цервикального канала в мазок попадают клетки влагалищной порции шейки матки (многослойный плоский неороговевающий эпителий), зоны стыка или трансформации (цилиндрический и, при наличии плоскоклеточной метаплазии, метаплазированный эпителий) и клетки цервикального канала (цилиндрический эпителий). Условно клетки многослойного плоского неороговевающего эпителия принято делить на четыре типа: поверхностные, промежуточные, парабазальные, базальные. Чем лучше выражена способность эпителия к созреванию, тем более зрелые клетки попадают в мазок. При атрофических изменениях на поверхности эпителиального пласта расположены менее зрелые клетки.
Интерпретация результатов цитологического исследования
Наиболее распространенная в настоящее время – классификация Bethesda (The Bethesda System), разработанная в США в 1988 г, в которую вносили несколько изменений. Классификация создана для более эффективной передачи информации из лаборатории врачам клинических специальностей и обеспечения стандартизации лечения диагностированных нарушений, а также последующего наблюдения за больными.
В классификации Bethesda выделяют плоскоклеточные интраэпителиальные поражения низкой и высокой степени (squamous intraepithelial lesions of low grade and high grade – LSIL и HSIL) и инвазивный рак. Плоскоклеточные интраэпителиальные поражения низкой степени включают изменения, связанные с папилломавирусной инфекцией и слабой дисплазией (CIN I), высокой степени – умеренную дисплазию (CIN II), тяжелую дисплазию (CIN III) и внутриэпителиальный рак (cr in situ). В этой классификации имеются также указания на специфические инфекционные агенты, вызывающие заболевания, передавае мые половым путем.
Для обозначения клеточных изменений, которые трудно дифференцировать между реактивными состояниями и дисплазией предложен термин ASCUS – atypical squamous cells of undetermined significance (клетки плоского эпителия с атипией неясного значения). Для клинициста этот термин мало информативен, однако он нацеливает врача на то, что данная пациентка нуждается в обследовании и/или в динамическом наблюдении. В классификацию Bethesda в настоящее время введен также термин NILM – no intraepithelial lesion or malignancy, объединяющий норму, доброкачественные изменения, реактивные изменения.
Так как данные классификации используются в практике врача-цитолога, ниже приведены параллели между классификацией Bethesda и классификацией, распространенной в России (Табл. 22). Цитологическое стандартизованное заключениепо материалу из шейки матки (форма № 446/у), утверждено приказом Минздрава России от 24.04.2003 № 174.
Причины получения неполноценного материала различны, поэтому цитолог перечисляет типы клеток, обнаруженные в мазках и по возможности указывает причину, по которой материал признан неполноценным.
Гиперплазия эндометрия
Специалисты ЦМРТ проводят информативные гинекологические обследования. Прием ведет опытный и квалифицированный врач-гинеколог.
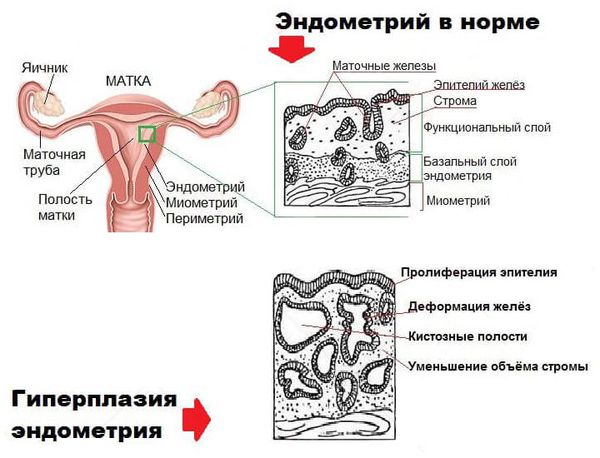
Распространенным гинекологическим заболеванием, обусловленным избыточным разрастанием слизистой оболочки внутреннего слоя матки, является гиперплазия эндометрия. Неинвазивная патологическая пролиферация эпителия имеет доброкачественный характер, однако именно она в 20-25% случаев становится основой злокачественных опухолей. И только своевременное выявление, уточнение характера и дифференцированный подход к лечению гиперпластического процесса дает высокий шанс на полное выздоровление.
Рассказывает специалист ЦМРТ
Дата публикации: 10 Августа 2021 года
Дата проверки: 30 Ноября 2021 года
Содержание статьи
Причины пролиферации эндометрия
Гиперплазия эндометрия матки (ГЭ) – это патологическое состояние, развивающееся на фоне хронической относительной или абсолютной гиперэстрогении. Существует множество факторов, способных спровоцировать избыточное образование женских половых гормонов, эстрогенов:
Причиной утолщения эндометрия матки может стать генетическая предрасположенность, гормональный дисбаланс, травматическое повреждение, вирусная инфекция.
Симптомы гиперплазии
Самым типичным морфологическим признаком, выявляемым только в ходе гистологического исследования, является неоднородность форм и размеров эпителиальных желез и увеличение их площади по отношению к строме.
На фоне развивающихся гиперпластических процессов у пациенток наблюдаются аномальные кровянистые выделения, нарушение менструального цикла, периодические тянущие боли в нижней части живота, дискомфорт во время и после сексуального контакта. У женщин, находящихся в менопаузе и постменопаузе, возможны интенсивные кровотечения и формирование в матке полипов. В отдельных случаях гиперплазия протекает бессимптомно и выявляется при прохождении планового гинекологического обследования.
Классификация и степени патологической пролиферации маточного эпителия
В зависимости от изменений архитектоники эндометрия различают 2 разновидности ГЭ: неатипическую (без признаков клеточной атипии) и атипическую (предраковое изменение клеток внутреннего слоя матки). Обе патологические формы бывают простыми и комплексными, очаговыми, диффузными или диффузно-очаговыми. Они могут быть покоящимися, умеренно-активными и активными.
При преобладании железистых компонентов речь идет о кистозной или железисто-кистозной гиперплазии. В случае формирования локальных выростов (полипов) диагностируется полиповидная гиперплазия. При выявлении атипичных клеток с измененной структурой устанавливается диагноз «аденоматоз». Предраковая пролиферация эпителия имеет 3 степени тяжести атипических изменений: слабо выраженную, умеренную и тяжелую.
Гиперплазия эндометрия: вероятность беременности
Гиперпластический процесс во внутреннем слое матки признан одной из разновидностей гормонального бесплодия. И даже при наступившей овуляции и оплодотворении измененный эндометрий не позволяет яйцеклетке нормально имплантироваться в слизистую оболочку.
Чтобы оптимизировать подготовку к физиологической беременности и обеспечить правильное развитие плода, пациенткам с гиперплазией назначается комплексное патогенетическое лечение и коррекция локального и системного иммунитета. При обнаружении инфекционных агентов дополнительно проводится антибактериальная терапия. Если подобный подход не дает эффекта, женщинам, желающим забеременеть, равно, как и другим пациенткам репродуктивного возраста, выполняется деструкция и удаление эндометрия.
Методы диагностики
Диагностические мероприятия должны быть направлены на выявление и уточнение формы гиперплазии. Для этого назначается:
Дополнительно может быть рекомендована компьютерная томография, гистеросальпингография, ИК-спектрометрия.
К какому врачу обратиться
Лечением ГЭ занимается гинеколог. При выборе врачебной тактики учитывается причина и форма болезни, возраст женщины и наличие сопутствующих патологий.
Как лечить гиперплазию эндометрия
Первый этап – диагностическое выскабливание и изучение морфологической структуры избыточно разросшегося эндометрия. Далее проводится сложная комплексная гормональная терапия, подавляющая пролиферацию клеток. Она рекомендована всем без исключения пациенткам репродуктивного возраста.
В пре- и менопаузу лечение гормонами считается целесообразным только при неатипических формах ГЭ. При отсутствии ожидаемого терапевтического эффекта (не ранее, чем через 3 месяца) проводится хирургическая операция: резекция, абляция эндометрия или гистерэктомия (тотальное удаление матки).
Последствия
Запущенная гиперплазия может стать причиной серьезных осложнений:
Профилактика
Профилактические мероприятия сводятся к постоянному контролю менструальных кровотечений, регулярным гинекологическим осмотрам, лечению имеющихся урогенитальных патологий и предотвращению рецидивов заболевания.
Лечение гиперплазии эндометрия в ЦМРТ
Сеть клиник ЦМРТ предлагает программы консервативного и послеоперационного лечения пациенток с гиперпластическими процессами матки. Терапевтический курс включает:
Гинеколог ЦМРТ принимает по предварительной записи. Оставляйте заявку на сайте клиники или звоните.
Что такое гиперплазия эндометрия? Причины возникновения, диагностику и методы лечения разберем в статье доктора Анькина А. О., врача УЗИ со стажем в 9 лет.
Определение болезни. Причины заболевания
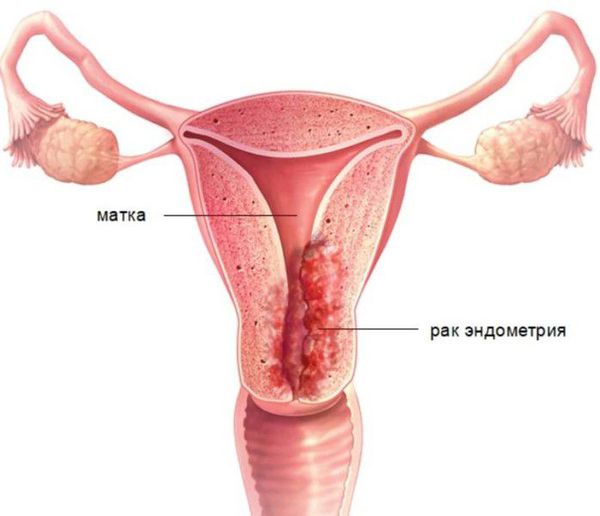
Диагноз « гиперплазия эндометрия » ставится только по заключению гистологического исследования. Без своевременной диагностики и целенаправленного лечения повышается риск развития рака эндометрия.
В составе маточного эндометрия есть специфические рецепторы, которые делают его органом-мишенью для половых гормонов. При гормональном сбое нарушается рост и дифференцировка эндометриальных клеток, что приводит к разрастанию эндометрия.
Факторы риска развития гиперплазии эндометрия [1] [8] [11] :
Симптомы гиперплазии эндометрия
В период перехода к менопаузе основным симптомом заболевания являются нерегулярные обильные менструации, сменяющиеся длительными мажущими кровянистыми выделениями.
Женщины менопаузального возраста жалуются на скудные кровянистые выделения из половых путей. Они могут проявляться эпизодически либо быть продолжительными.
Патогенез гиперплазии эндометрия
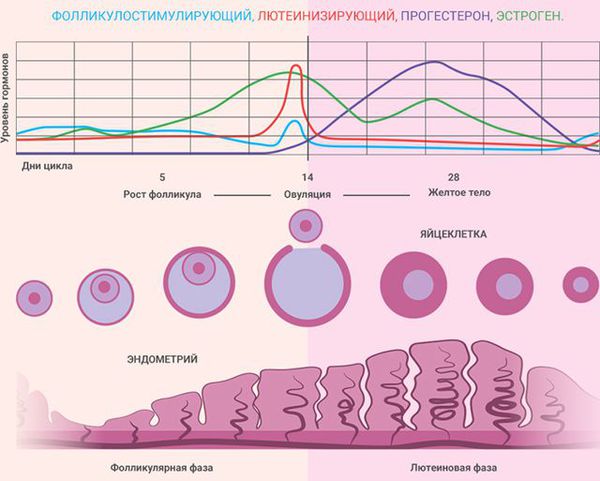
Состояние эндометрия зависит от фазы менструального цикла:
В патогенезе гиперплазии эндометрия выделяют два варианта развития событий:
В случае гиперплазии эндометрия с атипией избыток желёз эндометрия сочетается с клеточными мутациями (атипическим перерождением). Атипическая гиперплазия эндометрия является предраковым состоянием.
Классификация и стадии развития гиперплазии эндометрия
Международная классификация болезней 10-го пересмотра (МКБ-10):
Пересмотренная классификация ВОЗ 2014 года:
Осложнения гиперплазии эндометрия
Анемия. Для гиперплазии эндометрия характерны аномальные маточные кровотечения. В связи с этим женщины часто страдают от хронического малокровия разной степени выраженности.
Бесплодие. Гормональные изменения отражаются на качестве эндометрия, что создаёт риск неудачной имплантации эмбриона. Помимо этого, гиперплазия эндометрия часто выявляется на фоне хронической ановуляции, при которой зачатие невозможно.
Диагностика гиперплазии эндометрия
Диагностика основана на анализе данных анамнеза пациентки (истории болезни), клинической картины заболевания (жалоб и физикального осмотра), а также на результатах ультразвукового и гистероскопического исследования с обязательным патоморфологическим анализом соскоба из полости матки.
Диагноз «гиперплазия эндометрия» ставится только на основании гистологического исследования материала, полученного при диагностическом выскабливании слизистой оболочки матки или удалении матки.
Анамнез и клиническая картина
При сборе анамнеза врач-гинеколог задаёт пациентке вопросы:
Физикальный осмотр включает в себя местный осмотр наружных половых органов, исследование влагалища и шейки матки в зеркалах, а также бимануальное (двумя руками) исследование матки и придатков. Осмотр проводится на первичном приёме, чтобы исключить воспалительные заболевания и/или объёмные опухолевые образования.
Инструментальная диагностика
У женщин репродуктивного и пременопаузального возрастов при подозрении на гиперплазию эндометрия ТВУЗИ органов малого таза проводится на 5 – 7-й день менструального цикла. В норме в это время толщина эндометрия не превышает 6 мм. Патологию эндометрия подозревают, когда его толщина не соответствует определённой фазе менструального цикла:
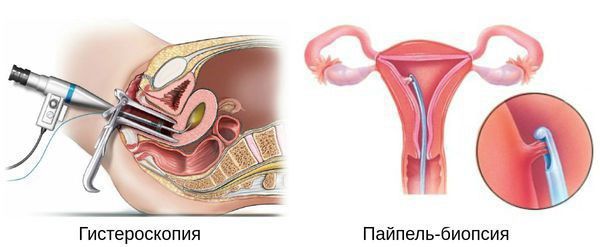
Гистероскопия с раздельным диагностическим выскабливанием (РДВ) матки и цервикального канала — информативный метод в диагностике гиперпластических процессов эндометрия. При помощи гистероскопа (эндоскопического прибора для осмотра полости матки) врач оценивает состояние слизистой оболочки матки и цервикального канала. При необходимости удаляет локальные поражения и обязательно берёт материал для последующего гистологического исследования.
Если выскабливание проводят как лечебную процедуру при обильном маточном кровотечении, врач полностью удаляет слизистую оболочку матки под контролем гистероскопии.
Дифференциальная диагностика гиперплазии эндометрия проводится с полипом эндометрия, субмукозной (подслизистой) миомой матки, эндометритом, прервавшейся беременностью и раком эндометрия.
Лечение гиперплазии эндометрия
Лечение патологии эндометрия основывается на трёх принципах:
Тактика лечения будет зависеть от результата гистологического исследования эндометрия, полученного в ходе выскабливания, от возраста женщины, сопутствующих заболеваний и репродуктивных планов.
Гиперплазия эндометрия без атипии:
Гиперплазия эндометрия с атипией:
Медикаментозное лечение гормональными препаратами проводится пациенткам репродуктивного возраста с неатипической гиперплазией эндометрия при наличии симптомов, факторов риска, отсутствии регресса за 6 месяцев наблюдения и при атипической гиперплазии эндометрия у женщин, планирующих беременность.
Гормональную терапию назначают не менее чем на 6 месяцев:
В качестве негормональной терапии возможно применение препаратов:
Лечение нужно сочетать с низкокалорийной диетой и достаточной физической нагрузкой согласно общему физическому развитию женщины. При необходимости врач назначает препараты, которые нормализуют метаболизм углеводов в организме: подавляют образование глюкозы клетками печени, повышают чувствительность тканей к инсулину, расщепляют сложные сахара.
Хирургическое лечение. Атипическая гиперплазия эндометрия на начальном этапе требует обязательной консультации онкогинеколога, который должен установить, нужна ли операция и в каком объёме.
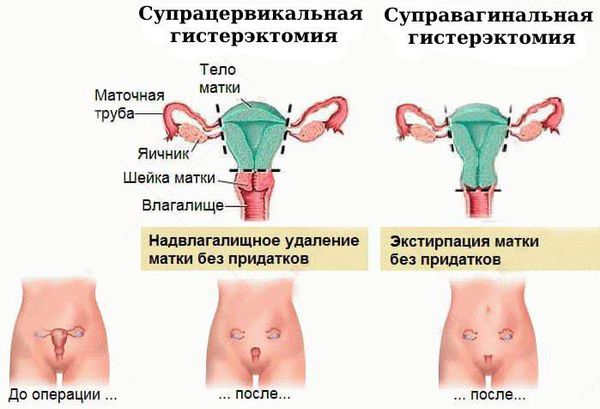
Чаще всего выполняется надвлагалищная ампутация матки — суправагинальная гистерэктомия (удаление тела и шейки матки). Вопрос о сохранении яичников решается строго индивидуально, зависит от возраста пациентки и факторов риска.
Показания к гистерэктомии:
Прогноз. Профилактика
Обследование для исключения гиперплазии или рака эндометрия показано в следующих случаях:
1. Если есть аномальные маточные кровотечения [29] [31] :
2. Если по результатам цитологического исследования соскоба шейки матки отмечается:
Профилактика: