Прижизненное патологоанатомическое исследование биопсийного материала что это
Гистологическое исследование биопсийного материала

Методика предусматривает микроскопическое изучение образца ткани, собранной из проблемной зоны больного. Получают биологический материал для ведения контрольного среза путем классического биопсии, либо во время хирургического вмешательства. Назначение процедуры проводится даже тогда, когда человек обратился к доктору по вопросам иссечения стандартной папилломы.
Зачем это нужно
Взятие материала на тестирование необходимо для решения нескольких задач. Зачастую к методу прибегают для того, чтобы подтвердить, либо опровергнуть ранее установленный предварительный диагноз. Но это не единственный случай, когда без гистологии не обойтись.
Во всех онкологических центрах ею пользуются, чтобы выяснить, на какой стадии развития находится новообразование. Также мониторинг подобного рода проводится на регулярной основе, чтобы проследить за течением патологического процесса в динамике. Без технологии не обходится на предварительной стадии планирования оперативного вмешательства для удаления ранее найденного новообразования. Итоги исследования выступают своеобразным компасом во время операции.
Также тест нужен для проведения классической дифдиагностики. Она направлена на то, чтобы точно разделить две похожие по всем признакам патологии. Особенно актуальным сравнение на микроскопическом уровне окажется при выявленных метастазах.
Заключительной популярной причиной использования меры числится определение структурного нарушения, которое образуется в тканях за весь период лечения.
Современная схема терапии в онкологических клиниках в обязательном порядке предусматривает множество аспектов комплексного восстановления. Речь идет об облучении и химиотерапии. Но ни одно лекарство онкологического спектра действия не будет назначено без получения врачом на руки результатов гистологического исследования.
Мифологический анализ позволяет с первого захода подобрать оптимальный набор препаратов и мер вспомогательного исцеления. Это означает, что человеку не придется около месяца принимать все подряд лекарства, чтобы посмотреть потом, насколько хорошо отреагировал организм на разрозненную медикаментозную поддержку. Гистология подскажет, какие лекарства окажутся наиболее действенными даже при условии, что пострадавший стал жертвой отнюдь не опухолевых процессов. Повышенным спросом подход пользуется в торакальной, абдоминальной хирургии.

Причем информационная сводка, полученная подобным образом, одинаково широко применяется для последующего лечения как мужчин, так и женщин. Речь идет о восстановлении репродуктивной системы, а также лечения шейки матки среди представительниц слабого пола и возвращения функциональности яичка среди сильных мира сего.
Как это происходит
Если у потерпевшего подтвердили опухоль, но еще не до конца разобрались с ее особенностями, то ему предписывают пройти прижизненную гистологию. Причем для лаборанта практически все равно из какой части тела будет извлечен биологический материал, лишь бы это была зона поражения и хирург смог достать достаточно поврежденных клеток.
Для осуществления задуманного привлекают несколько форматов биопсии в зависимости от текущих возможностей медиков и потребностей конкретного потребителя:
В большинстве случаев медики ограничиваются первым вариантом, так как он предусматривает получение нужного количества ткани во время иссечения, когда проводится общая операция. Не менее часто в медицинской практике встречается пункционная версия. Она характеризуется пункцией патологического очага за счет иглы, с помощью которой извлекается кусочек проблемной ткани.

Если же проблемной зоной оказалась полость, то тогда не обойтись без отсасывания со шприцом образовавшейся в полой части жидкости или вырабатываемого железой секрета.
Заключительной вариацией называют кюретаж. К нему прибегают, если приходится выскабливать потенциальный очаг поражения из органов с полостями, либо прямиком из полостей, которые образовались вследствие злокачественного процесса.
То, каким образом будет собираться биоптат, доктор решает еще на стадии предварительного обсуждения со своим подопечным. Для принятия окончательного решения в расчет берутся индивидуальные особенности организма испытуемого и предполагаемое место локализации воспаления.
Проводить контрольный срез должен только опытный врач, так как при несоблюдении правил забора материала в будущем велика вероятность получить итог с большими погрешностями. В лучшем случае сбор придется повторить, а при самом плохом раскладе онколог может вообще не заметить проблемы.
Не стоит опасаться ситуаций, когда лечащий специалист настаивает на том, что гистологию должен проводить патологоанатом. Именно он специализируется по заданному направлению исследований. Его иногда даже приглашают на саму операцию, а не только на стадию консультирования. Квалифицированный патологоанатом укажет на точное место для сбора тканевых образцов, а также заодно порекомендуют наиболее безопасный способ фиксации, подсказав точный объем клеток для замеров.
Если у потерпевшего обнаружили небольшой очаг, то тогда его отрезают целиком, а также дополнительно охватывают здоровую окружающую ткань в размере около одного сантиметра. Когда операция предусматривает удаление доброкачественного новообразования, то тогда хирургическое вмешательство подразумевает радикальную меру. Медики при подобном сценарии обязаны учитывать возможный эстетический эффект.
Иногда убрать все образование целиком не предоставляется возможным. Тогда объем нейтрализованного образца должен оказаться максимально большим, причем срезать ткани нужно там, где патология просматривается отчетливее всего. Также врач должен все время держать в голове риски травматизации желудка или любой другой изучаемой зоны. Настоящий профи постарается сделать так, что площадь здоровой части органа осталась максимально нетронутой, а произведенные действия не изменили структуру самого образца.

Еще одной важной стадией забора клеток становится корректное оформление документации. Клиницист обязан не только правильно промаркировать биоптат, но и заодно внести все необходимые в протокол сведения о типе проведенной операции, а также заполнить описание удаленной части органа.
Лаборант должен проследить за тем, чтобы инициалы пациента прописывались аккуратно вместе с адресом. На том же документе делается пометка касательно локализации патологии, связь полученного материала с окружающими:
Чтобы собранные ткани смогли успешно пережить транспортировку до исследовательского отдела, материал опускают в фиксирующий раствор. Также следует учитывать, что в первоначальном виде материал долго храниться не может из-за того, чтобы быстро подсыхает, искажая достоверность клинической картины. Первым в группу риска попали самые маленькие образцы, которые очень быстро теряют накопленную влагу.
Не все идеально, если оказывается, что образец слишком велик. Чтобы внутрь прошел формалин, медперсонал должен сделать небольшие надрезы. Вот здесь существует риск испортить заготовку из-за того, что неправильно сделанный надрез способен существенно нарушить первоначальную структуру волокон, что исказит результативность теста.
Из-за этого профи никогда не делают сквозных надрезов, а также всегда ограничиваются одним-двумя резами. По той же причине запрещено делить материал, чтобы отправить его в несколько лабораторий одновременно.
Объяснение тому – неоднородность опухолей, из-за чего срез с разных мест окажется неодинаковым по однородности. Это способно помешать корректному выбору тактики лечения.
Результаты, в зависимости от типа новообразования, обычно готовы в период от пяти дней до двух недель. Больше всего придется ждать при отправке теста на нормальность костной ткани.
Приблизительные результаты
В зависимости от того, какой формат ткани отправился на изучение, будет зависеть окончательная цена обследования. Высокая продуктивность гистологии объясняется тем, что морфология отобранного кусочка детально рассматривается под микроскопом. Это означает, что диагност может самостоятельно рассмотреть биоматериал и увидеть возможные патологические изменения без помощи УЗИ или компьютерной томографии.
Перед тем как поместить ткани под микроскоп, специалист сначала окрасит ее особенным химическим реактивом. Подобный вспомогательный этап направлен на то, чтобы лучше разграничить здоровую зону от аномалий.
Доктор, увидев результат во время увеличения размеров визуализации, сможет выявить микроскопические изменения, а также проведет анализ анатомического характера для обнаруженных изменений. Ориентировочный вердикт выносится, когда собранная информация трактуется в пользу предварительно выставленных диагнозов. При таком раскладе без вспомогательной дифдиагностики не обойтись.
Заключительное слово остается за результатами проведенной гистологии. Здесь доктор обязательно учтет итоги разных обследований, а также историю болезни из медицинской карточки, наследственную предрасположенность, текущие жалобы пациента.
Отдельно стоит учитывать, что не всегда с первого захода получается взять нужный по всем параметрам образец. Иногда лаборантам приходится оставить в покое описательный ответ. Это касается ситуаций, когда извлечено недостаточное количество биологического материала, либо при недостатке сопутствующих данных касательно характера подозреваемого недуга.
Когда биопрепарата оказалось недостаточно, либо доктор по какой-то причине умудрился срезать больше здоровой части, нежели больной, диагност выставляет в графе выводов запись о ложноотрицательном результате. Когда в том же месте есть отметка о ложноположительном результате, то расшифровка предусматривает отсутствие в направлении клинико-лабораторных данных о пациенте.
При обеих ситуациях придется все переделывать. Чтобы не допустить двойной работы, врачам следует сразу же наладить продуктивное сотрудничество с патологоанатомом.
Не менее важно следить за тем, что происходит при гистологии, назначенной с диагностической целью. Тогда в заключении указывают данные из микроскопического описания, а также прописывают нозологического заключение. В качестве шифровальной методики привлекается особая медицинская номенклатура.
Только при соблюдении правил на всех стадиях гистологии получится составить точную клиническую картину о состоянии здоровья больного. Это поможет ему в скорейшем выздоровлении оперативным или альтернативным путем.
Как проводится гистологическое исследование: виды, методы, особенности
Злокачественные новообразования — это группа заболеваний, насчитывающая несколько тысяч видов опухолей разных типов и разной степени злокачественности. Они подразделяются на большие группы в зависимости от того из каких тканей они развиваются: если из эпителиальных (барьерных) — то это раки, если из соединительных тканей (мягких тканей и костей) – саркомы, если из лимфоидных (иммунных) – лимфомы/лейкозы. От того насколько правильно верифицирована опухоль (определен ее тип, степень злокачественности и другие характеристики) зависит правильность и эффективность лечения. Важную роль в этом играют гистологические исследования.
О том, как проходят гистологические исследования, какие задачи кроме диагностических они позволяют решать, что влияет на сроки их выполнения рассказывает заведующая патологоанатомическим отделением с прозектурой НМИЦ онкологии им. Н.Н. Петрова, к.м.н. Анна Сергеевна Артемьева.
Что служит материалом для патоморфологических (гистологических) исследований?
Процесс получения фрагмента ткани (биоптата) — биопсия – это несколько разных способов забора материала для гистологического исследования.
Биопсию внутренних органов делают под УЗИ-навигацией, либо с помощью хирургического вмешательства.
Как обрабатывают эти материалы для проведения гистологического исследования?
1 Этап. Фиксация — «консервирование» биоптата в формалине — специальном химическом растворе, который предотвращает гниение, позволяет сохранить структуры ткани.
Фиксация биоптата может занимать от 6 до 24 часов – в зависимости от его вида и размера.
Операционный материал фиксируется дольше, в несколько этапов. Сначала предварительная фиксация, которая занимает примерно 12 часов. Затем вырезка нужных фрагментов и повторная фиксация еще 24 часа.
Соотношение объема материала к объему формалина должно быть 1:20.
2 Этап. Процессинг — процесс обезвоживания, обезжиривания и пропитки материала парафином. Автомат перемещает кусочек материала из раствора в раствор.
В качестве растворов применяются: абсолютированный изопропиловый спирт (6-8 смен), ксилол (2 смены), расплавленный парафин (2 смены).
Программа разнится для «жирного» материала (к которым относятся, например, ткани молочной железы) и «нежирного» – 36 и 24 часа соответственно.
Процесс получения парафиновых блоков.
3 Этап. Изготовление парафинового блока. Кусок материала помещается в форму с расплавленным парафином (уже другим нежели во время процессинга – с более высокой температурой плавления) и охлаждается. Выполняется вручную, сложно ускорить.
4 Этап. Изготовление срезов. Толщина образца — кусочка ткани, залитого в парафин – 1-3 мм. Толщина каждого среза 4-5 мкм (0,004-0,005 мм). Выполняет лаборант с использованием специального инструмента – микротома.
Срезы монтируются на стекла и должны высохнуть.
Несмотря на то, что часть материала теряется при выравнивании в микротоме, при должном профессионализме, из одного образца — материала от одной биопсии, операционного материала от одной опухоли, возможно изготовить около 100 стекол (микропрепаратов).
Для чего делаются срезы?
Срезы делаются для рутинной окраски гематоксилинном и эозином, иммуногистохимического исследования и других видов исследований.
Срезы для всех исследований используются одинаковые, различается окраска, могут отличаться стекла, на которые они монтируются, так для ИГХ и FISH нужны специальные адгезивные стекла или заряженные стекла.
Блоки и стекла способны храниться долгие годы и использоваться для проведения дополнительных гистологических исследований, пересмотров, а также в научных целях.
Архив гистологических материалов собирается в НМИЦ онкологии им. Н.Н. Петрова с 1927 года и содержит более 10 млн единиц хранения (микропрепараты — стекла, парафиновые блоки, архивные карточки, влажный архив).
Какие виды гистологических исследований наиболее информативны?
Что позволяют определить разные виды гистологических исследований
Гистологическое исследование – что это такое?
Позволяет верифицировать опухоль – то есть определить из каких клеток она состоит (из какой ткани она развивается), степень ее дифференцировки (зрелости).
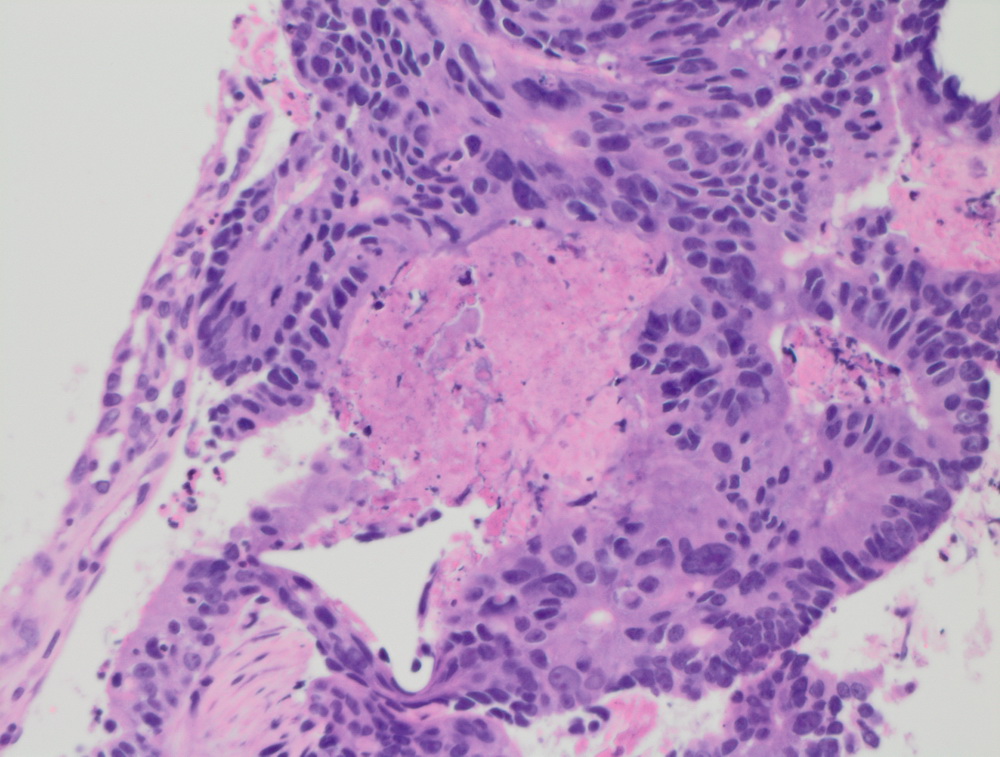
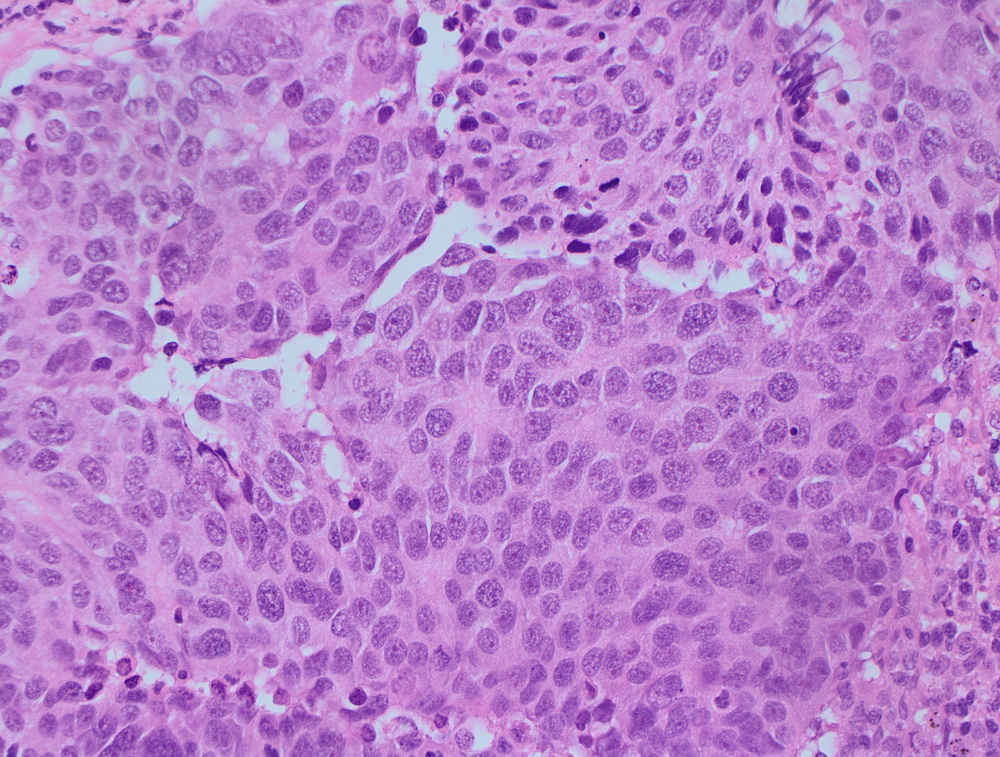
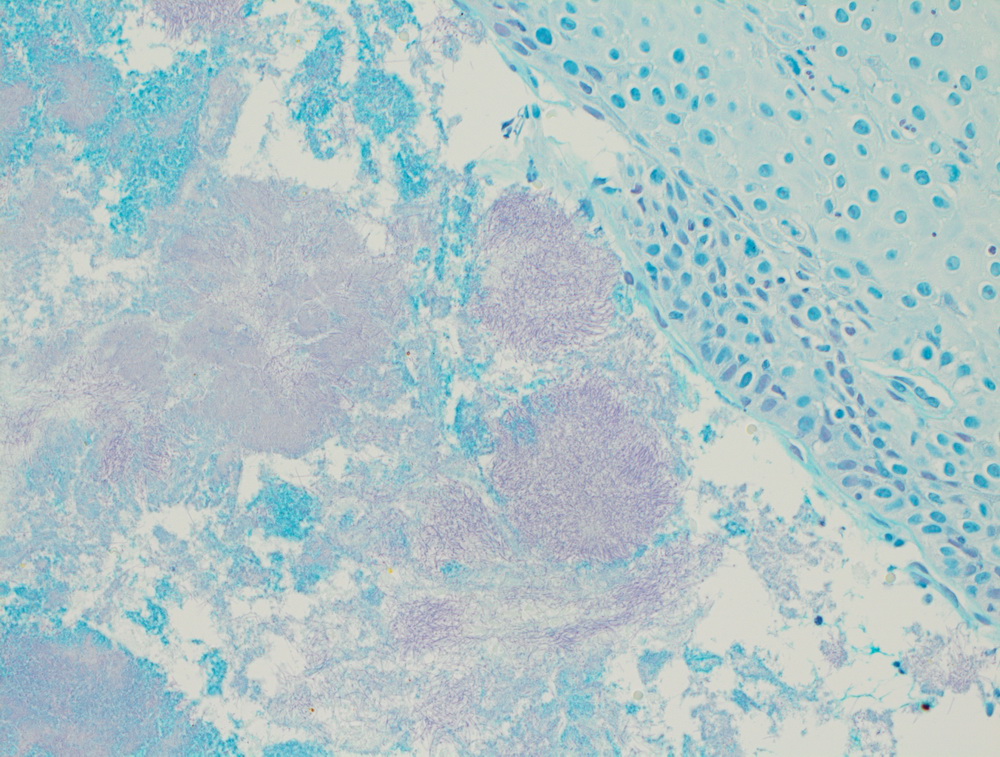
Рутинная окраска, выполняющаяся при гистологическом исследовании, позволяет выявить патологический процесс в анализируемом материале (биоптате, операционном материале):
Также, в большинстве случаев, благодаря рутинной окраске, можно определить степень злокачественности опухоли и, если она достаточно зрелая, то какова ее природа.
Окрашенные срезы под микроскопом
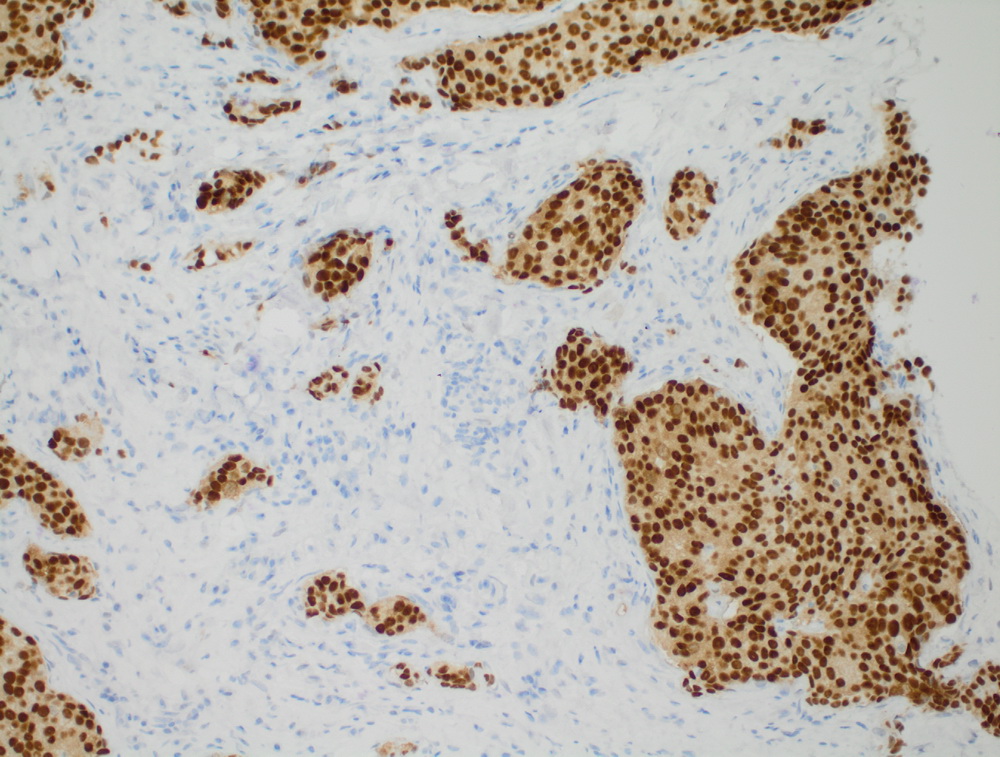 |
Инвазивный протоковый рак er 100%.
Карцинома сигмовидной кишки.
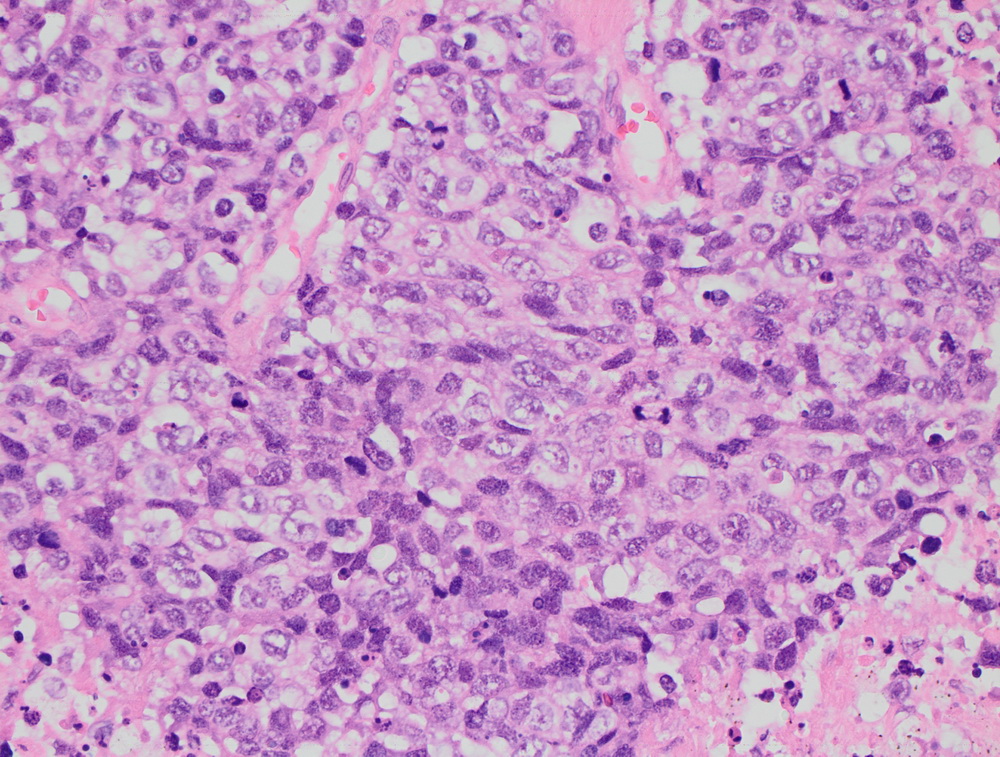
Крупноклеточная нейроэндокринная опухоль.
МТС крупноклеточной нейроэндокринной опухоли.
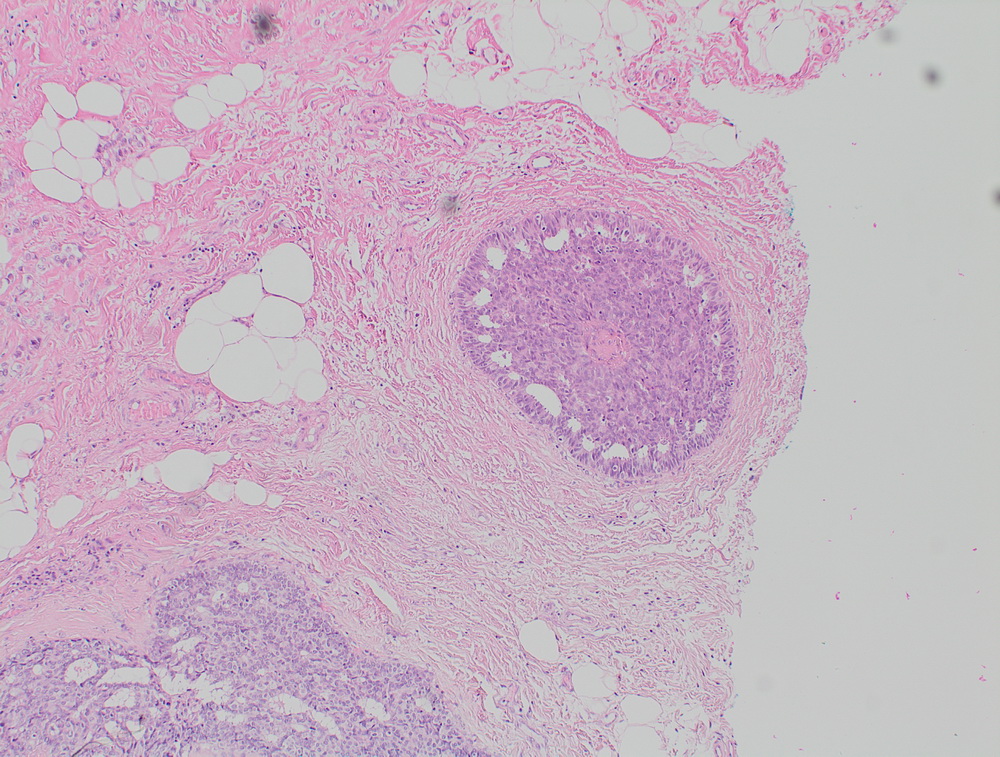
Неспецифический рак молочной железы. Участок in situ карциномы внутри протока, криброзного типа.
Низкодифферинцированный рак пищевода.
При гистологическом исследовании биоптата и операционного материала можно оценить распространенность: размер опухоли и прорастание в окружающие ткани, насколько затронуты лимфоузлы и есть ли метастазы в отдаленные органы (если эти все структуры присланы для гистологического исследования). При консультации готовых микропрепаратов – стекол, это, как правило, невозможно, если опухоль больше размеров гистологической кассеты или рассечена предыдущим исследователем и не предоставлены данные макроскопического исследования.
Во время гистологического исследования изучаются все стекла от одного образца – материала, полученного от одного вмешательства — одной операции или одной биопсии, вне зависимости от их количества, это считается одной консультацией.
Сроки выполнения гистологического исследования зависят от количества микропрепаратов и от категории сложности того процесса, который в них обнаруживается, сроки могут удлиняться, особенно при необходимости использования дополнительных методов исследования и анализа дополнительных сведений. На сроки выполнения гистологического исследования влияет полнота предоставленной пациентом клинической информации, в том числе данных уже проведенных исследований.
Иммуногистохимия (ИГХ)
Сложное многоэтапное исследование, выполняется после гистологического исследования на том же материале. Опухолевые срезы окрашиваются антителами, которые способны связываться антигенами (белками), которые несут опухолевые клетки. Разные опухолевые клетки несут разные антигены, к каждому из которых подобно ключа к замку подходит антитело.
Один из этапов ИГХ
ИГХ исследование — это комбинаторика. 100% специфичных и чувствительных к какой-то опухоли маркеров не существует, но есть набор антигенов, которые в определенном типе опухоль должны быть и набор тех, которых там быть не должно, таким образом ИГХ-панель строится так чтобы включать несколько антител, которые должны быть позитивны и несколько, которые должны быть негативны. Для разных опухолей различаются эти наборы позитивных/негативных маркеров.
При проведении прогностической ИГХ – выявлении маркеров чувствительности к терапии определяется набор таких маркеров для конкретных опухолей, например, рака молочной железы: рецепторы стероидных гормонов (эстроген, прогестерон), рецептор эпидермального фактора роста (HER2) и индекс пролиферативной активности Ki67 (скорости деления клеток).
Стекла окрашиваются последовательно — различными антителами красятся наборы маркеров в несколько этапов, процесс окраски стекол одним антителом занимает 48 часов.
Таким образом, каждое антитело наносится на отдельный срез ткани, монтированный на отдельное стекло, как правило с соответствующим внешним контролем, количество реакций (используемых антител) и этапов окраски может существенно варьировать в зависимости от конкретной диагностической ситуации, все зависит от индивидуальных особенностей опухоли. Проводится такое количество окрасок, которое необходимо для того, чтобы выявить наиболее характерный для определенной опухоли набор позитивных и негативных маркеров.
Кому-то для этого будет достаточно 5 антител, а кому-то необходимо сделать 20 окрасок и более. Максимальное количество окрасок, которое нам приходилось делать – 212.
Поэтому точные сроки и стоимость этого исследования невозможно определить заранее. Разные по течению и прогнозу опухоли могут быть очень похожи друг на друга, только минимальные различия в окрашивании, с учетом клинических данных и данных других методов обследования, могут позволить установить верный диагноз.
Есть целый ряд доброкачественных опухолей, симулирующих злокачественные, в том числе высокоагрессивные, а некоторые злокачественные высоко дифференцированные опухоли трудно отличить от воспалительных и реактивных процессов. В таких ситуациях только опыт и квалификация патоморфолога, анализ всего комплекса доступной информации (снимки КТ, МРТ, рентген, протокол операции, и др.) позволяют поставить диагноз.
В грамотной интерпретации результатов ИГХ очень важна роль эксперта, ведь те случаи, с которыми приходится работать, в большинстве своем, сложные. Практически не существует антител, которые могут выступать в качестве 100%-х маркеров той или иной опухоли, врачу всегда приходится взвешивать различные вероятности.
Что определяется с помощью ИГХ?
Иммуногистохимия позволяет оценить потенциальный темп роста опухоли, ответ на химио-, таргетную, гормональную терапию.
Флуоресцентная гибридизация in situ (FISH-тест)
Это метод молекулярно-генетической диагностики в ткани.
FISH проводится в срезе ткани и позволяет привязать генетическую перестройку к конкретной опухолевой клетке.
В этом тесте также используются специальные красители, которые связываются только с определенными участками хромосом. Их называют зондами, которые могут быть помечены флуоресцентным или хромогенным красителем, визуализирующимися при помощи флуоресцентного или светового микроскопа.
Технические операции по подготовке гистологических стекол к этому исследованию занимает 2 рабочих дня.
Анализ препарата с помощью многоголового микроскопа.
Полученные микропрепараты очень чувствительны к внешней среде – они могут выцвести со временем, чтобы избежать потерь информации все FISH-препараты сканируются, создается их цифровая копия, которая доступна для внешнего пересмотра. Специалисты просматривают флуоресцирующий материал в темном поле, в анализе препарата принимают участие как минимум 2 специалиста. При необходимости используется и цифровой анализ.
Что определяется с помощью FISH-теста?
FISH-тест позволят диагностировать некоторые виды опухолей, определяет целесообразность использования некоторых химиотерапевтических препаратов.
Проведение гистологического исследования, и в первую очередь FISH-теста — это экспертная работа, которая зависит от квалификации специалиста. Очень многие мутации, которые выявляются в опухолях, не всегда являются метками опухолей, они могут находиться и в доброкачественных образованиях или нормальных тканях.
За год патологоанатомическое отделение НМИЦ онкологии имени Н.Н. Петрова выполняет около 20000 гистологических исследований (пациентов), из них около 5000 консультативных случаев (пересмотров), более 30000 ИГХ исследований, а также участвует в программе внешнего контроля качества ИГХ исследований NordIQ.
Специалисты отделения обладают огромным опытом проведения гистологических исследований и экспертными компетенциями.
Скорость выполнения гистологических исследований и адекватность гистологического заключения зависят от ряда факторов:
После выполнения гистологического исследования пациент получает гистологическое заключение/протокол исследования гистологического материала.
Расшифровка гистологического исследования: на что обратить внимание?
Гистологическое заключение включает в себя несколько рубрик (полей):
Макроскопическое описание
Заполняется как для биоптатов — не обязательно, так и для операционного материала, для которого имеет крайне важное значение в ряде случаев.
Микроскопическое описание
Описание изменений на микроскопическом уровне, не обязательно к заполнению, так как вся необходимая информация может быть отражена в поле «заключение».
Результаты иммуногистохимического исследования
В этом поле описано какие антитела использовались в данном случае и каков результат окрашивания: наличие окрашивание или его отсутствие, локализация в клетке при необходимости, а также процент позитивных клеток и интенсивность реакции, когда это имеет значение.
Патологоанатомическое заключение
Содержит нозологическую/классификационную единицу, если ее возможно установить по исследованному материалу, то есть дает ответы на вопросы:
Также приводятся все необходимые прогностические данные: степень дифференцировки, параметры, влияющие на стадию, состояние краев резекции, если возможно их оценить и т.п.
Дополнительные замечания и рекомендации
Поле может содержать комментарии, относительно возможного направления дальнейшего обследования, вероятности того или иного диагноза, необходимости ознакомиться с теми или иными клиническими данными и др.
Мы не рекомендуем пациентам самостоятельно заниматься расшифровкой показателей гистологического исследования, используя информацию, полученную на различных Интернет-сайтах и форумах пациентов, так как на интерпретацию данных влияет большое количество факторов, в том числе, возраст пациента, данные других исследований и др.
Расшифровкой исследования может заниматься только специалист – врач онколог по профилю заболевания!
Авторская публикация:
АРТЕМЬЕВА АННА СЕРГЕЕВНА
заведующий патологоанатомического отделения с прозектурой ФГБУ «НМИЦ онкологии им. Н.Н. Петрова» Минздрава России, кандидат медицинских наук