Основные свойства ртути и температура плавления
Температура плавления ртути характеризует момент перехода металла из твердого состояния в жидкость. Свойства живого серебра (argentum vivum в переводе с латинского) расширяют границы применения металла в разных сферах производства с учетом мер безопасности, связанных с его использованием.
Распространенность в природе
В земной коре концентрация химического элемента низкая. Ртутные рудные минералы содержат до 2,5% живого серебра. Это отличает их от других пород. В основном меркурий находится в рассеянной форме, и лишь часть находится в месторождениях.
В магматических породах долевое содержание живого серебра равно между собой, а в осадочных толщах крупные концентрации металла сосредоточены в глинистых минералах. Воды Мирового океана содержат 0,1 мкг/л меркурия.
Высокая степень ионизации определяет особенности металла:
Химический элемент присутствует в составе сульфидных минералов (сфалерит, реальгар). Этот металл является индикатором месторождений ртути и скрытых рудных тел. В поверхностных условиях живое серебро и киноварь не растворяются в воде, но при наличии серной кислоты, озона способствует увеличению показателя растворимости минералов.
Меркурий обладает отличными сорбционными свойствами. В природе существует около 20 минералов, содержащих этот металл, но промышленная добыча производится на месторождениях киновари.
Одно из крупнейших месторождений находится в Испании. Технология производства металла предусматривает обжиг киновари с последующей конденсацией и сбором паров ртути.
Физические и химические свойства живого серебра
Ртуть (меркурий) имеет уникальные химические и физические особенности, что позволяет ее применять в различных сферах. Но в то же время ее испарения опасны для человека. Как уже упоминалось, ее называют живым серебром, она по цвету напоминает лунный металл.
Меркурий обладает переходными свойствами, при комнатной температуре он остается в жидком состоянии. Живое серебро легко образует с другими материалами твердые и жидкие сплавы (амальгамы). Наиболее популярными являются соединения золота и серебра.
Химический элемент является диамагнетиком, и в случае необходимости собрать его магнитом невозможно. Он неплохо проводит ток, поэтому в свое время его применяли при изготовлении реле и выключателей.
Плотность живого серебра при нормальных условиях составляет 13,5 г/см³. Этот химический элемент обладает устойчивостью в сухом воздухе, окисляется только при нагревании выше +300°C. После длительного хранения на открытом воздухе на поверхности образуется пленка из оксидов компонентов, содержащихся в основном материале в качестве примесей.
При нагревании вступает в реакцию с кислородом, образуя оксид красного цвета. Металл малоактивный, не реагирует с растворами кислот, но растворяется в царской водке. При нагревании в серной кислоте образует сульфат ртути.
Сферы использования живого серебра
Ртуть применяется для изготовления точных измерительных приборов для определения температуры и давления. Сегодня в электрохимическом производстве широко используются ртутные выпрямители тока.
В медицинской отрасли для проведения профилактических работ в качестве источников ультрафиолетового спектра применяются ртутные (газоразрядные) лампы, всем известные градусники для измерения температуры тела содержат этот химический элемент.
В связи с тем, что меркурий токсичен, его не используют для изготовления медицинских препаратов. Хотя до середины 70-х годов ее активно применяли для производства мази от педикулеза.
Измерительные приборы для низкотемпературных условий содержат амальгаму таллия, которая в отличие от чистой ртути застывает при температуре – 60°C. Сочетание 2 токсичных металлов значительно расширяет границы использования.
За рубежом кипящую ртуть используют в качестве охладителя. Ее преимущество поддерживать постоянную температуру позволяет интенсивно отводить тепло от пространства катализатора. Для увеличения коэффициента отдачи в ртуть добавляют натрий для образования амальгамы.
С целью размягчения кадмия, олова и серебра меркурий используют в стоматологии при изготовлении пломб. Раньше ее применяли для золочения деталей часов и ювелирных изделий, а амальгамы золота и серебра использовались при производстве зеркал.
Живое серебро применяется в качестве катода для извлечения ряда активных компонентов электролитическим путем, а также для переработки вторичного алюминия.
Существуют технологии извлечения золота из россыпей с использованием свойства химического элемента образовывать амальгаму с благородным металлом. Этот метод был широко распространен в Индии, где в местах предполагаемого скопления золота проделывали специальные углубления, в которые заливали металлическую ртуть. Через некоторое время вытаскивали амальгаму, и путем выпаривания извлекали золото.
В нефтеперерабатывающей промышленности для регулировки температурных процессов используют пары ртути. В сельском хозяйстве ее используют для подготовки семян к посеву.
С давних времен и сегодня соли меркурия используют при изготовлении фетра, дублении кожи в качестве катализатора органического синтеза.
В прошлом ртуть не считалась вредным веществом, ее применяли для исцеления от недугов. В Средневековье алхимики использовали меркурий в поисках философского камня и превращения ее в золото.
Ртуть опасна для человека, она токсична и даже в ничтожных концентрациях плохо влияет на иммунную систему, почки, глаза, кожу и пищеварительный тракт.
Кипение и плавление металла
Технология физико-химических исследований при условиях высоких температур рассматривает давление плавления металла при разных температурах. Точность опытов обеспечивает применение на практике свойств химического элемента № 80.
Для измерения температуры выше +360°C пользуются термопарами или специальными термометрами, в которых пространство надо ртутью заполнено газом. С целью повышения температуры кипения металла в капилляр надо ртутью закачивают азот. При давлении 30 атмосфер температурный градиент увеличивается до +600°C.
Такого типа термометры требуют постепенного нагрева. Нижним пределом такого измерительного прибора является температура перехода живого серебра в твердое состояние.
Теплоемкость металла с увеличением температуры последовательно уменьшается и после определенного порога температурного градиента начинает медленно расти. Это свойство и жидкое состояние роднит ртуть с водой.
О ртути
Ртуть: общие понятия
Консультация оперативного дежурного: +7(812)309-13-43
Химические свойства ртути
Ртуть – единственный из всех существующих в природе металлов, который остается жидким при комнатной температуре. В этих условиях на воздухе она не окисляется, в воде и щелочах не растворяется. Растворяется в холодной азотной кислоте и нагретой концентрированной серной. В обычных условиях активно испаряется, и скорость этого процесса прямо пропорциональна температуре и площади поверхности испарения. Пары ртути не имеют ни запаха, ни цвета, обнаружить их в воздухе можно только с помощью специальных приборов
Физические свойства ртути
Для ртути характерны низкая вязкость и высокое поверхностное натяжение. Эти свойства становятся причиной двух негативных с точки зрения ртутного загрязнения среды процессов:
Пары ртути отличает очень высокая летучесть, и слой воды или иной жидкости не представляет для них реальной преграды. То же самое можно сказать и о многих строительных материалах, таких как бетон, кирпич, лакокрасочное покрытие, линолеум или плитка. Ртутные пары равномерно пропитывают их на всю толщину, а также легко сорбируются из воздуха деревом, коврами и тканями. При повышении температуры или при механическом воздействии происходит обратная десорбция ртути в воздух помещения.
Чистая металлическая ртуть хорошо растворяет многие металлы, снижая тем самым прочность металлических конструкций, и образует непрочные соединения как с неорганическими, так и с органическими веществами.
Воздействие ртути на человека и животных
Основные пути попадания ртути в организм – это вдыхание ее паров с воздухом либо употребление с пищей или водой. Организм человека выводит не более 20% попавшей в него ртути, и она накапливается в почках и мозге, поражает плод, если женщина беременна, содержится в крови и грудном молоке. При концентрации паров ртути более 0,1 мг/м3 наступает острое отравление, признаки которого:
Следствием длительного воздействия малых доз ртути является хроническое отравление, которое может проявиться с задержкой на несколько лет. Все это время в организме накапливаются необратимые нарушения с такими внешними признаками:
Мнение эксперта:
Алена Парецкая, врач — педиатр
Пролитая ртуть: как с ней бороться
Существуют как природные (месторождения), так и техногенные (места добычи, горнорудные и предприятия цветной металлургии, специальные полигоны-хранилища, отходы сжигания нефтепродуктов и т. д.) источники ртути, загрязняющей воздух, воду и почву. Бытовые и производственные помещения загрязняются ртутью при неправильной эксплуатации ртутных приборов и устройств, таких как термометры, манометры, выпрямители электрического тока. Статистика утверждает, что 80% всех работ МЧС в Санкт-Петербурге источники паров ртути. Если не принимать во внимание злоумышленные проливы ртути, то наиболее частая причина их существования – разбитый ртутный термометр и преступно халатное отношение к последствиям этого события
Ликвидация розлива ртути: +7(812)309-13-43
ОЧЕНЬ ВАЖНО!
Если у Вас в семье есть ребёнок, заранее объясните ему, что если он нечаянно
разобьёт термометр, его никто не будет за это ругать. В противном случае ваше чадо, испугавшись наказания за разбитый градусник, спрячет его остатки куда-нибудь под кровать или шкаф и ничего Вам не скажет – в итоге вся Ваша семья долгое время будет дышать ядовитыми парами ртути.
При прохождении теста нужно помнить: Предельно допустимая концентрация ртути 300нг/м3
Ртуть
(молярная масса)
(первый электрон)
Содержание
История
Ртуть известна с древних времён. Нередко её находили в самородном виде (жидкие капли на горных породах), но чаще получали обжигом природной киновари. Древние греки и римляне использовали ртуть для очистки золота (амальгамирование), знали о токсичности самой ртути и её соединений, в частности сулемы. Много веков алхимики считали ртуть главной составной частью всех металлов и полагали, что если жидкой ртути возвратить твёрдость при помощи серы или мышьяка, то получится золото. Выделение ртути в чистом виде было описано шведским химиком Георгом Брандтом в 1735 году. Для представления элемента как у алхимиков, так и в настоящее время используется символ планеты Меркурий. Но принадлежность ртути к металлам была доказана только трудами Ломоносова и Брауна, которые в декабре 1759 года смогли заморозить ртуть и установить её металлические свойства в твёрдом состоянии: ковкость, электропроводность и др.
Происхождение названия
Нахождение в природе
Ртуть — относительно редкий элемент в земной коре со средней концентрацией 83 мг/т. Однако ввиду того, что ртуть слабо связывается химически с наиболее распространёнными в земной коре элементами, ртутные руды могут быть очень концентрированными по сравнению с обычными породами. Наиболее богатые ртутью руды содержат до 2,5 % ртути. Основная форма нахождения ртути в природе — рассеянная, и только 0,02 % её заключено в месторождениях. Содержание ртути в различных типах изверженных пород близки между собой (около 100 мг/т). Из осадочных пород максимальные концентрации ртути установлены в глинистых сланцах (до 200 мг/т). В водах Мирового океана содержание ртути — 0,1 мкг/л. Важнейшей геохимической особенностью ртути является то, что среди других халькофильных элементов она обладает самым высоким потенциалом ионизации. Это определяет такие свойства ртути, как способность восстанавливаться до атомарной формы (самородной ртути), значительную химическую стойкость к кислороду и кислотам.
Ртуть присутствует в большинстве сульфидных минералов. Особенно высокие её содержания (до тысячных и сотых долей процента) устанавливаются в блёклых рудах, антимонитах, сфалеритах и реальгарах. Близость ионных радиусов двухвалентной ртути и кальция, одновалентной ртути и бария определяет их изоморфизм во флюоритах и баритах. В киновари и метациннабарите сера иногда замещается селеном или теллуром; содержание селена часто составляет сотые и десятые доли процента. Известны крайне редкие селениды ртути — тиманит (HgSe) и онофрит (смесь тиманита и сфалерита).
Ртуть является одним из наиболее чувствительных индикаторов скрытого оруденения не только ртутных, но и различных сульфидных месторождений, поэтому ореолы ртути обычно выявляются над всеми скрытыми сульфидными залежами и вдоль дорудных разрывных нарушений. Эта особенность, а также незначительное содержание ртути в породах, объясняются высокой упругостью паров ртути, возрастающей с увеличением температуры и определяющей высокую миграцию этого элемента в газовой фазе.
В обычных условиях киноварь и металлическая ртуть не растворимы в воде, но в присутствии некоторых веществ (Fe2(SO4)3, озон, пероксид водорода) растворимость в воде этих минералов достигает десятков мг/л. Особенно хорошо растворяется ртуть в сульфидах щелочных металлов с образованием, например, комплекса HgS•nNa2S. Ртуть легко сорбируется глинами, гидроксидами железа и марганца, глинистыми сланцами и углями.
В природе известно около 20 минералов ртути, но главное промышленное значение имеет киноварь HgS (86,2 % Hg). В редких случаях предметом добычи является самородная ртуть, метациннабарит HgS и блёклая руда — шватцит (до 17 % Hg). На единственном месторождении Гуитцуко (Мексика) главным рудным минералом является ливингстонит HgSb4S7. В зоне окисления ртутных месторождений образуются вторичные минералы ртути. К ним относятся, прежде всего, самородная ртуть, реже метациннабарит, отличающиеся от таких же первичных минералов большей чистотой состава. Относительно распространена каломель Hg2Cl2. На месторождении Терлингуа (Техас) распространены и другие гипергенные галоидные соединения — терлингуаит Hg2ClO, эглестонит Hg4Cl.
Месторождения
Ртуть считается редким металлом.
Одно из крупнейших в мире ртутных месторождений находится в Испании (Альмаден). Известны месторождения ртути на Кавказе (Дагестан, Армения), в Таджикистане, Словении, Киргизии (Хайдаркан — Айдаркен), Донбассе (Горловка, Никитовский ртутный комбинат).
В России находятся 23 месторождения ртути, промышленные запасы составляют 15,6 тыс. тонн (на 2002 год), из них крупнейшие разведаны на Чукотке — Западно-Палянское и Тамватнейское.
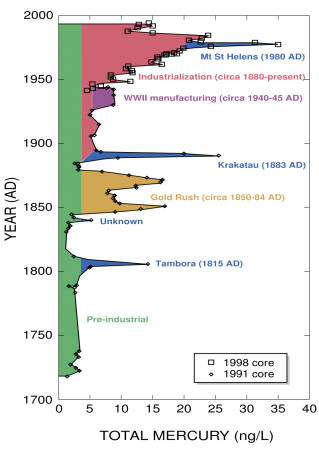
В окружающей среде
До индустриальной революции осаждение ртути из атмосферы составляло около 4 нанограммов на 1 кубический дециметр льда. Природные источники, такие, как вулканы, составляют примерно половину всех выбросов атмосферной ртути. Причиной появления остальной половины является деятельность человека. В ней основную долю составляют выбросы в результате сгорания угля (главным образом в тепловых электростанциях) — 65 %, добыча золота — 11 %, выплавка цветных металлов — 6,8 %, производство цемента — 6,4 %, утилизация мусора — 3 %, производство соды — 3 %, чугуна и стали — 1,4 %, ртути (в основном для батареек) — 1,1 %, остальное — 2 %.
Одно из тяжелейших загрязнений ртутью в истории случилось в японском городе Минамата в 1956 году, что привело к более чем трём тысячам жертв, которые либо умерли, либо сильно пострадали от болезни Минамата.
Изотопы
Природная ртуть состоит из смеси 7 стабильных изотопов: 196 Hg (распространённость 0,155 %), 198 Hg (10,04 %), 199 Hg (16,94 %), 200 Hg (23,14 %), 201 Hg (13,17 %), 202 Hg (29,74 %), 204 Hg (6,82 %). Искусственным путём получены радиоактивные изотопы ртути с массовыми числами 171—210.
Получение
Ртуть получают обжигом киновари (сульфида ртути II) или металлотермическим методом:
HgS + O2 ⟶ Hg + SO2↑ HgS + Fe ⟶ FeS↓ + Hg
Пары ртути конденсируют и собирают. Этот способ применяли ещё алхимики древности.
На протяжении многих столетий в Европе основным и единственным месторождением ртути был Альмаден в Испании. В Новое время с ним стала конкурировать Идрия во владениях Габсбургов (современная Словения). Там же появилась первая лечебница для поражённых отравлением парами ртути рудокопов. В 2012 г. ЮНЕСКО объявило промышленную инфраструктуру Альмадена и Идрии памятником Всемирного наследия человечества.
В надписях во дворце древнеперсидских царей Ахеменидов (VI—IV века до н. э.) в Сузах упоминается, что ртутную киноварь доставляли сюда с Зеравшанских гор и использовали в качестве краски.
Физико-химические свойства ртути
Необходимость специальной утилизации оборудования, содержащего ртуть или ее соединения, вызвана высокой токсичностью этих веществ. Острое отравление некоторыми из них грозит летальным исходом. Высокая токсичность, в свою очередь, обусловлена физическими и химическими свойствами этого элемента.
Физические свойства ртути
Данный металл обладает следующими физическими характеристиками:
Химические свойства ртути
Конфигурация электронной оболочки атома ртути обеспечивает ей два варианта валентности: образование одной или двух химических связей. Это соответствует степеням окисления +1 и +2. Более продуктивен второй вариант.
Чистый металл малоактивен, но все же двухвалентная ртуть образует минеральные соединения: хлорид HgCl, цианид Hg(CN)2, сульфид HgS, оксид HgO. Среди органических веществ – катион метилртути [CH3Hg]+, мертиолят (тиомерсал), меркузал, промеран.
Металл растворяется в царской водке – смеси азотной и соляной кислот, а также в концентрированной серной или азотной кислоте с образование сульфата HgSO4 и нитрата Hg(NO3)2 или Hg2(NO3)2 соответственно.
Ртуть образует множество минеральных и органических соединений. При нормальных условиях она находится в жидком состоянии и постоянно испаряется в атмосферу. Такое многообразие форм требует различных методов и подходов в демеркуризации и обработке отходов. От этих факторов зависит цена утилизации ртутьсодержащих ламп.
Что будет если ртуть нагреть
Справочник химика 21
Химия и химическая технология
Нагревание ртутью
При нагревании ртуть, расширяясь, поднимается из резервуара по капилляру вверх до определенного уровня. Высота, на которую поднялась ртуть, или, как говорят, высота столбика ртути, показывает температуру измеряемого тела. [c.167]
Способы добычи. Золото добывают промывкой измельченной горной породы (причем оно, как имеющее большую плотность, остается на дне, а пустая порода удаляется сильной струей воды) или растворением в ртути, с которой золото, как отмечалось выше, дает амальгаму. Затем нагреванием ртуть отгоняют, и золото сплавляют в слитки. Однако этот способ может быть применен лишь в тех случаях, когда золото находится в не слишком раздробленном состоянии. [c.410]
Цинк и кадмий устойчивы к коррозии из-за образования на их поверхности плотных пленок оксидов МеО, а при нагревании ртути на ее поверхности появляется налет красного цвета [c.431]
При нагревании ртуть улетучивается (отличие от аналогичной реак-Щ1И с солями серебра). [c.358]
Окись ртути НдО образуется в виде желтого осадка при добавле НИИ основания к раствору нитрата ртути(II) или в виде красного по рошка при нагревании сухого нитрата ртути (II) окись ртути медленно образуется и при нагревании ртути на воздухе. Желтая и красная формы различаются, кажется, только тем, что имеют зерна разных размеров вообще красные кристаллы [например, бихромата калия или гексацианоферрата (III) калия] при измельчении дают желтый порошок. При сильном нагревании окись ртути разлагается с выделением кислорода. [c.572]
При нагревании ртути амидохлорида со щелочью выделяется желтый оксид ртути и ощущается запах аммиака. [c.130]
Затем через кран 5 производят возможно полную откачку воздуха из всего прибора (можно обойтись и водоструйным насосом). При откачке ртуть из сосуда 7 поднимется по трубке 4, а из сосуда 2 по трубке / и заполнит часть сосуда 3. Необходимо все время смотреть, чтобы ртуть из сосуда 6 не перелилась через открытый конец трубки 4. По мере нагревания ртути ее пары будут оседать на внутренней поверхности трубки 4 в той ее части, которая проходит внутри трубки 1, служащей как бы холодильником. Постепенно капельки ртути начнут падать в капиллярную часть трубки 4. [c.33]
Извлечение нз породы амальгамным способом. Процесс основан на способности ртути растворять золото с образованием амальгамы при нагревании ртуть легко отгоняется, а золото остается. [c.398]
Нагревание ртути должно проводиться на специальных печах, конструкция которых исключает наличие горизонтальных нагреваемых при включении печи поверхностей. Под нагревательным прибором должен находиться поддон с листовым асбестом или фарфоровый сосуд, куда ртуть должна попадать при [c.171]
Нагревание ртутью и жидки-ши металлами. Ртуть как теплоноситель используется в некоторы [c.293]
Нагревание ртутью и жидкими металлами. Ртуть применяется как теплоноситель в некоторых промышленных установках, главным образом теплосиловых. Ртуть термически стойка, негорюча, обладае т высокой температурой кипения ( 327°) и низкой упругостью паров. Скрытая теплота конденсации ее невелика (70,7 ккал/кг), но зато удельный вес [c.340]
Аппаратуру с открытыми поверхностями ртути размещают, как правило, в вытяжных шкафах, с отсосом воздуха не только сверху, но и снизу. Скорость движения воздуха при всех открытых створках шкафа во время работ, не связанных с нагревом ртути, должна быть не менее 0,5 м/сек, а при нагревании ртути — не менее 1 м/сек. [c.719]
При длительном нагревании ртути до температуры, близкой к температуре ее кипения, образуется яркокрасная окись ртути HgO. При более сильном нагревании окись ртути разлагается на ртуть и кислород. При очень тонком измельчении красной окиси ртути цвет ее становится желтым. Подобная же желтая форма окиси ртути образуется при получении ее путем химических взаимодействий в растворах. Разница между красной и желтой модификациями окиси ртути заключается лишь в величине отдельных зерен вещества. В воде окись ртути почти нерастворима в 100 мл воды растворяется лишь 0,005 г HgO. Окись ртути — основной окисел. С кислотами реагирует, образуя соответствующие соли ртути. В щелочах не растворяется. [c.276]
Нормальное давление определяется по показаниям стандартного барометра. В стандартном барометре принимается во внимание то, что гравитационное притяжение ртути Землей мало изменяется в зависимости от места и что при нагревании ртуть расширяется и становится менее плотной. Так, столб ртути в барометре при 20° С на несколько миллиметров выше, чем при 0° С. В стандартном барометре ртуть находится при 0 С. По опубликованным таблицам можно рассчитать, насколько различаются показания обычного и стандартного барометров. Поправка редко превышает 1—2 мм рт. ст. и часто пренебрежимо мала по сравнению с другими возможными ошибками. Если другие ваши измерения недостаточно точны, не следует вносить поправку в показания обычного барометра. [c.81]
Наибольшее распространение имеют стеклянные ртутные термометры. Такой термометр состоит из небольшого стеклянного сосуда, соединенного с запаянной вверху стеклянной капиллярной трубкой. К трубке термометра прикреплена шкала. Капилляр со шкалой заключены в стеклянную трубку. При нагревании ртуть расширяется и поднимается в капилляре. По степени подъема ртути судят о температуре среды, куда помешен сосуде ртутью. [c.369]
Сульфиды. Цинк и кадмий взаимодействуют с серой при нагревании, ртуть — в обычных условиях. Сульфиды Э5 можно получить также по реакции обмена. Сульфид цинка 2л5 белого цвета, сульфид кадмия d5 eлтoгo, а HgS черного. При нагревании без доступа воздуха черный сульфид ртути превращается в красный. [c.423]
Процессы и аппараты химической технологии (1955) — [ c.315 ]
Химическая термодинамика (1950) — [ c.424 ]
Процессы и аппараты химической технологии Издание 3 (1966) — [ c.414 ]
Процессы и аппараты химической технологии Издание 5 (0) — [ c.414 ]
Большая Энциклопедия Нефти и Газа
Нагревание — ртуть
Коэффициент объемного расширения ртути равен р1 82 — 10 — 4 град-1. Найти коэффициент сжатия для нее, если известно, что, для того чтобы при нагревании ртути на 1 ее объем не изменился, необходимо увеличить внешнее давление на 47 атм. [31]
Убежденный сторонник учения о флогистоне, он рассматривал оксид ртути как простое вещество, образованное при нагревании ртути в воздухе и, следовательно, лишенное флогистона. Поэтому выделение дефлогистированного воздуха из HgO при нагревании казалось ему просто невозможным. Вот почему он был так далек от понимания того, что в действительности получил. [32]
Далее Блэк излагает и объясняет опыты Мартина — Рихмана. Мы должны только предположить, что равные количества теплоты сообщаются обеим жидкостям, но так как для нагревания ртути необходимо меньшее количество теплоты, чем для нагревания воды, то ртуть по необходимости будет нагреваться быстрее воды. Когда же обе жидкости, нагретые до одной и той же температуры, выставляются на холодный воздух, то воздух первоначально получает теплоту от обеих жидкостей с одинаковой скоростью, но ртуть, отдавая то же количество теплоты, что и вода, охлаждается гораздо быстрее, чем вода. Эти эксперименты доктора Мартина, хорошо согласующиеся с экспериментами Фаренгейта, ясно показывают, что ртуть, несмотря на ее большую плотность, требует меньше теплоты для заданного повышения температуры, чем равный объем воды. [33]
Аппаратуру с открытыми поверхностями ртути размещают, как правило, в вытяжных шкафах, с отсосом воздуха не только сверху, но и снизу. Скорость движения воздуха при всех открытых створках шкафа во время работ, не связанных с нагревом ртути, должна быть не менее 0 5 м / сек, а при нагревании ртути — не менее 1 м / сек. [34]
Нагревание ртути должно проводиться на специальных печах, конструкция которых исключает наличие горизонтальных нагреваемых при включении печи поверхностей. Под нагревательным прибором должен находиться поддон с листовым асбестом или фарфоровый сосуд, куда ртуть должна попадать при случайной аварии. Нагревание ртути должно проводиться внутри вытяжного шкафа при включенной вентиляции, обеспечивающей скорость движения воздуха, равную 1 5 м / сек в сечении вытяжного шкафа. [35]
После перегонки ртути под пониженным давлением она, с целью дальнейшей очистки, подвергается вакуумной перегонке в дегазаторах или ректификаторах. Для этого применяется специальный стеклянный дегазатор119 ( рис. 13, а), в котором ртуть вначале дегазируется, а затем производится ее фракционная перегонка. Нагревание ртути в течение продолжительного времени до высокой температуры, превышающей точку кипения ее на 20 — 40, а также перегрев паров ртути в трубке 3 до 500 способствуют хорошей дегазации и частичному разрушению органических соединений, загрязняющих ртуть. [36]
Нагревание ртути должно проводиться на специальных печах, конструкция которых исключает горизонтальные поверхности нагрева. Под нагревательным прибором должен находиться поддон с листовым асбестом или фарфоровый сосуд, куда ртуть должна попадать при случайной аварии. Нагревание ртути должно проводиться внутри вытяжного шкафа прп включенной вентиляции, обеспечивающей скорость движения воздуха в сечении вытяжного шкафа. [37]
Нагревание ртути должно проводиться на специальных печах, конструкция которых исключает наличие горизонтальных нггреваемых при включении печи поверхностей. Под нагревательным прибором должен находиться поддон с листовым асбестом или фарфоровый сосуд, куда может попасть ртуть при случайной аварии. Нагревание ртути должно проводиться внутри вытяжного шкафа при включенной вентиляции, обеспечивающей скорость движения воздуха, равную 1 5 м / сек в сечении вытяжного шкафа. [38]
Нагревание ртути должно проводиться на специальных печах, конструкция которых исключает горизонтальные поверхности нагрева. Под нагревательным прибором должен находиться поддон с листовым асбестом или фарфоровый сосуд, куда ртуть должна попадать при случайной аварии. Нагревание ртути должно проводиться внутри вытяжного шкафа при включенной вентиляции, обеспечивающей скорость движения воздуха в сечении вытяжного шкафа. [39]
Далее Блек излагает и объясняет опыты Мартина — Рихмана. Мы должны только предположить, что равные количества теплоты сообщаются обеим жидкостям. Но для нагревания ртути необходимо меньшее количество теплоты, чем для нагревания воды. [40]
При пропускании тока сероводорода в раствор соли ртути ( П) осаждается черный HgS. Черный моносульфид ртути получают и сухим способом при нагревании ртути с серой. Черная модификация путем возгонки или обработки раствором полисульфида щелочного металла переходит в красную. Последним способом получают киноварь более светлой окраски, широко применяемую в живописи как масляная краска. [42]
21 интересный факт про ртуть
Пожалуй, ртуть является одним из немногих химических элементов, обладающих массой интересных свойств, а также обширнейшей сферой применения. В современном мире ртуть пригодилась в электронике, где компоненты на ее основе используются во всевозможных лампах и прочей электротехнике. Также этот металл используют при переработке нефти для регулирования температуры процесса и т.д. Сегодня предлагаю на ваш суд несколько интересных фактов про этот удивительный, ни на что не похожий гибрид жидкости и металла, а также элемент с атомным номером 80.
1. Прежде всего, ртуть — это единственный металл и второе (наряду с бромом) вещество, которое при комнатной температуре пребывает в жидком состоянии. Твердым она становится только при температуре –39 градусов. А вот повышение ее до +356 градусов заставляет ртуть закипать и превращаться в ядовитый пар.
2. Благодаря своему цвету в античные времена этот металл даже отождествляли с живым серебром, о чем свидетельствует одно из её латинских названий: argentumvivum. И это немудрено, ведь находясь в своем естественном состоянии – жидком, она способна «бежать» быстрее воды.
3. Каких-нибудь пару столетий назад люди верили, что если от очищенной ртути добиться твердого состояния, то ее можно будет превратить в золото. Но еще больше они полагались на магические свойства этого вещества. Например, жрецы Древнего Египта клали в деревянный или гранитный сосуд несколько граммов ртути и помещали его в горло мумии фараона — они считали, что после смерти это будет оберегать их правителя. Рядовые египтяне также рассчитывали на помощь ртути, нося флакончик с ней в качестве амулета. Многие верили и верят, что ртуть приносит удачу, поэтому и в наши дни талисманы из ртути не редкость.
4. Человечество использует ртуть вот уже более 3000 лет. Благодаря своей токсичности она активно применялась древними химиками для того чтобы извлечь из руды золото, серебро, платину и другие металлы. Такой способ под названием амальгация позже был забыт, к нему вернулись только в XVI столетии. Возможно, благодаря именно ему добыча золота и серебра колонизаторами Южной Америки в свое время достигла колоссальных размеров.
5. При эксгумации тела Ивана Грозного ученые определили, что содержание ртути в организме царя в 5 раз превышало допустимые нормы. Известно, что на Руси ртуть использовали для лечения сифилиса еще в XV-XVI столетиях. Некоторые исследователи предположили, что Иван Грозный, страдавший этим опасным недугом, был подвергнут лечению «жидким серебром». Н. М. Карамзин писал, что царь так «изменился, что нельзя было узнать его: на лице изображалась мрачная свирепость, все черты исказились, взор угас, на голове и в бороде не осталось почти ни одного волоса». Резкое выпадение волос один из явных признаков отравления ртутью, как и эпилептические припадки, которые мучили царя. Ртутная интоксикация – такова причина смерти Ивана Грозного, по мнению современных экспертов.
6. Между прочим, металлом ртуть стала только лишь в 1759 году, когда Михаил Ломоносов и Иосиф Браун смогли доказать этот факт.
7. Благодаря своей плотности ртуть имеет большой удельный вес. Так, например, 1 литр вещества весит более 13 килограммов.
8. Кстати, впервые вес ртути в 1627 году измерил Роберт Бойль, но его цифры верны и сейчас. 1 литр ртути соответствует примерно 13,6 килограммам, на это же число плотность ртути выше плотности воды.
9. В природе ртуть может встречаться, как в чистом виде — вкраплениями небольших капель в других породах. Но чаще всего ртуть добывали, обжигая ртутный минерал киноварь. Также присутствие ртути можно обнаружить в сульфидных минералах, глинистых сланцах и др.
10. Большая часть ртути, используемой людьми, добывается из руды, названной киноварью. Чтобы получить чистую ртуть, киноварь нагревают в потоке воздуха. Кислород в воздухе объединяется с серой в руде, формируя газ двуокиси серы и оставляя ртуть.
12. Несмотря на свою токсичность, ртуть активно применяли лекари древности при лечении всевозможных заболеваний. На ее основе изготавливали медицинские препараты и снадобья для лечения различных кожных заболеваний. Она входила в состав мочегонных и слабительных препаратов, использовалась в стоматологии. А йоги древней Индии, согласно запискам Марко Поло, употребляли напиток на основе серы и ртути, который продлевал им жизнь и давал силы. Также известны случая изготовления китайскими знахарями «пилюлю бессмертия» на основе данного металла. Сегодня в медицине ртуть можно встретить только лишь в градусниках, измеряющих температуру тела. Но и в этой нише ее постепенно вытесняет электроника.
13. Ртуть применяют для производства краски, которой открашивают корабли. Дело в том, что на подводной части судна могут образовываться колонии бактерий и микроорганизмов, которые разрушают обшивку. Краска на основе ртути препятствует этому разрушительному воздействию.
14. Ртуть готова дружить со всеми металлами, кроме железа и платины.
15. Металлическая ртуть не так ядовита как принято считать. Наиболее опасны пары ртути и её растворимые соединения. Сама металлическая ртуть не всасывается в желудочно-кишечном тракте и выводится из организма.
16. Ртуть нельзя перевозить в самолетах. Но не из-за её токсичности как может показаться на первый взгляд. Все дело в том, что ртуть, контактируя с алюминиевыми сплавами, делает их хрупкими. Поэтому, случайно разлив ртуть, можно повредить самолет.
17. Помните Сумасшедшего Шляпника из «Алисы в стране Чудес»? Так вот раньше такие «шляпники» существовали на самом деле. Все дело в том, что фетр, используемый для производства шляп, обрабатывали ртутными соединениями. Постепенно ртуть накапливалась в организме мастера, а одним из симптомов ртутного отравления является сильное расстройство рассудка, проще говоря шляпники часто в итоге сходили с ума.
18. Между прочим, наш организм всё-таки «отягощен» ртутью, но её количество ничтожно — 13 миллиграмм.
19. Известно, что ртуть содержится в морской воде. Недавно было установлено, что мелкие рыбы способны накапливать это вещество. При этом хищники, как рыбы, так и птицы, которые охотятся на мелкую рыбу, могут сохранять ртуть в организме в еще более высоких концентрациях. Например, если сельдь содержит 0,01 промилле ртути, то у акулы показатель превышает 1 промилле.
20. В сельском хозяйстве высокотоксичные соединения ртути используют в качестве пестицидов.
21. Случайно разбившийся градусник требует соблюдения безопасного алгоритма действий. Первое правило — вывести всех из помещения, закрыть дверь, распахнуть окно. Загрязненный парами ртути воздух не распространится по квартире. Сама ликвидация начинается с подтягивания мелких капель друг к другу с помощью бумаги. Мелкие частицы собирают кисточкой, клейкой лентой. Оставшиеся капли втягивают грушей. Все погружают в банку. Вооружившись фонариком, необходимо убедиться в полном отсутствии ртути. Нельзя убирать вещество веником, бытовым пылесосом. За счет нагревания, дробления капель испарение усиливается в сотни раз. После механической уборки провести влажную. Протирать химическими чистящими средствами нельзя: при контакте с ртутью они образуют опасные соединения.
Ваш Промблогер №1 Игорь (ZAVODFOTO)! Подписывайтесь на мой канал, я Вам ещё много чего интересного покажу: https://zen.yandex.ru/zavodfoto
Р. S. Уважаемые собственники и акционеры, представители пресс-служб компаний, отделы маркетинга и другие заинтересованные лица, если на Вашем предприятие есть, что показать — «Как это делается и почему именно так!», смело приглашайте в гости. Для этого пишите мне сюда: akciirosta@yandex.ru Берите пример с лидеров!
На данный момент я уже лично посетил более 400 предприятий, а вот и ссылки на все мои промрепортажи:
Я всегда рад новым друзьям, добавляйтесь и читайте меня в:
Основные свойства ртути и температура плавления
Температура плавления ртути характеризует момент перехода металла из твердого состояния в жидкость. Свойства живого серебра (argentum vivum в переводе с латинского) расширяют границы применения металла в разных сферах производства с учетом мер безопасности, связанных с его использованием.
Распространенность в природе
В земной коре концентрация химического элемента низкая. Ртутные рудные минералы содержат до 2,5% живого серебра. Это отличает их от других пород. В основном меркурий находится в рассеянной форме, и лишь часть находится в месторождениях.
В магматических породах долевое содержание живого серебра равно между собой, а в осадочных толщах крупные концентрации металла сосредоточены в глинистых минералах. Воды Мирового океана содержат 0,1 мкг/л меркурия.
Высокая степень ионизации определяет особенности металла:
Химический элемент присутствует в составе сульфидных минералов (сфалерит, реальгар). Этот металл является индикатором месторождений ртути и скрытых рудных тел. В поверхностных условиях живое серебро и киноварь не растворяются в воде, но при наличии серной кислоты, озона способствует увеличению показателя растворимости минералов.
Меркурий обладает отличными сорбционными свойствами. В природе существует около 20 минералов, содержащих этот металл, но промышленная добыча производится на месторождениях киновари.
Одно из крупнейших месторождений находится в Испании. Технология производства металла предусматривает обжиг киновари с последующей конденсацией и сбором паров ртути.
Физические и химические свойства живого серебра
Ртуть (меркурий) имеет уникальные химические и физические особенности, что позволяет ее применять в различных сферах. Но в то же время ее испарения опасны для человека. Как уже упоминалось, ее называют живым серебром, она по цвету напоминает лунный металл.
Меркурий обладает переходными свойствами, при комнатной температуре он остается в жидком состоянии. Живое серебро легко образует с другими материалами твердые и жидкие сплавы (амальгамы). Наиболее популярными являются соединения золота и серебра.
Химический элемент является диамагнетиком, и в случае необходимости собрать его магнитом невозможно. Он неплохо проводит ток, поэтому в свое время его применяли при изготовлении реле и выключателей.
Плотность живого серебра при нормальных условиях составляет 13,5 г/см³. Этот химический элемент обладает устойчивостью в сухом воздухе, окисляется только при нагревании выше +300°C. После длительного хранения на открытом воздухе на поверхности образуется пленка из оксидов компонентов, содержащихся в основном материале в качестве примесей.
При нагревании вступает в реакцию с кислородом, образуя оксид красного цвета. Металл малоактивный, не реагирует с растворами кислот, но растворяется в царской водке. При нагревании в серной кислоте образует сульфат ртути.
Сферы использования живого серебра
Ртуть применяется для изготовления точных измерительных приборов для определения температуры и давления. Сегодня в электрохимическом производстве широко используются ртутные выпрямители тока.
В медицинской отрасли для проведения профилактических работ в качестве источников ультрафиолетового спектра применяются ртутные (газоразрядные) лампы, всем известные градусники для измерения температуры тела содержат этот химический элемент.
В связи с тем, что меркурий токсичен, его не используют для изготовления медицинских препаратов. Хотя до середины 70-х годов ее активно применяли для производства мази от педикулеза.
Измерительные приборы для низкотемпературных условий содержат амальгаму таллия, которая в отличие от чистой ртути застывает при температуре — 60°C. Сочетание 2 токсичных металлов значительно расширяет границы использования.
За рубежом кипящую ртуть используют в качестве охладителя. Ее преимущество поддерживать постоянную температуру позволяет интенсивно отводить тепло от пространства катализатора. Для увеличения коэффициента отдачи в ртуть добавляют натрий для образования амальгамы.
С целью размягчения кадмия, олова и серебра меркурий используют в стоматологии при изготовлении пломб. Раньше ее применяли для золочения деталей часов и ювелирных изделий, а амальгамы золота и серебра использовались при производстве зеркал.
Живое серебро применяется в качестве катода для извлечения ряда активных компонентов электролитическим путем, а также для переработки вторичного алюминия.
Существуют технологии извлечения золота из россыпей с использованием свойства химического элемента образовывать амальгаму с благородным металлом. Этот метод был широко распространен в Индии, где в местах предполагаемого скопления золота проделывали специальные углубления, в которые заливали металлическую ртуть. Через некоторое время вытаскивали амальгаму, и путем выпаривания извлекали золото.
В нефтеперерабатывающей промышленности для регулировки температурных процессов используют пары ртути. В сельском хозяйстве ее используют для подготовки семян к посеву.
С давних времен и сегодня соли меркурия используют при изготовлении фетра, дублении кожи в качестве катализатора органического синтеза.
В прошлом ртуть не считалась вредным веществом, ее применяли для исцеления от недугов. В Средневековье алхимики использовали меркурий в поисках философского камня и превращения ее в золото.
Ртуть опасна для человека, она токсична и даже в ничтожных концентрациях плохо влияет на иммунную систему, почки, глаза, кожу и пищеварительный тракт.
Кипение и плавление металла
Технология физико-химических исследований при условиях высоких температур рассматривает давление плавления металла при разных температурах. Точность опытов обеспечивает применение на практике свойств химического элемента № 80.
Для измерения температуры выше +360°C пользуются термопарами или специальными термометрами, в которых пространство надо ртутью заполнено газом. С целью повышения температуры кипения металла в капилляр надо ртутью закачивают азот. При давлении 30 атмосфер температурный градиент увеличивается до +600°C.
Такого типа термометры требуют постепенного нагрева. Нижним пределом такого измерительного прибора является температура перехода живого серебра в твердое состояние.
Теплоемкость металла с увеличением температуры последовательно уменьшается и после определенного порога температурного градиента начинает медленно расти. Это свойство и жидкое состояние роднит ртуть с водой.
Действие ртути на организм
Металлическая ртуть и ее соединения весьма токсичны. Пары ртути проникают в организм в основном через легкие, где они частично задерживаются, превращаясь в различные ртутные соединения. Основная же часть ртути переходит в кровь и затем накапливается в почках, печени и мозге. Кроме того, ртуть может попадать в организм и через желудочно-кишечный тракт, кожу и слизистые оболочки.
Обычно наблюдаются не острые, а хронические, обусловленные длительным действием паров отравления ртутью, которые выражаются в расстройстве нервной системы, повышенной возбудимости, головных болях, дрожании рук и головы, быстрой утомляемости и, наконец, в потере трудоспособности. Лица, у которых появились симптомы отравления ртутью, должны немедленно обратиться к врачу.
Как собрать ртуть?
Пролитую ртуть необходимо немедленно с максимальной тщательностью собрать под слой воды в толстостенный сосуд, а место, на котором она была пролита, дегазировать. В том случае, если было пролито большое количество ртути, основную часть ее можно собрать стеклянным капилляром, соединенным посредством каучуковых шлангов через склянку Тищенко или Дрекселя с водоструйным насосом, причем собирать ртуть надо начинать с периферии.
Собрать остатки ртути или пролитые небольшие количества ее можно одним из следующих двух способов:
а) ртутные шарики сметают (как в совок) при помощи волосяной кисточки в «фунтики» из фильтровальной или простой бумаги и затем переливают ртуть в толстостенную посуду с водой; использованные «фунтики» помещают в стеклянный сосуд под тягой и обрабатывают концентрированной азотной кислотой;
б) используют амальгамированные металлические пластинки, к которым способны прилипать мелкие капельки ртути, или кусок чистой оцинкованной жести.
После того как видимые капельки ртути будут собраны, необходимо провести дегазацию зараженного места.
Наиболее удобным агентом для дегазации, поверхности пола или стола является 20%-ный водный раствор хлорного железа, который способен эмульгировать капли ртути, что сильно ускоряет взаимодействие ртути с хлорным железом. Этим раствором обильно смачивают при помощи кисти всю зараженную ртутью поверхность и оставляют на 1-2 суток до полного высыхания. Если по каким-либо причинам столь длительная дегазация невозможна, раствор вместе с эмульгированной ртутью можно удалить через 4-6 ч. Продегазированное место несколько раз промывают водой.
Для дегазации вертикальных поверхностей наибольшее применение получил сероводород, который связывает ртуть в виде сульфида, не обладающего токсическим действием. На крупных каплях ртути при этом образуется пленка сульфида, которая снижает упругость паров самого металла. Недостатком этого метода является применение токсичного сероводорода (для дегазации используются высокие его концентрации); кроме того, помещение должно быть герметизировано и закрыто на 2-3 дня.
Меньшее практическое применение имеют способы дегазации ртути при помощи серы, перманганата калия, активированного угля с примесью йода, сероводородной воды.
Правила хранения и работы с металлической ртутью
При работе с металлической ртутью необходимо соблюдать следующие меры предосторожности. В лабораториях допустимо хранение лишь минимально необходимых количеств металлической ртути, которую помещают под слой воды в толстостенный, плотно закрытый каучуковой или притертой пробкой стеклянный сосуд. Последний должен стоять на противне из пластмассы или металла, покрытого эмалью. Все работы, связанные с переливанием ртути, следует проводить в вытяжных шкафах и только на специальных противнях (см. выше), с которых можно легко удалить пролитую ртуть и которые легко могут быть продегазированы.
Стеклянную посуду, находившуюся в контакте с металлической ртутью, обрабатывают в вытяжном шкафу несколькими порциями концентрированной азотной кислоты до тех пор, пока из свежей порции кислоты не перестанут выделяться окислы азота.
Для сбора загрязненной или отработанной ртути, остатков реакционных смесей, содержащих ртуть, а также кусков бумаги, в которые собиралась ртуть, в каждой лаборатории должен находиться специально предназначенный для этого толстостенный стеклянный сосуд с небольшим количеством воды, плотно закрытый каучуковой или притертой пробкой. Категорически запрещается выбрасывать остатки ртути и ее соединений в мусорные ящики и канализационные трубы.
Категорически запрещается проводить любые работы, связанные с нагреванием металлической ртути.