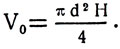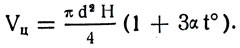Физика. 7 класс
Впишите в текст пропущенные слова.
Температура воздуха в комнате повысилась. Столбик жидкости в комнатном термометре:
Опустился вниз, так как объём жидкости при нагревании уменьшился.
Поднялся вверх, так как объём жидкости при нагревании увеличился.
Не изменился, так как объём жидкости не зависит от температуры.
Выберите утверждение, которое является наиболее наглядным экспериментальным доказательством существования атомов и молекул.
Фотография с помощью электронного микроскопа.
Капля масла растекается по поверхности воды плёнкой толщиной в одну молекулу.
Запах духов распространяется по всей комнате.
Объём вещества при нагревании увеличивается.
Определите верные и ложные высказывания.
Верные высказывания:
Ложные высказывания:
Вещество состоит из мельчайших частиц.
Молекулы воды точно такие же, как и молекулы льда.
Гвоздь при нагревании удлиняется и становится толще, потому что атомы железа увеличиваются в размере.
Плёнка масла, растекаясь по поверхности может занять любую площадь.
Атом состоит из молекул.
При сжатии газа уменьшается размер молекул.
При нагревании колбы с водой уровень воды в трубке поднимается. Выберите верное утверждение для объяснения этого явления.
Нагревании колбы с водой
В воде увеличивается число частиц.
Увеличивается размер частиц воды.
Изменяется форма частиц воды.
Увеличивается расстояние между частицами воды.
Впишите в текст пропущенные слова.
Составьте цепочку так, чтобы каждый последующий элемент входил в состав предыдущего.
Тепловое расширение
Подавляющее большинство веществ при нагревании расширяется. Это легко объяснимо с позиции механической теории теплоты, поскольку при нагревании молекулы или атомы вещества начинают двигаться быстрее. В твердых телах атомы начинают с большей амплитудой колебаться вокруг своего среднего положения в кристаллической решетке, и им требуется больше свободного пространства. В результате тело расширяется. Так же и жидкости и газы, по большей части, расширяются с повышением температуры по причине увеличения скорости теплового движения свободных молекул (см. Закон Бойля—Мариотта, Закон Шарля, Уравнение состояния идеального газа).
где α — так называемый коэффициент линейного теплового расширения. Аналогичные формулы имеются для расчета изменения площади и объема тела. В приведенном простейшем случае, когда коэффициент теплового расширения не зависит ни от температуры, ни от направления расширения, вещество будет равномерно расширяться по всем направлениям в строгом соответствии с вышеприведенной формулой.
Для инженеров тепловое расширение — жизненно важное явление. Проектируя стальной мост через реку в городе с континентальным климатом, нельзя не учитывать возможного перепада температур в пределах от —40°C до +40°C в течение года. Такие перепады вызовут изменение общей длины моста вплоть до нескольких метров, и, чтобы мост не вздыбливался летом и не испытывал мощных нагрузок на разрыв зимой, проектировщики составляют мост из отдельных секций, соединяя их специальными термическими буферными сочленениями, которые представляют собой входящие в зацепление, но не соединенные жестко ряды зубьев, которые плотно смыкаются в жару и достаточно широко расходятся в стужу. На длинном мосту может насчитываться довольно много таких буферов.
Однако не все материалы, особенно это касается кристаллических твердых тел, расширяются равномерно по всем направлениям. И далеко не все материалы расширяются одинаково при разных температурах. Самый яркий пример последнего рода — вода. При охлаждении вода сначала сжимается, как и большинство веществ. Однако, начиная с +4°C и до точки замерзания 0°C вода начинает расширяться при охлаждении и сжиматься при нагревании (с точки зрения приведенной выше формулы можно сказать, что в интервале температур от 0°C до +4°C коэффициент теплового расширения воды α принимает отрицательное значение). Именно благодаря этому редкому эффекту земные моря и океаны не промерзают до дна даже в самые сильные морозы: вода холоднее +4°C становится менее плотной, чем более теплая, и всплывает к поверхности, вытесняя ко дну воду с температурой выше +4°C.
То, что лед имеет удельную плотность ниже плотности воды, — еще одно (хотя и не связанное с предыдущим) аномальное свойство воды, которому мы обязаны существованием жизни на нашей планете. Если бы не этот эффект, лед шел бы ко дну рек, озер и океанов, и они, опять же, вымерзли бы до дна, убив всё живое.
При нагревании металлов жидкостей воздуха объем их увеличивается потому что
§ 31. Объемное расширение твердых тел и жидкостей при нагревании
Жидкости при нагревании также расширяются. Изменение объема жидкости при изменении ее температуры учитывается при наполнении ею сосудов. Например, на складах горючего баки не заполняются полностью керосином, бензином, нефтью. При работе трансформатора трансформаторное масло в баке расширяется и поступает в бачок-расширитель. Изменение объема ртути при изменении ее температуры используется в термометре.
При нагревании тела на 1°С его объем увеличивается на βV0. При нагревании на t° объем увеличивается на βV0t°. Следовательно, объем тела становится V = V0 + βV0t°, или
Обычно в таблицах даются только коэффициенты линейного расширения твердых тел, α коэффициенты объемного расширения не приводятся. Объясняется это тем, что величину β вычисляют по величине α, пользуясь формулой β = 3α.
Задача 12. При температуре 0°С цилиндрическая стальная цистерна, высота которой 4 м, заполняется нефтью. Учитывая изменение емкости цистерны при изменении температуры, определить, на сколько нефть должна быть недолита, чтобы при температуре 27° С она еще не выливалась из цистерны.
Тогда
Объем нефти после нагревания Vн = V0‘(1 + βt°), где объем нефти при 0°С равен
Увеличиваются ли молекулы при нагревании?
Все мы знаем, что если надуть пластиковую бутылку горячим воздухом, крепко-накрепко закрыть крышкой, а потом охладить, то бутылка сожмётся. Причина этого лежит в физике 8-го класса, или, если точнее, в законе Гей-Люссака, утверждающем, что отношение объёмов при разных температурах равно отношению абсолютных температур. То есть ещё со школьных времён (а может и раньше) нам всем известно, что при нагревании некоторого количества газа его объём увеличивается, а при охлаждении — уменьшается.
А что насчёт того, из чего этот газ состоит? Увеличивается ли объём самих частичек газа, то есть размер атомов и молекул? Банальный ответ на этот банальный вопрос под катом.

Ха-ха, попались!
Ответ на этот вопрос весьма прост: как мы определим объём размер частиц (что такое размер атома/молекулы в зависимости от температуры), такой ответ мы и получим. Поскольку атомы по-своей сути — это одноатомные молекулы, то дальше мы будем называть все эти частицы единым термином «молекула«.
Если взять бутылку с газом, и из этой бутылки взять одну единственную молекулу, то окажется, что для неё не возможно (по-честному) даже принципиально измерить температуру. Частица находится в каком-то конкретном (квантовом) состоянии, которое мы можем определить и измерить, но при этом мы не сможем засунуть ей в в неё термометр и узнать сколько там у неё градусов. Связанно это с тем, что «температура» — это свойство макроскопических (т.е. больших) систем, состоящих из большого числа частиц. А значит если молекул в системе мало, то и измерять у этой системы нечего. «Большое число частиц», конечно, это плавающее понятие, но обычно оно измеряется в молях, или в числах Авогадро (), поэтому очевидно, что одна молекула горааааздо меньше этого порядка величин, а значит само понятие температуры не применимо к одной, двум, да даже десяти молекулам.
Что такое температура?
Но что вообще такое температура? Ещё со школы мы знаем, что есть т.н. абсолютная температура T, измеряемая в градусах Кельвина. Именно она стоит во всех газовых законах, в частности в уравнении Менделеева-Клайперона.
абсолютная температура является мерой средней кинетической энергии молекул.
Но эта мантра не объясняет, что же именно из себя представляет температура.
Попробуем разобраться. Начнём с простого примера. Закроем глаза и представим себе Африку: жаркую, солнечную, заполненную равнинными саваннами, и с горой Килиманджаро торчащей посередине. А ещё там есть слоны.
Каждый слон имеет определённую (большую) массу, и поэтому любое поднятие своей туши из равнинной местности в горную — это большая затрата энергии.
Представим, что слоны голодные, поэтому энергии у них мало. Будучи слоном, я бы в таком состоянии не попёрся бы в гору, а тусовался бы в саванне. В горы бы я ходил только по очень-очень большой нужде. В результате, если бы мы сняли фотографию Африки со спутника, она бы выглядела примерно так, как показано на картинке ниже: много-много слонов на равнине, и очень мало смелых и отчаянных в горах, причём, чем выше — меньше вероятность найти слона.
А теперь представим, что слоны хорошенько поели, да ещё какой-нибудь [Роскомнадзор] ещё для скорости им в еду подсыпали, так что энергии у слонов много. В этом случае, что равнина, что гора, слоны будут туда переться без особой устали, поэтому теперь вероятность отыскать слона на равнине и в горах будет отличаться уже меньше, чем в предыдущем примере (см. картинку ниже), хотя всё ещё будет сохраняться правило: чем выше на гору — тем меньше слонов.
Эти два примера весьма точно иллюстрируют случаи газа с низкой (первый) и высокой (второй) температурой. У каждой молекулы (слона) есть какая-то своя энергия, в нашем примере — это гравитационная энергия , где m — масса, g = 9.8 м/c 2 — ускорение свободного падения, а h — высота над равниной. Из энергии каждой конкретной частицы (места, где нашли слона) мы не можем ничего сказать о том, как всех слонов покормили в целом, но именно то, сколько на всех выделили еды, или другими словами, сколько энергии вкачали в среднем во всю систему, даст нам распределение слонов по ландшафту Африки. Собственно, температура в наших примерах — это общая величина накормленности всех слонов во всей Африке. Именно поэтому мантра из школьного курса физики и оказывается верна — температура — это то, сколько в среднем энергии (причем, как кинетической, так и потенциальной) имеет каждая молекула, или, что в данном случае эквивалентно, какова вероятность найти частицу с очень большой энергией. Но более точно, температура — это параметр распределения Больцмана (или Гиббса) — распределения частиц по состояниям с различной энергией. Это распределение говорит нам, что чем выше температура, тем больше высокоэнергетических молекул относительно числа низкоэнергетических мы имеем.
где n(E) — это число частиц с энергией E, R — универсальная газовая постоянная (см. предыдущий спойлер), а T, само собой, температура.
В примере же со слонами мы иллюстрировали т.н. барометрическую формулу: частный случай распределения Больцмана, показывающий как меняется давление газа с увеличением высоты:
где P(h) — это давление на высоте h, , а M — это молярная масса газа.
Растут ли атомы от температуры?
Теперь, собственно, можно перейти к вопросу: а растут ли, например, атомы при росте температуры. Само собой, каждый конкретный атом находится в каком-то квантовом состоянии, поэтому от температуры его размер не зависит, но вот средний размер всех атомов в сосуде с газом от той самой температуры зависеть уже будет.
Представим себе, например, атом водорода: тяжёлый протон, а вокруг него летает электрон. Поскольку протон положительный, а электрон отрицательный, то один притягивает другой по закону Кулона, который выглядит точно так же как ньютоновская гравитация, поэтому в этом смысле атом вполне себе напоминает, например, Солнце и Землю, летающую вокруг него. Только, как говорит нам (далеко не полностью удачная, см. например, тут) атомная модель Бора, в отличие от системы «звезда + планета», электрон летает вокруг ядра только по орбитам определённого радиуса.
Так или иначе, чем больше энергии мы закачиваем в атом водорода, тем более широкая орбита будет доступна электрону для полёта вокруг ядра. Естественно, если мы возьмём один конкретный атом, мы можем узнать его орбиту, и она ничего нам о температуре всех атомов не скажет. Но вот если мы измерим радиусы у множества атомов, а потом усредним полученные величины, то у нас действительно возникнет зависимость от температуры для этого среднего числа. В результате получится что-то типа такой картинки:
Из неё видно, что чтобы начать замечать хоть какие-то изменения в размере электронной оболочки, нужно ооочень сильно нагреть атом (в данном случае до более 10000 градусов). Это в целом общий тренд.
Подробнее о формулах можно узнать в этом посте.
Если кратко, то радиус орбиты (R) в зависимости от главного квантового числа n=1,2,3… — это
где R0=5.3×10 −11 метра − это боровский радиус. Энергия (E) же орбиты имеет вид
где Eh= 4.3597447222071(85)×10 −18 Джоулей − это энергия Хартри.
Далее используя распределение Больцмана для одной частицы, мы можем посчитать среднее значение радиуса от температуры как
Знаменатель у нас появляется из-за того, что полная вероятность всех исходов измерений должна быть равна единице.
Иными словами, ответ на вопрос поста: да, при нагревании электронные оболочки атомов (и молекул) в среднем расширяются. Но, это увеличение очень маленькое, и требует нагрева до очень высоких температур, к которым мы в обыденной жизни не привыкли.
Растут ли молекулы от температуры?
Теперь зададимся вопросом: а что если наша молекула составлена не из одного, а из двух, трёх или более атомов? Можем ли мы что-то сказать о межатомных расстояниях в ней, как ведут они себя при повышении температуры? Для простоты, естественно, ограничимся двухатомными молекулами, кои, в частности, составляют как минимум 98.7 % нашей атмосферы (азот и кислород).
У нас есть один атом, у нас есть второй атом: ммммм, и расстояние между ними, обозначим его как R. Как ведёт себя потенциальная энергия взаимодействия этих атомов в зависимости от R?
Атомы в молекуле всегда колеблются, даже при абсолютном нуле, когда никакой лишней энергии не осталось. Из-за принципа неопределённости они не могут просто скатиться в минимальную по энергии точку на потенциале и сдохнуть лежать, свернувшись калачиком: им приходится совершать т.н. нулевые колебания. Если же энергия у них выше, то и колеблются они с большей амплитудой. Поэтому возникает вопрос: а как конкретно колеблются атомы?
Если бы слева и справа от точки минимума потенциал был одинаков, как, например, в случае закона Гука, то атомы во время колебаний отклонялись бы в область малых значений межатомных расстояний ровно то же количество времени, сколько и в область больших значений. В этом случае бы среднее значение межатомного расстояния при любой температуре было бы равно значению расстояния в точке минимума. Иными словами, если бы мы взяли газ, и в любой момент времени сфоткали все молекулы, а потом посчитали бы среднее значение для всех расстояний между атомами, то в итоге получили бы расстояние в точке минимума.
Но реальность у нас другая: слева от точки минимума (при R → 0) у молекулы стоит жёсткая стенка, а справа (при R → ∞) — мягкий диван. Вопрос: где будет больше времени проводить молекула: долбиться о стенку, или валяться на диване? Правильно: конечно на диване. Иными словами, распределение расстояний в молекуле, что при абсолютном нуле, что при какой-то температуре, будет несимметричным, поэтому среднее значение расстояний будет сдвинуто в сторону больших расстояний относительно минимального. Мало того, при повышении температуры, т.е. когда мы будем закачивать больше кинетической энергии в систему, увеличивая амплитуду колебаний, молекула будет видеть гораздо более жёсткую стенку, и гораздо более мягкий диван. Поэтому среднее значение межатомных расстояний будет расти с ростом температуры, а значит и средний размер молекул, причём всех, не только двухатомных, будет увеличиваться.
К сожалению, чтобы посчитать этот рост среднего расстояния, потребуется много больше усилий, чем в случае атома водорода. Но можно пойти другим путём, и поискать, а не исследовался ли этот вопрос в экспериментах?
И порывшись на просторах этих наших Интернетов, можно набрести на следующую работу: J. Chem. Phys. 79, 170 (1983). В ней делали эксперимент буквально описанный выше:
Из графика видно, что при нагреве от комнатной температуры до 1000 градусов К это среднее значение выросло почти на 0.004 Å (1 ангстрем, Å, = 10 —10 метров). Конечно, в наших привычных величинах это очень мало, но сама длина связи C=O в этой молекуле составляет 1.2 Å, так что это рост на почти 0.3 %! Вполне себе заметная величина при нагреве, достижимом привычными средствами (например, газовой плитой).
Зачем это вообще знать?
Да хотя бы просто ради любопытства. Разве не прикольно поспорить с коллегой на чашку кофе, что при нагреве контейнера с едой в микроволновке помимо объёма газа увеличится и размер частиц газа? Ну и в практическом смысле это тоже важно. Все эти температурные расширения/уменьшения всяких макроскопических объектов, таких как рельсы, провода линий электропередач, да даже крышки банки под горячей водой, работают ровно по тому же механизму, что и для молекул газа: средние межатомные расстояния увеличиваются, т.к. в систему при увеличении температуры закачивается больше энергии движения частиц. И по-моему, осознание того, что за такими обыденными явлениями стоят такие нетривиальные процессы, вдохновляет на новые подвиги и свершения.
Всех благ, и да пребудет с Вами межатомная сила.
Интегрированный урок по физике и химии.Агрегатные состояния вещества
Цели урока:
План урока
1. Актуализация знаний учащихся
Слайд №1
Учитель химии. Ребята! Сегодня у вас необычный урок, который будут вести сразу двое учителей. Это интегрированный урок по физике и химии. Тема нашего урока «Агрегатные состояния вещества».
У нас с учителем физики возник спор – какая же наука более важна? А вы как думаете?
(Учителя читают стихотворение о науках, которое иллюстрируется слайдами № 2-6)
Что такое физика? Физика – наука.
Полюбив ее, мы знать не будем скуки.
Разные явленья в природе, и в быту,
Объяснив, постигнем мира красоту.
Что такое химия? Химия – наука.
Полюбив ее, вы забудете о скуке!
Превращения разные будем наблюдать,
В опытах ответы станем получать.
Днем сияет солнце, ночью – темнота,
Звезды, как алмазы сказочно блестят.
Как от них доходят к нам тепло и свет?
Физика на это может дать ответ.
Речка серебрится под покровом льда.
Почему вдруг твёрдой стала в ней вода?
Почему туманы утром над рекой?
Химия ответит на вопрос такой.
Разные вопросы будем задавать,
Чтобы узнать природу, чтоб её понять.
Как должны мы землю милую беречь,
И об этом с вами поведем мы речь.
Учитель физики: Вот видите, нет наук важных и не очень – для всестороннего образования человека все науки важны и нужны.
Слайд №7
Прежде чем мы приступим к изучению темы, давайте заполним кластер «Свойства веществ в разных агрегатных состояниях» и посмотрим, что вы о них знаете до изучения темы…
Если у вас остались пустые стрелочки, будьте внимательны на уроке. В конце урока мы еще раз вернемся к этому кластеру и заполним его весь.
Слайд №8.
Учитель химии: Еще в глубокой древности, 2500 лет назад, греческий ученый Демокрит, считал, что все вещества состоят из частичек. В научную теорию эта идея превратилась в 18 в. И получила дальнейшее развитие в 19 веке благодаря работам нашего знаменитого соотечественника М.В. Ломоносова. Многие опыты подтверждают представления о строении вещества. Рассмотрим некоторые из них.
Слайд №9.
Учитель физики:
А) Демонстрация опыта «Нагревание твердых тел» одним из учащихся под руководством учителя физики. Обсуждение результатов опыта с учащимися.
– Что происходит с твердыми телами при нагревании?
– Что является причиной их расширения?
– Почему при охлаждении они снова приобретают начальный объем?
Вывод: При нагревании твердых тел происходит увеличение их объема, причиной которого является увеличение промежутков между частицами вещества.
Б) Демонстрация опыт «Нагревание жидкости» (колба, наполненная подкрашенной водой и закрытая пробкой со стеклянной трубочкой) одним из учащихся под руководством учителя. Обсуждение результатов опыта с учащимися.
– Что происходит с жидкими телами при нагревании?
– Что является причиной увеличения их объема?
– Как изменяется объем жидкости при охлаждении?
Вывод: При нагревании жидкостей их объем увеличивается, и вода начинает подниматься по трубке. Причиной увеличения объема жидкости является увеличение промежутков между молекулами жидкости.
Общий вывод: При нагревании увеличиваются объёмы не только твёрдых, но и жидких тел. Причиной этого является увеличение промежутков между молекулами веществ.
Учитель химии: Какими опытами можно еще доказать наличие частиц и промежутков между ними в веществе?
В) Организация демонстрации учащимися опыта «Диффузия газа в помещении» (можно использовать освежитель воздуха). Обсуждение результатов опыта.
– Почему распространение запаха происходит быстро? (благодаря движению молекул газа в воздухе и большому расстоянию между ними).
– В каком направлении возможно движение частиц газа? ( В беспорядочном. Это броуновское движение частиц).
Г) Демонстрация опыта «Диффузия в жидкостях» (Сосуд с водой и кристаллический перманганат калия). Обсуждение результатов опыта.
– Что происходит с кристаллами перманганата калия в воде? (Они растворяются).
– Почему через некоторое время раствор становится однородного цвета, даже без перемешивания? (Благодаря броуновскому движению частиц растворителя и растворенного вещества).
– Почему в газах и жидкостях смешивание частиц вещества происходит с разной скоростью? (Причина – расстояние между частицами вещества в газообразном состоянии больше, чем между молекулами в жидкости).
Вывод: Вещества состоят из частиц, которые способны смешиваться и взаимопроникать друг в друга. Это явление носит название «диффузии».
Слайды №10-11.
Учитель химии: Подумайте, играет ли роль в природе и жизни человека это явление? Беседа с учащимися.
Слайд №12.
«Значение диффузии в природе и жизни человека».
II. Изучение нового материала
1. Учитель химии: Мы повторили необходимые базовые знания для того, чтобы лучше усвоить новые понятия об агрегатных состояния вещества. Попробуйте отгадать загадку…
Слайд №13.
Я и туча, и туман,
И ручей, и океан,
И летаю, и бегу,
И стеклянной быть могу!
Ответьте на вопросы:
– О каких состояниях воды говорится в загадке?
– При каких условиях вода превращается в пар? Лед?
– Одинаковыми ли физическими свойствами обладает вода в разных физических состояниях?
Одно и тоже вещество в зависимости от условий может находиться в каждом из трех состояний: газообразном, жидком и твердом. Такие состояния принято называть агрегатными.
Слайд № 14.
Чтобы доказать, что физические свойства воды жидкой и льда отличаются, мы предлагаем вам посмотреть видеофрагмент «Домашнее исследование свойств воды в разных физических состояниях», которое подготовили для вас ученики. Смотрите внимательно, потому что вам предстоит ответить на вопрос:
– Какое свойство изменяется у воды при превращении в лед?
(Демонстрация видеофрагмента, снятого учеником дома.)
Обсуждение просмотренного видеофрагмента.
Вывод: При замерзании воды ее объем увеличивается, и, наоборот, при таянии воды ее объем уменьшается. Следовательно: при переходе из одного агрегатного состояния в другое физические свойства веществ изменяются.
Учитель физики: Ребята, давайте подумаем, что является причиной трех состояний одного вещества? (беседа с учащимися, демонстрация слайда).
Слайд №15.
Вывод: Причиной агрегатных состояний веществ является взаимное расположение и взаимодействие молекул.
2. Отчет по исследовательской деятельности учащихся.
Учитель химии: Ребята! При подготовке к этому уроку, заранее вы были поделены на группы, которые провели мини-исследования на тему: «Агрегатное состояние вещества». Слово предоставляется группе №1.
А) Выступление представителя группы «Туман».
Учащийся: тема нашего мини-исследования – «Изучение свойств веществ в газообразном состоянии».
Слайды №16-19.
Наиболее характерным свойством газов является их сжимаемость и способность расширяться. Газы не имеют собственной формы и расширяются до тех пор, пока не заполнят весь сосуд, принимая его форму. Газы не имеют собственного объема, объем газа определяется объемом сосуда, в котором он находится.
Газообразные вещества кажутся невесомыми. «Невесомость» газов – понятие относительное. В этом легко убедиться на следующем эксперименте.
Я покажу вам демонстрационный эксперимент, который называется «Переливание» углекислого газа из колбы в колбу на уравновешенных весах».
На весах уравновешивают две химических колбы. Одину из колб, не снимая с весов, наполняют углекислым газом, который получают при взаимодействии соляной кислоты и мела. (пауза, до тех пор, пока не начнет опускаться чашка весов одна из чашек весов)
Через некоторое время чашка весов, на которой находится эта колба, опускается, так как молекулярная масса углекислого газа равна 44 единицам атомной массы и гораздо больше, чем молекулярная масса воздуха, равная 29.
Наличие углекислого газа в стакане можно доказать с помощью горящей лучины. (опускает горящую лучину в колбу с углекислым газом, она тухнет, т.к. углекислый газ не поддерживает горения)
На основании эксперимента можно сделать вывод: Газы не имеют собственной формы и объем, но имеют вес.
Слайд №20.
Ф И З К У Л Ь Т М И Н У Т К А «Танцуют все!». Проводит ученик.
Б) Выступление представителя группы «Капелька».
Учащийся: Наша группа исследовала «Свойства веществ в жидком состоянии».
Слайды №21-24.
Подобно газам жидкости не имеют собственной формы и подобно газам принимают форму того сосуда, в котором они находятся.
Демонстрация опыта «Переливание жидкости в сосуды разной формы».
В отличие от газов, жидкости имеют вполне определенный собственный объем. Сжимаемость жидкостей, в отличие от газов, очень мала, и для того, чтобы заметно сжать жидкость, необходимо очень высокое давление. Это свойство применяют в гидравлических прессах.
В) Выступление представителя группы «Льдинка».
Учащийся: Мы работали над изучением «Свойств веществ в твердом состоянии».
Слайды №25-27.
Твердые тела отличаются от газов и жидкостей наличием собственной формы и собственного объема. Даже при очень высоких давлениях их сжимаемость очень мала.
(Ученик демонстрирует твердые вещества: соли (поваренная соль, медный купорос), щелочь (гидроксид натрия или калия), воду (лед), йод, металлы).
Существуют вещества настолько вязкие, что надолго сохраняют свою форму. Значит, их можно отнести к твердым веществам. Однако, подобно жидкостям, расположение частиц в таких веществах строго не упорядочено. Такие вещества называются аморфными.
(Словарная работа: Аморфными называются тела, которые не имеют кристаллического строения.)
Слайд №28.
К аморфным веществам можно отнести смолу, янтарь, пластмассу, стекло и др.
III. Систематизация знаний учащихся о свойствах веществ в различных агрегатных состояниях.
Учитель физики:
А теперь обобщим и систематизируем полученные на уроке знания, заполнив таблицу.
А) Самостоятельная работа учащихся.
Задание: Заполните таблицу: Слайд №29.
Характеристика свойств веществ
Характеристики или свойство