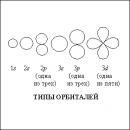
Правило вант гоффа гласит что
| FilIgor | Дата: Четверг, 08.11.2012, 11:41 | Сообщение # 1 | ||||
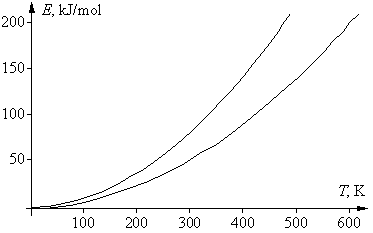
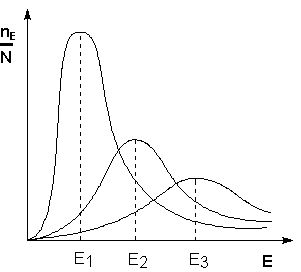
| 9. Скорость химических реакций. Правило Вант-Гоффа. Закон действия масс. 10.1. Зависимость скорости реакции от температуры. При 0 о С реакция, для которой температурный коэффициент равен 2, заканчивается за 120 сек. | 9.2., 9.2.1. Скорость и температурный коэффициент. Задание 2. За какое время закончится реакция при 30 о С, если при 10 градусах она заканчивется за 20 минут? По уравнению Вант-Гоффа, скорость возрастет в Реакция закончится за t = 20/4 = 5 минут. При 0 градусов Цельсия реакция заканчивается за 1 час 21 минуту, а при 40 оС за 1 минуту. | 9.3. Скорость и давление. Во сколько раз изменится скорость реакции 2СО(г.) + О2(г.) = 2СО2 при увеличении давления в 2 раза и неизменной температуре? Запишем закон действия масс для данной реакции. Увеличение давления в 2 раза означает увеличение концентраций в 2 раза. Аналогично предыдущему примеру, запишем: | 9.4. Скорость и концентрация. Во сколько раз уменьшится скорость реакции 2NO + O2 = 2NO2 при разбавлении смеси реагирующих газов в 3 раза? То есть, уменьшится в 27 раз. Реакция идет по уравнению: А + 2B ↔ C; константа ее скорости при определенной температуре равна 0,4, а начальные концентрации составляли (моль/дм 3 ): [А] =0,3 и [В]= 0,5. Вычислите скорость этой реакции при той же температуре в начальный момент и после того, как прореагирует 0,1 моль/дм 3 вещества А. | 9.5. Уравнение Аррениуса. Рассчитать температурный коэффициент Вант-Гоффа в интервале 10-50 градусов Цельсия, если энергия активации равна 85 кДж/моль. Определим коэффициент Вант-Гоффа. В интервале 12-52 градусов Цельсия коэффициент Вант-Гоффа составляет 3,5. Найти энергию активации. Вант-Гоффа правилоПравило Вант-Гоффа — эмпирическое правило, позволяющее в первом приближении оценить влияние температуры на скорость химической реакции в небольшом температурном интервале (обычно от 0 °С до 100 °С). Я.Х. Вант-Гофф на основании множества экспериментов сформулировал следующее правило: При повышении температуры на каждые 10 градусов константа скорости гомогенной элементарной реакции увеличивается в два — четыре раза. Уравнение, которое описывает это правило следующее: где V2-скорость реакции при данной температуре(T2), V1-скорость реакции при температуре T1, Y-температурный коэффициент реакции (если он равен 2, например, то скорость реакции будет увеличиватся в 2 раза при повышении температуры на 10 градусов). Из уравнения Вант-Гоффа температурный коэффициент вычисляется по формуле: Смотреть что такое «Вант-Гоффа правило» в других словарях:Вант-Гоффа правило — ЭМБРИОЛОГИЯ ЖИВОТНЫХ ВАНТ ГОФФА ПРАВИЛО – изменение температуры (если оно не выходит за определенные для каждого вида животного рамки нормальных температур) не приводит к качественным изменениям в развитии, а лишь сказывается на темпе дробления … Общая эмбриология: Терминологический словарь Вант-Гоффа правило — приближённое правило, согласно которому при повышении температуры на 10°С скорость химической реакции увеличивается примерно в 2 4 раза. Найдено Я. Х. Вант Гоффом. См. Кинетика химическая … Большая советская энциклопедия Правило Вант-Гоффа — Правило Вант Гоффа эмпирическое правило, позволяющее в первом приближении оценить влияние температуры на скорость химической реакции в небольшом температурном интервале (обычно от 0 °C до 100 °C). Я. Х. Вант Гофф на… … Википедия ПРАВИЛО ВАНТ-ГОФФА-АРРЕНИУСА — правило, сформулированное Вант Гоффом и дополненное Аррениусом, которое в биологической модификации гласит, что скорость обмена веществ организмов при повышении температуры на 10° может быть повышена в 2 3 раза. Экологический энциклопедический… … Экологический словарь правило Вант-Гоффа — Правило Вант Гоффа: при повышении температуры на каждые 10° скорость большинства химических реакций увеличивается в 2 4 раза. Общая химия : учебник / А. В. Жолнин [1] … Химические термины правило Вант-Гоффа — van’t Hofo dėsnis statusas T sritis fizika atitikmenys: angl. Van’t Hoff law vok. Van’t Hoffsche Regel, f; Van’t Hoffsches Gesetz, m rus. закон Вант Гоффа, m; правило Вант Гоффа, m pranc. loi de Van’t Hoff, f … Fizikos terminų žodynas правило Вант-Гоффа — van’t Hofo taisyklė statusas T sritis Standartizacija ir metrologija apibrėžtis Teiginys, kuriuo teigiama, kad padidinus temperatūrą 10 laipsnių reakcijos sparta padidėja nuo 2 iki 4 kartų. atitikmenys: angl. van’t Hoff law; van’t Hoff rule vok.… … Penkiakalbis aiškinamasis metrologijos terminų žodynas правило Вант-Гоффа — van t Hofo taisyklė statusas T sritis chemija apibrėžtis Pakėlus temperatūrą 10 laipsnių reakcijos greitis padidėja 2–4 kartus. atitikmenys: angl. van t Hoff law; van t Hoff rule rus. правило Вант Гоффа … Chemijos terminų aiškinamasis žodynas закон Вант-Гоффа — van’t Hofo dėsnis statusas T sritis fizika atitikmenys: angl. Van’t Hoff law vok. Van’t Hoffsche Regel, f; Van’t Hoffsches Gesetz, m rus. закон Вант Гоффа, m; правило Вант Гоффа, m pranc. loi de Van’t Hoff, f … Fizikos terminų žodynas ПРАВИЛО — (1) буравчика определяет направление вектора напряжённости магнитного поля прямолинейного проводника с постоянным током. Если буравчик ввёртывается по направлению тока, то направление его вращения определяет направление магнитных силовых линий… … Большая политехническая энциклопедия Правило вант гоффа гласит чтоФИЗИЧЕСКАЯ И КОЛЛОИДНАЯ ХИМИЯ Конспект лекций для студентов биофака ЮФУ (РГУ) 2.1 СКОРОСТЬ ХИМИЧЕСКОЙ РЕАКЦИИ 2.1.9 Влияние температуры на константу скорости реакции Константа скорости реакции есть функция от температуры; повышение температуры, как правило, увеличивает константу скорости. Первая попытка учесть влияние температуры была сделана Я. Г. Вант-Гоффом, который сформулировал следующее эмпирическое правило: При повышении температуры на каждые 10 градусов константа скорости элементарной химической реакции увеличивается в 2 – 4 раза. Однако правило Вант-Гоффа применимо лишь в узком температурном интервале, поскольку температурный коэффициент скорости реакции γ сам является функцией от температуры; при очень высоких и очень низких температурах γ становится равным единице (т.е. скорость химической реакции перестает зависеть от температуры). 2.1.10 Уравнение Аррениуса Очевидно, что взаимодействие частиц осуществляется при их столкновениях; однако число столкновений молекул очень велико и, если бы каждое столкновение приводило к химическому взаимодействию частиц, все реакции протекали бы практически мгновенно. С. Аррениус постулировал, что столкновения молекул будут эффективны (т.е. будут приводить к реакции) только в том случае, если сталкивающиеся молекулы обладают некоторым запасом энергии – энергией активации. Энергия активации есть минимальная энергия, которой должны обладать молекулы, чтобы их столкновение могло привести к химическому взаимодействию. Рассмотрим путь некоторой элементарной реакции Поскольку химическое взаимодействие частиц связано с разрывом старых химических связей и образованием новых, считается, что всякая элементарная реакция проходит через образование некоторого неустойчивого промежуточного соединения, называемого активированным комплексом: Образование активированного комплекса всегда требует затраты некоторого количества энергии, что вызвано, во-первых, отталкиванием электронных оболочек и атомных ядер при сближении частиц и, во-вторых, необходимостью построения определенной пространственной конфигурации атомов в активированном комплексе и перераспределения электронной плотности. Таким образом, по пути из начального состояния в конечное система должна преодолеть своего рода энергетический барьер. Энергия активации реакции приближённо равна превышению средней энергии активированного комплекса над средним уровнем энергии реагентов. Очевидно, что если прямая реакция является экзотермической, то энергия активации обратной реакции Е’А выше, нежели энергия активации прямой реакции EA. Энергии активации прямой и обратной реакции связаны друг с другом через изменение внутренней энергии в ходе реакции. Вышесказанное можно проиллюстрировать с помощью энергетической диаграммы химической реакции (рис. 2.5). Рис. 2.5 Энергетическая диаграмма химической реакции. Поскольку температура есть мера средней кинетической энергии частиц, повышение температуры приводит к увеличению доли частиц, энергия которых равна или больше энергии активации, что приводит к увеличению константы скорости реакции (рис.2.6): Поскольку константа равновесия есть отношение констант скоростей прямой и обратной реакции, можно переписать выражение (II.31) следующим образом: Представив изменение энтальпии реакции ΔHº в виде разности двух величин E1 и E2, получаем: Здесь С – некоторая константа. Постулировав, что С = 0, получаем уравнение Аррениуса, где EA – энергия активации : После неопределенного интегрирования выражения (II.35) получим уравнение Аррениуса в интегральной форме: Рис. 2.7 Зависимость логарифма константы скорости химической Здесь A – постоянная интегрирования. Из уравнения (II.37) нетрудно показать физический смысл предэкспоненциального множителя A, который равен константе скорости реакции при температуре, стремящейся к бесконечности. Как видно из выражения (II.36), логарифм константы скорости линейно зависит от обратной температуры (рис.2.7); величину энергии активации EA и логарифм предэкспоненциального множителя A можно определить графически (тангенс угла наклона прямой к оси абсцисс и отрезок, отсекаемый прямой на оси ординат). Зная энергию активации реакции и константу скорости при какой-либо температуре T1, по уравнению Аррениуса можно рассчитать величину константы скорости при любой температуре T2: ВАНТ-ГОФФА ПРАВИЛОВАНТ-ГОФФА ПРАВИЛО. Почти все химические реакции при повышении температуры идут быстрее. Зависимость скорости реакции от температуры описывается уравнением Аррениуса: Однако из уравнения Аррениуса следует, что температурный коэффициент реакции зависит как от энергии активации, так и от абсолютной температуры. Для данной реакции с определенным значением Еа ускорение при повышении температуры на 10° будет тем больше, чем ниже температура. Это почти очевидно и без расчетов: повышение температуры от 0 до 10° С должно сказаться на скорости реакции значительно сильнее, чем такое же повышение температуры, например, от 500 до 510° С. С другой стороны, для данного температурного интервала ускорение реакции будет тем сильнее, чем больше ее энергия активации. Так, если энергия активации реакции мала, то такая реакция идет очень быстро, и при повышении температуры на 10° С ее скорость почти не изменяется. Для таких реакций температурный коэффициент намного меньше 2. Для реакций же с большой энергией активации, которые при невысоких температурах идут медленно, ускорение при повышении температуры на 10° С может значительно превысить 4-кратное. Например, реакция диоксида углерода со щелочным раствором с образованием гидрокарбонат-иона (СО2 + ОН® НСО3 – ) имеет энергию активации 38,2 кДж/моль, поэтому при повышении температуры, например, от 50 до 60° С эта реакция ускорится всего в 1,5 раза. В то же время реакция распада этилбромида на этилен и бромоводород (С2Н5Вr ® С2Н4 + НВr) с энергией активации 218 кДж/моль ускорится при повышении температуры от 100 до 110 o С в 6,3 раза (правда, в этом интервале температур реакция идет очень медленно). Кинетика реакции атомов водорода с этаном H + C2H6 ® H2 + C2H5 была изучены в широком температурном интервале – от 300 до 1100 К (27–827° С). Для этой реакции Eа = 40,6 кДж/моль. Следовательно, повышение температуры на 10° вызовет увеличение скорости реакции в 1,7 раза в интервале 300–310 K и только в 1,04 раза в интервале 1090–1100 K. Так что при высоких температурах скорость этой реакции практически не зависит от температуры. А для реакции присоединения атома водорода к двойной связи H + C2H4 ® C2H5 энергия активации мала (Eа = 3,4 кДж/моль, так что ее скорость слабо зависит от температуры в широком температурном интервале. И только при температурах намного ниже 0° С начинает сказываться наличие активационного барьера. Подобных примеров можно привести множество. Очевидно, что правило Вант-Гоффа противоречит не только уравнению Аррениуса, но и многим экспериментальным данным. Откуда же оно взялось и почему нередко выполняется? Если посмотреть, какие реакции «укладываются» в указанную довольно узкую область, то окажется, что все эти реакции идут не слишком быстро и не слишком медленно, а с удобной для измерения (при данной температуре) скоростью. Скорость только таких реакций и могли изучать химики во времена Вант-Гоффа. Например, если энергия активации была невелика (меньше 50 кДж/моль), то такая реакция при комнатной температуре заканчивалась за 1–2 секунды; поэтому для изучения ее кинетики следовало значительно понизить температуру, чтобы реакция проходила не быстрее, чем за 10–20 минут. Только в этом случае химики 19 в. успевали отбирать пробы по ходу реакции и анализировать изменение в них концентрации реагентов. Других способов изучения скорости реакции в то время не было. Если это не удавалось (например, водный раствор замерзал), то скорость такой реакции не изучали. Если же энергия активации реакции была велика и при комнатной температуре она шла слишком медленно (многие сутки, или даже недели), то температуру повышали, чтобы реакция шла с удобной для измерения скоростью. И здесь были свои ограничения – например, раствор мог закипеть, т.е. в любом случае исследователи фактически «подстраивали» изучаемую реакцию под область между двумя параболами. Сейчас химики имеют возможность с помощью различных приборов экспериментально изучать и очень быстрые (идущие в микросекундной области), и очень медленные реакции, для которых температурный коэффициент может быть значительно меньше 2 или значительно больше 4. Поэтому правило Вант-Гоффа, которое, в отличие от уравнения Аррениуса, не имеет четкого физического смысла, представляет лишь чисто исторический интерес и в современной науке не используется. В подавляющем большинстве учебников и монографий по химической кинетике, а также в 5-томной Химической Энциклопедии это правило даже не упоминается. И, тем не менее, если изучаемая реакция идет с удобной для измерения скоростью, например, заканчивается за 30–40 мин, а энергия активации ее еще не измерена, то для предварительной грубой оценки зависимости скорости такой реакции от температуры можно использовать правило Вант-Гоффа. Поэтому это правило приводится во всех школьных учебниках химии. Правило Вант-ГоффаИз Википедии — свободной энциклопедииПравило Вант-Гоффа — эмпирическое правило, позволяющее в первом приближении оценить влияние температуры на скорость химической реакции в небольшом температурном интервале (обычно от 0 °C до 100 °C). Якоб Хендрик Вант-Гофф на основании множества экспериментов сформулировал следующее правило: При повышении температуры на каждые 10 градусов константа скорости гомогенной элементарной реакции увеличивается в два—четыре раза. Уравнение, которое описывает это правило, следующее: V 2 = V 1 ⋅ γ T 2 − T 1 10 <\displaystyle V_<2>=V_<1>\cdot \gamma ^<\frac Следует помнить, что правило Вант-Гоффа применимо только для реакций с энергией активации 60-120 кДж/моль в температурном диапазоне 10-400 o C. Правилу Вант-Гоффа также не подчиняются реакции, в которых принимают участие громоздкие молекулы, например, белки в биологических системах. Температурную зависимость скорости реакции более корректно описывает уравнение Аррениуса. Из уравнения Вант-Гоффа температурный коэффициент вычисляется по формуле: γ = ( V 2 / V 1 ) 10 / ( T 2 − T 1 ) <\displaystyle \gamma =(V_<2>/V_<1>)^<10/(T_<2>-T_<1>)>> |


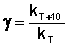 (II.29)
(II.29)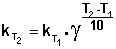 (II.30)
(II.30)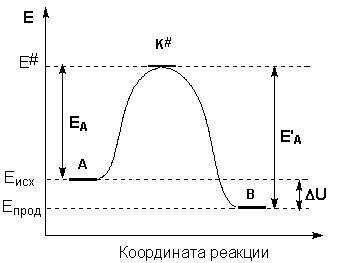
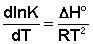 (II.31)
(II.31)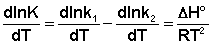 (II.32)
(II.32)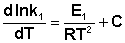 (II.33)
(II.33)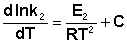 (II.34)
(II.34)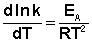 (II.35)
(II.35)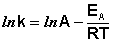 (II.36)
(II.36)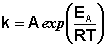 (II.37)
(II.37)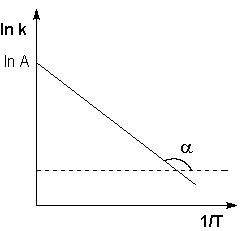
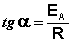 (II.38)
(II.38)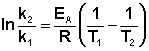 (II.39)
(II.39)