Подковообразная почка у ребенка что делать
Подковообразная почка
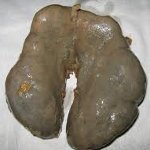
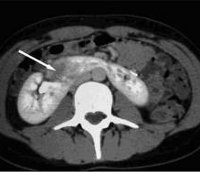
Подковообразная почка – это врожденная аномалия, при которой обе почки сращиваются между собой в области нижнего или верхнего полюса с образованием перешейка. Патология часто осложняется пиелонефритом, мочекаменной болезнью, гидронефрозом и другими заболеваниями мочевыделительной системы. В используется УЗИ, урография, пиелография, компьютерная томография почек. Хирургическое лечение показано при развитии в измененной почке урологического заболевания, требующего оперативной тактики.
МКБ-10
Общие сведения
В некоторых случаях почки срастаются между собой медиальными поверхностями (т. н. галетообразная почка), противоположными (верхний с нижним) полюсами (S или L-образная почка), обоими полюсами и срединной поверхностью (дискообразная почка). Патология может сочетаться с другими врожденными пороками – поликистозом почек, гидроцефалией, расщеплением позвоночника, пороками аноректальной системы, аномалиями скелета (расщелиной губы и нёба, полидактилией, косолапостью).
Причины
Формирование подковообразной почки является следствием дисэмбриогенеза. У плода развитие почки проходит три последовательных стадии: предпочка (пронефрос), первичная почка (мезонефрос) и вторичная почка. Параллельно с развитием вторичной почки происходит миграция парного органа в область будущего ложа в поясничной области. Окончательное формирование и фиксация почки заканчивается уже после рождения. Аномалия образуется в результате нарушений процессов миграции и ротации почки, обусловленных болезнями матери, инфекциями, воздействием на плод вредных химических или лекарственных веществ.
Патанатомия
Симптомы подковообразной почки
В связи со спецификой топографии, иннервации и кровоснабжения аномалия может сопровождаться характерным болевым симптомокомплексом: болью в области пупка, возникающей при перегибе или разгибании туловища, в пояснице, внизу живота, в эпигастрии после физической нагрузки. Сдавление перешейком почки нервных сплетений корня брыжейки может вызывать запоры, спастические боли в кишечнике, нарушение кишечной перистальтики.
На фоне постоянного боевого синдрома может развиваться эмоциональная неустойчивость, неврастения, истерия. Венозная внутрипочечная гипертензия, обусловленная сдавлением сосудов, иногда сопровождается гематурией. При сдавливании нижней полой вены развивается венозный застой в нижней половине тела: отеки нижних конечностей, варикоз вен нижних конечностей и малого таза, асцит. У женщин возможно нарушение менструального цикла и преждевременные роды. В ряде наблюдений подковообразная почка не сопровождается никакой симптоматикой и выявляется случайно.
Осложнения
Сжатие перешейком начального отдела мочеточника создает препятствие для оттока мочи из лоханок, что приводит к развитию:
Существуют сведения, что в перешейке подковообразной почки чаще развивается опухолевая трансформация клеток и рак почки.
Диагностика
План диагностического обследования включает УЗИ, УЗДГ, экскреторную урографию либо ретроградную пиелографию, почечную артериографию, сцинтиграфию, компьютерную томографию. Урограммы позволяют рассмотреть низкое расположение органа, ограниченную подвижность, наслоение теней нижних полюсов почки на контур позвоночного столба, тень перешейка. При ретроградной пиелографии в первые минуты визуализируется четкий силуэт подковообразной почки и ее перешейка, низкое положение почечных лоханок, аномальное расположение чашечек.
При УЗИ почек определяется отсутствие смещаемости почечных контуров, нетипичное расположение почечных лоханок и измененная форма чашечек; при УЗДГ выявляется аномальное кровоснабжение подковообразной почки. Выполнение нефросцинтиграфии фиксирует характерное накопление радионуклидного препарата в виде подковы, огибающей позвоночный столб. Почечная ангиография выполняется для исследования сосудистой архитектоники, определения количества, локализации и наличия дополнительных сосудов, толщины и васкуляризации перешейка, что имеет важное значения при планировании операции.
Лечение подковообразной почки
При отсутствии клинических проявлений лечения подковообразной почки не требуется. Такие пациенты подлежат наблюдению врача-уролога для предотвращения развития вторичных осложнений. При пиелонефрите, осложняющем течение подковообразной почки, назначается соответствующее курсовое патогенетическое лечение. В случае развития болевой симптоматики, гидронефротической трансформации, камнеобразования, опухолей почки показана дифференцированная хирургическая тактика.
При болях и нарушениях уродинамики, обусловленных давлением перешейка, производится его рассечение и разведение концов почки с фиксацией в новом положении. При поражениях одной из половин подковообразной почки и потере ее функций выполняется геминефрэктомия. При выявлении камней в подковообразной почке используют различные методы их удаления, включающие дистанционную литотрипсию, перкутанную нефролитотрипсию, пиелолитотомию, нефролитотомию.
Гидронефроз у детей: почему не стоит затягивать с обращением к врачу
Когда болеют дети, тяжело вдвойне. К счастью, сегодня многие врожденные патологии поддаются 100% коррекции. К их числу относится и такое тяжелое заболевание мочеполовой системы, как гидронефроз. О том, каким бывает гидронефроз, как его диагностируют и какие современные методики успешно применяют для лечения болезни, проекту «Москва — столица здоровья» рассказал Артур Владимирович Кулаев — детский хирург, уролог-андролог отделения детской урологии и андрологии Морозовской детской больницы.
Что представляет собой гидронефроз?
Гидронефроз — это заболевание почки, которое характеризуется расширением коллекторной системы и истончением ее паренхимы (основной ткани почки). Высокое давление, которое создается в лоханках и чашечках, отрицательно влияет на рабочую часть почки. Истончение паренхимы и ухудшение кровотока внутри нее вызывают нарушение функции почки, и, в итоге, могут привести к ее гибели.
Какие виды заболевания существуют?
Гидронефроз бывает двух видов: врожденный или приобретенный. Когда речь идет о детской урологии, чаще встречается врожденный гидронефроз. Как правило, заболевание вызвано стенозом (сужением) мочеточника в том месте, где он отходит от лоханки, но возможны и другие причины.
Что касается приобретенного гидронефроза, то он появляется в старшем возрасте, когда у детей развивается, например, мочекаменная болезнь. В этом случае нарушение проходимости вызывают конкременты (т. е. камни) в области верхней трети мочеточника. Также в основе приобретенного гидронефроза могут лежать различные онкологические заболевания, например, когда опухоль снаружи почки сдавливает зону отхождения мочеточника от лоханки.
Каковы симптомы гидронефроза?
К сожалению, специфических симптомов гидронефроза не существует. Единственный признак, который может говорить о том, что у ребенка критически расширилась лоханка — так называемый блок почки. Это комплекс симптомов, проявляющийся болью в поясничной области, тошнотой и рвотой. При их наличии следует немедленно обратиться за помощью к врачу, который проведет дифференциальную диагностику.
Как лечат гидронефроз почек у детей?
Мы лечим гидронефроз оперативным путем. Оперативные вмешательства при гидронефрозе делятся на две группы: это лапароскопические операции и открытые. Они направлены на то, чтобы восстановить проходимость мочевых путей, т. е. убрать препятствие, которое не дает моче без проблем оттекать из лоханки в мочеточник. В Морозовской больнице, начиная с 2010 года, отдается предпочтение именно лапароскопическим операциям, при которых травматичность для ребенка минимальна, а следовательно, менее выражен болевой синдром и короче период госпитализации.
Расскажите подробнее, как проходит лапароскопическая операция?
Правильное название операции «лапароскопическая пластика лоханки мочеточника» (или лапароскопическая пиелопластика). Лапароскопическая пиелопластика обладает высокой эффективностью и в данный момент считается золотым стандартом в лечении гидронефроза. Чем она отличается от открытой операции? Открытое оперативное вмешательство при гидронефрозе выполняется при помощи обычных хирургических инструментов: проводится разрез в поясничной области или на животе, а затем из этого разреза осуществляется реконструкция.
При лапароскопической пиелопластике операция проходит практически без крови: мы используем оптику, которую вводим в живот ребенка через 3 небольших прокола, и манипуляторы — специальные лапароскопические инструменты. Далее смотрим на монитор и работаем руками внутри брюшной полости ребенка. Операция выполняется под общей анестезией и может занять от 1,5 до 3 часов, в зависимости от того, как почка располагается по отношению к нашей камере (повернута она или нет и т. п.).
В чем залог успеха оперативного лечения гидронефроза в Морозовской детской клинической больнице?
Если коротко, то я бы выделил три слагаемых успеха: современное оборудование, профессионализм хирургов и мультидисциплинарный подход к лечению. У нас накоплен самый большой опыт из всех российских клиник в лечении гидронефроза с использованием лапароскопических технологий. Мы активно работаем с 3D-лапароскопией. Это уникальное оборудование, которое позволяет хирургу увидеть трехмерную картину и более точно выполнять движения, накладывать швы и делать другие манипуляции. Нам лучше видно и более понятно, что мы делаем, да и трехмерная картина для человеческого глаза более привычна. В итоге риск кровотечений, равно как и других послеоперационных осложнений, сводится практически к нулю.
Насколько операция по поводу гидронефроза у ребенка в Морозовской больнице доступна иногородним?
Все виды лапароскопической пиелопластики в Морозовской больнице выполняются для пациентов бесплатно, вне зависимости от их места жительства. Единственное условие — это наличие полиса ОМС.
Сколько времени уйдет на восстановление ребенка после лапароскопической пиелопластики?
В среднем, 5 — 7 дней. В течение первых суток после операции ребенку прописан постельный режим. Кроме того, пациент находится под круглосуточным наблюдением. Затем на протяжении 2 — 3 дней ребенок получает необходимую антибактериальную и инфузионную терапию (в виде капельниц), после чего его выписывают домой.
В чем на сегодняшний день заключается профилактика гидронефроза у детей?
К сожалению, болезнь нельзя предотвратить с помощью приема лекарств. Пользуясь случаем, я хочу обратиться ко всем родителям, столкнувшимся с проблемой гидронефроза у ребенка: не надо бояться. Просто как можно раньше обратитесь за помощью к профессионалам.
Современный подход к диагностике и лечению мочекаменной болезни у детей
Проблема детского здоровья сегодня не может быть решена глобально без анализа и обсуждения вопросов, связанных с лечением отдельных заболеваний. В урологической практике мочекаменная болезнь занимает одно из первых мест по частоте и тяжести клинического
Проблема детского здоровья сегодня не может быть решена глобально без анализа и обсуждения вопросов, связанных с лечением отдельных заболеваний. В урологической практике мочекаменная болезнь занимает одно из первых мест по частоте и тяжести клинического течения. Более того, настораживает тот факт, что за последнее десятилетие в России отмечен рост заболеваемости не только среди взрослого населения, но и среди детей практически всех возрастных групп. Так, по данным Госкомстата, с 1996 по 2004 г. в младшей возрастной группе на 100 000 населения число случаев мочекаменной болезни выросло с 17,8 до 20,1 (первично выявленной — с 5,4 до 6,0), в подростковой группе — с 25,4 до 28,9 (первично выявленной — с 68,7 до 81,7).
Еще большую значимость проблеме придает тот факт, что у детей до настоящего времени лечение мочекаменной болезни осуществляется только при помощи открытого оперативного вмешательства, производимого детскими хирургами без участия урологов. Как показал анализ историй болезни 1200 детей, прошедших лечение в детском отделении Научно-исследовательского института урологии, 49,5% из них перенесли от 1 до 5 оперативных вмешательств на мочевых путях, 57% имели снижение функции почки от 15 до 70% на стороне поражения, 96,2% имели инфекцию мочевых путей, из них 48,5% с титром бактериурии 105 и выше.
Среди факторов, провоцирующих увеличение частоты уролитиаза, можно упомянуть и современные условия жизни: гиподинамию, ведущую к нарушению фосфорно-кальциевого обмена, характер питания (обилие белка в пище, либо однообразная диета). Все вышесказанное позволило назвать это нарушение обмена веществ болезнью цивилизации. К развитию мочекаменной болезни предрасполагают также и другие факторы: климатические, географические и жилищные условия, профессия, вредные привычки, особенно в период беременности. Большое значение в развитии заболевания имеют наследуемые генетические факторы. Так, по данным J. A. Camacho Diaz [11] 49% обследованных детей имели семейный анамнез мочекаменной болезни. Вот почему людям, планирующим рождение ребенка, необходимо быть особенно требовательными к своему образу жизни: состояние их здоровья, бесспорно, скажется на формировании еще неродившегося человека.
Доминирующими причинами образования камней в почках у детей являются изменения местного характера: анатомические и патологические изменения в верхних мочевыводящих путях, нефроптоз и другие, приводящие к нарушению нормального оттока мочи из почек, а также метаболические и сосудистые нарушения в почке — до 30% (А. Ю. Павлов, 1998; R. M. Driano et al. 1996; A. Demircin et al., 1997), инфекции мочевыводящих путей 31–38% (Н. К. Дзеранов, 2004; J. A. Camacho Diaz, 1996; S. Seren et al., 2002). Любые изменения в анализах мочи у детей требуют проведения тщательного урологического обследования с использованием современных технологий. Так, анализ, проведенный нами более чем у 1000 детей с мочекаменной болезнью, показал, что аномалии развития имели место в 31,6% случаев в виде следующих нарушений: пузырно-мочеточниковый рефлюкс, пузырно-мочеточниково-почечный рефлюкс, ахалазия, гидронефроз, дисплазия мочеточника, стриктура лоханочно-мочеточникового сегмента, полное и неполное удвоение почек и мочеточников, дистопия, подковообразная почка и др.
Мочевая инфекция, являющаяся одной из причин камнеобразования, существенно усугубляет течение заболевания в 68% случаев. Она является важным дополнительным местным фактором в возникновении и поддержании хронического (рецидивирующего) течения мочекаменной болезни из-за неблагоприятного влияния на мочу продуктов метаболизма ряда микроорганизмов, способствующих резкому ее ощелачиванию и бурному образованию аморфных кристаллов фосфата кальция, а при наличии ядра кристаллизации — и быстрому росту камня. Оксалаты кальция являются доминирующими мочевыми камнями — 70–90% от всех камней (рис. 1). Инфицированные камни встречаются в 68% случаев и чаще наблюдаются у девочек с высоким риском воспалительных осложнений. При неполном удалении инфицированных камней риск рецидива крайне высок (до 70%). Метафилактика должна быть прежде всего направлена на борьбу с инфекцией мочевых путей — антибактериальная терапия назначается только по результату посева мочи с определением чувствительности к антибиотикам.
К факторам риска рецидива камней относятся:
Почки, являющиеся конечным органом-регулятором очищения крови и поддержания водно-электролитного баланса, чутко реагируют на любые изменения в жизнедеятельности организма и заболевания, которые приводят к метаболическим нарушениям, лежащим в основе мочекаменной болезни. Поэтому обследование детей, страдающих мочекаменной болезнью, должно включать в себя тщательное изучение анамнеза не только ребенка, но и родителей. Необходимо также изучение анатомо-функционального состояния почек, мочевых путей, функции желудочно-кишечного тракта и других органов, которые могут участвовать в процессе камнеобразования.
Для детей, страдающих мочекаменной болезнью, обязательным является диспансерное наблюдение и лечение у детского уролога в течение как минимум 5 лет, а метафилактику следует проводить только изучив химический состав камня и проводя контрольные исследования обменных нарушений — их следует выполнять как минимум 2 раза в год.
В целом у пациентов со впервые выявленными камнями существует 10-процентная вероятность появления нового камня в течение года или 50-процентная вероятность рецидива в течение 5 лет — при отсутствии медицинского обследования и лечения (D. A. Tolley, 2002).
Диагностика камней любого отдела мочевыделительной системы на сегодняшний день не вызывает каких-либо трудностей, в связи с широким внедрением в клиническую практику современных ультразвуковых и рентгено-радиологических методов. Однако, несмотря на внедрение в клиническую практику новых технологий в виде ударно-волновой дистанционной литотрипсии (ДЛТ), чрескожной и трансуретральной контактной литотрипсии и литоэкстракции, сегодня, как и прежде, необходим минимальный алгоритм обследования, поскольку новые технологии, как и открытое оперативное вмешательство, имеют определенные противопоказания при некоторых клинических формах мочекаменной болезни. Основными показателями, определяющими выбор тактики лечения, являются данные:
Так, выраженное снижение функции почки (на 50% и более) является противопоказанием к проведению ДЛТ крупных и цистиновых камней (когда требуется три и более сеансов). Острый калькулезный пиелонефрит также является противопоказанием к назначению дистанционной и эндоскопической контактной литотрипсии. Диагностированные стрикутры или аномалии верхних мочевых путей являются показанием к открытому оперативному удалению камней с реконструктивной коррекцией выявленных аномалий.
Возможно ли применение новых технологий в лечении мочекаменной болезни у детей и в чем особенности и преимущества их использования у детей? Так, ДЛТ применяли у 70% из 1240 детей, прошедших лечение в НИИ урологии по поводу мочекаменной болезни. Перкутанная эндоскопическая контактная литотрипсия использовалась в 10,2% случаев, трансуретральная контактная литотрипсия и литоэкстракция — у 6,0% пациентов, открытое оперативное вмешательство — в 13,8% случаев.
ДЛТ. На сегодняшний день этот метод является единственным неинвазивным и наименее травматичным. На первых литотриптерах фирмы Дорнье проводить ДЛТ у детей считалось опасным, так как даже у взрослых из-за мощной энергии ударных волн образовались различные травматические гематомы в зоне прохождения ударной волны. Проведенные в НИИ урологии (Москва) многочисленные экспериментальные исследования на животных по воздействию ударно-волновых импульсов на биологические ткани позволили найти оптимальные режимы, при которых отсутствовал травматический эффект, но сохранялся режим разрушения камней. Именно эти исследования легли в основу создания отечественного литотриптера, на котором осуществляются практически все дробления камней не только в НИИ урологии, но и в других региональных отделениях ДЛТ.
К особенностям применения ДЛТ у детей следует отнести близкое прилежание почки к поверхности кожи и тот факт, что процесс развития почки у ребенка не завершен. Вот почему у детей можно осуществлять дробление на аппаратах с минимальным отрицательным давлением и с использованием преимущественно низкоэнергетичных импульсов. Уже на ранних стадиях исследования анализ показал, что у детей камни разрушаются значительно легче и при меньшем количестве импульсов, чем у взрослых, даже при минимальных режимах литотриптера.
Применение ДЛТ in situ при лечении детей оказывается достаточно эффективным из-за хрупкости камней и эластичности мочевых путей [1–3]. Более того, у детей из-за более выраженных ретенционных особенностей фрагменты, а также «каменные дорожки» начинают отходить в первые сутки после ДЛТ и отходят в более короткие сроки и с меньшими болевыми ощущениями, чем у взрослых.
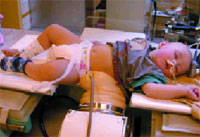 |
| Рисунок 2. Ребенок 8 мес во время дробления коралловидного камня левой почки |
На сегодняшний день с применением ДЛТ в Центре литотрипсии МЗиСР прошли лечение более 900 детей с различными формами мочекаменной болезни. Эффективность ДЛТ составила 96,3%. Самому маленькому пациенту с коралловидным камнем было 7 мес. Процесс дробления коралловидного камня показан на рисунках 2, 3. В возрасте до 3 лет получили необходимое лечение 42 ребенка. 239 детей имели рецидивный нефролитиаз после неоднократных оперативных вмешательств. Всего от коралловидных камней были избавлены 48 детей, 6 из них имели двусторонний коралловидный нефролитиаз.
Практически все сеансы дробления осуществляются под внутривенным наркозом, что позволяет детям уже через 2–3 ч после сеанса (средняя длительность которого составляет 20–25 мин) вести активный образ жизни. Более того, при необходимости проведения повторного сеанса (при дроблении крупных либо коралловидных камней) это не вызывает у детей какого-либо страха. Поскольку в 78% случаях у детей имеет место калькулезный хронический пиелонефрит (нередко с титром бактериурии 105 и выше), наиболее частым осложнением в раннем послеоперационном периоде оказывается острый пиелонефрит, который наблюдается в 5,8% случаев. Как правило, пусковым моментом развития осложнения является временное нарушение пассажа мочи, связанное с отхождением фрагментов разрушенного камня. В большинстве случаев он купируется консервативно (76%) либо на фоне дренирования почки катетеризацией (15%), или же с помощью пункционной нефростомии (9%).
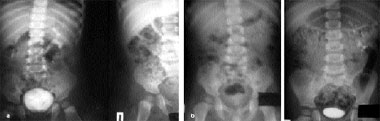 |
| Рисунок 3. Камень левой почки: а) до дробления; б) после дробления |
Для изучения отдаленных результатов лечения с применением ДЛТ в течение 8 лет после дробления проводились обследования 256 детей: с применением рентгенорадиологических и биохимических методов исследований оценивались функции почек в разных возрастных группах. Полное освобождение от камней к моменту контрольного обследования было установлено в 67,8% случаев. В 17,6% случаях диагностировались небольшие (до 0,5 см) резидуальные фрагменты в чашечках почки.
У 14,6% пациентов отмечался рост фрагментов, что потребовало проведения повторных сеансов ДЛТ.
Секреторная функция почек оставалась стабильной в 66% случаев, у 25% пациентов отмечалось улучшение секреторной функции, а у 9% — нараставшее снижение секреторной функции. Наряду с этим выделительная функция улучшилась в 82,6% случаев, причем улучшение отмечалось даже у пациентов с ухудшением секреторной функции. Наибольший процент случаев ухудшения функции почек приходится на долю детей, перенесших ранее операции и имевших резистентную бактериурию и исходный дефицит функции почки более 30%. Более того, при контрольном обследовании выяснилось, что большая часть таких детей не наблюдались и не лечились по месту жительства. Это обстоятельство еще раз подчеркивает тот факт, что удаление камня тем или иным методом является лишь частью комплексного лечения мочекаменной болезни, без чего трудно ожидать положительного результата.
Эндоскопическая трансуретральная и чрескожная литотрипсия и литоэкстракция. Еще 10 лет назад трансуретральная, а тем более чрескожная контактная литотрипсия считались опасными и травматичными методами, особенно в педиатрической практике. Сегодня положение сильно изменилось. Благодаря разработке новых эндоскопических инструментов и приборов для педиатрической практики расширились возможности эндохирургии и существенно снизилась частота осложнений (А. Г. Мартов, 2004).
Впервые в отечественной детской урологической практике профессором А. Г. Мартовым были разработаны показания, противопоказания и методики выполнения эндоскопических операций при мочекаменной болезни у детей в возрасте от 12 мес до 15 лет. Для выполнения эндоскопических операций имеется ряд противопоказаний, в числе которых и анатомо-функциональные особенности детей, такие как более низкое, чем у взрослых, расположение почек и большая их подвижность, более тесный контакт с прилежащими органами, «миниатюрность» чашечно-лоханочной системы и мочеточника.
Бесспорно, эндохирургия остается инвазивным методом, внедрение которого требует ответственной подготовки специалистов в ведущих урологических клиниках, занимающихся данной проблемой. По данным исследований, процент осложнений острого характера в верхней трети мочеточника составляет 11%, в нижней — 9% [13]. Стриктура мочеточника — единственное отдаленное осложнение, которое возникает в 1% случаев. Существует прямая зависимость между уровнем осложнений и применяемыми приборами и/или квалификацией уролога [4–12].
 |
| Рисунок 4. Ребенок 8 лет с коралловидным камнем левой почки во время операции перкутанной нефролитолапаксии |
Как трансуретральная, так и чрескожная эндоскопическая контактная литотрипсия не должны противопоставляться ДЛТ, поскольку в 18–27% случаях эти методы взаимно дополняют друг друга. Однако на сегодняшний день доказано, что при удалении коралловидных камней на долю чрескожной контактной литотрипсии приходится больше случаев успешного удаления основной массы камня за один сеанс (А. А. Лисенок, А. Г. Мартов, 2006). Более того, эндоскопические операции в ближайшем будущем позволят в ряде случаев, помимо удаления камня, одновременно устранять малоинвазивным методом причину камнеобразования (внутренняя уретротомия, рассечение уретероцеле, удаление лигатур и т. д.) (D. A. Tolley, 2002).
Инвазивный характер операции, обязательно выполняемой под эндотрахеальным наркозом, позволяет отнести эндоскопические операции при мочекаменной болезни к вмешательствам второго плана при камнях до 2,0 см у детей, хотя со временем, по мере совершенствования инструментария и широкого внедрения метода в детских урологических клиниках, эндохирургия должна выйти на первый план, особенно когда речь идет о крупных и коралловидных камнях (рис. 4, 5).
В связи с успешным применением ДЛТ и эндоурологического метода лечения (уретроскопия и перкутанная нефролитотомия) в течение последних 15–20 лет случаи проведения открытого хирургического вмешательства значительно сократились. По данным медицинских центров, специализирующихся на заболеваниях с образованием камней в мочевых путях, оснащенных хорошим хирургическим, лабораторным оборудованием и укомплектованных высококвалифицированным персоналом, необходимость в открытых хирургических вмешательствах составляет 1–5,4% [2, 7, 11].
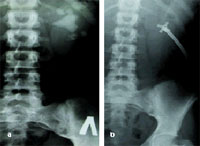 |
| Рисунок 5. Снимок коралловидного камня: а) до операции; б) перед удалением нефростомического дренажа |
Сегодня в некоторых случаях допускается проведение открытых хирургических вмешательств. Это касается сложных ситуаций (реконструкция мочевых путей, гнойно-воспалительный процесс, коралловидные камни, осложненные почечной недостаточностью и т. д.). Профессионализм урологов в проведении подобного рода операций на почках и мочеточниках должен быть очень высоким. Тем не менее при таком обилии методов лечения до конца неясно, надо ли прибегать в отдельных случаях к открытой хирургии или нет.
Какими бы темпами ни осуществлялись совершенствование и разработка новых малоинвазивных методов удаления камней, невозможно решать вопросы лечения мочекаменной болезни без применения комплексного междисциплинарного подхода к послеоперационному лечению детей (консультации уролога, педиатра, эндокринолога, диетолога). После успешного удаления камня наступает крайне важный этап метафилактики мочекаменной болезни, которая обязательно должна включать:
Литература
Н. К. Дзеранов, доктор медицинских наук, профессор
НИИ урологии, Москва