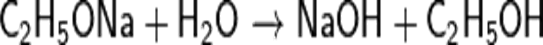Как зависит кислотность от природы растворителя?
Растворители оказывают сильное влияние на стабилизацию образующегося аниона (эффект сольватации). Лучше гидратируются небольшие по размеру ионы с низкой степенью делокализации заряда. Например, в ряду карбоновых кислот с увеличением длины алифатического (гидрофобного) радикала кислотность уменьшается.
33.Почему реакция натрия со спиртом идет медленнее, чем с водой?
Нужно отметить, что реакция между спиртом и натрием протекает не так энергично, как реакция натрия с водой. Еще медленнее действуют на спирт другие металлы, сравнительно легко вытесняющие водород из воды, как, например, кальций. Таким образом, кислотные свойства у спирта выражены слабее, чем у воды.
34. почему вода разлагает этилат натрия?
Реакция свелась к тому, что этилат-анион «оторвал» протон от молекулы воды.
Можно трактовать и иначе: будучи более сильной кислотой, чем этанол, вода передает свой протон этилат-аниону, при этом сама превращается в гидроксид-анион.
Таким образом, это самая обычная кислотно-основная реакция: более сильная кислота (вода) вытесняет более слабую кислоту (этанол) из ее соли (этилат натрия можно и нужно рассматривать как соль).
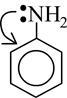
35. Основность диэтиламина и анилина
(C2H5)2NH.
Из-за наличия в молекулах неподеленной пары электронов амины, как и аммиак, проявляют основные свойства. В ряду
анилин аммиак первичный амин вторичный амин
основные свойства усиливаются, из-за влияния типа и числа радикалов.
Следовательно диэтиламин более сильное основание,чем анилин.
36 общая характеристика реакционной способности гетерофунсоединений. Кислотно-основная свойства.
В первом приближении химические свойства гетерофункциональных соединений представляют собой сумму свойств, обусловленных каждой группой в отдельности. Однако во многих случаях наличие двух (или более) различных функциональных групп приводит к усилению или ослаблению свойств, присущих монофункциональным соединениям, и, что важнее, порождает специфические химические свойства, присущие только гетерофункциональным соединениям. Кислотность гидроксикислот выше, чем незамещённых карбоновых кислот. Это обусловлено электроноакцепторным действием гидроксильной группы (-I-эффект), и чем ближе она к кислотному центру, тем это влияние сильнее. Так, pKa молочной кислоты на порядок выше, чем пропановой кислоты (3,9 и 4,9 соответственно).
Аминокислоты содержат одновременно кислотную (СООН) и основную (NH2) группы. Привычное написание формул аминокислот как соединений,
В сильнокислой среде в аминокислотах полностью протонирована аминогруппа (катионная форма) и не диссоциирована карбоксильная группа. В сильнощелочной среде, напротив, не протонирована аминогруппа, а карбоксильная группа полностью ионизирована (анионная форма)
37. Гетерофункциональный заместитель как фактор, влияющий на химические свойства реакционного центра. Специфические реакции гетерофункциональных соединений.


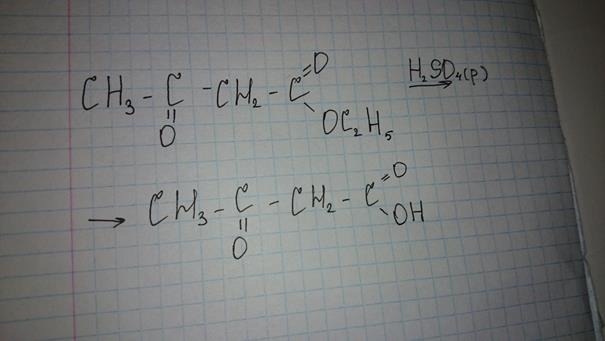
38.биологически важные классы гетерофункциональных соединений и их свойства. Ненасыщенные Карбоновые кислоты. Оксикислоты, аминокислоты, оксокислоты. Напишите реакцию взаимодействия ацетоуксусного эфира и серной кислоты.
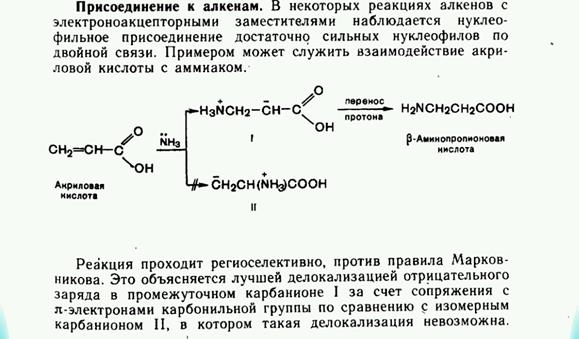
Среди гетерофункциональных соединений в природных объектах наиболее распространены аминоспирты, аминокислоты, гидроксикарбонильные соединения, а также гидрокси- и оксокислоты. Одноосновные непредельные кислоты содержат ненасыщенный углеводородный радикал, связанный с карбоксильной группой. Общая формула таких кислот (с одной двойной связью) имеет вид С Н2п- СООН. В молекуле ненасыщенных карбоновых кислот могут содержаться две и более этиленовых связей, а также тройная связь. Примерами таких кислот могут быть акриловая кислота СН2=СН—СООН, метакриловая кислота СН2=С(СНз)—СООН, кротоновая кислота СНз—СН=СН—СООН, пропиновая кислота СН=С—СООН, а также высшие ненасыщенные кислоты (олеиновая, линолевая и линоленовая). Оксокислотами называют соединения, содержащие в молекуле одновременно карбоксильную и альдегидную (или кетонную) группы.
В соответствии с этим различают альдегидокислоты и кетонокислоты.
Простейшей альдегидокислотой является глиоксалевая (глиоксиловая) кислота, которая обычно существует в виде гидрата (НО)2СНСООН. Она содержится в недозрелых фруктах, но по мере созревания ее количество уменьшается.Гидроксикислотами называют соединения, содержащие в молекуле одновременно гидроксильную и карбоксильную группы. Аминокислоты содержат в молекуле аминогруппу и карбоксильную группу.
В алифатическом ряду по взаимному расположению функциональных групп различают α-, β-, γ- и т. д. гидрокси- и аминокислоты. Буквой греческого алфавита указывают положение другой функциональной группы относительно карбоксильной, при этом отсчет ведется от ближайшего к карбоксильной группе атома углерода, т. е. от атома С-2. Отметим, что в заместительной номенклатуре для замещенных карбоновых кислот локанты α-, β-, γ- и т. д. не употребляются.
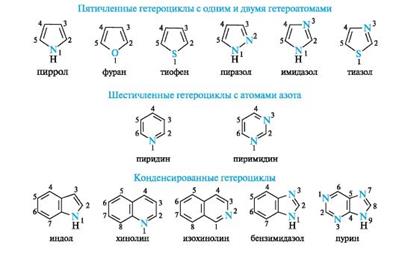
39. Биологически важные гетероциклические системы. Пятичленные гетероциклы с одним гетероатомом. Пиролл, фуран, тиофен. Понятие о строение тетрапирольных соединений. Линейные тетрапирольные соединения.
Наиболее важные гетероциклы, составляющие основу многих природных биологически активных веществ и лекарственных средств, приведены на схеме
70. Правило Дюкло-Траубе — зависимость, связывающая поверхностную активность водного раствора органического вещества с длиной углеводородного радикала в составе его молекулы. Согласно этому правилу, при увеличении длины углеводородного радикала на одну группу СΗ2 поверхностная активность вещества увеличивается в среднем в 3,2 раза.
71. Теория Ленгмюра базируется на следующих положениях:
1). Основное положение теории Лэнгмюра:поверхность адсорбента ограничена. Адсорбция вещества происходит не на всей поверхности, а только на активных центрах. Такими центрами могут служить отдельные атомы или группы атомов, выступающих над поверхностью адсорбента.
2). Каждый активный центр удерживает только одну молекулу.
3). Когда все активные центры заняты и поверхность адсорбента покрыта слоем толщиной в одну молекулу (мономолекулярный слой), наступает адсорбционное равновесие и дальнейшее увеличение адсорбции невозможно.
4). Процесс адсорбции имеет динамический характер. При равновесии скорость адсорбции и десорбции одинакова. Адсорбированные молекулы остаются некоторое время связанными с активными центрами, а затем покидают поверхность (десорбируются) и их место занимают другие молекулы Время пребывания молекулы на активном центре зависит от температуры.
5). Адсорбированные на активных центрах молекулы не взаимодействуют друг с другом.
Уравнение изотермы мономолекулярной адсорбции Ленгмюра имеет вид:
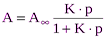
где А и А¥ соответственно величина адсорбции газа или пара при данном и предельном заполнении монослоя; К – константа адсорбционного равновесия 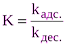
Это уравнение характеризует интенсивность взаимодействия адсорбента и адсорбата.
Для адсорбции веществ из растворов справедливо уравнение
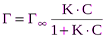
где Г – Гиббсовская адсорбция при концентрации С; Г¥– максимальная или предельная адсорбция, соответствующая образованию монослоя, С – равновесная концентрация вещества в растворе.
Зависимость величины адсорбции от концентрации представлена на следующем рисунке
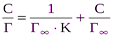
В координатах С/Г—Сполучаем прямую, и из графика находим величиныГ¥иК(рис. 1). Зная опытное значениеГ¥, можно рассчитать площадь поперечного сечения молекулы и ее длину.
74.КОЛЛОИДНАЯ ХИМИЯ, область химии, изучающая дисперсные системы и поверхностные явления, возникающие на границе раздела фаз.
Диспе́рсная систе́ма — это образования из двух или большего числа фаз (тел), которые практически не смешиваются и не реагируют друг с другом химически.
Дисперсность — физическая величина, характеризующая размер взвешенных частиц в дисперсных системах. Это величина, показывающая какое число частиц можно уложить вплотную в одном кубическом метре.
Опыты по химии. Одноатомные спирты
Постановка опытов и текст – к.п.н. Павел Беспалов.
Физические свойства спиртов
Одноатомные спирты, содержащие в своем составе до десяти атомов углерода, в обычных условиях — жидкости. Спирты, в составе которых 11 атомов углерода и более — твердые тела. Этиловый, бутиловый и изоамиловый спирт – жидкости.
Посмотрим, как спирты растворяются в воде. В три пробирки нальем по нескольку миллилитров спиртов и прибавим к ним подкрашенную воду. Спирты имеют плотность меньше единицы, поэтому они образуют верхний слой. При взбалтывании пробирок происходит полное растворение этилового спирта, частично растворяется бутиловый спирт, почти не растворяется изоамиловый спирт. Краситель из водного раствора переходит в спирты. С повышением молекулярной массы и увеличением углеводородного радикала растворимость спиртов в воде уменьшается.
Оборудование: пробирки, штатив для пробирок, стаканы.
Техника безопасности. Соблюдать правила работы с огнеопасными жидкостями.
Взаимодействие этилового спирта с бромоводородом
Спирты взаимодействуют с галогеноводородами. В прибор для получения галоидоалканов наливаем смесь этилового спирта с концентрированной серной кислотой. Прибавим к смеси вначале несколько капель воды, а затем – бромид натрия. В верхнюю часть прибора, холодильник, нальем воды и добавим кусочки льда. Нагреем колбу. Через некоторое время начинается реакция. Бромид натрия реагирует с серной кислотой с образованием бромоводорода.
NaBr + H2SO4 = NaHSO4 + HBr
Бромоводород реагирует с этиловым спиртом с образованием бромэтана.
HBr +С2Н5ОН = C2H5Br + H2O
Бромэтан — легкокипящая жидкость. Бромэтан испаряется, пары поступают в холодильник, где бромэтан конденсируется. Капли бромэтана падают в приемник. На дне приемника собирается тяжелая маслянистая жидкость – бромэтан.
Оборудование: прибор для получения галоидоалканов, штатив, шпатель, горелка, стакан, мерная пробирка
Техника безопасности. Соблюдать правила работы с огнеопасными жидкостями и кислотами.
Взаимодействие этилового спирта с металлическим натрием
При взаимодействии спиртов с натрием образуются газообразный водород и соответствующие алкоголяты натрия. Приготовим пробирки с метиловым, этиловым и бутиловым спиртами. Опустим в пробирку с метиловым спиртом кусочек металлического натрия. Начинается энергичная реакция. Натрий плавится, выделяется водород.
2СН3ОН + 2 Na = 2 CH3ONa + H2
Опустим натрий в пробирку с этиловым спиртом. Реакция идет немного медленней. Выделяющийся водород можно поджечь. По окончании реакции выделим этилат натрия. Для этого опустим в пробирку стеклянную палочку и подержим ее над пламенем горелки. Избыток спирта испаряется. На палочке остается белый налет этилата натрия.
2С2Н5ОН + 2 Na = 2 C2H5ONa + H2
В пробирке с бутиловым спиртом реакция с натрием идет еще медленнее.
2С4Н9ОН + 2 Na = 2 C4H9ONa + H2
Итак, с удлинением и разветвлением углеводородного радикала скорость реакции спиртов с натрием уменьшается.
Оборудование: штатив для пробирок, пробирки, пинцет, скальпель, фильтровальная бумага.
Техника безопасности. Соблюдать правила работы с огнеопасными жидкостями и щелочными металлами.
Горение спиртов
Нальем понемногу этилового, бутилового и изоамилового спиртов в фарфоровые чашки. Поднесем к чашкам горящую лучину. Этиловый спирт быстро загорается и горит голубоватым, слабосветящимся пламенем. Бутиловый спирт горит светящимся пламенем. Труднее загорается изоамиловый спирт, он горит коптящим пламенем. С увеличением молекулярной массы одноатомных спиртов повышается температура кипения и возрастает светимость их пламени.
Оборудование: огнезащитная прокладка, фарфоровые чашки, лучина.
Техника безопасности. Соблюдать правила работы с огнеопасными жидкостями.
Каталитическое окисление этанола
Окисление этилового спирта кислородом воздуха происходит очень легко в присутствии оксида хрома (III). В фарфоровую чашку поместим кусочек ваты, смоченный спиртом. Подожжем вату. Осторожно насыпаем на горящую вату оксид хрома. Пламя гаснет. Но оксид хрома начинает раскаляться. Реакция окисления спирта протекает с выделением энергии. Продукт реакции окисления спирта — уксусный альдегид.
2СН3-СН2-ОН + О2 = 2CH3 —COH + 2H2O
Оборудование: фарфоровая чашка, шпатель.
Техника безопасности. Соблюдать правила работы с огнеопасными жидкостями и концентрированными кислотами. После демонстрации осторожно разбавить содержимое чашки водой, нейтрализовать щелочью.
Качественная реакция на этанол
Чувствительной реакцией на этиловый спирт является так называемая йодоформная проба: образование характерного желтоватого осадка йодоформа при действии на спирт йода и щелочи. Этой реакцией можно установить наличие спирта в воде даже при концентрации 0,05%. Отберем пробу раствора и добавим раствор Люголя. Раствор Люголя содержит иод (1 часть иода, 2 части иодида калия, 17 частей стерильной дистиллированной воды). При охлаждении раствора появляется желтая взвесь йодоформа, при высоких концентрациях спирта выпадает желтый осадок йодоформа.
С2Н5ОН + 6 NaОН + 4 I2 = CHI3 +HCOONa + 5 NaI + H2O
Оборудование: пробирки, зажим пробирочный, горелка.
Техника безопасности. Соблюдать правила работы с нагревательными приборами.
Окисление этанола (тест на алкоголь)
Реакцию окисления спиртов сильными окислителями используют для установления факта алкогольного опъянения.
Приготовим трубку для определения алкоголя. Для этого разотрем в ступке хромовый ангидрид (оксид хрома (VI)) с небольшим количеством серной кислоты. Получается паста красного цвета. Нанесем пастой полосу на стенках трубки. Трубку соединим с прибором, подающим смесь воздуха с парами этилового спирта. Через некоторое время красная полоса в трубке зеленеет. Спирт окисляется в уксусный альдегид, а окислитель оксид хрома превращается в сульфат хрома (III), имеющий зеленую окраску.
Оборудование: фарфоровая чашка и ступка, трубка стеклянная, резиновые трубки, газометр или аспиратор
Техника безопасности. Соблюдать правила работы с огнеопасными жидкостями.
Окисление этилового спирта кристаллическим перманганатом калия
Очень энергично протекает реакция этилового спирта с перманганатом калия в присутствии концентрированной серной кислоты. В стеклянный цилиндр наливаем серную кислоту. Осторожно, по стенке приливаем этиловый спирт. Образуются два слоя жидкости. Сверху — этиловый спирт, снизу — серная кислота. В цилиндр бросаем немного кристаллического перманганата калия. Через некоторое время на границе раздела спирта и кислоты возникают вспышки и слышатся щелчки. При попадании кристаллов перманганата калия в серную кислоту образуется марганцевый ангидрид (оксид марганца (VII)) — очень сильный окислитель. Он взаимодействует с этиловым спиртом. При этом образуется уксусный альдегид.
СН3-СН2-ОН + [О] = CH3 —COH + H2O
Оборудование: цилиндр, шпатель.
Техника безопасности. Соблюдать правила работы с огнеопасными жидкостями и концентрированными кислотами. После демонстрации осторожно разбавить содержимое водой, нейтрализовать щелочью.
Окисление этилового спирта оксидом меди (II)
В прибор для окисления спиртов нальем немного этилового спирта. Присоединим к газоотводной трубке прибор для подачи воздуха. Раскалим в горелке медную спираль и поместим ее в прибор. Подадим в прибор ток воздуха. Медная спираль в приборе продолжает быть раскаленной, так как начинается окисление спирта. Продукт окисления спирта — уксусный альдегид.
СН3-СН2-ОН + СuO = CH3 —COH + Cu + H2O
Альдегид обнаруживаем, пропуская через фуксинсернистую кислоту выходящие из прибора газы. Под действием альдегида фуксинсернистая кислота приобретает фиолетовую окраску. Покажем, что медная спираль раскалена. Извлечем спираль из прибора и поднесем к ней спичку. Спичка загорается. Мы убедились в том, что при окислении одноатомных спиртов образуются альдегиды.
Оборудование: прибор для окисления спирта, резиновые трубки, горелка, газометр или аспиратор.
Техника безопасности. Соблюдать правила работы с огнеопасными жидкостями и нагревательными приборами.
Окисление этилового спирта раствором перманганата калия
Спирты легко окисляются раствором перманганата калия. В пробирку с этиловым спиртом прильем немного подкисленного раствора перманганата калия. Осторожно подогреем пробирку. Раствор постепенно обесцвечивается. В данных условиях этиловый спирт окисляется, превращаясь в уксусный альдегид.
СН3-СН2-ОН + [О] = CH3 —COH + H2O
Оборудование: пробирки, штатив для пробирок.
Техника безопасности. Соблюдать правила работы с огнеопасными жидкостями и нагревательными приборами.
Спирты
Классификация спиртов
Одноатомные спирты также подразделяются в зависимости от положения OH-группы: первичные (OH-группа у первичного атома углерода), вторичные (OH-группа у вторичного атома углерода) и третичные (OH-группа у третичного атома углерода).
Номенклатура и изомерия спиртов
Названия спиртов формируются путем добавления суффикса «ол» к названию алкана с соответствующим числом атомов углерода: метанол, этанол, пропанол, бутанол, пентанол и т.д.
Для спиртов характерна изомерия углеродного скелета (начиная с бутанола), положения функциональной группы и межклассовая изомерия с простыми эфирами, которых мы также коснемся в данной статье.
Получение спиртов
Присоединения молекулы воды (HOH) протекает по правилу Марковникова. Атом водорода направляется к наиболее гидрированному атому углерода, а гидроксогруппа идет к соседнему, наименее гидрированному, атому углерода.
В результате восстановления альдегидов и кетонов получаются соответственно первичные и вторичные спирты.
Синтез газом в промышленности называют смесь угарного газа и водорода, которая используется для синтеза различных химических соединений, в том числе и метанола.
В ходе брожения глюкозы выделяется углекислый газ и образуется этанол.
Химические свойства спиртов
Щелочные металлы (Li, Na, K) способны вытеснять водород из спиртов с образованием солей: метилатов, этилатов, пропилатов и т.д.
Необходимо особо заметить, что реакция с щелочами (NaOH, KOH, LiOH) для предельных одноатомных спиртов невозможна, так как образующиеся алкоголяты (соли спиртов) сразу же подвергаются гидролизу.
Реакция с галогеноводородами протекают как реакции обмена: атом галогена замещает гидроксогруппу, образуется молекула воды.
В результате реакций спиртов с кислотами образуются различные эфиры.
Дегидратация спиртов (отщепление воды) идет при повышенной температуре в присутствии серной кислоты (водоотнимающего) компонента.
Качественной реакцией на спирты является взаимодействие с оксидом меди II. В ходе такой реакции раствор приобретает характерное фиолетовое окрашивание.
Замечу, что в обычных условиях третичные спирты окислению не подвергаются. Для них необходимы очень жесткие условия, при которых углеродный скелет подвергается деструкции.
Вторичные и третичные спирты определяются другой качественной реакцией с хлоридом цинка II и соляной кислотой. В результате такой реакции выпадает маслянистый осадок.
Такой реакцией является взаимодействие многоатомного спирта со свежеприготовленным гидроксидом меди II. В результате реакции раствор окрашивается в характерный синий цвет.
Важным отличием многоатомных спиртов от одноатомных является их способность реагировать со щелочами (что невозможно для одноатомных спиртов). Это говорит об их более выраженных кислотных свойствах.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.