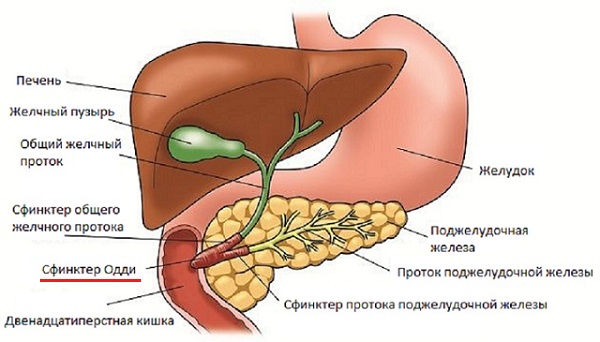
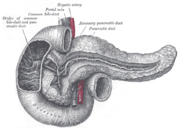
Постхолецистэктомический синдром
Рубрика МКБ-10: K91.5
Содержание
Определение и общие сведения [ править ]
У большинства больных желчнокаменной болезнью оперативное лечение приводит к выздоровлению и полному восстановлению трудоспособности. Иногда у пациентов сохраняются некоторые симптомы болезни, бывшие у них до операции, или появляются новые. Причины этого весьма разнообразны, тем не менее данное состояние больных, перенесших холецистэктомию, объединяют собирательным понятием «постхолецистэктомический синдром». Термин неудачен, т.к. далеко не всегда удаление желчного пузыря служит причиной развития болезненного состояния пациента.
Этиология и патогенез [ править ]
Основные причины так называемого постхолецистэктомического синдрома:
• органические изменения в желчных путях: оставленные при холецистэктомии конкременты в желчных протоках (так называемые забытые камни); стриктура большого сосочка двенадцатиперстной кишки или терминального отдела общего желчного протока; длинная культя пузырного протока или даже оставленная при операции часть желчного пузыря, где вновь могут образовываться конкременты; ятрогенные повреждения общего печеночного и общего желчного протоков с последующим развитием рубцовой стриктуры (эта группа причин связана как с дефектами оперативной техники, так и с недостаточным интраоперационным исследованием проходимости желчных протоков);
• заболевания органов гепатопанкреатодуоденальной зоны: хронический гепатит, панкреатит, дискинезия желчных протоков, перихоледохиальный лимфаденит.
Лишь болезни второй группы прямо или косвенно связаны с выполненной ранее холецистэктомией. Другие причины возникновения синдрома обусловлены дефектами дооперационного обследования больных и своевременно не диагностированными заболеваниями системы органов пищеварения.
В выявлении причин, приведших к развитию постхолецистэктомического синдрома, помогают тщательно собранный анамнез заболевания, данные инструментальных методов исследования органов пищеварительной системы.
Клинические проявления [ править ]
Клинические проявления постхолецистэктомического синдрома многообразны, но неспецифичны.
Клинические признаки постхолецистэктомического синдрома иногда появляются сразу же после операции, но возможен и «светлый промежуток» различной длительности до появления первых его симптомов.
Постхолецистэктомический синдром: Диагностика [ править ]
Инструментальные методы диагностики постхолецистэктомического синдрома
Из неинвазивных диагностических методов следует прежде всего назвать трансабдоминальную ультрасонографию, выявляющую холедохолитиаз (резидуальные и рецидивные камни холедоха, в том числе вколоченные в ампулу БДС). Она позволяет оценить анатомическую структуру печени и поджелудочной железы, выявить дилатацию общего желчного протока.
Диагностические возможности ультразвуковой (УЗ) диагностики могут быть повышены при использовании эндоскопической ультрасонографии (ЭУС) и функциональных УЗ-проб (с «жировым» пробным завтраком, с нитроглицерином). Под контролем УЗИ проводят такие сложные диагностические манипуляции, как тонкоигольная прицельная биопсия поджелудочной железы или наложение чрескожной чреспеченочной холангиостомы.
Эндоскопия верхних отделов пищеварительного тракта определяет наличие патологических процессов в пищеводе желудке, ДПК и позволяет провести их дифференциальную диагностику с использованием прицельной биопсии и последующим гистологическим изучением биоптатов; выявляет дуодено-гастральный и гастро-эзофагеальный рефлюксы.
Дифференциальный диагноз [ править ]
Постхолецистэктомический синдром: Лечение [ править ]
При функциональных (истинных) формах постхолецистэктомического синдрома используют консервативные методы лечения. Больные должны соблюдать диету в пределах лечебных столов № 5 и № 5-п (панкреатический) с дробным приемом пищи, что должно обеспечить отток желчи и предупредить возможность холестаза. Важен отказ от вредных привычек (курение, злоупотребление алкоголем и т.п.).
При органических поражениях желчных протоков больным показана повторная операция. Характер ее зависит от конкретной причины, вызвавшей постхолецистэктомический синдром. Как правило, повторные операции на желчных путях сложны и травматичны, требуют высокой квалификации хирурга. При длинной культе пузырного протока или оставлении части желчного пузыря их удаляют, в случае холедохолитиаза и стеноза большого сосочка двенадцатиперстной кишки выполняют те же операции, что и при осложненном холецистите. Протяженные посттравматические стриктуры внепеченочных желчных путей требуют наложения билиодигестивных анастомозов с выключенной по Ру петлей тощей кишки или с двенадцатиперстной кишкой.
Профилактика [ править ]
В профилактике постхолецистэктомического синдрома ведущая роль принадлежит тщательному обследованию больных до операции, выявлению сопутствующих заболеваний органов пищеварительной системы и их лечению в до- и послеоперационном периодах. Особое значение имеет тщательное соблюдение техники оперативного вмешательства с исследованием состояния внепеченочных желчных путей.
Постхолецистэктомический синдром
Постхолецистэктомический синдром – специфический симптомокомплекс, обусловленный перенесенной холецистэктомией и связанными с этим изменениями функционирования желчевыделительной системы. К проявлениям постхолецистэктомического синдрома относятся рецидивирующие болевые приступы, диспепсические расстройства, диарея и стеаторея, гиповитаминоз, снижение массы тела. Для выявления причин синдрома проводится УЗИ и МСКТ брюшной полости, фиброгастродуоденоскопия, РХПГ. Лечение постхолецистэктомического синдрома может быть консервативным (щадящая диета, прием спазмолитиков и ферментов) и хирургическим (дренирование желчных протоков, эндоскопическая сфинктеропластика и др.).
МКБ-10
Общие сведения
Постхолецистэктомический синдром – это комплекс клинических симптомов, развивающийся вследствие оперативного удаления желчного пузыря. В группу пациентов с постхолецистэктомическим синдромом не входят больные, у которых проведена холецистэктомия с погрешностями, остались камни в желчных протоках, развился послеоперационный панкреатит, сопровождающийся сдавлением общего желчного протока, холангит.
Постхолецистэктомический синдром встречается в среднем у 10-15% пациентов (при этом в разных группах этот показатель доходит до 30%). У мужчин он развивается практически в два раза реже, чем у женщин. Постхолецистэктомический синдром может развиться сразу после проведения оперативного удаления желчного пузыря, а может проявиться спустя длительное время (несколько месяцев, лет).
Причины
Основным патогенетическим фактором развития постхолецистэктомического синдрома является нарушение в билиарной системе – патологическая циркуляция желчи. После удаления желчного пузыря, являющегося резервуаром для вырабатываемой печенью желчи и участвующего в своевременном достаточном ее выделении в двенадцатиперстную кишку, привычный ток желчи изменяется. В некоторых случаях нормальное снабжение кишечника желчью не удается обеспечить. Окончательный механизм этих нарушений еще недостаточно изучен.
Факторами, способствующими развитию постхолецистэктомического синдрома, могут быть имеющие место дискинезии желчевыводящих путей, спазм сфинктера Одди (мышечного образования в месте впадения общего желчного протока в двенадцатиперстную кишку), оставшийся после операции пузырный проток значительной длины. Иногда причинами возникновения этого синдрома может быть выраженная послеоперационная боль и скопление жидкости в области произведенной операции. Только в 5% случаев причину развития постхолецистэктомического синдрома выявить не удается.
Симптомы постхолецистэктомического синдрома
Данный симптомокомплекс может проявляться сохранением клинических проявлений, имевших место до операции, в той или иной степени выраженности (чаще всего менее выраженных, но иногда отмечают и усиление дооперационной клиники). Иногда после холецистэктомии возникают новые симптомы.
Основной симптом – болевой. Боль может быть как режущей, так и тупой, различной степени интенсивности. Встречается приблизительно в 70% случаев. Вторым по распространенности является диспепсический синдром – тошнота (иногда рвота), вздутие и урчание в животе, отрыжка с горьким привкусом, изжога, диарея, стеаторея. Секреторные нарушения приводят к нарушению всасывания пищи в 12-перстной кишке и развитию синдрома мальабсорбции. Следствием этих процессов служат гиповитаминоз, снижение массы тела, общая слабость, ангулярный стоматит.
Также может подниматься температура тела, возникать желтуха (иногда проявляется только субиктеричностью склер). Постхолецистэктомический синдром может принимать различные клинические формы, проявляясь ложными и истинными рецидивами камнеобразования холедоха, стриктурами общего желчного протока, стенозирующим папиллитом, спаечным процессом в подпеченочном пространстве, холепанкреатитом, билиарными гастродуоденальными язвами.
Диагностика
В ряде случаев диагностирование развивающегося постхолецистэктомического синдрома бывает затруднено сглаженной, слабо выраженной клинической картиной. Для получения полноценной медицинской помощи пациенту в послеоперационном периоде и в дальнейшей жизни без желчного пузыря необходимо внимательно относиться к сигналам своего организма и однозначно сообщать об имеющихся жалобах своему врачу. Необходимо помнить, что постхолецистэктомический синдром – это состояние, требующее выявления причин его возникновения и соответствующей этиологической терапии.
Для выявления состояний, приведших к развитию постхолецистэктомического синдрома, назначают лабораторные исследования крови, чтобы обнаружить возможный воспалительный процесс, а также инструментальные методики, направленные на диагностирование патологий органов и систем, как непосредственно оказывающих влияние на работу билиарной системы, так и опосредованно действующих на общее состояние организма.
Спиральная компьютерная томография (МСКТ) и магнитно-резонансная томография (МРТ печени) максимально точно визуализирует состояние органов и сосудов брюшной полости, также информативной методикой является УЗИ брюшной полости. Эти методы могут выявить присутствие конкрементов в желчных протоках, послеоперационное воспаление желчных путей, поджелудочной железы.
При рентгенографии легких исключают заболевания легких и средостения (которые могут быть причиной болевого синдрома), рентген желудка с контрастным веществом может помочь выявить наличие язв и непроходимости в желудочно-кишечном тракте, рефлюкса.
Для исключения происхождения симптомов в результате иных заболеваний пищеварительного тракта, производят эндоскопическое исследование желудка (гастроскопия) и двенадцатиперстной кишки (фиброгастродуоденоскопия). Нарушения в циркуляции желчи выявляют с помощью радионуклеидного исследования – сцинтиграфии. При этом в организм вводится специфический маркер, который скапливается в желчи.
Одним из самых информативных методов, позволяющих изучить состояние протоков билиарной системы является РХПГ (эндоскопическая ретроградная панкреатохолангиография). В ходе этого исследования выявляются нарушения тока желчи, отмечают состояние желчных путей, протоков, ампулы Фатерова сосочка, выявляют мелкие конкременты, отмечают скорость выделения желчи. Также можно произвести манометрию сфинктера Одди и общего желчного протока.
Во время проведения РХПГ возможно осуществить некоторые лечебные мероприятия: удалить имеющиеся в протоках камни, расширить просвет желчных путей в местах сужений, произвести сфинктеротомию при стойком спазме. Однако стоит помнить, что в некоторых случаях эндоскопия желчных протоков способствует возникновению панкреатита. Для исключения патологии сердца используют ЭКГ.
Лечение постхолецистэктомического синдрома
Методы лечения постхолецистэктомического синдрома напрямую зависят от причин его развития. В том случае, если данный синдром является следствием какой-либо патологии органов пищеварения, лечение осуществляют согласно рекомендациям по терапии данной патологии.
Лечение, как правило, включает в себя щадящую диету: соблюдение режима питания – еда небольшими порциями 5-7 раз в день, пониженное суточное содержание жиров (не более 60 грамм), исключение жареных, кислых продуктов, острой и пряной пищи, продуктов, обладающих желчегонной активностью, раздражающих слизистые оболочки элементов, алкоголя. При выраженном болевом синдроме для его купирования применяют дротаверин, мебеверин. Лекарственные средства назначаются гастроэнтерологом в соответствии с принципами медикаментозного лечения основной патологии.
Хирургические методы лечения направлены на дренирование и восстановление проходимости желчных протоков. Как правило, проводится эндоскопическая сфинктеропластика. При неэффективности производят диагностическую операцию для детального изучения брюшной полости на предмет вероятных причин развития синдрома.
Профилактика и прогноз
В качестве профилактики постхолецистэктомического синдрома можно отметить меры по своевременному выявлению различных сопутствующих заболеваний, могущих послужить причиной развития нарушений циркуляции желчи: полное и тщательное комплексное обследование печени, поджелудочной железы, желчевыводящих путей, пищеварительного тракта, сосудистой системы брюшной полости при подготовке к операции.
Прогноз излечения от постхолецистэктомического синдрома связан с излечением от основного заболевания, послужившего причиной развития симптомокомплекса.
Постхолецистэктомический синдром
Общие сведения
Постхолецистэктомический синдром (ПХЭС) – это целый комплекс симптомов, которые проявляются у человека после того, как ему провели удаление желчного пузыря. Для этого состояния характерны приступы боли, проблемы с пищеварением, диарея, понижение массы тела и др.
Согласно медицинской статистике, постхолецистэктомический синдром, код по МКБ-10 которого — K91.5, проявляется у 5–40% пациентов. Специалисты предполагают, что такое состояние является либо продолжением болезни, которая и привела к оперативному вмешательству, либо следствием операции. Как правило, удаление желчного пузыря не приводит к серьезным негативным последствиям для работы желчных путей. Около 10% случаев желчной колики являются следствием нарушений сфинктера Одди – как структурных, так и функциональных. Термин «дисфункция сфинктера Одди» также применяется вместо определения «постхолецистэктомический синдром».
О том, как может проявляться постхолецистэктомический синдром, когда происходит спазм сфинктера Одди и как правильно действовать, чтобы устранить неприятные признаки, речь пойдет в этой статье, где описаны симптомы и лечение постхолецистэктомического синдрома.
Патогенез
У основной части больных с этим синдромом отмечаются функциональные моторные расстройства. Неотъемлемая часть патогенеза желчекаменной болезни – моторные нарушения желчного пузыря и сфинктерного аппарата желчевыводящих путей.
Вследствие удаления желчного пузыря отмечается нарушение функции сфинктерного аппарата желчных путей. Развитие боли после операции, как правило, связано с увеличением давления в билиарном тракте, что связано с нарушениями функции сфинктера Одди.
В организме сфинктер Одди обеспечивает анатомическую и физиологическую связь между желчевыводящими путями, поджелудочной железой и двенадцатиперстной кишкой.
Физиологический контроль сфинктера Одди определяется рядом гормональных и нервных стимулов. В частности, важная роль в этой регуляции отводится гастроинтестинальным гормонам. Особое значение имеет холецистокинин (панкреозимин) и секретин.
Когда желчный пузырь сокращается и синхронно расслабляется сфинктер Одди, концентрированная желчь поступает в двенадцатиперстную кишку. В это время происходит выделение панкреатического сока под действием холецистокинина, что обеспечиваются все условия для расщепления пищи. Если происходит спазм сфинктера этот процесс нарушается.
Желчный пузырь непосредственно задействован в модуляции ответа сфинктера Одди на влияние гастроинтестинальных гормонов. После удаления желчного пузыря реакция сфинктера Одди в ответ на холецистокинин снижается.
О том, как изменяется функциональное состояние сфинктера Одди после холецистэктомии, существуют разные мнения. В частности, есть теория, что после операции повышается тонус и расширяется общий желчный проток. Также есть мнение, что вследствие холецистэктомии проявляется недостаточность сфинктера Одди, так как он не может длительнее время выдерживать высокое давление желчи. Противоречия, которые отмечаются в описании состояния сфинктера Одди, связаны с тем, что его функции исследовались в разные сроки после проведения холецистэктомии.
Классификация
В современной медицине отсутствует общепринятая классификация постхолецистэктомического синдрома. В зависимости от причины, по которой проявляются такие симптомы, в своей практике медики определяют это состояние широко, применяя такую классификацию:
Однако Римские критерии II 1999 года, а также Римские критерии III 2006 года ограничивают рамки «ПХЭС» дисфункцией сфинктера Одди, возникшей после холециетэктомии. Применяется следующая классификация дисфункции сфинктера Одди:
Дисфункция сфинктера Одди по билиарному типу. Определяется три типа этой разновидности:
Дисфункция сфинктера Одди по панкреатическому типу. Панкреатический тип проявляется эпигастральной болью, которая характерна для панкреатита. Боль отдает в спину и уменьшается, когда пациент наклоняется вперед. У больного значительно повышается сывороточная амилаза и липаза. При манометрии определяется дисфункция сфинктера Одди в 39–90% случаях.
Дисфункция сфинктера Одди по смешанному типу. Смешанный тип характеризуется опоясывающей болью, или боль локализуется в эпигастрии. Также проявляются другие признаки, характерные как для билиарного, так и для панкреатического типов.
Причины
Чаще всего признаки ПХЭС проявляются вследствие таких причин:
Симптомы постхолецистэктомического синдрома
Основные симптомы спазма сфинктера Одди – это проявление приступов сильных или средней интенсивности болей, которые продолжаются более 20 минут и проявляются на протяжении больше чем трех месяцев. Также проявляются диспепсические и невротические расстройства. Беспокоит тяжесть в правом подреберье. Как правило, боль постоянная. Иногда приступы сначала проявляются редко и длятся несколько часов, а потом, в промежутках между приступами, боль вообще не ощущается. У некоторых больных со временем частота приступов и интенсивность болей увеличивается. Связь приступов с приемом пищи у всех проявляется по-разному. Но наиболее часто боль беспокоит через 2-3 часа после еды.
Иногда, в тяжелых случаях, боль длительна и упорна, она сочетается со рвотой и тошнотой, а также с мучительными приступами изжоги.
Если причины ПХЭС связаны с истинным рецидивом образования камней желчного протока, то неприятные симптомы появляются не раньше, чем через несколько лет после проведенной операции. В таком случае развиваются следующие признаки:
Анализы и диагностика

В процессе диагностики проводится ряд исследований и лабораторных анализов. Врач обязательно изучает анамнез, проводит опрос и осмотр пациента. Для установления диагноза проводят:
В процессе обследования больных, которые жалуются на признаки ПХЭС, используется принцип поиска причин таких проявлений от более простых к сложным, а также использования методик от неинвазивных к более травматичным, но позволяющим получить важную информацию.
Еще один важный момент касается хирургической настороженности при таких симптомах: она должна быть тем больше, чем меньше времени прошло от операции.
Как правило, после лабораторных анализов обследование таких больных начинают с проведения УЗИ брюшной полости, которое дает возможность исключить анатомические изменения органов и перейти к более целенаправленным обследованиям.
Однако, несмотря на то, что возможности современной диагностики достаточно широкие, у определенного количества людей не удается выяснить причину неприятных симптомов после перенесенной холецистэктомии.
Лечение постхолецистэктомического синдрома
Очень важно, чтобы лечение постхолецистэктомического синдрома было комплексным и направлялось на устранение причин проявления неприятных симптомов. Пациенту, который перенес удаление желчного пузыря, необходимо помнить, что правильное питание, четкий режим приема пищи, физическая активность – это важнейшие условия успешной реабилитации после хирургической операции. Также при проявлении болей и других неприятных симптомов проводится медикаментозное лечение.
Постхолецистэктомический синдром
Дисфу́нкция сфи́нктера О́дди (англ. sphincter of Oddi dysfunction ) — заболевание (клиническое состояние), характеризующееся частичным нарушением проходимости протоков жёлчи и панкреатического сока в сфинктере Одди. К дисфункциям сфинктера Одди относят, по современным представлениям, только доброкачественные клинические состояния некалькулёзной этиологии. Может иметь как структурную (органическую) так и функциональную, связанную с нарушение двигательной активности сфинктера, природу.
Сфинктер Одди — мышечный клапан, располагающийся в большом дуоденальном сосочке (синоним фатеров сосочек) двенадцатиперстной кишки, управляющий поступлением жёлчи и панкреатического сока в двенадцатиперстную кишку и препятствующий попаданию содержимого кишки в общий желчный и панкреатический (вирсунгов) протоки.
Содержание
Спазм сфинктера Одди
Спазм сфи́нктера О́дди (англ. spasm of sphincter of Oddi ) — заболевание сфинктера Одди, классифицированное МКБ-10 с кодом K83.4. Римским консенсусом 1999 года отнесён к дисфункциям сфинктера Одди.
Постхолецистэктомический синдром
По́стхолецистэктоми́ческий синдро́м (англ. postcholecystectomy syndrome ) — дисфункция сфинктера Одди, обусловленная нарушением его сократительной функции, препятствующая нормальному оттоку желчи и панкреатического секрета в двенадцатиперстную кишку при отсутствии органических препятствий, являющаяся следствием операции холецистэктомии. Встречается примерно у 40% больных, которым проводилась холецистэктомия по причине камней желчного пузыря. Выражается в проявлении тех же клинических симптомов, что были до операции холецистэктомии (фантомные боли и т.п.). Классифицирован МКБ-10 с кодом K91.5. Римским консенсусом 1999 года термин «постхолецистэктомический синдром» не рекомендован.
Клиническая картина
Основные симптомы дисфункции сфинктера Одди — приступы сильных или умеренных болей длительностью более 20 минут, повторяющихся в течение более 3 месяцев, диспепсия и невротические расстройства. Часто наблюдаются чувство тяжести в брюшной полости, тупые, длительные боли в области правого подреберья без четкой иррадиации. В основном боли постоянные, не коликообразные. У многих больных приступы сначала возникают довольно редко, продолжаются несколько часов, в промежутках между приступами боли полностью проходят. Иногда частота и выраженность болевых приступов увеличивается со временем. В период между приступами болевые ощущения сохраняются. Связь болевых приступов с приемом пищи у разных пациентов выражена неодинаково. Чаще всего (но не обязательно) боли начинаются в течение 2-3 часов после приема пищи.
Дисфункция сфинктера Одди может быть в любом возрасте. Однако чаще всего она встречается у женщин среднего возраста. Дисфункция сфинктера Одди очень часто проявляется у пациентов, перенёсших холецистэктомию (удаление желчного пузыря). У 40–45% больных причиной жалоб являются структурные нарушения (стриктуры желчных путей, невыявленные камни общего желчного протока и другие), у 55–60% — функциональные.
Классификация
Согласно Римскому консенсусу 1999 года различают 3 типа билиарной дисфункции сфинктера Одди и 1 тип панкреатической дисфункции.
1. Билиарный тип I, включает:
2. Билиарный тип II, включает:
50–63% пациентов этой группы имеют манометрическое подтверждение дисфункции сфинктера Одди при манометрическом исследовании. У пациентов II билиарного типа нарушения могут быть как структурными, так и функциональными.
3. Билиарный тип III характеризуется только приступами болей билиарного типа без каких–либо объективных нарушений, характерных для I типа. При манометрии сфинктера Одди пациентов этой группы подтверждение дисфункции сфинктера Одди только у 12–28% пациентов. В III билиарной группе дисфункции сфинктера Одди обычно носит функциональный характер.
4. Панкреатический тип проявляется характерной для панкреатита эпигастральной болью, иррадиирующей в спину и уменьшающейся при наклоне туловища вперёд, и сопровождается значительным повышением сывороточной амилазы и липазы. В группе пациентов с данными симптомами и отсутствию традиционных причин панкреатита (желчекаменная болезнь, злоупотребление алкоголем и др.) манометрия выявляет дисфункцию сфинктера Одди в 39–90% случаях.