Язвенная болезнь желудка код по мкб 10 у взрослых
Язва желудка и двенадцатиперстной кишки и гастроэнтероанастомоза, осложненные кровотечением
Общая информация
Краткое описание
Язвенная болезнь – это хроническое рецидивирующее заболевание, протекающее с чередованием периодов обострения и ремиссии, основным признаком которого является образование дефекта (язвы) в стенке желудка и ДПК. Основные осложнения язвенной болезни: кровотечение, перфорация язвы, пенетрация, стеноз привратника, малигнизация, рубцовая деформация желудка и ДПК, перивисцирит [8].
I. ВВОДНАЯ ЧАСТЬ
Название протокола: Язва желудка и двенадцатиперстной кишки и гастроэнтероанастомоза, осложненные кровотечением
Код протокола:
Дата разработки протокола: 2014 год.
Категория пациентов: взрослые.
Пользователи протокола: хирурги, анестезиологи-реаниматологи, гастроэнтерологи, участковые терапевты, врачи общей практики, врачи скорой и неотложной помощи, фельдшеры, врачи функциональной диагностики (эндоскописты).
Оценка на степень доказательности приводимых рекомендаций[4].
Шкала уровня доказательности:
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки результаты, которых могут быть распространены на соответствующую российскую популяцию. |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с невысоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую российскую популяцию. |
| С | Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+). Результаты, которых могут быть распространены на соответствующую российскую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую российскую популяцию. |
| D | Описание серии случаев или неконтролируемое исследование или мнение экспертов. |
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
13-15 октября, Алматы, «Атакент»
600 брендов, более 150 компаний-участников из 20 стран.
Новинки рынка стоматологии. Цены от производителей
Классификация
Клиническая классификация язвенной болезни [1]
В зависимости от локализации различают:
Сочетанные язвы: язва желудка и ДПК
• стадия рубцевания (красный рубец, белый рубец).
Осложнения:
• Латентное, легкое, средней степени, тяжелое
Классификация гастродуоденального кровотечения
I По локализации:
Диагностика
II. МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
Минимальный перечень обследования, который необходимо провести при направлении на плановую госпитализацию: не проводятся.
Основные (обязательные) диагностические обследования, проводимые на стационарном уровне (при экстренной госпитализации проводятся диагностические обследования непроведенные на амбулаторном уровне):
Относительные противопоказания: крайне тяжелое состояние с низким показателями АД ниже 90 мм.рт.ст (ЭФГДС необходимо провести после коррекции состояния больного в условиях ОРиТ и повышения систолического АД не менее 100 мм.рт.ст) [7] (УД-C).
Абсолютные противопоказания: агональное состояние больного, острый инфаркт миокарда, ОНМК. 1
Дополнительные диагностические обследования, проводимые на стационарном уровне (при экстренной госпитализации проводятся диагностические обследования непроведенные на амбулаторном уровне):
• физикальное обследование (подсчет пульса, ЧСС, подсчет ЧД, измерить АД, оценка характера рвотных масс, пальцевое исследование прямой кишки).
Диагностические критерии (описание достоверных признаков заболевания в зависимости от степени тяжести процесса)
Жалобы: Клинические признаки кровотечения: на рвоту алой (свежей) кровью или кофейной гущей, дегтеобразный стул или жидкий стул с малоизмененной кровью. Клинические признаки кровопотери: слабость, головокружение, холодный липкий пот, шум в ушах, частое сердцебиение, кратковременная потеря сознания, жажда.
Анамнез заболевания:
• Признаки гемокоагуляционного синдрома (ДВС).
Лабораторные исследования:
Общий анализ крови: снижение содержания эритроцитов, уровней гемоглобина и гематокрита.
Биохимический анализ крови: повышение содержания сахара крови, АСТ, АЛТ, билирубина, остаточного азота, мочевины, кретинина; снижение общего белка.
Коагулограмма: снижение ПТИ, фибриногена, повышение МНО, удлинение времени свертываемости.
Тактика лечения определяется в соответствии со степенью кровопотери и дефицита ОЦК (Приложение 1).
Дифференциальный диагноз
Лечение
• стабилизация гемостаза (медикаментозной коррекцией, эндоскопический гемостаз, хирургическое лечение)
Тактика лечения***
Медикаментозное лечение
ИТТ при легкой степени кровопотери:
комплекс аминокислот для парентерального питания) в соотношении 3:1 с общим объемом 300% от объема кровопотери (2,5-4,5 литров);
ИТТ при тяжелой степени кровопотери [7] (УД-А):
Критическим уровнем показателей гемоглобина является 65-70 г/л, гематокрит 25-28%. (придерживаться приказа № 501 от 2012 г. по переливанию компонентов крови);
• Перфторан в дозе 10-15 мл на 1 кг веса пациента, скорость введения – 100-120 капель в мин. Но необходимо помнить, что перфторан не заменяет гемоплазмотрансфузию;
В схеме «квадротерапии»: тетрациклин по 500 мг 4 раза в сутки, метронидазол по 500 мг 2 раза в сутки, висмута трикалия дицитрат по 120 мг 4 раза в сутки. В регионах с резистентностью >20% в качестве альтернативы квадротерапии в терапии первой линии для преодоления резистентности к кларитромицину рекомендуется последовательная терапия: ИПП + амоксициллин (5 дней), далее ИПП + кларитромицин + метронидазол (5 дней).
• Метамизол натрия 50% 2 мл в/м
• Неостигмин 0,5 мг 1 мл по требованию
Медикаментозное лечение, оказываемое на амбулаторном уровне
Перечень дополнительных лекарственных средств (менее 100% вероятности применения): натрий хлорид 0,9% 400мл в/в.
Язва желудка (K25)
[см. указанные выше подрубрики]
При необходимости идентифицировать лекарственное средство, вызвавшее поражение, используют дополнительный код внешних причин (класс XX)
Алфавитные указатели МКБ-10
Внешние причины травм — термины в этом разделе представляют собой не медицинские диагнозы, а описание обстоятельств, при которых произошло событие (Класс XX. Внешние причины заболеваемости и смертности. Коды рубрик V01-Y98).
Лекарственные средства и химические вещества — таблица лекарственных средств и химических веществ, вызвавших отравление или другие неблагоприятные реакции.
В России Международная классификация болезней 10-го пересмотра (МКБ-10) принята как единый нормативный документ для учета заболеваемости, причин обращений населения в медицинские учреждения всех ведомств, причин смерти.
МКБ-10 внедрена в практику здравоохранения на всей территории РФ в 1999 году приказом Минздрава России от 27.05.97 г. №170
Выход в свет нового пересмотра (МКБ-11) планируется ВОЗ в 2022 году.
Сокращения и условные обозначения в Международой классификации болезней 10-го пересмотра
БДУ — без дополнительных уточнений.
НКДР — не классифицированный(ая)(ое) в других рубриках.
† — код основной болезни. Главный код в системе двойного кодирования, содержит информацию основной генерализованной болезни.
* — факультативный код. Дополнительный код в системе двойного кодирования, содержит информацию о проявлении основной генерализованной болезни в отдельном органе или области тела.
Язва желудка. Хроническая или неуточненная с кровотечением (K25.4)
Версия: Справочник заболеваний MedElement
Общая информация
Краткое описание
Для хронической язвы характерно выраженное воспаление и разрастание рубцовой (соединительной) ткани в области дна, стенок и краев язвы. Язва имеет округлую или овальную (реже линейную, щелевидную или неправильную) форму. Ее размер и глубина могут быть различными. Края язвы плотные (каллезная язва), ровные; подрытые в проксимальном ее отделе и пологие в дистальном.
Хроническая язва является основным морфологическим субстратом язвенной болезни желудка и двенадцатиперстной кишки (ДПК).
Кровотечение является наиболее часто встречающимся осложнением язвенной болезни желудка и ДПК.
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
13-15 октября, Алматы, «Атакент»
600 брендов, более 150 компаний-участников из 20 стран.
Новинки рынка стоматологии. Цены от производителей
Классификация
В 1974 г. Forrest и соавторы описали эндоскопические признаки кровотечения из пептической язвы и систематизировали их.
В настоящее время эта классификация получила признание во всем мире.
Классификация Forrest:
Тип F I – активное кровотечение:
— I a – пульсирующей струей;
— I b – потоком.
Тип F II – признаки недавнего кровотечения:
— II а – видимый (некровоточащий) сосуд;
— II b – фиксированный тромб-сгусток;
— II с – плоское черное пятно (черное дно язвы).
Тип F III – язва с чистым (белым) дном.
Этиология и патогенез
Эпидемиология
Возраст: преимущественно зрелый и пожилой
Признак распространенности: Редко
Соотношение полов(м/ж): 3
15-20% пептических язв желудка осложняются кровотечением.
Факторы и группы риска
Клиническая картина
Клинические критерии диагностики
Cимптомы, течение
Диагностика
Лабораторная диагностика
При обследовании больных с подозрением на кровотечение осуществляют динамический контроль следующих лабораторных показателей:
— гематокрит;
— содержание гемоглобина, эритроцитов и тромбоцитов;
— концентрация протромбина, фибриноген.
Обязательно определение группы крови и резус-фактора.
Дифференциальный диагноз
Основной и самый ранний клинический симптом (рвота с кровью) при язве желудка отличается от такового при кровотечениях иной локализации.
Артериальное пищеводное кровотечение характеризуется рвотой с примесью неизмененной крови, кровотечение из варикозно-расширенных вен пищевода нередко бывает профузным и проявляется рвотой с кровью темно-вишневого цвета.
Осложнения
Возможные осложнения:
— шок;
— анемия;
— коагулопатия потребления;
— рецидивы кровотечения.
В соответствии с современными представлениями, риск развития рецидива кровотечения и/или летального исхода ассоциирован со следующими эндоскопическими признаками:
— обнаружение на дне язвы обнаженного сосуда (риск 90%);
— обнаженный сосуд на дне язвы без видимого кровотечения (риск 50%);
— большой несформированный «красный» тромб, закрывающий дефект и не смыкающийся при орошении язвы изотоническим раствором натрия хлорида (риск 25%).
Согласно Международным клиническим рекомендациям по ведению пациентов с неварикозными кровотечениями из верхних отделов желудочно-кишечного тракта (согласительное совещание было проведено в июне 2002 г. под эгидой Канадской ассоциации гастроэнтерологов), риск рецидива кровотечения можно определить согласно представленной ниже таблице.
Статистически достоверные предикторы рецидива кровотечения
Факторы риска
Показатели повышения риска
Клинические факторы
Возраст > 65 лет
Возраст > 70 лет
Общий статус (ASA*)
Нестабильный уровень сознания
Лабораторные факторы
Коагулопатия (длительное АЧТВ)
Признаки кровотечения
Алая кровь при ректальном исследовании
Кровь в желудке или зонде
Эндоскопические факторы
Активное кровотечение в ходе эндоскопии
Признаки высокого риска
Сгусток в дне язвы
Размер язвы > 2 см
Наличие язвенной болезни
Локализация язвы
Малая кривизна желудка
Лечение
Тактика лечения сводится к стабилизации состояния пациента с последующей эндоскопией.
При остром кровотечении перед любыми вмешательствами и обследованиями необходимо проведение мероприятий по стабилизации артериального давления и восстановлению объема циркулирующей крови.
Основные эндоскопические методики остановки кровотечения при пептических язвах, доступные в настоящее время:
1. Лазерная фотокоагуляция (аргоновый плазменный лазер, ниобий-гранатовый лазер).
2. Биполярная диатермия.
3. Тепловой электрод. Ни один из методов термокоагуляции не имеет особых преимуществ перед другими. В случае применения термокоагуляции, целесообразно сочетать ее с инъекционным эндоскопическим гемостазом.
4. Инъекционная склеротерапия и инъекция эпинефрина. В случае необходимости выполнения инъекций, следует помнить, что ни один из растворов, применяемых для эндоскопической инъекционной терапии, не имеет доказанных преимуществ перед другими, хотя традиционно предпочтение отдается эпинефрину.
Медикаментозная терапия
В лечении эрозивно-язвенных кровотечений (типа Forrest Ib) эффективно применение секретина или соматостатина.
Секретин вводят внутривенно капельно в изотоническом растворе натрия хлорида или 5% растворе фруктозы в дозе 800 ЕД (или 12 ЕД на 1 кг массы тела в сутки). Препарат в 80-95% случаев способствует остановке кровотечения.
Соматостатин вводят с помощью непрерывной инфузии в дозе 250мкг/ч.
Продолжительность применения секретина и соматостатина должна составлять не менее 48 часов.
Назначение Н2-блокаторов в ранний период после эндоскопического вмешательства снижает риск возникновения рецидива, оперативного вмешательства и летальности. Соматостатин также уменьшает риск возникновения рецидивов. ИПП возможно назначать для этих же целей как до, так и после эндоскопии.
К хирургическому лечению прибегают в случаях, когда эндоскопические методы остановки язвенного кровотечения неэффективны.
Альтернативой традиционным способам хирургического лечения считают лапароскопические операции. При лапараскопических вмешательствах меньше вероятность летального исхода и короче срок восстановительного лечения.
Прогноз
В группах пациентов ввысокого риска, где летальность в старческом и пожилом возрасте может достигать значительных цифр, предикторы летального исхода представлены в таблице ниже.
Факторы риска
Показатели повышения степени риска
Язва желудка в МКБ-11 и МКБ-10: сравнительные таблицы
Изучаем подход классификатора к распространенному заболеванию ЖКТ
Справка по МКБ-11 (подробнее здесь)
Напомним ключевые факты о МКБ одиннадцатого пересмотра:
Язва желудка
Также в новой МКБ (в отличие от предыдущей) дано развернутое определение рассматриваемого диагноза. Язва желудка определяется как отчетливое нарушение слизистой оболочки желудка в результате едкого воздействия кислоты и пепсина в просвете. Гистологически язва желудка определяется как некроз слизистой оболочки, проходящий через мышечную слизистую оболочку в подслизистую оболочку. При эндоскопическом или рентгенологическом исследовании наблюдается заметная глубина поражения. Когда разрыв эпителиальной оболочки ограничивается слизистой оболочкой, не проникая через мышечную слизистую оболочку, поверхностное поражение называется «эрозией».
В добавок к этому новый классификатор содержит «Диагностические требования» определения диагноза «Язва желудка». В частности, «язвы определяются как разрывы на поверхности слизистой оболочки размером > 5 мм с глубиной до подслизистой основы и обнаруживаются эндоскопическим или рентгенологическим методом».
В МКБ-10 иерархическая структура была несколько проще. Диагноз «Язвенная болезнь желудка» (K25) входил в группу «Заболевания пищевода, желудка и двенадцатиперстной кишки» (K20-K31). А эта группа, в свою очередь, являлась частью раздела «Заболевания органов пищеварения» (K00-K93).
Язва желудка в МКБ-10 (K25)
Язва желудка в МКБ-11 (DA60)
Острая с кровотечением (К25.0)
Эрозия желудка (DA60.0)
Острая с прободением (К25.1)
Язва желудка, ассоциированная с Helicobacter pylori (DA60.1)
Острая с кровотечением и прободением (К25.2)
Лекарственно-индуцированная язва желудка, ассоциированная с Helicobacter pylori (DA60.2)
Острая без кровотечения или прободения (К25.3)
Стрессовая язва желудка (DA60.3)
Хроническая или неуточнённая с кровотечением (К25.4)
Эозинофильная язва желудка (DA60.4)
Хроническая или неуточнённая с прободением (К25.5)
Лимфоцитарная язва желудка (DA60.5)
Хроническая или неуточнённая с кровотечением и прободением (К25.6)
Язва желудка, вызванная внешними причинами (DA60.6)
Хроническая без кровотечения или прободения (К25.7)
Язва желудка, ассоциированная со вторичной инфекцией (DA60.7)
Не уточненная как острая или хроническая без кровотечения или прободения (К25.9)
Другая уточненная язва желудка (DA60.Y)
Язва желудка, неуточненная (DA60.Z)
Как видно из таблицы, составители МКБ-11 выбрали принципиально иной подход к проблеме, заложив этиологический критерий для классификации. Изучим этот подход подробней.
Эрозия желудка (DA60.0) определена в МКБ-11 как «повреждение слизистой оболочки, достигающее мышечной стенки, но не проходящее сквозь неё». Эрозия желудка может представлять собой фазу развития язвы или сопровождать некоторые формы язвы желудка.
Далее, составители МКБ-11 сообщают, что стрессовые язвы желудка (DA60.3) — это «острые поражения слизистой оболочки, возникающие у тяжелобольных пациентов, которые могут привести к острому кровотечению из верхних отделов желудочно-кишечного тракта». По данным авторов справочника, стрессовая язва желудка может развиться в любом месте желудка, но с большей вероятностью возникает в слизистой оболочке тела и дна желудка.
Эозинофильная и лимфоцитарная язвы желудка (DA60.4 и DA60.5 соотвественно) определяются как результат эозинофильного или лимфоцитарного гастрита. Уточненный диагноз (DA60.2) в новой МКБ дан без пояснений, а «Язва желудка, ассоциированная со вторичной инфекцией» (DA60.7) определяется как «язва желудка, вызванная инфекционными заболеваниями, отличными от Helicobacter pylori, такими как микобактерии, вирусы, грибки и паразиты».
Язва желудка, вызванная внешними причинами (DA60.6)
Этот уточненный диагноз заслуживает особого внимания, так как он делится еще на 4 «поддиагноза»:
Язва желудка, вызванная влиянием алкоголя (DA60.60)
Язва желудка, вызванная химическим воздействием (DA60.61)
Лекарственно-индуцированная язва желудка (DA60.62)
Язва желудка, вызванная воздействием радиации (DA60.63)
Особого пояснения авторы МКБ-11 удостоили лишь «Лекарственно-индуцированную язву желудка». В частности, они сообщают, что ее могут вызывать нестероидные противовоспалительные препараты. Также риск заболевания повышает применение хлорида калия, а также сочетания стероидов с НПВП, бисфосфонатами и микофенолата мофетилом. Также к лекарственно-индуцированной язве желудка авторы классификатора относят особый ее вид «Токсическая язва желудка», однако этот вариант нозологии не имеет ни своего кода, ни определения.
Куда ушли кровотечения и прободения?
Указанные в МКБ-10 состояния отсутствуют в основном «язвенном» разделе МКБ-11, но упоминаются в других частях классификатора. Так, симптом прободения проработан в разделе «Прободения органов ЖКТ» (Digestive system perforation, код ME24.3). Он, в частности, включает уточняющие диагнозы «Пренатальное прободение желудка» (Prenatal gastric perforation, код KB82) и «Постнатальное прободение желудка» (Postnatal gastric perforation, код KB83).
Состояние кровотечения также описано в отдельной подгруппе диагнозов «Желудочно-кишечные кровотечения» (Gastrointestinal bleeding, код ME24.9). Подгруппа включает в себя пункты:
Острое желудочно-кишечное кровотечение, неклассифицированное (Acute gastrointestinal bleeding, not elsewhere classified, код ME24.90)
Хроническое желудочно-кишечное кровотечение, неклассифицированное (Chronic gastrointestinal bleeding, not elsewhere classified, код ME24.91)
Желудочно-кишечное кровотечение, неуточненное (Gastrointestinal bleeding, unspecified, код ME24.9Z).
Обсудить последние новости со всеми коллегами России вы можете в чатах:
Язва желудка хроническая без кровотечения или прободения
Рубрика МКБ-10: K25.7
Содержание
Определение и общие сведения [ править ]
Отличие эрозии от язвы в том, что эрозии не проникают за мышечную пластинку слизистой оболочки.
а) По локализации:
— сочетанные язвы желудка и двенадцатиперстной кишки.
б) По стадии заболевания:
в) По наличию осложнений
Возможные осложнения: кровотечение, пенетрация, перфорация, стенозирование.
Этиология и патогенез [ править ]
— наличие Helicobacter pylori;
— повышение секреции желудочного сока и снижение активности защитных факторов слизистой оболочки (мукопротеины, бикарбонаты).
— нервно-психический (стрессовый) фактор;
— наличие вредных привычек (курение, злоупотребление алкоголем);
— наличие язвенной болезни у близких родственников.
Следует дифференцировать язвенную болезнь желудка и двенадцатиперстной кишки от симптоматических язв, возникающих в рамках гастропатии, индуцированной приёмом НПВС.
Факторы риска формирования язвы на фоне приёма НПВС:
— возраст старше 65 лет;
— наличие в анамнезе язвенной болезни и её осложнений, в первую очередь кровотеченияA;
— необходимость применения высоких доз НПВС;
— необходимость одновременного применения глюкокортикоидов;
— наличие в анамнезе ИБС;
— одновременный приём антикоагулянтов.
Клинические проявления [ править ]
— Ранние боли возникают через 0,5-1 ч после еды, постепенно нарастают по интенсивности, сохраняются в течение 1,5-2 ч, уменьшаются и исчезают по мере продвижения желудочного содержимого в двенадцатиперстную кишку; характерны для язв тела желудка. При поражении кардиального, субкардиального и фундального отделов болевые ощущения возникают сразу после приёма пищи.
— Поздние боли возникают через 1,5-2 ч после еды, постепенно усиливаются по мере эвакуации содержимого из желудка; характерны для язв пилорического отдела желудка и луковицы двенадцатиперстной кишки.
— «Голодные» (ночные) боли возникают через 2,5-4 ч после еды, исчезают после очередного приёма пищи; характерны для язв двенадцатиперстной кишки и пилорического отдела желудка.
— Сочетание ранних и поздних болей наблюдают при сочетанных или множественных язвах.
Наиболее типичной проекцией болей в зависимости от локализации язвенного процесса считают следующую:
Пальпация эпигастральной области может оказаться болезненной.
Отсутствие типичного характера болей не противоречит диагнозу язвенной болезни.
Возможны тошнота и рвота. Обязательно необходимо уточнить у больного наличие эпизодов рвоты кровью или чёрного стула (мелена). Дополнительно при физикальном обследовании следует целенаправленно пытаться выявить признаки возможного злокачественного характера изъязвления или наличия осложнений язвенной болезни.
Язва желудка хроническая без кровотечения или прободения: Диагностика [ править ]
Язвенную болезнь следует подозревать при наличии у пациента болей, связанных с приёмом пищи в сочетании с тошнотой и рвотой, в эпигастральной, пилородуоденальной областях или правом и левом подреберьях. Клиническая картина может зависеть от локализации язвенного дефекта, его размеров и глубины, секреторной функции желудка, возраста больного. Следует всегда иметь в виду возможность бессимптомного обострения язвенной болезни.
Следует понимать, что анамнестические данные о выявленной ранее инфекции Helicobacter pylori и длительном приёме больным НПВC не могут выступать решающим фактором для установления диагноза язвенной болезни. Анамнестическое выявление факторов риска язвенной болезни у больных, принимающих НПВC может оказаться полезным в плане установления показаний для проведения ФЭГДС (фиброэзофагогастродуоденоскопии).
Патогномоничных для язвенной болезни лабораторных признаков нет.
Следует проводить исследования с целью исключения осложнений, в первую очередь язвенного кровотечения:
— общий анализ крови (ОАК);
— анализ кала на скрытую кровь.
ФЭГДС (фиброэзофагогастродуоденоскопия) позволяет достоверно диагностировать и охарактеризовать язвенный дефект. Дополнительно ФЭГДС позволяет контролировать его заживление, проводить цитологическую и гистологическую оценку морфологической структуры слизистой оболочки желудка, исключать злокачественный характер изъязвления. При наличии язвы желудка необходимо взятие 4-6 биоптатов из дна и краёв язвы с последующим их гистологическим исследованием для исключения наличия опухоли.
Контрастное рентгенологическое исследование верхних отделов ЖКТ также позволяет выявить язвенный дефект, однако по чувствительности и специфичности рентгенологический метод уступает эндоскопическому.
Внутрижелудочная рН-метрия. При язвенной болезни наиболее часто обнаруживают повышенную либо сохранённую кислотоообразующую функцию желудка.
УЗИ органов брюшной полости для исключения сопутствующей патологии.
Выявление Helicobacter pylori
Проводят забор не менее 5 биоптатов слизистой оболочки желудка: по два из антрального и фундального отделов и одного из области угла желудка. Для подтверждения успешности эрадикации микроба данное исследование выполняют не ранее 4-6-й недели после завершения терапии.
— Бактериологический метод мало используется в рутинной клинической практике.
— Иммуногистохимический метод с применением моноклональных АТ: обладает большей чувствительностью, так как используемые АТ избирательно окрашивают H. pylori. Мало используется в рутинной клинической практике для диагностики H. pylori.
— Серологические методики: обнаружение АТ к H. pylori в сыворотке крови. Метод наиболее информативен при проведении эпидемиологических исследований. Клиническое применение теста ограничено тем, что он не позволяет дифференцировать факт инфицирования в анамнезе от наличия H. pylori в настоящий момент. В последнее время появились более чувствительные системы, которые позволяют диагностировать эрадикацию по снижению титра антихеликобактерных АТ в сыворотке крови больных в стандартные сроки 4-6 нед методом иммуноферментного анализа.
— ПЦР-диагностика. Можно исследовать как биоптат, так и фекалии больного.
При соблюдении всех правил выполнения методик и надлежащей стерилизации эндоскопической аппаратуры первичная диагностика H. pylori обосновывает начало антихеликобактерной терапии при обнаружении бактерии одним из описанных методов.
Диагностика результата эрадикационной терапии H. pylori
— Диагностику любым методом проводят не ранее 4-6 нед после окончания курса антихеликобактерной терапии.
— Референтным методом для определения успешности эрадикационной терапии H. pylori служит дыхательный тест с пробным завтраком мочевиной, меченной 14 С. При использовании методов непосредственного обнаружения бактерии в биоптате (бактериологический, морфологический, уреазный) необходимо исследование как минимум двух биоптатов из тела желудка и одного из антрального отдела.
— Цитологический метод для установления эффективности эрадикации неприменим.
Дифференциальный диагноз [ править ]
Дифференциальный диагноз проводят между язвами различной локализации, между язвенной болезнью и симптоматическими язвами, а также между доброкачественными язвами и язвенной формой рака желудка. Такая форма рака может какое-то время протекать под «маской» доброкачественной язвы. В пользу злокачественного изъязвления свидетельствуют его большие размеры (особенно у пациентов молодого возраста), локализация язвенного дефекта на большой кривизне желудка, повышение СОЭ. При рентгенологическом и эндоскопическом исследовании в случаях злокачественных изъязвлений желудка выявляют язвенный дефект неправильной формы с неровными и бугристыми краями; слизистая оболочка желудка вокруг язвы инфильтрирована, стенка желудка в месте изъязвления ригидна. Окончательное заключение о характере изъязвления выносят после гистологического исследования биоптатов. Во избежание ложноотрицательных результатов биопсию следует проводить повторно вплоть до полного заживления язвы.
Язва желудка хроническая без кровотечения или прободения: Лечение [ править ]
Больные с неосложнённым течением язвенной болезни подлежат консервативному лечению.
— Эрадикация H. pylori.
— Быстрая ликвидация симптоматики заболевания.
— Достижение стойкой ремиссии.
— Предупреждение развития осложнений.
Показания к госпитализации
— Язвенная болезнь с клинической картиной выраженного обострения: сильный болевой синдром, рвота.
— Обнаружение изъязвлений в желудке, требующих дифференциального диагноза между доброкачественными язвами и раком желудка.
— Признаки желудочно-кишечного кровотечения (мелена, рвота кровью и др.), перфорации и пенетрации язвенного дефекта.
— Язвенная болезнь желудка и двенадцатиперстной кишки с наличием осложнений в анамнезе (прежде всего желудочно-кишечного кровотечения).
— Язвенная болезнь с сопутствующими заболеваниями.
Больных с обострением язвенной болезни желудка лечат в условиях общетерапевтического или гастроэнтерологического отделений.
Больные с неосложнённым течением язвенной болезни подлежат консервативному лечению в амбулаторных условиях.
Больным необходимо обеспечить охранительный режим с ограничением физических и эмоциональных нагрузок, прекратить курение и употребление алкоголя. Рекомендации по изменению образа жизни следует давать в соответствии с общим состоянием больного и наличием у него других заболеваний.
Питание должно быть частым, дробным, механически и химически щадящим с исключением блюд, вызывающих или усиливающих клинические проявления заболевания (например, острых приправ, маринованных и копчёных продуктов).
в) Прочие рекомендации
Следует убедиться в том, что пациент не принимает НПВП (в том числе анальгетики в связи с различными болевыми синдромами или ацетилсалициловую кислоту с профилактической целью). При необходимости их длительного применения следует рассмотреть возможность уменьшения дозы препарата или замены на другое ЛС, обладающее меньшим воздействием на слизистую оболочку ЖКТ. Нужно помнить, что приём НПВП вместе с пищей не ослабляет их негативного воздействия на слизистую оболочку желудка и двенадцатиперстной кишки. Замена НПВП на лекарственные формы с кишечно-растворимым покрытием также не устраняет их нежелательного влияния.
Показанием для проведения эрадикационной терапии (при наличии H. pylori) выступает язвенная болезнь желудка или двенадцатиперстной кишки в фазе обострения или ремиссии, включая осложнённую язвенную болезнь.
Эта схема назначается только в том случае, если показатели резистентности штаммов H. pylori к кларитромицину в данном регионе не превышают 20%. Эффективность 14-дневного курса эрадикации на 9-12% выше, чем 7-дневного.
При неосложнённой язвенной болезни двенадцатиперстной кишки нет необходимости продолжать антисекреторную терапию после проведения курса эрадикации. При обострении язвенной болезни желудка, а также при обострении протекающей на фоне сопутствующих заболеваний или с осложнениями язвенной болезни двенадцатиперстной кишки рекомендуют продолжить антисекреторную терапию с использованием одного из антисекреторных препаратов (более эффективные ингибиторы протонного насоса или блокаторы Н2-рецепторов гистамина) в течение 2-5 нед для эффективного заживления язвы.
При неэффективности терапии первой линии рекомендуется назначение терапии второй линии (квадротерапии), включающей:
— ингибитор протонного насоса (омепразол, или лансопразол, или рабепразол, или эзомепразол, или пантопразол) в стандартной дозе 2 раза в день;
— метронидазол (500 мг 3 раза в день) или фуразолидон (50-150 мг 4 раза в день) в течение как минимум 7 дней.
Кроме того, в качестве резервных схем эрадикации могут назначаться комбинация амоксициллина (750 мг 4 раза в сутки) с блокаторами протонного насоса, рифабутином (300 мг/сут) или левофлоксацином (500 мг/сут).
При отсутствии H. pylori больным язвенной болезнью желудка назначают базисную терапию ингибиторами протонного насоса, которые предпочтительны по сравнению с блокаторами H2-рецепторов гистаминаB. Различные представители группы блокаторов протонного насоса одинаково эффективныA. Применяют следующие препараты:
— омепразол в дозе 20-40 мг/сут;
Блокаторы Н2-рецепторов гистамина менее эффективны по сравнению с ингибиторами протонного насосаB. Назначают следующие препараты:
— ранитидин в дозе 150 мг 2 раза в сутки или 300 мг на ночь;
— фамотидин в дозе 20 мг 2 раза в сутки или 40 мг на ночь.
Антацидные препараты (алюминиево-магниевые антациды или алюминиево-магниевые с добавлением кальция алгината через 1,5-2 ч после еды или по требованию, или алюминиево-магниевый антацид с добавлением симетикона и БАВ (порошок корней солодки голой), усиливающий антацидный эффект и слизеобразование) применяют дополнительно в качестве симптоматических средств.
Показаниями к хирургическому лечению язвенной болезни служат осложнения этого заболевания.
Профилактика [ править ]
Прочее [ править ]
Прогноз благоприятный при неосложнённой язвенной болезни. В случае успешной эрадикации рецидивы язвенной болезни в течение первого года возникают у 6-7% больных. Прогноз ухудшается при большой давности заболевания в сочетании с частыми, длительными рецидивами, при осложнённых формах язвенной болезни.
Клинические рекомендации Российской гастроэнтерологической ассоциации по диагностике и лечению язвенной болезни
Год утверждения рекомендаций — 2016.
Целевая аудитория клинических рекомендаций: гастроэнтерологи, терапевты, врачи общей практики.
Diagnostics and treatment of peptic ulcer: clinical guidelines of the Russian gastroenterological Association
The year of guidance approval — 2016.
Target audience for the clinical guidelines: gastroenterologists, physicians, general practitioners.
Шептулин Аркадий Александрович — доктор медицинских наук, профессор кафедры пропедевтики внутренних болезней ФГБОУ ВО «Первый МГМУ им. И. М. Сеченова». Контактная информация: arkalshep@gmail.com; 119991, Москва, ул. Погодинская, д. 1, стр. 1
Sheptulin Arkady A. — MD, PhD, professor, Chair of internal diseases propedeutics, medical faculty, Sechenov First Moscow state medical university. Contact information: arkalshep@gmail.com; 119991, Moscow, Pogodinskaya str., 2, bld.1
Поступила: 07.10.2016 / Received: 07.10.2016
Цель публикации. Довести до практикующих врачей современные представления об этиологии и патогенезе язвенной болезни (ЯБ), познакомить с применяющимися в настоящее время методами диагностики и основными подходами к лечению данной патологии. распространенных Основные положения. ЯБ продолжает оставаться одним из наиболее распространенных заболеваний органов пищеварения. Несмотря на тенденцию к снижению частоты госпитализаций больных с неосложненным течением ЯБ, отмечено увеличение частоты осложненных форм заболевания, что связано главным образом с растущим приемом нестероидных противовоспалительных препаратов (НПВП). Ведущая роль в этиологии ЯБ принадлежит инфекции Helicobacter pylori. Не ассоциированными с H. pylori могут быть гастродуоденальные язвы, обусловленные приемом НПВП, а также язвенные поражения, возникшие в рамках других заболеваний (симптоматические язвы желудка и двенадцатиперстной кишки). Диагностика ЯБ включает в себя обязательное тестирование на H. pylori и проведение эрадикации инфекции в случае получения положительных результатов. Схемами антигеликобактерного лечения первой линии в настоящее время служат стандартная тройная терапия с кларитромицином и амоксициллином, а также квадротерапия с препаратами висмута. В качестве схем второй линии применяются квадротерапия с препаратами висмута и тройная терапия с левофлоксацином. Схемы терапии третьей линии подбирают после индивидуального определения чувствительности штаммов H. pylori к антибиотикам. Контроль антигеликобактерного лечения проводится не ранее чем через 4 недели после окончания эрадикации.
Заключение. Строгое соблюдение алгоритма обследования рассматриваемой категории больных и протокола эрадикационной терапии позволяет значительно снизить риск развития рецидивов ЯБ и ее осложнений.
Ключевые слова: язва желудка, язва двенадцатиперстной кишки, инфекция Helicobacter pylori, эрадикация, ингибиторы протонной помпы.
The aim of publication. To present modern concept on etiology and pathogenesis of the peptic ulcer (PUD) to general practitioners, to acquaint them with modern diagnostic methods and main treatment approaches of this disease.
Summary. The PUD continues to remain one of the most widespread digestive disease. Despite a tendency to decrease of hospital admission rate of patients with uncomplicated PUD, increase in complicated forms of disease rate is noted that it is related mainly to the growing intake of non-steroidal anti-inflammatory drugs (NSAID). Helicobacter pylori infection has a leading role as PUD ethological factor. Non-H. pylori-associated gastroduodenal ulcers may be caused by NSAID intake or may develop within the other nosological entities (symptomatic stomach and duodenal ulcers). PUD diagnosis includes obligatory testing for H. pylori infection and carrying out eradication in the case of positive takes. At the present time the first line of antihelicobacter therapy includes standard triple clarithromycin and amoxicillin-based therapy, as well as quadrotherapy with bismuth drugs. The second line eradication therapy includes quadrotherapy with bismuth drugs and triple levofloxacin-based therapy. The third line therapy modes should be chosen after assessment of individual antibiotic sensitivity of H. pylori strains. The efficacy control of antihelicobacter treatment should be carried out not earlier than 4 weeks after the end of eradication.
Conclusion. Strict conformance of diagnostic algorithm for this category of patients as well as the eradication therapy protocol allows to decrease considerably the risk of recurrence of PUD and its complications.
Key words: stomach ulcer, duodenal ulcer, Helicobacter pylori infection, eradication, proton pump inhibitors.
Для цитирования: Ивашкин В. Т., Шептулин А. А., Маев И. В., Баранская Е. К., Трухманов А. С., Лапина Т. Л., Бурков С. Г., Калинин А. В., Ткачев А. В. Клинические рекомендации Российской гастроэнтерологической ассоциации по диагностике и лечению язвенной болезни. Рос журн гастроэнтерол гепатол колопроктол 2016; 26(6):40-54
For citation: Ivashkin V.T., Sheptulin A.A., Mayev I.V., Baranskaya Ye.K., Trukhmanov A.S., Lapina T.L., Burkov S.G., Kalinin A.V., Tkachev A.V. Diagnostics and treatment of peptic ulcer: clinical guidelines of the Russian gastroenterological Association. Ross z gastroenterol gepatol koloproktol 2016; 26(6):40-54 (In Russ.)
Актуальность проблемы обусловливается сохраняющейся в частотой и распространенностью настоящее время высокой язвенной болезни (ЯБ), ее длительным течением с возможным формированием часто рецидивирующих и трудно рубцующихся язв, риском развития серьезных осложнений, требующих во многих случаях проведения оперативных вмешательств, значительными расходами, которые несет здравоохранение на обследование и лечение таких пациентов.
Не всегда удовлетворительные результаты обследования и лечения являются нередко следствием ошибок, допускаемых в диагностике (в частности, инфекции Helicobacter pylori) и лечении больных. Большое клиническое значение имеет растущая устойчивость H. pylori к антибиотикам. Все это ставит на повестку дня необходимость подготовки рекомендаций, которые помогли бы врачу выбрать для каждого конкретного пациента оптимальный план диагностики и терапии.
1. Определение
Язвенная болезнь представляет собой хроническое рецидивирующее заболевание, протекающее с чередованием периодов обострения и ремиссии, ведущим проявлением ЯБ служит образование дефекта (язвы) в стенке желудка или двенадцатиперстной кишки.
2. Этиология и патогенез
В 1910 г. К. Schwarz сформулировал ставший впоследствии известным тезис «без кислоты нет язвы», который отражает основной патогенетический фактор возникновения язвенных дефектов.
В дальнейшем наши знания о патогенезе ЯБ значительно расширились. Согласно современным представлениям, патогенез ЯБ в общем виде сводится к нарушению равновесия между факторами кислотно-пептической агрессии желудочного содержимого и элементами защиты слизистой оболочки желудка и двенадцатиперстной кишки и изображается в виде «весов», предложенных H. Shay и D.C.H. Sun [1]. На одной чаше этих весов помещены факторы агрессии, а на другой — факторы защиты. Если обе чаши весов уравновешивают друг друга, ЯБ у человека не развивается. Усиление факторов агрессии или ослабление факторов защиты приводит к нарушению этого равновесия и возникновению язвы.
Агрессивное звено язвообразования включает в себя увеличение массы обкладочных клеток (часто наследственно обусловленное), гиперпродукцию гастрина, нарушение нервной и гуморальной регуляции желудочного кислотовыделения, расстройство выработки пепсиногена и пепсина, нарушение гастродуоденальной моторики (задержка или, наоборот, ускорение эвакуации из желудка), обсеменение слизистой оболочки микроорганизмами H. pylori.
Ослабление защитных свойств слизистой оболочки желудка и двенадцатиперстной кишки может возникнуть в результате снижения выработки и изменения качественного состава желудочной слизи, уменьшения секреции бикарбонатов, снижения регенераторной активности эпителиальных клеток, ухудшения кровоснабжения слизистой желудка, уменьшения содержания простагландинов в желудочной стенке, например, при приеме нестероидных противовоспалительных препаратов (НПВП).
Определенное место в патогенезе ЯБ занимают также гормональные факторы (половые гормоны, гормоны коры надпочечников, гастроинтестинальные пептиды), биогенные амины (гистамин, серотонин, катехоламины), нарушения процессов перекисного окисления липидов.
Решающая этиологическая роль в развитии ЯБ отводится сегодня микроорганизмам H. pylori, обнаруженным в 1983 г. австралийскими учеными Б. Маршаллом (B. Marshall) и Дж. Уорреном (J. Warren).
Спектр неблагоприятного влияния H. pylori достаточно многообразен. Эти бактерии вырабатывают целый ряд ферментов, повреждающих защитный барьер слизистой оболочки (уреаза, протеазы, фосфолипазы), а также различные цитотоксины. Наиболее патогенными являются VacA-штамм H. pylori — продуцирующий вакуолизирующий цитотоксин, приводящий к образованию цитоплазматических вакуолей и гибели эпителиальных клеток, и CagA-штамм, экспрессирующий ген, ассоциированный с цитотоксином. Этот ген кодирует белок массой 128 кДа, который оказывает повреждающее действие на слизистую оболочку.
H. pylori способствуют высвобождению в слизистой оболочке желудка интерлейкинов, лизосомальных энзимов, фактора некроза опухолей, что вызывает развитие воспалительных процессов.
Обсеменение слизистой оболочки желудка H. pylori сопровождается формированием поверхностного антрального гастрита и дуоденита и ведет к повышению уровня гастрина с последующим усилением секреции соляной кислоты. Избыточное количество соляной кислоты, попадая в просвет двенадцатиперстной кишки, в условиях относительного дефицита панкреатических бикарбонатов способствует прогрессированию дуоденита и, кроме того, обусловливает появление в кишке участков желудочной метаплазии (перестройку эпителия дуоденальной слизистой оболочки по желудочному типу), которые быстро заселяются H. pylori. В дальнейшем при неблагоприятном течении, особенно при наличии дополнительных этиологических факторов (наследственная предрасположенность, 0 (I) группа крови, курение, нервно-психические стрессы и др.) в участках метаплазированной слизистой формируется язвенный дефект. Ассоциированными с H. pylori оказывается около 80% язв двенадцатиперстной кишки и 60% язв желудка [2]. H. pylori-негативные язвы чаще всего бывают обусловлены приемом НПВП.
3. Эпидемиология
Несмотря на некоторое снижение частоты ЯБ к концу минувшего столетия, это заболевание, по-прежнему, остается одним из наиболее распространенных заболеваний органов пищеварения. Показано, что 11–14% мужчин и 8–11% женщин в течение своей жизни могут заболеть ЯБ [3]. Например, в США ежегодно выявляют 500 000 больных с впервые обнаруженной ЯБ и более 4 млн пациентов с рецидивами заболевания [2, 4]. Локализация язв в двенадцатиперстной кишке встречается в 4 раза чаще, чем в желудке. Среди пациентов с дуоденальными язвами мужчины преобладают над женщинами, тогда как при язвах желудка соотношение мужчин и женщин примерно одинаково [5].
В последние годы наблюдается тенденция к снижению госпитализаций больных с неосложненными формами ЯБ как в зарубежных странах [6], так и в России. Анализ частоты и распространенности ЯБ в Российской Федерации по материалам Министерства здравоохранения РФ показывает, что за период с 2006 по 2009 г. уменьшилось как общее число пациентов с ЯБ (с 1 663 660 до 1 522 938) и число больных в пересчете на 100 000 населения (с 1446,5 до 1314,6), так и число лиц с впервые выявленной ЯБ (с 148 019 до 136 363 в абсолютных цифрах и с 128,7 до 117,7 в пересчете на 100 000 населения).
Эта положительная динамика, безусловно, связана с активным обследованием больных, предъявляющих жалобы на диспепсические расстройства, на наличие инфекции H. pylori, и с проведением последующей эрадикационной терапии.
В то же время во всем мире отмечено увеличение частоты осложнений ЯБ (кровотечений, перфораций). Так, согласно статистическим данным Минздрава Российской Федерации (2000), число больных с язвенными кровотечениями увеличилось в нашей стране с 28 913 в 1990 г. до 64 045 в 1999 г. [7]. Увеличение осложненных форм ЯБ обусловливается растущим применением НПВП [6]. В Великобритании от осложнений язвенных поражений желудка и двенадцатиперстной кишки, связанных с приемом НПВП, ежегодно погибает более 2000, в США — более 16 500 пациентов [8].
4. Классификация
Код по МКБ Х*: К25 — язва желудка; К26 — язва двенадцатиперстной кишки.
Общепринятой классификации ЯБ не существует. Прежде всего, в зависимости от наличия или отсутствия инфекции H. pylori, выделяют ЯБ, ассоциированную и не ассоциированную с H. pylori. Последнюю форму иногда называют идиопатической. Различают также ЯБ как самостоятельное заболевание и симптоматические язвы желудка и двенадцатиперстной кишки (лекарственные, «стрессовые», при эндокринной патологии, при других хронических заболеваниях внутренних органов), которые возникают на фоне иных заболеваний и по механизмам развития связаны с особыми этиологическими и патогенетическими факторами.
В зависимости от локализации выделяют язвы желудка (кардиального и субкардиального отделов, тела желудка, антрального отдела, пилорического канала), двенадцатиперстной кишки (луковицы, постбульбарного отдела), а также сочетанные язвы желудка и двенадцатиперстной кишки. При этом язвы могут располагаться на малой или большой кривизне, передней и задней стенках желудка и двенадцатиперстной кишки.
По числу язвенных поражений различают одиночные и множественные язвы, а в зависимости от размеров язвенного дефекта — язвы малых (до 0,5 см в диаметре) и средних (0,6–1,9 см в диаметре) размеров, большие (2,0–3,0 см) и гигантские (свыше 3,0 см).
В диагнозе отмечаются стадия течения заболевания — обострение, рубцевание (эндоскопически подтвержденная стадия «красного» и «белого» рубца) и ремиссия, а также рубцово-язвенная деформация желудка и двенадцатиперстной кишки.
При формулировке диагноза указываются наличие осложнений ЯБ (в том числе анамнестических) — кровотечений, прободений, пенетраций, рубцово-язвенного стеноза привратника, а также характер оперативных вмешательств, если они проводились.
5. Диагностика
5.1. Клиническое обследование
Ведущим симптомом обострения ЯБ являются боли в подложечной области, которые могут иррадиировать в левую половину грудной клетки и левую лопатку, грудной или поясничный отдел позвоночника. Боли возникают сразу после приема пищи (при язвах кардиального и субкардиального отделов желудка), через полчаса–час после еды (при язвах тела желудка). При поражениях пилорического канала и луковицы двенадцатиперстной кишки обычно наблюдаются поздние боли (через 2–3 часа после еды), «голодные» боли, возникающие натощак и проходящие после приема пищи, а также ночные боли. Боли проходят после приема антисекреторных и антацидных препаратов [5].
При обострении ЯБ часто отмечаются также отрыжка кислым, тошнота, запоры. Рвота кислым желудочным содержимым, приносящая облегчение и потому вызываемая больными искусственно, всегда считалась признаком ЯБ, однако в настоящее время она встречается сравнительно редко.
Типичными для ЯБ являются сезонные (весной и осенью) периоды усиления болей и диспепсических симптомов. При обострении заболевания нередко регистрируется похудание, поскольку, несмотря на сохраненный, а иногда даже повышенный аппетит, больные ограничивают себя в еде, опасаясь усиления болей.
В период обострения ЯБ при объективном обследовании часто удается выявить болезненность в эпигастральной области при пальпации, сочетающуюся с умеренной резистентностью мышц передней брюшной стенки. Также может обнаруживаться локальная перкуторная болезненность в этой же области (симптом Менделя). Но эти признаки не являются строго специфичными для обострения болезни.
5.2. Лабораторная диагностика
Клинический анализ крови при неосложненном течении ЯБ чаще всего остается без существенных изменений. Иногда отмечается незначительное повышение содержания гемоглобина и эритроцитов, вместе с тем может обнаруживаться и анемия, свидетельствующая о явных или скрытых кровотечениях. Лейкоцитоз и повышение СОЭ встречаются при осложненных формах болезни (например, при пенетрации язвы).
Определенное место в диагностике обострений ЯБ занимает анализ кала на скрытую кровь. При интерпретации получаемых при этом данных необходимо помнить, что положительные результаты на скрытую кровь встречаются и при многих других заболеваниях, что требует их обязательного исключения.
Важную роль в диагностике играет исследование кислотообразующей функции желудка, которое в последние годы проводится с помощью суточного мониторирования внутрижелудочного рН. При язвах двенадцатиперстной кишки и пилорического канала обычно отмечаются повышенные показатели секреции HCl, при язвах тела и субкардиального отдела желудка — нормальные или сниженные. Обнаружение и подтверждение гистаминустойчивой ахлоргидрии практически всегда исключает диагноз ЯБ двенадцатиперстной кишки и ставит под сомнение доброкачественный характер язвы желудка.
5.3. Инструментальная диагностика
Основное значение в диагностике ЯБ имеют рентгенологический и эндоскопический методы исследования. При рентгенологическом исследовании выявляются прямой признак ЯБ — «ниша» на контуре или на рельефе слизистой оболочки и косвенные признаки (местный циркулярный спазм мышечных волокон на противоположной по отношению к язве стенке желудка в виде «указующего перста», конвергенция складок слизистой оболочки к «нише», рубцово-язвенная деформация желудка и луковицы двенадцатиперстной кишки, гиперсекреция натощак, нарушения гастродуоденальной моторики).
В настоящее время к рентгенологическому исследованию с целью диагностики ЯБ прибегают не столь часто, как раньше. Его применяют в тех случаях, когда по каким-то причинам (например, наличие противопоказаний) не удается провести эндоскопию, когда с целью дифференциальной диагностики с инфильтративно-язвенной формой рака необходимо оценить перистальтику стенки желудка, когда нужно оценить характер эвакуации из желудка.
Эзофагогастродуоденоскопия (ЭГДС) подтверждает наличие язвенного дефекта, уточняет его локализацию, глубину, форму, размеры, позволяет оценить состояние дна и краев язвы, выявить сопутствующие изменения слизистой оболочки, нарушения гастродуоденальной моторики. При локализации язвы в желудке проводится биопсия с последующим гистологическим исследованием, позволяющим исключить злокачественный характер язвенного поражения.
5.4. Диагностика инфекции H. pylori
Морфологический (гистологический) метод также относится к распространенным методам первичной диагностики инфекции H. pylori при проведении биопсии. Исследование биоптатов слизистой оболочки желудка с применением различных окрасок (акридиновый оранжевый, краситель Гимзы, серебрение по Вартину–Старри) позволяет не только с высокой степенью надежности выявить наличие инфекции, но и количественно определить степень обсеменения. При использовании эндоскопических методов диагностики берут, как минимум, 2 биоптата из тела желудка и 1 биоптат из антрального отдела.
Если больному не проводится ЭГДС, то для диагностики H. pylori предпочтительно применять уреазный дыхательный тест с использованием мочевины, меченной изотопами 13 С или 14 C. Этот метод предполагает наличие массспектрографа для улавливания этих изотопов в выдыхаемом воздухе. В России дыхательный уреазный тест стал доступен благодаря отечественным разработкам. При этом анализ изотопического соотношения 13 СО2/ 12 СО2 может проводиться с помощью оригинальной диодной лазерной спектроскопии [9].
В качестве неинвазивного метода первичной диагностики инфекции можно применять также определение антигена H. pylori в кале с помощью иммуноферментного анализа и определение ДНК H. pylori (в слизистой оболочке желудка, в кале) с помощью полимеразной цепной реакции (ПЦР).
Серологический метод выявления антител к H. pylori используется в научных исследованиях в основном с целью оценки инфицированности различных групп населения, поскольку не требует проведения эндоскопии, наличия сложных приборов, специально обученного персонала. Но его можно применять и для первичной диагностики инфекции H. pylori в широкой клинической практике. К недостаткам относится то, что данный метод не позволяет отличить текущую инфекцию от перенесенной (т. е. его нельзя применять для контроля эрадикации), а также он обладает более низкой чувствительностью у детей.
В то же время серологический метод имеет и ряд преимуществ — дает возможность обнаружить H. pylori у больных с низкой обсемененностью, может применяться при язвенных кровотечениях, на его результаты не влияют предшествующая антисекреторная терапия и прием антибиотиков. Однако достоверность результатов обеспечивается только в том случае, если применяемые методики валидизированы и определяемые антитела относятся к классу IgG [10].
Микробиологический (бактериологический) метод получения культуры H. pylori отличается тем, что с его помощью можно определить чувствительность микроорганизма к тому или иному антибактериальному препарату. Но при этом существует ряд трудностей, обусловленных необходимостью наличия специальных сред, проведения в условиях определенной температуры, влажности, качества атмосферного воздуха и т. д. Все это приводит к тому, что рост колоний микроорганизмов удается получить далеко не всегда. Неудобство метода связано и с тем, что его результатов приходится ждать, как правило, не менее 10–14 дней. В настоящее время он применяется для установления индивидуальной чувствительности бактерий к антибиотикам в случаях неэффективности лечения. Определение конкретного штамма H. pylori (CagA, VacA и др.) не играет роли в решении вопроса об антигеликобактерном лечении. Обнаружение любого штамма H. pylori служит показанием к его устранению.
Для контроля эрадикации, который проводят через 4–6 недель после окончания эрадикационной терапии, лучше всего применять уреазный дыхательный тест или определение антигена H. pylori в кале.
Проблема диагностики инфекции H. pylori заключается в возможности получения ложно отрицательных результатов, связанных главным образом с тем, что исследование выполняется на фоне терапии ингибиторами протонной помпы (ИПП) или вскоре после нее. Во избежание ложноотрицательных результатов прием ИПП необходимо прекратить за 2 недели, а антибиотиков и препаратов висмута — за 4 недели до предполагаемого контрольного исследования [10]. Кроме того, отрицательный результат исследования на инфекцию H. pylori должен быть обязательно подтвержден другими методами диагностики.
5.5. Дифференциальный диагноз
Язвенную болезнь необходимо дифференцировать с симптоматическими язвами желудка и двенадцатиперстной кишки. К ним относятся стрессовые и лекарственные язвы, язвы при эндокринной патологии и при некоторых других заболеваниях внутренних органов.
В число стрессовых гастродуоденальных язв входят острые, обычно множественные язвы желудка и двенадцатиперстной кишки, возникающие при распространенных ожогах (язвы Курлинга), после черепно-мозговых травм и нейрохирургических операций (язвы Кушинга), после обширных полостных операций, особенно связанных с трансплантацией органов, при остром инфаркте миокарда, терминальной стадии хронической почечной и печеночной недостаточности, других критических состояниях. Стрессовые язвы нередко протекают малосимптомно, отличаются наклонностью к желудочно-кишечным кровотечениям (их частота достигает 40–45%) и характеризуются высоким числом летальных исходов, обусловленных часто тяжелым течением фонового заболевания.
Среди лекарственных язв наибольшее значение имеют острые эрозивно-язвенные поражения, связанные с приемом НПВП (НПВП-ассоциированная гастропатия), блокирующих фермент циклооксигеназу‑1, отвечающий за синтез простагландинов в стенке желудка. Гастродуоденальные язвы возникают у 20–25% больных, длительно принимающих НПВП, эрозивные поражения — более чем у 50% пациентов, К факторам риска их развития относятся пожилой возраст, наличие ЯБ в анамнезе, сопутствующие заболевания сердечно-сосудистой системы и печени, высокая доза НПВП, одновременный прием антикоагулянтов.
Гастродуоденальные язвы и эрозии, обусловленные приемом НПВП, также часто имеют множественный характер, нередко протекают малосимптомно и манифестируются внезапными желудочно-кишечными кровотечениями (меленой или рвотой содержимым типа «кофейной гущи»), риск развития которых у таких пациентов возрастает в 4–5 раз.
К язвам желудка и двенадцатиперстной кишки, возникающим на фоне эндокринных заболеваний, относят язвы у больных с синдромом Золлингера–Эллисона и гиперпаратиреозом. Патогенез гастродуоденальных язв при синдроме Золлингера–Эллисона связан с резкой гиперсекрецией соляной кислоты в результате наличия у больных гастринпродуцирующей опухоли (чаще всего в поджелудочной железе). Эти язвы обычно бывают множественными, локализуются не только в желудке и двенадцатиперстной кишке, но и в тощей кишке, а иногда и пищеводе, протекают с выраженными болевыми ощущениями, упорной диареей. При обследовании больных отмечается резко повышенный уровень желудочного кислотовыделения (особенно в базальных условиях), определяется увеличенное содержание сывороточного гастрина (в 3–4 раза по сравнению с нормой). В распознавании синдрома Золлингера–Эллисона помогают провокационные тесты с секретином, глюкагоном, ультразвуковое исследование и компьютерная томография поджелудочной железы.
Гастродуоденальные язвы у больных гиперпаратиреозом отличаются от язвенной болезни (помимо тяжелого течения с частыми рецидивами, с наклонностью к кровотечениям и перфорации) наличием признаков повышенной функции паращитовидных желез (мышечная слабость, боли в костях, жажда, полиурия). Диагноз ставится на основании определения уровня кальция и фосфора в сыворотке крови, признаков гиперпаратиреоидной остеодистрофии, характерных симптомов поражения почек и неврологических расстройств.
Кроме того, выделяют симптоматические язвы у больных распространенным атеросклерозом, полицитемией, системным мастоцитозом с карциноидным синдромом. Язвы желудка и двенадцатиперстной кишки при болезни Крона (БК), которые также обычно относят к симптоматическим гастродуоденальным язвам, на самом деле представляют собой самостоятельную форму БК с поражением желудка и двенадцатиперстной кишки.
При обнаружении язв в желудке необходимо обязательно проводить дифференциальный диагноз между доброкачественными язвенными поражениями, малигнизацией язв и инфильтративно-язвенной формой рака желудка. В пользу злокачественного поражения свидетельствуют его очень большие размеры (особенно у больных сравнительно молодого возраста), локализация язвенного дефекта на большой кривизне желудка, повышение СОЭ и гистаминустойчивая ахлоргидрия.
При рентгенологическом и эндоскопическом исследовании в случаях злокачественных изъязвлений выявляют неправильную форму язвенного дефекта, его неровные и бугристые края, инфильтрацию слизистой оболочки вокруг язвы, ригидность стенки желудка в месте изъязвления. Большую помощь в оценке характера поражения желудочной стенки в зоне изъязвления, а также состояния региональных лимфатических узлов может оказать эндоскопическая ультрасонография. Окончательное заключение выносится после гистологического исследования биоптатов язвы. С учетом возможности ложноотрицательных результатов биопсию следует проводить повторно, вплоть до полного заживления язвы, с взятием при каждом исследовании не менее 3–4 кусочков ткани.
Гастродуоденальные язвы, при которых не удается выявить инфекцию H. pylori или связь с приемом лекарственных препаратов (в частности, НПВП), а также отсутствует симптоматический характер язвенных поражений, носят название идиопатических. Факторами, предрасполагающими к их возникновению, служат пожилой возраст больных, нарушения процессов слизеобразования в желудке, нервно-психические стрессы, мезентериальная ишемия [11].
5.6. Течение и осложнения
В неосложненных случаях ЯБ протекает обычно с чередованием периодов обострения (продолжительностью от 3–4 до 6–8 недель) и ремиссии (длительностью от нескольких недель до многих лет). Под влиянием неблагоприятных факторов (например, таких как физическое перенапряжение, прием НПВП и/или препаратов, снижающих свертываемость крови, злоупотребление алкоголем) возможно развитие осложнений, К ним относятся кровотечение, перфорация и пенетрация язвы, формирование рубцово-язвенного стеноза привратника, малигнизация язвы.
Язвенное кровотечение наблюдается у 15–20% больных ЯБ, чаще при локализации язв в желудке. Факторами риска его возникновения служат прием ацетилсалициловой кислоты и НПВП, инфекция H. pylori и размеры язв >1 см [6]. Язвенное кровотечение проявляется рвотой содержимым типа «кофейной гущи» (гематемезис) или черным дегтеобразным стулом (мелена). При массивном кровотечении и невысокой секреции соляной кислоты, а также локализации язвы в кардиальном отделе желудка в рвотных массах может отмечаться примесь неизмененной крови, Иногда на первое место в клинической картине язвенного кровотечения выступают общие жалобы (слабость, потеря сознания, снижение артериального давления, тахикардия), тогда как мелена может появиться лишь спустя несколько часов.
Перфорация (прободение) язвы встречается у 5–15% больных ЯБ, чаще у мужчин. К ее развитию предрасполагают физическое перенапряжение, прием алкоголя, переедание. Бывают случаи, когда перфорация возникает внезапно, на фоне бессимптомного («немого») течения ЯБ. Клинически перфорация язвы манифестируется острейшими («кинжальными») болями в подложечной области, развитием коллаптоидного состояния, При обследовании больного обнаруживаются «доскообразное» напряжение мышц передней брюшной стенки и резкая болезненность при пальпации живота, положительный симптом Щеткина–Блюмберга. В дальнейшем, иногда после периода мнимого улучшения, прогрессирует картина разлитого перитонита.
Под пенетрацией понимают проникновение язвы желудка или двенадцатиперстной кишки в окружающие ткани — поджелудочную железу, малый сальник, желчный пузырь и общий желчный проток. При этом возникают упорные боли, которые теряют прежнюю связь с приемом пищи, повышается температура тела, в анализах крови выявляется повышение СОЭ. Наличие пенетрации язвы подтверждается рентгенологически и эндоскопически.
Стеноз привратника формируется обычно после рубцевания язв, расположенных в пилорическом канале или начальной части двенадцатиперстной кишки. Нередко развитию данного осложнения способствует операция ушивания прободной язвы данной области. Наиболее характерными клиническими симптомами стеноза привратника являются рвота пищей, съеденной накануне, а также отрыжка с запахом «тухлых» яиц. При пальпации живота в подложечной области можно выявить «поздний шум плеска» (симптом Василенко), у худых больных становится иногда видимой перистальтика желудка. При декомпенсированном стенозе может прогрессировать истощение больных, присоединяются электролитные нарушения.
Малигнизация (озлокачествление) доброкачественной язвы желудка является не таким частым осложнением, как считалось раньше. За малигнизацию нередко ошибочно принимаются случаи своевременно не распознанного инфильтративно-язвенного рака. Диагностика не всегда оказывается простой. Клинически иногда удается отметить изменение характера течения ЯБ с утратой периодичности и сезонности обострений. В анализах крови обнаруживаются анемия, повышение СОЭ. Окончательное заключение ставится при гистологическом исследовании биоптатов, взятых из различных участков язвы.
5.7. Особенности течения ЯБ у отдельных групп больных
5.7.1. Особенности течения при беременности
Клиническая картина. Клинические проявления определяются локализацией язвы, общим состоянием женщины, возрастом, частотой обострений в прошлом, сопутствующим токсикозом. Нередки жалобы на чувство тяжести, переполнения в подложечной области, связанные с приемом пищи, ночные, «голодные» боли, уменьшающиеся после приема антацидов, на тошноту, рвоту, приносящую облегчение, изжогу, появление (усиление) запоров [12]. При пальпации отмечается болезненность в подложечной области и/или правом верхнем квадранте живота.
Диагностика. Диагноз устанавливается на основании клинических проявлений, анамнестических данных, результатов ЭГДС и ультразвукового исследования [13]. Рентгенологическое исследование желудка и двенадцатиперстной кишки беременным противопоказано.
В диагностически неясных случаях, при подозрении на развитие осложнений (кровотечение, стеноз антрального отдела желудка, рак) ЭГДС в силу своей безопасности для плода может быть выполнена при любом сроке беременности. Возможно ее проведение под глубокой седацией с использованием пропофола (категория В по классификации FDA) во втором и третьем триместрах беременности [14].
Ультразвуковое исследование желудка позволяет выявить наличие гиперсекреции, дуоденогастрального рефлюкса, утолщение стенки (за счет воспалительного инфильтрата) в области язвенного дефекта; осуществить дифференциальный диагноз с желчнокаменной болезнью, хроническим холециститом.
Для исключения оккультного кровотечения проводятся исследование кала на скрытую кровь, клинический анализ крови.
Дифференциальный диагноз. Разграничение обострений ЯБ затруднено, необходимо проводить дифференциальный диагноз с эрозивным гастродуоденитом, панкреатитом, заболеваниями желчевыводящих путей, острым аппендицитом и ранним токсикозом — рвотой. Стенозирующая язва антрального отдела желудка может симулировать чрезмерную рвоту. Для раннего токсикоза характерны мучительная, почти постоянная тошнота, усиливающаяся на различные запахи, слюнотечение. При этом рвота бывает независимо от еды, особенно по утрам, боль в животе, как правило, отсутствует. Кровотечение, обусловленное ЯБ, необходимо дифференцировать с эрозивным гастритом, синдромом Маллори–Вейсса, кровотечением из дыхательных путей, раком желудка.
Течение. Беременность оказывает благоприятное влияние на течение ЯБ: у 75–80% женщин отмечается ремиссия заболевания. Однако у некоторых больных может произойти обострение. Чаще это наблюдается в первом (14,8%), третьем (10,2%) триместрах беременности, за 2–4 недели до срока родов или в раннем послеродовом периоде. Нередким осложнением ЯБ является желудочно-кишечное кровотечение (3,4%), требующее проведения срочного эндоскопического исследования и активного лечения. Неосложненная ЯБ не оказывает отрицательного влияния на развитие плода.
Лечение. Лечение включает соблюдение общепринятых «режимных» мероприятий и диеты, прием в обычных терапевтических дозах невсасывающихся антацидов (фосфалюгеля по 1 пакетику 3 раза в день через 1 час после еды и адсорбентов в виде смекты по 1 пакетику также 3 раза в день спустя 1 час после еды). При отсутствии эффекта назначаются Н2-блокаторы (ранитидин 150/300 мг однократно на ночь), а в случае их недостаточной эффективности и при развитии осложнений допустимо применение ИПП утром до первого приема пищи (омепразола по 20–40 мг, лансопразола по 30–60 мг, пантопразола по 40 мг, категория В по классификации FDA) [15]. При выраженных болях, обусловленных двигательными нарушениями, возможно назначение спазмолитиков (дротаверина по 40 мг 3–4 раза в день, мебеверина по 200 мг 2 раза в день за 20 минут до еды) и прокинетиков (метоклопрамид по 5–10 мг 2–3 раза в сутки). Препараты висмута беременным противопоказаны. Эрадикационная терапия инфекции H. pylori у беременных не проводится.
5.7.2. Особенности течения у лиц пожилого и старческого возраста
В развитии гастродуоденальных язв у больных пожилого возраста, помимо инфекции H. pylori и кислотно-пептического фактора, могут также играть роль атеросклеротические изменения сосудов желудка, некоторые фоновые заболевания (например, хронические неспецифические заболевания легких), снижающие защитные свойства слизистой оболочки желудка, прием лекарственных средств (в первую очередь, НПВП), обладающих ульцерогенным действием.
Язвы у больных пожилого и старческого возраста локализуются преимущественно в желудке (по малой кривизне тела или в субкардиальном отделе), имеют иногда очень большие размеры, часто протекают со стертой и неопределенной клинической симптоматикой, отличаются наклонностью к развитию осложнений (прежде всего желудочно-кишечных кровотечений). При обнаружении у пожилых больных язвы в желудке важное значение имеет проведение дифференциального диагноза с инфильтративно-язвенной формой рака желудка.
Гастродуоденальные язвы у лиц пожилого и старческого возраста характеризуются медленным рубцеванием. В процессе медикаментозной терапии следует соблюдать осторожность, учитывая более высокий риск развития побочных эффектов у пожилых больных по сравнению с пациентами молодого и среднего возраста.
6. Лечение
Лечение ЯБ должно быть комплексным и включать не только лекарственные средства, но и широкий круг различных мероприятий: диетическое питание, прекращение курения и зло употребления алкоголем, отказ от приема препаратов, обладающих ульцерогенным действием, нормализацию режима труда и отдыха, санаторно-курортное лечение.
Больные с неосложненным течением ЯБ подлежат консервативной терапии. В большинстве случаев она проводится амбулаторно. Однако при выраженных болях, высоком риске развитии осложнений (например, большие и гигантские язвы), необходимости дообследования с целью верификации диагноза (в частности, при неясном характере язвенного поражения желудка), тяжелых сопутствующих заболеваниях целесообразна госпитализация пациентов.
6.1. Диета
Основные принципы диетического питания больных язвенной болезнью, выработанные много лет назад, сохраняют актуальность и в настоящее время. Остаются в силе рекомендации частого (5–6 раз в сутки), дробного питания, механического, термического и химического щажения слизистой оболочки желудка. В большинстве случаев показано назначение диеты № 1 по М. И. Певзнеру. Прежде рекомендовавшиеся диеты 1а и 1б, как физиологически неполноценные, сегодня практически не применяются.
Из пищевого рациона необходимо исключить продукты, раздражающие слизистую оболочку желудка и возбуждающие секрецию соляной кислоты: крепкие мясные и рыбные бульоны, жареную и наперченную пищу, копчености и консервы, приправы и специи (лук, чеснок, перец, горчицу), соления и маринады, газированные фруктовые воды, пиво, белое сухое вино, шампанское, кофе, цитрусовые.
Следует отдавать предпочтение продуктам, обладающим выраженными буферными свойствами (т. е. способностью связывать и нейтрализовать соляную кислоту). К ним относятся мясо и рыба (отварные или приготовленные на пару), яйца, молоко и молочные продукты). Разрешаются также макаронные изделия, черствый белый хлеб, сухой бисквит и сухое печенье, молочные и вегетарианские супы. Овощи (картофель, морковь, кабачки, цветная капуста) можно готовить тушеными или в виде пюре и паровых суфле. В пищевой рацион можно включать каши, кисели из сладких сортов ягод, муссы, желе, печеные яблоки, какао с молоком, некрепкий чай.
Нужно помнить и о таких простых, но в то же время важных рекомендациях, как необходимость принимать пищу в спокойной обстановке, не спеша, сидя, тщательно прожевывать пищу. Это способствует лучшему пропитыванию пищи слюной, буферные возможности которой являются достаточно выраженными.
6.2. Фармакотерапия
Многообразие различных патогенетических факторов ЯБ обусловило в свое время появление большого числа лекарственных препаратов, избирательно воздействовавших, как предполагалось первоначально, на те или иные патогенетические механизмы заболевания.
В 1990 г. D.W. Burget и соавт. [16] опубликовали данные мета-анализа 300 работ, на основании которого пришли к заключению, что язвы желудка и двенадцатиперстной кишки рубцуются почти во всех случаях, если удается поддерживать рН внутрижелудочного содержимого >3 около 18 часов в сутки. С учетом этого правила в качестве базисной противоязвенной терапии на данном этапе могут рассматриваться только антациды, Н2-блокаторы и ингибиторы протонной помпы.
Ниже дается оценка их эффективности с позиций медицины, основанной на доказательствах: уровень А (высокий) характеризуется хорошей доказательной базой и маловероятно, что дальнейшие исследования изменят существующее положение; уровню B (средний) присуща умеренная доказательная база, и дальнейшие исследования могут повлиять на убеждение в верности существующего положения; уровень С (низкий) характеризуется слабой доказательной базой, и дальнейшие исследования могут изменить мнение о существующем положении. Кроме того, используется цифровая шкала уровня исследований: уровень 1 — вывод основан на результатах рандомизированных контролируемых исследований, уровень 2 — вывод основан на результатах когортных исследований, а также исследований «случай–контроль», уровень 3 — мнение экспертов, основанное на собственных клинических наблюдениях.
В соответствии с опубликованными данными уровень доказательности эффективности антацидов составляет 3С, Н2-блокаторов — 1А, ИПП — 1А.
6.2.1. Антациды
Антациды способны поддерживать уровень внутрижелудочного рН >3 на протяжении 4–6 часов в течение суток, что определяет их недостаточно высокую эффективность при применении в качестве монотерапии [2]. Тем не менее, многие больные ЯБ охотно принимают антацидные препараты для купирования болей и диспепсических жалоб, учитывая быстроту их действия и доступность при безрецептурной продаже.
При систематическом применении антацидных препаратов следует помнить о возможных побочных эффектах. К ним относятся: феномен «рикошета» — вторичное (после первоначального антацидного эффекта) повышение секреции соляной кислоты, наблюдающееся, в частности, при приеме антацидов, содержащих карбонат кальция; «молочно-щелочной синдром» (при одновременном приеме карбоната кальция и употреблении большого количества молока); нарушение всасывания некоторых лекарственных препаратов (например, антибиотиков, Н2-блокаторов), если они применяются вместе с антацидами; повышение уровня алюминия и магния в крови у больных с нарушенной функцией почек, принимающих магний- и алюминийсодержащие антациды; нарушения стула (запор или диарея) и т.д.
6.2.2. Н2-блокаторы
В 80-х годах прошлого столетия Н2-блокаторы (циметидин, ранитидин, фамотидин, низатидин, роксатидин) были наиболее популярными противоязвенными препаратами. Они подавляют секрецию соляной кислоты за счет вытеснения гистамина из связи с Н2-рецепторами париетальных клеток. Эти препараты поддерживают показатели внутрижелудочного рН >3 в течение суток на протяжении 8–10 часов. Многочисленные исследования показали, что применение Н2-блокаторов в течение 4–6 недель приводит к рубцеванию язвенного дефекта у 70–80% больных с дуоденальными язвами и у 55–60% пациентов с язвами желудка [2]. После того как в клинической практике в качестве базисной антисекреторной терапии стали широко применяться ИПП, Н2-блокаторы утратили свои позиции и в настоящее время используются редко, главным образом при невозможности применения ИПП или же в комбинации с ними для усиления антисекреторного действия.
6.2.3. Ингибиторы протонной помпы
Лишь препараты этой группы могут поддержать требуемую продолжительность повышения рН в желудке, необходимую для заживления гастродуоденальных язв. Сегодня ИПП являются средством базисной терапии обострений ЯБ. Они назначаются с целью купирования болей и диспепсических расстройств, а также для достижения рубцевания язвенного дефекта в возможно более короткие сроки. Многочисленные рандомизированные сравнительные исследования (включая мета-аналитические) свидетельствовали о значительно более высокой эффективности ИПП по сравнению с Н2-блокаторами в устранении клинических симптомов и рубцевании язв [17].
Существует четкий протокол фармакотерапии ЯБ, который предусматривает назначение выбранного препарата в строго определенной дозе: омепразола — 20 мг, лансопразола — 30 мг, пантопразола — 40 мг, рабепразола — 20 мг, эзомепразола — 20 мг. Продолжительность лечения определяется результатами эндоскопического контроля, который проводится с интервалами 2–4 недели. Для оценки эффективности того или иного препарата используется подсчет не средних сроков рубцевания, как это было раньше, а частоты зарубцевавшихся язв за конкретный период времени (4, 6, 8 недель и т. д.).
При применении ИПП, метаболизирующихся системой цитохрома Р450, могут остро вставать вопросы конкурентного лекарственного взаимодействия с препаратами, метаболизм которых также осуществляется с помощью указанной системы. Среди всех ИПП самое низкое сродство к системе цитохрома Р450 проявляют пантопразол и рабепразол, основной метаболизм которых осуществляется без участия данной ферментной системы.
Следует подчеркнуть отсутствие принципиальных различий в подходах к лечению язв желудка и язв двенадцатиперстной кишки. Длительное время считалось, что язвы двенадцатиперстной кишки требуют назначения антисекреторных препаратов, а язвы желудка — препаратов, стимулирующих процессы регенерации. Сейчас уже считается общепризнанным, что после подтверждения доброкачественного характера язв желудка лечение этих больных проводится точно так же, как пациентов с дуоденальными язвами. Единственное различие может быть связано со сроками терапии, которые при язвах желудка — с учетом их более значительного размера и более медленного рубцевания — часто бывают более продолжительными.
6.2.4. Меры по устранению инфекции H. pylori
«Ахиллесовой пятой» консервативного лечения ЯБ является высокая частота рецидивов после прекращения курсового приема антисекреторных препаратов, которая составляет в среднем 70% в течение первого года после достижения рубцевания язвы. В настоящее время краеугольным камнем противорецидивного лечения признано проведение эрадикационной антигеликобактерной терапии.
Ликвидация инфекции H. pylori приводит прежде всего к снижению частоты последующих рецидивов ЯБ в течение года с 70 до 4–5%, и эта частота остается столь же низкой в последующие годы [18]. Кроме того, эрадикационная терапия у больных с язвенными кровотечениями (сразу после перевода на пероральный прием лекарственных препаратов) способствует значительному снижению риска возникновения ранних рецидивов таких кровотечений. После эрадикации H. pylori уменьшается также частота повторного возникновения язв после хирургического лечения.
Успешное проведение эрадикации в соответствии с утвержденным протоколом впервые сделало реальным обсуждение вопроса о принципиальной излечимости ЯБ.
Схемы эрадикационной терапии обязательно включают в себя — наряду с антибиотиками — ИПП. Целесообразность назначения последних обусловливается несколькими обстоятельствами. Установлено, что H. pylori выживают при значениях рН 4,0–6,0 и хорошо размножаются при рН 6,0–8,0 [18]. ИПП повышают показатели внутрижелудочного рН, и это приводит к тому, что размножающиеся в таких условиях бактерии становятся более чувствительными к действию антибиотиков. Кроме того, ИПП уменьшают объем желудочного сока, в результате чего повышается концентрация антибиотиков в желудочном содержимом, они увеличивают вязкость желудочного сока и замедляют эвакуацию содержимого из желудка, вследствие чего возрастает время контакта антибиотиков и микроорганизмов. Наконец, ИПП сами обладают антигеликобактерной активностью. Перечисленные свойства делают их обязательным компонентом различных схем эрадикации. В настоящее время при проведении эрадикационной терапии предпочтение отдается эзомепразолу и рабепразолу [10].
Согласно рекомендациям последнего согласительного совещания Европейской рабочей группы по изучению H. pylori и микробиоты «Маастрихт V/Флоренция» (2016), выбор той или иной схемы эрадикации зависит от частоты резистентности штаммов H. pylori в данном регионе к кларитромицину. Если она не превышает 15%, то в качестве схемы первой линии назначается стандартная тройная терапия [10].
Поскольку показатели устойчивости штаммов H. pylori к кларитромицину в России не превышают 10%, схемой первой линии является стандартная тройная схема эрадикационной терапии, включающая ИПП (в стандартной дозе 2 раза в сутки), кларитромицин (по 500 мг 2 раза в сутки), амоксициллин (по 1000 мг 2 раза в сутки). В настоящее время разработаны меры, которые позволяют повысить эффективность указанной терапии:
Назначение дважды в день повышенной дозы ИПП (удвоенной по сравнению со стандартной).
Увеличение продолжительности тройной терапии с ИПП и кларитромицином до 14 дней. Отмечено, что только такие сроки обеспечивают сопоставимую эффективность стандартной тройной терапии с эффективностью других схем.
Добавление к стандартной тройной терапии висмута трикалия дицитрата в дозе 240 мг 2 раза в сутки.
Присоединение к стандартной тройной терапии пробиотика Saccharomyces boulardii (по 250 мг 2 раза в сутки).
Подробное инструктирование пациента и контроль за точным соблюдением назначенного режима приема лекарственных средств.
Как вариант эрадикационной терапии первой линии (например, при непереносимости препаратов группы пенициллина) может быть назначена классическая четырехкомпонентная схема на основе висмута трикалия дицитрата (120 мг 4 раза в сутки) в комбинации с ИПП (в стандартной дозе 2 раза в сутки), тетрациклином (500 мг 4 раза в сутки), метронидазолом (по 500 мг 3 раза в сутки). Продолжительность квадротерапии с препаратами висмута должна составлять 14 дней, при условии если в данном регионе не доказана высокая эффективность 10-дневного курса [10].
Квадротерапия с висмута трикалия дицитратом применяется также как основная схема второй линии при неэффективности стандартной тройной терапии. Другой схемой второй линии служит схема эрадикации, включающая ИПП (в стандартной дозе 2 раза в сутки), левофлоксацин (по 500 мг 2 раза в сутки) и амоксициллин (по 1000 мг 2 раза в сутки). Тройная терапия с левофлоксацином может быть назначена только гастроэнтерологом по взвешенным показаниям.
Как альтернативные варианты терапии первой линии предложены также последовательная терапия и квадротерапия без препаратов висмута. При последовательной терапии больной получает первые 5 дней ИПП (в стандартной дозе 2 раза в сутки) в комбинации с амоксициллином (по 1000 мг 2 раза в сутки), а в последующие 5 дней ИПП (в стандартной дозе 2 раза в сутки) в комбинации с кларитромицином (по 500 мг 2 раза в сутки) и метронидазолом (500 мг 2 раза в сутки). В состав квадротерапии без препаратов висмута входят ИПП (в стандартной дозе 2 раза в сутки), амоксициллин (1000 мг 2 раза в сутки), кларитромицин (по 500 мг 2 раза в сутки) и метронидазол (по 500 мг 2 раза в сутки). Оба альтернативных варианта применяются и в случаях устойчивости штаммов H. pylori к кларитромицину, однако подтверждение эффективности этих схем в России нуждается в проведении собственных исследований. В последние годы обращено внимание на низкую эффективность последовательной терапии и квадротерапии без препаратов висмута в регионах с высокой частотой устойчивости H. pylori к метронидазолу, к которым в том числе относится и Россия.
Терапия третьей линии основывается на определении индивидуальной чувствительности H. pylori к антибиотикам [19].
6.2.5. Ребамипид
Новым препаратом, предложенным для лечения больных ЯБ, служит ребамипид, представляющий собой производное хинолинов и являющийся одновременно как гастропротектором, так и энтеропротектором.
В основе механизмов действия препарата лежит индукция синтеза эндогенных простагландинов E2 и GI2 в слизистой оболочке ЖКТ, что приводит к активации ее физиологической защиты. В результате улучшается кровоток в стенках ЖКТ и усиливается пролиферация эпителиальных клеток (цитопротективный эффект), происходит подавление повышенной проницаемости слизистой оболочки, выведение свободных радикалов, повышается секреция гликопротеинов желудочной слизи и реализуется противовоспалительное действие. Применение ребамипида при ЯБ позволяет ускорить сроки заживления язв и улучшить качество образующегося рубца.
Добавление ребамипида к схемам эрадикации повышает их эффективность, в частности, существенно увеличивается частота устранения H. pylori; за счет снижения адгезии бактерий к слизистой оболочке желудка уменьшается риск ее повторной колонизации, а следовательно, снижается вероятность развития рецидивов [20, 21].
При ЯБ ребамипид следует применять в дозе 100 мг 3 раза в день в течение 2–4 недель, при необходимости продолжительность приема может быть увеличена до 8 недель. Защитные свойства препарата позволяют рекомендовать его не только для курса эрадикационной терапии, но и для последующего продолжения лечения пациентов.
Отличительной особенностью ребамипида служит его способность оказывать протективное действие в отношении слизистой оболочки как желудка, так и тонкой, и толстой кишки, и предупреждать развитие ее поражений при приеме НПВП.
Неэффективность консервативного лечения ЯБ проявляется в двух вариантах: часто рецидивирующим течением заболевания (с числом рецидивов более 2 раз в год) и формированием трудно рубцующихся язв, не заживающих в течение 12 недель непрерывного лечения. Факторами, способствующими частым рецидивам и замедленному заживлению язв, являются: персистирование инфекции H. pylori, прием НПВП, наличие скрыто протекающего синдрома Золлингера–Эллисона и низкая приверженность больных к лечению (курение, злоупотребление алкоголем, неправильный прием лекарственных препаратов) [18].
К наиболее типичным ошибкам при проведении эрадикационной терапии относится прежде всего отсутствие тестирования на наличие H. pylori, в результате чего такие пациенты получали только антисекреторную терапию. Другой частой ошибкой служит неправильное признание язвенной болезни H. pylori-негативной. Как показали собственные наблюдения, частота указанных язв зависит от того, сколько различных способов диагностики инфекции было применено у больного. Так, если пациенту проводится только эндоскопический уреазный тест (на практике диагностика инфекции H. pylori у больных ЯБ часто ограничивается лишь этим методом), то частота H. pylori-негативных язв составляет 37,5%. Если у одного больного применяются параллельно два метода (например, быстрый уреазный тест + гистологическое исследование), частота H. pylori-негативных язв уменьшается до 12,4%, а если добавляется еще и третий метод (полимеразная цепная реакция для выявления инфекции в кале), то этот показатель снижается до 4,2%. Поэтому признанию язвенной болезни H. pylori-негативной должно предшествовать проведение, как минимум, двух (а еще лучше трех) различных методов диагностики H. pylori [22].
К распространенным ошибкам относится и использование в разработанных схемах лекарственных препаратов, не входящих в утвержденные варианты (например, Н2-блокаторов вместо ИПП, метронидазола в тройных схемах эрадикации и др.) или их применение в недостаточных дозах. К снижению эффективности эрадикационной терапии приводит и назначение ее 7–10-дневных курсов в тех случаях, когда следовало бы использовать 14-дневные (например, при проведении повторных курсов эрадикации).
Одной из наиболее частых ошибок является отказ (по разным причинам) от проведения контроля эрадикации в установленные сроки. Поэтому когда спустя какое-то время у больного ЯБ вновь возникает рецидив заболевания и вновь выявляется инфекция H. pylori, это расценивается как результат повторного инфицирования H. pylori, хотя на самом деле речь в таких ситуациях чаще всего идет о неэффективной предшествующей эрадикации.
Таким образом, прежде чем вынести заключение о неэффективности консервативного лечения ЯБ у того или иного пациента, необходимо убедиться, что это лечение (в частности, обследование на наличие инфекции H. pylori и ее эрадикация) было проведено в строгом соответствии с протоколом.
Что касается показаний к хирургическому вмешательству при ЯБ, то к ним в настоящее время относятся только осложненные формы заболевания (перфорация язвы, декомпенсированный рубцово-язвенный стеноз привратника, профузные желудочно-кишечные кровотечения, которые не удается остановить консервативными методами, в том числе с применением эндоскопического гемостаза). При соблюдении необходимого протокола консервативного лечения случаи его неэффективности (как рекомендация на проведение операции) могут быть сведены до минимума.
6.3. Лечение язвенных кровотечений
Обнаружение при эндоскопии признаков активного язвенного кровотечения (струйного или с медленным выделением крови) служит показанием к применению эндоскопических методов его остановки, которые в таких случаях эффективно уменьшают риск повторных кровотечений, снижают показатели летальности и число экстренных хирургических вмешательств.
Чаще всего используют различные термоактивные способы эндоскопической остановки кровотечения. К указанным методам относятся лазеротерапия, мультиполярная электрокоагуляция, термокоагуляция. С гемостатической целью применяют также инъекционное введение в область язвы различных склерозирующих и сосудосуживающих препаратов (растворов адреналина, полидоканола, этанола и др.). Методом выбора считаются электрокоагуляция, термокоагуляция, инъекционная склеротерапия, а также комбинированное применение термокоагуляции и инъекционной терапии.
Остановке язвенных кровотечений и снижению риска их повторного возникновения способствует применение ИПП. При этом одномоментно болюсно внутривенно вводится 80 мг эзомепразола с последующей непрерывной внутривенной инфузией этого препарата (по 8 мг в час) в течение 72 ч [23]. После перевода больного на пероральный прием препаратов осуществляется эрадикационная терапия.
7. Реабилитация
Важное место в реабилитации больных ЯБ занимает санаторно-курортное лечение. Оно проводится не ранее чем через 2–3 месяца после стихания обострения в санаториях Дорохово, Ессентуки, Железноводск и др. и включает в себя грязе- и торфолечение, хвойно-морские ванны, питье щелочных минеральных вод.
8. Профилактика и диспансерное наблюдение
Профилактика ЯБ предполагает устранение факторов, способствующих язвообразованию: борьбу с вредными привычками (курением и злоупотреблением алкоголем), нормализацию режима труда и отдыха, а также характера питания, проведение эрадикации инфекции H. pylori у больных с хроническим гастритом и функциональной диспепсией, одновременное назначение ИПП при необходимости приема НПВП и антикоагулянтов (особенно лицам пожилого возраста, пациентам с ЯБ в анамнезе, больным с сопутствующими заболеваниями сердечно-сосудистой системы и циррозом печени).
9. Критерии оценки качества медицинской помощи
| Используемые методы | Уровень достоверности доказательств | Уровень убедительности рекомендаций | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| МКБ-10 | |
| Код | Название |
| К 29.3 | Хронический поверхностный гастрит |
| К 29.4 | Хронический атрофический гастрит |
| К 29.9 | Хронический аутоиммунный гастрит |
Дата разработки протокола: 2017год.
Сокращения, используемые в протоколе:
| в/в | внутривенно |
| в/м | внутримышечно |
| п/к | подкожно |
| р/день | раз в день |
| АИГ | аутоиммунный гастрит |
| АЛТ | аланинаминотрансфераза |
| АСК | ацетил салициловая кислота |
| АСТ | аспртатаминотрансфераза |
| АТ | антитела |
| АПК | антитела к париетальным клеткам |
| БХА | биохимический анализ |
| БУТ | быстрый уреазный тест |
| ГДЗ | гастродуоденальная зона |
| ГЭР | гастроэзофагеальный рефлюкс |
| ДГР | дуоденогастральный рефлюкс |
| ДПК | двенадцатиперстная кишка |
| ЖКК | желудочно-кишечные кровотечения |
| ЖКТ | желудочно-кишечный тракт |
| ИПП | ингибиторы протонной помпы |
| КМ | кишечная метаплазия |
| ОАК | общий анализ крови |
| ОБП | органы брюшной полости |
| ОАМ | общий анализ мочи |
| ПГ | пепсиноген |
| РЖ | рак желудка |
| СО ГДЗ | слизистая оболочка гастродуоденальной зоны |
| СО ДПК | слизистая оболочка двенадцатиперстной кишки |
| СОЖ | слизистая оболочка желудка |
| СОЭ | скорость оседания эритроцитов |
| УЗИ | ультразвуковое исследование |
| УД | уровень доказательности |
| ФД | функциональная диспепсия |
| ФЭГДС | фиброэзофагогастродуоденоскопия |
| ЦНС | центральная нервная система |
| ЯБДПК | язвенная болезнь двенадцатиперстной кишки |
| ЯБЖ | язвенная болезнь желудка |
| H.pylori | Helicobacter pylori |
Пользователи протокола: ВОП,терапевты,гастроэнтерологи.
Категория пациентов: взрослые.
Шкала уровня доказательности:
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки результаты которых могут быть распространены на соответствующую популяцию |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с невысоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию |
| С | Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+), результаты которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию |
| D | Описание серии случаев или неконтролируемое исследование или мнение экспертов |
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
13-15 октября, Алматы, «Атакент»
600 брендов, более 150 компаний-участников из 20 стран.
Новинки рынка стоматологии. Цены от производителей
Классификация
Классификации
Общепринятой клинической классификацией является Хьюстенская модификация гастритов, 1996 г (Таблица 1) [4].
Таблица 1. Сиднейская система классификации хронических гастритов
| Тип гастрита | Этиологические факторы | Синонимы (прежние классификации) |
| Неатрофический | Helicobacterpylori Другие факторы | Поверхностный Хронический антральный Гастрит типа В Гиперсекреторный гастрит |
| Атрофический аутоиммунный | Иммунные механизмы | Гастрит типа А Диффузный гастрит тела желудка, ассоциированный с В12-дефицитной анемией и с пониженной секрецией |
| Атрофический мультифокальный | Helicobacter pylori Нарушения питания Факторы среды | Смешанный гастрит типа А и В |
| Особые формы | ||
| Химический | Химические раздражители: Желчь (ДГР) Приём НПВП | Реактивный гастрит типа С |
Реактивный рефлюкс-гастрит
Иммунные механизмы
Глютен
Саркоидоз
ГранулематозВегенера
Инородные тела
Идиопатический
Другие аллергены
инфекционные
Грибы, Паразиты
гипертрофический
Таблица 2. Классификация атрофического гастрита (OLGA 2007 г.)
| Антрум | Тело | |||
| 0 | I | II | III | |
| 0 | Степень 0 | Степень I | Степень II | Степень II |
| I | Степень I | Степень II | Степень II | Степень III |
| II | Степень II | Степень II | Степень III | Степень IV |
| III | Степень II | Степень III | Степень IV | Степень IV |
| Антрум | Тело | |||
| 0 | I | II | III | |
| 0 | Стадия 0 | СтадияI | СтадияII | СтадияII |
| I | СтадияI | СтадияII | СтадияII | СтадияIII |
| II | СтадияII | СтадияII | СтадияIII | СтадияIV |
| III | СтадияII | СтадияIII | СтадияIV | СтадияIV |
В каждом столбце атрофия показана по четырехуровневой шкале (0-3) в соответствии с визуальной аналоговой шкалой модифицированной Сиднейской системы классификации гастрита [15]. Под степенью гастрита подразумевается выраженность суммарной воспалительной инфильтрации (нейтрофильными лейкоцитами и мононуклеарными клетками), под стадией – выраженность атрофии.
Диагностика
МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
Диагностические критерии:
Перечень дополнительных диагностических мероприятий:
· ОАК – по показаниям;
· определение сывороточного железа в крови – при анемии;
· анализ кала на скрытую кровь – при анемии;
· УЗИ печени, желчных путей и поджелудочной железы – по показаниям(при хроническом аутоиммунном атрофическом гастритеи/или при сопутствующей патологии гапатобилиарнойсистемы);
· биохимические анализы крови: общий билирубин и его фракций, общий белок, альбумин, холестерин, АЛТ,АСТ, глюкозы, амилазы – (при хроническом аутоиммунном атрофическом гастрите и/илипри сопутствующей патологии гапатобилиарнойсистемы);
· Определение антител к париетальным клеткам–при хроническом аутоиммунном атрофическом гастрите;
· Определение в крови уровня гастрина-17 и пепсиногенаI(ПГ I) и пепсиногенаII(ПГ II)– при мультифокальном атрофическом гастрите;
· интрагастральная рН-метрия – при тяжелой степени атрофического гастрита;
· рентгенологическое исследование верхних отделов ЖКТ с барием – по показаниям (при пилоростенозе, наличии противопоказаний к эндоскопическим исследованиям и отказе пациента от ФЭГДС).
Показания для консультации специалистов:
Дифференциальный диагноз
| Нозологии | Характеристика симптомов | План обследования | Клинические критерии | Лабораторно-инструментальные признаки |
| Хронический поверхностный (антральный) H.pylori ассоциированный гастрит |
| Нозологии | Характеристика симптомов | Диагностические исследования | Клинические критерии | Лабораторно-инструментальные признаки |
| Хронический мультифокальный атрофический гастрит |
гистологические признаки кишечной метаплазии СОЖ
Лечение
ТАКТИКА ЛЕЧЕНИЯ НА АМБУЛАТОРНОМ УРОВНЕ
Цель лечения:
· достижение полной ремиссии заболевания
· предупреждение дальнейшего прогрессирования атрофии и развития осложнений
Основные задачи лечения:
· снижение активности кислотно-пептического фактора;
· нормализация секреторно-моторной функции желудка;
· повышение защитных свойств СОЖ и слизистой оболочки ДПК;
· эрадикацияH.рylori.
Немедикаментозное лечение и общие мероприятия включают:
Диета:
· питание полноценное и разнообразное;
· режим питания дробный, до 6 раз в сутки, малыми порциями;
· ограничение механических и химических раздражителей ЖКТ, стимуляторов желудочной секреции, веществ, длительно задерживающихся в желудке;
· исключение очень горячих и очень холодных блюд;
Медикаментозное лечение.
Учитывая различные этиопатогенетические факторы развития хронического гастрита медикаментозная терапия различается при различных формах хронического гастрита.
Принципы фармакотерапии неатрофического гастрита:
· эрадикационная антихеликобактерная терапия у НР–положительных больных;
· обязательный контроль эффективности антихеликобактериной терапии через 4–6 недель;
· влияние на факторы риска (замена НПВП парацетамолом, селективными ингибиторами ЦОГ–2, сочетание НПВП с мизопростолом, обеспечение комплаентности больных и др.).
Принципы фармакотерапии атрофического гастрита:
· эрадикационная антихеликобактерная терапия у НР–положительных больных;
· обязательный контроль эффективности антихеликобактерной терапии через 4–6 недель;
· применение витамина В12 с целью профилактики и лечения пернициозной анемии.
Ингибиторы протонной помпы –ИПП являются самыми мощными антисекреторными препаратами Они назначаются с целью купирования болевого синдрома и диспепсических расстройств, а также для достижения быстрой ремиссии [1, 2].
Блокаторы Н2гистаминовых рецепторов являются препаратами 2-й линии, которые могут применяться в случаях непереносимости или противопоказаниях ИПП. Также блокаторы Н2гистаминовых рецепторов могут использоваться в качестве дополнительной терапии совместно с ИПП.
Антацидыспособны поддерживать уровень внутрижелудочного рН> 3 на протяжении 4-6 часов в течение суток, что определяет их недостаточно высокую эффективность при применении в качестве монотерапии. Тем не менее, больные сХГ принимают антациды для купирования болей и диспепсических жалоб, что во многом объясняется быстротой их действия и безрецептурным отпуском [2].
Противомикробные препараты применяются при ХГ, ассоциированной с H. Pylori. С эрадикационной целью в комбинации с ИПП используются аминопенициллины (амоксициллин), макролиды (клатримицин) в качестве препаратов линии и препараты резерва при неэффективности стандартного лечения: фторхинолоны (левофлоксацин),нитроимидазолы (метронидазол), тетрациклины и препараты висмута.
Медикаментозная терапия ХГ, ассоциированного с H. Pylori
Успешность эрадикации H.Pylori, обуславливает безрецидивное течение, что является положительным прогностическим признаком в лечении ХГ.
Рекомендуемые схемы эрадикации(Маастрихт-V, 2015)
Терапия первой линия(10-14 дней):
· 3-х компонентная схема: ИПП +амоксициллин +кларитромицин;
· квадротерапия без висмута: ИПП+амоксициллин+кларитромицин +нитроимидазол.
Терапия второй линии(10-14 дней):
· 3-х компонентная схема: ИПП+амоксициллин+фторхинолон
· квадротерапия без висмута: ИПП+амоксициллин+кларитромицин +нитроимидазол[8,9,10], (УД А);
· квадротерапия с висмутом: ИПП+амоксициллин+кларитромицин +висмута трикалиядицитрат.
Эффективность лечения повышается при назначении дважды в день повышенной дозы ИПП (удвоенной стандартной) [11,12], (УД B).
При 14-дневной терапии увеличение частоты эрадикации более значительно, чем при 10-дневной [11,12,13],(УД С).
Эрадикационная терапия H. pylori может приводить к развитию антибиотико-ассоциированной диареи [14],(УД С). Добавление к стандартной тройной терапии пробиотика Saccharomycesboulardii повышает скорость эрадикации H.pylori [11,12, 13](УД D).
Перечень основных медикаментов, применяемых при ХГ
| № | МНН | Форма выпуска | Режим дозирования | УД |
| Ингибиторы протонной помпы | ||||
| 1 | Омепрозол | Капсулы (в т.ч. кишечнорастворимые, с пролонгированным высвобождением, гастрокапсулы) 10 мг, 20 мг и 40 мг | Перорально 20 мг 2 раза в сутки | А |
| 2 | Лансопразол | Капсулы (в т.ч. с модифицированным высвобождением) 15 мг и 30 мг | Перорально 15 мг 2 раза в сутки | А |
| 3 | Пантопразол | Таблетки, покрытые оболочкой (в т.ч. кишечнорастворимой); с отложенным высвобождением 20мг и 40 мг | Перорально 20 мг 2 раза в сутки. | А |
| 4 | Рабепразол | Таблетки / капсулы, покрытые кишечнорастворимой оболочкой 10 мг и 20 мг | Перорально 10 мг 2 раза в сутки. | А |
| 5 | Эзомепразол | Таблетки / Капсулы (в т.ч. кишечнорастворимые, твердые и пр.) 20 мг и 40 мг | Перорально 20 мг 2 раза в сутки. | А |
| Блокаторы Н2гистаминовых рецепторов | ||||
| 6 | Фамотидин | Таблетки, покрытые оболочкой (в т.ч. пленочной) 20 мг и 40 мг | ||
П/к, при анемиях, связанных с дефицитом витамина В12, вводят по 0,1 – 0,2 мг 1 раз в 2 дня
Тройная терапия на основе кларитромицина: 500 мг перорально два раза в сутки
NB! * показание не зарегистрировано
Перечень дополнительных медикаментов, применяемых при ХГ
| № | МНН | Форма выпуска | Режим дозирования | УД |
| 2 | Магния гидроксид и алюминия гидроксид | Таблетки, в т.ч. жевательные Суспензия для приема внутрь | Разовая доза по требованию | А |
| 3 | Кальция карбонат + натрия гидрокарбонат + натрия альгинат | Таблетки жевательные Суспензия для приема внутрь | Разовая доза по требованию | А |
Хирургическое вмешательство: нет.
Профилактические мероприятия:
Хронический гастрит (код по МКБ 10 – К29): признаки и терапия
На сегодняшний день хронический гастрит (код по МКБ 10 – К29) является одним из самых распространенных заболеваний со стороны желудочно-кишечного тракта. Суть данной патологии заключается в длительно протекающем, рецидивирующем воспалении слизистой оболочки желудка под воздействием инфекционных, термических, химических и других факторов. Как показывает статистика, более чем в 80% случаев такая болезнь ассоциирована с хеликобактерной инфекцией. В этой статье мы рассмотрим основные симптомы и принципы лечения хронического гастрита.
Основные симптомы хронического гастрита

Прежде чем говорить о симптомах, необходимо разобраться в классификации данного заболевания. Хронический гастрит может протекать с:
На основании гистологической картины такая патология бывает:
В зависимости от того, в какой форме протекает хронический гастрит, сопутствующая клиническая картина может несколько отличаться.
Данное заболевание, как мы уже сказали, имеет рецидивирующее течение. Вне обострения больного человека, как правило, ничего не беспокоит. В период обострения гастрита будет наблюдаться симптоматика, о которой мы поговорим ниже.
Наиболее типичными признаками хронического гастрита являются тяжесть и ноющая болезненность в области эпигастрия. Чувство дискомфорта усиливается через несколько минут после еды, дополняется тошнотой и рвотой. Примечательно то, что после рвоты пациент отмечает некоторое улучшение своего состояния.
Клиническая картина дополняется значительным снижением аппетита. При атрофии слизистого слоя присоединяются симптомы, указывающие на авитаминоз, анемию вследствие нарушения всасывания необходимых веществ.
Гастрит с повышенной кислотностью также протекает с тяжестью и болями в эпигастральной области. При этом болевой синдром появляется не только после приема пищи, но и на голодный желудок, что обусловлено агрессивным действием соляной кислоты. Кроме этого, характерны изжога, кислая отрыжка, тошнота и рвота, приносящая облегчение, проблемы с работой других отделов желудочно-кишечного тракта, например, в виде диареи или запора.
Терапия при хроническом гастрите
Первоочередным моментом в лечении хронического гастрита является специальная диета (стол №1 при повышенной кислотности, стол №2 при пониженной кислотности).
Из лекарственных препаратов могут назначаться:
Стоит заметить, что любые лекарственные средства могут применяться только после предварительной консультации с врачом.
В 2017 году ученые из Российского университета дружбы народов опубликовали работу, по результатам которой было установлено, что лечение хронического гастрита должно быть комплексным и включать препараты для уменьшения повреждения (ингибиторы протонной помпы), заживления слизистой и гастропротекции (ребамипид), препараты, улучшающие моторику (итоприд).
Кроме этого, хорошо зарекомендовали себя различные физиотерапевтичекие методы, например, КВЧ-терапия.
Дуоденит (K29.8)
Версия: Справочник заболеваний MedElement
Общая информация
Краткое описание
Первичный хронический дуоденит рассматривается как самостоятельное заболевание.
Вторичный хронический дуоденит представляет собой заболевание, сопутствующее или осложняющее различные другие заболевания, прежде всего, заболевания органов пищеварения.
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
13-15 октября, Алматы, «Атакент»
600 брендов, более 150 компаний-участников из 20 стран.
Новинки рынка стоматологии. Цены от производителей
Классификация
Общепризнанная классификация дуоденита отсутствует. Ниже приводятся несколько вариантов классификации.
Формы дуоденита:
— поверхностный (умеренно выраженный);
— выраженный;
— резко выраженный;
— атрофический дуоденит;
— отдельно рассматривают фолликулярный дуоденит.
По морфологии и течению:
— острый дуоденит;
— хронический дуоденит.
Острый дуоденит:
— катаральный острый дуоденит;
— эрозивно-язвенный острый дуоденит;
— флегмонозный острый дуоденит.
Хронический дуоденит. Общепринятая классификация хронического дуоденита отсутствует. С учетом особенностей развития и преимущественной локализации процесса выделяют 4 варианта:
— хронический дуоденит, преимущественно бульбит, ацидопептического генеза;
— хронический дуоденит, сочетающийся с атрофическим гастритом или энтеритом;
— хронический дуоденит, развившийся на фоне дуоденостаза;
— локальный дуоденит (папиллит, околососочковый дивертикулит).
По эндоскопической картине хронического дуоденита различают:
— поверхностный хронический дуоденит;
— атрофический хронический дуоденит;
— интерстициальный хронический дуоденит;
— эрозивно-язвенный хронический дуоденит.
Этиология и патогенез
Причины возникновения острого дуоденита:
— нарушения пищевого режима (прием недоброкачественной пищи, употребление продуктов, вызывающих раздражение слизистой оболочки ДПК, злоупотребление алкоголем);
— воздействие на организм пищевых токсикоинфекций;
— отравления токсическими веществами;
— повреждения слизистой оболочки ДПК инородными телами.
Эпидемиология
Признак распространенности: Редко
Соотношение полов(м/ж): 3.5
Факторы и группы риска
Клиническая картина
Клинические критерии диагностики
Cимптомы, течение
При объективном исследовании больных выявляют обложенность языка, умеренную локальную болезненность в пилородуоденальной зоне и эпигастральной области, где в период обострения может присутствовать небольшое напряжение мышц передней брюшной стенки.
Диагностика
Только инструментальные методы исследования обеспечивают достоверную диагностику хронического дуоденита.
Критерии эндоскопической диагностики форм дуоденита
Атрофический дуоденит. Наряду с отеком и гиперемией отмечают более или менее широкие участки истонченной, бледной слизистой. Оболочка с просвечивающей сеткой многочисленных мелких веточек сосудов. Слизистая оболочка чаще чистая, без скоплений слизи.
Фолликулярный дуоденит. На фоне бледно-розовой слизистой оболочки присутствуют чаще многочисленные, реже одиночные, мелкие бледные выбухания округлой формы (0,2-0,3 см) на широком основании беловатого цвета. Множественные выбухания могут располагаться кучно, а могут и на расстоянии. Обычно локализованы в луковице. Часто бывают при паразитарной инвазии: лямблии, гельминты.
Папиллиты:
— умеренно выраженный;
— выраженный.
Встречаются 2 варианта нормы большого дуоденального сосочка (БДС):
— БДС не отличается по цвету от окружающей слизистой;
— часть БДС покрыта протоковым эпителием белесоватого, блестящего, «лучистого» вида.
При умеренно выраженном папиллите слизистая в области соска отечна, сосок бледный, отсутствует блеск и возможны очажки гиперемии. Ворсины могут иметь белесоватый оттенок.
При выраженном папиллите наблюдаются резкая гипeремия, отек, лучистый рисунок исчезает. Поверхность бугристая и неровная. Размеры соска могут увеличиваться до 1,5-2,0 см.
Морфологическая картина
В зависимости от характера морфологических изменений выделяют дуоденит поверхностный, диффузный, атрофический и эрозивный.
При диффузном хроническом дуодените более значительно выраженыизменения, описанные для поверхностного дуоденита.
При поверхностном и диффузном дуодените наблюдаются гиперплазия и гиперсекреция поверхностного эпителия, увеличение количества бокаловидных клеток, усиление их секреторной функции. Указанные изменения следует рассматривать как компенсаторно-адаптационные в ответ на воздействие агрессивных факторов, повреждающих слизистую оболочку ДПК.
Для атрофического хронического дуоденита характерна атрофированная и истонченная слизистая оболочка, ворсинки которой уплощены.
При эрозивном дуодените на слизистой оболочке ДПК появляются единичные или множественные эрозии.
Фолликулярный бульбит встречается относительно редко. На фоне бледно-розовой слизистой оболочки луковицы видны чаще многочисленные, реже одиночные, бледные мелкие выбухания беловатого цвета с диаметром 0,2-0,3 см. Указанные изменения слизистой оболочки обычно ограничиваются луковицей ДПК, на остальных участках слизистая оболочка такая же, как при умеренном поверхностном или атрофическом дуодените.
2. Рентгеноскопия желудка и ДПК
3. pН-метрия не является диагностическим критерием, но позволяет уточнить уровень желудочной секреции, который может быть самым различным.
4. Слепое дуоденальное зондирование не информативно (признаки холецистита, панкреатита).
5. Антродуоденальная манометрия.
Лабораторная диагностика
Дифференциальный диагноз
1. Язвенная болезнь желудка и ДПК или гастрит.
Ацидопептический дуоденит, как правило, сочетается с антральным гастритом типа В. Они объединяются в понятие пилородуоденит, поскольку по существу являются единым заболеванием.
Пилородуоденит в основном сопутствует язвенной болезни пилородуоденальной локализации. В случае отсутствия данных о язвенной болезни, пилородуоденит рассматривается как предъязвенное заболевание.
Дуоденит, развившийся на фоне хронической дуоденальной непроходимости, часто сочетается с рефлюкс-гастритом.
Хронический дуоденит может представлять собой часть патологии тонкой кишки (энтерита) и в этих случаях не выделяется.
2. Панкреатит, холецистит, спазм сфинктера Одди.
При сочетании локального дуоденита с заболеваниями панкреатобилиарной системы необходимо выяснить причинно-следственные связи. В качестве причины поражения печени, желчных путей и поджелудочной железы могут рассматриваться только выраженный папиллит или крупный парафатеральный дивертикул.
3. Грыжа пищеводного отверстия диафрагмы.
4. Рак большого дуоденального сосочка.
Дифференциальная диагностика папиллита с раком большого дуоденального сосочка является наиболее сложной и ответственной.
Для эндоскопической картины рака в далеко зашедших стадиях, как правило, характерна бугристая опухоль багрово-красного или малинового цвета, которая занимает часть или весь сосочек. Нередко опухоль изъязвляется. На ранних стадиях рака часто возникают трудности в интерпретации полученных данных. При малейшем подозрении на злокачественную опухоль большого дуоденального сосочка необходимо проводить прицельную биопсию через эндоскоп с последующим гистологическим исследованием биоптатов. При наличии сомнений следует провести повторное исследование и установить динамическое наблюдение за больным.
Осложнения
— кровотечения (составляют около 10% всех кровотечений из верхнего отдела желудочно-кишечного тракта);
— рак большого дуоденального сосочка.
Лечение
При вторичных дуоденитах необходимо лечение основного заболевания.
При положительных тестах на хеликобактерную инфекцию, в первую очередь, проводят эрадикацию возбудителя.
В период обострения хронического дуоденита лечение проводят в стационаре. Назначения:
— диета № 1;
— антацидные (при сохраненной кислотности желудочного сока), вяжущие, спазмолитические, ганглиоблокирующие и холинолитические средства (не достаточно доказательств эффективности);
— витамины (А, В6, В12) при их дефиците;
— частичное парентеральное питание при гипопротеинемии.
Больным хроническим дуоденитом показано диспансерное наблюдение, проведение противорецидивного лечения и регулярная биопсия при признаках атрофии и дисплазии.
Возможно применение антидепрессантов в связи с изменениями характера пациента, обусловленными как метаболическими нарушениями, так и хроническим диспептическим синдромом.
Показания к хирургическому лечению хронической дуоденальной непроходимости:
— упорные болевой и диспепсический синдромы, сочетающиеся со стойким похуданием;
— выраженный дуоденогастральный рефлюкс;
— вовлечение в патологический процесс органов, сопряженных с ДПК.
Оперативное лечение проводится, как правило, при хронической дуоденальной непроходимости механического происхождения.
Что такое простой герпес? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 14 лет.
Определение болезни. Причины заболевания
Простой герпес — это высококонтагиозное острое и хроническое инфекционное заболевание, при котором поражается кожа и слизистые оболочки. Его провоцируют вирусы простого герпеса I и II типов, вызывая типичную пузырьковую сыпь и изъязвления, как правило, локализованного характера. У людей с выраженным иммунодефицитом эти вирусы могут вызывать тяжёлые генерализованные формы болезни.
Заболевание входит в TORCH-комплекс, так как влияет на развитие плода: при первичном заражении или реактивации (реже) у беременных оно вызывает врождённую инфекцию.
Этиология
Семейство — Herpesviridae (от греч. herpes — ползучий)
Подсемейство — α-герпесвирусы (Alphaherpesvirinae)
Виды — вирус простого герпеса I, II (Herpes simplex virus I, II)
ДНК-содержащие вирусы. В их составе есть нуклеоид — вирусный геном-ДНК, который окружён капсидом сложного строения, покрытым оболочкой белково-липидного характера. Также вирусы содержат гликопротеиды gG1 и gG2, что позволяет провести серотипическое деление вируса герпеса на I и II тип.
Обладают специфической способностью прикрепляться к покровным тканям человека. Это сопровождается постоянной или периодической персистенцией — способностью к размножению в инфицированных клетках без проявлений патологического действия, т. е. простым неактивным носительством.
Эпидемиология
Данным вирусом инфицировано более 90 % населения планеты. После 30-40 лет им заражается почти 100 % людей, причём преимущественно I типом вируса.
Единожды инфицированный человек становится пожизненным носителем вируса одного или обоих типов. Данных об эпизодах самоизлечения нет.
В последнее время появились случаи носительства вируса простого герпеса с отсутствием специфических антител IgG к обоим типам вируса. Клиническое и эпидемиологическое значение этого феномена неизвестно. Возможно, такое явление перекрёстно связано с лицами, которые не поддаются заражению.
Источник инфекции — инфицированный человек. Он заразен в любую фазу болезни или носительства, но преимущественно при обострении.
Вирус может находиться в любой биологической жидкости организма — слюне, сперме, вагинальном секрете, отделяемом пузырьков и других.
Восприимчивость всеобщая. Риск заражения возрастает при травмировании кожи и слизистых оболочек здорового человека и попадании на них инфицированных биологических субстратов. Причём вирус может передаваться даже при отсутствии видимых поражений у инфицированного человека.
Большая часть случаев протекает в виде неактивного носительства. Как правило, первично человек приобретает I тип вируса простого герпеса (с детства), а II тип появляется в период половой зрелости. Однако всё относительно.
Основные способы передачи вируса:
В 20% случаев возможна обратная связь типов вирусов и способов их передачи.
Симптомы простого герпеса
Инкубационный период при приобретённой форме длится 2-14 дней. Чаще всего установить его не удаётся из-за отсутствия манифестации.
Простой герпес у детей обычно протекать по типу стоматита и гингивита — повышается температура, появляется лихорадка, общая интоксикация, очаговая гиперемия (покраснение) всех слизистых образований ротовой полости, болезненность при жевании, повышенное слюноотделение. Маленькие дети из-за болевых явлений отказываются от еды. В короткий промежуток времени на месте гиперемии появляются мелкие везикулярные высыпания, которые быстро вскрываются, оставляя после себя болезненные эрозии — афты. Увеличиваются и становятся болезненными регионарные лимфоузлы. С течением времени иммунитет укрепляется и симптомы постепенно регрессируют без каких-либо следов поражения. Рецидивы наблюдаются редко.
При поражении кожи (преимущественно у взрослых) везикулярные высыпания чаще появляются вокруг рта, крыльев носа, иногда на туловище и ягодицах. Сыпь представляет собой небольшие везикулы с серозным содержимым на слегка гиперемированном фоне кожи. Впоследствии они вскрываются и подсыхают, после чего образуются бесследно отпадающие корки.
Иногда пузырьки сливаются в достаточно большие пузыри. Нередко их содержимое нагнаивается, образуется мокнутий, и присоединяется вторичная стрептококковая или стафилококковая инфекция (стафило- и стрептодермии).
Общее самочувствие, как правило, не изменяется. Иногда может быть несколько увеличен и болезнен регионарный лимфоузел. В основном процесс редко продолжается более недели.
При серьёзных иммунодефицитах инфекция может принять более распространённое (генерализованное) течение. В таком случае возникает синдромом общей инфекционной интоксикации и затрагиваются внутренние органы: увеличивается печень и селезёнка, поражается нервная система (менингоэнцефалиты, энцефалиты и менингиты), а также лёгкие, почки и другие органы. При рецидивах хронической инфекции больные иногда ощущают слабый дискомфорт и пощипывание в области будущих высыпаний.
При генитальном герпесе высыпания появляются на коже и слизистых в области половых органов и промежности. Обычно они сопровождаются болезненностью, гиперемией окружающей ткани, увеличением и болезненностью паховых лимфоузлов. Частота рецидивирования зависит от индивидуальных особенностей иммунной системы.
При офтальмогерпесе — герпесе глаз — чаще наблюдаются односторонние поражения из-за перехода первичного процесса на орган зрения, т. е. происходит вторичное поражение. Могут наблюдаться кератиты, блефароконъюнктивиты, иридоциклиты, увеиты, хориоретиниты, невриты зрительного нерва и другие проявления.
Весьма необычной является форма проявления простого герпеса, известная под названием герпетиформная экзема Капоши — герпетическая экзема. Как правило, она возникает у лиц, имеющих какое-либо кожное заболевание или предрасположенность к нему (дерматоз или «проблемная кожа»). При этом наблюдается интоксикация и высокая температура тела, повсеместно появляются герпетические пузырьки, достаточно обильные и близко расположенные, периодически сливающиеся, иногда с геморрагической пропиткой. В некоторых случаях происходит их нагноение, далее они вскрываются, подсыхают и образуют сплошную корку. При тотальной обработке высыпаний зелёнкой кожа больного приобретает вид кожи крокодила. Заболевание нередко протекает достаточно тяжело, может привести к летальному исходу.
При беременности инфицирование ребёнка происходит:
При первичном инфицировании беременной в первый триместр или при восходящем инфицировании плода зачастую развиваются пороки развития, несовместимые с жизнью, или происходит выкидыш, особенно при заражении II типом вируса герпеса, который является инфицирующим агентом чаще всего — до 80 % случаев.
Патогенез простого герпеса
Ворота инфекции — повреждённая кожа и слизистые оболочки.
Вирус прикрепляется к поверхности клетки эпителия, проникает в неё и начинает размножаться. Это может привести к гибели самой клетки, а при массивном процессе — к явным воспалительным процессам, появлению характерной гиперемии, везикулёзных высыпаний и попаданию вируса в кровь и лимфу. В крови вирус обнаруживается на поверхности эритроцитов, лимфоцитов, тромбоцитов. В этот период вирус может попасть в различные органы и ткани, в т. ч. передаться плоду при первичном заражении матери во время беременности.
Вирус простого герпеса инфицирует чувствительные нервные окончания, паравертебральные нервные ганглии. Оттуда может произойти нейрогенное распространение вируса до кожи, в связи с чем появляются новые высыпания. Они далёки от места первичного внедрения:
Если иммунная система адекватна, то вирус исчезает из органов и тканей, но при этом пожизненно сохраняется в чувствительных нервных волокнах. Там он может передаваться из клетки в клетку, минуя межклеточное пространство, и в итоге оказывается недоступным для противодействия иммунной системы – т. н. «иммунное ускользание». После этого вирус может более никогда не иметь манифестных проявлений, но при иммунных нарушениях — Т-клеточном иммунодефиците, нарушении продукции интерферона и работы макрофагов — возможна его реактивация, гиперразмножение, выход из нейросенсорных депо и вновь поражение кожи и слизистых оболочек.
Предрасполагающими факторами реактивации вируса могут являться:
Одну из ключевых ролей в появлении симптомов простого герпеса играют макрофаги. Они «позволяют» или «не позволяют» осуществлять размножение вируса внутри себя (т. н. пермиссивность). В первом варианте развивается инфекция с выраженными симптомами, во втором — субклиническая картина заболевания.
Особую роль играет повышение чувствительности организма антигенами вируса. Оно проявляется в развитии местных аллергических реакций замедленного типа в местах высыпаний. При СПИДе данная реактивация приобретает генерализованный вторичный характер с поражением большинства внутренних органов — головного мозга, печени, лёгких, почек и других.
Классификация и стадии развития простого герпеса
В МКБ-10 (Международной классификации болезней) выделяют на две группы, связанных с вирусом простого герпеса:
По степени тяжести простой герпес бывает:
По форме возникновения заболевания различают:
По форме и распространённости инфекции выделяют четыре стадии простого герпеса:
По клинической картине и локализации высыпаний различают две формы простого герпеса:
Осложнения простого герпеса
Диагностика простого герпеса
Лабораторная диагностика:
Дифференциальная диагностика:
Лечение простого герпеса
Больные с осложнёнными формами простого герпеса подлежат госпитализации в инфекционный стационар. Остальные пациенты при отсутствии серьёзных сопутствующих состояний могут лечиться на дому амбулаторно.
Существует две стратегии этиотропного лечения:
Применение средств местного действия в виде мазей и кремов имеет ограниченный малоэффективный результат.
Высокоэффективное этиотропное лечение вполне может быть дополнено средствами повышения иммунной защиты организма (при наличии резервов организма) и витаминотерапией.
Прогноз. Профилактика
При неосложнённых формах болезни прогноз благоприятный, при генерализованных или формах с поражением ЦНС — серьёзный, возможен летальный исход или инвалидизация.
Важное значение в профилактике развития манифестной инфекции имеет ведение здорового образа жизни, правильное питание, предупреждение и лечение сопутствующих заболеваний, избегание переохлаждений и стрессов.
Специальных ограничительных мероприятий при заболевании не проводят. Больного следует обеспечить индивидуальной посудой, не допускать поцелуев с неинфицированными людьми.
При генитальном герпесе высокоэффективным мероприятием является использование презерватива. Определённое снижение риска распространения инфекции даёт регулярный приём противогерпетических средств уже инфицированным людям.
Если у беременной выявлен генитальный герпес при наличии частых рецидивов, высокой вирусной нагрузке области гениталий и родовых путей, то пациентке показан профилактический приём противогерпетических средств, начиная с 36 недели беременности и до родов (если планируются естественные роды). Или же выполняется плановое кесарево сечение.
Желудочно-кишечное кровотечение неуточненное (K92.2)
Версия: Справочник заболеваний MedElement
Общая информация
Краткое описание
Из данной подрубрики исключены:
— Острый геморрагический гaстрит (K29.0);
— Кровотечения из заднего проходa и прямой кишки (K62.5);
— Желудочно-кишечное кровотечение вследствие пептической язвы (K25-K28);
— Ангиодисплазии желудка с кровотечением (K31.8);
— Дивертикулит с кровотечением (K57).
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
13-15 октября, Алматы, «Атакент»
600 брендов, более 150 компаний-участников из 20 стран.
Новинки рынка стоматологии. Цены от производителей
Классификация
Этиология и патогенез
Механизм развития желудочно-кишечного кровотечения зависит от вызвавшей его причины.
Эпидемиология
Факторы и группы риска
Клиническая картина
Cимптомы, течение
Кровотечения из верхних отделов ЖКТ
Прямые симптомы (основные клинические признаки): рвота с кровью (гематемезис), черный дегтеобразный стул.
В случае ускоренного (менее 8 часов) транзита содержимого по кишечнику и кровопотере свыше 100 мл, с калом может выделиться алая кровь (гематохезия).
Кровотечение из нижних отделов ЖКТ
Диагностическое значение имеет цвет выделяющейся крови. При кишечных кровотечениях наиболее часто встречается появление неизмененной крови (гематохезия). При этом, чем светлее выделяющаяся из прямой кишки кровь, тем дистальнее находится источник кровотечения.
Кровь алого цвета выделяется в основном при кровотечениях, вызванных поражением сигмовидной кишки. Как правило, при расположении источника кровотечения в более проксимальных отделах толстой кишки, отмечается появление темно-красной крови.
При кровотечениях, связанных с поражением перианальной области (геморрой, анальные трещины), выделяющаяся кровь (в виде следов на туалетной бумаге или капель, попадающих на стенки унитаза) обычно не смешана с калом, который сохраняет коричневую окраску.
При локализации источника кровотечения проксимальнее ректосигмоидного отдела кровь бывает более или менее равномерно перемешана с калом.
Диагностика
Диагностика кровотечения из верхних отделов ЖКТ
1. Оценка (диагностика) кровопотери
| Показатель шокового индекса (ШИ) | Дефицит ОЦК в % |
| 1 | 30 |
| 2 | 70 |
| Степень тяжести | Объем кровопотери в литрах | Дефицит ОЦК % |
| I | 1-1,5 | |
| II | 1,5-2,5 | 20-40 |
| III | >2,5 | 40-70 |
| Количество баллов | Частота повторных кровотечений (%) | Смертность больных (%) |
| 0 | 5 | 0 |
| 1 | 3 | 0 |
| 2 | 5 | 0,2 |
| 3 | 11 | 3 |
| 4 | 14 | 5 |
| 5 | 24 | 11 |
| б | 33 | 17 |
| 7 | 44 | 27 |
| >8 | 42 | 41 |
Также используют Шкалу оценки и прогноза состояния больного с кровотечением из верхних отделов желудочно-кишечного тракта — Glasgow-Blatchford score (GBS).
Оценка рассчитывается по следующей таблице:
| Критерии Глазго-Блэтчфорд | |
| Показатель | Оценочный балл |
| Мочевина крови ммоль\л | |
| ≥ 6,5 | 2 |
| ≥ 8,0 | 3 |
| ≥ 10,0 | 4 |
| ≥ 25 | 6 |
| Гемоглобин (г / л) для мужчин | |
| ≥ 12,0 | 1 |
| ≥ 10,0 | 3 |
| 6 | |
| Гемоглобин (г / л) для женщин | |
| ≥ 10,0 | 1 |
| 6 | |
| Систолическое артериальное давление (мм рт.ст.) | |
| 100-109 | 1 |
| 90-99 | 2 |
| 3 | |
| Другие маркеры | |
| Пульс ≥ 100 (в минуту) | 1 |
| Мелена (дегтеобразный стул) | 1 |
| Потеря сознания | 2 |
| Заболевания печени | 2 |
| Сердечная недостаточность | 2 |
Диагностика кровотечений из нижних отделов ЖКТ
1. Установление факта кровотечения и оценка степени его тяжести (см. выше).
Лабораторная диагностика
Дифференциальный диагноз
Осложнения
Лечение
Алгоритм терапии зависит от наличия или отсутствия признаков шока.
Алгоритм терапии у пациентов с шоком:
— обеспечение проходимости дыхательных путей, оксигенотерапия;
— обеспечение венозного доступа (установка двух периферических венозных катетеров 14-16G);
— в/в ведение кровезаменителей (стартовая доза 500-1000 мл), определение группы крови и резус-фактора, расчет необходимой дозы донорской крови;
— катетеризация центральной вены, измерение центрального венозного давления;
— рассмотреть вопрос о терапии ИПП (поражение желудка и двенадцатиперстной кишки), октреотидом и глипрессином (при кровотечении из варикозно расширенных вен пищевода) или иной патогенетической терапии (при кровотечениях другой этиологии).
В 80% случаев происходит самопроизвольное прекращение острых кишечных кровотечений. При умеренно выраженных кровотечениях проводят консервативную терапию в соответствии с заболеванием, вызвавшим кровотечение.
Язвенная болезнь
Общая информация
Краткое описание
Код протокола: H-Т-029 «Язвенная болезнь»
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
13-15 октября, Алматы, «Атакент»
600 брендов, более 150 компаний-участников из 20 стран.
Новинки рынка стоматологии. Цены от производителей
Классификация
По нозологической самостоятельности
1. Язвенная болезнь.
По локализации поражения
— атипичные (с атипичным болевым синдромом, безболевая, бессимптомная).
— рубцово-язвенная деформация луковицы двенадцатиперстной кишки.
Факторы и группы риска
Диагностика
Физикальное обследование
1. Ранние боли возникают через 0,5-1 ч. после еды, постепенно нарастают по интенсивности, сохраняются в течение 1.5-2 ч., уменьшаются и исчезают по мере продвижения желудочного содержимого в двенадцатиперстную кишку; характерны для язв тела желудка. При поражении кардиального, субкардиального и фундального отделов болевые ощущения возникают сразу после приема пищи.
2. Поздние боли возникают через 1,5-2 ч. после еды, постепенно усиливаются по мере эвакуации содержимого из желудка; характерны для язв пилорического отдела желудка и луковицы двенадцатиперстной кишки.
Наиболее типичной проекцией болей в зависимости от локализации язвенного процесса считают следующую:
При кровотечении из язвы реакция на скрытую кровь в кале становится положительной.
Наличие НР подтверждается микроскопическими, серологическими тестами и уреазным дыхательным тестом (см. ниже).
Показания для консультации специалистов: по показаниям.
Публикации в СМИ
Демпинг-синдром
Демпинг-синдром — патологическое состояние, возникающее после резекции желудка (особенно по модификации Билльрот-II), гастрэктомии, ваготомии, пилоропластики вследствие быстрого поступления желудочного содержимого в тонкую кишку.
Статистические данные. Частота после селективной проксимальной ваготомии — у 0,9% оперированных больных; после стволовой ваготомии с пилоропластикой — 10–22% случаев; у женщин после резекции желудка — до 100%.
Классификация • По времени возникновения •• Ранний демпинг-синдром (признаки появляются в течение 30 мин после еды) •• Поздний (гипогликемический) демпинг-синдром (через 2 ч после еды) • По степени тяжести •• Лёгкая степень (демпинг-реакция возникает только после молочных и сладких блюд): незначительная слабость, учащение пульса на 10–15 в минуту; продолжительность приступа — до 30 мин; дефицит массы тела — не более 5 кг; трудоспособность сохранена •• Средняя степень (демпинг-реакция возникает при приёме любой пищи, на высоте реакции больной вынужден ложиться): учащение пульса на 20–30 в минуту; АД с тенденцией к повышению систолического компонента; длительность приступа — до 1 ч; дефицит массы тела — до 10 кг; трудоспособность снижена •• Тяжёлая степень (демпинг-реакция развивается при приёме любой пищи): больные принимают пищу лёжа и находятся в горизонтальном положении до 2–3 ч после еды; учащение пульса более чем на 30 в минуту; АД лабильное, иногда брадикардия, артериальная гипотензия, коллапс; дефицит массы тела — более 10 кг; трудоспособность утрачена.
Факторы риска: дренирующие операции, резекция желудка.
Патогенез • Быстрое поступление в верхний отдел тонкой кишки пищи, имеющей высокую осмолярность, приводит к перемещению в просвет внеклеточной жидкости, растяжению стенки кишки и выделению биологически активных веществ: гистамина, серотонина, брадикинина. В результате: вазодилатация, уменьшение ОЦК, усиление перистальтики кишечника • Другая форма демпинг-синдрома (реактивная гипогликемия) связана с резким увеличением содержания глюкозы после приёма пищи. Быстрое увеличение концентрации глюкозы в крови стимулирует выделение инсулина. Однако к этому времени (примерно через 2 ч после еды) принятая пища уже утилизирована, и запоздалое действие инсулина вызывает клинические признаки гипогликемии. На фоне гипогликемии изменяется содержание электролитов, особенно калия, в сыворотке крови.
Клинические проявления • Приступы слабости во время еды или через 15–20 мин после неё • Сонливость, головокружение, шум в ушах, дрожание конечностей • Чувство дискомфорта в животе, боль • Метеоризм • Тошнота • Диарея • Сердцебиение • Повышенное потоотделение • Снижение массы тела • Преходящая эритема • Спутанное сознание и обморочное состояние • Тяжесть проявлений демпинг-синдрома уменьшается в положении лёжа. Напротив, пища, богатая углеводами, усиливает симптоматику.
Методы исследования • Провокационная проба. Демпинг-синдром может быть спровоцирован приёмом 150 мл 50% р-ра глюкозы или сахара. При этом больной не должен ложиться • Рентгеноскопия желудка: выявляют мгновенное опорожнение желудка от контрастной массы • Анализ крови: послеобеденная гипогликемия, признаки анемии, гипоальбуминемия • Препарат, влияющий на результаты, — инсулин; заболевание, влияющее на результат: СД.
Дифференциальная диагностика • Частичная кишечная непроходимость • Желудочно-ободочный свищ • Хронический энтерит • Спру • Болезнь Крона • Инсулинома • Секреторная недостаточность поджелудочной железы • Нейроэндокринные опухоли (карциноид).
ЛЕЧЕНИЕ
Консервативное лечение • Диета. Назначают диету №1, содержащую 130 г белков, 100 г жиров, 350–400 г углеводов (30 г сахара). Возможно полное исключение сахара с заменой на ксилит или сорбит. Для снижения скорости эвакуации пищи из культи желудка готовят вязкие и желеобразные блюда. Целесообразен раздельный приём плотной и жидкой пищи. Приём пищи — не менее 6 р/день. После еды желательно лежать около 30 мин • Для уменьшения реакции на быстрое поступление пищи в тонкую кишку перед едой назначают прокаин, анестезин, антигистаминные препараты • Октреотид по 200–400 мг/сут п/к в равных дозах каждые 8 ч • Заместительная терапия: желудочный сок, соляная кислота, панзинорм форте, панкреатин, панкреатин+жёлчи компоненты+гемицеллюлаза, витамины • Другие методы •• Антихолинергические средства (например, атропин, платифиллин) обычно малоэффективны •• При нарушениях питания — переливание крови и кровезаменителей •• Психотерапия.
Хирургическое лечение • Показания к операции: демпинг-синдром тяжёлой степени в случае неэффективности лечебного питания и длительного комплексного медикаментозного лечения • Оперативное вмешательство заключается в редуоденизации с гастродуоденопластикой. Тонкокишечный трансплантат замедляет опорожнение культи желудка, включение двенадцатиперстной кишки улучшает пищеварение и у ряда больных может уменьшить интенсивность демпинг-реакции.
Осложнения • Гипогликемия • Нарушения питания • Электролитные нарушения, включая гипокалиемию • Анемия.
Сопутствующая патология • Пептические язвы • Реактивная гипогликемия • Спаечная болезнь брюшины • Хронический панкреатит • Хронический энтерит • Дискинезия желчевыводящих путей.
Профилактика: широкое применение органосохраняющих операций (например, селективной проксимальной ваготомии) при лечении язвенной болезни двенадцатиперстной кишки. В случае необходимости резекции желудка следует стремиться к наложению прямого гастродуоденоанастомоза.
Синонимы • Постгастрорезекционный синдром • Болезнь оперированного желудка • Агастральная астения • Синдром «малого желудка» • Синдром сбрасывания
МКБ-10 • K91.1 Синдромы оперированного желудка
Код вставки на сайт
Демпинг-синдром
Демпинг-синдром — патологическое состояние, возникающее после резекции желудка (особенно по модификации Билльрот-II), гастрэктомии, ваготомии, пилоропластики вследствие быстрого поступления желудочного содержимого в тонкую кишку.
Статистические данные. Частота после селективной проксимальной ваготомии — у 0,9% оперированных больных; после стволовой ваготомии с пилоропластикой — 10–22% случаев; у женщин после резекции желудка — до 100%.
Классификация • По времени возникновения •• Ранний демпинг-синдром (признаки появляются в течение 30 мин после еды) •• Поздний (гипогликемический) демпинг-синдром (через 2 ч после еды) • По степени тяжести •• Лёгкая степень (демпинг-реакция возникает только после молочных и сладких блюд): незначительная слабость, учащение пульса на 10–15 в минуту; продолжительность приступа — до 30 мин; дефицит массы тела — не более 5 кг; трудоспособность сохранена •• Средняя степень (демпинг-реакция возникает при приёме любой пищи, на высоте реакции больной вынужден ложиться): учащение пульса на 20–30 в минуту; АД с тенденцией к повышению систолического компонента; длительность приступа — до 1 ч; дефицит массы тела — до 10 кг; трудоспособность снижена •• Тяжёлая степень (демпинг-реакция развивается при приёме любой пищи): больные принимают пищу лёжа и находятся в горизонтальном положении до 2–3 ч после еды; учащение пульса более чем на 30 в минуту; АД лабильное, иногда брадикардия, артериальная гипотензия, коллапс; дефицит массы тела — более 10 кг; трудоспособность утрачена.
Факторы риска: дренирующие операции, резекция желудка.
Патогенез • Быстрое поступление в верхний отдел тонкой кишки пищи, имеющей высокую осмолярность, приводит к перемещению в просвет внеклеточной жидкости, растяжению стенки кишки и выделению биологически активных веществ: гистамина, серотонина, брадикинина. В результате: вазодилатация, уменьшение ОЦК, усиление перистальтики кишечника • Другая форма демпинг-синдрома (реактивная гипогликемия) связана с резким увеличением содержания глюкозы после приёма пищи. Быстрое увеличение концентрации глюкозы в крови стимулирует выделение инсулина. Однако к этому времени (примерно через 2 ч после еды) принятая пища уже утилизирована, и запоздалое действие инсулина вызывает клинические признаки гипогликемии. На фоне гипогликемии изменяется содержание электролитов, особенно калия, в сыворотке крови.
Клинические проявления • Приступы слабости во время еды или через 15–20 мин после неё • Сонливость, головокружение, шум в ушах, дрожание конечностей • Чувство дискомфорта в животе, боль • Метеоризм • Тошнота • Диарея • Сердцебиение • Повышенное потоотделение • Снижение массы тела • Преходящая эритема • Спутанное сознание и обморочное состояние • Тяжесть проявлений демпинг-синдрома уменьшается в положении лёжа. Напротив, пища, богатая углеводами, усиливает симптоматику.
Методы исследования • Провокационная проба. Демпинг-синдром может быть спровоцирован приёмом 150 мл 50% р-ра глюкозы или сахара. При этом больной не должен ложиться • Рентгеноскопия желудка: выявляют мгновенное опорожнение желудка от контрастной массы • Анализ крови: послеобеденная гипогликемия, признаки анемии, гипоальбуминемия • Препарат, влияющий на результаты, — инсулин; заболевание, влияющее на результат: СД.
Дифференциальная диагностика • Частичная кишечная непроходимость • Желудочно-ободочный свищ • Хронический энтерит • Спру • Болезнь Крона • Инсулинома • Секреторная недостаточность поджелудочной железы • Нейроэндокринные опухоли (карциноид).
ЛЕЧЕНИЕ
Консервативное лечение • Диета. Назначают диету №1, содержащую 130 г белков, 100 г жиров, 350–400 г углеводов (30 г сахара). Возможно полное исключение сахара с заменой на ксилит или сорбит. Для снижения скорости эвакуации пищи из культи желудка готовят вязкие и желеобразные блюда. Целесообразен раздельный приём плотной и жидкой пищи. Приём пищи — не менее 6 р/день. После еды желательно лежать около 30 мин • Для уменьшения реакции на быстрое поступление пищи в тонкую кишку перед едой назначают прокаин, анестезин, антигистаминные препараты • Октреотид по 200–400 мг/сут п/к в равных дозах каждые 8 ч • Заместительная терапия: желудочный сок, соляная кислота, панзинорм форте, панкреатин, панкреатин+жёлчи компоненты+гемицеллюлаза, витамины • Другие методы •• Антихолинергические средства (например, атропин, платифиллин) обычно малоэффективны •• При нарушениях питания — переливание крови и кровезаменителей •• Психотерапия.
Хирургическое лечение • Показания к операции: демпинг-синдром тяжёлой степени в случае неэффективности лечебного питания и длительного комплексного медикаментозного лечения • Оперативное вмешательство заключается в редуоденизации с гастродуоденопластикой. Тонкокишечный трансплантат замедляет опорожнение культи желудка, включение двенадцатиперстной кишки улучшает пищеварение и у ряда больных может уменьшить интенсивность демпинг-реакции.
Осложнения • Гипогликемия • Нарушения питания • Электролитные нарушения, включая гипокалиемию • Анемия.
Сопутствующая патология • Пептические язвы • Реактивная гипогликемия • Спаечная болезнь брюшины • Хронический панкреатит • Хронический энтерит • Дискинезия желчевыводящих путей.
Профилактика: широкое применение органосохраняющих операций (например, селективной проксимальной ваготомии) при лечении язвенной болезни двенадцатиперстной кишки. В случае необходимости резекции желудка следует стремиться к наложению прямого гастродуоденоанастомоза.
Синонимы • Постгастрорезекционный синдром • Болезнь оперированного желудка • Агастральная астения • Синдром «малого желудка» • Синдром сбрасывания
МКБ-10 • K91.1 Синдромы оперированного желудка
Язвенная болезнь желудка и двенадцатиперстной кишки без кровотечения и прободения (педиатрия)
Общая информация
Краткое описание
Язвенная болезнь желудка и двенадцатиперстной кишки – хроническое заболевание, характерным признаком которого в период обострения является воспаление слизистой оболочки желудка и двенадцатиперстной кишки и образование язв [3].
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
13-15 октября, Алматы, «Атакент»
600 брендов, более 150 компаний-участников из 20 стран.
Новинки рынка стоматологии. Цены от производителей
Классификация
Ведущую роль в диагностике язвенной болезни желудка и двенадцатиперстной кишки играет диагностика Нelicobacter pylori инфекции. Правила диагностики и лечения НР-инфекции у детей рекомендованы ESPGHAN/NASPGHAN в 2011 году [1,2 и приложение].
Диагностика
II. МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
• исследование перианального соскоба.
• исследование кала (копрограмма).
Диагностические мероприятия, проводимые на этапе скорой неотложной помощи: не проводится.
• Симптомы хронической интоксикации и астено-вегетативные нарушения.
Дифференциальный диагноз
Таблица 1. Дифференциальная диагностика ЯБЖ и ДПК

Лечение
• предупреждение осложнений и возникновения рецидивов заболевания.
Оптимизация режима дня и нагрузок.
Продолжительность трехкомпонентной терапии – 10 дней.
Соблюдение терапии и побочные эффекты должны контролироваться.
Терапия второй линии (квадротерапия) назначается в случае неэффективности препаратов первой линии с дополнительным включением коллоидного субцитрата висмута (висмута трикалия дицитрат):
Включение цитопротекторов (сукральфат, висмута трикалия дицитрат, висмута субгаллат) потенцирует антихеликобактерное действие антибиотиков.
При появлении НР-бактерии в организме больного через год после окончания лечения ситуацию следует расценивать как рецидив инфекции, а не как реинфекцию. При рецидиве инфекции необходимо применение более эффективной схемы лечения.
Медикаментозное лечение, оказываемое на амбулаторном уровне
Пептическая язва неуточненной локализации. Острая без кровотечения или прободения (K27.3)
Версия: Справочник заболеваний MedElement
Общая информация
Краткое описание
Пептическая язва может возникнуть в следующих случаях:
— когда в организме больного пепсин и кислота присутствуют в аномально высокой концентрации;
— при снижении нормальных защитных механизмов, предохраняющих слизистую оболочку пищеварительного тракта от повреждения;
— в результате воздействия желчи (особенно язвы желудка).
Первой морфологической стадией язвенной болезни является эрозия, которая представляет собой неглубокий дефект (повреждение) слизистой оболочки в границах эпителия и образуется при некрозе участка слизистой оболочки.
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
13-15 октября, Алматы, «Атакент»
600 брендов, более 150 компаний-участников из 20 стран.
Новинки рынка стоматологии. Цены от производителей
Классификация
Этиология и патогенез
Эпидемиология
Возраст: старше 7 лет
Признак распространенности: Распространено
Соотношение полов(м/ж): 2
Язвенной болезнью страдают 5-10% населения.
По мнению ряда авторов, инфицирование H. pylori (как основная потенциальная причина возникновения ЯБЖ) значительно выше и составляет от 25 до 80% в различных странах. Уровень инфицирования коррелирует в первую очередь с социально-экономическим уровнем. Среди городских жителей заболевание регистрируется чаще в 2-3 раза, чем среди сельских. Мужчины до 50 лет болеют чаще, чем женщины. ЯБЖ является более редкой формой по сравнению с язвой ДПК.
В структуре язвенных поражений желудочно-кишечного тракта (ЖКТ) у детей я звенная болезнь желудка составляет около 13% и встречается примерно у 2 из 10 000 детей. Язвенная болезнь ДПК встречается в 8 раз чаще. Заболеванию подвержены дети в возрасте от 7 лет. Мальчики и девочки болеют одинаково часто.
Факторы и группы риска
Клиническая картина
Клинические критерии диагностики
Cимптомы, течение
Боли при обострении язвенной болезни обычно связаны с приемом пищи. Они могут возникать сразу после еды (при язвах кардиального и субкардиального отделов желудка), спустя 0,5-1 час после приема пищи (при язвах тела желудка).
Для язв пилорического канала и луковицы ДПК типичны поздние боли (через 2-3 часа после еды), «голодные» боли (возникают натощак и купируются приемом пищи), а также ночные боли.
Боли уменьшаются и исчезают после приема антацидов, антисекреторных и спазмолитических препаратов, применения тепла.
Течение болезни обладает рядом особенностей у женщин, в юношеском и подростковом возрасте, а также в старческом и пожилом возрасте.
Клиника язвенной болезни при атипичном течении или атипичных формах:
1. Боли зачастую локализуются преимущественно в области правого подреберья или в правой подвздошной области.
2. Возможна атипичная локализация боли в области сердца («сердечная маска») или в поясничной области («радикулитная маска»).
3. Наличие «немых» язв, которые имеют только диспепсические проявления при отсутствии болевого синдрома. «Немые» язвы могут проявиться желудочным кровотечением или перфорацией. Часто они приводят к развитию рубцового стеноза привратника, и больные обращаются за медицинской помощью лишь в случае появления симптоматики самого стеноза.
У детей
Клиническая картина язвенной болезни у детей отличается от взрослых в некоторых деталях. Наиболее выраженные клинические особенности имеют место у детей с локализацией язвы в кардиальном или субкардиальном отделе желудка.
Среди особенностей проявлений язв верхнего отдела желудка отмечают слабую выраженность болевого синдрома, атипичную локализацию и иррадиацию боли. Дети часто жалуются на ощущение жжения и давления под мечевидным отростком, за грудиной или слева от нее. Боль может иррaдиировать в область сердца, левое плечо, под левую лопатку; появляется через 20-30 минут после еды и уменьшается при приеме антисекреторных средств.
Диагностика
Диагностика язвенной болезни базируется на совокупности данных клинического обследования, результатов инструментальных, морфологических и лабораторных методов исследования.
Инструментальная диагностика. Диагностика факта наличия язвы
Обязательные исследования
Основное значение имеет эндоскопическое исследование, которое позволяет уточнить локализацию язвы и определить стадию заболевания. Чувствительность метода составляет около 95%. Язва представляет собой дефект слизистой оболочки, достигающий мышечного и даже серозного слоя. Хронические язвы могут быть округлой, треугольной, воронкообразной или неправильной формы. Края и дно язвы могут быть уплотнены за счет соединительной ткани (каллезная язва). При заживлении хронической язвы происходит образование рубца.
В случае невозможности проведения ЭГДС осуществляется рентгеноскопия желудка и ДПК, которая позволяет обнаружить язву примерно в 70% случаев. Диагностическую точность повышает метод двойного контрастирования. Кратер язвы (ниша) имеет вид углубления на контуре стенки слизистой или стойкого контрастного пятна. Складки конвергируют к основанию язвы, окруженному широким воспалительным валом (линия Хемптона). Кратер язвы гладкий, округлой или овальной формы.
Рентгеновское исследование чаще используется с целью выявления осложнений (рубцовых деформаций, пенетрации).
Диагностика H.pylori (хеликобактериоза), как основной причины язвенной болезни, имеет большое значение.
Неинвазивные методы:
— определение антигена в стуле (хроматография с моноклональными антителами);
— дыхательный тест с мочевиной меченой изотопом углерода (С13-14);
— серологические методы (определение антител к H.pylori).
Дополнительные исследования
Проводят суточную рН-метрию, исследование интрагастральной протеолитической активности желудка. Для оценки моторной функции желудка применяют ультразвуковое, электрогастрографическое, рентгенологическое исследования, антродуоденальную манометрию.
УЗИ органов брюшной полости проводят для диагностики сопутствующей патологии гепатобилиарной системы и поджелудочной железы.
«Диспепсия неуточненная»: дифференциальный диагноз, тактика ведения пациента на амбулаторном этапе
В обзоре представлены современные данные о тактике ведения пациента с синдромом диспепсии на амбулаторно-поликлиническом этапе.
The current data about patient management strategy of dyspepsia syndrome at outpatient stage are reported in the review.
Синдром диспепсии — один из наиболее распространенных гастроэнтерологических синдромов, до 95% болезней органов пищеварения сопровождаются его развитием. Синдром диспепсии включает один или несколько симптомов в различных сочетаниях: боли или чувство жжения в эпигастрии; чувство переполнения в эпигастрии после еды; раннее насыщение; возможны тошнота, отрыжка [1]. Распространенность в популяциях симптомов диспепсии колеблется от 7% до 41% [2–4]. Эти данные относятся к больным с так называемой «диспепсией неуточненной» (uninvestigated dyspeрsia), включающей как органическую (вторичную) диспепсию, так и функциональную. Установить форму диспепсии и распознать причину на амбулаторном приеме — непростая клиническая задача, которую усложняют ограниченность времени первичного приема и широкий круг заболеваний, среди которых должен проводиться дифференциальный диагноз.
Классификационные подходы
Если пациенту не проводили эндоскопического исследования, следует выставлять диагноз «диспепсия неуточненная» [1, 5].
«Вторичная диспепсия» диагностируется у пациентов с органическими, системными или метаболическими заболеваниями [6].
Диагноз «диспепсия, ассоциированная с Н. pylori» устанавливается у пациентов, у которых симптомы диспепсии выявлены на фоне инфекции Н. pylori и эффективно купируются эрадикационной терапией [6].
В случае сохранения диспепсических симптомов после проведенной эрадикации Н. pylori есть основание для постановки диагноза «функциональная диспепсия» [6]. Диагноз «функциональная диспепсия» является диагнозом исключения вторичной диспепсии и диспепсии, ассоциированной с Н. pylori, и может быть установлен только после обследования больного и при соответствии выявленных признаков IV Римским критериям [1, 5].
Алгоритм диагностического поиска
Начальным этапом диагностического поиска при первом контакте с пациентом является активное выявление или исключение у него «тревожных признаков». «Тревожные признаки» — симптомы, позволяющие врачу заподозрить наличие у пациента серьезного органического заболевания [7].
К «тревожным признакам» относят диспепсию постоянного или прогрессирующего характера; симптомы, впервые возникшие в возрасте после 45 лет, короткий (менее 6 месяцев) анамнез заболевания; дисфагию или одинофагию; повторную рвоту; рвоту с кровью; мелену, гематохезис; лихорадку; необъяснимое снижение массы тела (более 5% за период от 6 до 12 месяцев); ночные симптомы, вызывающие пробуждение; семейный анамнез по онкологическим заболеваниям; изменения, выявленные при непосредственном обследовании больного или при рутинных исследованиях [8–10]. Рутинные исследования включают общеклинический анализ крови и мочи, биохимическое исследование крови на билирубин, холестерин, глюкозу, аминотрансферазы, щелочную фосфатазу, гамма-глутамилтранспептидазу, амилазу, липазу, общий белок, С-реактивный белок, креатинин; ультразвуковое исследование органов брюшной полости; кал на скрытую кровь; электрокардиографию; рентгенологическое исследование органов грудной клетки; гинекологический осмотр [8–10]. Наличие «тревожных признаков» должно расцениваться врачом как показание для проведения неотложной эндоскопии. Такие пациенты нуждаются в осмотре хирурга, консультации других специалистов, в незамедлительном полном клиническом обследовании (включая компьютерную томографию, колоноскопию и др.) и госпитализации.
Диспепсия и другие тревожные признаки могут быть связаны с раком верхних отделов пищеварительного тракта, в частности пищевода и желудка [11].
Персистенция симптомов диспепсии относится к тревожным признакам, поэтому важна их динамическая оценка с учетом ответа на проводимую терапию. Как правило, наличие тревожных признаков при злокачественных новообразованиях встречается при более выраженных (клинически и гистологически) стадиях заболевания.
Учитывая неблагоприятную ситуацию по раку желудка, проведение эзофагогастродуоденоскопии (ЭГДС) показано всем пациентам с синдромом диспепсии [12]. На основании характера жалоб, возраста, данных анамнеза, результатов физикального и общеклинических методов исследования врачу необходимо исключить «вторичную диспепсию». Вторичная диспепсия диагностируется у пациентов с органическими, системными или метаболическими заболеваниями. У пациентов с впервые возникшей диспепсией в возрасте старше 45 лет ее функциональный характер маловероятен. Причинами органической (вторичной) диспепсии чаще всего являются:
Следует также помнить, что симптомы заболеваний верхних отделов желудочно-кишечного тракта (ЖКТ) наблюдаются в 2 раза чаще среди пациентов с сердечно-сосудистыми заболеваниями. Наличие атеросклероза, лабораторные признаки дислипидемии повышают риск возникновения симптомов болезней верхних отделов ЖКТ. При курации пациентов старших возрастных групп следует учитывать, что диспепсия может быть продромальными проявлениями острого коронарного синдрома или начальными проявлениями мезентериальной недостаточности [13].
Соотношение диагнозов «диспепсия» и «хронический гастрит»
До недавнего времени полагали, что хронический гастрит не является причиной возникновения диспепсических симптомов, однако в последние годы эта точка зрения претерпела существенные изменения. В соответствии с положениями так называемого Киотского консенсуса (2014 г.) у части больных с синдромом диспепсии имеющиеся клинические симптомы могут быть обусловлены хроническим гастритом, ассоциированным с Н. pylori, если после эрадикации отмечается их стойкое исчезновение. В таких случаях рекомендовано ставить диагноз «диспепсия, ассоциированная с инфекцией Н. pylori» [6]. Такая же рекомендация дана и в последнем согласительном совещании «Маастрихт V», которое к истинной функциональной диспепсии относит только те диспепсические симптомы, которые сохраняются, несмотря на успешно проведенную эрадикацию [14].
Диагноз «хронический гастрит» был и остается наиболее распространенным в клинической практике. Длительное время термин «гастрит» ошибочно был использован в качестве замены для клинического диагноза «функциональная диспепсия» [15].
С одной стороны, хронический гастрит может не иметь клинического эквивалента и протекать бессимптомно. Но у части пациентов инфекция Н. pylori может быть причиной развития симптомов с явлениями диспепсии. Во-первых, острая ятрогенная или самостоятельная инфекция Н. pylori может индуцировать острые симптомы диспепсии. Несмотря на то, что персистирующая колонизация практически всегда приводит к развитию хронического гастрита, у большинства лиц тяжелые диспепсические явления возникают периодически.
Н. pylori-индуцированный гастрит приводит к хроническому активному гастриту разной степени тяжести практически у всех инфицированных лиц. Однако выраженность структурных повреждений слизистой оболочки существенно варьирует в зависимости от индивидуума, соответственно, ассоциированные физиологические изменения также различаются.
Диагноз диспепсии, связанной с Н. pylori, выставляется пациентам, у которых симптомы эффективно купируются эрадикацией инфекции [6].
В настоящее время критерии, позволяющие с высокой степенью надежности прогнозировать, ответит ли пациент с симптомами диспепсии на эрадикационную терапию, отсутствуют.
Расчетное количество пролеченных больных на одного излеченного составляет, по данным литературы, — восемь человек [14].
С современных позиций диагноз «хронический гастрит» должен отражать не только наличие инфекции Н. pylori (для определения варианта Н. pylori-ассоциированной диспепсии), но и формироваться с учетом как эндоскопических, так и морфологических признаков. Топография хронического гастрита находит отражение в клинических особенностях и тесно взаимосвязана с этиологическим фактором. Хронический антральный Н. pylori-ассоциированный гастрит протекает с гиперсекрецией соляной кислоты, при этом повышается риск дуоденальной язвы. При фундальном гастрите с атрофией слизистой оболочки наблюдается низкая секреция кислоты и повышенный риск возникновения язвы желудка и дистального рака желудка [16, 17].
Гастрит — это морфологический диагноз, который обязательно должен отражать выраженность и распространенность воспаления и атрофии. Тяжесть и распространенность атрофического гастрита и кишечной метаплазии используют в качестве индикаторов повышенного риска развития рака желудка. Тяжелый Н. pylori-ассоциированный гастрит тела желудка связан с повышенным риском рака желудка. Это обосновывает необходимость использования методов стратификации риска. Взятие биоптатов из разных отделов желудка может быть использовано для получения наиболее важной информации с целью классификации рисков [18–20]. Оценка биоптатов слизистой оболочки по системе OLGA и OLGIM необходима для стратификации риска развития рака желудка. Риск возникновения рака желудка коррелирует с тяжестью и распространенностью атрофического гастрита. Более высокий риск развития рака желудка у пациентов на стадии III или IV по системе OLGA или OLGIM [18–20].
Точная оценка характера гастрита требует взятия биоптатов как из антрального отдела, так и из тела желудка, при этом, помимо стандартных 5 точек (антральный и фундальный отдел по малой и большой кривизне, угол желудка), необходимо взятие биопсии из всех эндоскопически измененных участков слизистой оболочки [18–20].
К сожалению, повседневная практика гастробиопсии, а также морфологического исследования гастробиоптатов в 95,97% диагностических случаев не соответствует требованиям Российского пересмотра Международной классификации хронического гастрита OLGA-system [21].
Подходы к терапии
В соответствии с рекомендациями Киотского консенсуса [6], положениями IV Римского консенсуса [5], согласительного совещания «Маастрихт V» [14], Рекомендациями Российской гастроэнтерологической ассоциации [8, 22], эрадикационная терапия у больных хроническим гастритом с симптомами диспепсии служит терапией первого выбора, позволяющей исключить из группы пациентов с функциональной диспепсией больных с диспепсией, ассоциированной с инфекцией Н. pylori.
Антисекреторная терапия
У пациентов в возрасте до 45 лет при исключении «тревожных признаков» терапия ингибиторами протонной помпы (ИПП) считается целесообразной. Антисекреторная терапия может облегчить симптомы диспепсии. Ингибиторы протонной помпы рассматриваются как эффективные средства лечения диспепсии на основании результатов нескольких контролируемых исследований с 10–15% терапевтическим преимуществом по сравнению с плацебо [1, 5]. Это также было проиллюстрировано в метаанализе шести рандомизированных контролируемых исследований, которые включают 2709 пациентов с диспепсией, которые получали терапию ИПП, в сравнении с терапией плацебо или антацидами [23]. Симптомы диспепсии присутствовали значительно в меньшей пропорции в группах ИПП по сравнению с контрольными (50% против 73%).
У пациентов с стойкими симптомами после эрадикации H. pylori предлагается антисекреторная терапия ИПП в течение четырех-восьми недель [23].
ИПП малоэффективны для борьбы с симптомами постпрандиального дистресс-синдрома (тяжесть, переполнение в эпигастрии после еды) [23]. На этом фоне прокинетики оказывают значимое положительное влияние на перистальтику по сравнению с плацебо, с относительным снижением риска на 33% и числом пролеченных больных на одного излеченного, равным шести [1, 5].
При исключении «тревожных признаков» у пациента в возрасте до 45 лет эффективной является терапия ингибиторами протонной помпы (омепразол или рабепразол 20 мг/сут), прокинетиками. Оправдано применение фиксированной комбинации омепразола 20 мг с домперидоном модифицированного высвобождения 30 мг/сут (Омез® ДСР). Данная комбинация в одной лекарственной форме решила сразу несколько проблем: повысила комплаентность пациентов, эффективность и безопасность терапии. Включение прокинетика домперидона с постепенным высвобождением позволяет принимать препарат один раз в день вместо трехразового приема. Безопасность определяется тем, что отсутствуют пиковые значения концентраций домперидона, неизбежные при использовании обычных лекарственных форм, что снижает вероятность проявления нежелательных дозозависимых явлений. Концентрация домперидона в плазме крови на фоне применения фиксированной комбинации омепразола 20 мг с домперидоном модифицированного высвобождения 30 мг не выходит за пределы таковой при приеме однократной дозы домперидона 10 мг, что позволяет назначать препарат как короткими, так и длительными курсами [24].
Лечение вторичной диспепсии при каждой нозологической форме определяется соответствующими стандартами.
Оценка стойких симптомов
Несмотря на терапию, некоторые пациенты продолжают испытывать симптомы диспепсии. Пациенты с продолжающимися симптомами диспепсии относятся к следующим категориям: пациенты с альтернативным диагнозом, пациенты с персистирующей инфекцией Н. pylori и пациенты с функциональной диспепсией [25].
Пациенты с сохраняющимися симптомами диспепсии требуют особого внимания с анализом текущих симптомов, степени их улучшения или ухудшения на фоне медикаментозного лечения. В случае отсутствия эффекта от терапии в стандартные сроки или при прогрессировании диспепсии выставленный ранее диагноз должен быть пересмотрен, пациенту необходимо провести уточняющие диагностические исследования (компьютерная томография, магнитно-резонансная томография, колоноскопия и др.), следует привлечь для консультации других специалистов.
Диагноз «функциональная диспепсия» может быть выставлен при наличии соответствующих диагностических критериев (Римские критерии IV, 2016) лицам с симптомами диспепсии, регистрируемыми в течение трех месяцев с их началом по крайней мере за шесть месяцев до постановки диагноза при отсутствии признаков органической патологии, которая могла бы вызвать появление симптомов [1, 5].
Заключение
Синдром диспепсии — один из наиболее распространенных гастроэнтерологических синдромов, который встречается при широком спектре заболеваний.
Диспепсия может быть органической (вторичной) или функциональной. Вторичная диспепсия диагностируется у пациентов с органическими, системными или метаболическими заболеваниями.
Диагноз диспепсии, связанной с Н. pylori, выставляется подгруппе пациентов, у которых симптомы эффективно купируются эрадикацией инфекции.
Хронический гастрит, вызванный инфекцией Н. pylori, следует рассматривать как показание к проведению эрадикационной терапии, так как это является эффективной мерой профилактики ассоциированных с Н. pylori заболеваний.
При первичном обращении пациента на этапе обследования целесообразно использовать термин «диспепсия неуточненная».
Активный поиск «тревожных признаков» является обязательным на амбулаторном этапе диагностики. Симптомы тревоги свидетельствуют, как правило, о наличии у пациента органической патологии ЖКТ или других органов и систем, что требует дополнительного обследования и консультации специалистов.
Проведение ЭГДС показано всем пациентам с синдромом диспепсии независимо от «тревожных признаков», наличие которых определяет лишь срочность эндоскопического исследования.
Диагноз хронического гастрита является морфологическим. Оба заболевания (гастрит и диспепсия) не противоречат друг другу и могут сочетаться у одного и того же больного.
Диагноз хронического гастрита требует взятия биоптатов из 5 стандартных точек, биопсию необходимо брать также из всех визуально измененных участков слизистой оболочки. Гистологическая оценка биоптатов слизистой оболочки по системе OLGA и OLGIM необходима для стратификации риска развития рака желудка, который коррелирует с тяжестью и распространенностью атрофического гастрита.
Реализация современных международных и российских рекомендаций в клинической практике позволит избежать ошибок при постановке диагноза, улучшить прогноз и качество жизни пациентов.
Литература
* ФГБОУ ВПО ОмГМУ МЗ РФ, Омск
** ФГАОУ ВО Первый МГМУ им. И. М. Сеченова МЗ РФ, Москва
*** ФГБОУ ВО РНИМУ им. Н. И. Пирогова МЗ РФ, Москва
«Диспепсия неуточненная»: дифференциальный диагноз, тактика ведения пациента на амбулаторном этапе/ Е. А. Лялюкова, В. Н. Дроздов, Е. Н. Карева, С. Ю. Сереброва, А. К. Стародубцев, Д. О. Кургузова
Для цитирования: Лечащий врач № 8/2018; Номера страниц в выпуске: 15-19
Теги: желудочно-кишечный тракт, боль в эпигастрии, диагностика




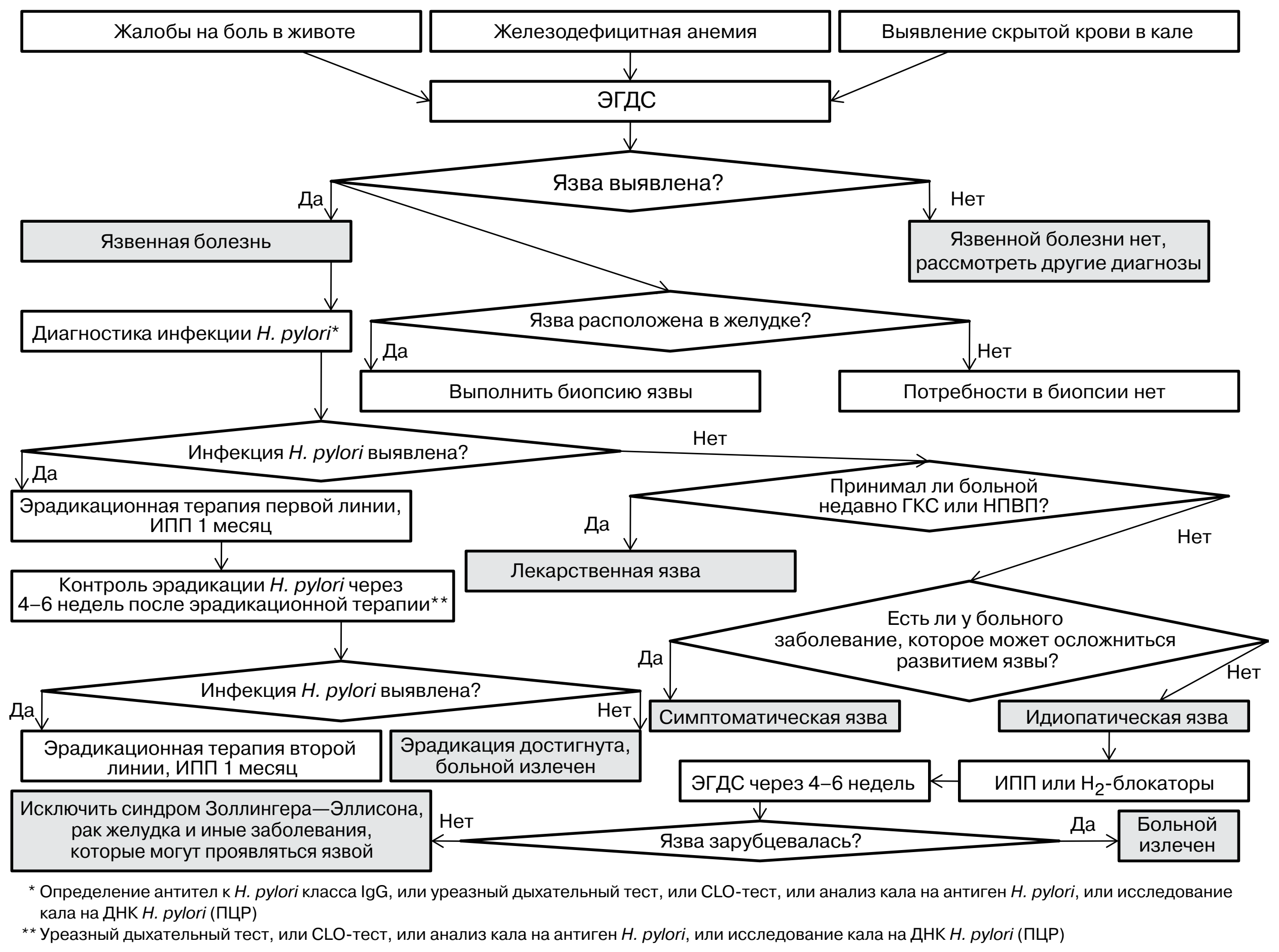






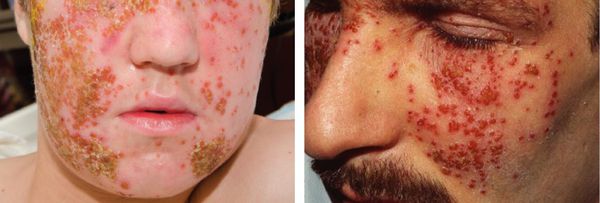
_575.gif)