сколько раз делится клетка в организме человека за жизнь
Теория предельного деления клеток
Клетки: особенности строения и деления
Клеточная теория является одной из основополагающих в современной биологии. Ее разработка стала неопровержимым доказательством единства всего живого на Земле.
Согласно клеточной теории, клетка это — структурно-функциональная элементарная единица строения, функционирования, размножения и развития всех живых организмов. Вне клетки нет жизни.
Все клеточные формы жизни на Земле можно разделить на две большие группы на основании структуры их строения.
Прокариоты (доядерные) — более простые по строению, которые возникли на ранних стадиях процесса эволюции.
Эукариоты (ядерные) — более сложные, которые возникли и развивались на более поздних стадиях процесса эволюции.
Клетки, составляющие тело человека, являются эукариотическими. По последним данным ученых в теле обычного человека насчитывается в среднем 37,2 триллиона клеток.
Справочно: группа ученых из Италии, Греции и Испании поставила себе задачу определить реальное количество клеток в человеческом организме. Они изучили все ранние научные труды в этой области за последние сто лет.
В результате обнаружили большой разброс в оценках данного показателя, который вирировался от 5 миллиардов до 200 триллионов клеток.
Поэтому авторам пришлось проделать скрупулезную работу, сделав отдельный подсчет клеток для каждого органа человеческого тела и для разных типов клеток организма.
Были посчитаны число и плотность клеток в сердце, легких, мозге, центральной нервной системе, кишечнике, желчном пузыре, костях, соединительных тканях, крови и многих других частях человеческого организма.
Просуммировав полученные результаты, ученые пришли к выводу, что в организме человека в среднем насчитывается 37.2 триллионов клеток.
В организме человека присутствует примерно 300 типов клеток, которые подразделяются на две большие группы:
• клетки, которые могут делиться и размножаться, то есть, они митотически компетентны;
• клетки, которые не делятся, их называют постмитотические. Это достигшие крайней стадии дифференцировки нейроны, кардиомиоциты, зернистые лейкоциты и другие.
Несмотря на многообразие форм, организация клеток всех живых организмов подчинена единым структурным принципам.
Большинство клеток человеческого организма постоянно делятся, на смену старым приходят новые. Благодаря этому процессу в течение жизни организм имеет возможность обновляться и восстанавливаться.
По подсчетам ученых, клетки человека за 70 лет жизни суммарно претерпевают порядка 1014 клеточных делений.*
Таким образом, каждая мышца, каждый орган, каждая функциональная система, человека в течение жизни несколько раз «молодеет», как бы рождаясь заново.
Наиболее распространённый способ репродукции эукариотических клеток человека, один из фундаментальных процессов онтогенеза это митоз – непрямое деление клетки.
Процесс размножения клеток называют пролиферацией. Размножение регулируется как самой клеткой (аутокринными ростовыми факторами), так и ее микроокружением (паракринными сигналами).
Активация пролиферации происходит через клеточную мембрану, в которой присутствуют рецепторы, воспринимающие митогенные сигналы. Это в основном ростовые факторы и межклеточные контактные сигналы.
Ростовые факторы обычно имеют белковую, пептидную природу (определенную последовательность соединения аминокислот). В настоящее время ученым известно около 100 таких факторов, в том числе:
• фактор роста тромбоцитов, который участвует в тромбообразовании и заживлении ран;
• эпителиальный фактор роста;
• фактор некроза опухолей;
• колониестимулирующие факторы;
• различные цитокины — интерлейкины и т.д.
Время существования клетки от деления до деления называется клеточным циклом.
После активации пролиферации клетка выходит из фазы покоя G0 и начинается клеточный цикл. Клеточный цикл может активироваться или инактивироваться.
В процессе активации могут участвовать киназы – ферменты катализаторы переноса фосфатной группы от молекулы аденозинтрифосфата (АТФ), обеспечивая включение клюкозы и гликогена в процесс гликолиза в живых клетках.
Инактивированиия регулируется за счет различных ингибиторов – веществ подавляющих или задерживающих течение физиологических и физико-химических, ферментативных процессов.
Молекулярные механизмы, приводящие к необратимой остановке клеточного цикла, контролируются генами-супрессорами.
Цель такой сложной организации процесса регуляции — обеспечить синтез ДНК с минимально возможным числом ошибок, чтобы и дочерние клетки имели абсолютно идентичный наследственный материал.
Проверка правильности копирования ДНК осуществляется в четырех «контрольных точках» клеточного цикла. Если обнаруживаются ошибки, то клеточный цикл останавливается, и включается репарация ДНК.
Если нарушения структуры ДНК удается исправить — клеточный цикл продолжается. Если нет — клетка может «покончить с собой» путем апоптоза, чтобы избежать вероятности превращения в раковую.
Супрессию клеточного цикла в фазе G1 осуществляет белок p53, действующий через ингибитор циклин-зависимой киназы р21.
Следует отметить, что в последние годы, пожалуй, ни один другой белок не изучался так интенсивно, как р53. За четверть века с момента открытия ему было посвящено более 40 тысяч научных работ, и их число неуклонно продолжает расти.
Очевидно, белок р53 не только получает сигналы о превышении некоторых пороговых величин в каждом из клеточных процессов, но и обеспечивает адекватные этим величинам ответы, обеспечивающие координированную коррекцию этих процессов, дальнейшее поведение и судьбу клеток.
Роль р53 в организме можно сравнить с ролью дирижера в оркестре – его функции осуществлять контроль за выполнением выработанных эволюцией программ, схем поведения клеток в разнообразных условиях.
Основная его биологическая роль заключается в обеспечении стабильности генома и генетической однородности клеток в целостном организме.
Контролирующая функция р53 заключается в предотвращении отклонений и связанных с ними патологий,
Транскрипционный фактор р53 активируется при повреждениях ДНК, и в этом случае его функция заключается в удалении из реплицирующихся клеток тех, которые являются потенциально онкогенными.
Не случайно ген р53 часто метафорически называют как «стражом генома», «ангелом-хранителем», «геном совести клетки».; Эти эпитеты наглядно отражают роль белка в предотвращении многих болезней.
Биологические пределы способности клетки к делению,
порог Хейфлика
Одна из современных гипотез старения организма носит название «клеточной смерти» или теории предельного деления клеток.
Эта теория, также как и свободно-радикальная теория рассматривает процесс старения на клеточном уровне.
Еще в 1957 г. знаменитый американский физик Лео Силард (1898-1964), изучавший влияние на клетки радиации, приводящей к прогерии — ускоренному старению, предположил, что в старости организм может быть еще вполне здоров, только количество клеток в каждой мышце, в каждом органе становится все меньше.
Развивая эту гипотезу, американский профессор анатомии медицинской школы Калифорнийского университета Леонард Хейфлик (20 мая 1928 г.) выдвинул гипотезу о том, что процесс старения связан с биологическим пределом способности клетки к делению.
В 1961 г., проводя серию экспериментов, ученый обнаружил определенные закономерности в процессах деления клеток.
Он предположил, что легочная ткань, по-видимому, отмирает после того, как ее клетки поделились определенное количество раз. Затем он экспериментально установил, что соматические (телесные) клетки могут делиться только ограниченное число раз.
Вероятно, в клетках существует своеобразный молекулярный счетчик. Он фиксирует, сколько делений уже сделано, и не дает клетке делиться сверх определенного генетически заданного предела.
Позднее, в 1969–1977 гг., проводя исследования человеческого эмбриона в Институте Уистара в Филадельфии, Хейфлик установил, что основная клеточная форма соединительной ткани организма, так называемые фибробласты клеток кожи делятся примерно 50 раз плюс-минус 10 раз, после чего процесс деления останавливается.
При этом у новорожденных клетки могут делиться 80–90 раз, а у стариков (70 лет и старше) только 20–30 раз.
Кроме того, в культуре ткани, т.е. вне организма, клетки человека могут делиться также не больше 50 раз, после чего погибают.
Усложнив эксперимент, ученый взял клеточные культуры, которые были заморожены после того, как клетки разделились 25 раз.
Оттаяв, эти клетки продолжили делиться, пока не достигли предела в 50 делений, а затем все же погибли.
Особо следует подчеркнуть, что когда клетки приближались к своему пределу деления, они начинали напоминать старую ткань с возрастными пигментами, которые обнаруживаются в постаревших клетках сердца и головного мозга.
Гибель клеток или ослабление функции в тех клетках, которые не подвержены делению, по окончании развития приводит к ослаблению организма.
В результате постепенно тело утрачивает способность к обновлению, а весь организм теряет возможность к восстановлению, что приводит к старению органов и систем.
Выявленные американским профессором закономерности предельного деления клеток в научной среде получили название «порог Хейфлика».
 masterok
masterok
Мастерок.жж.рф
Хочу все знать
Кратко и по простому это звучит так: Даже если человека минуют болезни и несчастные случаи, его клетки со временем перестанут делиться, будут разрушаться и в конце концов умрут. Это явление известно как предел Хейфлика. Исследования показывают, что в настоящее время максимальная продолжительность жизни составляет около 125 лет.
А вот более подробно на эту тему…
Леонард Хейфлик обнаружил границу числа делений соматических клеток, которая составляет примерно 50-52 деления.
«Есть два типа человеческих клеток: половые, то есть женская яйцеклетка и сперма мужчин, и соматические, включающие порядка сотни триллионов других клеток, составляющих остальное тело. Все клетки размножаются делением.
В 1961 году Леонард Хейфлик открыл, что у соматических клеток есть верхний предел общего числа делений, и число возможных делений уменьшается с возрастом клетки. Существует не одна теория, объясняющая, почему существует этот так называемый предел Хейфлика.
Принципиально, эксперимент проведённый Леонардом Хейфликом в коллаборации с Полом Мурхедом, был довольно простым: смешивали равные части нормальных мужских и женских фибробластов, различавшихся по количеству пройденных клеточных делений (мужские — 40 делений, женские — 10 делений) для того, чтобы фибробласты можно было отличить друг от друга в дальнейшем. Параллельно был поставлен контроль с мужскими 40-дневными фибробластами. Когда же контрольная несмешанная популяция мужских клеток перестала делиться, то смешанная опытная культура содержала только женские клетки, ведь все мужские клетки уже погибли[3]. На основании этого Хейфлик сделал вывод, что нормальные клетки имеют ограниченную способность к делению в отличие от раковых клеток, которые иммортальны[4]. Так было выдвинуто предположение, что так называемые «митотические часы» находятся внутри каждой клетки, на основании следующих наблюдений:
1. Нормальные фетальные фибробласты человека в культуре способны удваивать популяцию только ограниченное количество раз;
2. Клетки, которые подверглись криогенной обработке, «помнят», сколько раз они делились до заморозки.
В основе главной из них лежит накопление случайных повреждений гена при репликации клетки. При каждом клеточном делении действуют факторы среды, например, дым, радиация, химикаты, известные под названием свободных гидроксильных радикалов, и продукты распада клеток, которые мешают точному воспроизведению ДНК в следующем поколении клетки. В организме существует много ферментов восстановления ДНК, которые следят за процессом копирования и устраняют неполадки транскрипции по мере их возникновения, но все ошибки они отловить не в состоянии. При неоднократной репликации клетки повреждения ДНК накапливаются, приводя к неверному синтезу белков и неправильному функционированию. Эти ошибки функционирования являются, в свою очередь, причиной болезней, характерных для старения, например, артериосклероза, заболеваний сердца и злокачественных опухолей.
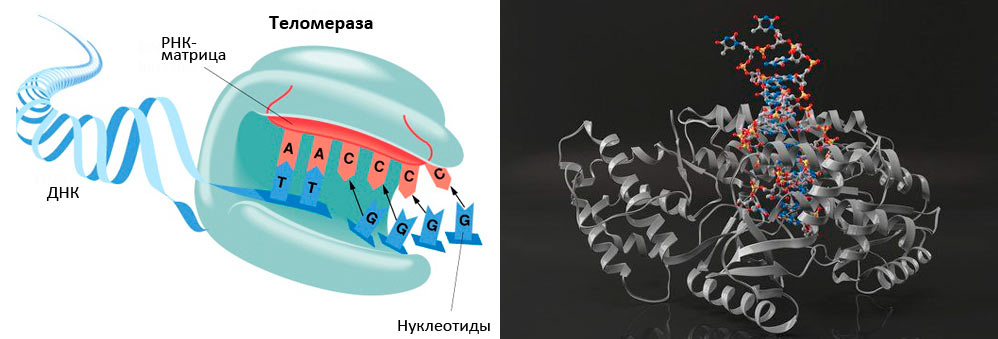
Ещё одна теория утверждает, что барьер Хейфлика связан с теломерами, то есть некодирующими участками ДНК, присоединенными к концу каждой хромосомы. Теломеры действуют как лидеры кинопленки, обеспечивая точную репликацию ДНК. В процессе деления клетки происходит расплетание двух нитей ДНК и создание новых полных копий этой молекулы в дочерних клетках. Но при каждом делении клетки теломеры становятся чуть короче, и в итоге они уже не в состоянии защитить концы нитей ДНК; тогда клетка, сочтя короткие теломеры за поврежденные ДНК, прекращает рост. У овечки Долли, клонированной из соматической клетки взрослого животного, оказались укороченные теломеры взрослого организма, а не теломеры новорождённого ягнёнка, и, возможно, она не проживёт столь же долго, сколь её нормально рожденные братья и сестры.
Есть три основных типа клеток, для которых не существует лимита Хейфлика: половые клетки, раковые клетки и некоторые типы стволовых клеток.
Причина, из-за которой эти клетки способны к бесконечному размножению, связана с наличием фермента теломеразы, впервые выделенного в 1989 году — этот фермент препятствует укорочению теломер. Вот что позволяет клеткам зародышевого пути продолжаться через поколения, и вот что лежит в основе взрывного роста раковых опухолей».
[ источники ]
источники
Фрэнсис Фукуяма, Наше постчеловеческое будущее: последствия биотехнологической революции, М., «Аст», 2004 г., с. 89-90.
Старение — плата за подавление раковых опухолей?
Старение — плата за подавление раковых опухолей?
Деление клетки. Клеточный цикл.
Автор
Редакторы
Статья на конкурс «био/мол/текст»: Уже более 50 лет прошло с тех пор, как на культуре фибробластов доказан феномен старения клеток, но существование старых клеток в организме долгое время подвергалось сомнению. Не было доказательств, что старение отдельных клеток играет важную роль в старении всего организма. В последние годы были открыты молекулярные механизмы старения клеток, их связь с онкологическими заболеваниями и воспалением. По современным представлениям, воспаление играет ведущую роль в генезе практически всех возраст-зависимых заболеваний, которые в конечном итоге приводят организм к смертельному исходу. Оказалось, что старые клетки, с одной стороны, выступают в качестве супрессоров опухолей (поскольку необратимо перестают делиться сами и снижают риск трансформации окружающих клеток), а с другой — специфический метаболизм старых клеток может вызывать воспаление и перерождение соседних предраковых клеток в злокачественные. В настоящее время проходят клинические испытания лекарственных препаратов, избирательно элиминирующих старые клетки в органах и тканях, тем самым предотвращая дегенеративные изменения органов и рак.
Конкурс «био/мол/текст»-2012
Эта статья представлена на конкурс научно-популярных работ «био/мол/текст»-2012 в номинации «Лучший обзор».
Спонсор конкурса — дальновидная компания Thermo Fisher Scientific.
В организме человека присутствует примерно 300 типов клеток, и все они делятся на две большие группы: одни могут делиться и размножаться (то есть, они митотически компетентны), а другие — постмитотические — не делятся: это достигшие крайней стадии дифференцировки нейроны, кардиомиоциты, зернистые лейкоциты и другие.
В нашем организме существуют обновляющиеся ткани, в которых есть пул постоянно делящихся клеток, которые заменяют отработанные или погибающие клетки. Такие клетки есть в криптах кишечника, в базальном слое эпителия кожи, в костном мозге (кроветворные клетки). Обновление клеток может происходить довольно интенсивно: так, клетки соединительной ткани в поджелудочной железе заменяются каждые 24 часа, клетки слизистой желудка — каждые три дня, лейкоциты — каждые 10 дней, клетки кожи — каждые шесть недель, примерно 70 г пролиферирующих клеток тонкого кишечника удаляется из организма ежедневно [1].
Стволовые клетки, существующие практически во всех органах и тканях, способны делиться неограниченно. Регенерация тканей происходит за счет пролиферации стволовых клеток, которые могут не только делиться, но и дифференцироваться в клетки той ткани, регенерация которой происходит. Стволовые клетки есть в миокарде, в головном мозге (в гипокампе и в обонятельных луковицах) и в других тканях. Это открывает большие надежды в плане лечения нейродегенеративных заболеваний и инфаркта миокарда [2–4].
Постоянно обновляющиеся ткани способствуют увеличению продолжительности жизни. При делении клеток происходит омоложение тканей: новые клетки приходят на место поврежденных, при этом интенсивнее происходит репарация (устранение повреждений ДНК) и возможна регенерация при повреждении тканей. Не удивительно, что у позвоночных значительно выше продолжительность жизни, чем у беспозвоночных — тех же насекомых, у которых во взрослом состоянии клетки не делятся.
Стоит, в прочем, помнить, что мутация мутации рознь, и согласно новейшим геномным исследованиям в каждом поколении человек приобретает около 60 новых мутаций (которых не было в ДНК у его родителей). Очевидно, что большая часть из них вполне нейтральная (см. «Перевалило за тысячу: третья фаза геномики человека»). — Ред.
В целях защиты от самого себя, в организме сформировались специальные клеточные механизмы супрессии опухолей. Один из них — репликативное старение клеток (сенесценция), заключающееся в необратимой остановке деления клетки в стадии G1 клеточного цикла. При старении клетка перестает делиться: она не реагирует на ростовые факторы и становится устойчивой к апоптозу.
Лимит Хейфлика
Эта концепция считалась неопровержимой во многом благодаря экспериментам Карреля, который поддерживал культуру клеток сердца цыпленка 34 года (ее выбросили лишь после его смерти). Однако, как выяснилось впоследствии, бессмертие культуры Карреля было артефактом, поскольку вместе с эмбриональной сывороткой, которая добавлялась в культуральную среду для роста клеток, туда попадали и сами эмбриональные клетки (и, скорее всего, культура Карреля стала уже далеко не тем, чем была в начале).
О захватывающей истории бессмертия Генриетты Лакс см. в статье «Бессмертные клетки Генриетты Лакс», а также «Наследники клеток HeLa». — Ред.
Как выяснилось, лимит Хейфлика зависит от возраста: чем старше человек, тем меньшее число раз удваиваются его клетки в культуре. Интересно, что замороженные клетки при разморозке и последующем культивировании как будто помнят число делений до замораживания. Фактически, внутри клетки существует «счетчик делений», и по достижении определенного предела (лимита Хейфлика) клетка перестает делиться — становится сенесцентной. Сенесцентные (старые) клетки имеют специфическую морфологию — они крупные, уплощенные, с большими ядрами, сильно вакуолизированы, у них меняется профиль экспрессии генов. В большинстве случаев они устойчивы к апоптозу.
Однако старение организма нельзя свести только к старению клеток. Это значительно более сложный процесс. Старые клетки есть и в молодом организме, но их мало! Когда же с возрастом сенесцентные клетки накапливаются в тканях, начинаются дегенеративные процессы, которые приводят к возраст-зависимым заболеваниям. Один из факторов этих заболеваний — так называемое старческое «стерильное» воспаление, которое связано с экспрессией провоспалительных цитокинов старыми клетками.
Еще один важный фактор биологического старения — строение хромосом и их кончиков — теломеров.
Теломерная теория старения
Рисунок 1. Теломеры — концевые участки хромосом. Поскольку хромосом у человека 23 пары (то есть, 46 штук), теломер получается 92.
В 1971 году наш соотечественник Алексей Матвеевич Оловников предположил, что лимит Хейфлика связан с «недорепликацией» концевых участков линейных хромосом (они имеют специальное название — теломеры). Дело в том, что в каждом цикле деления клетки теломеры укорачиваются из-за неспособности ДНК-полимеразы синтезировать копию ДНК с самого кончика [8], [9]. Кроме того, Оловников предсказал существование теломеразы (фермента, добавляющего повторяющиеся последовательности ДНК на концы хромосом), исходя из того факта, что иначе в активно делящихся клетках ДНК быстро бы «съелась», и генетический материал был бы утерян. (Проблема в том, что активность теломеразы угасает в большинстве дифференцированных клеток.)
Теломеры (рис. 1) играют важную роль: они стабилизируют кончики хромосом, которые иначе, как говорят цитогенетики, стали бы «липкими», т.е. подверженными разнообразным хромосомным аберрациям, что приводит к деградации генетического материала. Теломеры состоят из повторяющихся (1000–2000 раз) последовательностей (5′—TTAGGG—3′), что в сумме дает 10–15 тысяч нуклеотидных пар на каждый хромосомный кончик. На 3′-конце теломеры имеют довольно длинный однонитевой участок ДНК (150–200 нуклеотидов), участвующий в образовании петли по типу лассо [10], [11] (рис. 2). С теломерами связано несколько белков, образующих защитный «колпачок» — этот комплекс называется шелтерином (рис. 3). Шелтерин предохраняет теломеры от действия нуклеаз и слипания и, видимо, именно он сохраняет целостность хромосомы.
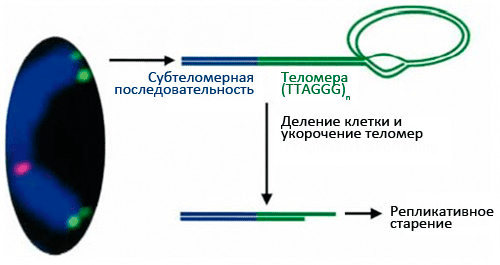
Рисунок 2. Состав и структура теломер. Многократное деление клетки в случае отсутствия активности теломеразы ведет к укорочению теломер и репликативному старению.
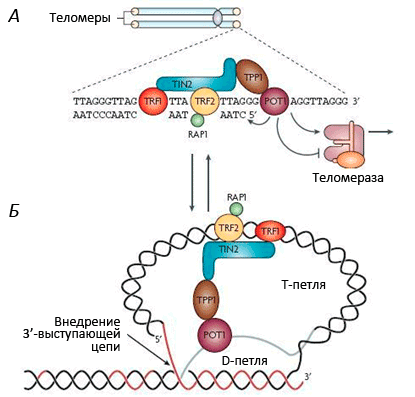
Рисунок 3. Строение теломерного комплекса (шелтерина). Теломеры находятся на концах хромосом и состоят из тандемных повторов TTAGGG, которые заканчиваются 32-членным выступающим одноцепочечным фрагментом. С теломерной ДНК связан шелтерин — комплекс из шести белков: TRF1, TRF2, RAP1, TIN2, TPP1 и POT1.
Незащищенные концы хромосом воспринимаются клеткой как повреждение генетического материала, что активирует репарацию ДНК. Теломерный комплекс вместе с шелтерином «стабилизирует» хромосомные кончики, защищая всю хромосому от разрушения. В сенесцентных клетках критическое укорочение теломер нарушает эту защитную функцию [12], [13], в связи с чем начинают формироваться хромосомные аберрации, которые часто приводят к малигнизации. Чтобы этого не произошло, специальные молекулярные механизмы блокируют клеточное деление, и клетка переходит в состояние сенесцентности — необратимой остановки клеточного цикла. При этом клетка гарантированно не может размножаться, а значит, не сможет и сформировать опухоль. В клетках с нарушенной способностью к сенесценции (которые размножаются, несмотря на дисфункцию теломер), образуются хромосомные аберрации.
Длина теломер и скорость их укорочения зависит от возраста. У человека длина теломер варьирует от 15 тысяч нуклеотидных пар (т.н.п.) при рождении до 5 т.н.п. при хронических заболеваниях. Длина теломер максимальна у 18-месячных детей, а затем она быстро снижается до 12 т.н.п. к пятилетнему возрасту. После этого скорость укорачивания снижается [14].
Теломеры укорачиваются у разных людей с разной скоростью. Так, на эту скорость сильно влияют стрессы. Э. Блекберн (лауреат Нобелевской премии по физиологии и медицине 2009 г.) установлено, что женщины, постоянно испытывающие стресс (например, матери хронически больных детей), имеют значительно более короткие теломеры по сравнению со сверстницами (примерно на десять лет!). Лабораторией Э. Блекберн разработан коммерческий тест для определения «биологического возраста» людей на основании длины теломер.
Любопытно, что у мышей очень длинные теломеры (50–40 т.н.п., по сравнению с 10–15 т.н.п. у человека). У некоторых линий лабораторных мышей длина теломер достигает 150 т.н.п. Более того, у мышей теломераза всегда активна, что не дает теломерам укорачиваться. Однако это, как всем известно, не делает мышей бессмертными. Мало того: у них опухоли развиваются намного чаще, чем у людей, что позволяет предположить, что укорачивание теломер как механизм защиты от опухолей у мышей не работает [15].
При сравнении длины теломер и теломеразной активности у разных млекопитающих оказалось, что виды, для которых характерно репликативное старение клеток, имеют большую продолжительность жизни и большой вес. Это, например, киты, продолжительность жизни которых может достигать 200 лет. Таким организмам репликативное старение просто необходимо, поскольку слишком большое число делений порождает множество мутаций, с которыми необходимо как-то бороться. Предположительно, репликативное старение и есть такой механизм борьбы, который сопровождается к тому же репрессией теломеразы [16].
Старение диференцированных клеток происходит иначе. Стареют и нейроны, и кардиомиоциты, а ведь они не делятся! Например, в них накапливается липофусцин — старческий пигмент, который нарушает функционирование клеток и запускает апоптоз. В клетках печени и селезенки с возрастом накапливается жир.
Связь репликативного старения клеток со старением организма, строго говоря, не доказана, но возрастная патология сопровождается и старением клеток (рис. 4). Злокачественные новообразования пожилого возраста в большинстве своем связаны с обновляемыми тканями. Онкологические заболевания в развитых странах — одна из основных причин заболеваемости и смертности, причем независимым фактором риска раковых заболеваний является просто. возраст. Число смертей от опухолевых заболеваний увеличивается с возрастом по экспоненте, так же как и общая смертность. Это говорит нам, что между старением и канцерогенезом существует фундаментальная связь.
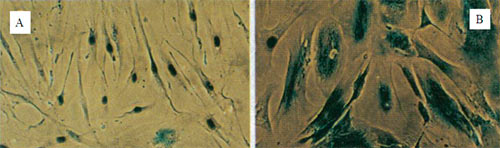
Рисунок 4. Гистохимически окрашенные на наличие β-галактозидазной активности фибробласты человека линии WI-38. A — молодые; B — старые (сенесцентные).
Теломераза — фермент, который был предсказан
В организме должен существовать механизм, компенсирующий укорочение теломер, — такое предположение сделал А.М. Оловников. Действительно, в 1984 г. такой фермент был открыт Кэрол Грейдер и назван теломеразой. Теломераза (рис. 5) — это обратная транскриптаза, которая увеличивает длину теломер, компенсируя их недорепликацию. В 2009 году Э. Блэкберн, К. Грэйдер и Д. Шостак за открытие этого фермента и цикл работ по изучению теломер и теломеразы была присуждена Нобелевская премия (см: «„Нестареющая“ Нобелевская премия: в 2009 году отмечены работы по теломерам и теломеразе»).
Рисунок 5. Теломераза содержит каталитический компонент (обратную транскриптазу ТERT), теломеразную РНК (hTR или TERC), содержащую две копии теломерного повтора и являющуюся матрицей для синтеза теломеров, и белок дискерин.
По данным Э. Блекберн, теломераза участвует в регуляции активности примерно 70 генов. Теломераза активна в зародышевых и эмбриональных тканях, в стволовых и пролиферирующих клетках. Ее обнаруживают в 90% раковых опухолей, что обеспечивает неудержимое размножение раковых клеток. В настоящее время среди препаратов, которые используют для лечения рака, есть и ингибитор теломеразы. Но в большинстве соматических клеток взрослого организма теломераза не активна.
В состояние сенесценции клетку могут привести многие стимулы — дисфункция теломер, повреждения ДНК, причиной которых могут быть мутагенные воздействия окружающей среды, эндогенные процессы, сильные митогенные сигналы (сверхэкспрессия онкогенов Ras, Raf, Mek, Mos, E2F-1 и др.), нарушения хроматина, стрессы и др. Фактически, клетки перестают делиться — становятся сенесцентными — в ответ на потенциально вызывающие рак события.
Страж генома
Дисфункция теломер, которая происходит при их укорачивании либо нарушении работы шелтерина, активирует белок р53. Этот транскрипционный фактор приводит клетку в состояние сенесценции, либо вызывает апоптоз. При отсутствии р53 развивается нестабильность хромосом, характерная для карцином человека. Мутации в белке р53 обнаруживаются в 50% аденокарцином груди и в 40–60% случаев колоректальной аденокарциномы. Поэтому p53 зачастую называют «стражем генома».
Теломераза реактивируется в большинстве опухолей эпителиального происхождения, которые характерны для пожилых людей. Считается, что реактивация теломеразы — важный этап злокачественных процессов, поскольку это позволяет раковым клеткам «не обращать внимания» на лимит Хейфлика. Дисфункция теломер способствует хромосомным слияниям и аберрациям, что в отсутствии p53 чаще всего приводит к злокачественным новообразованиям.
О молекулярных механизмах старения клеток
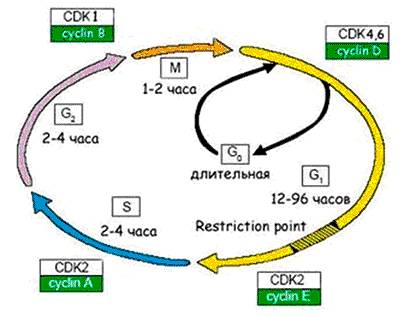
Рисунок 6. Схема клеточного цикла. Клеточный цикл подразделяют на четыре стадии: 1. G1 (предсинтетическая) — период, когда клетка готовится к репликации ДНК. В этой стадии может произойти остановка клеточного цикла в случае обнаружения повреждений ДНК (на время репарации). Если обнаруживаются ошибки в репликации ДНК, и они не могут быть исправлены репарацией, клетка не переходит на стадию S. 2. S (cинтетическая) — когда происходит репликация ДНК. 3. G2 (постсинтетическая) — подготовка клетки к митозу, когда происходит проверка точности репликации ДНК; если обнаружены недореплицированные фрагменты или другие нарушения в синтезе, переход на следующую стадию (митоз) не происходит. 4. М (митоз) — формирование клеточного веретена, сегрегация (расхождение хромосом) и формирование двух дочерних клеток (собственно деление).
Чтобы были понятны молекулярные механизмы перехода клетки в состояние сенесцентности, я напомню вам, как происходит деление клетки.
Процесс размножения клеток называют пролиферацией. Время существования клетки от деления до деления именуют клеточным циклом. Процесс пролиферации регулируется как самой клеткой — аутокринными ростовыми факторами, — так и ее микроокружением — паракринными сигналами.
Активация пролиферации происходит через клеточную мембрану, в которой присутствуют рецепторы, воспринимающие митогенные сигналы — это в основном ростовые факторы и межклеточные контактные сигналы. Ростовые факторы обычно имеют пептидную природу (к настоящему времени их известно около 100). Это, например, фактор роста тромбоцитов, который участвует в тромбообразовании и заживлении ран, эпителиальный фактор роста, различные цитокины — интерлейкины, фактор некроза опухолей, колониестимулирующие факторы и т.д. После активации пролиферации клетка выходит из фазы покоя G0 и начинается клеточный цикл [19] (рис. 6).
Клеточный цикл регулируется циклин-зависимыми киназами, разными для каждой стадии клеточного цикла. Они активируются циклинами и инактивируются рядом ингибиторов. Цель такой сложной регуляции — обеспечить синтез ДНК с как можно меньшим числом ошибок, чтобы и дочерние клетки имели абсолютно идентичный наследственный материал. Проверка правильности копирования ДНК осуществляется в четырех «контрольных точках» цикла: если обнаруживаются ошибки, то клеточный цикл останавливается, и включается репарация ДНК. Если нарушения структуры ДНК удается исправить — клеточный цикл продолжается. Если нет — клетке лучше «покончить с собой» (путем апоптоза), чтобы избежать вероятности превращения в раковую.
Молекулярные механизмы, приводящие к необратимой остановке клеточного цикла, контролируются генами-супрессорами опухолей, среди которых p53 и pRB, связанные с ингибиторами циклин-зависимых киназ. Супрессию клеточного цикла в фазе G1 осуществляет белок p53, действующий через ингибитор циклин-зависимой киназы р21. Транскрипционный фактор р53 активируется при повреждениях ДНК, и функция его заключается в удалении из пула реплицирующихся клеток тех, которые являются потенциально онкогенными (отсюда и прозвище р53 — «страж генома»). Данное представление подтверждается тем фактом, что мутации р53 обнаруживают в
50% случаев злокачественных опохолей. Другое проявление активности р53 связано с апоптозом наиболее поврежденных клеток.
Сенесценция клеток и возраст-зависимые заболевания
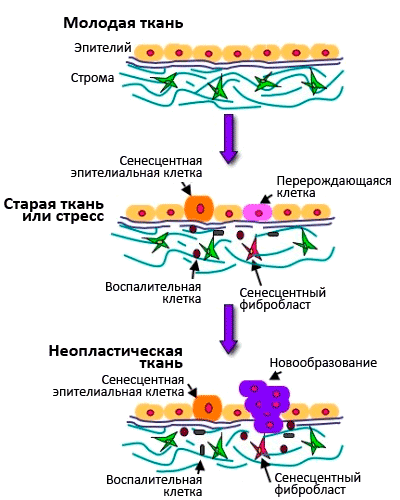
Рисунок 7. Взаимосвязь между старением клеток и старением организма.
Сенесцентные клетки накапливаются с возрастом и способствуют возрастным заболеваниям. Они снижают пролиферативный потенциал ткани и истощают пул стволовых клеток, что приводит к дегенеративным нарушениям ткани и снижает способность к регенерации и обновлению.
Сенесцентные клетки характеризуются специфической экспрессией генов: они секретируют воспалительные цитокины и металлопротеиназы, разрушающие межклеточный матрикс. Получается, что старые клетки обеспечивают вялотекущее старческое воспаление, а накопление старых фибробластов в коже служит причиной возрастного снижения способности к заживлению ран (рис. 7). Старые клетки также стимулируют пролиферацию и малигнизацию близлежащих предраковых клеток, благодаря секреции эпителиального фактора роста [20].
Сенесцентные клетки накапливаются во многих тканях человека, присутствуют в атеросклеротических бляшках, в язвах кожи, в пораженных артритом суставах, а также в доброкачественных и пренеопластических гиперпролиферативных поражениях простаты и печени. При облучении раковых опухолей некоторые клетки также переходят в состояние сенесценции, тем самым обеспечивая рецидивы заболевания.
Таким образом, клеточное старение демонстрирует эффект отрицательной плейотропии, суть которого состоит в том, что хорошее для молодого организма, может стать плохим для старого. Самый яркий пример — процессы воспаления. Выраженная реакция воспаления способствует быстрому выздоровлению молодого организма при инфекционных заболеваниях. В пожилом же возрасте активные воспалительные процессы приводят к возрастным заболеваниям. Сейчас принято считать, что воспаление играет определяющую роль практически при всех возраст-зависимых заболеваниях, начиная с нейродегенеративных.
Получается парадокс: старение клеток в молодом организме предохраняет от рака, а в старом — способствует ему! В настоящее время в США в клинике Майо ведутся исследования влияния «ликвидации» старых клеток из организма. На животных получены обнадеживающие результаты об увеличении продолжительности жизни и замедлении клинических проявлений возраст-зависимых заболеваний, если из тканей старых животных селективно устранять сенесцентные клетки — хороших граждан, но плохих соседей.
 masterok
masterok