Псв что это в медицине
Что такое ПСВ, ОФВ1, с какой целью их определяют при бронхиальной астме?
ПСВ — это при бронхиальной астме один из главных методов контроля за заболеванием, расшифровывается как «пиковая скорость выдоха» и измеряется пикфлоуметром. Это очень важный показатель, необходимый для полноценного мониторинга. Для получения картины заболевания в целом надо регулярно делать 2 основных исследования.
Главные обследования в диагностике и лечении бронхиальной астмы
Спирометрия используется для взрослых и детей старше 5 лет и определяет ОФВ1 (объем форсированного выдоха за первую секунду) и ФЖЕЛ (форсированную жизненную емкость легких). Обычно проводится с применением бронхолитика быстрого действия. При проведении процедуры сначала измеряется ОФВ1 и ФЖЕЛ без применения лекарства, затем пациент вдыхает бронхолитик (например, Сальбутамол или Беротек) и примерно через 20-25 мин проводится повторная процедура спирометрии, которая позволяет узнать, насколько улучшились показатели ОФВ1 и ФЖЕЛ.
Эти показатели зависят от многих факторов, в том числе от возраста, пола и веса пациента, и могут разниться. По результатам спирометрии оценивают соотношение двух показателей (это называется индекс Тиффно — ИТ). В норме у взрослого человека ИТ должен превышать 0,80, а у детей — 0,90. Если есть понижение этого показателя, то можно говорить об обструкции, характерной для бронхитов или бронхиальной астмы.
Спирометрия проводится исключительно в больнице специалистом, перед началом врач подробно инструктирует пациента о том, как и когда надо дышать и выдыхать. Нос во время процедуры зажимается специальным зажимом, что может вызвать определенный дискомфорт у ребенка, потому перед тем, как вести его на спирометрию, родителям следует рассказать ребенку о том, что будет происходить в кабинете у врача, чтобы он не испугался, в противном случае процедура не сможет быть проведена. По окончании пациенту на руки выдается заключение с графиками.
Пикфлоуметрия — еще один метод обследования и контроля за течением бронхиальной астмы. В отличие от спирометрии, она может проводиться как в кабинете доктора, так и дома самостоятельно. Всем больным бронхиальной астмой врачи настоятельно рекомендуют приобрести пикфлоуметр и вести дневник пикфлоуметрии, чтобы регулярно замерять ПСВ.
ПСВ при бронхиальной астме необходимо знать для того, чтобы оценивать состояние больного и эффективность проводимой терапии.
Пикфлоуметр и правила его применения
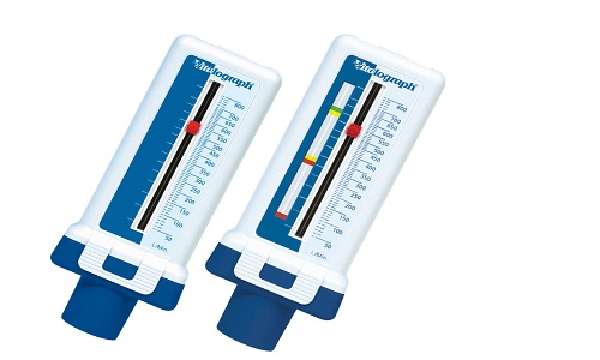
Пикфлоуметр — небольшой портативный и относительно недорогой прибор, который можно приобрести в аптеке. У каждого больного бронхиальной астмой должен быть персональный прибор. Его необходимо содержать в чистоте и нежелательно давать в пользование другим людям.
Для того чтобы замерить ПСВ, следует полностью выдохнуть, затем сделать глубокий вдох и, плотно обхватив губами мундштук, резко выдохнуть в пикфлоуметр. При этом прибор держать надо ровно горизонтально, пальцами не перекрывая шкалы. После каждого замера указатель ставить на начальную отметку. Процедуру по возможности проводят стоя. Замеры следует делать утром и вечером до приема противоастматических препаратов, выдыхать — 3 раза, записывать наилучший результат в график пикфлоуметрии, который можно взять у врача или сделать самостоятельно, нарисовав систему координат на миллиметровой бумаге. Так можно будет отследить снижение ПСВ, что будет говорить о недейственной терапии.
При сильном понижении результата выдоха следует немедленно обратиться к врачу для лечения. На каждый прием пульмонолога больной должен приносить график пикфлоуметрии, чтобы специалист мог оценить ПСВ и понять, помогают или нет пациенту подобранные лекарственные препараты.
При правильном контроле за бронхиальной астмой график ПСВ близок к прямой линии, а вот если он резко скачет то вверх, то вниз, это уже может говорить о том, что терапия не помогает, контроль следует улучшить путем подбора других медикаментозных средств или увеличения дозы.
Нормы ПСВ и зоны пикфлоуметрии
Для каждого пациента существует своя индивидуальная норма ПСВ, которую можно узнать у лечащего пульмонолога или рассчитать самостоятельно.
Для удобства врачей и пациентов была разработана систем трех цветовых зон результатов пикфлоуметрии.
Зеленая зона: лучший показатель ПСВ вне обострений следует умножить на 0,8 — это будет тем минимумом, являющимся нижней границей зеленой зоны. Если все значения выше этой цифры находятся в зеленой зоне, это значит, что терапия проходит успешно и поводов для беспокойства нет.
Желтая зона: здесь лучший показатель умножается на коэффициент 0,6, таким образом определяется нижняя граница желтой зоны. Если результаты пикфлоуметрии находятся в этой зоне, уже стоит прислушаться к организму: может появляться небольшая одышкаа, нарушения сна, затруднения в элементарных физических упражнениях. В этом случае необходимо обратиться к врачу, чтобы он либо назначил дополнительные медицинские препараты, либо увеличил дозу уже используемых. Не стоит игнорировать желтую зону — это может привести к развитию приступа и резкому и сильному обострению заболевания.
Красная зона — это все показатели, находящиеся после нижней границы желтой зоны. Это та зона, при которой появляется одышкаа и сильный кашель в состоянии покоя, становится очень трудно дышать, в груди появляется свист и сипы. Здесь, во-первых, необходим прием экстренных препаратов для быстрого купирования приступа, а во-вторых — срочное обращение к врачу для пересмотра лечебной терапии. Понижение показателей до этой зоны игнорировать ни в коем случае нельзя — это большая угроза для жизни.
Бронхиальная астма — заболевание, безусловно, тяжелое и неприятное, однако при правильном подходе к ее лечению как врача, так и самого пациента, она может протекать практически бессимптомно, не мешая человеку вести нормальную полноценную жизнь.
Роль пикфлоуметрии и самоконтроля при лечении этого заболевания очень важна, ведь таким образом человек может самостоятельно оценивать свое состояние и вовремя обращаться за врачебной помощью.
Пикфлоуметрия
Что такое пикфлоуметр?
Это небольшого размера трубочка с градуированной шкалой, измеряющая максимальную скорость воздушного потока при выдохе.
Сама манипуляция получила название пикфлоуметрия.
Что такое пикфлоуметрия и для чего она нужна?
У многих пациентов, страдающих хроническими не легочными заболеваниями есть аппаратура, которая помогает им контролировать определенные показатели (частоту пульса, давление, уровень сахара крови), В зависимости от их значений человек может контролировать свое лечение. Люди, у которых повышается давление, всегда имеют дома тонометр, болеющие сахарным диабетом — глюкометр. А что делать человеку, страдающему бронхиальной астмой? Как он может контролировать свое состояние. Можно, конечно, опираться на собственные ощущения, но это не надежно. Учащение приступов затрудненного дыхание, усиление кашля, нарастание одышки. Все эти признаки обострения бронхиальной астмы человек начинает отмечать, когда обострение в полном разгаре и его лечение требует больших усилий и значительного увеличения доз препаратов.
Выход есть. Для людей страдающих бронхиальной астмой изобретен простейший прибор, помогающий контролировать состояние бронхов и вовремя принять необходимые меры. Это значит — раньше начать лечение с меньшими дозами лекарственных препаратов, и предотвратить развитие тяжелого обострения. Это и есть, та самая градуированная трубочка, о которой мы говорили, и которая называется пикфлоуметр.
Пикфлоуметр показывает наибольшую скорость, с которой воздух может проходить через дыхательные пути при максимально резком выдохе. Значит, он позволяет оценить степень сужения бронхов и степень их расширения при приеме лекарственных препаратов.
Пикфлоуметрия-это метод самоконтроля за течением бронхиальной астмы.
Как правильно проводится пикфлоуметрия?
Проводится пикфлоуметриядва раза в день: утром сразу после подъёма с постели до приема препаратов и вечером пред сном.
Как следует оценивать результаты пикфлоуметрии?
Норма показателей выдоха расчитывается индивидуально с учетом пола, возраста и роста.
Для простоты оценки пиковой скорости выдоха (ПСВ) используется принцип «Светофора», когда значения показаний делятся на зоны, которые соответствуют цветам светофора: зеленая, желтая и красная.
Зеленая зона. Показатель нормы. Она сигнализирует, что астма находится под контролем. Нет выраженных симптомов астмы, больной физически активен, не имеет проблем со сном и может принимать лекарства, как обычно. Показатели ПВС в зеленой зоне составляют от 80% до 100% от Ваших лучших значений.
Желтая зона. Показатель начинающегося обострения. При этом данные пикфлоуметрии находятся в интервале от 50% до 80% от Ваших лучших значений ПСВ. Скорее всего, у Вас могут наблюдаться приступы затрудненного дыхания, кашель, свистящие хрипы, требующие дополнительно приема ингаляторов или назначения иных препаратов. Обязательно обратитесь к Вашему врачу.
Красная зона. Это — сигнал тревоги. В красной зоне показатели ПСВ находятся в интервале ниже 50% от Ваших лучших значений. Вероятнее всего начинается тяжелое обострение заболевания. Немедленно обратитесь к врачу.
Если Вы постоянно наблюдаетесь у пульмонолога, то чаще всего врач заранее объясняет, что надо сделать при переходе показателей пикфлоуметрии в желтую или красную зону, говорит дозу каких ингаляторов надо увеличить или что прибавить к проводимой терапии.
Как рассчитать нормальные показатели скорости выдоха?
Лучшие значения показателей скорости выдоха рассчитываются при отсутствии симптомов астмы на том же пикфлоумерте, которым Вы постоянно пользуетесь. Самый лучший показатель пикфлоуметрии нужно умножить на 0,8. Например, если у Вас лучшее значение пикфлоуметрии — 400, Вам необходимо 400 умножить на 0,8, результат 320. Любое значение выше 320 будет относиться к зеленой зоне, что означает — нормальный уровень проходимости бронхов. Для определения границ желтой зоны Вам необходимо умножить Ваш лучший показатель (например 400) на 0,5, полученный результат (200) будет нижней границей желтой зоны, а верхнюю границу мы уже знаем (ранее подсчитанное значение), т. е. желтая зона в нашем примере будет находится между 200 и 320 л/мин. Все показатели ниже 200 будут относиться к красной зоне.
Что такое бронхиальная астма? Причины возникновения, диагностику и методы лечения разберем в статье доктора Сергеева А. Л., аллерголога со стажем в 15 лет.
Определение болезни. Причины заболевания
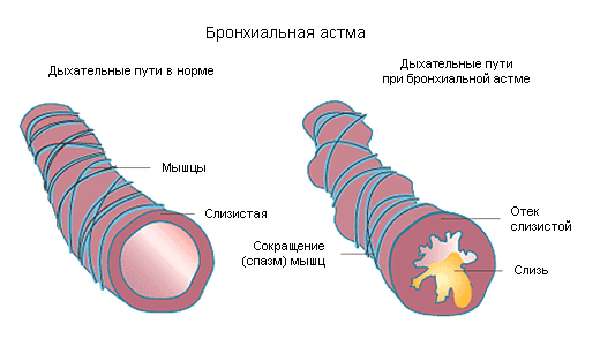
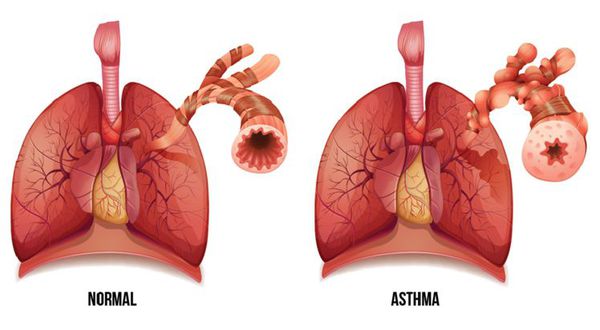
Бронхиальная астма (БА) — это заболевание, характерным проявлением которого является хроническое воспаление дыхательных путей, респираторные симптомы (свистящие хрипы, одышка, заложенность в груди и кашель), которые варьируют по времени и интенсивности и проявляются вместе с вариабельной обструкцией дыхательных путей. [1]
БА занимает лидирующую позицию по распространенности среди населения. Если верить статистике, за 15 лет зафиксировано удвоение количества заболевших этой патологией.
На появление и развитие БА влияет ряд причин. Среди них: бытовые аллергены, условия труда, генетические причины и других факторы.
Бытовые аллергены
Условия труда
Согласно эпидемиологическим исследованиям, удельный вес бронхиальной астмы, возникающей под влиянием неблагоприятных факторов производственной среды, составляет от 2 до 15 %. Существует множество веществ, которые приводят к развитию профессиональной астмы. Среди них: фталаты, альдегиды, изоцианаты, металлы, зерновая и мучная пыль, флюсы, эпихлоргидрин, формальдегид, аллергены животных, смолы и древесная пыль, клеи, латекс.
Перечень профессий, у представителей которых чаще всего развивается профессиональная астма:
Генетические причины
К другим предрасполагающим факторам относятся:
Симптомы бронхиальной астмы
Характерные симптомы бронхиальной астмы:
Признаки бронхиальной астмы изменчивы по тяжести, частоте появления и зависят от контакта с различными аллергенами и другими триггерными факторами. Зависят они и от подобранного противоастматического лечения, количества и тяжести сопутствующих заболеваний. Чаще всего симптомы БА беспокоят в ночное время или в ранние утренние часы, а также после физических усилий, что приводит к снижению физической активности больных. Воспалительные изменения в бронхиальном дереве и гиперреактивность дыхательных путей выступают основными патофизиологическими признаками БА. [5]
Механизмы, вызывающие основные симптомы БА [5]
| Симптом | Механизм |
|---|---|
| Кашель | Раздражение рецепторов бронхов, сокращение гладкой мускулатуры бронхов |
| Свистящее дыхание | Бронхообструкция |
| Заложенность в груди | Констрикция мелких дыхательных путей, воздушные ловушки |
| Одышка | Стимулированная работа дыхания |
| Ночные симптомы | Воспалительный процесс, гиперреактивность бронхов |
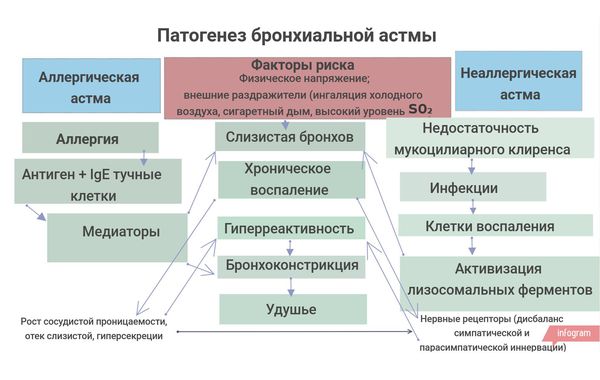
Патогенез бронхиальной астмы
Патогенез бронхиальной астмы можно наглядно представить в виде схемы:
Классификация и стадии развития бронхиальной астмы
Сегодня есть огромное количество классификаций БА. Ниже представлены основные, они помогают в понимании причин и необходимы для статистики. Кроме того, приведен современный подход в рассмотрении проблемы астмы, как выделение фенотипов астмы. [1] [6]
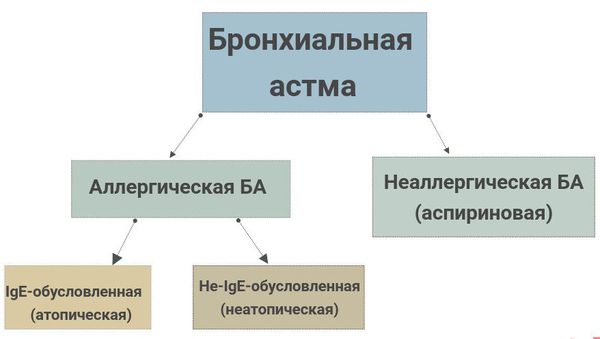
В России используется следующая классификация БА:
Классификация БА (МКБ-10)
| J45, J45.0 Астма с преобладанием аллергического компонента |
| аллергическая экзогенная |
| атопическая |
| Бронхит аллергический без доп. уточнений |
| Ринит аллергический с астмой |
| Сенная лихорадка с астмой |
| J45.1 Астма неаллергическая |
| идиосинкратическая |
| эндогенная неаллергическая |
| J45.8 Астма сочетанная |
| ассоциация с состояниями, упомянутыми в J45.0, J45.1 |
| J45.9 Астма без уточнения |
| астма поздно начавшаяся |
| астматический бронхит без доп. уточнений |
| J46 Астматический статус |
| астма тяжелая острая |
Приоритетное внимание сейчас уделяется персонализированной медицине, которая на данный момент не имеет возможности создания индивидуального лекарственного препарата и способов обследования или предупреждения развития заболевания для конкретного больного, но предложено выделять отдельные категории. Эти подгруппы больных называют фенотипами БА, характеризующимися особенностями в причинах, развитии, методах обследования и терапии. [1] [8]
На данный момент существуют следующие фенотипические формы БА:
Осложнения бронхиальной астмы
Если вовремя не поставить диагноз бронхиальной астмы и не подобрать терапию, которая позволит контролировать течение болезни, могут развиться осложнения:
Диагностика бронхиальной астмы
Бронхиальная астма представляет собой клинический диагноз, который устанавливает врач, учитывая жалобы, анамнестические особенности пациента, функциональные методы диагностики с учетом степени обратимости обструкции бронхов, специального обследования на наличие аллергопатологии и дифференциальной диагностики с прочими болезнями со схожими жалобами. Дебют развития заболевания чаще всего происходит в возрасте от 6 лет, реже после 12 лет. Но появление возможно и в более позднем возрасте. [9] Пациенты жалуются на эпизоды затрудненного дыхания ночью, в предутренние часы или связывают жалобы с эмоциональной, а иногда и физической перегрузкой. Эти симптомы сочетаются с затруднением дыхания, с нарушениями выдоха, «свистами» в груди, рецидивирующим кашлем с небольшим количеством мокроты. Эти симптомы могут купироваться самостоятельно или с использованием лекарственных бронхорасширяющих препаратов. Необходимо связать появления признаков БА после взаимодействия с аллергенными веществами, сезонность появления симптомов, связь с клиническими признаками насморка, присутствие в анамнезе атопических заболеваний или астматических проблем.
При подозрении на диагноз БА следует задать вопросы:
Специфические методы постановки диагноза
1. Оценка функции работы легких и степени возвратимости бронхиальной констрикции
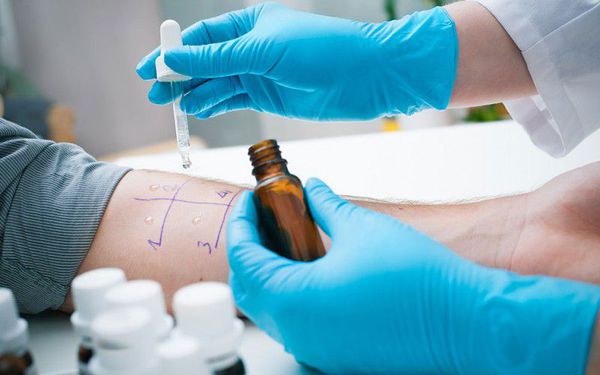
2. Аллергообследование. Подразумевает проведение аллергопроб на коже, тестов-провокаторов с некоторыми видами аллергенов, лабораторного исследования для выявления специфических IgE-антител. Наиболее распространенными являются кожные пробы, так как это простые методы по технике выполнения, достоверно точные и безопасные для пациентов.
2.1. Существуют следующие виды кожных аллергопроб по технике выполнения:
Чтобы проводить кожные пробы, необходимы данные из истории болезни пациента, свидетельствующие за однозначную связь жалоб и контакта с тем аллергеном или их группой в патогенезе болезни, IgE-зависимый тип аллергической реакции.
Кожное тестирование не проводится в случаях:
2.2. Провокационный ингаляционный тест. Эксперты Респираторного Общества из Европы рекомендуют проводить данное исследование. Перед исследованием проводят спирометрию, и если уровень ОФВ1 не снижается ниже отметки 70% от нормы, пациент допускается до провокации. Используют небулайзер, с помощью которого можно струей выдавать определенные дозы аллергена, и пациент делает несколько ингаляций с определенными разведениями аллергенов под постоянным контролем врача-аллерголога. После каждой ингаляции оцениваются результаты через 10 мин трижды. Тест расценивается как положительный при уменьшении ОФВ1 на 20% и больше от начальных показателей.
2.3. Методы лабораторной диагностики. Диагностика в лаборатории выступает неосновным методом. Проводится, если необходимо еще одно исследование для подтверждения диагноза. Основными показаниями для назначения лабораторной диагностики являются:
В лабораториях применяют следующие методы определения общего и специфического IgE — радиоизотопный, хемилюминисцентный и иммуноферментный анализы.
Самый новый подход к диагностике аллергических заболеваний на данный момент — это молекулярное аллергообследование. Оно помогает более точно поставить диагноз, рассчитать прогноз течения болезни. Для диагностики важно учитывать следующие нюансы:
Лечение бронхиальной астмы
К сожалению, современная медицина не может вылечить больного от бронхиальной астмы, однако все усилия сводятся к созданию терапии с сохранением качества жизни пациента. В идеале при контролируемой БА должны отсутствовать симптомы заболевания, сохраняться нормальными показатели спирометрии, отсутствовать признаки патологических изменений в нижних отделах легких. [1]
Консервативные методы лечения
Фармакотерапию БА можно разделить на 2 группы:
Препараты для купирования приступов следующие:
К препаратам для поддерживающей терапии бронхиальной астмы относят:
Для лечения бронхиальной астмы важны как лекарственные препараты, так и способы введения данных веществ в организм и дыхательные пути. Препараты могут назначаться внутрь per os, парентерально, ингаляционно.
Выделяют следующие группы доставки лекарственных препаратов через дыхательные пути:
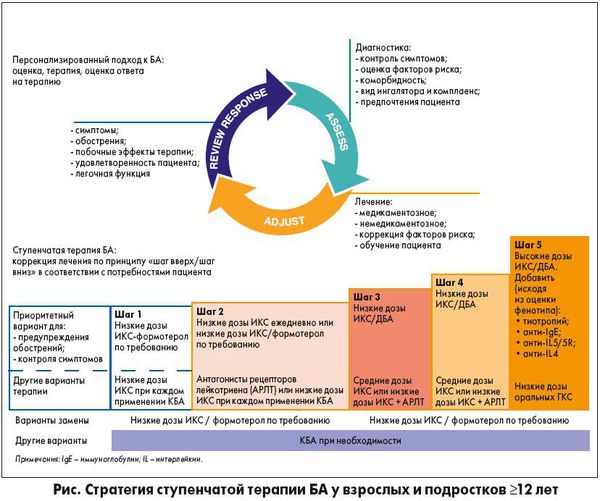
Европейские рекомендации по лечению астмы (GINA, 2019)
Европейскими рекомендациями предложен ступенчатый подход к лечению бронхиальной астмы. Выбор ступени зависит от степени выраженности симптомов. Увеличение выраженности при отсутствии контроля или при высоком риске обострений — подъём на ступень вверх.
Снижаться на ступень следует не ранее чем через три месяца стабильного контроля астмы. Снижение должно быть очень плавным — каждые три месяца уменьшать дозировку ингаляционных глюкокортикостероидов (иГКС) не более чем на 50 %.
Монотерапия короткодействующищими β2-агонистами (КДБА), по новым рекомендациям, не рекомендуется даже для устранения симптомов в связи с высоким риском обострений и смерти.
На второй ступени используют низкие дозы иГКС плюс ДДБА ежедневно. Лечение низкими дозами ингаляционных кортикостероидов (иКС) позволяет избежать обострений, улучшает качество жизни, уменьшает выраженность симптомов.
У взрослых стартовая доза бекламетазона дипропионата составляет 400 мкг, у детей — 200 мкг. Дети, получающие более 400 мкг иГКС, должны наблюдаться у педиатра.
Антилейкотриеновые препараты, как добавление к иГКС, применяются при наличии гиперчувствительности дыхательных путей, вирусозависимой астме и аллергическом рините.
При противопоказаниях к приёму длительно действующих β2-агонистов ( ДДБА) следует к иГКС добавить тиотропий бромид. Также его добавляют к комбинации иГКС и ДДБА при частых или тяжёлых обострениях.
При назначении высоких доз иГКС все пациенты, особенно дети, должны наблюдаться у специалиста по тяжёлой бронхиальной астме.
Для улучшения качества жизни, уменьшения выраженности симптомов и частоты обострений назначают омализумаб, меполизумаб, реслизумаб, бенрализумаб, дупиламаб. Назначение препаратов и подбор дозировки проводит врач.
При бронхиальной астме применяется дыхательная гимнастика по Бутейко, но она не уменьшает воспаление. Гимнастика состоит из серии упражнений, направленных на мышечное расслабление и уменьшение частоты дыхания, которое должно стать плавным и медленным, без глубоких и частых вдохов.
Таким образом, по новым рекомендациям следует:
Коронавирусная инфекция и бронхиальная астма
В связи с новой коронавирусной инфекцией рекомендовано по возможности уменьшить использование спирографии (метод оценки состояния лёгких путем измерения объёма и скорости выдыхаемого воздуха) и сократить лечение небулайзерами, заменив их на спейсеры с маской. По сравнению с небулайзером, спейсером проще пользоваться, он более компактный и эффективный.
Народные способы лечения
Прогноз. Профилактика
В современных условиях нет доказательств, что экологические, климатические факторы, нарушения питания могут ухудшать течение БА, и устранение этих триггеров поможет снизить тяжесть заболевания и уменьшить объем фармакотерапии. Требуется проведение дальнейших клинических наблюдений в этом ключе. [7]
Выделяют первичную профилактику. Она включает:
Вторичная профилактика включает:
За дополнение статьи благодарим Елену Лобову — врача-пульмонолога, научного редактора портала «ПроБолезни».
Использование метода спирометрии
Общая информация
Краткое описание
Российское респираторное общество
ФЕДЕРАЛЬНЫЕ КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО ИСПОЛЬЗОВАНИЮ МЕТОДА СПИРОМЕТРИИ
ОПРЕДЕЛЕНИЕ
Спирометрия
представляет собой неинвазивный метод измерения воздушных потоков и объемов как функции времени с использованием форсированных маневров [1].
ПОКАЗАНИЯ [2]:
Диагностика:
1) установление причины респираторных жалоб больного, клинических симптомов либо отклонений в лабораторных показателях;
2) оценка влияния болезни на легочную функцию;
3) скрининг популяций людей с высоким риском легочных заболеваний;
4) предоперационная оценка риска;
5) оценка прогноза заболевания;
6) оценка функционального состояния перед участием пациента в программах с физическими нагрузками высокого уровня.
Наблюдение
1) оценка эффективности лечебных мероприятий;
2) мониторирование течения заболевания с нарушением легочной функции;
3) наблюдение за популяциями лиц, подвергающихся воздействию неблагоприятных факторов;
4) мониторирование побочных эффектов лекарств с известной способностью вызывать повреждения легких.
Экспертная оценка нетрудоспособности
1) обследование больного перед началом реабилитации;
2) оценка рисков как части экспертной оценки нетрудоспособности;
3) экспертная оценка состояния здоровья по другим юридическим поводам.
ПРОТИВОПОКАЗАНИЯ
Спирометрия не имеет абсолютных противопоказаний, но маневр форсированного выдоха следует выполнять с осторожностью:
1) у больных с развившимся пневмотораксом и в течение 2 нед после его разрешения [3];
2) в первые 2 недели после развития инфаркта миокарда, после офтальмологических и полостных операций [3];
3) выраженном продолжающемся кровохарканье [3];
4) тяжелой бронхиальной астме [3].
Лечение
ТЕХНИЧЕСКИЕ УСЛОВИЯ
Все спирометры должны удовлетворять минимальным техническим требованиям, которые достаточны для повседневной клинической практики. Соблюдение этих требований необходимо для точности измерений и минимизации вариабельности результатов. В отдельных ситуациях, например, в некоторых клинических исследованиях, объем технических требований может быть увеличен.
Спирометр должен позволить оценивать объем воздуха в течение ≥15 сек и измерять объемы не менее 8 л с точностью как минимум ± 3%, или ± 0,05 л, а воздушные потоки – от нуля до 14 л/с [2]. Для оптимального контроля за качеством измерений спирометр должен оснащаться дисплеем, на котором отражается кривая поток-объем или объем-время, для визуальной оценки каждого выполненного маневра перед началом следующего. Для оценки воспроизводимости повторных маневров в течение одного исследования желательно, чтобы все кривые в данном исследовании накладывались на дисплее друг на друга.
Калибровка спирометра
Все спирометрические параметры измеряют при условиях окружающей среды ATPS-условиях измерения (ambient temperature pressure saturated = лабораторные условия): температура (Татм.) и давление (Ратм.) окружающей среды, при полном насыщении водяным паром (РН2О = давление насыщенного пара при Tатм.). Далее необходимо преобразовать полученные данные в условия измерения BTPS (body temperature pressure saturated = условия организма): температура тела (37 °С = 310 K), окружающее давление (Pатм.) и полное насыщение водяным паром (РН2О = 6,3 кПа) [2]. При калибровке спирометра должны вноситься соответствующие поправки.
Как правило, все спирометры рассчитаны на работу при температуре окружающего воздуха не менее 17 °С и при снижении температуры ниже этого значения могут искажать результаты измерений. Если спирометр рассчитан на работу при более низких температурах, это должно быть указано в инструкции от производителя [2].
Перед началом работы необходимо калибровать спирометр (табл. 1); это неотъемлемая часть международных требований качественной лабораторной практики.
Калибровка – процедура, во время которой устанавливается взаимосвязь между параметрами потоков и объемов, рассчитанными сенсором, и реальными величинами. Помимо этого, существует процедура проверки калибровки, во время которой исследователь удостоверяется, что спирометр по-прежнему находится в пределах калибровки (±3% от параметров калибровки) [2]. Если спирометр не соответствует параметрам калибровки, выполняют новую калибровку.
Проверка калибровки проводится ежедневно или чаще, если это оговорено в инструкции от производителя.
Объем шприца, используемого для калибровки объема, должен составлять 3 литра и иметь точность ±15 мл, или ±0,5% от всего диапазона измерений [2]. Калибровка самого шприца проводится с периодичностью, указанной в инструкции от производителя. Кроме того, время от времени (например, ежемесячно) шприцы следует проверять на утечку воздуха; для этого надо попытаться опорожнить шприц при закрытом выходном отверстии. Внеплановые калибровки шприца должны проводиться при его повреждении.
Калибровочный шприц должен храниться в помещении с той же температурой и влажностью воздуха, что и в помещении, где проводится спирометрия. Лучше всего хранить калибровочный шприц рядом со спирометром, но вне доступа прямых солнечных лучей и вдали от источников тепла.
Калибровка объема должна выполняться не реже чем 1 раз в день однократным введением в спирометр 3 л воздуха из калибровочного шприца [2]. Благодаря ежедневной калибровке можно выявить нарушение точности измерений в пределах одного дня. В особых ситуациях (при скрининге больших популяций, быстром изменении температуры воздуха и т.д.) требуются более частые калибровки.
Спирометры, измеряющие поток и объем, должны ежедневно проверяться на предмет утечки воздуха. Обнаружить утечку можно, создавая постоянное положительное давление ≥3 см вод.ст. (0,3 кПа) на выходе спирометра (желательно с учетом загубника). При наличии утечки объем через 1 мин снизится более чем на 30 мл через 1 мин [2].
Спирометры, измеряющие объем, не реже 1 раза в 3 мес следует калибровать пошагово на протяжении всего измеряемого диапазона с помощью калибровочного шприца или другого эквивалентного стандартного объема. Измеренный объем должен отличаться от должного не более чем на ±3,5%, или на 65 мл [2].
Спирометры, измеряющие поток, должны калиброваться ежедневно с помощью 3-литрового шприца, который опорожняют как минимум трижды с тем, чтобы получить несколько потоков между 0,5 и 12 л/с. Объем воздуха при каждом потоке должен соответствовать требованиям точности на ±3,5% [2].
Таблица 1. Варианты и периодичность калибровки спирометра [2].
| Параметр | Минимальная периодичность | Действие |
| Объем | Ежедневно | Калибровка 3-литровым калибровочным шприцем |
| Утечка воздуха | Ежедневно | Постоянное давление 3 см вод.ст (0,3 кПа) в течение 1 мин |
| Линейность | Еженедельно | Тестирование как минимум при трех разных диапазонах потока |
| Время | 1 раз в 3 мес | Проверка механического счетчика времени с помощью секундомера |
| Программное обеспечение | Обновление версии | Регистрация данных инсталляции и выполнение теста у «известного» пациента |
С помощью маневра форсированного выдоха измеряют форсированную жизненную емкость легких (ФЖЕЛ) и показатели объемной скорости воздушного потока.
Измерение ФЖЕЛ может быть проведено различными способами (максимальный вдох делается после спокойного или после полного выдоха, перед форсированным выдохом делается или нет пауза). Но предшествующий маневру ФЖЕЛ вдох оказывает существенное влияние на экспираторные скоростные показатели, поэтому для получения максимальных результатов исследования мы рекомендуем после спокойного выдоха делать максимально глубокий вдох и сразу же после этого без паузы выдохнуть весь воздух с максимальным усилием. Пауза на высоте вдоха может вызвать «стрессовое расслабление» со снижением эластической тяги и увеличением растяжимости дыхательных путей, что ведет к уменьшению скорости выдоха [4].
Маневр ФЖЕЛ можно разделить на 3 этапа: максимальный вдох, форсированный выдох и продолжение выдоха до конца исследования [2]. Рекомендуется, чтобы исследователь сначала продемонстрировал пациенту правильное выполнение маневра.
Все исследования легочной функции выполняются с носовым зажимом либо зажатием ноздрей пальцами, загубник спирометра следует плотно обхватить губами и зубами. После максимально глубокого вдоха (от уровня функциональной остаточной емкости) пациент должен сделать мощный выдох с максимальным усилием, продолжая его до полного опорожнения легких. Во время маневра рекомендуется словами и жестами поощрять пациента делать максимально мощный выдох и продолжать его максимально долго. В то же время следует внимательно наблюдать за пациентом во избежание нежелательных явлений, связанных с резким и глубоким выдохом (например, синкопальных состояний). Одновременно необходимо следить за графическим отражением результатов теста на дисплее спирометра, что позволяет визуально оценить качественность маневра. Если пациент жалуется на головокружение или другое ухудшение самочувствия, следует сделать паузу до исчезновения нежелательных явлений или прекратить исследование. Уменьшение усилия при форсированном выдохе приводит к завышению спирометрических показателей и неправильной интерпретации результатов исследования [2].
Подготовка к спирометрии
Перед началом исследования рекомендуется:
1) проверить калибровку спирометра;
2) задать пациенту вопросы о недавнем курении перед исследованием, имеющихся заболеваниях, использовании лекарственных препаратов, которые могут повлиять на результаты;
3) измерить рост и вес пациента;
4) внести данные о пациенте в спирометр;
5) правильно усадить пациента перед спирометром: пациент должен сидеть с прямой спиной и слегка приподнятой головой. Спирометрию рекомендуется выполнять в положении пациента сидя в кресле с подлокотниками, но без колесиков. Если особые обстоятельства требуют проведения исследования в положении пациента стоя или каком-либо другом, это должно отражаться в протоколе исследования.
6) объяснить и показать пациенту, как правильно выполнить дыхательный маневр;
7) при наличии у пациента съемных зубных протезов не рекомендуется снимать их перед исследованием, чтобы не нарушать геометрию ротовой полости. Однако иногда плохо установленные протезы не позволяют пациенту герметично обхватывать загубник и становятся причиной утечки воздуха; в этой ситуации рекомендуется повторить дыхательный маневр после снятия протезов [2].
Курение пациента должно быть исключено как минимум за 1 час, употребление алкоголя – за 4 ч до исследования, значительные физические нагрузки – за 30 мин до исследования. Одежда пациента не должна стягивать грудную клетку и живот. В течение 2 ч перед исследованием не рекомендуется обильный прием пищи [3].
Критерии качества спирометрии
Начало исследования. Начало теста (нулевая точка, от которой начинается измерение всех временнЫх параметров спирометрии) определяется методом обратной экстраполяции. Согласно этому методу, нулевая точка – это точка пересечения касательной линии к кривой объем-время до горизонтальной оси (рис. 2). Объем экстраполяции не должен превышать 5% от ФЖЕЛ, или 0,150 л [2]. Увеличение объема экстраполяции происходит при медленном начале маневра форсированного выдоха.
Завершение исследования. Для оценки достаточного экспираторного усилия пациента и определения момента завершения теста рекомендуется использовать 2 критерия:
1) пациент не может продолжать выдох. Несмотря на активную словесную стимуляцию продолжать выдох как можно дольше пациент может прекратить дыхательный маневр в любой момент, особенно при появлении дискомфортных ощущений.
2) объем на кривой объем-время перестает меняться (
Форсированная жизненная емкость легких (ФЖЕЛ)
Объем форсированного выдоха за 1 секунду (ОФВ1)
Соотношение ОФВ1/ФЖЕЛ
Важным спирометрическим показателем является отношение ОФВ1/ФЖЕЛ, которое обычно выражается в процентах и является модификацией индекса Тиффно (ОФВ1/ЖЕЛвд, где ЖЕЛвд – максимальный объем воздуха, который можно вдохнуть после полного спокойного выдоха). Объем воздуха, выдыхаемый за первую секунду, представляет собой достаточно постоянную долю ФЖЕЛ независимо от размера легких. У здорового человека это соотношение составляет 75–85%, но с возрастом скорость выдоха снижается в большей степени, чем объем легких, и отношение несколько уменьшается. У детей, наоборот, скорости воздушных потоков высокие, поэтому соотношение ОФВ1/ФЖЕЛ у них, как правило, выше – около 90%. При обструктивных нарушениях отношение ОФВ1/ФЖЕЛ снижается, поскольку ОФВ1 снижается соответственно тяжести обструкции. ФЖЕЛ при этом также уменьшается, но, как правило, в меньшей степени. При легочной рестрикции без обструктивных изменений ОФВ1 и ФЖЕЛ снижаются пропорционально, следовательно, их соотношение будет в пределах нормальных величин или даже немного выше. Таким образом, при необходимости дифференцировать обструктивные и рестриктивные нарушения оценивают соотношение ОФВ1/ФЖЕЛ.
Другие показатели максимального экспираторного потока
Максимальные инспираторные потоки
Особенности спирометрии у детей
Спирометрия может выполнять у детей не моложе 5 лет [2]. Большинство детей начиная с возраста 9 лет способны выполнить маневр форсированного выдоха, удовлетворяющий тем же критериям, которые применимы у взрослых пациентов [5], однако для детей до 9 дет необходимо соблюдать некоторые правила. Желательно, чтобы специалист, обследующий ребенка, имел опыт выполнения функциональных исследований у детей. В лаборатории, занимающейся обследованием маленьких детей, должна быть очень доброжелательная атмосфера, можно использовать игрушки, соответствующие возрасту маленьких пациентов. Перед началом исследования ребенку следует объяснить в доступной манере, что он должен делать. Хорошие результаты дает применение визуальной «обратной связи» (изображение свечей или других картинок на дисплее спирометра, меняющихся при выполнении ребенком форсированного выдоха). Даже если первые попытки были неудачными, продолжение исследования в большинстве случаев позволяет ребенку привыкнуть к обстановке и лучше выполнить дыхательный маневр. Не рекомендуется обследовать детей в лабораториях для взрослых пациентов, в которых обстановка не адаптирована к особенностям детей [2].
Во время тестирования исследователь должен внимательно наблюдать за ребенком для своевременного устранения утечки воздуха и контроля за правильностью выполнения дыхательного маневра. [5]. Для оценки качества выполненного маневра, как и у взрослых, используют метод обратной экстраполяции. Если объем обратной экстраполяции превышает 80 мл, или 12,5 % ФЖЕЛ, этот маневр может быть сохранен для дальнейшего анализа при отсутствии других дефектов [5]. Для детей младшего возраста преждевременным завершением маневра форсированного выдоха считается прекращение маневра на уровне более 10% от пиковой скорости выдоха. ФЖЕЛ и форсированные экспираторные потоки, полученные в таком маневре, не должны использоваться для анализа [5].
В идеале, при проведении спирометрии ребенку достаточно получить 2 приемлемых кривых поток-объем, в которых ФЖЕЛ и ОФВ1 отличаются не более чем на 0,1 л, или 10% от максимальных значений. Но даже при получении единственной кривой, удовлетворяющей техническим требованиям, она может использоваться для анализа, однако в протоколе исследования должно быть отражено число технически удовлетворительных маневров и степень воспроизводимости результатов. Как и у взрослых, у детей для анализа выбирают кривую с максимальными значениями ФЖЕЛ и ОФВ1 [5].
У детей моложе 6 лет не должны использоваться должные величины, применяемые у взрослых пациентов. В литературе предложены несколько различных уравнений для расчета должных величин у детей этого возраста [5].
ИНТЕРПРЕТАЦИЯ РЕЗУЛЬТАТОВ
Выбор результата для анализа
ФЖЕЛ и ОФВ1 выбирают не менее чем из трех воспроизводимых технически приемлемых маневров. Результаты исследования анализируют по маневру с максимальными ФЖЕЛ и ОФВ1 [2].
Должные величины
Существуют различные таблицы и формулы для расчета должных величин показателей спирометрии. В большинстве случаев исследования по разработке должных величин ограничиваются уравнениями расчета средних значений, которые получают при обследовании здоровых некурящих людей. Практика использования 80% от должных значений в качестве фиксированного значения для нижней границы нормальных значений (НГН) ФЖЕЛ и ОФВ1 приемлема у детей, но может приводить к существенным ошибкам при интерпретации функции легких у взрослых. Использование 70% в качестве нижней границы нормы для отношения ОФВ1/ФЖЕЛ приводит к значительному числу ложно-положительных результатов (гиподиагностике ХОБЛ) у мужчин в возрасте старше 40 лет и у женщин старше 50 лет и к гипердиагностике ХОБЛ у пожилых лиц, никогда не куривших и не имеющих характерных клинических симптомов. Как известно, с возрастом соотношение ОФВ1/ФЖЕЛ снижается, поэтому некоторые авторы для диагностики ХОБЛ у людей старше 70 лет рекомендуют использовать для ОФВ1/ФЖЕЛ 65% порог нормы.
Для скоростных показателей НГН составляет 60% от должных значений.
При выборе должных значений необходимо сравнить данные, получаемые с помощью выбранных уравнений должных значений, с собственными измерениями, проведенными на репрезентативной выборке здоровых лиц. Следует выбрать те уравнения должных значений, при которых у взрослых разница между измеренными и рассчитанными значениями является минимальной. У детей ориентируются на минимальную разницу логарифмов измеренных и рассчитанных значений. Чтобы быть уверенным, что выбранные должные значения приемлемы, необходимо обследовать достаточно большое число добровольцев (около 100). К сожалению, это трудновыполнимо для большинства лабораторий.
При использовании должных величин следует избегать экстраполяции за указанный диапазон роста и возраста. Если все же возраст или рост пациента выходят за границы популяции, для которой были разработаны должные значения, то в интерпретации необходимо указать, что была проведена экстраполяция.
Должные величины зависят от антропометрических параметров (в основном от роста), пола, возраста, расы. Чем выше человек, тем больше его легкие и протяженность дыхательных путей и, следовательно, максимальная экспираторная скорость. При вычислении нормальных значений для людей с кифосколиозом вместо роста в формулу следует поставить размах рук. У женщин объем легких меньше, чем у мужчин такого же роста. С возрастом эластичность легочной ткани снижается, в результате происходит снижение объема и скорости выдоха. Вместе с тем следует принимать во внимание и индивидуальные вариации нормы. Например, легочные заболевания могут возникать у людей с исходными показателями легочных объемов и потоков выше среднего уровня и, несмотря на снижение их на фоне заболевания относительно исходных значений, они по-прежнему могут оставаться в пределах, нормальных для популяции в целом.
Анализ результатов спирометрии
Интерпретация результатов спирометрии строится на анализе основных спирометрических параметров (ОФВ1, ЖЕЛ, ОФВ1/ЖЕЛ).
Интерпретация результатов функционального исследования должна быть четкой, краткой и информативной. Простая констатация фактов, что какие-то показатели в норме, а какие-то снижены, не годится. В идеале, к интерпретации результатов функционального исследования должны применяться принципы клинического принятия решения, где вероятность болезни после проведения исследования оценивается с учетом вероятности болезни до проведения исследования, качества исследования, вероятности ложно-положительной и ложно-отрицательной интерпретации, и, наконец, непосредственно результатов исследования и должных значений. Это часто невозможно, потому что интерпретация многих, если не большинства, исследований проводится при отсутствии какой-либо клинической информации. Чтобы улучшить ситуацию, по возможности следует спрашивать врачей, направляющих пациента на исследование, на какой клинический вопрос необходимо ответить, а также до исследования поинтересоваться у пациента, почему его направили в лабораторию. В этом отношении также желательно записать респираторные симптомы (например, кашель, мокрота, хрипы и одышка), недавнее использование бронхорасширяющих препаратов, анамнез курения.
Интерпретация будет более точной при учете клинического диагноза, данных рентгенограммы грудной клетки, концентрации гемоглобина и любых подозрений на нейромышечные заболевания или обструкцию верхних дыхательных путей.
Обструктивные вентиляционные нарушения
Наиболее частое показание к проведению спирометрического исследования – выявление обструкции дыхательных путей и оценка ее выраженности. Обструктивный тип вентиляционных нарушений характеризуется снижением соотношения ОФВ1/ФЖЕЛ при нормальной ФЖЕЛ. Патофизиологической основной снижения максимального экспираторного потока при бронхиальной обструкции является повышение сопротивления дыхательных путей, однако при недостаточном усилии, приложенном пациентом во время выполнения маневра ФЖЕЛ, максимальный экспираторный поток также будет снижен. Дифференцировать эти ситуации можно при количественной оценке усилия пациента, измерив плевральное давление (с помощью внутрипищеводного баллона) или компрессионный объем при проведении бодиплетизмографии.
Ранними признаками обструктивных нарушений вентиляции у пациентов без клинических проявлений, возможно, могут служить изменение формы экспираторной кривой поток-объем и снижение скоростных показателей, измеренных при низких легочных объемах во время теста ФЖЕЛ (СОС25-75, МОС50, МОС75) (рис.4), однако в настоящее время не существует убедительных доказательств существования таких корреляционных связей. Более того, значительная вариабельность показателей затрудняет интерпретацию индивидуальных отклонений от должных значений.
Обструкция верхних дыхательных путей. Форма максимальной кривой поток-объем существенно отличается от должной при обструкции верхних дыхательных путей. Своеобразная форма кривой поток-объем при поражениях верхних дыхательных путей обусловлена различным воздействием динамических факторов на экстра- и интраторакальные дыхательные пути. На экстраторакальные дыхательные пути влияет атмосферное давление, на интраторакальные – внутриплевральное. Разница между внешним давлением (атмосферным или плевральным) и давлением внутри дыхательных путей называется трансмуральным давлением. Положительное трансмуральное давление создает компрессию и уменьшает просвет дыхательных путей. Наоборот, отрицательное трансмуральное давление поддерживает дыхательные пути открытыми, увеличивая их просвет. Если обструкция возникает только во время вдоха либо выдоха, она считается переменной. Если воздушные потоки снижены во время обеих фаз дыхания, обструкция называется фиксированной.
Переменная экстраторакальная обструкция (например, при параличе голосовых связок, увеличении щитовидной железы) вызывает избирательное ограничение воздушного потока при вдохе. Во время выдоха давление внутри дыхательных путей увеличивается и превышает атмосферное, воздействующее на зону поражения снаружи, поэтому экспираторный поток меняется мало. Во время вдоха наблюдается обратная картина: атмосферное давление значительно превышает давление в дыхательных путях, что приводит к снижению инспираторных потоков. Изменения инспираторных потоков хорошо видны на кривой поток–объем (рис. 5, А).
При переменной интраторакальной обструкции (например, при опухоли нижнего отдела трахеи (ниже яремной ямки грудины), трахеомаляции, гранулематозе Вегенера или редицивирующем полихондрите) высокое внутриплевральное давление во время форсированного выдоха превышает давление в дыхательных путях, что приводит к выраженному сужению их просвета с критическим снижением экспираторных потоков. Инспираторные потоки могут мало меняться, если плевральное давление более отрицательное, чем давление в дыхательных путях. Характерная кривая поток–объем представлена на рисунке 5, Б.
При фиксированной обструкции (например, при опухолях на любом уровне верхних дыхательных путей или параличе голосовых связок с фиксированным стенозом, рубцовых стриктурах) инспираторные и экспираторные потоки нарушаются почти в одинаковой степени. Локализация поражения не имеет значения, поскольку размеры трахеи при этом не зависят от давления внутри и снаружи дыхательных путей (рис.5, В).
Для характеристики вышеуказанных поражений верхних дыхательных путей используются различные показатели, например, соотношение инспираторных и экспираторных потоков на уровне 50% жизненной емкости (МОС50вд/МОС50выд, в норме это соотношение приблизительно равно 1,5). Это соотношение наиболее значительно меняется при переменной экстраторакальной обструкции и неспецифично для другой патологии (рис.5). При подозрении на изолированную обструкцию верхних дыхательных путей следует подтвердить диагноз эндоскопически или рентгенологически.
Таблица 2. Классификация тяжести обструктивных нарушений легочной вентиляции
| ОФВ1, %должн. | |
| Легкие | >70% |
| Умеренные | 60 – 69% |
| Среднетяжелые | 50 – 59% |
| Тяжелые | 35 – 49% |
| Крайне тяжелые | |
Рестриктивные вентиляционные нарушения
Рестриктивные нарушения вентиляции обусловлены процессами, снижающими растяжимость легких и, следовательно, ограничивающими наполнение легких воздухом. В начале развития патологических нарушений, когда объем легких еще не снижен, скоростные показатели и отношение ОФВ1/ФЖЕЛ могут увеличиваться вследствие того, что паренхима легких оказывает большее растягивающее действие на дыхательные пути: просвет бронхов увеличивается относительно объема легких. При прогрессировании заболевания происходит уменьшение воздушности легочной ткани. Это проявляется снижением ЖЕЛ, кривая поток-объем становится высокой и узкой (рис. 6, А). Пиковая объемная скорость обычно остается нормальной, после пика наблюдается быстрое линейное снижение потока. Форма кривой может и не меняться, а представлять собой пропорционально уменьшенную копию должной кривой, как, например, при пневмонэктомии (рис. 6, Б).
Рестриктивные нарушения могут встречаться при интерстициальных заболеваниях легких, обширной воспалительной инфильтрации легочной ткани, гипоплазии и ателектазах легкого, после резекции легочной ткани. При подозрении на интерстициальные заболевания легких следует измерить диффузионную способность легких и общую емкость легких. К рестрикции также может приводить и внелегочная патология, например, поражение грудного отдела позвоночника, ребер, дыхательной мускулатуры; высокое стояние диафрагмы, что делает невозможным выполнение глубокого полноценного вдоха; нарушение регуляции дыхания при угнетении дыхательного центра наркотическими препаратами или его повреждении опухолью, кровоизлиянием. При подозрении на мышечную слабость как причину рестрикции следует измерить силу дыхательных мышц. Кроме того, у больных с выраженной мышечной слабостью ФЖЕЛ, измеренная в вертикальном положении и в положении лежа, будет существенно различаться из-за воздействия гравитации на органы брюшной полости. В норме ФЖЕЛ в положении лежа на 5-10% меньше, чем в положении сидя. При выраженной диафрагмальной дисфункции эта разница превышает 30%.
Для диагностики рестриктивных нарушений недостаточно спирометрического исследования, а следует выполнить бодиплетизмографию и измерить легочные объемы.
Смешанные вентиляционные нарушения
Смешанные нарушения легочной вентиляции развиваются при сужении просвета дыхательных путей на фоне уменьшения легочных объемов. При этом спирометрия будет регистрировать одновременное снижение ФЖЕЛ, ОФВ1 и ОФВ1/ФЖЕЛ.
Для уточнения характера функциональных нарушений необходимо выполнять бодиплетизмографию с измерением легочных объемов.
БРОНХОДИЛАТАЦИОННЫЙ ТЕСТ
При первичном исследовании функции дыхания почти всегда желательно выполнить бронходилатационный тест (или бронходилатационную пробу), то есть повторить спирометрию после ингаляции бронходилататора.
Показания для проведения бронходилатационного теста:
1. установление обратимости бронхиальной обструкции, включая пациентов с нормальными показателями исходной спирометрии;
2. определение потенциального эффекта бронхолитической терапии;
3. мониторирование динамики легочной функции у больных с хроническими респираторными заболеваниями при длительном (многолетнем) наблюдении.
Противопоказаний к проведению бронходилатационного теста не существует за исключением тех ситуаций, в которых противопоказано выполнение спирометрии, и случаев непереносимости бронхорасширяющих препаратов. Если пациент не переносит β2-агонисты, то в качестве бронходилататора можно использовать М-холинолитик короткого действия.
Методика проведения бронходилатационного теста
Реакция на бронходилататор является интегральной физиологической реакцией, в которую вовлечены эпителий дыхательных путей, нервы, медиаторы и гладкие мышцы.
Если бронходилатационный тест проводится с целью выявить возможность дополнительного улучшения легочной функции на фоне базисной терапии заболевания, то вся плановая терапия сохраняется перед исследованием в обычном для пациента режиме [2].
Курение не допускается в течение 1 ч до и на протяжении всего тестирования.
Интерпретация результатов бронходилатационного теста
Обратимость бронхиальной обструкции определяется по изменению ОФВ1 или ФЖЕЛ. Другие показатели спирометрии, в том числе потоки, измеренные на разных уровнях ФЖЕЛ (МОС25, МОС50, МОС75, СОС25-75), не используются для оценки обратимости обструкции дыхательных путей в связи с их крайне высокой вариабельностью [7].
Интерпретация результатов бронходилатационного ответа состоит из нескольких этапов. На первом этапе необходимо определить, превышают ли полученные данные вариабельность измерения, которая составляет