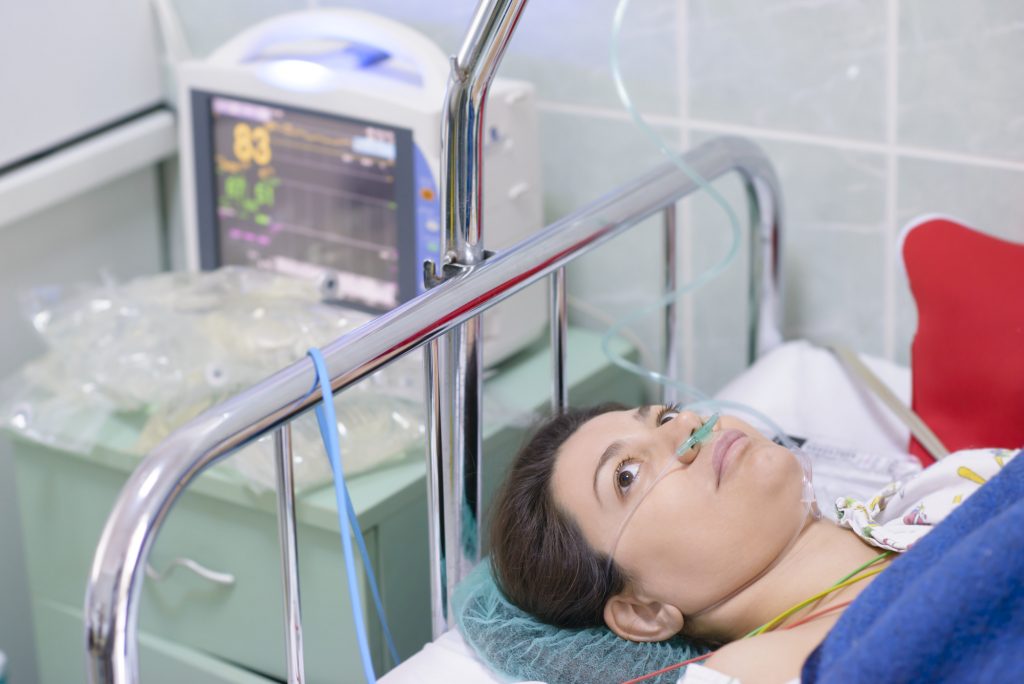
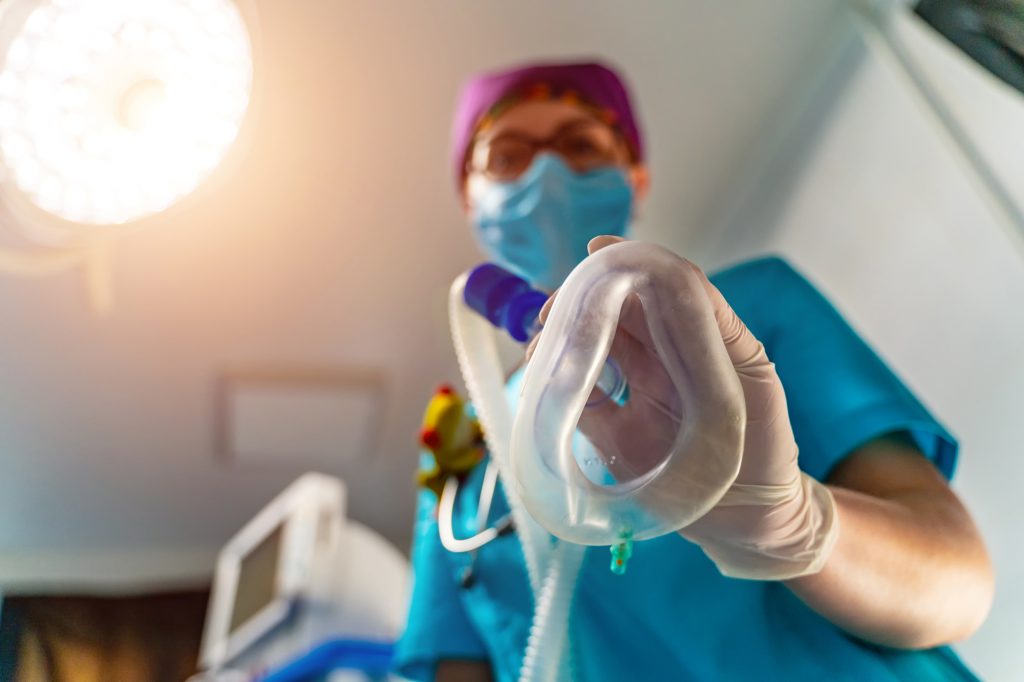
Оксигенотерапия при коронавирусе
Как используется лечение кислородом при коронавирусе
Нужно сразу отметить, что кислород применяется лишь как вспомогательный метод терапии — респираторная поддержка. Он не способен вылечить инфекцию и лишь устраняет гипоксемию (низкое содержание кислорода в крови).
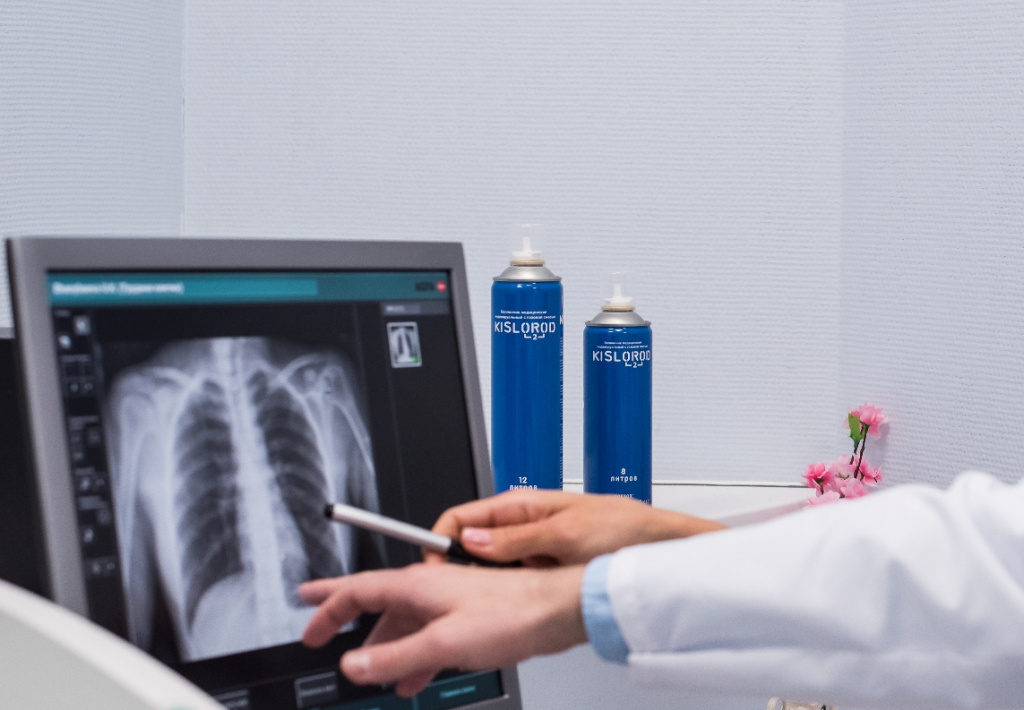
В клиниках применяют несколько методик, нацеленных на борьбу с острой дыхательной недостаточностью. Это кислородная терапия с использованием маски, высокопоточная назальная кислородотерапия, неинвазивная вентиляция легких (НИВЛ) и инвазивная искусственная вентиляция легких (ИВЛ). Конкретный способ кислородной терапии при коронавирусе подбирается в зависимости от тяжести состояния пациента.
Метод кислородотерапии при ковиде
Дыхательная недостаточность средней тяжести
Кислородотерапия с использованием маски или канюль
Средне-тяжелое и тяжелое состояние
Высокопоточные канюли или НИВЛ
Тяжелая и крайне тяжелая дыхательная недостаточность
Искусственная вентиляция легких с интубацией трахеи
Какая доза кислорода нужна пациентам с COVID-19
Тяжелобольные пациенты с сатурацией ниже 92 % должны проходить лечение коронавируса кислородом в больнице. Для насыщения крови необходимо подключаться к кислородным концентраторам мощностью более 5 литров в минуту. Как правило, врачи сначала используют высокопоточные канюли. При падении показателя сатурации ниже 85 % пациента забирают в реанимацию и начинают искусственную вентиляцию легких. Аппаратная терапия нужна, чтобы пережить жизнеугрожающее состояние. Тяжелым больным с COVID-19 регулярно измеряют показатель воздуха в крови, чтобы вовремя отследить изменения и предпринять меры.
Больные со средней формой дыхательной недостаточности также получают кислород через канюли или маски, подсоединенные к концентратору. Производительность последнего составляет 1-4 литра в минуту. Врачи рекомендуют начать кислородотерапию при коронавирусе, если сатурация упала ниже 95 %. Помимо подачи кислорода желательно перевернуть пациента на живот, в так называемую прон-позицию.
Если у человека легкая форма COVID-19, то его, как правило, не увозят в больницу. Получать кислород на дому при коронавирусе можно для профилактики гипоксемии, используя кислородный баллончик. В нем находится концентрированная смесь с содержанием кислорода в 4 раза выше, чем в атмосферном воздухе. Такие ингаляции помогают за считанные секунды насытить кровь O2 и улучшить общее состояние организма.
Последствия COVID-19 для легких
Исследования показали, что при интенсивной лечебной терапии воспаление в легких начинает рассасываться через 14-20 дней после начала болезни. При средней и тяжелой форме пневмонии на фоне COVID в первые 2-3 месяца после отрицательного теста наблюдается снижение легочной функции. Оно может достигать 30 %. Причина в том, что новая волокнистая ткань, которая восстанавливается вместо поврежденной, не способна раскрываться полностью.
Тяжелым последствием короновируса может стать легочный фиброз. Это рубцевание легочной ткани, приводящее к ухудшению прохождения кислорода по альвеолам и, как следствие, нарушению функции дыхания. При фиброзе больной обязательно должен встать на учет к пульмонологу.
Как оценивают работу легких после COVID-19
Понять, что после ковида нужна кислородная терапия или другие методы поддержки организма, можно по следующим признакам:
Для оценки дыхательных функций лечащий врач может использовать следующие виды диагностики:
Оксигенотерапия при восстановлении после коронавирусной инфекции
Лечение кислородом при ковиде будет полезно и на этапе восстановления после заболевания. Поврежденные легкие хуже обогащают кровь О2. Для ее насыщения, а также общего укрепления организма и разработки легких используются все доступные методы:
Прогулки на свежем воздухе, умеренные занятия спортом.
Кислородотерапия с использованием кислородных баллончиков, кислородных подушек, домашних концентраторов.
Некоторые из этих методов имеют большее воздействие, чем другие. Например, использование медицинского кислорода на дому при восстановлении после ковида помогает укрепить иммунитет, наполнить тело энергией, прояснить голову, повысить концентрацию внимания. Такая оксигенотерапия особенно полезна для пожилых людей или больных, перенесших COVID-19 в тяжелой форме. Они быстро теряют силы, и прогулки их изматывают. Кислородные баллоны выглядят наиболее удобным в использовании, недорогим и простым вариантом терапии: они способны заменить времяпрепровождение на свежем воздухе до тех пор, пока организм не окрепнет.
Респираторная поддержка при COVID-19
Время чтения: 9 мин.
В декабре 2020 года прошла первая «Респираторная школа» для врачей. Организовали школу фонд «Живи сейчас», он помогает людям с боковым-амиотрофиечским склерозом. В рамках школы лекцию об особенностях респираторной поддержки и ведения пациентов с COVID-19 прочитала Зульфия Сукмарова, к.м.н, кардиолог-аритмолог, врач функциональной диагностики госпиталя им П.В.Мандрыка.
Течение ОРДС и осложнения при COVID-19
Пандемия COVID-19 простимулировала два позитивных процесса. Во-первых, консолидировала врачебное сообщество, стали бурно развиваться междисциплинарные связи. Во-вторых — способствовала развитию респираторной школы. Думаю, если бы все врачи до пандемии имели представление о неинвазивной вентиляции легких (НИВЛ), мы пережили бы пандемию с меньшими потерями.
Задумывая Респираторную школу в апреле 2020 года, мы надеялись, что она будет благодатной почвой для расширения знаний по разным видам вентиляции легких, и эти знания пригодятся в работе с паллиативным, пульмонологическими пациентами, с пациентами с нарушениями дыхания во время сна и т. д. Чем больше врачей знают про неинвазивную вентиляцию, тем лучше для наших пациентов. Потому что COVID-19 — это частный случай дыхательной недостаточности, тогда как дыхательная недостаточность — огромная проблема, с ней сталкиваются врачи почти всех специальностей.
Респираторная школа фонда «Живи сейчас» / Alsfund.ru
Основные патологические изменения при COVID-19 происходят в дыхательной системе (острая вирусная пневмония, пневмонит, острый респираторный дистресс-синдром). Сейчас мы знаем, что ОРДС при COVID-19 нетипичный, как и тактика его ведения. По статистике 20% пациентов имеют тяжелую форму пневмонии и требуют госпитализации, а 25% из госпитализированных нуждаются в пребывании в отделении интенсивной терапии. Это как раз та часть пациентов, которая требует инвазивной стратегии вентиляции. Оставшиеся 75% – кандидаты для той или иной неинвазивной стратегии вентиляции.
Структура и частота осложнений у пациентов с COVID-19 следующая:
8% – острая дыхательная недостаточность по другой причине,
7-20% – острая сердечная недостаточность,
6-10% – вторичная инфекция,
14-53% – острая почечная недостаточность,
4-8% – септический шок.
У 33% пациентов, которые были в критическом состоянии, выявлялась кардиомиопатия, а у 71 % погибших был ДВС (диссеминированное внутрисосудистое свертывание).
Повреждения сердца при COVID-19
Как кардиолог, расскажу о повреждениях сердца при COVID-19.
Ранние повреждения сердца это:
8% – инфаркт миокарда как обострение коронарной болезни сердца атеросклеротической или стрессовой кардиомиопатии,
18% – наджелудочковые нарушения ритма сердца,
8% – желудочковые нарушения,
14% – острая остановка сердца.
Крайне редко бывает острое легочное сердце (вследствие ТЭЛА или ОСН). А вот выпотной перикардит в той или иной степени встречается очень часто.
Среди поздних повреждений:
2% – сердечная недостаточность.
Почти у всех переболевших даже в легкой форме наблюдается адгезивный перикардит (уплотнение плевры и перикарда), вызывающий дискомфорт в грудной клетке. Часто после COVID-19 на приёме у кардиолога обнаруживаются манифестация и ухудшение контроля гипертонии.
COVID-19 и повреждения легких
Теперь сконцентрируемся на лёгких. Основным морфологическим субстратом COVID-19 является диффузное альвеолярное повреждение, и даже при легком течении болезни у большинства пациентов на КТ видны инфильтративные изменения. Даже если пациенты малосимптомные и практически без жалоб, у 88% из них выявляются изменения на КТ, хотя бы маленькие. А вот вторичная бактериальная пневмония при COVID-19 встречается редко – примерно в 12% случаев (при других вирусных заболеваниях присоединение вторичной инфекции типично и встречается чаще).
Дыхательная недостаточность при COVID-19 чаще — первого типа (гипоксическая), но нас будет интересовать более редкая дыхательная недостаточность второго типа (гиперкапническая). Она реже встречается и еще реже диагностируется, ведь люди с лёгкой и средней степенью заболевания лечатся дома, где у них никто не берёт газ-анализ, а по пульсоксиметру они классифицируются чаще как гипоксические пациенты.
Особенности течения дыхательной недостаточности при COVID-19 таковы, что одышка возникает относительно поздно, в среднем через 6-6,5 дней после первых симптомов. Но если она уже возникла, до тяжёлого ОРДС проходит в среднем всего два с половиной дня.
Среди тех, кто находится в критическом состоянии, тяжёлая, острая гипоксическая дыхательная недостаточность является доминирующей находкой. Потребность в искусственной вентиляции лёгких у больных в критическом состоянии — от 30% до 100%. Такой большой разброс обусловлен тем, что в разных сообществах реаниматологов, в разных странах и клиниках — разный порог к интубации. Кстати, отмечу, что баротравмы развиваются нечасто, в 2% случаев, поэтому вентилировать неинвазивно — довольно безопасно даже в домашних условиях.
Факторы риска тяжелого течения COVID-19 уже всем известны. Это пожилой возраст, курение, ожирение, хронические заболевания легких, заболевание сердца и сосудов, диабет. Я их перечисляю только для того, чтобы подчеркнуть, что одновременно это факторы риска вентиляторной недостаточности и нарушений дыхания во время сна.
Я изучила рекомендации по НИВЛ общества интенсивной терапии, Китайского торакального общества, Австралийского и новозеландского общества интенсивной терапии, Всемирной организации здравоохранения, Центров США по контролю и профилактике заболеваний, национальных институтов, Немецкого общества пульмонологов. Лучше всего неинвазивная вентиляция развита в Германии. Там все врачи имеют представление о ней, понимают, когда и кому она показана. Кроме того, многие умеют сами налаживать систему.
Поговорим о госпитализированных пациентах.
Если нет показаний к инвазивной вентиляции, то рекомендуется прон-позиция столько времени, сколько пациент сможет ее переносить, и столько, сколько будет для него безопасно (без пролежней и так далее). Надо пациентов к этому мотивировать.
Следующий этап – низкопоточный кислород (1-6 л/мин), который есть в любом стационаре. Далее – высокопоточный кислород (6-20 л/мин) и, наконец, неинвазивная вентиляция.
Согласно немецким рекомендациям нужно опираться на газ-анализ, так как периферическая сатурация и оксигенация не всегда совпадают. У итальянцев описан случай, когда прибыл пациент с уровнем периферической сатурации 67%, но чувствовал себя относительно нормально – был в сознании, дышал, ухаживал за собой. Его не стали интубировать, и он неинвазивно пережил обострение. Поэтому мы в широком смысле опираемся на периферическую оксигенацию, но если есть возможность, контролируем через артериальную концентрацию.
И обязательно следим за частотой дыхания – это один из главных критериев. К тому же подавляющее большинство авторов говорит, что нужно избегать гипероксии, чтобы не подавлять дыхательный драйв.
При неэффективном достижении целей оксигенации переходим на неинвазивную вентиляцию или высокопоточный кислород . Признаки неэффективности низкопоточного кислорода (и на остальных ступенях тоже) – когда не снижается частота дыхания, показатели кислорода не растут до целевых цифр или снижаются, сохраняется работа вспомогательных мышц (обращаем внимание на шею!) или ухудшается гемодинамика.
Если динамика хуже, чем ожидалось, стоит задуматься: только ли в том дело, что кислорода подается недостаточно, вентиляция плохая? Или есть какая-то другая проблема (тромбоэмболия легочной артерии , инфаркт и т. д.)? Поэтому на этапе оценки эффективности стратегии имеет смысл задуматься о дообследовании.
Разные общества выбирали разные преимущественные стратегии при неэффективности обычной низкопоточной канюли. В Испании это высокопоточный кислород, в Италии – шлем CPAP, в США – высокопоточный кислород, в Португалии или то, или другое, в Соединенном Королевстве – CPAP, в Китае давали высокопоточный кислород, в Австралии и Новой Зеландии – тоже, а вот в Германии предпочитали шлем.
Система подачи высокопоточного кислорода состоит из концентратора, датчика кислорода, увлажнителя. Давление может достигать 60 литров в минуту, FiO2 можно увеличивать до 100%. В общих показаниях по высокопоточному кислороду – гипоксемия без гиперкапнии, ОРДС, острая гипоксемическая дыхательная недостаточность любого генеза (особенно после экстубации, т.к. высокопоточный кислород, в отличие от обычного, уменьшает риск реинтубации).
Есть очень интересное исследование, которое все время дополняется, обновляется: сравнение эффективности начальной стартовой терапии какой-то неинвазивной стратегии и ранней ИВЛ. Согласно большому китайскому исследованию на 548 пациентах, применение высокопоточного кислорода давало значительное уменьшение риска интубации и смерти при тяжелом ОРД.
Частота применения высокопоточного кислорода на настоящий момент в разных сообществах составляет 14-63%. Накапливаются уверенные данные о снижении риска или, как минимум, неувеличении риска при использовании высокопоточного кислорода. Это важно, так как мы часто боимся, что неинвазивная стратегия ухудшит прогноз.
Расскажу о неинвазивной вентиляции при дыхательной недостаточности на фоне вирусной пневмонии в предыдущие эпидемии. Рассмотрим три исследования. Первое – о гриппозной пневмонии с тяжелым ОРДС. Одиннадцати из двадцати пациентов при помощи неинвазивной вентиляции удалось избежать интубации. У девяти пациентов неинвазивная вентиляция не была успешной (но у большинства из них показатели PO2/FIO2 изначально были очень низкими).
Дальше – атипичная пневмония 2004 года. 77% пациентов благодаря НИВЛ избежали интубации и всех связанных с ней рисков и последствий. Затем эпидемия МЕRS. Было масштабное исследование четырнадцати клиник Саудовской Аравии. Они поставили себе целью попытаться вести этот синдром неинвазивно. Большая часть пациентов потом переходила на инвазивную вентиляцию, однако применение НИВЛ не увеличило 90-дневную летальность по сравнению с ранней ИВЛ.
Таким образом, было доказано, что инвазивная вентиляция эффективна в 70% случаев при ОРДС средней и легкой степени, а в отдельных случаях – и при тяжелой. Также неинвазивная вентиляция не ухудшает отдаленный прогноз по сравнению с первичной ИВЛ даже у пациентов с тяжелой степенью ОРДС.
Одно из исследований показало, что PO2 и FIO2 увеличиваются быстрее и лучше, если использовать неинвазивную вентиляцию вместе прон-позицией. Далее по убывающей: просто НИВ, высокопоточный кислород плюс прон-позиция, просто высокопоточный кислород. Это еще раз подчеркивает важность позиционирования.
Исследование, основанное на случаях 141 пациента, показало, что неинвазивная вентиляция снизила смертность по сравнению с инвазивной. С другой стороны, на инвазивную вентиляцию попадают люди в тяжелом состоянии, смертность в этой категории пациентов составляет до 80%, поэтому оценить эти данные корректно сложно. Но, согласно нескольким другим исследованиям, применение НИВЛ вместо раннего ИВЛ не ухудшало показатели смертности, что тоже важно. В целом пока нет окончательных данных по этому вопросу, но все больше авторов солидарны в том, что применение НИВЛ часто бывает более выигрышным.
Все рассмотренные авторы сходятся в том, что при легком течении болезни (PaO2/FiO2-200-300) показан высокопоточный кислород (ВПК) и прон-позиция (ПП), а при умеренном (PaO2/FiO2-100-200) предпочтительнее неинвазивная вентиляция (НИВ) и ПП. Сочетание ВПК с НИВЛ может быть лучшим вариантом.
О тактике при тяжелой степени ОРДС еще остается много вопросов. Некоторые исследователи рекомендуют раннюю эндотрахеальную ИВЛ, другие уверены, что даже при тяжелой форме заболевания и выраженной гипоксии все равно стоит пытаться использовать НИВЛ (естественно, с низким порогом к интубации и с четким отслеживанием эффективности).
Из этого обзора исследований можно сделать вывод о том, что из-за неоднородности клинической картины пневмонии и ОРДС при COVID-19 высоко оправдан индивидуальный несхематичный подход к вентиляции.
Оказалось, что новую коронавирусную инфекцию люди переносят очень по-разному. Например, поражение очаговое одинаковое, но у кого-то гипоксия, у кого-то нет. У одних пациентов очень выраженная одышка и перегрузка вентиляторной мускулатуры, а другие довольно спокойны. Это тоже определяет показания к вентиляции. Авторы говорят о том, что при тяжелом течении COVID-19 не всегда бывает ОРДС, а если он и развивается, то протекает нетипично, не ступенчато, поэтому не всегда типично отвечает на предложенную по схемам ОРДС-терапию.
Параметры НИВЛ при пневмонии COVID-19
Рекомендовано начинать с низких параметров:
В общем, это неагрессивные, маленькие цифры, которые даже во время бодрствования вполне себе переносимы.
Лучшие кандидаты для применения ранней неинвазивной стратегии — это пациенты с ХОБЛ, с гиперкапнической дыхательной недостаточностью любого генеза (нейромышечной, паллиативной, кардиогенным отеком легких, обострением астмы, после операций на грудной клетке и брюшной полости, пациенты с ожирением, иммуносупрессией). Для этой маски очень важен комплаенс, а если нет приверженности, пациент против, ажитирован, все остальное уже не имеет значения.
В исследованиях я нашла несколько интересных моментов. Пишут, что при развитии у этих пациентов дыхательной недостаточности (ДН) второго типа, гиперкапния, скорее всего, объясняется увеличением мертвого пространства. Также пишут, что если тяжелую гиперкапнию невозможно контролировать, несмотря на увеличение частоты дыхания до 35/ мин, то нужно увеличивать объем вентиляции (начинаем с 6 и можно увеличивать дальше, но не превышать PEEP более 15 и PРlat более 30 см Н2О, то есть вентиляция не должна быть слишком агрессивной).
Итак, мы смотрим за падением сатурации, всегда имея в виду, что она падает не только из-за неэффективности вентиляции, но и из-за того, что пациент снимал маску, из-за того, что в этот момент произошла аспирация, и по другим причинам. То есть не обязательно сразу грешить на неэффективность инвазивной вентиляции. Если PaO2/FiO2 значительно улучшаются, частота дыхания снижается при относительно низком используемом объеме, тогда принимаем решение продолжать НИВЛ, откладывая ИВЛ. Если сатурация сохраняется на уровне 90% или снижается и сохраняется тахипноэ при использовании максимального дыхательного объема, тогда рассматривается вопрос об интубации.
Почти все авторы практикуют комбинацию неинвазивной вентиляции с кислородотерапией. Во-первых, можно давать кислород вместо неинвазивной вентиляции, когда плохо переносится маска. В этом случае можно периодически ее снимать и предлагать пациенту канюлю или высокопоточный кислород. Во-вторых, в перерывах, когда нужно поговорить с пациентом, или покормить его и т.д. В-третьих, вместе с неинвазивной вентиляцией, когда нужно корректировать и то, и другое одновременно. Причем можно под маску поставить канюлю, а можно присоединить кислород к контуру. Допустимо использовать НИВЛ и кислород в комплексе, если при нахождении на неинвазивной вентиляции у пациента сохраняется сатурация менее 90% или напряжение кислорода менее 55 на максимально рекомендованных настройках.
Уже доказано, что среднее время на ИВЛ при COVID-19 значительно больше, чем при классическом ОРДС. И это отличает его от других описанных ранее ОРДС. При этом у большинства пациентов с COVID-19 наблюдается высокий респираторный драйв, т.е. одышка.
Она выражена иногда даже неадекватно гипоксемии: бывает, что одышка сильная, хотя сатурация неплохая. Это происходит в том числе из-за цитокинового шторма и прямых нейротропных эффектов этого вируса на дыхательный центр, вызывающих нейропатию. НИВЛ рекомендуется в том числе для того, чтобы после экстубации предотвратить повреждение легких. Порой в случае чрезмерных усилий на вдохе происходит перерастяжение легких из-за низкого внутриплеврального давления и высокого дыхательного объема, что может вызвать повреждение паренхимы, т.е. пациент сам себя повреждает.
Следующее – это защита диафрагмы. НИВЛ позволяет уменьшить слишком интенсивную работу мышц после экстубации, т.е. неконтролируемую одышку. Ведь если чрезмерная работа какое-то время сохраняется, возникает отек диафрагмы со снижением в последующем ее сократительной способности, из-за прямого разрушения саркомера. То есть из-за этой гиперактивности разрушается вещество мышцы. Это называется вентилятор-индуцированное повреждение диафрагмы, оно ведет к более длительному времени вентиляции и увеличению количества осложнений.
Применять НИВЛ следует с осторожностью, учитывая опасность аэрозолизации. Основные меры предосторожности: отбор пациентов:
Рекомендации по НИВЛ при COVID-19 в домашних условиях заключаются в том, что дома НИВЛ можно продолжать с соблюдением дистанцирования, с использованием бактериальных фильтров. Возможно потребуется коррекция режима: если у пациента исходно был ХОБЛ или тяжелое апноэ, вероятно, придется сделать терапию менее агрессивной. При поступлении в стационар при отсутствии условий нужно отменить НИВЛ (если это открытый контур, чтобы не подвергать риску соседей), а если условия есть, нужно продолжить НИВЛ в стационаре, по возможности, заменив на закрытый контур.
Поскольку легкие – основной “орган-мишень” вируса SARS-CoV-2, для более эффективного восстановления организма необходимо, в первую очередь, восстановление дыхательной функции. Физическая реабилитация здесь приобретает огромное значение.
Многие рекомендации по реабилитационному периоду основаны на международных рекомендациях по ХОБЛ (с некоторыми модификациями). Пациентам с сохраняющимися астеническими ощущениями особенно нужна реабилитация по восстановлению и мышечной силы, и дыхательной функции.
Много информации содержится в “Методических рекомендациях проведения легочной реабилитации у пациентов с новой коронавирусной инфекцией (COVID-19), внебольничной двухсторонней пневмонии. Версия 1 (11.07.2020)”. Там говорится о реабилитации респираторной функции, мышечной дисфункции и так далее. Во всем мире пристальное внимание сейчас уделяется нутритивной поддержке. Говорится и о реабилитации коморбидных состояний (психологической и медикаментозной).
Цели реабилитации, в первую очередь, облегчить одышку и снять тревогу и депрессию, а в долгосрочной перспективе – максимально сохранить функциональность, улучшить качество жизни и способствовать возвращению пациента в общество.
Методы легочной реабилитации улучшают жизнедеятельность, уменьшают одышку, улучшают качество жизни, сокращают продолжительность и количество госпитализаций, увеличивают толерантность к нагрузке, увеличивают выживаемость, увеличивают бронходилатационный эффект.
Направления респираторной реабилитации:
К.м.н. Зульфия Сукмарова.
Материал подготовлен с использованием гранта Президента Российской Федерации, предоставленного Фондом президентских грантов.
Использовано стоковое изображение от Depositphotos.
Оксигенотерапия при сердечно-сосудистых заболеваниях и инфекции COVID-19
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
В статье рассматриваются вопросы патофизиологии гипоксии, механизмы ее устранения с помощью оксигенотерапии, токсические эффекты кислорода. Освещены современные рекомендации и алгоритмы применения при сердечно-сосудистых заболеваниях, в т. ч. при сочетании с бронхолегочной патологией. С учетом данных доказательной медицины обсуждаются спорные и неясные аспекты кислородотерапии, возможность негативных последствий при неправильном использовании. Обсуждается мировой опыт применения оксигенотерапии при новой коронавирусной инфекции COVID-19, в т. ч. дополнительные методы улучшения оксигенации (прон-позиция), также автор делится личным опытом лечения коморбидных пациентов с COVID-19. Изложены современные методы ингаляционной оксигенотерапии и показания к их применению, включая неинвазивную вентиляцию легких, высокопоточную назальную оксигенацию (перспективную, но малораспространенную в нашей стране методику), различные виды масочной оксигенотерапии, устройства для домашнего применения кислорода.
Ключевые слова: оксигенотерапия, кислородотерапия, гипоксемия, кислород, насыщение крови кислородом, сатурация, острый респираторный дистресс-синдром, новая коронавирусная инфекция, COVID-19, ингаляции, кислородные маски.
Для цитирования: Ухолкина Г.Б. Оксигенотерапия при сердечно-сосудистых заболеваниях и инфекции COVID-19. РМЖ. 2020;11:14-18.
Oxygen therapy for cardiovascular diseases and COVID-19 infection
1 City Clinical Hospital named after S.S. Yudin of the Moscow Health Department, Moscow
2 Multidisciplinary Medical Center of the Central Bank of the Russian Federation, Moscow
The article discusses the pathophysiology of hypoxia, the mechanisms of its elimination with oxygen therapy, and the toxic effects of oxygen. It also highlights modern recommendations and algorithms for application in cardiovascular diseases, including in combination with bronchopulmonary pathology. Given the data of evidence-based medicine, controversial and unclear aspects of oxygen therapy and the possibility of negative consequences if used incorrectly are discussed. The world experience of using oxygen therapy for the new COVID-19, including additional methods for improving the oxygenation (prone position), is discussed, and the author also shares his personal experience in treating comorbid patients with COVID-19. The modern methods of inhalation oxygen therapy and indications for their use, including non-invasive ventilation, high-flow nasal oxygenation (a promising, but no t widely used technique in our country), various types of oxygen therapy with masks, devices for home oxygen therapy are described.
Keywords: oxygen therapy, hypoxemia, oxygen, blood oxygen saturation, saturation, acute respiratory distress syndrome, new coronavirus infection, COVID-19, inhalations, oxygen masks.
For citation: Ukholkina G.B. Oxygen therapy for cardiovascular diseases and COVID-19 infection. RMJ. 2020;11:14–18.
Введение
Оксигенотерапия — применение кислорода с лечебно-профилактическими целями. Получение кислорода (вероятно, из селитры) для обогащения им воздуха впервые применил в XV в. К. ван Дреббель, изобретатель подводной лодки. Идея лечебного применения кислорода была высказана английским естествоиспытателем J. Pristley в 1775 г. В это же время французский врач F. Chaussier применил кислород для реанимации новорожденных, родившихся с асфиксией. В дальнейшем разработкой лечебного применения кислорода активно занимался Пневматический институт, основанный в Англии Т. Beddoes. С начала XIX в. кислородная терапия стала использоваться во врачебной практике, но наиболее широкое распространение она получила с начала XX в. с появлением баллонов со сжатым кислородом. По мере появления промышленного производства приборов и устройств для ингаляционного введения кислорода, разработки новых методик оксигенотерапия прочно вошла в арсенал каждого стационара [1].
Оксигенотерапия широко используется для восстановления доставки кислорода к тканям и устранения гипоксии, которая является существенным звеном патофизиологии многих сердечно-сосудистых и бронхолегочных заболеваний, в т. ч. новой коронавирусной инфекции COVID-19. Однако при кажущейся очевидности и широте применения оксигенотерапии ее эффективность во многих случаях остается недоказанной, нередко она нецелесообразна, а в ряде случаев может увеличить риск смерти. Рассмотрению этих вопросов и посвящен данный обзор.
Физиология оксигенации тканей и патофизиология гипоксии
Поступление кислорода в кровь осуществляется путем простой диффузии через альвеоло-капиллярную мембрану, по градиенту парциального давления. При содержании кислорода около 21% в атмосферном воздухе парциальное давление кислорода в атмосфере составляет около 150 мм рт. ст., при этом в крови его содержание достигает 100 мм рт. ст. Транспорт кислорода кровью осуществляется в двух формах: растворенной в плазме и связанной с гемоглобином. В 100 мл крови растворяется 0,31 мл O2, что недостаточно для оксигенации тканей. Преимущественно кислород переносится в соединении с гемоглобином в эритроцитах: 100 мл крови переносят до 200 мл кислорода. Наиболее важный параметр, по которому можно судить о количестве кислорода, связанного с гемоглобином, — это насыщение гемоглобина кислородом — SаO2, или сатурация. При парциальном давлении кислорода в 100 мм рт. ст. насыщение гемоглобина кислородом в артериальной крови составляет около 97% [2].
Простым способом оценки SаО2 и выявления гипоксемии стала пульсоксиметрия, основанная на различиях в поглощении гемоглобином света в зависимости от насыщения гемоглобина кислородом.
При снижении содержания кислорода в крови в первую очередь (в течение миллисекунд) реагируют клетки каротидного тельца сонных артерий, благодаря чему усиливается вентиляция легких и сердечный выброс. Далее включается множество компенсаторных механизмов для адаптации к условиям гипоксии: изменение вентиляции легких, сердечного выброса, ударного объема, концентрации гемоглобина, дилатации системного микрососудистого русла при одновременном спазме легочного русла, увеличение объема альвеол, спазм артериол в зоне гиповентиляции с целью перераспределения крови в зоны легкого с лучшей вентиляцией.
Молекулярная биология и биохимия клеточного ответа
Прогресс молекулярной биологии позволяет понять связь между патофизиологией заболеваний и клеточным ответом на гипоксию. Разные ткани имеют различную потребность в кислороде, наиболее чувствительна нервная ткань. Механизмы, ведущие к гипоксии, различны: ишемия (снижение доставки крови к ткани), отравление углекислым газом, асфиксия, апноэ сна, тяжелая анемия, высотная болезнь, нарушения соотношения вентиляции и перфузии. В то же время последствия гипоксии для тканей одинаковы.
На уровне клетки 80% кислорода используется митохондриями, 20% — другими органеллами. При этом его парциальное давление в митохондриях чрезвычайно мало — 1–3 мм рт. ст. Кислород используется как донатор электронов в конце электронной транспортной цепочки, в комплексе IV, цитохром-C-оксидазы, с целью синтеза аденозинтрифосфата. В случае дефицита кислорода и его электронов электронная цепь претерпевает компенсаторные модификации. В то же время показано, что в условиях гипоксии клетки происходит прямой перенос электронов в электронную цепь из-за уменьшения потока переносчиков, и таким образом увеличивается количество активных форм кислорода и азота, чьи свободные радикалы чрезвычайно токсичны и приводят к гибели клетки.
Клеточный ответ на гипоксию реализуется через фермент, воспринимающий снижение напряжения кислорода в клетке — пролилгидроксилазу, который запускает реакцию другого фермента — индуцируемого гипоксией фактора (hypoxia-inducible factor — HIF). HIF регулирует транскрипцию генов, ответственных за изменение метаболизма с аэробного на анаэробный. Ферменты, участвующие в окислительном фосфорилировании, блокируются HIF, таким образом, пируват вместо гликолиза используется для образования лактата, способствуя ацидозу. Также HIF способствует увеличению выработки эритропоэтина и фактора роста эндотелия, активирует местный ангиогенез, ускоряя пролиферацию клеток, увеличивая выработку эндотелиального сосудистого фактора роста, дифференциацию и инвазию. HIF стимулирует выработку оксида азота, способствуя вазодилатации. Помимо активации генов, стимулирующих ангиогенез, HIF увеличивает выработку ангиопоэтина, тромбоцитарного фактора роста, фактора роста фибробластов, регулирует метаболизм железа.
Кроме того, было показано, что гипоксия индуцирует воспалительный ответ, в частности, отмечено увеличение содержания в крови провоспалительных цитокинов, интерлейкина 6 (ИЛ-6) и рецепторов к ним, фактора некроза опухоли альфа, С-реактивного белка. В свою очередь, воспаление ведет к уменьшению доставки кислорода к тканям. Таким образом, гипоксия и воспаление оказываются взаимно индуцирующими процессами.
HIF влияет и на имунный ответ: увеличивает содержание аденозинтрифосфата в миелоидных клетках, усиливает фагоцитарную активность нейтрофилов, предотвращает апоптоз нейтрофилов, увеличивая продолжительность жизни нейтрофилов в тканях, испытывающих гипоксию [3].
Оксигенотерапия при сердечно-сосудистых заболеваниях
Оксигенотерапия улучшает кровоток в альвеолах, уменьшает шунтирование крови и снижает давление в легочном артериальном русле, повышая ударный объем и сердечный выброс. При хронических бронхолегочных заболеваниях при длительном применении ингаляции кислорода способствуют обратному ремоделированию в легочных артериолах (уменьшению пролиферации гладкомышечных клеток, фибробластов и синтеза протеинов матрикса). Среди дополнительных эффектов оксигенотерапии было показано усиление бактерицидной активности нейтрофилов, снижение уровня дофамина в каротидных тельцах и, как следствие, уменьшение стимуляции хемотактических триггерных зон в головном мозге.
Следует учитывать, что оксигенотерапия направлена на лечение гипоксемии, но не одышки, таким образом, эффекта при лечении одышки в случае нормального содержания кислорода в крови ожидать не стоит. Кроме того, оксигенотерапия не устраняет причину гипоксемии. У всех пациентов с одышкой или в тяжелом состоянии следует проводить пульсоксиметрию с целью контроля сатурации и своевременного выявления гипоксемии.
Согласно различным рекомендациям по оксигенотерапии пороговым значением для начала оксигенотерапии в большинстве случаев является SaO2 менее 90%, однозначно оксигенотерапия не показана при SaO2 более 92% [4]. Среди пациентов, нередко получающих оксигенотерапию при отсутствии показаний, оказываются пациенты с инсультом без гипоксемии, большинство пациентов с инфарктом миокарда, сердечной недостаточностью. В то же время никогда не нужно прекращать оксигенотерапию у пациента, определенно в ней нуждающегося, с целью уточнения выраженности у него гипоксемии [5].
В зависимости от состояния пациента и ожидаемой потребности в кислороде выбирают средство доставки кислорода. В случае острого заболевания с ожидаемой очень высокой потребностью в кислороде (реанимационные мероприятия, остановка сердца, шок, сепсис, легочное кровотечение, эпилептический статус) выбирают нереверсивную маску, начиная с потока 15 л/мин и достигая целевых значений SaO2. Затем скорость потока постепенно уменьшают, обеспечивая сохранение целевых значений SaO2.
В случае ожидаемой меньшей потребности в кислороде (бронхиальная астма, пневмония, другие заболевания легких, пневмоторакс, тромбоэмболия легочной артерии, сердечная недостаточность) выбор также осуществляется с учетом заболевания и исходной сатурации: это могут быть назальные канюли с потоком 2–6 л/мин или простая лицевая маска с потоком 5–10 л/мин. Если предполагается гиперкапния и исходная сатурация менее 85%, то начинать оксигенотерапию следует также с нереверсивной маски с потоком 15 л/мин.
В большинстве случаев целевые значения SaO2 составляют 94–96%. Некоторые рекомендации указывают на целевые значения 94–98%. Однако результаты исследований свидетельствуют, что среди пациентов, находящихся на оксигенотерапии с достижением сатурации более 96%, отмечается небольшое, но определенное увеличение смертности — на 1% [5].
Для пациентов с риском развития гиперкапнии (например, пациенты с хронической обструктивной болезнью легких — ХОБЛ) целевым значением является сатурация 92% (88–92%). В случае чрезмерной оксигенации риск гиперкапнии возрастает. Риск гиперкапнии имеют также пациенты с тяжелым ожирением (синдром Пиквика), выраженными деформирующими заболеваниями грудной клетки и позвоночника: кифосколиозом, болезнью Бехтерева, нервно-мышечными заболеваниями, бронхоэктатической болезнью, муковисцидозом. В некоторых случаях необходима дополнительная респираторная поддержка при наличии гипоксемии и/или гиперкапнии с респираторным ацидозом.
Оксигенотерапию следует прекратить, если сатурация при дыхании воздухом сохраняется на уровне равном или превышающем целевые значения. В случае риска повторного ухудшения состояния оксигенотерапия может быть продолжена [5].
До недавнего времени считалось, что оксигенотерапия практически безвредна, однако систематический обзор свидетельствует о том, что излишняя оксигенация у пациентов с нормальной сатурацией увеличивает смертность. Обзор включал 25 рандомизированных контролируемых исследований, где пациенты получали свободную или контролируемую оксигенотерапию, смертность пациентов в группе свободной оксигенотерапии оказалась выше [6].
Имеются данные, что у пациентов с инфарктом миокарда и инсультом при SaO2 более 92% проведение оксигенотерапии может оказывать негативное воздействие: среди пациентов с инсультом отмечается увеличение смертности с 69 до 87 на 1000 человек, среди пациентов с инфарктом миокарда достоверного увеличения смертности не наблюдается, однако отмечено увеличение частоты повторной реваскуляризации в течение 6 мес. с 72 до 106 на 1000 человек, развитие повторного инфаркта миокарда в течение 1 года с 51 до 62 на 1000 человек [4].
Оксигенотерапия при коронавирусной инфекции COVID-19
Приблизительно у 14% пациентов с новой коронавирусной инфекцией заболевание протекает в тяжелой форме, основным критерием тяжести при этом является снижение насыщения кислородом крови, что требует госпитализации и оксигенотерапии. Около 5% всех пациентов (и около 25% госпитализированных) нуждаются в пребывании в отделении реанимации, чаще всего в связи с развитием картины острого респираторного дистресс-синдрома [7]. Механизмы развития гипоксемии при COVID-19 продолжают изучаться, одним из основных является тромбообразование в микроциркуляторном русле, связанное с повреждением эндотелия, что приводит к шунтированию крови, развитию ателектазов альвеол. В случае стабильного течения заболевания целевые значения SaO2 — более 90%. В случае тяжелого течения заболевания, картины дыхательной недостаточности, шока — целевые значения SaO2 более 94% [8]. В этом случае оксигенотерапия через носовые канюли или маску чаще всего оказывается недостаточно эффективной, предпочтительна высокопоточная назальная терапия или неинвазивная масочная вентиляция с положительным давлением. Своевременно начатые, эти методы позволяют снизить необходимость интубации и искусственной вентиляции легких (ИВЛ), по данным исследований и метаанализа, проведенных до пандемии COVID-19, причем высокопоточная вентиляция через носовые канюли имеет преимущество по сравнению с обычной оксигенотерапией через носовые канюли и вентиляцией с повышенным давлением [9, 10]. Учитывая нехватку аппаратов ИВЛ и мест в отделении реанимации в период эпидемии, трудно переоценить значение данных методов.
В случае недоступности оксигенотерапии через высокопоточные носовые канюли и неинвазивной вентиляции, а также при развивающейся полиорганной недостаточности или серьезных сопутствующих хронических заболеваниях показана ранняя интубация и инвазивная вентиляция легких. Специальных исследований по изучению оксигенотерапии при COVID-19 не проводилось. Но с учетом опыта, полученного при лечении других критических состояний, оптимальный уровень SaO2 находится между 92 и 96%. Метаанализ 25 рандомизированных исследований показал, что оксигенотерапия без контроля сатурации (с достижением сатурации, близкой к 100%) приводит к росту смертности. В то же время в небольшом исследовании выявлено, что поддержание SaO2 на относительно невысоких значениях (88–92%) также сопровождалось ростом смертности [11].
Вспомогательная методика, используемая в дополнение к оксигенотерапии, — прон-позиция (положение лежа на животе). Этот метод улучшает оксигенацию и исходы у пациентов со среднетяжелым и тяжелым течением респираторного дистресс-синдрома. Предположительно механизм связан с улучшением вентиляционно-перфузионного соотношения и раскрытием спавшихся альвеол в нижнебазальных отделах легких. Как в исследованиях до эпидемии среди пациентов с гипоксемией на спонтанном дыхании, так и в нескольких исследованиях среди пациентов с новой коронавирусной инфекцией, находящихся на оксигенотерапии, было показано улучшение оксигенации и уменьшение потребности в интубации при использовании прон-позиции. Прон-позиция хорошо совмещается с оксигенотерапией через канюли и удовлетворительно — через маску. Используется у пациентов, которые могут длительное время находиться в положении лежа на животе и самостоятельно изменять положение тела. Не применяется у гемодинамически нестабильных пациентов, перенесших в недавние сроки хирургическое вмешательство на органах брюшной полости, имеющих нестабильность позвоночника. Убедительных данных о влиянии прон-позиции на отдаленный исход при COVID-19 в настоящее время нет [12, 13].
В числе практических рекомендаций при лечении пациентов с новой коронавирусной инфекцией и одышкой следует помнить о возможности декомпенсации сопутствующих хронических заболеваний и своевременно проводить дифференциальную диагностику одышки. При COVID-19 одышка не изменяется при перемене положения тела, и практически всегда одышка в покое и при минимальной нагрузке сопровождается снижением SaO2. Иногда можно наблюдать катастрофически низкие показатели пульсоксиметра (до 35–45%), однако без перевода на ИВЛ такие пациенты быстро погибают. Если у пациента одышка в покое, усиливающаяся в горизонтальном положении, но SaO2 в норме, следует думать о декомпенсации сердечной недостаточности, особенно при наличии влажных хрипов в нижних отделах легких. Введение фуросемида в этом случае будет намного эффективнее оксигенотерапии. При новой коронавирусной инфекции преимущественно наблюдается различной степени ослабленное везикулярное дыхание, больше в нижних отделах. Степень ослабления дыхания обычно коррелирует с данными компьютерной томографии; иногда выслушивается крепитация в нижних отделах.
У пациентов с ХОБЛ, наоборот, на фоне сниженной сатурации (82–90%) одышка не отмечается, и оксигенотерапия должна проводиться с осторожностью, с контролем содержания СО2 в крови (исследование кислотно-щелочного состояния) с целью избежать гиперкапнии. Появление свистящих хрипов позволяет заподозрить бронхообструкцию, в этом случае введение бронходилататоров через небулайзер заметно облегчит состояние пациента, малопоточная оксигенотерапия может выступать дополнительным методом лечения. Несмотря на кажущуюся простоту такой дифференциальной диагностики, на практике в связи с перегруженностью врачей и ориентацией на «типовое» лечение COVID-19 данные состояния нередко распознаются с задержкой.
Технические аспекты оксигенотерапии
Основным методом получения медицинского кислорода является низкотемпературная (криогенная) ректификация: производят сжатие воздуха и разделение на составные газы из-за разности температур кипения кислорода (-183 °C), азота (-195,8 °C) и аргона (-185,8 °C).
С учетом токсичности кислорода в концентрации более 60% для длительной оксигенотерапии используют воздушную смесь с 40–60% кислорода. Чистый кислород при ингаляции более 30 мин оказывает повреждающее действие на слизистую оболочку дыхательных путей (трахеит), кроме того, из-за нарушения образования и стойкости сурфактанта в альвеолах возникают адсорбционные ателектазы с последующим шунтированием крови, что не позволяет адекватно устранить гипокcемию. Таким образом, высокие концентрации кислорода применяют кратковременно при терминальных состояниях: апноэ, гипоксической коме, остановке сердца, отравлениях окисью углерода.
Основным методом оксигенотерапии является ингаляционный, который включает в себя различные способы введения кислорода и кислородных смесей в легкие через дыхательные пути, проводится с использованием различной кислородно-дыхательной аппаратуры.
Оксигенотерапия хорошо переносится, изредка отмечается сухость и раздражение слизистой носа и глотки, дискомфорт может доставлять ограничение двигательной активности, трудности при принятии пищи. Чтобы уменьшить высушивающее действие кислородно-воздушной смеси на слизистую оболочку дыхательных путей, кислородную смесь увлажняют, пропуская через воду, затем подают под давлением 2–3 атмосферы.
В клинических условиях в зависимости от показаний используются:
Носовые катетеры. Необходимая концентрация кислорода достигается путем регуляции потока кислородно-воздушной смеси: скорость потока от 1 до 6 л/мин создает во вдыхаемом воздухе его концентрацию, равную 24–44%. При выраженной одышке (что приводит к высокой минутной вентиляции легких, превышающей поток кислорода) концентрация вдыхаемого кислорода снижается из-за избыточной потери при выдохе. Назальные канюли (носовые катетеры) обычно хорошо переносятся. В связи с вышеуказанными причинами их не следует применять при гипер- и гиповентиляции.
Лицевые маски. Достоинством масок является их способность лучше справляться с утечкой потока кислорода через рот. С помощью клапанов выдыхаемый воздух выводится наружу, позволяя поддерживать необходимую концентрацию кислорода. При применении стандартной лицевой маски поток кислорода может составлять до 15 л/мин, что обеспечивает более высокую его концентрацию (50–60%) по сравнению с канюлями. При высокой минутной вентиляции легких применение масок, как и катетеров, может быть неэффективно. Маска является самым распространенным способом доставки кислорода. Существуют различные типы масок:
простая (маска Хадсона);
маска с клапаном Вентури — обеспечивает стабильную концентрацию кислорода независимо от типа дыхания пациента путем использования различных клапанов. Достигаемая концентрация кислорода составляет 24–60% в зависимости от типа (цвета) используемого клапана-насадки, для чего скорость потока устанавливается также в зависимости от типа клапана-насадки. Часто используется при ХОБЛ,
т. к. позволяет давать кислород строго в необходимой концентрации, избегая гиперкапнии;
нереверсивная маска (маска с ребризером). Позволяет достичь максимальной концентрации кислорода во вдыхаемой смеси, при этом используется резервуар-мешок, который постоянно наполняется дыхательной смесью с кислородом и благодаря наличию клапана работает только на вдох. Клапаны маски позволяют осуществлять выдох, но препятствуют попаданию воздуха под маску снаружи. Позволяет достичь концентрации кислорода 85–90% при потоке 15 л/мин, не используется для длительной оксигенотерапии.
При проведении оксигенотерапии необходим периодический контроль SaО2. Частота контроля зависит от заболевания, тяжести состояния пациента, выраженности гипоксемии. Контролируя насыщение крови кислородом, подбирают, поддерживают и при необходимости корректируют способ подачи кислорода. Если перечисленные методы оказываются неэффективны и гипоксемия нарастает, может быть показан перевод пациента на инвазивную вентиляцию легких с интубацией трахеи. Однако до этого рассматривают возможность неинвазивной вентиляции легких с созданием положительного давления в дыхательных путях пациента во время выдоха или постоянно. Возможно проведение вентиляции легких через лицевую, носовую маску, шлем или носовые канюли.
Неинвазивная вентиляция легких снижает потребность в инвазивной вентиляции. Позволяет избежать интубации трахеи, тем самым минимизируя риск повреждений верхних дыхательных путей, избежать введения седативных препаратов, обеспечивает: большие безопасность и комфорт для больного; сохранение спонтанного дыхания; снижение риска развития ИВЛ-ассоциированной пневмонии; оставляет возможность контакта с больным; экономически выгодна. Однако методика более сложна и трудоемка для врача, т. к. необходимо непрерывно адаптировать различные параметры под постоянные изменения функции дыхания больного. Имеются и ограничения: невозможность применения при низком уровне сознания, анатомических особенностях больного; возможно повреждение кожи лица при длительном использовании масочной вентиляции; при неадекватном увлажнении и согревании газовой смеси могут наблюдаться повреждение слизистой верхних дыхательных путей, аэрофагия, тошнота, изжога, индивидуальная непереносимость (клаустрофобия) [2].
Высокопоточная оксигенотерапия является разновидностью неинвазивной вентиляции легких, имеет несомненные преимущества перед традиционной оксигенотерапией, более комфортна, лишена многих недостатков масочной вентиляции легких и может быть эффективной альтернативой при острой дыхательной недостаточности различного генеза. При высокопоточной назальной оксигенотерапии увлажненная и нагретая газовая смесь доставляется в дыхательные пути через носовые канюли со скоростью потока 15–60 л/мин с возможностью варьирования доли вдыхаемого кислорода от 0,21 до 1 [14].
При неэффективности неинвазивной вентиляции легких необходима своевременная интубация трахеи и проведение инвазивной (искусственной) вентиляции легких. Рассмотрение данного метода выходит за рамки настоящего обзора.
В домашних условиях при стабильном течении хронических заболеваний бронхолегочной системы или в стационаре при отсутствии возможности доступа к центральному источнику медицинского кислорода (качество которого выше) для продолжительной оксигенотерапии может использоваться медицинский концентратор кислорода. Также применяются кислородные баллоны — обычно для транспортировки пациента с гипоксемией бригадой скорой помощи или внутри стационара, продолжительность ингаляции при требуемой концентрации кислорода около 40% ограничена приблизительно 20 мин.
Можно встретить также кислородные баллончики, например баллончик «Основной элемент» (состав смеси: 90% кислорода, 10% азота, объем кислорода до 17 л, рассчитанных на 110–150 вдохов, без регулятора потока кислорода), однако для продолжительной коррекции гипоксемии объем кислорода в нем недостаточен. Данное устройство позиционируется как средство, позволяющее устранить негативные последствия пребывания в душном помещении, чрезмерных физических и умственных нагрузок.
Заключение
Таким образом, оксигенотерапия, несмотря на более чем вековую историю применения, продолжает активно развиваться, занимая значимое место в лечении основных сердечно-сосудистых и бронхолегочных заболеваний. Значение ее трудно переоценить — нередко она позволяет спасти жизнь пациента, являясь одним из основных методов лечения пациентов с новой коронавирусной инфекцией. Различные аспекты применения кислорода подробно освещены в современных рекомендациях, разработаны показания и алгоритмы применения. В то же время остается ряд спорных вопросов, продолжаются исследования, подтверждающие эффективность оксигенотерапии в одних случаях, демонстрирующие бесполезность и даже негативные эффекты — в других. Дальнейшее изучение применения кислорода, в т. ч. с использованием достижений молекулярно-клеточной биологии, а также прогресс технологий, благодаря которому продолжается разработка новых устройств для оксигенотерапии, закрепят за оксигенотерапией прочное место в повседневной лечебной практике.
Только для зарегистрированных пользователей