Контроль «прорывов» боли и ротация опиоидов
Представляем фрагмент брошюры для врачей «Обезболивание в паллиативной помощи. Практическое руководство для врача», подготовленной благотворительным фондом «Вера». Полная версия брошюры доступна для скачивания по ссылке.
Во время терапии сильной боли у пациентов, которые получают сильные опиоиды замедленного высвобождения, возможны «прорывы» боли, обусловленные непроизвольными или произвольными действиями или процедурами (кашель, икота, тенезмы или боль при движении, при проведении клизмы, боль при санации трахеи и прочее).
• Если в течение нескольких дней приходится применять 3–4 экстренных дозы для «прорыва» боли, то следует повысить дозу основного опиоидного препарата.
• Для расчета экстренной дозы препарата при «прорыве» боли следует воспользоваться таблицей ниже.
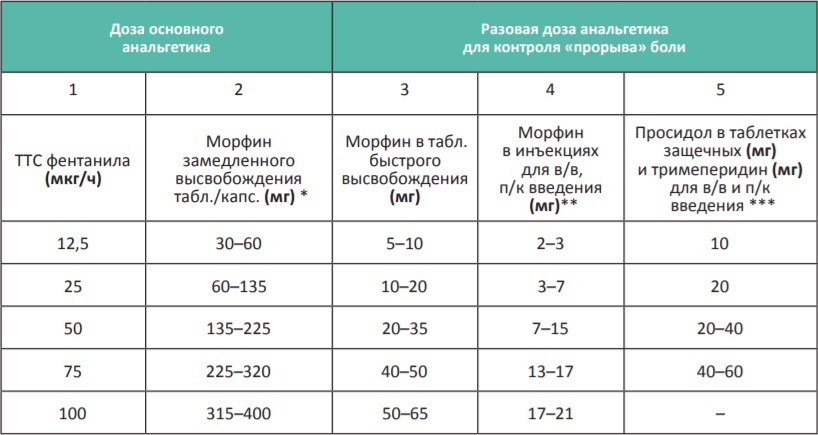
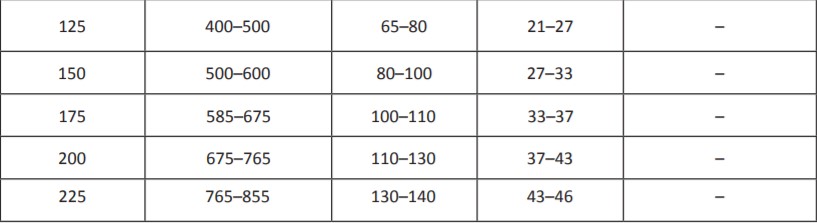
Таблица. Расчет «экстренной» дозы анальгетика для терапии «прорыва» боли и эквипотенциальных доз (ротации опиоидов) различных препаратов в зависимости от дозы основного опиоида
Ротация опиоида проводится в случае плохой переносимости препарата или невозможности дальнейшего приема опиоида. Для этого надо рассчитать по таблице нужную дозу нового анальгетика, но при первом назначении снизить ее на 25–50% для оценки переносимости нового препарата, а затем постепенно повышать до эффективной дозы.
«Прорывная боль» – новый термин, не новая проблема
Как возникает прорывная боль, как ее эффективно диагностировать и чем купировать – об этом статья авторов Г.Р. Абузаровой, С.Е. Лапиной, Р.Р. Сарманаевой, опубликованной в журнале «Российский журнал боли». Текст публикуется с разрешения редакции журнала.
Термин «прорывная боль» (ПБ) появился около 25 лет назад, однако споры по поводу дефиниции этого вида боли до сих пор продолжаются. Еще в 1989 г. Эдмонтонская система стадирования боли при раке ввела впервые термин « incidental pain » – инцидентной боли у онкологических пациентов, подразумевая под ним «боль при провоцирующих обстоятельствах, возникающую внезапно, в результате движений, глотания, мочеиспускания или дефекации» [6]. Годом позже, в 1990 г., R.K. Portenoy и N.A. Hagen впервые предложили термин «прорывная боль» и дали ее собственное определение: «Транзиторное увеличение боли, которое произошло на фоне исходного болевого синдрома умеренной или низкой интенсивности» [26]. Однако в этом определении не оговаривалось, что боль возникает на фоне применения опиоидов, хотя все пациенты, участвовавшие в исследовании, применяли стабильные дозы опиоидов в течение двух дней подряд.
Дальнейшая дискуссия по этой теме получила продолжение в дефиниции ПБ, которую дала экспертная группа Ассоциации паллиативной медицины Великобритании и Ирландии: «Транзиторное обострение боли, которая возникает либо спонтанно, либо в связи с конкретным предсказуемым или непредсказуемым провоцирующим фактором, несмотря на относительно стабильную и адекватно контролируемую фоновую боль» [10]. Кроме этого, экспертная группа также предложила рекомендации по выявлению ПБ и ее терапии:
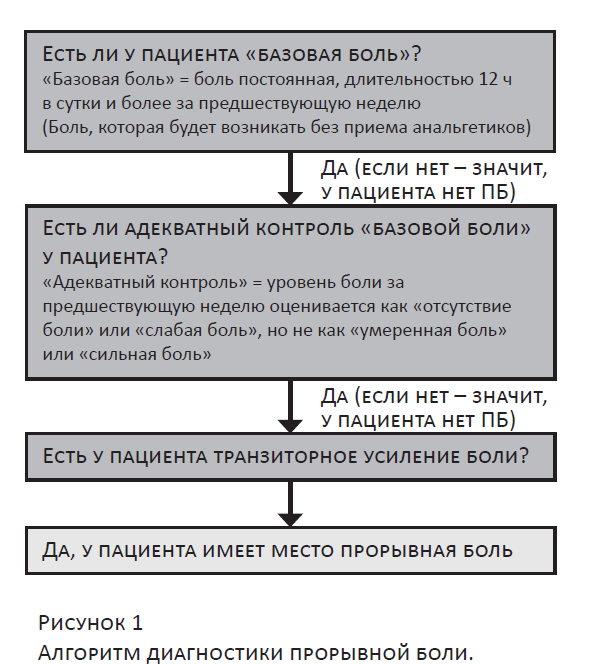
Большинство этих рекомендаций экспертов имеет уровень доказательности D, т.е. это мнение – консенсус экспертов, и только одна рекомендация получила доказательность уровня В: «Доза опиоидного «препарата спасения» должна определяться индивидуально, титрованием препарата». Под дозой «препарата спасения» подразумевается необходимая доза опиоида для контроля ПБ. В рекомендациях был предложен алгоритм выявления и терапии ПБ (рис. 1), который однозначно указывает на то, что базовый уровень боли должен адекватно контролироваться до того, как будет установлен диагноз ПБ.
Принципиальная разница этого определения ПБ в том, что эксперты Ассоциации паллиативной медицины Великобритании и Ирландии признали, что ПБ – это вид боли, который возникает на фоне подобранной адекватной анальгетической терапии. Таким образом, под это определение не попадают боли, обусловленные окончанием действия разовой дозы основного анальгетика, или спонтанные боли, возникающие у пациентов, которые не получают какой-либо вид анальгезии.
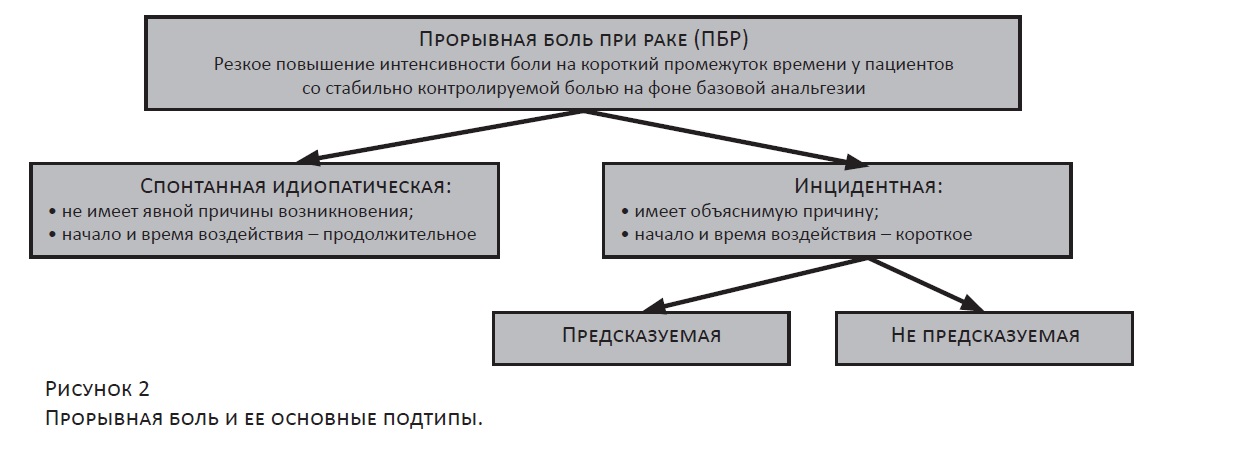
По мнению ведущих специалистов Международной ассоциации по изучению боли (IASP), исследователей в области опиоидной терапии при онкологической боли S. Mercadante и R.K. Portenoy, в настоящее время достигнут консенсус в определении дефиниции ПБ при раке. В конце 2016 г. в декабрьском выпуске онлайн журнала «Боль» достаточно подробно описан 25-летний процесс формирования определения ПБ и предложена современная его трактовка: «Прорывная боль – это эпизод сильной боли, которая возникает у пациентов, получающих стабильную опиоидную терапию в режиме, позволяющем контролировать постоянную боль на уровне слабой» [20]. Авторы предлагают ввести классификацию прорывной боли при раке (ПБР), выделяя два основных типа: спонтанную идиопатическую и инцидентную. В свою очередь идиопатическую боль также предложено разделить на предсказуемую – ожидаемую (или прогнозируемую) и непредсказуемую – внезапную (рис. 2) [20].
Эпидемиология ПБ
Распространенность ПБ значительно варьирует в зависимости от методики обследования и способа ее выявления, а также от индивидуальных особенностей обследованных больных. В исследованиях по изучению ПБ распространенность составляла от 19% до 90% [5, 12, 31, 36]. Многие авторы сообщают о распространенности ПБ в диапазоне 40–70% [13]. Распространённость ПБ в разных странах оценивается следующим образом: 80,1% – в англоговорящих странах, 69,4% – в странах Северной и Западной Европы, 54,8% – в странах Южной Америки и 45,9% – в странах азиатского региона [8].
Типичные характеристики ПБ при злокачественных новообразованиях Актуальность поднятой проблемы вызвала большое число публикаций на тему диагностики и терапии ПБ, что дало возможность систематизации полученных данных. Во втором издании учебника по паллиативной медицине, вышедшем в 2015 г. под редакцией E. Bruera и соавт., приводятся следующие характеристики ПБ [32]:
В настоящее время принято считать, что ПБ имеет гетерогенный характер и возникает 3–4 раза в сутки, хотя частота приступов может заметно изменяться. У многих пациентов ПБ зависит от времени суток, поэтому возникает преимущественно днем или ночью, может зависеть от положения тела, от двигательной активности [9, 35].
Иногда пик болевой активности может продолжаться до 2–4 ч. В большинстве случаев ПБ является обострением исходной боли, но она может быть усугублением различной по природе происхождения боли. Некоторые пациенты испытывают боль более одного типа ПБ. Интенсивность ПБ оценивается, как правило, от умеренной до тяжёлой [9]. Начало приступа ПБ зачастую непредсказуемо, хотя есть исследования о том, что 20–40%случаевПБассоциированыс двигательной активностью, а от 13% до 30% возникают из-за окончания действия разовой дозы основного анальгетика [16, 36]. Некоторые авторы утверждают, что приступы невропатической ПБ значительно короче и чаще, чем приступы ноцицептивной ПБ [25, 36].
Факторы, провоцирующие прорывную боль
Больные с ПБ, как правило, имеют более высокие показатели интенсивности основной боли, чем пациенты без эпизодов ПБ. Некоторые авторы утверждают, что ПБ при метастатическом поражении костей, возникающая при движениях (в отличие от боли в покое), плохо поддается лечению и является толерантной к обезболивающим препаратам [16, 18].
Так, например, только у 6% пациентов с болевым синдромом, обусловленным метастатическим поражением костей, удалось адекватно контролировать боль при обращении по поводу обезболивания в многопрофильную клинику в Дании [3]. В одном из международных многоцентровых исследований ECS-CP было установлено, что пациенты с «инцидентной болью» нуждаются в тщательно подобранных и более высоких дозах опиоидов [11]. Наличие ПБ в значительной степени ограничивает качество жизни больных, влияет на двигательную активность и вызывает повышение уровня депрессии и тревоги, бессонницу, ограничивая социальную и общую активность [8, 12, 16].
Считается, что неконтролируемые приступы ПБ напоминают пациентам об их онкологическом заболевании и усиливают ощущение потери контроля над онкологическим процессом. [34]. Больные с ПБ вынуждены менять свой образ жизни или даже прекращать трудовую деятельность, что в свою очередь сопровождается значительным психологическим стрессом.
Диагностика и выявление ПБ
Для диагностики ПБ используются опросники, предложенные разными авторами. Начиная с 2007 г., Breakthrough Pain Questionnaire (BPQ) (10 вопросов) был использован в нескольких исследованиях как для оценки эпидемиологических данных, так эффективности лекарственных препаратов, однако его валидность не была подтверждена. Позже международная группа экспертов разработала усовершенствованную его версию под названием «Alberta Breakthrough Pain Assessment Tool» (ABPAT), которая состоит из 13 вопросов [15]:
Уже спустя несколько лет, в 2012 г., этот опросник был дополнен и до сих пор применяется для оценки распространенности и описания характеристик боли в относительно больших когортах онкологических пациентов. Он эффективен в выявлении неудовлетворенных потребностей онкологических больных и подходит для оценки результатов лечения [30].
Лечение прорывной боли
Большинство авторов и исследователей в области ПБ признают, что она является общепризнанной проблемой, которая еще далека от полноценного решения [4, 14, 28, 29]. Идеальный препарат для терапии ПБ должен обладать характеристиками:
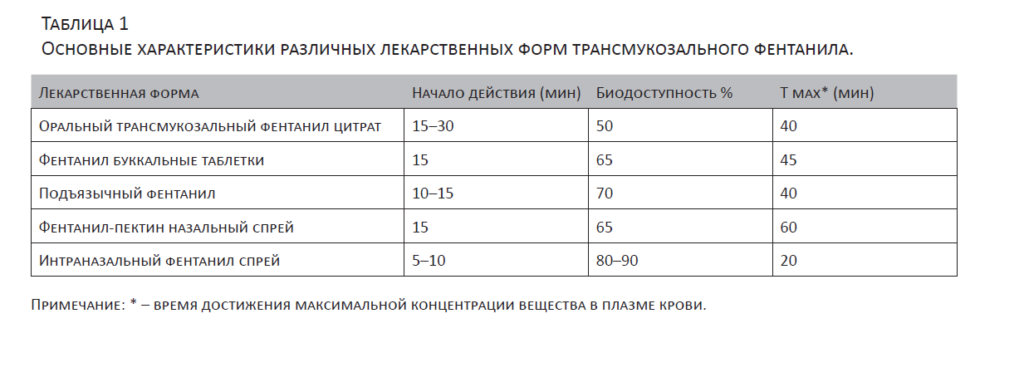
Первым лекарственным препаратом, специально предназначенным для терапии ПБ, с наиболее быстрым началом действия и более короткой его продолжительностью были оральные трансмукозные пластины с фентанилом цитратом [17]. Эта лекарственная форма фентанила была создана менее чем через десять лет после публикации первого углубленного обзора по ПБР, когда стала очевидной необходимость применения специальных лекарственных форм с быстрым началом действия в лечении ПБР [17]. Для изучения его эффективности при ПБР была разработана новая методология исследования, в котором оценивались безопасность и эффективность в принимаемых самостоятельно опиоидов в домашних условиях. Эта методика была впоследствии использована для изучения других аналогичных препаратов, применяемых трансмукозально (интраорально или назально) с сильнодействующим липофильным опиоидным препаратом, как правило, это был фентанил. В течение последних 15 лет были созданы многочисленные трансмукозальные лекарственные формы, содержащие фентанил, каждая из которых имеет свои особенности (табл. 1) [20].
Данные, приведённые в табл. 1, дают основания считать, что интраназальный спрей является на сегодняшний день наиболее оптимальной лекарственной формой фентанила для терапии прорывов боли. Из всех существующих неинвазивных препаратов фентанила интраназальный спрей имеет наиболее быстрое начало действия, оптимальную продолжительность и наиболее высокую биодоступность, что удовлетворяет требованиям «идеального» препарата для терапии ПБ.
Представленные для анализа данные проведенных исследований не дали возможности сравнить корреляцию применяемых доз фентанила в различных лекарственных формах (таблетках буккальных, трансмукозальных пластинах и интраназальном спрее) с дозой базового опиоидного анальгетика, хотя такая взаимосвязь прослеживалась в двух открытых исследованиях [21, 23], о ней также сообщили авторы в обсервационном когортном исследовании [22]. В результате эксперты ЕАПП пришли к следующим выводам:
В тесном сотрудничестве с ЕАПП в 2012 г. было подготовлено французское руководство по паллиативной помощи, включавшее раздел лечения ПБ [27, 33].
Однако, несмотря на то, что руководство ЕАПП 2012 приводит недостаточно доказанные рекомендации по использованию опиоидов немедленного освобождения с коротким периодом полураспада для превентивного лечения ПБ, французское руководство по ПБ предлагает использовать зарегистрированные в 2011 г. 5 новых трансмукозальных форм фентанила для контроля ПБ, вызванной медицинскими процедурами у пациентов, которые уже получают сильные опиоиды.
Французская группа экспертов считает, что одинаковые дозы разных лекарственных форм препаратов фентанила трансмукозального не являются равноэквивалентными из-за различной скорости их адсорбции и биодоступности. В руководстве предлагается применять соответствующие методы для титрования дозы для каждой отдельной лекарственной формы фентанила на основании оригинальных исследований каждого лекарственного средства, в связи с чем французское законодательство (Haute Autorité de Santé) ввело ограничения для повторного применения трансмукозального фентанила; его применение рекомендуется не ранее чем через 4 часа после первого приема. Однако французская группа экспертов допускает использование дополнительных доз фентанила в течение более короткого периода для пациентов с ПБ, если пациент находится под постоянным наблюдением. В руководстве обращается внимание на то, что фармакокинетика фентанила требует осторожности при повторном назначении, поэтому французская группа экспертов рекомендует осуществлять мониторинг за сонливостью, седацией и урежением частоты дыхания [27].
В марте 2010 г. правительство Италии приняло новое законодательство, направленное на улучшение диагностики и лечения боли, которое обязывает врачей и медсестер регистрировать интенсивность и характеристики боли в карте каждого пациента. Это дало возможность экспертам по терапии онкологической боли организовать национальный наблюдательный центр по контролю за исполнением этих мер (Italian Oncologic Pain Survey – IOPS), а также за диагностикой и лечением боли [19]. В частности, эксперты IOPS исследовали ПБ и ее эпидемиологию, типы, варианты терапии. В результате было показано, что трансмукозальные формы фентанила обеспечивают более эффективное и быстрое обезболивание по сравнению с пероральным морфином. По мнению итальянских коллег пероральные опиоидные препараты показаны при прогрессирующих ПБ или для упреждающей пероральной терапии за 30 мин до предсказуемого приступа ПБ. С точки зрения итальянских экспертов у пациентов, получающих высокие дозы опиоидов в качестве базового обезболивания, не следует проводить титрование, начиная с минимальных доз фентанила, так как они имеют толерантность к опиоидным препаратам, процесс будет занимать много времени. Проблема пропуска нескольких шагов титрования у таких пациентов пока не решена и требует дальнейшего исследования на большей выборке пациентов. Выбор лекарственной формы фентанила должен зависеть от клинических и практических условий использования препарата в соответствии с показаниями к применению и от возможности применить систему доставки препарата и состояния слизистой оболочки, которая может пострадать из-за предшествующей лучевой терапии или химиотерапии. Для обеспечения постоянной эффективности лекарственных форм фентанила необходимо периодически проводить оценку клинической картины и условий, способных влиять на биодоступность этих форм.
В заключение, эксперты IOPS пришли к выводам, что необходимо следовать четкому алгоритму диагностики ПБ: тщательно проводить оценку боли, что позволит индивидуализировать лечение; препараты фентанила, независимо от их стоимости, являются основой фармакотерапии ПБ, хотя пероральные опиоиды тоже могут быть эффективны в определенных случаях; при определении дозы трансмукозального фентанила, следует учитывать исходный уровень опиоидной толерантности больных. Принимая во внимание недостаточное количество сравнительных исследований между разными системами доставки фентанила, выбор должен быть основан на индивидуальном подходе в соответствии с началом ПБ, а также после тщательной диагностики состояния слизистых оболочек с учетом предпочтений и опыта пациентов [19].
Рекомендации NCCN предлагают для терапии прорыва боли применять «спасительную» дозу того же опиоида, который применяется для терапии базовой боли. Величина дозы препарата «спасения» составляет 10–20% от суточной дозы основного опиоида. В рекомендациях американских коллег оговаривается, что препараты фентанила трансмукозального могут быть рекомендованы только для пациентов, толерантных к опиоидам, и могут применяться при тех видах боли, которые не являются следствием недостаточной дозы основного опиоида. Титрацию препаратов фентанила начинают с самых низких доз.
В России в 2016 г. были одобрены Минздравом и опубликованы клинические рекомендации «Хронический болевой синдром (ХБС) у взрослых пациентов, нуждающихся в паллиативной медицинской помощи», в которых дается определение ПБ: «Прорывная боль – временное резкое спонтанное или эпизодически возникающее усиление боли на фоне приема препаратов в пролонгированных лекарственных формах [1]. Обычно проявляется внезапным, очень интенсивным и коротким по времени приступом боли». Кроме того, отдельная глава посвящена титрованию дозы опиоида и терапии «прорывов боли». Доза препарата «спасения» при прорыве боли определяется в размере 1/6 от общей суточной дозы базового анальгетика.
Заключение
В заключение следует признать, что опиоидные анальгетики очень важны в терапии ПБ, однако необходимо учитывать, что боль является многофакторным феноменом, и для ее контроля надо придерживаться мультимодального подхода, ориентированного на особенности и нужды пациента, учитывать направленность терапии основного заболевания, являющегося причиной боли. Многопрофильный и междисциплинарный врачебный план терапии боли должен базироваться на следующих параметрах: стадия заболевания, течение болезни, функциональный статус пациента, цель терапии основного патологического процесса пациента. Следует поддерживать контакт с пациентом и его семьей, знать опасения и ожидания, проводить постоянное наблюдение за состоянием больного и оказывать духовную поддержку. Несмотря на большой опыт применения опиоидных анальгетиков для терапии хронической боли, вызванной злокачественными опухолями, существует острая необходимость в дальнейшем накоплении научного опыта, практических рекомендаций по этой проблеме, что даст возможность обучать медицинский персонал, пациентов и их родственников способам безопасного контроля ПБ.