Пропионовые (пропионовокислые) бактерии
Пропионовые бактерии: ближе, чем вы думаете
Эксперты подсчитали, что общий вес бактерий, живущих в организме человека, составляет два килограмма. Они населяют его как жители в многоквартирном доме – повсюду. Знакомим вас с одним из «жильцов» — пропионовые бактерии.
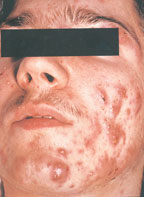
Пропионовые бактерии найдете на коже лица и не только…
Пропионовокислые бактерии входят в состав облигатной микрофлоры желудочно-кишечного тракта. Они продуцируют пропионовую кислоту, которая образуется в результате пропионового брожения (аналогичного молочнокислому, вызываемому лактобактериями). Но, в отличие от лактобактерий, все штаммы которых являются полезными и которые ни при каких обстоятельствах не могут стать патогенными, некоторые виды пропионовых бактерий могут быть условно-патогенными и причинять вред организму человека при снижении иммунитета.
Штамм Propionibacterium acnes относится к условно-патогенной флоре и живет на коже здоровых людей, не вызывая патологии. Вы можете не замечать их активности, но лишь до той поры, пока иммунитет организма высокий. Когда он ослаблен и защитные механизмы снижены, даже самые безобидные представители патогенной сферы способны причинить дискомфорт.
Как способны вам навредить пропионовые бактерии? Их «работу» легко увидеть воочию – на своем лице. Именно они становятся причиной возникновения угрей или прыщей — акне, а также они могут стать причиной блефарита, эндофтальмита и других заболеваний глаз.
Дело в том, что пока иммунитет человека высокий и нет предпосылок к каким-либо заболеваниям, пропионовые бактерии безобидно живут в полостях сальных желез и волосяных фолликул. В своем большинстве они никак себя не проявляют. Но это лишь до той поры, когда организм не дает сбой.
Как развивается воспалительный процесс с участием пропионовых бактерий
В воспалительном процессе с участием пропионовых бактерии можно выделить четыре стадии, которые развиваются одновременно:
Избавляемся от проблемы: профилактика и лечение
Акне, воспалительный процесс с участием пропионовых бактерии, поддаётся лечению. В зависимости от сверхчувствительности организма к этому типу бактерий одни пациенты довольно быстро избавляются от акне, у других оно проходит с осложнениями.
Схему лечения назначает врач-дерматолог. Она может включать в себя диету, нанесение лечебных мазей, приём антибиотиков, в сложных случаях применение лазера.
Роль пропионобактерий в развитии угревой болезни
Акне – мультифакторная болезнь, но специалисты выделяют 4 основных звена ее патогенеза: фолликулярный гиперкератоз, повышенная выработка кожного сала, воспаление, увеличение колонизации пропионибактерий. Каждый квадратный сантиметр кожи заселен более чем миллионом микроорганизмов, P. Acnes – один из ее жителей. Но при определенных условиях из дружелюбных бактерий Propionibacterium acnes превращаются в провокаторов угревой сыпи.
Как пропионибактерии влияют на развитие угревой болезни? 17
Propionibacterium acnes – грамположительные факультативные анаэробнык бактерии. В результате закупорки каналов сальных желез и увеличения выработки кожного сала (себума) создается благоприятная среда для их размножения внутри волосяных фолликулов.
Постоянный рост колонизации P. acnes влияет на активность метаболических процессов, в результате выделяются медиаторы воспаления. К этой группе веществ относятся липазы пропионибактерий, которые расщепляют триглицериды себума на свободные жирные кислоты. Они оказывают раздражающее действие на стенки фолликулов.
Активация патогенетических свойств пропионибактерий может быть связана с рядом экзогенных факторов, например, полом, возрастом, генетикой. На образование кожного сала в свою очередь оказывают влияние андрогены.
Как Клиндовит® борется с пропионибактериями?
Использование антибиотиков в терапии угревой болезни связано с их противомикробным и противовоспалительным действием. Но исследования показывают рост штаммов пропионибактерий, резистентных к антибактериальным препаратам. Так, в 1976 году не было зафиксировано ни одного случая антибиотикорезистентности, а в 2011 году, обследовав 1000 пациентов с угревой болезнью, ученые обнаружили 100% резистентность к эритромицину. 10
АКНЕ: патогенез и современные методы лечения
Угревую болезнь (акне) относят к числу часто встречающихся в практике врача-дерматолога заболеваний кожи. Дебют заболевания обычно проявляется у девочек в возрасте от 12 до 14 лет, у мальчиков — в 14–15 лет.
Угревую болезнь (акне) относят к числу часто встречающихся в практике врача-дерматолога заболеваний кожи. Дебют заболевания обычно проявляется у девочек в возрасте от 12 до 14 лет, у мальчиков — в 14–15 лет. В этом возрасте возможны два варианта течения заболевания — «физиологические» акне и «клинические» акне, наблюдаемые у 15% пациентов, которые требуют назначения лечения. У 7% пациентов возможно развитие поздних акне, возникающих после 40 лет [1, 3, 5].
Угревая болезнь нередко является одним из осложнений жирной или смешанной форм себореи. У значительной части больных угревая болезнь склонна к хроническому течению, частым рецидивам и нередко оказывается резистентной к проводимой терапии.
Патоморфологически вульгарные угри представляют собой гнойное воспаление сальной железы и перигландулярной ткани. Принято различать несколько клинических разновидностей этого заболевания. К более легким и относительно благоприятно протекающим формам относят вульгарные или юношеские, папулезные и пустулезные угри. Они легче поддаются лечению и обычно не оставляют после себя грубых рубцовых изменений на коже. Напротив, индуративные, сливные, флегмонозные и конглобатные угри в связи с резистентностью к проводимой терапии, частыми рецидивами и возникновением при этих формах грубых косметических дефектов представляют для врача и больного сложную медицинскую и социально-психологическую проблему [3].
Психоэмоциональные расстройства выявляются у 40–50% пациентов с угревой болезнью, ведущим является нозогенная депрессия невротического уровня, чаще протекающая по астено-тревожному и тревожному типам. Наибольшая частота психоэмоциональных расстройств наблюдается при II–III степени тяжести акне, при этом характерна обратная зависимость выраженности психоэмоциональных расстройств от степени тяжести и длительности болезни [2].
Поэтому важным для практического врача является ранняя диагностика, правильная клиническая оценка, своевременное назначение эффективных и безопасных препаратов в зависимости от клинической формы заболевания, что позволяет избежать состояния дисморфофобии, неудач в лечении и улучшить качество жизни больных.
Патогенез акне является мультифакторным. На сегодняшний день выделяют четыре ведущих фактора в этиологии заболевания: фолликулярный гиперкератоз, увеличение количества Propionibacterium acnes, изменение продукции кожного сала и воспаление.
Начальным этапом формирования заболевания является появление микрокомедонов, которые в дальнейшем колонизируются Propionibacterium acnes. Микрокомедоны являются результатом развития двух процессов — гиперпролиферации кератиноцитов акроворонки волосяного фолликула и избыточной продукции кожного сала, что в сочетании приводит к закупорке фолликула и формированию открытых и закрытых комедонов. Для кератиноцитов характерно увеличение тонофиламентов и десмосом, повышенное количество кератинов К6 и К16 [9].
Propionibacterium acnes являются анаэробными резидентными представителями микрофлоры кожи человека, способными проявлять свои патогенные свойства только в определенных условиях. Propionibacterium acnes участвуют в развитии воспаления в очаге заболевания, способствуя освобождению хемотаксических факторов и цитокинов, а также превращению триглицеридов кожного сала в свободные жирные кислоты.
В механизме развития акне важными являются следующие компоненты патогенеза — относительный недостаток линолевой кислоты, действие андрогенов и свободных жирных кислот. На продукцию кожного сала огромное влияние оказывают андрогены, которые в большом количестве начинают поступать в кожу в пубертатном периоде, определенное значение имеет гормон роста, инсулиноподобный фактор роста и вещества, активирующие образование пероксисом [8].
Мишенями действия половых гормонов в коже являются эпидермис, волосяные фолликулы, сальные железы, фибробласты. На продукцию кожного сала влияют гормоны тестикулярного или овариального (свободный тестостерон) и надпочечникового (дегидроэпиандростерон, андростендион) происхождения. Подобное действие оказывает и предшественник тестостерона, эстрогенов и адренокортикостероидов — прогестерон, обладающий андрогенным и антиэстрогенным воздействием на секрецию сальных желез. Этим объясняется повышение салоотделения и усиление образования акне в предменструальный период.
Важное значение имеет не только повышение уровня андрогенов, но и повышенная чувствительность клеток-мишеней, в частности клеток сальной железы, к андрогенам, циркулирующим в крови.
В патогенезе угрей важная роль отводится дефициту цинка, который регистрируется у 80% больных. На фоне цинкдефицитного состояния возрастает темп экскреции кожного сала, а тяжесть течения болезни коррелирует со степенью снижения цинка в организме больного. Цинк снижает активность 5a-редуктазы, что способствует нормализации соотношения гормонов и ведет к уменьшению салоотделения.
Наружная терапия является первой линией лечения акне у новорожденных, в детском возрасте, при дебюте акне и юношеских угрях. Назначение только наружной терапии показано при легких воспалительных и невоспалительных формах акне, невоспалительных формах акне средней тяжести. Во всех остальных случаях назначается комбинированная терапия с системными препаратами.
Препараты для наружной терапии назначаются длительно, минимальный курс лечения составляет 3 мес, после окончания курса необходимо назначение лекарственных средств с профилактической целью для предотвращения обострения заболевания.
В 2002 г. разработаны рекомендации и алгоритм патогенетического лечения различных форм акне (XX Всемирный конгресс по дерматологии, Париж, 2002), в которых препаратами первого выбора врача при лечении акне являются местные ретиноиды. Топические ретиноиды влияют на процессы ороговения (кератинизацию и десквамацию), снижают салоотделение, усиливают пролиферацию эпителиоцитов кожи и обладают определенным противовоспалительным действием. Наиболее перспективным является адапален (дифферин), обладающий хорошей переносимостью, отсутствием фотосенсибилизирующего действия, высокой эффективностью при комедональных и папуло-пустулезных акне [6]. Адапален применяется после очищения кожи 1 раз в сут на ночь, стойкое клиническое улучшение наблюдается через 3 мес, в поддерживающем режиме препарат наносят 2–3 раза в неделю.
Бензоила пероксид (базирон АС, окси-5, окси-10) после нанесения на кожу приводит к освобождению активных форм кислорода, уменьшению синтеза свободных жирных кислот и образования микрокомедонов. Препарат обладает выраженным влиянием на P. acnes, St. epidermidis, Malassezia furfur и снижает риск развития резистентности при комбинировании с антибиотиками. Выпускается бензоил пероксид в виде геля 2,5 –10% и 5–10% лосьона. Бензоил пероксид наносят на кожу 2–3 раза в день в течение 1–3 мес. Побочными эффектами препарата являются раздражающее действие, особенно при применении высоких концентраций, а также повышение фоточувствительности за счет истончения рогового слоя. Препарат способен обесцвечивать волосы, поэтому рекомендуется его применение при сочетании акне и гипертрихоза. Противопоказанием является повышенная чувствительность к компонентам препарата.
Широко применяется для наружного лечения акне азелаиновая кислота (скинорен), обладающая способностью нормализовать процессы кератинизации фолликула, антимикробным и противовоспалительным действием, способная уменьшать пигментацию кожи [6]. Препарат выпускают в виде 20% крема и 15% геля. Наносят его на всю поверхность лица или другие пораженные участки кожи утром и вечером, лечение продолжают до достижения терапевтического эффекта. Специфических противопоказаний к препарату нет.
Топические антибиотики. Назначение показано при папуло-пустулезных акне легкой и средней тяжести в комбинации с топическими ретиноидами или бензоил пероксидом. Среди антибиотиков для наружного применения на первом месте стоят эритромицин, клиндамицин, фузидиевая кислота. Монотерапия местными антибиотиками не даст желательного эффекта, так как не оказывает достаточного влияния на основные патогенетические факторы, кроме колонизации P. acnes.
Эритромицин выпускается в комбинации с препаратом цинка (зинерит). Лосьон наносят на кожу 2 раза в день в течение 12 нед. Побочное действие — сухость, жжение, дерматит.
Клиндамицин выпускается в виде 1% геля или лосьона, который при нанесении на кожу гидролизуется в выводных протоках сальных желез. Несмотря на минимальное всасывание, препарат может вызывать нарушения со стороны желудочно-кишечного тракта, аллергические реакции. Наносят препарат 1–2 раза в день в течение 3 мес.
Фузидиевая кислота выпускается для наружного применения в виде 2% крема (фуцидин), обладает способностью хорошо проникать через неповрежденную кожу и оказывает выраженное бактерицидное действие [7]. Крем применяют 2 раза в день в течение 7 дней. Не отмечено системного действия препарата и индивидуальной непереносимости.
Местные формы антибиотиков обычно хорошо переносятся, аллергический контактный дерматит развивается редко. Длительное наружное применение антибиотиков может привести к развитию бактериальной резистентности P. acnes.
α-гидроксикислоты (АНА) — яблочная, тартаровая, цитрусовая, молочная, гликолевая — обладают комедолитическим свойством. При концентрации АНА 30–70% (гликолевый пилинг) лечение проводится утром 1 раз в день, в вечернее время назначают ретиноиды. Препараты с концентрацией кислоты 10–15% (эксфолиак, крем 10; эксфолиак, крем 15) назначают пациентам с акне ежедневно в течение 8 нед. При низких концентрациях АНА лекарственные средства назначаются в межрецидивный период и для профилактики осложнений угревой болезни (рубцов и пигментации).
β-гидроксикислоты — салициловая кислота, резорцин — влияют на фолликулярный гиперкератоз, так как являются слабыми кератолитиками и обладают противовоспалительными свойствами. Применяются в различных лекарственных формах, чаще — растворах (салициловая кислота 0,5%–5%, резорцин 1–3%).
Гиалуроновая кислота в сочетании с цинком (куриозин, гель) используется как профилактическое средство после разрешения клинических проявлений акне. Гиалуроновая кислота способствует формированию косметических рубцов. Препарат наносят 2 раза в сут до достижения клинического эффекта. Побочными реакциями являются жжение, чувство стягивания кожи, легкая гиперемия, которые самостоятельно исчезают при продолжении терапии.
Системная терапия акне показана для лечения больных с акне средней или тяжелой формы, особенно в случаях образования рубцов, дисхромий или значительных психосоциальных расстройств. Системная терапия может быть необходима при непереносимости или неэффективности местного лечения.
Наиболее эффективным препаратом для лечения акне среднетяжелой и тяжелой форм является изотретиноин (роаккутан), который при системном применении вызывает длительные ремиссии или излечение у большинства больных. Препарат является ретиноидом, рекомендуемым для системного применения, влияет на процессы дифференцировки и кератинизации клеток эпидермиса, в том числе сальных желез, обладает выраженным себостатическим и противовоспалительным действием. Оптимальная суточная доза изотретиноина составляет 0,5–1,0 мг на 1 кг массы тела больного. Стандартная начальная терапевтическая доза 0,5 мг/кг. Обычные сроки лечения составляют 4–8 мес. После достижения выраженного терапевтического эффекта (чаще к концу 2-го месяца) начальная суточная доза снижается (с 1,0 до 0,5 мг/кг; с 0,5 до 0,2–0,3 мг/кг) и используется до излечения пациента. При флегмонозных и конглобатных угрях снижение суточной дозы целесообразно проводить в более поздние сроки (через 3–4 мес после начала лечения) [3].
Роаккутан обладает тератогенным действием, что ограничивает его применение для женщин детородного возраста. До начала лечения обязательно исключается беременность, пациентки должны использовать эффективные контрацептивные средства за 1 мес до начала лечения, весь период лечения и в течение 1 мес после его прекращения.
Побочные реакции при приеме роаккутана многообразны и касаются различных органов и систем (сухость кожи и слизистых, хейлит, конъюнктивит, носовые кровотечения, ретиноидный дерматит, фотосенсибилизация кожи, мышечная скованность, гиперостоз, повышение активности трансаминаз, липидов крови и др.), кроме тератогенного эффекта остальные побочные реакции являются дозозависимыми. До начала и в процессе лечения необходим тщательный контроль состояния пациента. Пациенты с почечной и печеночной недостаточностью, сахарным диабетом, склонностью к нарушению обмена веществ (гиперлипидемия) не должны получать лечение этим препаратом.
Системные антибиотики. Наиболее часто применяют эритромицин и тетрациклин. Лечение антибиотиками проводят длительно, 6–8 нед и дольше. Назначаются дозы с 1 г в сутки циклами по 5–10 дней без перерывов, но со снижением суточной дозы в каждом последующем цикле на 0,1–0,2 г, доводя постепенно суточную дозу до 0,1–0,2 г [3]. Одновременно с антибиотиками необходимо назначать противогрибковые препараты для профилактики кандидозов и препараты цинка (сульфат или окись цинка 0,02–0,05 — 2–3 раза в день после еды). Противопоказаниями для назначения системных антибиотиков являются индивидуальная непереносимость, беременность и кормление грудью, наличие сопутствующих грибковых поражений кожи и слизистых, тяжелые заболевания печени и почек, лейкопении.
Оральные контрацептивы (диане-35) обладают фармакологическим действием, связанным с блокированием рецепторов андрогенов и уменьшением их эндогенного синтеза. В результате тормозится секреция сальных желез. Диане-35 содержит 2 мг ципротерона ацетата и 35 мкг этинилэстрадиола. Препарат назначают только женщинам, с 5-го дня менструального цикла ежедневно 1 драже в сутки в течение 21 дня, затем — 7-дневный перерыв. Противопоказаниями для назначения препарата являются беременность и лактация, тяжелые заболевания печени, тромбоэмболические процессы, сахарный диабет, нарушения липидного обмена, гипертоническая болезнь.
По степени влияния на основные факторы патогенеза действие препаратов проявляется так, что ретиноиды являются самыми эффективными средствами для контроля гиперкератинизации фолликула и предотвращения развития микрокомедонов. В меньшей степени на этот процесс влияют бензоил пероксид, азелаиновая и салициловая кислота. По влиянию на P. acnes на первом месте стоит бензоил пероксид, затем антибиотики и азелаиновая кислота и в меньшей степени изотретиноин. Уменьшению секреции кожного сала способствуют ретиноиды и гормональные препараты. Менее всего современные лекарственные средства влияют на процесс воспаления в области угревых элементов [8].
Ни один из современных методов лечения угрей не может гарантировать отсутствие рецидивов заболевания в будущем. Поэтому при достижении клинического выздоровления каждому пациенту следует рекомендовать комплекс лечебно-профилактических мероприятий, которые могут быть разделены на рекомендации по уходу за кожей и общие.
Среди общих рекомендаций важными являются санация очагов хронической инфекции, обследование органов желудочно-кишечного тракта и эндокринной системы, общее закаливание организма.
Диета с ограничением шоколада, кофе, углеводов, алкоголя должна рекомендоваться в тех случаях, когда употребление в пищу этих продуктов приводит к усилению жирности кожи лица и обострению заболевания.
Развитие акне не связано с недостаточностью ухода за кожей лица, как это часто считают пациенты, начиная лечение заболевания с посещения косметолога. В то же время выполнение ежедневных очищающих процедур косметического характера показано при любой тяжести заболевания. Рекомендуется ежедневное очищение кожи с использованием различных моющих средств, поддерживающих нейтральный или кислый рН кожи и обладающих антибактериальным действием. Пациент должен знать о необходимости исключения косметических средств, вызывающих закупорку протоков сальных желез (мази, жирные кремы), и скрабов.
Таким образом, располагая широким выбором средств для лечения акне и косметической продукцией для ухода за кожей, склонной к угревой болезни, врач в процессе лечения может переходить от направленного воздействия на одни механизмы патогенеза к препаратам, влияющим на его другие компоненты. При этом самым важным является регулярная коррекция назначенного лечения и длительное динамическое, диспансерное наблюдение за пациентом, даже после достижения клинической ремиссии.
Литература
И. Г. Сергеева, кандидат медицинских наук
Ю. М. Криницына, доктор медицинских наук
Новосибирский государственный университет, Новосибирск
Пропионибактерии P. freudenreichii как косметическое средство против жирной кожи
Молочные пропионовокислые бактерии против себореи и угревой сыпи

Propionibacterium freudenreichii как активное косметическое средство против жирной кожи
Уже давно признано, что многие заболевания и эстетические проблемы, связанные с состоянием кожи, во многом связаны (и зависят) от микрофлоры кишечного тракта. Воздействие различными средствами (в т.ч. пробиотиками) на дисбиотически измененную кишечную микробиоту зачастую приводит к восстановлению нормального состояния кожи. Из собственной практики и отзывов клиентов мы знаем о благотворном действии биоконцентратов на основе пропионовокислых бактерий (далее ПКБ) в случаях терапии кожных заболеваний, таких как себорейный дерматит (разной степени).
Не так давно мы также разместили собственную обзорную статью ( » Роль супероксиддисмутазы (SOD) при акне и терапевтический потенциал пропионовокислых бактерий» ), в которой попытались обосновать и донести для читателей информацию о том, что метаболиты пробиотических бактерий (такие, как, антиоксидантные ферменты) могут благотворно воздействовать на организм в плане решения проблем с кожей.
Также, на сайте есть раздел о том, что косметические маски с использованием заквасок чистых культур Propionibacterium Shermanii (на основе творожной сыворотки) и бентонитовой глины способствует увлажнению, питанию, повышению упругости и эластичности кожи, улучшению цвета лица и разглаживанию морщин. Однако, заявленный способ (плюс еще 2 аналогичных способа – см. Применение пропионовокислых бактерий в косметологии и эстетической медицине ) технологически трудно выполнить в домашних условиях.
С учетом описанной проблемы мы дадим здесь альтернативный и обоснованный вариант использования ПКБ для наружного применения (для проблемной кожи) в составе кисломолочной матрицы. Известно, что молоко и кисломолочные продукты в косметических целях используются во всем мире. Особенно популярны кисломолочные маски для лица и волос.
В своем исследовании (с последующей заявкой на патент в 2014 г.) французские ученые, Одри Гениш и Мария Далко, заметили, что штамм молочных пропионовокислых бактерии P. freudenreichii подвид shermanii (такой подвид используется в биоконцентратах PROPIONIX – ред.) позволяет ингибировать угри и таким образом в целом поддерживать сбалансированную экофлору при одновременном снижении выработки кожного сала, а также поддерживать Staphylococcus epidermidis, который является важным агентом в кожном равновесии.
Немного подробнее…
В дополнение к своему неприглядному виду, это поле, на котором могут возникнуть осложнения, и оно достигает областей, где сальные железы многочисленны, что является результатом главным образом андрогенной чрезмерной стимуляции выработки сала этими железами. Таким образом, гиперсеборея участвует в возникновении очагов вульгарных угрей (угревой сыпи, акне).
Гиперсеборея – состояние кожи, обусловленное избыточной выработкой кожного сала, из-за чего кожа приобретает жирный блеск. Гиперсеборея является причиной жирной кожи и может стать одной из причин появления акне.
В результате гиперсеборея, очевидно, является биологическим феноменом, который представляется важным эффективно контролировать, чтобы предотвратить проявление сопутствующих кожных заболеваний.
Лизаты, экстракты и супернатанты Propionibacterium freudenreichii, в частности P. freudenreichii ssp. shermanii уменьшают признаки жирной и блестящей кожи, воздействуя непосредственно на сальные железы и уменьшая синтез липидов, в том числе уменьшение P. acnes, предпочтительно избирательно, что помогает уменьшить стимуляцию себоцитов (сальных желез). Кроме того, иммунорегуляторная активность поддерживает гомеостаз кожи.
Изобретение французов было направлено, в частности, на использование эффективного количества лизата или супернатанта культуры по меньшей мере одного микроорганизма вида Propionibacterium freudenreichii в качестве активного ингредиента в косметической композиции для регулирования себореи.
Супернатант культуры по меньшей мере одного микроорганизма вида Propionibacterium freudenreichii действует путем уменьшения или предотвращения развития Propionibacterium acnes, в частности, действуя путем уменьшения или предотвращения развития Propionibacterium acnes избирательно по отношению к Staphylococcus epidermidis. Лизат или супернатант культуры по крайней мере одного микроорганизма вида Propionibacterium freudenreichii также действует, поддерживая гомеостаз кожи своими противовоспалительными и иммунорегуляторными свойствами.
Лизаты и супернанты клеток ПКБ
Примечание редактора: Так как цель данной статьи дать практическую обоснованную рекомендацию по наружному использованию ПКБ, то сразу оговоримся, что термины «лизат» и «супернант» применимы и к использованию жидких пробиотиков с ПКБ на сывороточной основе и к ферментированному ПКБ молоку, т.к. в них присутствуют продукты клеточного распада и высвобожденные бактериальные эндометаболиты. Безусловно в ферментированном ПКБ молоке всегда присутствует процент условных суперната и лизата (условных, т.к. они не отделены от живых бактерий в кисломолочной среде).
Лизат обычно относится к материалу, полученному в конце разрушения или растворения биологических клеток в результате явления, называемого «лизисом клеток», вызывающего, таким образом, высвобождение внутриклеточных биологических компонентов, естественно содержащихся в клетках рассматриваемого микроорганизма.
Для целей настоящего приложения (речь идет об описании изобретения к патенту – ред.) термин «лизат» используется взаимозаменяемо для обозначения всего лизата, полученного лизисом соответствующего микроорганизма, или только его части («экстракт»). Таким образом, используемый лизат образуется во всех или части внутриклеточных биологических компонентов и компонентов клеточных стенок и мембран. Этот лизис клеток может быть осуществлен различными технологиями, такими как, например, осмотический шок, термический шок, ультразвук, или же под механическим напряжением центрифугирующего типа.
Культуральный супернатант обычно получают путем культивирования соответствующего микроорганизма в среде, пригодной для выживания и / или роста микроорганизма, а затем путем разделения среды и микроорганизма таким образом, чтобы собрать среду, находящуюся в контакте с микроорганизмом. Предпочтительно культивирование проводят в течение некоторого времени и в условиях, позволяющих микроорганизму высвобождать в среду активные агенты, обладающие желаемыми антисеборейными свойствами.
Средой, пригодной для выживания и / или роста микроорганизма, будет любая питательная среда, пригодная для выживания и / или культивирования микроорганизма. Она обычно содержит источники углерода и азота, такие как, например, аминокислоты, сахара, белки, жирные кислоты, фосфаты, сульфаты, минералы и факторы роста, а также витамины в достаточном количестве.
Для целей настоящего приложения (речь идет об описании изобретения к патенту – ред.) термин «культуральный супернатант» используется взаимозаменяемо для обозначения всей совокупности культурального супернатанта, полученного после культивирования рассматриваемого микроорганизма, или любой фракции или субкомпонента супернатанта, полученного диализом, фракционированием, разделением фазы, фильтрационной хроматографией, аффинной хроматографией, осаждением, концентрацией, лиофилизацией и т.д.
Косметическая композиция
Таким образом, французские ученые считают, что их изобретение относится к косметической композиции, содержащей эффективное количество лизата или супернатанта культуры по меньшей мере одного микроорганизма вида Propionibacterium freudenreichii, в физиологически приемлемом носителе (в нашем случае носителем упрощенно будут выступать ферментированное ПКБ молоко, содержащее компонетны лизисных клеток и (или) бактериальные эндометаболиты).
Французы отмечают, что пробиотические косметические композиции могут, в частности, представлять собой кремы для чистки, пилинга, лечения или ухода за лицом, руками, ногами, большими анатомическими складками или телом (например, дневные кремы, ночные кремы), кремы для снятия макияжа, тональные кремы, солнцезащитные кремы), продукты для макияжа, такие как жидкие основы, молочные средства для снятия макияжа, молочные средства для ухода за телом или ухода за кожей, молочные средства после загара, лосьоны, гели для ухода за кожей или муссы, такие как очищающие или дезинфицирующие лосьоны, солнцезащитные лосьоны, лосьоны для искусственного загара, композиции для ванн, дезодоранты, содержащие бактерицидное средство, гели или лосьоны после бритья, кремы для удаления волос или укусы насекомых.
Из перечисленного списка нам вполне сгодятся «молочные средства для ухода за телом или ухода за кожей».
Опуская подробности исследования высвобождения противовоспалительных циткинов IL-10 при использовании лизатов /супернантов ПКБ (а они достаточно выражены, в т.ч. и при применении живых клеток в концентрате на сывороточной основе), а также иные выкладки, отметим, что в своем исследовании французские специалисты подытожили, что штамм молочных ПКБ P. freudenreichii подвид shermanii позволяет подавлять образование угревой сыпи (акне) и поддерживать баланс кожной экофлоры при одновременном снижении выработки кожного сала, а также поддерживать эпидермальный стафилококк (Staphylococcus epidermidis), который является важным агентом в кожном равновесии.
Более подробно с материалами патента описания изобретения к патенту WO 2014/053621 A2 см. по ссылке →
В целом, анализ Патента РФ № 2414886 о применении пропионовокислых бактерий P. freudenreichii в косметологии (в масках) в совокупности с данными французских исследователей, дает все основания полагать, что косметические маски на основе ферментированного ПКБ молока для лица и волосяной части головы будут наиболее эффективны в решении проблемы гиперсебореи, чем их простые аналоги (т.е. традиционные кисломолочные косметические маски на основе кефира или сметаны).
Дополнительно см. также:
В целом, Патент РФ № 2414886 о применении пропионовокислых бактерий в косметологии дает все основания полагать, что косметические маски на основе ферментированного ПКБ молока для лица и волос будут наиболее эффективны в решении проблемы гиперсебореи, чем их простые аналоги (т.е. традиционные кисломолочные косметические маски).