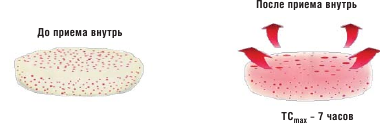ПРЕПАРАТЫ ПРОДЛЁННОГО ДЕЙСТВИЯ
ПРЕПАРАТЫ ПРОДЛЁННОГО ДЕЙСТВИЯ (син.: дюрантные препараты; препараты пролонгированного действия) — лекарственные препараты, обеспечивающие более длительное терапевтическое действие но сравнению с обычными препаратами, содержащими те же лекарственные средства. Принцип их действия заключается в постепенном освобождении определенных доз лекарственных средств в течение длительного времени, благодаря чему поддерживается оптимальная их концентрация в организме.
Увеличение времени пребывания лекарственного средства в организме достигается путем замедления всасывания, биотрансформации и выделения. Пролонгирование действия лекарственных средств, применяемых для инъекций, может осуществляться путем создания труднорастворимых солей, эфиров и комплексных соединений лекарственных средств (напр., новокаиновая соль бензилпенициллина, протамин-цинкинсулин, эфиры стероидных гормонов и др.).
Всасывание лекарственного средства из инъекционного р-ра зависит также от вязкости последнего. На этом принципе основано использование в качестве растворителей для инъекционных р-ров растительных масел с добавлением воска и стеарата алюминия. Увеличение вязкости растворителя может быть достигнуто путем добавления к водным р-рам высокомолекулярных соединений (декстрана, поливинилпирролидона, карбоксиметилцеллюлозы, желатина). Весьма значительно замедляется всасывание инъекционных препаратов в форме микрокристаллических суспензий. Так, микрокристаллическая суспензия инсулина обеспечивает продолжительность действия этого гормона до 36 час. Масляные р-ры труднорастворимых веществ и суспензии вводят внутримышечно. На месте инъекции таких препаратов создается депо лекарственного средства, откуда оно постепенно всасывается в кровь, что обеспечивает увеличение продолжительности действия.
В офтальмол. практике в качестве П. п. д. применяют р-ры пилокарпина гидрохлорида, скополамина гидробромида и гоматропина гидробромида с метилцеллюлозой.
П. п. д. для приема внутрь выпускают в виде микрокапсул, спансул, медул, лакированного гранулята, импрегнированных таблеток с оболочками, таблеток типа «дуплекс», многослойных таблеток. Содержащееся в этих лекарственных формах (см.) вещество может освобождаться через определенное время независимо от локализации препарата в жел.-киш. тракте или в заданном его отделе. Некоторые таблетки содержат две или более однократных доз лекарственного средства, каждая из которых освобождается последовательно. При этом освобождение последующей дозы начинается в момент, когда концентрация вещества в крови от предыдущей дозы начинает снижаться.
Особую лекарственную форму с пролонгированным типом действия представляют имплантационные таблетки и стерильные капсулы, которые оперативным путем имплантируют под кожу. Этот способ введения лекарств обеспечивает равномерное поступление их в кровь и действие в течение нескольких месяцев. В таких лекарственных формах выпускают некоторые гормональные препараты и средства, применяемые для лечения алкоголизма (напр., тетурам).
К мягким лекарственным формам с пролонгированным действием относятся мази и суппозитории на специальных основах, суппозитории с оболочками, ректальные тампоны. Пролонгирование эффекта лекарственного средства можно получить также за счет фармакол. взаимодействия с другими веществами, напр. применение адреналина с местноанестезирующими средствами пролонгирует фармакол. эффект последних.
Библиография: Муравьев И. А. Технология лекарств, т. 1—2, М., 1980; Voigt R. Lehrbuch der pharmazeutischen Technologie, S. 721, B., 1973.
C. И. Золотухин, В. Ф. Кремнева.
Метформин с пролонгированным высвобождением (Глюкофаж Лонг) – высокоэффективный и безопасный препарат первой линии в лечении сахарного диабета 2 типа
Опубликовано в журнале:
Русский Медицинский Журнал, Том 19, No 12, 2011
Следует отметить, что метформин оказывает влияние на всасывание углеводов в желудочно-кишечном тракте, замедляя его скорость, а также снижает аппетит [10,13]. Интестинальные эффекты метформина вносят существенный вклад в предотвращение постпрандиальных гипергликемических пиков, ассоциированных с риском преждевременной смертности от ССЗ [12,16,20]. Полагают, что один их механизмов анорексигенного действия метформина связан с влиянием препарата на метаболизм глюкогоноподобного пептида-1 (ГПП-1), регулирующего пищевое поведение. Так, в работе Mannucci E. с соавт. (2001) определяли уровни ГПП-1 (7-36) амида/(7-37) исходно и через 15 дней терапии метформином (25-50 мг/сут.) у больных с ожирением до и после нагрузки глюкозой [13]. С целью устранения влияния инсулинемии и гликемии на секрецию ГПП-1 исследование проводилось в условиях эугликемического гиперинсулинемического клэмпа. Авторы не обнаружили изменений концентраций ГПП-1 у лиц контрольной группы. В то же время у больных с ожирением метформин вызывал существенное увеличение концентрации ГПП-1 (7-36)амида/(7-37) на 30 и 60-й минутах теста при неизмененном базальном уровне пептида. В смешанной плазме (после 30 мин. инкубации при 37°), а также в растворе буфера, содержащем дипептидил-пептидазу-4, метформин ингибировал деградацию ГПП-1. Согласно результатам экспериментальных исследований на животных моделях анорексигенный эффект метформина, по-видимому, также связан с центральным действием препарата на уровне гипоталамических нейронов [5]. Модулируя экспрессию орексигенного нейропептида Y, метформин способствует снижению массы тела. Другим важным эффектом метформина является уменьшение или стабилизация массы тела, а также снижение отложения висцерального жира [4,11,17].
Абсолютная биодоступность метформина, введенного per os, cоставляет 50-60%. Почти весь метформин, попадающий в кровоток, всасывается на ограниченном участке верхних отделов желудочно-кишечного тракта (рис. 1), и лишь незначительная часть метформина всасывается в более дистальных отделах пищеварительного тракта.
Рис. 1. Создание метформина пролонгированного действия с однократным приемом: сложная задача
Кроме того, всасывание метформина в тонком кишечнике является «насыщающимся». Это означает, что при увеличении концентрации метформина в просвете кишечника выше определенного порогового уровня происходит «насыщение всасывания», тем самым значительная часть препарата проходит мимо «окна абсорбции» и не всасывается вовсе. Таким образом, уровень всасывания метформина из ЖКТ зависит от скорости эвакуации метформина из желудка.
Эти особенности определяют сложность разработки таблеток метформина с замедленным высвобождением, пригодных для приема один раз в сутки.
Традиционно используемые для этого лекарственные формы основываются на простом замедлении высвобождения активного вещества из таблетки, а его всасывание происходит на всем протяжении кишечника. Но даже в этом случае нередко имеется период относительно быстрого поступления препарата в кровоток вскоре после приема таблетки.
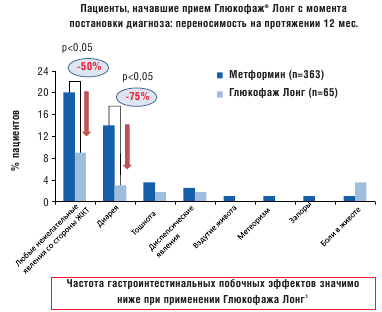
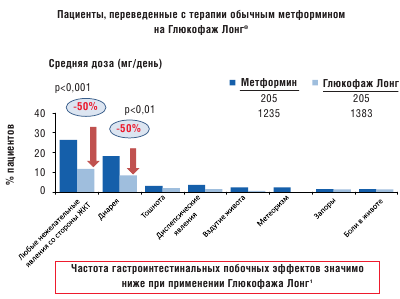
Такое традиционное строение таблетки нельзя применить для препарата Глюкофаж ® Лонг ввиду того, что метформин не будет всасываться после прохождения таблеткой абсорбционного окна. Кроме того, начальный период быстрого высвобождения вещества из таблетки может «насытить» абсорбционное окно и привести к потере активного ингредиента. После приема метформина с быстрым высвобождением пиковая концентрация препарата в крови наступает в течение 3 часов. Разработанная новая форма метформина XR (Глюкофаж Лонг) имеет целью устранить проблемы, связанные с желудочно-кишечной непереносимостью, с одной стороны, и многократным приемом препарата, с другой стороны. Замедленное высвобождение препарата увеличивает время достижения пиковой концентрации до 7 часов при снижении ее максимального уровня [19]. Таким образом, лекарственная форма Глюкофаж Лонг имеет сниженную пиковую концентрацию, но аналогичную с метформином быстрого высвобождения биодоступность. В рандомизированном двойном слепом исследовании в параллельных группах Глюкофаж Лонг показал такую же эффективность в снижении уровня гликированного гемоглобина, как и метформин быстрого высвобождения [7]. С целью сравнения гастроинтестинальной переносимости метформина с пролонгированным и быстрым высвобождением был проведен ретроспективный анализ медицинских карт пациентов с сахарным диабетом 2 типа в четырех центрах США, где было выявлено существенное снижение частоты желудочно-кишечных нежелательных явлений у пациентов, переведенных с терапии метформином быстрого высвобождения на Глюкофаж Лонг [2] (рис. 2 и 3).
Рис. 2. Сравнение частоты гастроинтестинальных побочных эффектов у пациентов, принимавших метформин и Глюкофаж Лонг с момента постановки диагноза
Рис. 3. Сравнение частоты гастроинтестинальных побочных эффектов у пациентов, принимавших метформин и переведенных с терапии обычным метформином на Глюкофаж Лонг
Пролонгированный эффект Глюкофажа Лонг обеспечивается оригинальной структурой таблетки (рис. 4), в которой создана система диффузии через гелевый барьер (рис. 5). Метформин содержится внутри двухслойного гидрофильного полимерного матрикса, что обеспечивает высвобождение препарата путем диффузии. Наружный, закрытый полимерный матрикс (без метформина) окружает внутренний полимер, содержащий суммарно 500 мг метформина в таблетке. При проглатывании, таблетка впитывает влагу и набухает, образуя слой геля на внешней стороне таблетки, что обеспечивает дозированное высвобождение метформина в кишечнике. Важно отметить, что скорость растворения метформина не зависит от перистальтики, уровня pH, что помогает свести к минимуму вариабельность поступления метформина в ЖКТ как у одного пациента, так и в группах пациентов.
Рис. 4. строение таблетки Глюкофаж Лонг
Рис. 5.Глюкофаж Лонг: инновационная технология производства
Всасывание метформина из таблетки с пролонгированным высвобождением медленное и более длительное по сравнению с обычной формой. В исследовании по фармакокинетике изучались метформин с пролонгированным высвобождением (2000 мг один раз в сутки) и обычный метформин (1000 мг два раза в сутки) после достижения равновесной концентрации. Время достижения максимальной концентрации в плазме (Tmax) после приема метформина с пролонгированным высвобождением было больше, чем после обычного метформина (7 часов по сравнению с 3-4 часами). Кроме того, максимальная концентрация препарата в плазме (Cmax) на фоне приема пролонгированной формы была на 25% меньше. Суммарное воздействие метформина на пациента было сходным. В действительности, анализ площади под кривой зависимости концентрация-время свидетельствует о биоэквивалентности данных препаратов.
Таким образом, фармакокинетический профиль метформина с пролонгированным высвобождением позволяет избежать быстрого подъема концентрации метформина в плазме, характерного для обычного метформина. Более плавное поступление метформина позволяет избежать появления нежелательных явлений со стороны ЖКТ, и может улучшать переносимость препарата.
Повышение приверженности пациентов к лечению, а также снижение нежелательных явлений со стороны желудочно-кишечного тракта являются важными достоинствами препарата, однако первостепенное значение имеет влияние на показатели гликемии у больных сахарным диабетом 2 типа. Полученные результаты подтверждают имеющиеся данные, что сахароснижающий эффект метформина с пролонгированным высвобождением при приеме 1 раз в сутки сравним с эффектом обычного метформина, назначаемого в несколько приемов в течение дня.
В исследовании по определению дозы Глюкофажа Лонг была показана его дозозависимая эффективность при приеме 1 раз в сутки. Максимальное действие этой формы препарата было достигнуто на дозе 1500-2000 мг/сут. В проведенном исследовании также изучалась эффективность Глюкофажа Лонг 1000 мг, назначаемым 2 раза в сутки по сравнению с однократным приемом той же формы, но в дозе 2000 мг 1 раз в сутки. Динамика уровня HbA1c (снижение в среднем на 1,2% при режиме 1000 мг 2 раза в сутки) была сходной с таковой для группы пациентов, получавших препарат 2000 мг 1 раз в сутки (снижение в среднем на 1%).
Препараты пролонгированного действия
Понятие и особенности лекарственных препаратов пролонгированного действия, принципы их действия. Применение полимеров в качестве носителя для иммобилизированных лекарственных веществ. Стадии разработки перспективных продуктов и технологий в фармацевтике.
| Рубрика | Медицина |
| Вид | реферат |
| Язык | русский |
| Дата добавления | 10.02.2015 |
| Размер файла | 186,8 K |
Отправить свою хорошую работу в базу знаний просто. Используйте форму, расположенную ниже
Студенты, аспиранты, молодые ученые, использующие базу знаний в своей учебе и работе, будут вам очень благодарны.
Размещено на http://allbest.ru
Министерство образования и науки РФ
Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования «Московский государственный университет тонких химических технологий имени М.В. Ломоносова»
Факультет биотехнологии и органического синтеза (БС)
Кафедра химии и технологии биологически активных соединений им. Н.А. Преображенского
Пролонгирующие вещества в технологии готовых лекарственных форм
Работу выполнила студентка группы ХТ-401
Ларкина Екатерина Александровна
1. Лекарственные формы пролонгированного действия
2. Методы пролонгирования действия лекарственных веществ
3. Некоторые полимеры, используемые в качестве носителя для иммобилизированных лекарственных веществ
Список используемой литературы
В настоящее время важным и актуальным для фармацевтической технологии является процесс создания не только эффективных и безопасных, но и пролонгированных лекарственных средств [2]. Это связано с тем, что пролонгирование действия лекарственного препарата является одним из требований современной медицинской практики, так как позволяет при сокращении числа приемов и уменьшенной дозе лекарственного средства уменьшить и возможные негативные воздействия на организм, что в свою очередь позволяет повысить эффективность лечения и снизить его себестоимость. Пролонгирование лечебного действия лекарственного средства достигается, как правило, с помощью вспомогательных веществ. В качестве ВВ в производстве пролонгированных лекарственных средств используют природные, синтетические и полусинтетические соединения [1].
1. Лекарственные формы пролонгированного действия
В настоящее время продление времени действия лекарственных средств является важной проблемой фармацевтической технологии, так как во многих случаях необходимо длительное поддержание строго определенной концентрации препаратов в биологических жидкостях и тканях организма. Это требование фармакотерапии особенно важно соблюдать при приеме антибиотиков, сульфаниламидов и других антибактериальных лекарств, при снижении концентрации которых падает эффективность лечения и вырабатываются резистентные штаммы микроорганизмов, для уничтожения которых требуются более высокие дозы лекарства, а это, в свою очередь, ведет к увеличению побочного действия [5].
Таким образом, использование пролонгированных лекарственных форм было вызвано отрицательными явлениями, возникающими при быстром выведении ЛВ из организма или при быстром разрушении ЛВ в организме. При этом возникает необходимость частого введения лекарственных веществ, что нередко приводит к резкому колебанию концентрации их в организме и, в свою очередь, обусловливает токсичность, побочные нежелательные явления (аллергические реакции, раздражение и т.п.). Поэтому вводят вещества, однократный прием которых сохранял бы в организме терапевтически активную концентрацию ЛВ в течение длительного или заданного времени, а также обеспечивал бы поступление ЛВ с заданной скоростью.
Так, например в 1970-х годах для лечения гипертонии и сердечнососудистых заболеваний использовали препарат нифедипин быстрого действия, а уже в 2000-х годах появилась пролонгированная лекарственная форма этого препарата. Эти таблетки относятся к группе антагонистов кальция (блокаторов кальциевых каналов).
· Химически нифедипин представляет собой 1,4-дигидро-2,6-диметил-4-(2-нитрофенил)-3,5-пиридиндикарбоновой кислоты диметиловый эфир.
Действие нифедипина зависит от того, как сильно колеблется его концентрация в крови, насколько быстро она нарастает и спадает. На рис. 1.1 изображена динамика концентрации нифедипина в крови при приеме обычных таблеток и лекарственной пролонгированной формы ГИТС.
Обычные таблетки нифедипина отличаются тем, что резко снижают артериальное давление. В ответ на это происходит рефлекторный выброс адреналина и других “стимулирующих” гормонов. Эти гормоны могут вызывать тахикардию (сердцебиение), головную боль, чувство жара, покраснение кожи. Для постоянного приема при гипертонии и сердечно-сосудистых заболеваниях подходит нифедипин в лекарственной форме пролонгированного действия (рис. 1.2).
Пролонгированная форма и ее преимущества
Рис. 2. Таблетка нифедипина пролонгированного действия, с замедленным высвобождением лекарственного вещества
Таким образом, пролонгирующие компоненты должны не только соответствовать требованиям, предъявляемым к вспомогательным веществам, но и поддерживать оптимальный уровень лекарственного вещества в организме, препятствовать возникновению резких колебаний его концентрации.
2. Методы пролонгирования действия лекарственных веществ
В настоящее время установлено, что пролонгирование действия лекарственных веществ может быть обеспечено за счёт:
· уменьшения скорости высвобождения их из лекарственной формы;
· депонирования лекарственного вещества в органах и тканях;
· снижения степени и скорости инактивации лекарственных веществ ферментами и скорости выведения из организма [1].
Известно, что максимум концентрации лекарственного вещества в крови прямо пропорционален введенной дозе, скорости всасывания и обратно пропорционален скорости выделения вещества из организма [1].
Пролонгированного действия лекарств можно достигнуть использованием различных методов, среди которых можно выделить группы физиологических, химических и технологических методов [5].
Наиболее часто это достигается следующими путями:
— охлаждение тканей в месте инъекции лекарства;
— использование кровососной банки;
— введение гипертонических растворов;
— введение вазоконстрикторов (сосудосуживающих средств);
— подавление выделительной функции почек (например, применение этамида для замедления выведения пенициллина) и др. [5].
Однако необходимо отметить, что эти методы могут быть довольно не безопасными для пациента, в связи с чем мало используются. В качестве примера можно привести совместное применение в стоматологии местных анестетиков и вазоконстрикторов для продления местноанестезирующего действия первых за счет сокращения просвета кровеносных сосудов. В качестве вазоконстриктора часто применяется адреналин, он суживает сосуды и замедляет всасывание анестетика из области инъекции. Побочно при этом развивается ишемия тканей, что приводит к снижению поступления кислорода и развитию гипоксии вплоть до некроза ткани [7].
Аминотаниновый комплекс образуется в результате реакции спиртового раствора лекарственного вещества с избытком танина. Затем комплекс осаждают водой с йодом и подвергают вакуумной сушке. Комплекс нерастворим, но в присутствии электролитов или при понижении рН способен постепенно освобождать лекарственное вещество. Выпускается в виде таблеток [8].
Образование комплексных соединений с лекарственными веществами может быть осуществлено при помощи: полигалактуроновых кислот (полигалактуроновый хинидин), карбоксиметилцеллюлозы (дигитоксин) или декстрана (например, противотуберкулезный препарат «Изодекс», который представляет собой комплекс изониазида и радиационно-активированного декстрана (рис. 2.1.)) [5,8].
Рис. 2.1 Комплекс изониазида и радиационно-активированного декстрана
Технологические методы пролонгирования действия лекарственных веществ получили наибольшее распространение и чаще всего используются на практике [5]. В этом случае продление действия достигается следующими приемами:
· Повышение вязкости дисперсионной среды.
Этот способ обусловлен тем, что при увеличении вязкости растворов замедляется процесс всасывания лекарственного вещества из лекарственной формы. Лекарственное вещество вводят в дисперсионную среду повышенной вязкости. Такой средой могут служить как неводные, так и водные растворы. В случае инъекционных форм возможно применение масляных растворов, масляных суспензий (в том числе микронизированных). В данных лекарственных формах выпускаются препараты гормонов и их аналогов, антибиотиков и иных веществ [5].
Пролонгирующий эффект других можно получить и при использовании в качестве дисперсионной среды других неводных растворителей, таких как:
Таблетка с двойным дном
Изучаем лекарственные формы с модифицированным высвобождением — от пеллетов профессора Лебовски до современных систем coat-core
Фармация — отрасль постоянно развивающаяся, ищущая новые формулы и формы. Создание принципиально новых лекарственных субстанций сопряжено с огромными временными и материальными затратами. В среднем вывод на рынок нового препарата занимает 12–14 лет, а доля потенциально эффективных молекул в общей массе составляет 1:10 000 [1]. Есть и второй путь развития — использование хорошо известных субстанций в новых лекарственных формах с повышенной эффективностью, улучшенной биодоступностью и минимизированными побочными эффектами. Мы решили подробней остановиться на этой инновационной стороне фармакологической отрасли и осветить ее в цикле материалов о современных лекарственных формах, которые уже есть в наших аптеках или вот-вот появятся в ассортименте. И начнем мы погружение в интересный мир современных фармтехнологий с понятия, которое уже знакомо провизорам и фармацевтам, — модифицированного высвобождения лекарственных веществ.
Где действующее вещество, Лебовски?
Наверное, самой ранней попыткой создания лекарственной формы (ЛФ) с регулируемым высвобождением стала работа профессора Израэля Лебовски, который в 1938 году предложил использовать пероральные пеллеты, покрытые оболочкой, обеспечивающей пролонгированное высвобождение действующего вещества. Так же как и современные фармакологи, Лебовски хотел создать идеальное лекарство, быстро проникающее в зону действия в оптимальной концентрации и сохраняющееся в необходимой дозе определенный период времени, достаточный для достижения терапевтического эффекта [2]. Безусловно, с 30‑х годов прошлого века технологии ушли далеко вперед, но принцип, задекларированный Лебовски, остался неизменным.
Современные препараты с модифицированным высвобождением характеризуются в первую очередь изменением механизма и характера высвобождения лекарственного вещества. Они могут быть предназначены для разных путей введения — перорального, парентерального, имплантационного, трансдермального, ингаляционного и других.
Пероральные лекарственные формы с модифицированным высвобождением могут обозначаться различными английскими и русскими терминами [1].
Таблица 1: Термины для ЛФ с модифицированным высвобождением
| Аббревиатура (англ.) | Вид лекарственной формы | |
| Английское название | Русское название | |
| ER, XR | Extended release | Длительное высвобождение |
| SR | Sustained (slow) release | Пролонгированное (замедленное) высвобождение |
| CR | Controlled release | Контролируемое высвобождение |
| CD | Controlled delivery | Контролируемая доставка |
| СС | Coat-core system | Система «оболочка-ядро» |
| LA | Long-acting | Длительное действие |
| PF | Prolonged action | Пролонгированное действие |
| SL | Short-long form | Двухфазное высвобождение |
| XL | Extra-long | Экстрадлительное высвобождение |
| ZOK | Zero-order kinetics | Кинетика нулевого порядка |
| OROS | Oral osmotic system | Пероральная осмотическая система |
| L-OROS | Liquid oral osmotic system | Жидкостная пероральная осмотическая система |
| GITS | Gastrointestinal therapeutic system | Желудочно-кишечная терапевтическая система |
Технологии модифицированной доставки
Для модификации высвобождения и доставки лекарственного вещества применяются различные методы [3].
Таблица 2: Методология модификации высвобождения
| Физические методы | Использование вспомогательных веществ, изменяющих растворимость, всасывание, распределение, элиминацию; использование физических сил – диффузии, осмоса, гидродинамики, аэродинамики и так далее |
| Химические методы | Образование солей, комплексов, добавление или замена функциональных химических групп в молекуле лекарственного вещества, конъюгация (биосинтез, – прим. ред.) с веществом-носителем |
| Технологические методы | Производство наноразмерных лекарственных форм – создание матриц, однослойных или многослойных оболочек, резервуаров, микросфер, липосом, наночастиц; микрогранулирование, микрокапсулирование |
| Применение таргетных инновационных препаратов | Обеспечение наноразмерного воздействия на биомишень и достижение оптимального терапевтического эффекта |
При использовании разных технологий модифицированного высвобождения можно получить пероральные лекарственные формы двух типов:
В монолитных формах модификацию высвобождения обеспечивает медленно распадающееся вещество полимерной природы, которое способно к разрушению или набуханию с образованием пор. В качестве матриц часто используются [2, 3]:
В резервуарных формах модифицированное высвобождение обеспечивают оболочки — прессованные, многослойные, кишечнорастворимые и другие. Их прессование позволяет включать лекарственное вещество как в ядро таблетки, так и в оболочку в качестве второго слоя. Яркий пример резервуарной формы — прессованная таблетка (coat-core). Она содержит две фазы лекарственного вещества, которые растворяются в определенное время: вещество, входящее в состав оболочки, — в первые 12 часов после приема, а содержимое в ядре — в следующие 12 часов после приема таблетки.
Рассмотрим самые распространенные формы модифицированного высвобождения более подробно.
Очень популярной формой модификации высвобождения активного вещества является форма резервуарного типа с кишечнорастворимыми оболочками. Она может обеспечивать решение сразу нескольких задач:
Для создания кишечнорастворимых оболочек используются pH-чувствительные полимеры, растворимые при pH >5. Благодаря способности растворяться в среде с четко установленным водородным показателем они остаются устойчивыми в кислой среде желудка, но быстро растворяются в тонком кишечнике.
Первые осмотические системы появились на фармацевтическом рынке в начале 80‑х годов прошлого века — они использовались для создания препаратов индометацина. Этот опыт нельзя назвать успешным. Из-за зарегистрированных случаев выраженного раздражения слизистой ЖКТ и перфорации пищеварительного тракта препарат был отозван из обращения. Тем не менее, осмотические насосы получили широкое распространение и стали одним из самых востребованных инновационных способов контроля высвобождения лекарственного вещества.
Внешне осмотические системы выглядят, как обычные таблетки, однако представляют собой резервуар для лекарственных компонентов и осмотического вещества. Он имеет отверстие диаметром 300–500 мкм, сформированное с помощью лазерного луча. Сам резервуар окружает полупроницаемая оболочка. После приема таблетки вода проникает через нее, и лекарственное вещество частично растворяется с образованием суспензии. При этом создается осмотическое давление. Для его повышения иногда в состав препарата вводятся осмотические агенты — хлорид натрия, хлорид калия, ксилит [4]. Осмотическое давление обеспечивает выведение лекарственной суспензии из резервуара через отверстие со скоростью, равной скорости проникновения в систему жидкости.
В некоторых современных осмотических системах используются несколько слоев-оболочек: наружный, имеющий поры, и внутренний, «толкающий». Он состоит из материала, расширяющегося в присутствии воды и за счет этого выталкивающего слой лекарственного вещества из отверстия с контролируемой скоростью.
Все пероральные осмотические системы очень стабильны в желудочно-кишечном тракте, не реагируют на колебания pH, моторику кишечника, прием пищи и другие факторы.
Системы множественных микрогранул, или пеллет
Лекарственные формы этого типа имеют множество микрогранул, размещенных в матриксе и заключенных в таблетку или макрокапсулу (спансулу). Пеллеты (от англ. рellet — «шарик», «гранула», «дробинка») представляют собой частицы лекарственного вещества малого размера — микрогранулы, микросферы, мини-таблетки и так далее. Они могут быть как готовой лекарственной формой, так и промежуточным этапом в производстве готовой формы.
Чаще всего пеллеты производят путем компактирования и нанесения лекарственного вещества на фармакологически инертные микросферы, к которым предъявляется ряд требований [5]:
Пеллетам свойственна высокая текучесть, поэтому их легко компактировать до однородного состояния. Лекарственная форма с множеством пеллет может включать микросферы с разными активными и вспомогательными веществами, что позволяет объединять в одном препарате два и более действующих компонентов. При этом они могут быть как совместимыми, так и несовместимыми, а также всасывающимися в одном или разных отделах ЖКТ [5].
Лекарственная форма с системой множественных пеллет имеет ряд преимуществ: таблетки, созданные по этой технологии, можно делить, в их составе можно комбинировать два и более лекарственных препарата, в том числе и несовместимых. Это позволяет повысить профиль безопасности лекарственного средства и его эффективность.
Типы модифицированного высвобождения
Лекарственные формы с модифицированным высвобождением различаются по ряду критериев:
Для препаратов с контролируемым высвобождением свойственно изменение времени высвобождения активного ингредиента в соответствии с характеристиками терапевтического эффекта. Препараты с этой формой выпуска должны отвечать следующим требованиям:
При соблюдении всех этих условий процесс высвобождения становится предсказуемым, точным по скорости, продолжительности и месту высвобождения, что позволяет прогнозировать терапевтический эффект. Если какое‑то из этих условий не выполняется, лекарственная форма является пролонгированной.
Из лекарственных форм с пульсирующим или прерывистым высвобождением лекарственное вещество высвобождается в определенное время или через определенный период времени в необходимом месте и требуемой дозировке. Как правило, такие формы имеют резервуарный тип устройства, а механизм высвобождения обеспечивают оболочки, осмотические системы и другие технологические приемы. Период высвобождения регулируется толщиной, пористостью оболочки или свойствами полимерной «пробки».
В системы с модифицированным пульсирующим высвобождением под полупроницаемую наружную оболочку вводят слой полимера, обеспечивающего период плато с заданной продолжительностью (примерно 4–5 часов), и отсроченное время действия препарата. Чтобы обеспечить повторное высвобождение, применяют многослойные системы или системы со множественными пеллетами.
Модифицированные формы: день сегодняшний
Создание лекарственных форм с модифицированным высвобождением позволяет контролировать процесс доставки активных компонентов, управлять терапевтическим эффектом, улучшить переносимость лекарственных препаратов, повысить приверженность к терапии и достичь оптимального по выраженности и продолжительности эффекта. На сегодняшний день фармкомпаниям удалось создать формы с модифицированным высвобождением для ряда препаратов, применяющихся для лечения сердечно-сосудистых заболеваний, сахарного диабета, а также антибиотиков, ферментов и гормональных лекарственных средств.
Таблица 3: Примеры препаратов, имеющих ЛФ с модифицированным высвобождением
Широкие возможности, которые открывают для фармакотерапии лекарственные формы с модифицированным высвобождением, стали мощным катализатором дальнейшего развития инновационных технологий и появления ультрасовременных нано- и таргетных препаратов. Но об этом — в следующей статье.
Нашли ошибку? Выделите текст и нажмите Ctrl+Enter.