Какие причины и признаки увеличенного сердца
Сердечно-сосудистые заболевания — одна из ведущих причин ранней инвалидности и смерти в мире. Особенно озабочены кардиологи мужским здоровьем, ведь по статистике мужчины в среднем живут на 13 лет меньше женщин. Одна из патологий — увеличенное сердце, или кардиомегалия. Этот дефект может указывать на развитие заболевания, но также является вариантом нормы. Например, у спортсменов сердце имеет большие размеры. Причины и последствия увеличенного сердца у взрослого — тема нашего сегодняшнего разговора. Игнорировать проблему не стоит, поскольку у такого явления могут быть серьезные осложнения.
Увеличено сердце: причины и последствия
Если человек долго занимался спортом и накачал сердечную мышцу, при завершении карьеры ему требуется реабилитация. Снижение физической активности должно проходить под наблюдением врача, хотя в данном случае и не идет речь о патологическом состоянии. Основная причина, почему увеличено сердце у женщины, беременность на позднем сроке или недавние роды. У беременных сердце может увеличиваться из-за увеличения объема циркулирующей крови. Такие причины возникают не из-за болезней. Однако, увеличение сердца может быть симптомом более серьезных заболеваний.
Причины увеличенного сердца у взрослого:
Кардиомегалия может быть неопасным состоянием, а тяжесть патологии зависит от того, какой отдел увеличен. Наибольшую опасность дефект представляет для мужчин и пожилых людей. Если по какой-либо причине сердце увеличено в размерах, особенно в течение длительного времени, возрастает риск сердечной недостаточности, от которой половина пациентов умирает в течение 5 лет. У пациентов с большим сердцем увеличивается вероятность тромбоза и обратного тока крови. Главная опасность кардиомегалии — риск внезапной сердечной смерти.
Признаки увеличенного сердца
В большинстве случаев кардиомегалия протекает бессимптомно. Со временем из-за того, что сердце не может эффективно перекачивать кровь, могут появиться следующие симптомы:
Симптомы неспецифичны и могут указывать на другое заболевание. Поэтому для дальнейшего прогноза важна качественная и своевременная диагностика.
Диагностика и лечение
Обследование позволяет установить причины, почему увеличено сердце, а также подобрать грамотное лечение. Иногда потребуется пожизненный прием медикаментов. Возможно, потребуется имплантация кардиостимулятора или кардиовертера-дефибриллятора (ИКД), операция на сердечном клапане и аортокоронарное шунтирование. Вид лечения подбирается индивидуально в зависимости от тяжести состояния и наличия дополнительных кардиологических проблем.
Диагностика поможет вовремя выявить причины, почему увеличено сердце у человека, а значит вовремя оказать необходимую помощь.
У некоторых людей кардиомегалия — это временное состояние, а кто-то может вести привычный образ жизни даже с увеличенным сердцем. Для других пациентов потребуется срочное лечение.
В целом же, с кардиомегалией нужно придерживаться здорового образа жизни:
Как бы банально ни звучало, но здоровый образ жизни был и остается лучшим средством профилактики сердечно-сосудистых заболеваний в любом возрасте. Конечно, не все проблемы можно решить только упражнениями и диетами, но вкупе с качественной медицинской помощью прогноз становится более благоприятным. Позаботьтесь о своем здоровье вместе с кардиологами из Чеховского сосудистого центра в Московской области. Здесь вы можете пройти диагностику и получить современное эффективное лечение.
Признаки увеличения левого предсердия на экг что это значит
Гипертрофия миокарда предсердий и желудочков сердца развивается при различных болезнях, которые вызывают хронические гемодинамические перегрузки в большом и малом круге кровообращения. Это ведет к увеличению мышечных волокон и всей массы миокарда отделов сердца, что в свою очередь увеличивает электродвижущую силу и отклоняет увеличенный вектор сердца в сторону гипертрофированного желудочка или предсердия. В связи с этим на ЭКГ увеличивается соответствующий зубец R или Р. Кроме того, гипертрофированный отдел продолжительнее возбуждается, и поэтому компплекс QRS или зубец Р уширяется или деформируется.
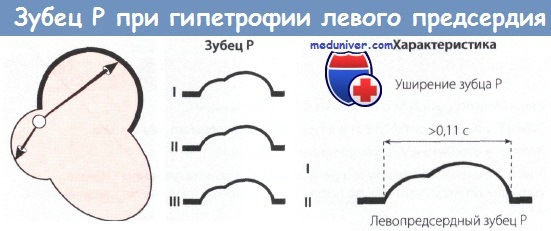
Гипертрофия левого предсердия. В левом предсердии возбуждение начинается и заканчивается позже, чем в правом, поэтому при гипертрофии левого предсердия общее время возбуждения предсердий увеличено и соответственно ширина зубца Р больше нормы и составляет 0,11—0,15 с. В связи с увеличением электродвижущей силы левого предсердия возрастает амплитуда второй (левопредсердной) фазы зубца Р. Последний принимает двугорбую форму с большой второй фазой. Такой зубец Р регистрируется в отведениях I, II, aVF или aVL. В левых грудных отведениях зубец Р двугорбый, увеличенный с приблизительно одинаковой амплитудой обеих положительных фаз. В отведении VI зубец Р двухфазный с преобладанием глубокой и широкой отрицательной фазы, что является весьма частым и надежным признаком гипертрофии левого предсердия.
Уширенный двугорбый зубец Р принято называть P-mitrale, так как он чаще всего встречается на ЭКГ больных с митральным пороком сердца.
Гипертрофия правого предсердия. Только при большой гипертрофии правого предсердия (с дистрофическими и склеротическими изменениями его миокарда) ширина зубца Р может достигнуть 0,11—0,13 с. В отведениях II, III, aVF зубец Р становится высоким, иногда с заостренной вершиной, так как электродвижущая сила возбуждения предсердий увеличивается, а продолжительность его остается прежней. Такой формы зубец принято называть P-pulmonale, потому что он чаще всего наблюниях от конечностей. Основным признаком гипертрофии, относящейся к любому из этих типов, является высокий зубец R (выше нормы) в отведении, ось которого параллельна электрической оси сердца.
При горизонтальном положении электрической оси отмечается высокий зубец RI (RI > RII) и выраженный зубец S III, амплитуда которого больше амплитуды низкого зубца г ш, при RaVF > SavF. Одним из признаков гипертрофии левого желудочка, предложенным Sokolow и Lyon (1948), является амплитуда RI >15 мм. Нередко комплекс QRS уширяется (более 0,1 с), и сегмент S—Т, смешается вниз от изолинии. Зубец TI, aVL, иногда зубец Тп становятся низкими изоэлектричными или отрицательными. Отрицательный зубец Т при гипертрофии левого желудочка обычно имеет асимметричную форму, покатое нисходящее колено и крутое восходящее. Зубец TaVR может быть положительным.
При отклонении электрической оси влево отмечаются высокий зубец RI,avL (RaVL>11 мм) и глубокий зубец S и r. Часто наблюдаются уширение комплекса QRS, значительное смещение вниз от изоэлектрической линии сегмента S—ТI,II,aVL и вверх от изолинии сегмента S—ТIII,avF. Зубец TI,II,aVL низкий или отрицательный, зубец ТIII положительный.
Лечение гипертрофической кардиомиопатии
Гипертрофическая кардиомиопатия (ГКМП) – это генетически обусловленное заболевание миокарда, проявляющееся комплексом специфических морфо-функциональных изменений
Лечение гипертрофической кардиомиопатии
Гипертрофическая кардиомиопатия (ГКМП) – это генетически обусловленное заболевание миокарда, проявляющееся комплексом специфических морфо-функциональных изменений и постепенно прогрессирующим течением с высоким риском развития жизнеугрожающих аритмий и внезапной смерти.
Типичными являются морфологические изменения: аномалия архитектоники сократительных элементов миокарда (гипертрофия и дезориентация мышечных волокон), развитие фибротических изменений мышцы сердца, патология мелких интрамиокардиальных сосудов.
При ГКМП происходит массивная гипертрофия миокарда левого (и реже правого желудочка), чаще асимметричного характера за счет утолщения межжелудочковой перегородки, часто с развитием обструкции выходного тракта левого желудочка (ЛЖ) при отсутствии каких-либо явных причин.
Общепризнанной является представление о преимущественно наследственной природе ГКМП. В связи с этим, широкое распространение получил термин «семейная гипертрофическая кардиомиопатия». К настоящему времени установлено, что более половины всех случаев заболевания являются наследуемыми, при этом основной тип наследования – аутосомно-доминантный. Оставшиеся приходятся на так называемую спорадическую форму; в этом случае у пациента нет родственников, болеющих ГКМП или имеющих гипертрофию миокарда. Считается, что большинство, если не все случаи спорадической ГКМП, также имеют генетическую причину, т. е. вызваны случайными мутациями.
Гипертрофическая кардиомиопатия – это генетически гетерогенное заболевание, причиной которого являются более 200 описанных мутаций нескольких генов, кодирующих белки миофибриллярного аппарата. К настоящему времени известны 10 белковых компонентов сердечного саркомера, выполняющих контрактильную, структурную или регуляторную функции, дефекты которых наблюдаются при ГКМП. Причем в каждом гене множество мутаций могут становиться причиной заболевания (полигенное мультиаллельное заболевание).
Наличие той или иной ассоциированной с ГКМП мутации признается «золотым» стандартом диагностики заболевания. При этом описанные генетические дефекты характеризуются разной степенью пенетрантности, выраженностью морфологических и клинических проявлений. Тяжесть клинической картины зависит от присутствия и степени гипертрофии.
Таким образом, ГКМП характеризуется крайней гетерогенностью вызывающих ее причин, морфологических, гемодинамических и клинических проявлений, разнообразием вариантов течения и прогноза, что существенно затрудняет выбор адекватных и наиболее эффективных лечебных подходов по контролю и коррекции имеющихся нарушений.
Возможны три гемодинамических варианта обструктивной ГКМП:
Cимптомы болезни разнообразны и малоспецифичны, связаны с гемодинамическими нарушениями (диастолическая дисфункция, динамическая обструкция путей оттока, митральная регургитация), ишемией миокарда, патологией вегетативной регуляции кровообращения и нарушением электрофизиологических процессов в сердце. Диапазон клинических проявлений крайне велик: от бессимптомных до неуклонно прогрессирующих и трудно поддающихся медикаментозному лечению форм, сопровождающихся тяжелой симптоматикой.
Повышение диастолического давления в левом желудочке из-за диастолической дисфункции, динамическая обструкция выносящего тракта левого желудочка проявляются одышкой в покое и при физической нагрузке, утомляемости, слабости. Нарастание давления в малом круге кровообращения сопровождается развитием острой левожелудочковой недостаточности (чаще в ночные часы – сердечная астма, альвеолярный отек легких).
Падение фракции выброса при физической нагрузке или нарушениях сердечного ритма сопровождается ухудшением кровообращения головного мозга. Преходящая ишемия мозговых структур проявляется кратковременной потерей сознания (обморок) или предобморочными состояниями (внезапная слабость, головокружение, потемнение в глазах, шум и «заложенность» в ушах).
Методы исследования:
ЭХО-КГ – основной метод диагностики ГКМП. Критериями диагностики ГКМП на основании данных ЭХО-КГ являются:
Если в покое обструкции выносящего тракта левого желудочка нет, ее можно спровоцировать медикаментозными (ингаляция амилнитрита, введение изопреналина, добутамина) или функциональными пробами (проба Вальсальвы, физическая нагрузка), которые уменьшают преднагрузку или повышают сократимость левого желудочка.
Катетеризация сердца и коронарная ангиография проводятся для оценки коронарного русла перед миоэктомией или операцией на митральном клапане, а также чтобы выяснить причину ишемии миокарда. При этом к характерным признакам ГКМП относят:
Сцинтиграфия миокарда и позитронно-эмиссионная томография
При гипертрофической кардиомиопатии сцинтиграфия миокарда имеет некоторые особенности, однако в целом ее значение в диагностике ишемии такое же, как и обычно. Стойкие дефекты накопления указывают на рубцовые изменения после инфаркта миокарда, обычно они сопровождаются снижением функции левого желудочка и плохой переносимостью физической нагрузки. Обратимые дефекты накопления указывают на ишемию, вызванную снижением коронарного резерва при нормальных артериях или коронарным атеросклерозом. Обратимые дефекты часто никак не проявляются, однако, по-видимому, они повышают риск внезапной смерти, особенно у молодых больных с гипертрофической кардиомиопатией. При изотопной вентрикулографии можно выявить замедленное наполнение левого желудочка и удлинение периода изоволюмического расслабления.
Позитронно-эмиссионная томография – более чувствительный метод, кроме того, она позволяет учесть и устранить помехи, связанные с затуханием сигнала. Позитронно-эмиссионная томография с фтордезоксиглюкозой подтверждает наличие субэндокарлиальной ишемии, вызванной снижением коронарного резерва.
Современные подходы к лечению ГКМП
По современным представлениям, лечебная стратегия определяется в процессе разделения больных на категории в зависимости от описанных выше вариантов течения и прогноза.
Все лица с ГКМП, включая носителей патологических мутаций без фенотипических проявлений болезни и пациентов с бессимптомным течением заболевания, нуждаются в динамическом наблюдении, в ходе которого оцениваются характер и выраженность морфологических и гемодинамических нарушений. Особое значение имеет выявление факторов, определяющих неблагоприятный прогноз и повышенный риск внезапной смерти (в частности, скрытых, прогностически значимых аритмий).
Общие мероприятия
Ограничение значительных физических нагрузок и запрещение занятий спортом, способных вызывать усугубление гипертрофии миокарда, повышение внутрижелудочкового градиента давления и риска внезапной смерти.
Медикаментозное лечение
До настоящего времени окончательно не решен вопрос о необходимости проведения активной медикаментозной терапии у наиболее многочисленной группы больных с бессимптомной или малосимптомной формами ГКМП и низкой вероятностью внезапной смерти. Противники активной тактики обращают внимание на то, что при благоприятном течении заболевания продолжительность жизни и показатели смертности не отличаются от таковых в общей популяции. Некоторые же авторы указывают на то, что использование в этой группе пациентов β-адреноблокаторов и антагонистов кальция (верапамил) может приводить к сдерживанию гемодинамических нарушений и клинической симптоматики. При этом никто не оспаривает тот факт, что выжидательная тактика в случаях бессимптомного или малосимптомного течения ГКМП возможна лишь при отсутствии признаков внутрижелудочковой обструкции, обмороков и серьезных нарушений сердечного ритма, отягощенной наследственности и случаев ВС у близких родственников.
Следует признать, что лечение ГКМП, генетически обусловленного заболевания, обычно распознаваемого на поздней стадии, пока может быть в большей степени симптоматическим и паллиативным. Тем не менее к основным задачам лечебных мероприятий относятся не только профилактика и коррекция основных клинических проявлений заболевания с улучшением качества жизни пациентов, но и положительное влияние на прогноз, предупреждение случаев ВС и прогрессирования заболевания.
Основу медикаментозной терапии ГКМП составляют препараты с отрицательным инотропным действием: β-адреноблокаторы и блокаторы кальциевых каналов. Для лечения весьма распространенных при этом заболевании нарушений сердечного ритма используются также дизопирамид (антиаритмический препарат IA класса) и амиодарон.
Предпочтение отдается β-блокаторам без внутренней симпатомиметической активности. Наибольший опыт накоплен по применению пропранолола (обзидан, анаприлин). Его назначают начиная с 20 мг 3-4 раза в день, с постепенным увеличением дозы под контролем пульса и артериального давления (АД) до максимально переносимой в большинстве случаев 120–240 мг/сут. Следует стремиться к применению возможно более высоких доз препарата, так как отсутствие эффекта терапии β-блокаторами, вероятно, связано с недостаточной дозировкой. При этом нельзя забывать о том, что повышение дозировок существенно увеличивает риск известных побочных эффектов.
Инвазивные методы лечения:
1. Чрезаортальная септальная миэктомия
2. Вальвулопластики или протезирования митрального клапана
В ряде случаев при наличии дополнительных показаний для уменьшения выраженности обструкции и митральной регургитации одномоментно выполняется операция вальвулопластики или протезирования митрального клапана низкопрофильным протезом. Улучшить отдаленные результаты миэктомии позволяет последующая длительная терапия верапамилом, обеспечивающая улучшение диастолической функции ЛЖ, что не достигается при хирургическом лечении.
3. Иссечения межжелудочковой перегородки
В настоящее время разработаны и успешно применяются отличные от классической миэктомии методики. В частности, в НЦССХ им. А. Н. Бакулева под руководством академика Л. А. Бокерия разработана оригинальная методика иссечения зоны гипертрофированной МЖП из конусной части правого желудочка. Этот способ хирургической коррекции обструктивной ГКМП является высокоэффективным и может стать методом выбора в случаях одновременной обструкции выходных отделов обоих желудочков, а также в случаях среднежелудочковой обструкции ЛЖ.
4. Транскатетерная септальная аблация
Другим альтернативным методом лечения рефракторной обструктивной ГКМП является транскатетерная алкогольная септальная аблация. Методика предполагает инфузию через баллонный катетер в перфорантную септальную ветвь 1–3 мл 95% спирта, вследствие чего возникает инфаркт гипертрофированного отдела МЖП, захватывающей от 3 до 10% массы миокарда ЛЖ (до 20% массы МЖП). Это приводит к значимому уменьшению выраженности обструкции выходного тракта и митральной недостаточности, объективной и субъективной симптоматике заболевания.
В Волынской больнице отработана методика выполнения транскатетерной септальной аблации при ГКМП. Доказан положительный результат данного вмешательства при относительно низком риске развития осложнений.
Другая гипертрофическая кардиомиопатия (I42.2)
Версия: Справочник заболеваний MedElement
Общая информация
Краткое описание
Необструктивная гипертрофическая кардиомиопатия
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
По локализации
— гипертрофия базальных отделов МЖП
— тотальная гипертрофия МЖП
— тотальная гипертрофия МЖП и свободной стенки ЛЖ
— гипертрофия верхушки сердца с возможным распространением на свободную стенку ЛЖ и перегородку
б) Симметричная (концентрическая)
II. По гемодинамической форме
III. По градиенту давления (при обструктивной форме)
IV. По клиническим проявлениям
V. По стадиям клинического течения
Этиология и патогенез
Выделяют несколько патогенетических механизмов развития заболевания:
— Гипертрофия межжелудочковой перегородки. В результате образовавшегося генетического дефекта в саркомере миокарда может развиваться непропорциональная гипертрофия межжелудочковой перегородки, которая в ряде случаев возникает даже в период эмбрионального морфогенеза. На гистологическом уровне изменения миокарда характеризуются развитием нарушений метаболизма в кардиомиоците и значительным увеличением количества ядрышек в клетке, что ведёт к разволокнению мышечных волокон и развитию в миокарде соединительной ткани (англ. феномен «disarray» — феномен «беспорядка»). Дезорганизация клеток сердечной мышцы и замещение миокарда соединительной тканью ведут к снижению насосной функции сердца и служат первичным аритмогенным субстратом, предрасполагающим к возникновению жизнеугрожающих тахиаритмий.
— Обструкция выходного отдела левого желудочка. Большое значение при ГКМП придают обструкции ВОЛЖ, которая возникает в результате непропорциональной гипертрофии межжелудочковой перегородки, что способствует контакту передней створки митрального клапана с межжелудочковой перегородкой и резкому увеличению градиента давления в ВОЛЖ во время систолы.
— Нарушение расслабления миокарда левого желудочка. Длительное существование обструкции и гипертрофии межжелудочковой перегородки приводит к ухудшению активной мышечной релаксации, а также к увеличению ригидности стенок ЛЖ, что обусловливает развитие диастолической дисфункции ЛЖ, а в терминальной фазе заболевания — систолической дисфункции.
— Ишемия миокарда. Важным звеном патогенеза ГКМП выступает ишемия миокарда, связанная с развитием гипертрофии и диастолической дисфункции ЛЖ, что приводит к гипоперфузии и увеличению разволокнения миокарда. В результате происходит истончение стенок левого желудочка, его ремоделирование и развитие систолической дисфункции.
Эпидемиология
Факторы и группы риска
Факторы риска внезапной смерти при гипертрофической кардиомиопатии:
— манифестация заболевания в молодом возрасте (до 16 лет),
— наличие в семейном анамнезе эпизодов внезапной смерти,
— частые синкопальные состояния,
— непродолжительные эпизоды желудочковой тахикардии, выявленные при 24-часовом мониторировании ЭКГ,
— патологическое изменение уровня артериального давления во время нагрузок.
Клиническая картина
Cимптомы, течение
ГКМП может манифестировать в любом возрасте. Клиническая картина обычно вариабельна, и пациенты могут оставаться стабильными длительный период времени.
Классическая триада симптомов при гипертрофической кардиомиопатии включает стенокардию напряжения, одышку при нагрузке и обмороки. Болевые ощущения в грудной клетке отмечаются у 75% больных с гипертрофической кардиомиопатией, классическая стенокардия напряжения— у 25%.
Одышка и часто сопутствующая ей боль в грудной клетке, головокружение, синкопальные и пресинкопальные состояния обычно встречаются при сохранённой систолической функции ЛЖ. Перечисленная симптоматика связана с возникновением диастолической дисфункции миокарда и другими патофизиологическими механизмами (ишемия миокарда, обструкция ВОЛЖ и сопутствующая митральная регургитация, ФП).
У значительного числа больных (5-28%) возникает фибрилляция предсердий, повышающая риск развития тромбоэмболических осложнений.
При объективном исследовании больных необструктивной формой гипертрофической кардиомиопатии отклонений от нормы может не быть, но иногда определяются увеличение продолжительности верхушечного толчка, IVтон сердца.
Диагностика
Фонокардиография. Весьма характерным, но неспецифичным, является патологическое усиление III и особенно IV тонов сердца.Важным признаком субаортальной обструкции является так называемый поздний, не связанный с I тоном, систолический шум ромбовидной или лентовидной формы с эпицентром на верхушке или в III-IV межреберье у левого края грудины. Он проводится в подмышечную область и реже на основание сердца и сосуды шеи. Отличительными особенностями шума, позволяющими заподозрить обструктивную ГКМП, служат специфические изменения его амплитуды и продолжительности при физиологических и фармакологических пробах, направленных на увеличение или уменьшение степени обструкции и связанной с ней митральной недостаточности. Подобный характер динамики шума имеет не только диагностическое значение, но и является ценным критерием дифференциальной диагностики ГКМП с первичными поражениями митрального и аортального клапанов. Шуму может предшествовать дополнительный тон, образующийся при соприкосновении митральной створки с межжелудочковой перегородкой.У части больных в диастоле регистрируется следующий за III тоном короткий низкоамплитудный шум притока, то есть относительного митрального или изредка трикуспидального стеноза. В последнем случае шум усиливается на вдохе. При значительной выраженности препятствия кровотоку определяется парадоксальное расщепление II тона вследствие удлинения периода изгнания левого желудочка пропорционально величине систолического градиента давления.
Рентгенологическое исследование грудной клетки. Данные рентгенологического исследования сердца мало информативны. Даже при значительной гипертрофии миокарда существенные изменения тени сердца могут отсутствовать, поскольку объем полости левого желудочка не изменен или уменьшен. У части больных отмечается незначительное увеличение дуг левого желудочка и левого предсердия и закругление верхушки сердца, а также признаки умеренной венозной легочной гипертензии. Аорта обычно уменьшена.
Допплерэхокардиография
Ни один из ЭхоКГ признаков ГКМП, несмотря на высокую чувствительность, не является патогномоничным.
Основные ЭХОКГ-признаки :
— Ассиметричная гипертрофия миокарда левого желудочка. Общепринятый критерий ГКМП — толщина межжелудочковой перегородки более 15 мм при нормальной или увеличенной толщине задней стенки ЛЖ. Учитывая, что заболевание генетически детерминировано, степень гипертрофии может быть различной. Тем не менее, наличие симметричной гипертрофии не исключает диагноз ГКМП.
Стресс-ЭхоКГ используется для выявления коронарной болезни сердца, сопутствующей ГКМП, что имеет важное прогностическое и терапевтическое значение.
Радионуклидная вентрикулография как наиболее воспроизводимый метод оценки систолической и диастолической функции не только левого, но и правого желудочка используется в основном для наблюдения за больными ГКМП в динамике и для оценки эффективности лечебных мероприятий.
Позитронно-эмиссионная томография представляет уникальную возможность для неинвазивной оценки регионарной перфузии и метаболизма миокарда. Предварительные результаты ее применения при ГКМП показали снижение коронарного расширительного резерва не только в гипертрофированных, но и неизмененных по толщине сегментах левого желудочка, что особенно выражено у больных с ангинозной болью. Нарушение перфузии часто сопровождается субэндокардиальной ишемией
При измерении давления в полостях сердца наиболее важное диагностическое и терапевтическое значение имеет обнаружение градиента систолического давления между телом и выносящим трактом левого желудочка в покое или при провокационных тестах. Этот признак характерен для обструктивной ГКМП и не наблюдается при необструктивной форме заболевания, что не позволяет исключить ГКМП при его отсутствии. При регистрации градиента давления в полости левого желудочка по отношению к его выносящему тракту необходимо удостовериться, что он обусловлен субаортальной обструкцией изгнанию крови, а не является следствием плотного схватывания конца катетера стенками желудочка при так называемой «элиминации» или «облитерации» его полости. Наряду с субаортальным градиентом важным признаком препятствия изгнанию крови из левого желудочка служит изменение формы кривой давления в аорте. Как и на сфигмограмме, она приобретает форму «пика и купола».У значительной части больных ГКМП, независимо от наличия или отсутствия субаортального градиента, определяется повышение конечно-диастолического давления в левом желудочке и давления на путях его притока — в левом предсердии, легочных венах, «легочных капиллярах» и легочной артерии. При этом легочная гипертензия носит характер пассивной, венозной. Увеличение конечно-диастолического давления в гипертрофированном левом желудочке обусловлено нарушением его диастолической податливости, характерным для ГКМП. Иногда, в терминальной стадии развития заболевания, оно усугубляется в результате присоединения систолической дисфункции миокарда.
Эндомиокардинальная биопсия левого или правого желудочков рекомендуют проводить в тех случаях, когда после клинического и инструментального обследования остаются сомнения относительно диагноза. При выявлении характерных патогистологических признаков заболевания делают заключение о соответствии морфологических изменений в миокарде клиническому диагнозу ГКМП.С другой стороны, обнаружение структурных изменений, специфичных для какого-либо другого поражения миокарда (например, амилоидоза) позволяет исключить ГКМП.
При наличии допплерэхокардиографии и магнитно-резонансной томографии ЭМБ для диагностики ГКМП сейчас практически не используется.
Лабораторная диагностика
Дифференциальный диагноз
Дифференциальная диагностика проводится с рядом заболеваний, сопровождающихся развитием гипертрофии левого желудочка, прежде всего «сердце спортсмена», приобретенные и врожденные пороки, ДКМП, а при склонности к повышению АД — эссенциальную артериальную гипертензию. Дифференциальная диагностика с пороками сердца, сопровождающимися систолическим шумом, приобретает особо важное значение в случаях обструктивной формы ГКМП. У больных с очаговыми и ишемическими изменениями на ЭКГ и ангинозной болью первостепенной задачей является дифференциальная диагностика с ИБС. При преобладании в клинической картине признаков застойной сердечной недостаточности в сочетании с относительно небольшим увеличением размеров сердца ГКМП следует дифференцировать от миксомы предсердий, хронического легочного сердца и заболеваний, протекающих с синдромом рестрикции — констриктивного перикардита, амилоидоза, гемохроматоза и саркоидоза сердца и рестриктивнойкардиомиопатии.
Ишемическая болезнь сердца. Наиболее часто ГКМП приходится дифференцировать с хроническими и реже острыми формами ИБС. В обоих случаях могут наблюдаться ангинозная боль в области сердца, одышка, нарушения сердечного ритма, сопутствующая артериальная гипертензия, добавочные тоны в диастолу, мелко- и крупноочаговые изменения и признаки ишемии на ЭКГ.Важное значение для постановки диагноза имеет ЭхоКГ, при которой у части больных определяются свойственные ИБС нарушения сегментарной сократимости, умеренная дилатация левого желудочка и снижение его фракции выброса. Гипертрофия левого желудочка весьма умеренная и чаще носит симметричный характер. Впечатление о непропорциональном утолщении межжелудочковой перегородки может создавать наличие зон акинезии вследствие постинфарктного кардиосклероза в области задней стенки левого желудочка с компенсаторной гипертрофией миокарда перегородки. При этом, в противоположность асимметричной гипертрофии межжелудочковой перегородки как формы ГКМП, гипертрофия перегородки сопровождается гиперкинезией. В случаях заметной дилатации левого предсердия вследствие сопутствующей митральной регургитации при ИБС неизменно отмечается дилатация левого желудочка, несвойственная больным ГКМП. Подтвердить диагноз ГКМП позволяет обнаружение признаков субаортального градиента давления.При отсутствии ЭХОКГ- данных в пользу субаортальной обструкции дифференциальная диагностика значительно затрудняется. Единственно надежным методом распознавания или исключения ИБС в таких случаях является рентгеноконтрастная коронарография. У лиц среднего и старшего возраста, особенно у мужчин, необходимо иметь в виду возможность сочетания ГКМП с ИБС.
Осложнения
Течение заболевания может осложняться развитием таких осложнений, как:
Лечение
К общим мероприятиям относятся ограничение значительных физических нагрузок и запрещение занятий спортом, способных вызывать усугубление гипертрофии миокарда, повышение внутрижелудочкового градиента давления и риска ВС. Для предупреждения инфекционного эндокардита в ситуациях, связанных с развитием бактериемии, при обструктивных формах ГКМП рекомендуется антибиотикопрофилактика, аналогичная таковой у больных с пороками сердца.
Основу медикаментозной терапии ГКМП составляют препараты с отрицательным инотропным действием: β-адреноблокаторы и блокаторы кальциевых каналов (верапамил).
β-адреноблокаторы стали первой и остаются и по сей день наиболее эффективной группой лекарственных средств, применяемых в лечении ГКМП. их следует назначать больным независимо от выраженности градиента внутрижелудочкового давления в покое. Предпочтительно воздерживаться от назначения блокаторов β-aope-норецепторов с внутренней симпатомиметической активностью (пин-дол ол, окспренолол). Пропранолол назначают в дозе 240-320 мг в сутки и более (максимальная суточная доза — 480 мг), метопролол — в дозе 200 мг в сутки и более. Кардиоселективные блокаторы бета-адренорецеп-торов при гипертрофической кардиомиопатии не имеют преимуществ перед неселективными, так как в высоких дозах селективность практически утрачивается.
В случае противопоказаний к назначению блокаторов бета-адренорецепторов или неполного исчезновения симптомов альтернативой могут быть блокаторы кальциевых каналов. Среди блокаторов кальциевых каналов препаратом выбора является верапамил (изоптин, финоптин). Он обеспечивает симптоматический эффект у 65–80% больных. При назначении блокаторов кальциевых каналов необходима максимальная осторожность при наличии выраженной гипертрофии и очень высоком давлении наполнения левого желудочка. Следует иметь в виду, что блокаторы кальциевых каналов, включая верапамил, при длительном применении могут повышать диастолическое давление и снижать сердечный выброс. Лечение верапамилом следует начинать с назначения в низких дозах — по 20-40 мг 3 раза в сутки, постепенно повышая до суточной дозы 240-320 мг и более. Клиническое улучшение при приеме верапамила сопровождается повышением толерантности к физической нагрузке.
Для лечения аритмий используются антиаритмические препараты, из которых наиболее эффективными являются дизопирамид и амиодарон. Дизопирамид (ритмилен), относящийся к антиаритмикам IA класса, обладает выраженным отрицательным инотропным эффектом, у больных ГКМП способен снижать уровень обструкции выходного тракта левого желудочка, положительно влияет на структуру диастолы. Начальная доза обычно составляет 400 мг/сут с постепенным увеличением до 800 мг. При этом необходимо контролировать продолжительность интервала Q-T по ЭКГ.
Единственным препаратом, на фоне которого на сегодняшний день отмечено устранение желудочковой тахиаритмии, снижение частоты случаев внезапной смерти и улучшение прогноза заболевания, является амиодарон. Амиодарон назначают в суточной дозе 1200 мг в течение 5-7 дней, затем в суточной дозе 800 мг и 600 мг в течение 2-й и 3-й недель лечения с последующим переходом на поддерживающую суточную дозу 200 мг.
При отсутствии клинического эффекта от активной медикаментозной терапии симптоматичным больным III-IV функционального класса по классификации Нью-Йоркской ассоциации кардиологов с выраженной асимметричной гипертрофией МЖП и субаортальным градиентом давления в покое, равным 50 мм рт. ст. и более, показано хирургическое лечение ( ссылка на лечение из I42.1)
Прогноз
Необструктивные формы ГКМП обладают, в целом, более благоприятным течением с меньшей выраженностью ограничения функционального состояния и большей продолжительностью периодов стабилизации.Прогноз наиболее благоприятен при длительном бессимптомном течении заболевания и неотягощенном семейном анамнезе, особенно при верхушечной форме ГКМП. В отдельных таких случаях заболевание может не отражаться на продолжительности жизни.