Синдром вегетативной дисфункции
Что это такое? Это комплекс симптомов, возникающих из-за нарушения нейро-гуморальной регуляции работы органов и систем. В норме симпатическая и парасимпатическая нервная системы гармонично и слаженно работают вместе. Симпатическая система преобладает, если человеку нужно действовать быстро, активно: бежать, прятаться, бояться. Парасимпатическая, наоборот – когда человек отдыхает, расслаблен, спит.
При сбое в работе этих двух систем и возникает синдром вегетативной дисфункции.
Это нарушение бывает центрального и периферического происхождения. В первом случае проблема локализуется в структурах мозга. Во втором – сбой возникает в структурах симпатической и парасимпатической нервных систем.
Первичные нарушения возникают редко – только в случае органического поражения мозговых структур. Чаще бывают вторичные нарушения при наличии соматических заболеваний, психических или неврологических.
Течение синдрома вегетативной дисфункции может быть перманентное (постоянное), или приступообразное.
Люди с избытком симпатической иннервации имеют определенный склад характера – это активные, очень работоспособные энергичные люди, которые быстро думают, быстро принимают решения, креативны. Но при этом часто им трудно заснуть, в большей или в меньшей степени присутствует тревожность.
Как правило, они привыкают к своему складу личности, но в определенные моменты жизни, когда берут на себя слишком много, не рассчитав свои силы, или обстоятельства складываются так, что они не успевают восстановиться, их симпатическая система становится слишком напряжена, и тогда возникают следующие жалобы:
Люди с преобладанием в конституции парасимпатической нервной системы часто задумчивы, медлительны, нерешительны, мечтательны, склонны к депрессиям. В тяжелых жизненных ситуациях или при избыточной нагрузке их парасимпатическая нервная система становится еще активней:
Личности с синдромом вегетативной дисфункции, как правило, приятные, чувствительные, отзывчивые. Среди таких людей много поэтов, писателей, художников, журналистов, педагогов или просто творческих людей.
Задача невролога – помочь пациенту с синдромом вегетативной дисфункции, объяснить, успокоить, обследовать и назначить лечение.
Прежде всего, необходимо наладить режим сна и бодрствования пациента. Также необходимо обеспечить ему правильное питание, восполнить недостаток витаминов и микроэлементов. Очень важно пить достаточное количество воды. Следует убрать из спальной комнаты телевизор и компьютер, комнату для сна максимально затемнить. По возможности, исключить общение с неприятными людьми, соблюдать информационную гигиену, то есть снизить количество раздражающих факторов.
Невролог должен осмотреть пациента для исключения первичного поражения нервной системы, назначить ряд обследований и выработать схему лечения. В таких случаях нет единого шаблона, к каждому пациенту нужен индивидуальный подход и подбор терапии. В лечении используются антиоксиданты, ноотропы, антидепрессанты, транквилизаторы, витамины, сосудистые средства, симптоматическая терапия.
Вегето-висцеральные нарушения у новорожденных детей с перинатальными поражениями мозга
Ведущее звено в формировании вегето-висцеральных нарушений — поражение диэнцефальных структур мозга, лимбической системы, продолговатого мозга и последующее расстройство нейроэндокринной регуляции Под вегето-висцеральными нарушениями у новорожд
Ведущее звено в формировании вегето-висцеральных нарушений — поражение диэнцефальных структур мозга, лимбической системы, продолговатого мозга и последующее расстройство нейроэндокринной регуляции
 |
Под вегето-висцеральными нарушениями у новорожденных подразумевается широкий спектр морфологических и функциональных сдвигов во многих органах и системах, обозначаемых как соматоневрологические, нейросоматические или нейроэндокринные. Преимущественно имеются в виду сосудистые, желудочно-кишечные нарушения, а также нарушения терморегуляции.
При любом из клинико-неврологических синдромов могут отмечаться соматические нарушения различной степени выраженности. Так, синдром общего угнетения, как правило, сопровождается расстройствами дыхания, нарушениями сосудистого тонуса и терморегуляции, синдром повышенной нервно-рефлекторной возбудимости и гипертензионно-гидроцефальный — дисрегуляцией сфинктров, нарушением моторики желудочно-кишечного тракта. Синдром вегето-висцеральных нарушений часто относят к восстановительному периоду энцефалопатии, когда на фоне стихания собственно неврологических нарушений, нормализации мышечного тонуса и рефлекторной сферы указанные нарушения выступают на первый план, доминируют в клинической картине энцефалопатии. По данным нашей клиники, частота синдрома вегето-висцеральных нарушений у детей первого года жизни, перенесших перинатальную энцефалопатию, составляет около 10%; однако и при других синдромах восстановительного периода наряду с преобладающими неврологическими расстройствами (двигательными или психоэмоциональными) могут быть отмечены отдельные соматовегетативные отклонения.
| В практике врача-педиатра особое значение придается следующим функциям вегетативной системы: регуляции тонуса сосудов и сердечной деятельности, регуляции секреторной деятельности желез внутренней секреции, терморегуляции, регуляции метаболизма, влиянию на гладкую мускулатуру, адаптационно-трофическому влиянию на рецепторы и синапсы |
Ведущее звено в формировании вегето-висцеральных нарушений — поражение диэнцефальных структур мозга, лимбической системы, продолговатого мозга, последующее расстройство нейроэндокринной регуляции. У новорожденных, особенно у недоношенных детей, высшие вегетативные центры развиты недостаточно, в том числе симпатическая система спинного мозга и пограничного симпатического ствола и парасимпатические ядра среднего мозга. В связи с этим значительно возрастает роль гипоталамуса и лимбико-ретикулярной системы (паравентрикулярные и супраоптические ядра, гипокамп и миндалевидное ядро). Гипоталамус через систему регуляции «Гипофиз — щитовидная железа — надпочечники» осуществляет интеграцию адаптационных процессов. Каждый отдел гипоталамуса осуществляет регуляцию определенной функции симпатической и парасимпатической нервной системы.
Экспериментальными исследованиями установлено, что раздражение задних отделов гипоталамуса приводит к симпатикотонии, повышению АД, снижению температуры тела; патологические процессы в задних отделах гипоталамуса способствуют трофическим нарушениям, половому инфантилизму. Передние отделы гипоталамуса (прежде всего лимбическая система) связаны с регуляцией водного и солевого обмена, сна и бодрствования.
В практике врача-педиатра особое значение придается следующим функциям вегетативной системы: регуляции тонуса сосудов и сердечной деятельности, регуляции секреторной деятельности желез внутренней секреции, терморегуляции, регуляция метаболизма, влияния на гладкую мускулатуру, адаптационно-трофическому влиянию на рецепторы и синапсы.
Показатели состояния вегетативной нервной системы у новорожденных детей
Нарушение любой из этих функций (изолированное или в сочетании с другими нарушениями) возможно при перинатальных энцефалопатиях. Морфологическим субстратом поражения может быть как преходящее нарушение кровообращения в диэнцефально-гипоталамической области, так и стойкие ишемические нарушения и кровоизлияния. Как правило, речь идет о нарушениях кровообращения в бассейнах средней и задней мозговых артерий. Тяжелые сомато-вегетативные нарушения развиваются при внутрижелудочковых кровоизлияниях, типичных для перинатальных поражений мозга у крайне маловесных детей (глубокое коматозное состояние, расстройства дыхания, гипо- и гипертермия, нарушения сердечной деятельности, трофические дисфункции). Среди кровоизлияний других локализаций следует упомянуть субэпендимальные, которые могут отмечаться при разрыве мелких вен между хвостатым ядром и зрительным бугром; они могут разрушать головку хвостатого ядра, что приводит к выраженным расстройствам вегетативно-трофических функций.
Клиническим проявлением синдрома вегетативно-висцеральных нарушений у новорожденных являются вегето-сосудистые дисфункции (лабильность сосудистого тонуса и сердечного ритма). Ребенок имеет «мраморный» рисунок кожи, преходящий цианоз. У недоношенных детей вследствие незрелости центров регуляции сосудистого тонуса более резко, чем у доношенных, выражены изменения окраски кожи, цианоз стоп и кистей. Считается, что даже практически здоровые недоношенные дети в первые недели жизни склонны к гипостазам, т. е. к скоплению крови в нижележащих отделах. У глубоконедоношенных детей может наблюдаться симптом Финкельштейна (или Арлекино). Если этот симптом наблюдается у более зрелых детей, он свидетельствует о поражении диэнцефальных сосудодвигательных центров или о недостаточности функции надпочечников.
Описанные выше нарушения сосудистого тонуса при синдроме вегетативно-висцеральных нарушений сопровождаются изменением показателей артериального давления и лабильностью частоты пульса. Уровень артериального давления при однократном измерении может оказаться как повышенным, так и пониженным: для адекватной оценки АД необходимо его измерение не менее 8 раз в сутки, в дневное и ночное время.
Не менее важным является измерение СО2 и рСО2. Установлено, что у здоровых детей в первые недели жизни происходит постепенное становление биоритма АД — повышение его амплитуды, смещение максимальных показателей АД на вторую половину дня. При легких и среднетяжелых проявлениях перинатальной энцефалопатии возможна задержка становления суточных и недельных ритмов в гемодинамических показателях, при тяжелых — значительное нарушение формирования биоритмов, снижение среднесуточных показателей со смещением систолического и диастолического артериального давления — очень маленькая амплитуда, резкие колебания амплитуд АД; все это свидетельствует о нарушении авторегуляции кровообращения. Лабильность АД при синдроме вегетососудистых нарушений сопровождается лабильностью сердечного ритма и ЧСС.
Число сердечных сокращений варьируется от минуты к минуте в пределах 5—10%. В отличие от тахикардий, связанных с нарушениями сердечной проводимости, нет соответствующих зубцов R и Т на ЭКГ и жесткой стабильности интервалов R—R. Повышение внутричерепного давления может сопровождаться стойкой брадикардией. Иногда указанные нарушения сердечного ритма при перинатальных энцефалопатиях сопровождаются метаболическими изменениями в миокарде (по данным ЭКГ), систоло-диастолическими шумами (при отсутствии персистирующих фетальных коммуникаций).
| Наиболее информативными показателями состояния вегетативного статуса ребенка являются: состояние кожных покровов, ЧСС, АД на правой и левой руке, частота дыхания |
Дыхательные нарушения при синдроме вегето-висцеральных дисфункций обычно сочетаются с сердечно-сосудистыми (приступы брадипноэ и периодическими апноэ, или соответственно тахикардия и тахипноэ) и с лабильностью сосудистого тонуса. Это обусловлено общими механизмами нарушения нейроэндокринной регуляции в системе «гипоталамус — гипофиз — надпочечники» и щитовидной железы. Тяжелые формы дыхательных нарушений [синдром дыхательных расстройств (СДР) центрального генеза], как правило, не относят к вегето-висцеральным расстройствам. К последним относят более легкие функциональные изменения, не сопровождающиеся серьезными нарушениями гомеостаза. У недоношенных детей апноэ 10 — 12 секунд в сочетании с периодами брадикардии может объясняться общей незрелостью.
Тесно связано с нарушениями сосудистого тонуса такое проявление вегето-висцерального синдрома, как нарушение терморегуляции. У доношенных детей оно может проявляться в виде длительного субфебрилитета, извращения характера температурной кривой (утренняя выше вечерней); у недоношенных, находящихся в инкубаторах, — чаще в виде склонности к перегреванию. Возможна также локальная гипотермия (холодные конечности при нормальной или повышенной температуре тела) и асимметрия кожной температуры (рис. 1).
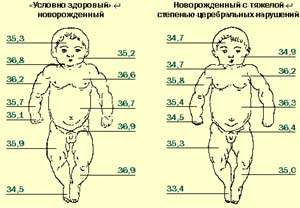 |
| Рисунок 1. Показатели кожной температуры (°C) у недоношенных новорожденных детей |
Одно из наиболее частых проявлений синдрома вегетативно-висцеральных дисфункций — различные дискинезии желудочно-кишечного тракта. В зависимости от преимущественного поражения симпатических и парасимпатических отделов вегетативной нервной системы может наблюдаться гипер- и гипомоторный тип дискинезии кишечника, различные нарушения функции сфинктеров (зияние или спазм).
Часто встречаются такие формы дисфункций желудочно-кишечного тракта, как персистирующие рвоты и срыгивания (функциональная непроходимость), которые могут быть обусловлены халазией кардии и дискоординацией пищеводно-желудочного сфинктера. Стойкое расширение кардиального сфинктера приводит к желудочно-пищеводному рефлюксу и эзофагиту. В свою очередь эзофагит может вызвать сердечно-сосудистую недостаточность, поскольку усиливает свойственную новорожденным симпатикотонию и провоцирует висцеро-висцеральные рефлексы, снижающие коронарный кровоток.
Рвоты и срыгивания при перинатальной энцефалопатии могут быть также обусловлены отсутствием торможения моторики желудка во время и сразу после кормления, как показывают ультразвуковые исследования и электрогастрография. Опасное осложнение срыгиваний и рвот — аспирационный синдром с последующим развитием аспирационной пневмонии. К синдрому срыгиваний и рвот может привести также пилороспазм, реже — дуоденоспазм; как правило, эти виды дискинезий желудочно-кишечного тракта сопровождаются задержкой стула.
При раздражении парасимпатических отделов возможны учащение стула, усиление перистальтики кишечника, для спинальных поражений более характерны метеоризм и ослабление перистальтики. Как правило, при выраженных вегето-висцеральных нарушениях изменения со стороны желудочно-кишечного тракта быстро теряют чисто функциональный характер — наслаиваются дисбактериоз, вторичная ферментативная недостаточность, нарушения всасывания, расстройства питания. Все вышеописанные системные нарушения при перинатальной энцефалопатии могут отмечаться как в комплексе, так и изолированно.
Ведущее значение в установлении диагноза синдрома вегетативно-висцеральных нарушений церебрального генеза имеют соответствующая клиническая картина и исключение органной патологии (пилоростеноза при синдроме срыгивания; кардиопатий — при сердечно-сосудистых нарушениях и т. п. ). Тем не менее в неонатологии могут быть использованы дополнительные способы диагностики и оценки степени тяжести вегетативных дисфункций.
Наиболее информативными показателями состояния вегетативного статуса ребенка являются: состояние кожных покровов, ЧСС, АД на правой и левой руке, частота дыхания (ЧД). Выявить особенности вегетативных нарушений помогают пробы: ортостатическая, эпигастральная, глазо-сердечная (проба Ашнера).
Более тяжелые формы энцефалопатии сопровождаются более выраженной асимметрией кожной температуры (и в центральных, и в периферических участках, тогда как при более легких формах — только в верхней половине тела). Наиболее стойкие и выраженные изменения функциональных проб отмечены у наименее зрелых (глубоконедоношенных) детей.
С целью оценки характера вегетативных дисфункций, подбора терапии и прогнозирования отдаленной патологии целесообразно длительное мониторирование показателей гемодинамики, УЗИ-контроль динамики мозгового кровотока, особенно в бассейне средней и задней мозговых артерий (допплеровское исследование). В связи с широким использованием УЗИ у новорожденных РЭГ-исследование отходит на второй план, хотя с помощью РЭГ можно оценивать реакции ребенка на ортостатическую пробу.
Катамнестические наблюдения при тяжелой энцефалопатии показали, что вегетативные нарушения могут сохраняться в течение нескольких лет, при этом сочетаясь с различными двигательными нарушениями, астено-невротическими состояниями, минимальными мозговыми дисфункциями (ММД). Эти нарушения характеризуются чаще всего вегетососудистой дистонией по гипертоническому (реже гипотоническому) типу, термоневрозами, извращенными реакциями на функциональные пробы. Почти у всех детей длительно сохраняется асимметрия кожной температуры; у некоторых имеются стойкие нарушения сердечного ритма, негрубый систолический шум. Большинство этих детей относится к группе часто и длительно болеющих ОРВИ.
У недоношенных детей, рожденных матерями с ВСД и имеющих в периоде новорожденности резкую «мраморность» кожи, в возрасте 6 — 14 лет высока вероятность развития функционально-гипоталамических синдромов, сопровождающихся эмоционально-волевыми и нейроэндокринными расстройствами (дисфункция щитовидной железы, ожирение, задержка полового созревания и т. п.).
В лечении вегетативно-висцеральных дисфункций новорожденных сочетаются два подхода — патогенетический и посиндромный. Первый включает воздействия, направленные на коррекцию метаболических нарушений, расстройств мозгового кровотока и на улучшение реологических свойств крови. При тяжелых поражениях с выраженными сдвигами метаболизма, дыхательными и сердечно-сосудистыми нарушениями проводится интенсивная терапия, включающая оксигенацию, антиоксидантную терапию, инфузии антигеморрагических и антигипоксических средств, гормонов и антибиотиков, витаминно-энергетических смесей.
Ведущее место в патогенетической терапии принадлежит немедикаментозным воздействиям. Комплексное регулирующее воздействие на механизмы нейроэндокринной регуляции и вегетативные центры оказывают различные виды лечебного массажа, упражнения в воде и сухая иммерсия.
Из традиционных физиотерапевтических способов лечения используется электрофорез (с магнезией, эуфиллином, витаминами), чаще на шейную («воротниковую» ) зону.
Условно к физическим методам воздействия может быть отнесена аэроионотерапия (лампа Чижевского), ароматерапия, возможно использование музыкотерапии, выбор которой определяется преобладанием у ребенка угнетения (в частности, с аритмичностью дыхания) или возбуждения (например, при синдроме срыгиваний). В первом случае используется программа активизирующей музыки (Моцарт, первая часть «Маленькой ночной серенады», Шуберт и т. п.), во втором — успокоительная программа (колыбельные песни, некоторые произведения Баха и т. п.). При чередовании вялости и возбуждения установлена эффективность программы В. В. Кирюшина (чередование различных по характеру звуковысотных упражнений).
Посиндромная терапия некоторых вегето-висцеральных нарушений предполагает использование различных медикаментов. Так, при синдроме дискинезии желудочно-кишечного тракта используются средства, воздействующие на диэнцефальные структуры и периферические рецепторы, — церукал, биморал, но-шпа, ноуспазм, пипольфен, аминазин. При гипомоторном типе дискинезии желудка и кишечника иногда применяется прозерин. Для коррекции сопутствующего дисбактериоза используются препараты-эубиотики, ферменты. При сочетании замедления мозгового кровотока, по данным УЗИ, и лабильности общего сосудистого тонуса («мраморность» кожи) используются кавинтон или винпоцетин, пирацетам. Однако следует заметить, что лекарственная терапия редко является основной. Для коррекции легких вегето-висцеральных нарушений иногда бывает достаточно нормализации условий среды (режим, питание, прогулки, спокойная обстановка).
Клинические проявления и лечение синдрома вегетативной дисфункции у детей и подростков
Опубликовано в журнале, Педиатрия, Том 91, № 2, 2012 Н.Н. Заваденко, Ю.Е. Нестеровский
Кафедра неврологии, нейрохирургии и медицинской генетики педиатрического факультета ГБОУ ВПО РНИМУ им. Н.И. Пирогова Минздравсоцразвития России, Москва
В статье представлены современные взгляды на причины, патогенез, классификацию, клинические проявления и лечение детей и подростков с синдромом вегетативной дисфункции. Дано краткое описание редких генетических заболеваний, сопровождающихся вегетативной дисфункцией. Рассматриваются современные подходы к лечению, в том числе использование магний-содержащих препаратов, в частности Магне В6 в различных лекарственных формах.
Ключевые слова: дети, подростки, вегетативная нервная система, синдром вегетативной дисфункции, магний-содержащие препараты.
Authors present current view on causes, pathogenesis, classification and treatment of autonomic dysfunction in children and adolescents. Brief description of rare genetic diseases accompanied by signs of autonomic dysfunction was presented. Usage of magnesium preparations including Magne-B6 in different medicinal forms was emphasized in discussion of therapeutic tactics.
Key words: children, adolescents, autonomic nervous system, syndrome of autonomic dysfunction, Magnesium-contained preparations.
ВНС выполняет две глобальные функции 2:
К надсегментарным отделам ВНС относятся структуры верхних отделов ствола мозга, гипоталамус, лимбическая система и ассоциативные зоны коры головного мозга. Их функции отличается интегративным характером, то есть на этом уровне происходит согласование вегетативных реакций с эмоциональными, моторными, эндо кринными для обеспечения целостного поведенческого акта [1, 2, 4].
В основе функционирования ВНС лежит принцип взаимодействия симпатической и парасимпатической ВНС. Для обеих этих систем преганглионарная иннервация является в основном холинергической, и в нервных окончаниях на ганглионарных синапсах высвобождается ацетилхолин. Для симпатической системы основным нейромедиатором является норадреналин, но также существуют другие не менее важные постганглионарные нейромедиаторы, среди которых субстанция Р, дофамин и вазоактивный интестинальный полипептид. В течение двух последних десятилетий стало очевидно, что внутри как одного вегетативного нейрона, так и ганглия одновременно присутствует несколько медиаторных систем. В свою очередь различные органы отвечают на высвобождение нейромедиаторов посредством различных систем рецепторов [5]. Несмотря на то, что симпатический и парасимпатический отделы ВНС часто рассматриваются как антагонисты, это далеко не всегда так. Их взаимодействие можно определить как «взаимостимулирующий антагонизм» [6].
Причинами нарушений вегетативной регуляции считаются [1, 2, 4, 7] наследственно-конституциональная предрасположенность; патология пре- и интранатального периодов; травматические и воспалительные заболевания ЦНС; очаги хронического воспаления и соматические заболевания; гормональные перестройки, в частности пре- и пубертатный периоды; хроническое психоэмоциональное перенапряжение; чрезмерные физические нагрузки; неблагоприятные условия окружающей среды. Различают первичные, то есть генетически обусловленные или связанные с физиологическими процессами нарушения функций ВНС, а также вторичные, возникшие вследствие других заболеваний.
В классификации МКБ 10 [9] нарушения, соответствующие СВД, рассматриваются в рубри ках G90 Расстройства ВНС, G90.9 Расстройства ВНС неуточненные, а также F45.3 Соматоформная вегетативная дисфункция из категории F4 «Невротические, связанные со стрессом и соматоформные расстройства». Термин «соматоформный» заменил ранее применявшийся «психосоматический».
Диагностическими критериями соматоформной вегетативной дисфункции являются следующие:
Далее в МКБ 10 классифицируются отдельные расстройства этой группы, определяя орган или систему, беспокоящих пациента как источник симптомов: F45.30 Сердце и ССС; F45.31 Верхние отделы ЖКТ; F45.32 Нижний отдел ЖКТ; F45.33 Дыхательная система; F45.34 Урогенитальная система; F45.38 Другие органы или системы.
В детском возрасте СВД исключительно полиморфен по клиническим проявлениям [7, 8, 10] и наряду с функциональными нарушениями со стороны различных органов и систем представлен психоэмоциональными расстройствами. Развитию соматовегетативных расстройств у дошкольников способствует легкость возникновения отрицательных эмоциональных реакций. Среди их наиболее частых причин встречаются срыв привычного стереотипа поведения (смена круга общения или окружающей обстановки), нерациональный режим дня, отсутствие необходимых условий для игры и самостоятельной деятельности, создание односторонней аффективной привязанности, неправильные воспитательные приемы и отсутствие единого подхода к ребенку [11]. В школьном возрасте появляются факторы конфликтов со сверстниками и учителями, неспособность справиться с учебной нагрузкой [12].
При диагностике СВД у детей важным условием является указание на общую направленность вегетативных изменений (симпатико-тоническая, ваготоническая, смешанная). Ее определение позволяет точнее сориентироваться в диагнозе и выборе терапии [4, 13]. Чем младше ребенок, тем большую парасимпатическую окраску имеют его вегетативно-висцеральные реакции. Симпатоадреналовые влияния усиливаются в пубертате, отражая общую возрастную активацию нейроэндокринной системы.
Симпатикотонический тип чаще отмечается у детей с астеническим телосложением и пониженным питанием. Характерны повышенный аппетит и жажда в сочетании с жалобами на запоры, редкие, но обильные мочеиспускания. Кожные покровы у них сухие, бледные, могут быть горячие или теплые на ощупь, потоотделение скудное, сосудистый рисунок не выражен. Иногда встречаются экзематозные высыпания и зуд. При оценке дермографизма отмечается белое или розовое окрашивание кожи в месте раздражения. Со стороны ССС отмечается склонность к тахикардии, повышению АД. Границы относительной сердечной тупости с тенденцией к сужению («капельное сердце» при рентгенографии грудной клетки). Тоны сердца звучные. Часто предъявляются жалобы на болевые ощущения в области сердца (кардиалгии). Дети отличаются эмоциональной нестабильностью, повышенной отвлекаемостью, часто присутствуют жалобы на нарушения сна (трудности засыпания, поверхностный сон с большим количеством пробуждений и явлениями парасомний).
Дети с преобладанием ваготонии более склонны к избыточной полноте, хотя аппетит у них часто бывает снижен. При общей склонности к покраснению кожных покровов кисти рук цианотичны (акроцианоз), влажные и холодные на ощупь. На теле отмечается мраморность кожных покровов («сосудистое ожерелье»), повышена потливость (общий гипергидроз), имеется склонность к угревой сыпи (особенно в период пубертата), задержке жидкости в виде преходящих отеков под глазами, могут наблюдаться проявления нейродермита, различные аллергические реакции. Волосы сальные. Дермографизм красный, стойкий, разлитой с возникновением приподнятого кожного валика. Могут отмечаться полилимфоаденопатия, увеличение миндалин, аденоидов. Часто после простудных заболеваний длительно отмечается субфебрильная температура либо она наблюдается без указаний на инфекцию. Со стороны сердца типичны брадикардия или брадиаритмия, снижение АД, небольшое расширение границ сердца, приглушение тонов. Встречаются обмороки, головокружения, вестибулопатии, чувство нехватки воздуха. Типичны жалобы на боли в животе, тошноту, метеоризм, гиперсаливацию, отмечаются частые, но необильные мочеиспускания, энурез.Характерны аллергические заболевания, хронические воспалительные заболевания носоглотки. Психоэмоциональный фон спокойный, но могут быть апатия, склонность к развитию депрессий. Сон обычно не нарушен.
При полисистемности нарушений у детей с СВД степень вовлечения различных систем организма может быть неодинаковой. Выделяются следующие клинические варианты СВД, которые встречаются изолированно или в сочетаниях [7]: синдромы артериальной гипер- и гипотензии; нейрогенные обмороки; цефалгический синдром; вестибулопатический синдром; нейрогенная гипертермия; функциональная кардиопатия; гипервентиляционный синдром; дискинезия верхних отделов ЖКТ; дискинезия нижних отделов ЖКТ (синдром раздраженной толстой кишки); ангиотрофоневроз; нейрогенный мочевой пузырь; функциональная легочная гипертензия; гипергидроз; нейроэндокринный синдром; вегетативные кризы (панические атаки).
В современных исследованиях стала отчетливо прослеживаться тенденция к оценке клинических проявлений СВД не с позиций психосоматического подхода, а с учетом новых данных о генетических нарушениях, которые сопровождаются расстройствами ВНС и могут явиться моделями для улучшения понимания патофизиологических механизмов, вызывающих вегетативную дисфункцию. Хотя эти болезни считаются редкими, в описаниях обычно указывается на индивидуальные различия в характере и тяжести клинических проявлений. По этой причине случаи с менее тяжелым течением могут оставаться не выявленными. Остановимся на некоторых из них.
Синдром Оллгрова был описан в 1978 г. [17]. Наследуется по аутосомно-рецессивному типу, локус мутации находится на хромосоме 12q13. Первоначально его называли «синдром три А» в связи с характерной триадой: резистентность к АКТГ с надпочечниковой недостаточностью, ахалазия кардии и нарушения слезоотделения (алакримия). Но поскольку установлено, что этот синдром сочетается с вегетативной дисфункцией, более уместным считается термин «синдром четырех А» [5]. Часто выражены не все составляющие синдрома, возраст дебюта различен. Синдром может проявиться в первое десятилетие жизни тяжелыми гипогликемическими эпизодами или дисфагией, возникающей вследствие ахалазии и сниженной секреции слюны. Тем не менее, до подросткового или даже взрослого возраста редко обнаруживают сочетание резистентности к АКТГ и ахалазии. У многих пациентов отмечается прогрессирование неврологических симптомов, в частности, сенсомоторной дегенерации, невропатии зрительного нерва, нарушений со стороны мозжечка и парасимпатической ВНС. При исследовании вегетативных функций глаза можно обнаружить алакримию, сухой кератоконъюнктивит, атрофию слезной железы, нарушения зрачковых реакций и аккомодации. Вегетативная дисфункция проявляется также в ортостатической гипотензии с сохранением компенсаторной тахикардии, снижением потоотделения и секреции слюны.
Синдром циклической рвоты (СЦР) характеризуется тяжелыми периодическими эпизодами тошноты, рвоты и вялости с полным выздоровлением между приступами [5]. Это расстройство отмечается у 1,9% детей школьного возраста и в дальнейшем часто трансформируется в мигрень [18]. Приступы часто провоцируются эмоциональным и физическим стрессом, сопровождаются многими вегетативными симптомами, включая повышенное слюно- и потоотделение, бледность, повышение АД, диарею и головокружение. Часто рвоте предшествует продромальный период, проявляющийся головной болью, фотофобией или головокружением. При исследовании вегетативной регуляции выявлены нарушения, характерные для активации симпатической нервной системы, в частности вариабельность сердечного ритма и постуральная непереносимость. Несмотря на то, что СЦР часто рассматривается как вариант мигрени, в ее основе лежит вегетативная дисфункция. Причины СЦР до конца не выяснены, но показана роль генетических факторов: СЦР у некоторых детей наследовался по материнской линии и ассоциировался с изменениями митохондриальной ДНК [19].
При ряде заболеваний, обусловленных мутациями митохондриальной ДНК (например, синдроме MELAS), отмечаются мигренеподобные головные боли, что может указывать на участие нарушений функций митохондрий в патогенезе мигрени.
По клиническим особенностям выделяют мигрень без ауры (75% случаев) и мигрень с аурой. Мигрень с аурой ранее носила название «ассоциированной мигрени», клиническая картина приступа сопровождается комплексом преходящих локальных неврологических нарушений (аурой), продолжительность которых не превышает 60 мин. Головная боль при приступе мигрени у детей может носить как пульсирующий, так и давящий характер, ее локализация чаще двусторонняя или в области лба с возможным усилением в одной половине головы, интенсивность варьирует от умеренной до нестерпимой. Чувствительность к внешним раздражителям выражена меньше, чем у взрослых. Приступ сопровождается выраженными вегетативными симптомами: на стороне боли могут отмечаться инъецированность сосудов конъюнктивы, слезотечение, отечность периорбитальных тканей и височной области, иногда сужаются глазная щель и зрачок, отмечаются тошнота и рвота, иногда многократная, бледность или гиперемия кожных покровов, учащение сердцебиения, затруднения дыхания, гипергидроз, нестабильность температуры тела; возможны озноб, головокружение. Мигренозному приступу может предшествовать продромальная фаза. За несколько часов до головной боли отмечается смена настроения в сторону эйфории или подавленности, возможно появление раздражительности и беспокойства или апатии, чувства усталости, сонливости, возникают изменение аппетита, тошнота, иногда пастозность тканей. Постприступная фаза продолжается несколько часов или суток; отмечаются астения, сонливость, затем самочувствие постепенно нормализуется. В межприступном периоде у детей с мигренью не имеется отчетливых нарушений со стороны нервной системы, в том числе ВНС.
Ранее были приняты такие обозначения ГБН, как «головная боль мышечного напряжения», «психомиогенная головная боль», «стрессорная головная боль», «простая головная боль», что отражает представления о патогенетических механизмах ГБН. ГБН провоцируются хроническими психоэмоциональными перегрузками, стрессами, конфликтными ситуациями [20]. Эти ситуации приводят к тоническому напряжению перикраниальных мышц (лобных, височных, затылочных) как универсальной реакции защиты на действие хронического стресса. Следует отметить предрасполагающие к развитию ГБН особенности личности: эмоциональные нарушения (повышенная возбудимость, тревожность, склонность к депрессии), демонстративные реакции, ипохондрическая фиксация на болевых ощущениях, пассивность и снижение стремления к преодолению трудностей. Патогенетической особенностью служит незрелость механизмов психологической защиты ребенка, что приводит к появлению ГБН при воздействии даже незначительных, с точки зрения взрослых, стрессовых факторов.
В межприступном периоде, в отличие от мигрени, большинство больных предъявляет жалобы на боли и чувство дискомфорта в других органах (боли в ногах, кардиалгии, затруднения дыхания, дискомфорт в животе), характеризующиеся непостоянством и достаточно неопределенным характером, однако при обследовании патологических изменений не определяется. Для больных ГБН характерны нарушения сна: трудности засыпания, поверхностный сон с множеством сновидений, частыми пробуждениями, снижается общая длительность сна, наблюдается раннее окончательное пробуждение, отсутствие ощущения бодрости после ночного сна и дневная сонливость.
При исследовании состояния церебральной гемодинамики с помощью ультразвуковой допплерографии проявления ангиодистонии в виде усиления ангиоспастических реакций определялись только у 30% детей с ГБН. У 55% больных отмечалось снижение сосудистого тонуса, что свидетельствует о преобладании парасимпатикотонии [21].
а) дискретный эпизод интенсивного страха или дискомфорта;
б) внезапное начало;
в) ПА достигает максимума в течение нескольких минут и длится не менее нескольких минут;
Клинические картина ПА развивается внезапно с нарастанием интенсивности за короткое время (до 10-15 мин). Далее следует постприступный период, который характеризуется состоянием усталости и слабости. Чаще всего ПА возникают в состоянии бодрствования, редко при засыпании или при ночных пробуждениях. Частота приступа варьирует от ежедневных до одного в несколько месяцев. В среднем, частота приступов варьирует от двух до четырех за неделю или реже.
ПА могут быть связаны с представляющимися пациенту опасными ситуациями и местами (транспорт, общественное место, лифт), хотя объективной угрозы не существует. Из-за сильной тревоги пациент начинает избегать эти места или ситуации. Такое тревожно-фобическое расстройство называется агорафобия. Паническое расстройство сочетается с агорафобией в 30-50% случаев [22].
Терапия СВД достаточно сложна и требует индивидуального подхода. Положительных результатов можно добиться только при хорошем взаимопонимании и взаимодействии между врачом, пациентом и его родителями. Ошибочным является мнение о том, что СВД является состоянием, отражающим особенности растущего организма, которое со временем самостоятельно проходит. Лечение должно быть своевременным, комплексным и достаточно длительным. Для обеспечения его патогенетической направленности учитывают направленность вегетативных реакций (симпатикотоническая, ваготоническая, смешанная).
Лечение СВД начинают с общих мероприятий, направленных на нормализацию показателей вегетативного статуса. Широко используются немедикаментозные методы: коррекция режима дня и питания, лечебная физкультура, закаливающие и физиотерапевтические процедуры.
Важно соблюдать режим дня, чередовать умственные и физические нагрузки. Продолжительность сна должна быть достаточной и соответствовать возрастным потребностям (от 8 до 10 ч). Хроническое недосыпание служит причиной нарушений в работе нервной и эндокринной систем или может усугублять симптомы СВД.
Необходимо поддерживать нормальный психологический климат в семье ребенка, устранять конфликтные ситуации и нервно-психические перегрузки в семье и школе. Во избежание переутомления в ходе спокойного обсуждения с ребенком регламентируется время просмотра телепередач, игр и работы за компьютером.
Большое значение имеет правильное питание. При его коррекции следует увеличить поступление в организм солей калия и магния. Эти вещества участвуют в проведении нервных импульсов, улучшают работу сосудов и сердца, способствуют восстановлению нарушенного баланса между отделами ВНС. Калий и магний содержатся в гречневой, овсяной кашах, сое, фасоли, горохе, абрикосах, шиповнике, кураге, изюме, моркови, баклажанах, луке, салате, петрушке, орехах.
Частой ошибкой является освобождение детей с СВД от занятий физкультурой. Гиподинамия приводит к ухудшению состояния. Оптимальными при СВД являются плавание, ходьба, катание на лыжах, пешие прогулки, подвижные игры на свежем воздухе. Водные процедуры оказывают общеукрепляющее воздействие на организм, поэтому при всех типах вегетативной деятельности могут быть рекомендованы контрастные ванны, веерный и циркулярный души, гидромассаж, плавание. Во время и после занятий и процедур пациенты не должны испытывать неприятных ощущений, чрезмерной усталости, раздражительности.
Из средств фитотерапии при расстройствах по парасимпатикотоническому типу применяются растительные стимуляторы: элеутерококк, женьшень, заманиха, аралия, левзея, различные мочегонные травы и сборы (толокнянка, можжевельник, брусника). При расстройствах по симпатикотоническому и смешанному типам назначают седативные травы и сборы: валериана, пустырник, шалфей, мята, мелисса, хмель, корень пиона.
Эффективностью в терапии СВД обладают комбинированные препараты, содержащие магний и витамин B6 (пиридоксин). Пиридоксин участвует в обмене белков, углеводов, жирных кислот, синтезе нейромедиаторов и многих ферментов, оказывает нейро-, кардио-, гепатотропное, а также гемопоэтическое влияние, способствует пополнению энергетических ресурсов. Высокая активность комбинированного препарата обусловлена синергизмом действия компонентов: пиридоксин увеличивает концентрацию магния в плазме и эритроцитах и снижает количество магния, выводимого из организма, улучшает всасывание магния в ЖКТ, его проникновение в клетки, а также фиксацию. Магний, в свою очередь, активизирует процесс трансформации пиридоксина в его активный метаболит пиридоксаль-5-фосфат в печени. Магний и пиридоксин потенцируют действие друг друга, что позволяет успешно использовать их комбинацию для нормализации магниевого баланса и профилактики недостатка магния.
Препараты магния способствуют выраженному снижению возбудимости нервной ткани и, как следствие, улучшению регуляции функций внутренних органов. Поэтому препараты магния широко используются в качестве лекарственного средства при различных заболеваниях, и прежде всего при патологии ССС. Н.А. Коровина и соавт. [25] исследовали эффективность терапии препаратами магния в течение 3 недель у35 детей и подростков с сердечно-сосудистыми заболеваниями. После курса лечения отмечалось достоверное снижение частоты клинических проявлений нейровегетативных нарушений у большинства обследованных больных. При этом наиболее существенной была динамика таких симптомов, как кардиалгии, тахикардия, повышение АД, головные боли, головокружения, слабость, утомляемость, тревожность и раздражительность, нарушение качества сна. Применение терапии магнием сопровождалось отчетливым гипотензивным эффектом при повышении АД, обусловленном преобладающими симпатикотоническими влияниями у детей с вегетативной дисфункцией, вплоть до полной нормализации АД в 62,5% случаев. Эти данные согласуются с представлениями о депрессорном влиянии магния на активность и выделение катехоламинов, частичной блокаде рецепторов, чувствительных к адреналину, и возможном влиянии магния на центральные механизмы регуляции АД. Положительная динамика ЭКГ подтвердила кардиотрофический, антиаритмический, вегетотропный эффекты терапии магнием. Положительное терапевтическое действие Магне В6 подтверждено при лечении СВД у взрослых пациентов [26].
Учитывая полисистемность клинических проявлений СВД у детей и подростков, следует подчеркнуть необходимость активного участия и согласованных усилий врачей различных специальностей и других специалистов в обследовании и лечении этих пациентов, преемственность предписываемых рекомендаций и терапевтических назначений, а также достаточную длительность лечения с обязательным динамическим контролем за состоянием детей и подростков.
