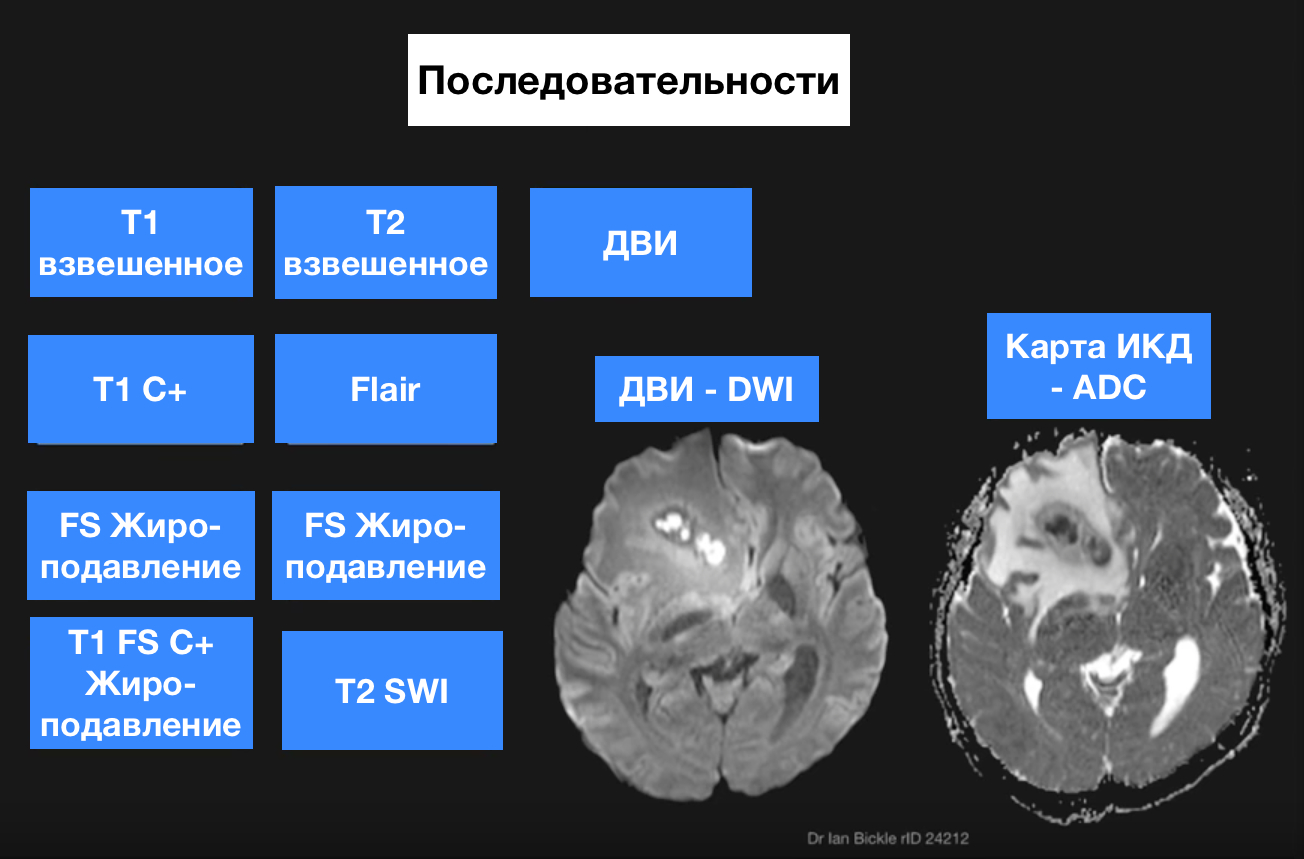
МРТ-последовательность — DWI и ADC
В создании ДВИ участвуют молекулы, чувствительные к диффузионному измерению. Благодаря этому может быть измерено движение молекул за определенный период времени — b. Использование сильных градиентных импульсов позволяет маркировать каждую молекулу воды в системе и ее положение по отношению к используемому градиенту.
Существенную роль в получении ДВИ играет принцип диффузионной контрастности, в основе которого диффузия молекул воды вдоль градиента поля уменьшает МР-сигнал.
Эта зависимость является экспоненциальной: сигнал = Sо exp (–bD), где D — коэффициент диффузии ткани (здоровая ткань около 10 мм2/с); b — коэффициент диффузионного взвешивания (b-значение, с/мм2).
Чем больше b-значение, тем сильнее диффузионное взвешивание. Область сниженной диффузии показывает отно- сительную гиперинтенсивность сигнала. В клиническом применении интересны области, в которых диффузия уменьшена по отношению к окружающей области, например, в клеточных мембранах. Благодаря сниженной диффузии уменьшение сигнала здесь несколько меньше и соответствующие зоны на изображении представлены более светлыми. Интенсивность сигнала на изображениях зависит от направления диффузион- ного взвешивания. Создаются три проекции одного и того же сечения (при b-значениях > 0). Подобное диффузионное обследование помогает отличить изотропную патологию от анизотропной структуры окружающей ткани.
Создаются следующие типы изобра- жений: ортогональные изображения, ИКД-карты (ADC — Apparent Diffusion Coefficient), следящие изображения (контрастность показывает средний ко- эффициент диффузии во всех направлениях), сравнительные Т2-ВИ в том же положении сечения (b = 0).
Все рассчитанные изображения соз- даются непосредственно после измере- ния. Для каждого положения сечения и b-значения (не равного 0) получают изображения в направлениях диффузионного взвешивания (в направлениях выбора сечений, считывания и фазового кодирования).
Все ДВИ обозначены интенсивно- стью и направлением диффузионного взвешивания. Интенсивность сигнала в ДВИ зависит не только от скорости диффузии, но и от значений времени релаксации Т1-, Т2-ВИ и протонной плотности. Относительный вклад этих факторов зависит от параметров после- довательности (ТE, TR, времени диффузии, напряженности диффузионно- го градиента и т. п.). В связи с этим с целью отделения влияния диффузии от других параметров рассчитываются карты кажущегося коэффициента диффузии.
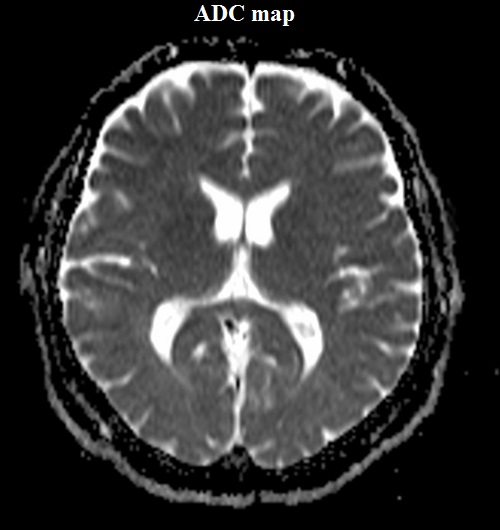
На ИКД-изображениях, а чаще на- зываемых также ADC-картах, значение серого характеризует (с помощью пикселов) распределение коэффициентов диффузии в обследуемой зоне. Чем меньше степень выраженности диффузии, тем темнее пикселы.
Определяемый ИКД зависит от процессов диффузии в имеющихся раз- личных структурах, внутриклеточных и межуточных пространствах. ИКД- изображения не содержат ни Т1-, ни Т2- составляющих, и считается, что таким образом это исключает наличие артефактов.
ДВИ получают после подачи сильных биполярных импульсов на фоне последовательности спин-эха или градиент- эха с различными параметрами, которые представляют собой фактор b, измеряемый в с/мм2, и силу градиентов диффузии. А новые МР-томографы с более мощными и быстрыми градиентными подсистемами и новыми катушками способствуют повышению соотношения сигнал/шум на получаемых изображениях при использовании значений b в диапазоне от 500 до 1000 с/мм2, что значительно повышает качество изображения.
Клиническое применение:
Источник:
Диффузные и очаговые изменения – что это?
Диффузные и очаговые изменения – что это, в чем разница
В заключении ультразвукового исследования при выявлении патологии врач может указывать наличие очаговых или диффузных изменений. Это диагностические критерии, описывающие степень поражения органа при разных заболеваниях.
При УЗИ врач должен определить, в каком состоянии находится орган. Внимательно его осматривая, специалист делает вывод – патология или норма. Если орган нормальный, то он просто описывается, на чем все заканчивается.
Если же при исследовании видно отклонение, то определяется степень поражения органа. Врач должен ответить на вопрос, какие имеются изменения – очаговые или диффузные.
Диффузные и очаговые изменения – в чем разница
Следует уточнить, что деление на очаговые и диффузные изменения условное. Оно помогает в работе специалистов для лучшего понимания картины заболевания.
Диффузные – это поражение всего органа. Какую бы часть не исследовал врач, он видит патологические изменения. Орган полностью отличается от здорового. Нельзя выделить, какой участок нормальный.
Очаговые изменения – это патологический процесс, затрагивающий часть органа. Имеются участки, что отличаются от здоровых. При этом все остальные части выглядят нормальными.
Примеры диффузных и очаговых изменений
При запущенном гепатите, воспалительном заболевании печени, поражается весь орган. Врач будет видеть диффузные изменения. Когда патология еще на ранней стадии, будут определяться и здоровые участки, то есть изменения очаговые.
При злокачественной опухоли печени на начальной стадии врач видит очаговые изменения. Когда рак поражает весь орган, определить здоровые его границы уже невозможно – это диффузная патология.
Связь изменений с заболеванием
То, какие изменения произошли, имеет большое значение. Диффузное поражение – это всегда признак тяжелой патологии, которая уже успела поразить весь орган. При этом наличие очаговых изменений не говорит о том, что заболевание еще на начальной стадии. Это зависит от болезни.
Ультразвуковое исследование не может показать конкретного заболевания. Врач может видеть только анатомические изменения. Одинаковые диффузные и очаговые процессы могут наблюдаться при совершенно разных отклонениях. Обычно после УЗИ при выявлении участка поражения назначаются другие, более точные варианты исследования.
Методика диффузионно-взвешенных магнитно-резонансных изображений у онкологических больных
1) Дорожная клиническая больница на ст. Новосибирск-главный ОАО «РЖД», Новосибирск, Россия
2) Военно-медицинская академия им. С.М. Кирова, Санкт-Петербург, Россия
3) Городская больница №40, Сестрорецк, Россия
Цель исследования: оценить возможности диффузионно-взвешенной магнитно-резонансной томографии всего тела у больных онокологического профиля.
Материалы и методы. На базе наших учреждений в период с сентября 2012 г. по март 2013 г. была разработана и опробована методика комплексной ДВ-МРТ всего тела у 120 онкологических пациентов. Исследование проводили на МР-системах с напряженностью магнитного поля 1,5Т (Magnetom Espree, Siemens); зона сканирования включала область от свода черепа до середины бедра.
Результаты. В обозначенный период было обследовано 120 пациентов, из которых у 117 имели место верифицированные первичные злокачественных опухоли вариабельной локализации как вне лечения (n=39), так и на фоне проводимого лечения (n=68). Большую часть пациентов составили больные с раком молочной железы (28%), колоректальным раком (27%) и раком желудка (15%). Для корреляции использовали результаты других методов исследования (сцинтиграфия, ПЭТ, КТ и/или МРТ отдельных зон с использованием стандартных протоколов), оперативного вмешательства, пункционной биопсии. Не все выявленные в ходе исследования очаги могут с уверенностью расцениваться как метастазы, поскольку не все очаги были морфологически верифицированы. В данной работе мы ставили перед собой цель сопоставить возможности традиционных на сегодняшний день методов визуализации (КТ, МРТ, сцинтиграфия, ПЭТ) и ДВ-МРТ в выявлении потенциальных метастатических изменений у онкологических пациентов. В результате ДВ-МРТ всего тела в сумме был выявлен 371 очаг, подозрительный на неоплазию, из них 206 (55,5%) составляли метастазы, о наличии которых было известно до исследования, 92 очага (25%) были выявлены впервые по результатам данного исследования и интерпретированы как метастатические. 73 очага (19,5%) интерпретированные как доброкачественные. К ложноположительным результатам относились очаговые изменения в легких (n=4, не обнаружены при КТ грудной клетки), к ложноотрицательным − остеосклеротические метастазы (n=1, обнаружены при ПЭТ-КТ) и метастаз в легком (n=1, обнаружен при КТ).
Выводы. В 27% наблюдений исследование ДВ-МРТ всего тела повлекло за собой смену тактики лечения пациента (отказ от хирургического в пользу химиотерапии, изменение объема планируемого оперативного вмешательства и др.). Первичный опыт применения диффузионно-взвешенной магнитно-резонансной томографии свидетельствует о том, что возможности ДВ-МРТ всего тела в выявлении очагов, подозрительных на метастатические, сопоставимы с традиционными методами визуализации (сцинтиграфия, ПЭТ, КТ, МРТ).
Ключевые слова: магнитно-резонансная диффузия всего тела, диффузионно-взвешенные изображения, магнитно-резонансная томография, метастазы, онкология.
В группе пациентов с опухолями, характеризующимися высоким риском метастазирования (рак молочной железы, предстательной железы, колоректальный рак и др.), скрининговые исследования всего тела являются необходимым этапом отбора для проведения оперативного лечения, а также одним из факторов, определяющих его тактику [1].
На сегодняшний день основным методом скрининга отдаленных и регионарных метастазов является позитронно-эмиссионная томография (ПЭТ) с 18-F-дезоксиглюкозой (FDG), однако ввиду низкой доступности данного исследования в нашей стране чаще для этой цели используют компьютерную томографию (КТ) грудной клетки, живота и таза [2].
Помимо аспекта доступности ПЭТ характеризуется такими ограничениями, как низкое анатомическое разрешение (что частично преодолено в совмещенных ПЭТ/КТ и ПЭТ/МРТ сканерах) и интенсивное накопление метаболита не только в опухолевой ткани, но также в зонах воспаления и грануляционной ткани, что служит источником ложно-положительных результатов [3]. Среди ограничений КТ в качестве метода М-стадирования злокачественных опухолей необходимо отметить низкую чувствительность к костным метастазам, относительно низкие показатели в дифференциальной диагностике изменений тазовых органов и мелких образований печени [3].
Альтернативой перечисленным методам исследования является магнитно-резонансная томография (МРТ) всего тела с включением в протокол исследования магнитно-резонансной-диффузии (МР-диффузии). Важными преимуществами диффузионно-взвешенных изображений (ДВИ) всего тела является отсутствие ионизирующего излучения и необходимости применения радиоизотопов. Исследование не занимает много времени (30-50 минут в зависимости от используемого протокола) и является относительно простым в техническом исполнении, что позволяет легко применять его в рутинной практике.
При интерпретации ДВИ необходимо помнить, что за счет особенностей гистологического строения, связанных с высокой клеточной плотностью, ряд органов и тканей характеризуется в норме гиперинтенсивным сигналом на изображениях с высоким фактором взвешенности (головной и спинной мозг, надпочечники, лимфоидная ткань − лимфатические узлы, миндалины, селезенка) [4,5].
ДВИ, как и ПЭТ, характеризуется достаточно низким анатомическим разрешением. Компенсировать это позволяет использование Т2-взвешеных изображений или STIR последовательностей. Комбинированный анализ ДВИ и Т2(STIR) дает возможность не только оптимизировать локализацию выявляемых очагов, но также избежать ошибок интерпретации и повысить специфичность исследования, что наглядно продемонстрировано в ряде исследований [4,5].
Первые публикации о применении ДВИ тела в онкологии относятся к 2004 г. С тех пор данная методика находит все новые точки приложения и показывает свою эффективность даже в прямом сопоставлении с ПЭТ и ПЭТ/КТ. На данный момент имеется достаточное количество публикаций, не только доказывающих эффективность ДВ-МРТ тела, но и впрямую сопоставляющих ДВ-МР тела и ПЭТ. Так, Yoshiharu Ohno и соавт. (2008) в своей работе показали, что точность МР-диффузии всего тела в сочетании с МРТ всего тела в выявлении метастазов сопоставима с показателями ПЭТ (87,7% против 88,2%), чувствительность МР-диффузии всего тела даже выше, чем показатели ПЭТ (70,0% и 62,5%), а по специфичности методика приближается к ПЭТ (92,0% против 94,5%) [6].
Материалы и методы
В обозначенный период было выполнено исследование 120 пациентов (возраст от 38 до 84 лет), которых условно можно разделить на 3 группы:
Распределение пациентов в зависимости от локализации первичного опухолевого процесса представлено на рисунке 1. В первой группе у 21 из 39 человек были выявлены отдаленные метастазы и/или нерегионарная лимфаденопатия, о наличии которых не было известно до выполнения исследования, что в ряде наблюдений послужило причиной отмены запланированного хирургического лечения.
Рис. 1. Распределение пациентов в зависимости от локализации первичной опухоли.
Во второй группе у 27 из 68 человек был выявлен рецидив или прогрессирование заболевания, в том числе появление новых очагов метастазирования в ранее непораженном органе (печень, тазовая и абдоминальная брюшина, кости, головной мозг и др.). У 9 из 68 пациентов был пересмотрен характер изменений, ранее трактовавшихся как метастатические. В результате исследования были выявлены простые кисты, очаги фокальной нодулярной гиперплазии или гемангиомы печени, абсцессы вариабельной локализации и др.
В третьей группе у 4 пациентов были выявлены злокачественные опухоли, в том числе с отдаленными метастазами, у 3 причиной лимфаденопатии послужили воспалительные изменения (тазовые и абдоминальные абсцессы и др.), у 5 предполагаемые метастазы были трактованы как доброкачественные изменения с последующим подтверждением альтернативными методами исследования (КТ, МРТ с использованием традиционного протокола). У одного больного был заподозрен лимфопролиферативный процесс, и пациент в настоящее время проходит обследование в гематологическом стационаре.
В результате исследования в сумме был выявлен 371 очаг, подозрительный на неоплазию, из них 206 (55,5%) составляли метастазы, о наличии которых было известно до исследования, 92 очага (25%) были выявлены впервые по результатам МР-диффузии всего тела и интерпретированы как метастатические, в 73 очагах (19,5%) – злокачественность процесса была снята (рис. 2). В 27% наблюдений ДВИ тела повлекло за собой смену тактики ведения пациента (отказ от хирургического лечения в пользу химиотерапии, изменение объема планируемого вмешательства и др.).
Рис. 2. МР-томограммы пациентки с аденокарциномой толстой кишки и метастазами в позвонках грудного и поясничного отделов позвоночника (стрелки) с распространением в эпидуральное пространство. MIP реформат ДВИ тела во фронтальной плоскости (а); ДВИ в аксиальной плоскости (b-фактор 900 с/мм 2 ) (б, в); STIR в аксиальной (г) и сагиттальной (д) плоскостях.
Отдельного внимания требует высокая чувствительность данной методики к выявлению метастатического поражения костей даже на фоне реконверсии костного мозга, в том числе на этапе до деструкции костных трабекул, что определяет преимущество ДВИ перед КТ (рис. 3).
Рис. 3. МР-томограммы пациентки с раком левой молочной железы. Состояние после хирургического лечения и химиотерапии: рецидив в рубце, метастазы в аксиллярных лимфатических узлах и печени (стрелки). MIP реформат ДВИ тела во фронтальной плоскости (а, б); ДВИ в аксиальной плоскости (b-фактор 900 с/мм 2 ) (в, г, д).
Одним из потенциальных приложений МР-диффузии всего тела представляется скрининг вторичного поражения костей при опухолях с высоким риском такого метастазирования (рак молочной и предстательной железы), а также оценка эффективности проводимой терапии при метастазах в костях.
Основным источником как ложно-положительных, так и ложно-отрицательных результатов в исследованной нами группе пациентов являлись небольшие очаги в легочной паренхиме, в особенности прикорневой локализации, так как данная область является сложной для МР-визуализации по причине пульсационных артефактов от крупных сосудов, и выявляемые изменения требуют дополнительного проведения КТ.
Опыт применения ДВ-МРТ всего тела на базе наших учреждений показал, что данная методика высокоинформативна в выявлении новообразований и их дифференциальной диагностике; у каждого четвертого пациента (27%), прошедшего исследование, полученные результаты оказали существенное влияние на тактику лечения.
Несмотря на большое количество исследований, посвященных ДВИ всего тела, в доступной литературе пока нет единой точки зрения относительно места данной методики в алгоритме обследования онкологических пациентов. На основании первичного опыта внедрения данной методики в рутинную практику нам представляется обоснованным ее использование для М-стадирования опухолей с высоким риском метастазирования вне возможности применения ПЭТ, в особенности при опухолях с высоким риском вторичного поражения костей. Отдельное место данная методика может найти в исследовании онкологических пациентов, у которых необходимо избежать лучевой нагрузки (в том числе у детей), а также у пациентов с противопоказаниями к введению йод-содержащих контрастных препаратов (непереносимость йода, почечная недостаточность и др.).
Согласен Данный веб-сайт содержит информацию для специалистов в области медицины. В соответствии с действующим законодательством доступ к такой информации может быть предоставлен только медицинским и фармацевтическим работникам. Нажимая «Согласен», вы подтверждаете, что являетесь медицинским или фармацевтическим работником и берете на себя ответственность за последствия, вызванные возможным нарушением указанного ограничения. Информация на данном сайте не должна использоваться пациентами для самостоятельной диагностики и лечения и не может быть заменой очной консультации врача.
Сайт использует файлы cookies для более комфортной работы пользователя. Продолжая просмотр страниц сайта, вы соглашаетесь с использованием файлов cookies, а также с обработкой ваших персональных данных в соответствии с Политикой конфиденциальности.
МРТ-диффузия
Некоторые пациенты заинтересованы в комплексном обследовании организма. Существуют разные способы диагностики, включая сканирование в режиме МРТ-диффузия, всего тела. В чем суть процедуры, можно узнать из нашей статьи.
МРТ в режиме диффузии, что это?
Пациенты нередко путают данный режим со спектральной магнитно-резонансной томографией. В чем разница между процедурами? В живых клетках и пространстве между ними содержится много воды. Молекулы постоянно перемещаются. Проникают сквозь мембрану в клетку и обратно. Процесс перехода называют диффузией. Нормальный обмен молекулами воды отличается от патологического: при развитии заболеваний порядок нарушается. Клетки отдают воду медленнее, чем получают, в результате набухают и деформируются. Бывает обратная ситуация. Из клетки уходит больше молекул воды, чем поступает. Магнитно-резонансная томография в последовательности DWI фиксирует показатели диффузии в тканях, рентгенолог сравнивает полученные данные с нормой и делает заключение о наличии или отсутствии нарушений.
Области применения технологии:
Спектральная МРТ определяет биохимические изменения, вызываемые различными патологическими состояниями. Как и DWI, диагностика неинвазивна. Исследование позволяет оценить резонансную частоту протонов, входящих во всевозможные химические соединения внутренних органов и биологических жидкостей.
Что показывает МРТ-диффузия всего тела?
Магнитная томография с использованием данного режима подходит для сканирования отдельных областей (головного мозга, брюшной полости и т.д.) и целого организма. Так называемое “диффузное МРТ” помогает в обнаружении:
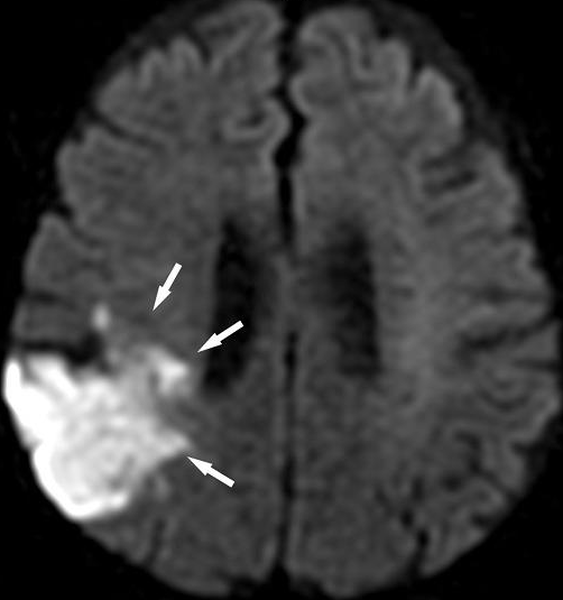
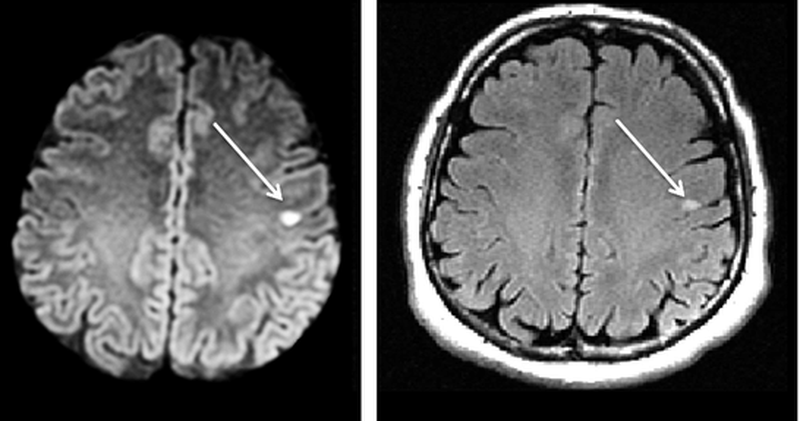
Дополнительное исследование головного мозга позволит провести дифференциацию инсульта и рассеянного склероза или очагов онкологии. По снимкам можно определить давность острого нарушения кровообращения.
Показания и противопоказания к “диффузному МРТ”
Процедуру назначают для уточнения диагноза при:
У онкологических больных диффузионную томографию применяют на всех этапах лечения:
Противопоказания к использованию данного вида магнитно-резонансной диагностики те же, что и для обычной. Процедуру нельзя проводить при наличии у пациента:
Диффузионную МРТ всего тела не делают беременным женщинам в первом триместре. Сложности с диагностикой на аппарате закрытого типа могут возникнуть при избыточной массе тела человека. Тоннельные томографы рассчитаны на вес не более 120 кг. В ситуациях превышения данного параметра и при клаустрофобии подбирают альтернативные виды исследования.
Как проходит МРТ-диффузия?
Перед процедурой человеку необходимо избавиться от предметов, содержащих металл: украшений, зубного протеза, съемного слухового аппарата, очков и т.д. Электронные устройства и другие личные вещи оставляют в раздевалке. Если у пациента есть эндопротез, надо принести в клинику документ с информацией о материале изделия.
МРТ-диффузия отдельной области или всего тела проходит следующим образом:
Исследование всего тела всегда выполняют не только в диффузионно-взвешенном режиме. Для максимальной информативности изображений рекомендуют сделать фото в идентичной плоскости в последовательностях STIR или Т2 ВИ с подавлением жира.
Расшифровка снимков МРТ-диффузии
По завершении интерпретации томографических снимков рентгенолог отдает заключение и диск с фотографиями пациенту. Результаты предоставляют доктору, который выписал направление на диффузную МРТ. Если пациент обратился в диагностическую клинику самостоятельно, проводивший сканирование специалист пояснит алгоритм дальнейших действий. При сомнениях в точности расшифровки больной может попросить рассмотреть “диффузные снимки МРТ” другого врача-рентгенолога, это снизит вероятность ошибки.
Многие пациенты пытаются самостоятельно расшифровать изображения магнитно-резонансной томографии. Это сложная задача: для интерпретации фото необходимо не только знать структуры зоны интереса, но и пространственное соотношение анатомических областей. Человек без профильного образования не сумеет рассмотреть все детали и правильно истолковать результаты исследования.
Лечащий врач “прочитает” снимки, ознакомится с заключением рентгенолога, сопоставит данные магнитно-резонансной томографии с другой информацией (анамнезом, лабораторными анализами, итогами прочих методов инструментальной диагностики), определит заболевание и подберет способ терапии.



МР-диффузия
МР-диффузия: инструкция по применению.
Диффузия – это процесс взаимного проникновения молекул или атомов одного вещества между молекулами или атомами другого вещества, и данный процесс приводит к самопроизвольному выравниванию концентрации веществ по всему занимаемому объему.
Получить данные МР-диффузии возможно на базе различных импульсных последовательностей:
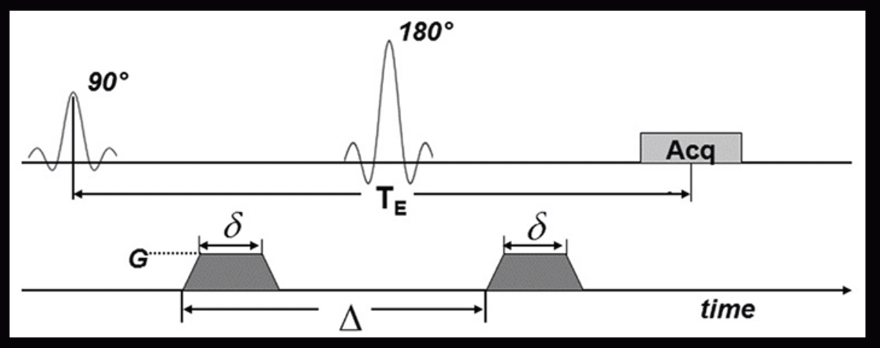
Single shot EPI
На графике заметно, что у данной импульсной последовательности 90 градусный импульс и 180 градусный импульс. У Single shot EPI TR=8000 мс, а TE=60 мс, то есть DWI изображение построено с Т2 контрастностью.
Отличие от Т2 изображений:
В нижней части графика видно, что при получении изображения накладываются два градиента. Данные градиенты и его показатели кодируют b-фактор, который в свою очередь определяет контраст диффузно-взвешенного изображения и зависит от таких показателей, как длительность градиентов, расстояние между данными градиентами и амплитудой данных градиентов.
Чем длиннее градиент, чем дольше они накладываются, чем больше амплитуда градиентов, чем больше расстояние между ними, тем больше b-фактор.
Контрастность ДВИ помимо Т2-эффекта определяется b-фактором.
Высокое значение b-фактора прямо пропорционально времени сбора данных.
Подавление сигнала от жировой ткани.
Для элиминации артефактов химического сдвига ДВИ всегда требует подавления сигнала от жировой ткани.
Если использовать ДВИ изображения с нулевым b-фактором, то есть не накладывать никаких градиентов, то в данном случае получится изображение с контрастностью, как у Т2 FS изображений.
По мере увеличения b-фактора от 0 до 700 увеличивается эффект диффузии. Интенсивность сигнала от органов с ограниченной диффузией на изображениях с низким b фактором будет низкая, а на изображениях b=600 сигнал от того же органа будет повышаться. Чем выше b-фактор, тем выше контраст изображения обусловлен диффузионным эффектом.
Слева представлены ДВИ с b=0, 100, 200, 500, 1000, 2000
Градиент, который идет первый до 180 градусного импульса помечает спины, а второй градиент после 180 градусного считывает.
Изображение с b=0 является аналогом Т2 изображения с подавлением жировой ткани.
Изображения с b=100. Вода не успевает покинуть пределы вокселя за данный период времени.
Изображения с b=500. Молекулы воды частично покинули воксель. В областях с ограниченной диффузией данное явление менее выраженное и протекает медленнее.
Изображения с b=1000.В зонах со свободной диффузией в вокселе не остается практически молекул воды, а в вокселе с ограниченной диффузией только часть молекул воды покинет.