Кишечная лимфангиэктазия — это врожденное или приобретенное расширение лимфатических сосудов тонкой кишки, вызванное их мальформацией или обструкцией. Проявляется отечностью, диареей, стеатореей, тошнотой, признаками нутритивной недостаточности, хилотораксом, хилезным асцитом. Диагностируется с помощью копрограммы, общего и биохимического анализов крови, контрастной рентгенографии, эндоскопии и биопсии тонкой кишки, радиосцинтиграфии. При лечении используют аналоги соматостатина, блокаторы опиатных рецепторов, выполняют резекцию пораженных лимфатических сосудов, кишечника, лимфовенозное шунтирование, торакоцентез, лапароцентез.
МКБ-10
Общие сведения
Кишечная лимфангиэктазия (кишечная лимфангиэктатическая болезнь, экссудативная гипопротеинемическая энтеропатия) — гетерогенная группа редких гастроэнтерологических заболеваний, выявляемых преимущественно у детей и молодых пациентов. Идиопатическая форма расстройства была впервые описана в 1959-1961 годах Р. Гордоном и Т.А. Вальдманом. Первичная лимфангиэктазия одинаково часто выявляется у девочек и мальчиков, вторичная чаще диагностируется у мужчин. Актуальность своевременной диагностики патологии обусловлена высокой вероятностью задержки развития в детском возрасте и тяжелыми метаболическими нарушениями у взрослых, выраженность которых может быть уменьшена при назначении симптоматического лечения и коррекции рациона.
Причины
Гипопротеинемическая экссудативная энтеропатия является полиэтиологическим патологическим состоянием, обусловленным аномалией строения лимфатических сосудов или нарушением оттока лимфы от кишечника. Специалистами в области клинической гастроэнтерологии, ангиологии и лимфологии определены следующие основные причины возникновения кишечной лимфангиэктатической болезни:
Блокада мезентериальных лимфатических сосудов возможна при ретроперитонеальном фиброзе, саркоидозе, констриктивном перикардите, ряде аутоиммунных процессов (системной красной волчанке, склеродермии, дерматомиозите). В этих случаях причинами нарушения лимфооттока являются как непосредственное сжатие лимфатических сосудов из-за разрастания соединительной ткани, так и застой в основных венозных коллекторах, принимающих лимфу из брюшной полости.
Патогенез
Основой патофизиологических нарушений при всех вариантах кишечной лимфангиэктазии служит повышенное давление лимфы, однако при идиопатической и приобретенной формах патологии пусковые моменты нарушений лимфодренажа различны. У больных с врожденным вариантом патологии — болезнью Гордона-Вальдмана — переполнение лимфатического русла обусловлено аномальным строением сосудов. При приобретенной энтеральной лимфангиэктазии застой лимфы вторичен и развивается из-за наличия препятствий на путях ее оттока.
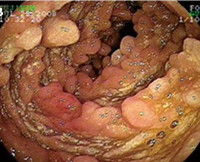
Повышение давления в кишечной лимфатической системе провоцирует эктазию сосудов, набухание слизистой оболочки, сброс лимфы в тонкую кишку. Постоянные потери белка и лимфоцитов сопровождаются возникновением гипопротеинемии, приводящей к образованию отеков, лимфопении. Из-за морфологических изменений слизистой нарушается абсорбция хиломикронов и липопротеинов, вследствие чего ухудшается всасывание жиров, белков, жирорастворимых витаминов, ряда макро- и микроэлементов (кальция, железа, меди).
Классификация
Систематизация клинических форм кишечной лимфангиэктазии основана на критерии первичности-вторичности патологического процесса. Такой подход максимально учитывает особенности развития каждого из вариантов экссудативной энтеропатии, позволяет правильно оценить прогноз заболевания и определиться с врачебной тактикой. Выделяют следующие виды лимфангиэктатической болезни кишечника:
Симптомы кишечной лимфангиэктазии
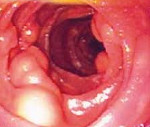
Заболевание характеризуется хроническим течением с постепенным нарастанием симптоматики. Основные признаки первичной лимфангиэктазии — обширные симметричные отеки, сочетающиеся с диспепсическими расстройствами (тошнотой, диареей, светлым зловонным калом с жирным блеском, умеренными болями в животе). При прогрессировании болезни наблюдается ухудшение общего состояния, бледность кожных покровов, потеря массы тела вплоть до истощения, отставание детей в росте и физическом развитии. При вторичной эктазии интестинальных лимфатических сосудов проявления ведущего заболевания усугубляются образованием асимметричных периферических отеков, признаками мальабсорбции. В тяжелых случаях наблюдается выпот в серозные полости — хилоторакс, хилезный асцит.
Осложнения
При первичной кишечной лимфангиэктазии значительно повышается вероятность возникновения лимфопролиферативных заболеваний, что связано с мутациями в генетическом аппарате клеток. Также возможно развитие обратимой слепоты, которая обусловлена отеком макулы сетчатки. В случае длительного течения лимфангиэктазия может приводить к развитию фиброзных сужений тонкой кишки, вызывая симптомы кишечной непроходимости.
Среди других осложнений заболевания выделяют дефекты зубной эмали (вследствие дефицита кальция), воспаление десен, склонность к частым ОРВИ (при снижении иммунной функции лимфоцитов), гипопротеинемические дистрофические изменения в мышцах, внутренних органах. На фоне недостатка жирорастворимых витаминов ухудшается сумеречное зрение, повышаются кровоточивость, сухость кожных покровов, склер, слизистых, развиваются остеопороз, мышечная слабость, снижается фертильность.
Диагностика
Постановка диагноза зачастую затруднена из-за редкой встречаемости заболевания и сходства клинической картины с проявлениями других патологий пищеварительного тракта. Подозревать наличие кишечной лимфангиэктазии необходимо у детей, молодых пациентов с хроническими энтеритами невыясненной этиологии. Наиболее информативными в диагностическом плане являются:
В клиническом анализе крови при лимфангиэктазии выявляется относительная лимфоцитопения, снижение содержания гемоглобина и эритроцитов. Биохимический анализ крови позволяет обнаружить гипопротеинемию (в основном за счет уменьшения количества альбуминов и гамма-глобулинов), снижение концентрации кальция, церулоплазмина, трансферрина, α-1-антитрипсина. Для комплексной оценки состояния ЖКТ может выполняться УЗИ или КТ органов брюшной полости.
Дифференциальная диагностика энтеральной лимфангиэктазии проводится с рецидивирующими энтеритами и энтероколитами, инфекционными заболеваниями (сальмонеллезом, иерсиниозом), целиакией, спру, пахидермопериостозом, кишечной мальабсорбцией, наследственными ферментопатиями. Кроме наблюдения гастроэнтеролога, пациенту рекомендованы консультации ангиолога, лимфолога, инфекциониста, иммунолога, гематолога, онколога, онкогематолога, кардиолога.
Лечение кишечной лимфангиэктазии
Тактика ведения пациента определяется клинической формой гипопротеинемической энтеропатии. Независимо от причин заболевания больному рекомендована диета с низким содержанием жиров (менее 30 г/сут.), обогащенная протеинами, кальцием, жирорастворимыми витаминами. Употребление синтетических жировых эмульсий со среднецепочечными триглицеридами, абсорбируемыми в портальный кровоток, частично обеспечивает организм необходимыми жирами. Коррекция рациона позволяет уменьшить интенсивность диареи и восполнить дефицит основных нутриентов. Общему улучшению лимфотока и уменьшению периферических отеков способствует достаточная двигательная активность, комплексы ЛФК с упражнениями, предполагающими подъем рук выше плеч. Схемы лечения энтеральной лимфангиэктатической болезни включают:
При сочетании лимфангиэктазии кишечника с хилотораксом рекомендовано выполнение торакоцентеза. Наличие значительного выпота при сопутствующем хилезном асците служит показанием для 3-4-недельной замены энтерального питания парентеральным, выполнения лапароцентеза, наружного дренирования брюшной полости, накладывания перитонеовенозных шунтов. В качестве симптоматического средства для коррекции выраженного отечного синдрома обычно используют калийсберегающие диуретики (антагонисты альдостерона).
Прогноз и профилактика
У 64% пациентов с врожденной лимфангиэктазией, которая проявляется в первые 10 лет жизни, положительная динамика не наблюдается, прогноз неблагоприятный. У большинства больных часто отмечаются отставание в росте, выраженная задержка развития. Летальность достигает 13%. Мероприятия по предупреждению развития первичной формы патологии не разработаны. Для предупреждения вторичной кишечной лимфангиэктазии важно проводить своевременную комплексную терапию болезней, которые могут вызывать нарушение лимфооттока от энтеральной стенки и изменения в лимфатических сосудах.
Что такое лимфостаз (лимфедема)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Иванов О. О., флеболога со стажем в 12 лет.
Определение болезни. Причины заболевания
Лимфостаз, или лимфедема — это избыточное накопление богатой белком жидкости в тканях.
Нарушенная функция лимфатических сосудов нарушает дренажную функцию лимфатической системы, которая является так же частью системы кровообращения, как артериальная и венозная. Лимфатические сосуды удаляют избыток жидкости из тканей и переносят ее обратно в кровоток. Кроме того, в лимфатической системе происходит созревание иммунных клеток, и таким образом, она представляет собой один из самых основных защитных систем всего организма. Лимфатические капилляры, расположенные в дерме, представляют собой сплетения, которые сливаются в лимфатические сосуды в подкожной клетчатке, в конечном счете, идут к более глубокой системе и грудному протоку. Лимфедема может быть как первичной, так и вторичной. Независимо от этиологии, клинически данное состояние характеризуется хроническим отеком, локализованной болью, атрофическими изменениями кожи и вторичными инфекциями. [1]
Лимфедема в соответствии с этиологией делится на первичную (наследственную) или вторичную (приобретенную). Первичная лимфедема достаточна редка и является результатом генетических мутаций, которые приводят к недоразвитию лимфатических сосудов и недостаточности лимфатической дренажной функции.
Первичная лимфедема может быть изолированной болезнью или частью комплексного синдрома. Большинство случаев первичной лимфедемы наследуются по аутосомно-доминантному признаку с неполной пенетрацией и переменной экспрессией генов. Почти 30% пациентов с первичной лимфедемой имеют идентифицируемые генетические мутации, часто в сигнальном варианте для эндотелиального фактора роста C. [2] Установлено, что более 20 генов связаны с лимфатическими аномалиями при первичной лимфедеме. Однако существует высокая степень генетической гетерогенности. [3] Первичная лимфедема часто встречается именно в нижних конечностях, и лишь в редких случаях это может появиться на гениталиях или верхних конечностях. Заболеваемость у женщин встречается в два раза чаще, чем у мужчин. [4]
В зависимости от возраста первичная лимфедема подразделяется на 3 вида:
Вторичная лимфедема встречается гораздо чаще, чем первичная. Она возникает из-за повреждения или обструкции ранее нормальных лимфатических сосудов при различных заболеваниях, рецидивирующих инфекциях, травмах, хирургических вмешательствах, ожирении или вследствие злокачественных процессов и их лечении, таких как лучевая терапия. [5] Лимфедема может возникать при хронические венозной гипертензии и венозных язвах, что связано с нарушенной лимфатической функцией при данной патологии. У пациентов с хроническими заболеваниями вен в 20% случаев также имеется вторичное лимфатическое поражение вследствие жидкостной перегрузки. [6] Таким образом, флеболимфедема относится к лимфедеме, вызванной хронической венозной недостаточностью. Вторичная лимфедема также может быть связана с генетической предрасположенностью. [7]
Инфекционные заболевания. Лимфатический филяриоз (также известный как слоновость) является наиболее распространенной причиной вторичной лимфедемы во всем мире. Это приобретенная инфекция, вызванная личинкой комара Wuchereria bancrofti. Она заражает людей, которые проживают или прибывают в районы, эндемичные по данному заболеванию, главным образом в странах Африки к югу от Сахары и в Индии. Личинки взрослого червя высаживаются на кожу человека москитами. Затем данные личинки мигрируют в лимфатические сосуды, вызывая обструкцию лимфатических протоков. Герпетическая инфекция также может, хотя и редко, вызывать лимфедему. Рецидивирующий целлюлит и рожистое восполение тоже приводят к повреждению кожных лимфатических протоков и могут быть причиной односторонней лимфедемы. [8]
Венерическая лимфогранулема — заболевание, передающееся половым путем, вызванное хламидиозом, может быть причиной лимфедемы наружных половых органов. Пораженные туберкулезом лимфатические узлы шеи являются гораздо менее распространенной причиной лимфедемы. [9]
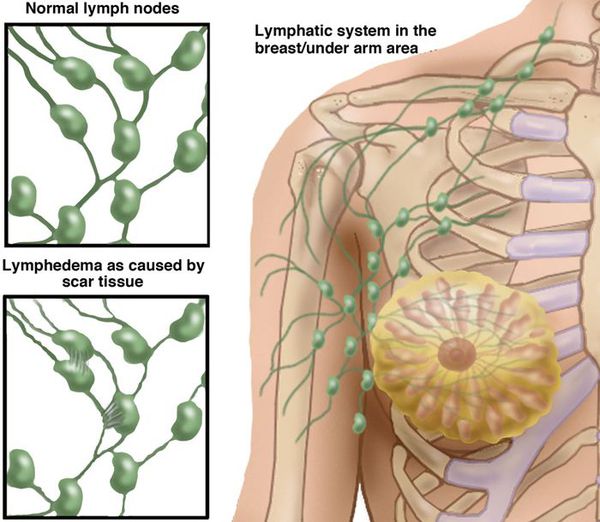
Хирургическое удаление лимфоузлов во время мастэктомии при раке молочной железы или лечении меланомы приводит к нарушению лимфатической дренажной функции. Радиационная терапия, которая приводит к практически необратимому повреждению интрадермальных лимфатических сосудов и узловому фиброзу. Вышеуказанная посттерапевтическая лимфедема, обычно проявляется хроническим односторонним отеком. Однако вмешательства на предстательной железе и шейки матки могут вызывать двусторонние отеки. [10]
Подокониоз является причиной неинфекционной слоновости, вызванной хроническим повреждением стоп, при длительной ходьбе босиком по глинистой почве, содержащей кремнезем. Это вторая по частоте причина тропической лимфедемы во всем мире. Поглощенные через кожу минеральные частицы индуцируют воспаление лимфатических сосудов и вызывают субэндотелиальный лимфатический отек и обструкцию сосудов. Подокониоз является эндемическим заболеванием в высокогорьях тропической Африки, Северной Индии и Центральной Америки. [11]
Морбидное ожирение является одним из главных факторов риска развития вторичной лимфедемы. Увеличение количества жировой ткани в зависимых областях вызывает обструкцию лимфатических сосудов. Снижение физической активности у пациентов с ожирением является усугубляющим фактором. [12]
Симптомы лимфостаза
Изменения кожных покровов. Лимфедема может быть односторонней или двусторонней. Пациенты часто жалуются на чувство тяжести и дискомфорт в пораженной конечности, особенно в конце дня. Преходящий незначительный отек является ранним симптомом лимфедемы. Со временем кожа приобретает ямочную текстуру по типу «апельсиновой корки». По мере прогрессирования заболевания кожа становится более текстурной и грубой из-за ее утолщения и фиброза. Стойкий, непродавливаемый и непроходящий отек указывает на необратимую стадию лимфедемы. Невозможность ущипнуть складку кожи у основания второго пальца (знак Стеммера) крайне патогномонична для хронической лимфедемы. Кроме того, для лимфедемы характерен такой симптом, как отек тыльной части стопы, который носит название «буйволиный горб».
С течением времени развивается слоновость. Кожа над пораженным участком имеет бородавчатый гиперкератотический или »мшистый» внешний вид. Кожа при хронической лимфедеме обычно имеет трещины, изъязвления с явлениями рецидивирующего целлюлита. Характерно выделение прозрачной светло-желтой жидкости (лимфоррея). Импетиго также является распространенным проявлением.
В более редких случаях пациенты с длительно существующей лимфедемой имеют риск развития кожной ангиосаркомы. Эта агрессивная опухоль обычно представляет собой красновато-фиолетовые пятна или узелки, которые могут увеличиваться, изъязвляться и в редких случаях метастазировать. На ранних стадиях лимфедема может быть трудно отличима от других распространенных причин отека конечностей, таких как верикозная болезнь, липедема и морбидное ожирение. Отек при хронической венозной недостаточности может имитировать раннюю стадию лимфедемы. Хотя в обоих случаях отеки неспадающие и очень похожи, венозный отек обычно ассоциируется с другими клиническими проявлениями заболеваний вен, такими как варикозное расширение вен, гиперпигментация, липодерматосклероз и наличие венозных язв. Более того, венозный отек купируется после поднятия конечности. При хронической венозной недостаточности отеки обычно связаны с увеличением капиллярного гидростатического давления. При лимфедеме оно, как правило, нормальное, и поэтому подъем ног не приводит к уменьшению отека. Это и является основным отличием от хронической венозной недостаточности. [13]
Липедема, также известная как липоматоз нижних конечностей, является хроническим прогрессирующим расстройством жировой ткани. Она часто ошибочно диагностируется как первичный лимфостаз. Липедема почти исключительно характерна для женщин и чаще всего возникает через несколько лет после наступления полового созревания. Проявляется как двустороннее симметричное накопление подкожного жира, преимущественно в нижних конечностях, с небольшими гематомами и тенденцией к прогрессирующему отеку ног. Одна из отличительных особенностей заключается в том, что отек резко прекращается на уровне лодыжек. Легкие гематомы связаны с повышенной хрупкостью капилляров в жировой ткани. [14]
Патогенез лимфостаза
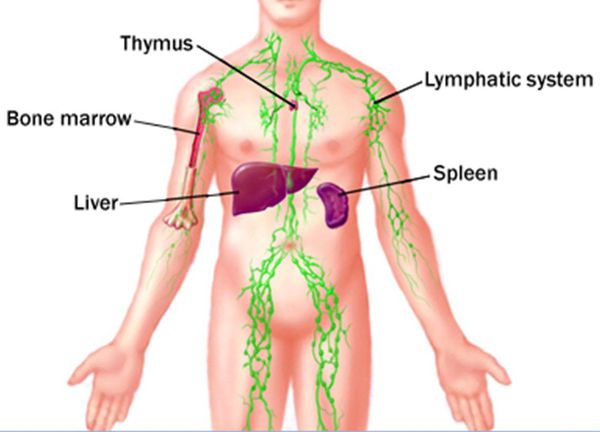
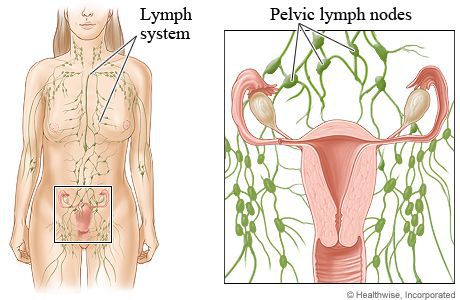
Лимфатическая система состоит из следующих лимфатических органов: лимфатические узлы, миндалины, тимус и селезенка. Все они связаны через сеть лимфатических сосудов, которые проходят параллельно венозной сосудистой сети.
Лимфатическая система имеет три основных функции: дренаж избыточной интерстициальной жидкости, абсорбция жира и иммунный контроль. Интерстициальная жидкость относится к части жидкости, которая выходит из капилляров в межтканевые пространства. Большее количество интерстициальной жидкости (90%) повторно поглощается за счет венозной микроциркуляции и возвращается обратно в кровоток. Оставшаяся часть (10%) межтканевой жидкости имеет относительно высокую концентрацию белка и дренируется лимфатическими капиллярами. Когда эта интерстициальная жидкость входит в лимфатические капилляры, она уже называется лимфой. Затем лимфа переносится через собирающие лимфатические сосуды, фильтруемые через лимфатические узлы, и в конечном счете, в точку рядом с правым предсердием. Нормальный лимфатический ток равен 2-3 литрам в день. В отличие от лимфатических капилляров, собирающие лимфатические сосуды имеют гладкую мускулатуру в их стенках и, следовательно, способны сжимать и продвигать лимфатическую жидкость проксимально.
Нарушение проходимости, вызванное обструкцией или лимфатической гипоплазией, приводит к накоплению интерстициальной жидкости и отеку тканей, известному как лимфедема. Последующее снижение содержания напряжения кислорода в тканях приводит к хроническому воспалению и реактивному фиброзу тканей.
Лимфатическая система выполняет также иммунную функцию посредством циркуляции различных антигенов и антител. Кожа имеет обширное присутствие лимфатических капилляров. Пациенты с лимфедемой склонны к рецидивирующим инфекциям кожи из-за накопления периферических тканевых антигенов в ней, что приводит к хроническому воспалению и последующему фиброзу мягких тканей. [15]
Классификация и стадии развития лимфостаза
Большинство членов Международного Общества Лимфологов в целом полагаются на трехступенчатую шкалу классификации лимфедем, увеличение номера определяет стадию 0 (или Ia), которая дает отсылку к скрытому или субклиническому состоянию, где отек еще не проявляется, несмотря на поврежденную лимфодинамику и тонкие механизмы нарушений в тканях (жидкость/состав) и уже видимые клинические изменения в субъективных специфических симптомах. Это состояние может существовать длительное время, как месяцы, так и годы, прежде чем появляется отек (стадии I-III).
Стадия I представляет собой раннее накопление жидкости с относительно высоким содержанием белка (например, по сравнению с «венозным» отеком) и проявляется отеком, который уменьшается при подъеме конечности. В эту стадию может иметь место питтинг (след от надавливания). Кроме того в данную стадию происходит увеличение различных пролиферирующих клеток.
Стадия II: возвышенное положение конечности не приводит к снижению отека тканей, что проявляется вышеуказанным питтингом. Поздний этап второй стадии характеризуется стойким отеком, гиперплазией жировой ткани и фиброзом.
Стадия III включает лимфостатическую слоновость, где питтинг может отсутствовать. Кроме того, выявляются трофические нарушения кожи, такие изменения, как акантоз, отложение жира и фиброза, бородавчатые разрастания. Эти стадии относятся только к физическому состоянию конечностей. Более подробная и всеобъемлющая классификация должна быть сформулирована в соответствии с пониманием патогенетического механизма лимфедемы (например, с точки зрения генеза и степени лимфангиодисплазии, нарушений лимфатического потока, дисфункции лимфатических узлов, как на основании анатомических визуальных особенностей, так и посредством физиологических и визуализационных методов диагностики). Также немаловажным является исследование лежащих в основе патогенеза лимфедемы генетических нарушений, которые постепенно выясняются специалистами в этой области. Недавние публикации, объединяющие как физические (фенотипические) результаты с функциональной лимфатической визуализацией (по лимфангиосцинтиграфии (LAS) на данный момент) могут дать прогноз о будущей эволюции классификации данного заболевания.
В дополнение стоит отметить, что включение генотипической информации, которая сейчас доступна даже при текущем скрининге, даст в будущем ценную информацию для предварительной постановки диагноза и классификации пациентов с периферической (и иной) лимфедемой. На каждой стадии может быть использована простая классификация, хотя и ограниченная, но тем не менее функциональная оценка тяжести заболевания с использованием простого измерения объема конечностей.
Минимальная степень лимфедемы характеризуется 40% объема. Клиницисты также включают такие факторы, как экстенсивность, наличие приступов, воспаление и другие дескрипторы или их индивидуальные определения степени тяжести. Некоторые врачи полагаются на классификацию по потере трудоспособности, согласно нормам Всемирной Организации Здравоохранения. Вопросы качества жизни (социальные, эмоциональные, физические недостатки и т. д.) также могут рассматриваться отдельными врачами для установления стадии заболевания. [16]
Осложнения лимфостаза
Основным осложнением лимфедемы являются часто встречающиеся множественные кожные язвы. Пациенты с лимфедемой восприимчивы к рецидивирующим инфекциям мягких тканей, таких как целлюлит и рожистое воспаление. Основной причиной целлюлита является инфицирование пациента стрептококком группы А. Каждый эпизод целлюлита приводит к дополнительному повреждению лимфатической системы, что способствует ухудшению состояние пациента. [17] [18]
Такое грибковое заболевание, как дермотофития стоп, чрезвычайно распространено у пациентов с лимфостазом вследствие хронических межпальцевых мацераций. Кроме того, у данных пациентов имеется 10%-ный риск развития ангиосаркомы. Причем это характерно для пациентов с хронической лимфедемой длительностью 10 лет. Синдром Стюарта-Тревиса относится именно к кожной ангиосаркоме, развивающейся у пациентов с постмастэктомической лимфедемой. Ангиосаркома является высокоагрессивной злокачественной опухолью с чрезвычайно негативным прогнозом и 5-летней выживаемостью менее 10%.
В периодической медицинской литературе были сообщения и о других злокачественных опухолях, которые также ассоциированы с лимфедемой: плоскоклеточная карцинома, базально-клеточная карцинома, кожная лимфома, меланома и саркома Капоши. [19] [20] Несмотря на распространенность специфических онкологических заболеваний у этих пациентов, до сих пор не удалось установить четкую причинно-следственную связь между лимфедемой и развитием опухолей. Одним из возможных объяснений может быть нарушение местного иммунного ответа в лимфедематозной конечности. [21]
Кроме того, важными осложнениями являются психосоциальная стигматизация и снижение самооценки, которые считаются распространенными среди пациентов с лимфостазом из-за нарушения подвижности, затруднениями в подборе одежды, деформаций конечностей и гениталий. [22] Резюмируя вышесказанное, можно констатировать, что хронический отек нижних или верхних конечностей вызывает дискомфорт и утрату полноценного функционального состояния пораженного органа. Рецидивирующие бактериальные и грибковые инфекции достаточно распространены при лимфедеме. Рецидивирующий целлюлит и лимфангиты способствуют прогрессированию повреждения всей лимфатической системы. Часто возникают трофические хронические трудноизлечимые язвы. Кожная ангиосаркома является редким и часто летальным осложнением, основным морфологическим признаком которого является появление красно-фиолетовых пятен. Серьезные психосоциальные последствия могут иметь место из-за стойких косметических нарушений и ограничения качества жизни пациентов с лимфостазом.
Диагностика лимфостаза
Лимфедема — это прежде всего клинический диагноз, и поэтому тщательный сбор анамнеза и физикальное обследование играют неоценимую роль. Поздние стадии лимфостаза могут быть диагностированы клинически без помощи дополнительных методов. Однако на ранних стадиях заболевания, сопутствующие состояния, такие как ожирение, липодистрофия и венозная недостаточность, могут осложнить постановку правильного диагноза, поэтому дополнительные методы обследования могут быть крайне необходимы. Существует много диагностических инструментов для оценки лимфатической функции. Но решение использовать любой из них должно основываться на состоянии пациента. Ранняя диагностика лимфостаза важна, потому что это значительно увеличивает успех терапии. [23]
Сбор анамнеза и физикальный осмотр
Анамнез должен включать возраст начала заболевания, семейную историю лимфостаза, наличие в анамнезе различных травм, инфекций, онкозаболеваний, сердечной патологии, гипотиреоза, гипоальбуминемии, сепсиса, венозной недостаточности или лимфатической обструкции. Кроме того, значимым фактом анамнеза являются перенесенная лучевая терапия на паховых/подмышечных областях, лимфаденэктомия, а также путешествие в районы, эндемичные по филяриозу. Лимфостаз нижней конечности обычно проявляется как отек на дорсальной поверхности стопы и пальцев с характерным тупым «квадратным» внешним видом. Лимфедема начинается обычно с отека дистальной части конечности, а затем отек прогрессирует проксимально. Кожаная или ямочная текстура кожи (феномен апельсиновой корки) и знак Копоши-Стеммера (невозможность ущипнуть складки кожи на дорсальной поверхности основания второго пальца) являются характерными признаками хронического лимфостаза. На поздних стадиях кожа на пораженном участке становится гиперкератотической, развиваются папулы, бляшки и узелки с выраженным фиброзом.
Визуализационные методики
В большинстве случаев использование различных методов визуализации не требуется для постановки диагноза. Однако они могут быть использованы для подтверждения диагноза и оценки степени поражения лимфатической системы для определения наиболее оптимальной терапевтической тактики.
Также используются и методы лабораторной диагностики, оценивающие функцию печени и почек. Гистологические исследования имеют низкую чувствительность и специфичность для постановки диагноза лимфостаза. [24]
Лечение лимфостаза
К сожалению, лимфостаз является неизлечимым заболеванием. С другой стороны, эффективное лечение при данной патологии доступно. Два основных направления лечения включают нехирургические и хирургические варианты. Основу нехирургических методов лечения лифедемы составляют полная деконгестивная (противоотечная) терапия, компрессионная терапия, современные методы аппаратной пневмокомпрессии и специальные упражнения. Эти методы лечения эффективны главным образом на ранней стадии лимфедемы. Сегодня существует глобальная тенденция к хирургическому вмешательству и хирургическим методам, включая физиологические и восстановительные методы. [27]
Нехирургическое лечение
Обучение пациентов самоконтролю является одновременно решающим и обязательным фактором для эффективного лечения лимфостаза. Основными принципами самоконтроля являются уход за кожей, выполнение лифодренажного массажа своими силами, контроль за правильным положением повязок и одежды, правильное питание, физические упражнения и контроль веса.
Полная деконгестивная или противоотечная терапия. Полная противоотечная терапия считается золотым стандартом при лечении лимфедемы и включает в себя две фазы: редуктивную (фаза 1) и фазу поддержания (фаза 2). Данная терапия включает в себя ручной лимфодренаж, компрессионную терапию, физические упражнения, уход за кожей, а затем ношение компрессионного трикотажа. Хотя это безопасно и эффективно, но для большинства пациентов это затратно и требует много времени и наличия квалифицированных врачей для контроля качества выполняемых процедур. [28]
Ручной лимфодренаж отличается от стандартного массажа тем, что он ориентирует лимфедематозную жидкость на правильное функционирование лимфатических узлов. Кохрановское исследование показало его значимую эффективность в сочетании с компрессионной терапией, особенно у пациентов с начальными формами лимфостаза. Внешняя компрессия важна на всех этапах лечения лимфедемы. Эффективность компрессионной терапии одной или в сочетании с ручным лимфодренажным массажем доказана многочисленными рандомизированными клиническими исследованиями.
Компрессия достигает нескольких целей: улучшение лимфатического и венозного оттока, уменьшение накопления продуктов белкового обмена тканей, правильное формирование конечности, стойкий контроль объема конечности, поддержание целостности кожных покровов и защита конечности от потенциальной травмы. [29] В ряде рандомизированных исследований также сообщалось, что низкоуровневая лазерная терапия улучшает измеряемые физические параметры, а также субъективные критерии оценки боли у пациентов с лимфостазом. Лазерная терапия увеличивает лимфатический дренаж, стимулируя образование новых лимфатических сосудов, улучшая лимфатическую моторику и предотвращая образование фиброзной ткани. Обычно данный метод используется в комбинации с остальными нехирургическими методами. [30] Кроме того, в консервативной комплексной терапии лимфостаза применяются аппаратные методы пневмокомпрессии, специальные упражнения. Эффективно показал себя метод подъема ног для физического увеличения лимфатического оттока, особенно на ранних стадиях заболевания. Снижение массы тела и гигиена кожи играют важную роль на всех стадиях заболевания. Медикаментозная терапия диуретиками и бензопиронами не показала своей эффективности в исследованиях по лечению лимфостаза.
Хирургическое лечение
Различные хирургические методы были опробованы на протяжении многих лет в прошлом. Однако большинство этих методов были отвергнуты из-за их крайней неэффективности. Лишь несколько хирургических подходов являются по-прежнему жизнеспособными. Они применимы при тяжелой слоновости и массивной локальной лимфедеме, особенно когда консервативная терапия безуспешна.
Существуют следующие основные подходы к хирургическому лечению лимфедемы:
Дебуляция — резекция избыточной лимфедематозной ткани. При этом нормальные ткани, которые по-прежнему дренируются компетентной лимфатической системой, остаются нетронутыми, после чего область покрывается кожными аутотрансплантатами. Наиболее часто используемым методом является метод Чарльза и процедура Томпсона.
К реконструктивному подходу относятся два микрохирургических метода лечения, которые показали многообещающие результаты: создание лимфовенозных анастомозов и реваскуляризация лимфатических узлов. Однако хирургическое лечение имеет ограничения. Слабое заживление ран остается самым главным фактором. Дополнительные хирургические риски включают сенсоневральные повреждения, гипертрофическое рубцевание, некроз трансплантата, экзофитный кератоз и рецидив лимфедемы.
Прогноз. Профилактика
Недавнее обнародование списка факторов риска вторичной лимфедемы по типу «это делать, а это не делать» в значительной степени анекдотично и недостаточно исследовано. Хотя некоторые предостережения основаны на вполне надежных физиологических принципах (например, избегать чрезмерного нагревания заинтересованной конечности или для предотвращения заражения), другие менее поддерживаются.
Следует отметить, что большинство опубликованных исследований по частоте возникновения вторичной лимфедемы сообщают о менее чем 50% вероятности развития лимфедемы. Поэтому стандартное использование некоторых из этих методов профилактики для «предотвращения» лимфедемы может быть неприемлемым и, вероятно, подвергает пациентов ненужной терапии. Многие методы профилактики не имеют под собой доказательной базы и не продемонстрировали четко определенные риски и профилактические меры.
Если диагноз лимфедемы неясен или нуждается в более четком определении прогноза, то рекомендовано обратиться за консультацией к клиническому лимфологу или в специализированный лимфологический центр, если он доступен. В редких случаях хроническая лимфедема может привести к кожной ангиосаркоме, известной как синдром Стюарта-Тревиса. Прогноз данного осложнения неблагоприятный, средняя выживаемость пациентов составляет примерно 19 месяцев после постановки диагноза.