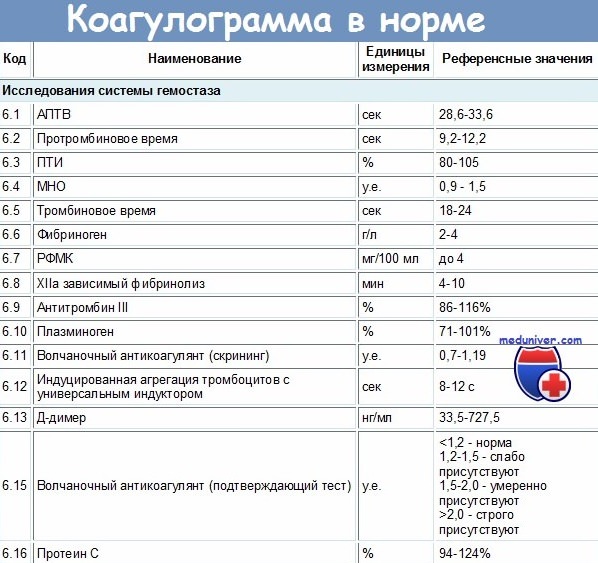
О чем расскажет коагулограмма?
Для хорошего движения по сосудам кровь должна быть достаточно текучей. Гемостаз — биологическая система, которая, с одной стороны, сохраняет жидкое и текучее состояние крови, а с другой стороны, останавливает кровотечения путем свертывания крови (коагуляции). Коагулограмма – лабораторный тест, который как раз и оценивает, насколько эффективно работает гемостаз.
Кому нужен этот анализ?
Все знают: если вы порезались или как-то еще повредили сосуд, то сначала кровь течет, а потом образует плотный сгусток, который закупорит место повреждения. Этот сгусток — тромб. Он может образоваться и внутри сосуда, вены или артерии, если там имеется повреждение.
Если у крови повышенная свертываемость, тромб формируется очень быстро и плохо рассасывается. Кровяные сгустки могут вызвать закупорку сосудов, привести к тромбозу вен или инсульту. Высокая свертываемость крови может быть симптомом некоторых заболеваний. Так же ее важно контролировать во время беременности и при приеме некоторых препаратов, в том числе оральных контрацептивов и заместительной гормональной контрацепции в менопаузе. На их фоне коагулограмму надо делать регулярно.
Если у крови плохая свертываемость, то тромб формируется медленно. Это особенно опасно, если вы планируете хирургическую операцию, ведь в этой ситуации риск кровотечения возрастает.
Развеять опасения
Комплекс лабораторных тестов Коагулограмма, скрининг даст полноценную картину состояния вашего гемостаза. Она включает основные показатели, по которым врач-терапевт сможет оценить, насколько сбалансированно работают свертывающая и противосвертывающая системы крови. Если вы посетите врача до сдачи анализа, то можете услышать другие названия этого комплекса тестов: анализ гемостаза, коагулограмма, гемостазиограмма, анализ свертывания крови, анализ на свертываемость.
Обычно удобнее идти к врачу, уже имея на руках результаты комплекса Коагулограмма, скрининг. В него входят следующие тесты:
На данные коагулограммы влияет прием некоторых препаратов, даже витаминов. Поэтому при отклонениях в нем обязательно сообщите врачу, что, как долго и в какой дозировке вы принимаете. Лучше даже взять инструкцию от препарата с собой на прием.
Не мучайтесь сомнениями, все ли у вас в порядке! Сдавайте анализы и консультируйтесь по их результатам у врачей.
Диссеминированное внутрисосудистое свёртывание крови (ДВС-синдром)
Диссеминированное внутрисосудистое свёртывание крови (ДВС-синдром) – это один из наиболее распространённых в интенсивной терапии и представляющих большую опасность для больных вид патологии гемостаза. ДВС-синдром в настоящее время является важной проблемой медицины, так как осложняет течение практически любого заболевания, может являться причиной их развития и нередко предопределяет прогноз заболевания. Данный синдром универсален и может протекать как молниеносно с развитием смертельного исхода, так и латентно. При ДВС-синдроме возможно свёртывание крови в сосудистом русле, так и регионарные и органные тромбозы.
ДВС-синдром является полиэтиологическим заболеванием и может развиваться при различных заболеваниях и патологических процессах, которые приведены в таблице 1.
Заболевания системы крови
Острый промиелоцитарный лейкоз
Хронический мегакориоцитарный лейкоз
Серповидноклеточная анемия (гемолитический криз)
Эмболия околоплодными водами
Конфликт матери и плода по АВО и резус-фактору
Заболевания сосудистой стенки и сосудов
Тромбоэмболия лёгочной артерии
Тромботическая тромбоцитопеническая пурпура
Шок (травматический, ожоговый, септический)
Массивные поражения тканей (краш-синдром, большие операции)
Синдром массивных трансфузий
Переливание несовместимой крови
Отравления и интоксикации (лекарственные, змеиные яды)
В основе патогенеза ДВС-синдрома лежит преобладание активирующих свёртывающую систему механизмов над антикоагулянтной системой.
Развитие тяжёлого ДВС-синдрома начинается в результате массивной и длительной активации свёртывающей системы в под воздействием внешнего фактора. В результате этого развивается состояние гиперкоагуляции, что приводит к повсеместному образованию мелких сгустков, которые оседают в микроциркуляторном русле.
Обязательным элементом ДВС-синдрома является агрегация тромбоцитов. В результате гиперкоагуляции тромбоциты склеиваются между собой. Постепенно количество тромбоцитов уменьшается, в связи с чем развивается тромбоцитопения потребления.
В патогенезе ДВС-синдрома центральное место занимают образование в сосудистом русле тромбина и истощение механизмов, препятствующих свёртыванию крови и агрегации тромбоцитов. В процессе развития ДВС-синдрома может происходить снижение уровня основного физиологического антикоагулянта – антитромбина III в плазме. В результате запущенного патологического процесса в крови накапливается огромное количество активированных факторов свёртывания, что приводит к истощению системы фибринолиза и образовавшиеся сгустки практически перестают лизиироваться. Развивается блокада микроциркуляции, приводящая к нарушению кровоснабжения почек, печени, лёгких, слизистых оболочек кишечника, что создаёт предпосылки к развитию полиорганной недостаточности (ПОН).
Основными типичными клиническими проявлениями ДВС-синдрома являются геморрагии и/или тромбозы и ПОН. ПОН развивается в результате тромбогеморрагических поражений органов, имеющих богатую микроциркуляторную сеть. К данным органам относятся лёгкие, почки, головной мозг, кожа, надпочечники и печень.
Первыми признаками поражения лёгких является одышка и падение артериальной оксигенации. Нарушение микроциркуляции под воздействием вазоактивных субстанций приводит к развитию острой дыхательной недостаточности с нарастающей одышкой, цианозом, ателектазами в лёгких и прогрессирующим отёком лёгких.
Отложение фибрина в сосудах почечных клубочков может привести к почечной недостаточности. В клинической картине наблюдается олигоурия, рефрактерная к диуретикам, микро-и макрогематурия, высокие показатели мочевины и креатинина сыворотки крови.
Нарушения микроциркуляции головного мозга приводит к энцефалопатии, нарушению психики, потери сознания. В случае тяжёлого течения ДВС-синдрома возможно кровоизлияние в головной мозг.
Для ДВС-синдрома характерно образование стрессовых, гипоксических эрозий и язв слизистой желудочно-кишечного тракта, осложняющихся диффузным кровотечением.
При ДВС-синдроме отмечается геморрагический синдром, который носит смешанный гемотомно-петехиальный характер. На коже спонтанно или при незначительных воздействиях появляются синяки. Течение геморрагического синдрома сопровождается носовыми, десневыми кровотечениями и кровотечениями из места инъекций.
Кровотечения, геморрагический синдром и внутрисосудистый гемолиз приводят к развитию анемического синдрома. Анемический синдром сопровождается снижением уровня гемоглобина, эритроцитов.
В результате нарушения микроциркуляции, наличия гематом и повышения проницаемости слизистой оболочки желудочно-кишечного тракта создаются благоприятные условия для развития генерализованной инфекции – сепсиса.
По клиническому течению ДВС-синдрома выделяют:
Острый ДВС-синдром характерен для акушерской патологии, сепсиса, массивного краш-синдрома, обширных ожогов, массивного распада опухолей, переливания несовместимой крови. Для острого ДВС-синдрома характерна диффузная кровоточивость из операционной раны, носовые, десневые, постинъекционные кровотечения.
Подострое течение ДВС-синдрома наблюдается при аутоиммунных заболеваниях, хронических инфекциях и при всех перечисленных выше патологических состояниях. Длительность подострого течения занимает от нескольких недель до месяцев.
Хронический ДВС-синдром может длительное время не проявляться клинически. Возникновение ДВС-синдрома связано с прогрессированием основного заболевания. Хронический ДВС-синдром встречается при терапевтической патологии, например при сердечной недостаточности, хроническом гломерулонефрите, септическом эндокардите.
Рецедивирующий ДВС-синдром проявляется необильными носовыми кровотечениями, синяками на коже в период обострения основного заболевания.
В настоящее время в течение ДВС-синдрома выделяют три стадии:
I стадия – гиперкоагуляции. Для стадии гиперкоагуляции характерно повышение агрегации тромбоцитов и тромбообразование. При остром течении ДВС-синдрома данная стадия кратковременна и быстро переходит в стадию гипокоагуляции.
II стадия – нормокоагуляция. В этой стадии наблюдается субкомпенсация гемостаза.
III стадия – гипокоагуляция, при которой развивается выраженная кровоточивость, являющаяся следствием истощения фибринолиза.
ДВС-синдром является вторичным проявлением патологического процесса. Поэтому главной задачей является устранение провоцирующего фактора или своевременное лечение основного заболевания.
Лечение ДВС-синдрома включает в себя:
Использование гепарина оправдано на любой стадии ДВС-синдрома. В стадии гиперкоагуляции ДВС-синдрома гепарин применяется в суточной дозе 500-800 ЕД/кг. Доза гепарина подбирается в соответствии с лабораторными показателями гемостаза. Считается, что исходное время свертывания по Ли-Уайту должно увеличиться в 2 раза. Определёнными преимуществами обладают препараты фракционированного гепарина (фраксипарин, клексан, фрагмин), которые можно вводить 1-2 раза в сутки без значительных колебаний времени свертывания. В стадии гипокоагуляции гепарин вводят вместе со свежезамороженной плазмой (СЗП). В данном случае доза гепарина составляет 2500-5000 ЕД. Введение гепарина перед СЗП повышает активность антитромбина-III (AT-III) по отношению к факторам Ха и IХа, обрывает процесс внутрисосудистого свёртывания и тем самым не даёт развиться коагулопатии потребления.
Заместительная терапия предназначена для восстановления гемостаза больного. К заместительной терапии относится переливание СЗП, которая содержит достаточную концентрацию необходимых компонентов гемостаза. На начальных этапах лечения ДВС-синдрома доза СЗП составляет 800-1600 мл/сут. В стадии гипокоагуляции доза СЗП увеличивается до 15-20 мл/кг/сут.
Эффективно применение криопреципитата, содержащего более высокие концентрации фибриногена, фактора Виллебранда, фибронектина и фактора ХIII. Криопреципитат показан при остром или молниеносном течении ДВС-синдрома.
Для восстановления объёма циркулирующей крови используются растворы кристаллоидов, альбумина и коллоидов. В I стадии применяется растворы гидроксиэтилкрахмала, что способствует улучшению микроциркуляции.
При снижении уровня гемоглобина ниже 70-80 г/л, гематокрита менее 25% показано переливание отмытых эритроцитов, а при их отсутствии — эритроцитной массы. Тромбоцитарный концентрат переливают при снижении уровня тромбоцитов до 50•109/л.
В стадии гипокоагуляции показано введение ингибиторов протеаз: контрикала или апротинина (трисалол). Контрикал в водят внутривенно в начальной дозе 350000 АтрЕ и затем в поддерживающей дозе 140000 АтрЕ каждые 4 ч до нормализации показателей гемостаза. Начальная доза трасилола составляет 500000 КИЕ и поддерживающая – 50000 КИЕ/ч.
Одним из компонентов терапии ДВС-синдрома является использование препаратов улучшающих микроциркуляцию и дезагрегантов.
Важным компонентом комплексной терапии ДВС-синдрома являются методы экстракорпоральной детоксикации. Методы экстракорпоральной детоксикации повышают эффективность лечения ДВС-синдрома и его осложнений, что позволяет снизить летальность.
Плазмаферез (ПФ) позволяет удалять продукты паракоагуляции, активаторы свёртывания, циркулирующие иммунные комплексы, крупномолекулярные соединения. ПФ необходимо проводить в максимально ранние сроки ДВС-синдрома. Для достижения клинического эффекта необходимо, чтобы объём удаляемой плазмы за один сеанс ПФ был не менее 50% объёма циркулирующей плазмы. Замещение должно производиться СЗП в объёме, равном объёму удаляемой плазмы.
Развитие ПОН и в частности острого повреждения почек является показанием для проведения заместительной почечной терапии (ЗПТ): гемодиализ, гемофильтрация, гемодиафильтрация. ЗПТ удаляет низко- и среднемолекулярные токсины, медиаторы воспаления, снижает объём жидкости, улучшает кислородтранспортную функцию крови.
Прогноз при ДВС-синдроме определяется степенью его выраженности, распространенностью и характером течения. Опыт современной медицины даёт основание говорить о возможности эффективного лечения больных с острыми вариантами ДВС-синдрома, однако летальность может составлять 50 %.
Признаки хронометрической нормокоагуляции что это
Ввиду огромной важности системы гемостаза для стабильной работы организма, в клинической медицине разработаны различные методы исследования этой защитной реакции организма. Наиболее распространенным анализом для исследования свертываемости крови является определение коагулограммы, которая включает в себя определение времени, необходимое для остановки кровотечения и количества различных факторов этой системы. Данное исследование дает очень много информации о состоянии организма в целом, ведь нормальная работа системы гемостаза зависит от правильного функционирования различных органов и систем, поэтому любые нарушения в их работе находят свое отражение в коагулограмме.
Существует базовый и развернутый анализ крови на определение коагулограммы. Норма базовой коагулограммы выглядит примерно так:
Снижение этого показателя коагулограммы является причиной повышенной кровоточивости и увеличения времени свертываемости крови. Причиной этого состояния могут быть некоторые заболевания печени (гепатит, цирроз), нехватка витаминов (К, С, В) и взаимосвязанные с ней заболевания желудочно-кишечного тракта (дисбактериоз, болезнь Крона, синдром мальабсорбции), прием некоторых лекарственных веществ, а также вторая стадия ДВС-синдрома.
Как правило, после проведения анализа на составление базовой коагулограммы, который используется для подтверждения проблем со свертываемостью крови, производится расширенное исследование. Целью получения расширенной коагулограммы является более точное определение причин тех или иных нарушений свертываемости крови. В рамках расширенного анализа определяют целый ряд дополнительных показателей.
Протеин С является одним из важнейших противосвертывающих факторов. Его уровень выражается в процентах от эталонного показателя, норма определения в расширенной коагулограмме составляет 60-140%. При снижении этого показателя начинает превалировать свертывающая система крови, что ведет к повышенному тромбообразованию. Причиной снижения могут выступать заболевания печени и дефицит витамина К, что нередко развивается в результате дисбактериоза толстой кишки. Также снижение уровня протеина С может быть обусловлено генетическими факторами.
Антитромбин-3, также как и протеин С, является противосвертывающим фактором, норма которого составляет от 75 до 110 % от эталонного значения. Особую роль играет резкое снижение содержания этого фактора, так как в такой ситуации в разы повышается риск тромбообразования с развитием эмболии или даже ДВС-синдрома.
Уровень тромбоцитов при определении коагулограммы редко определяется, так как зачастую это значение уже известно из общего анализа крови. Однако роль тромбоцитов, норма содержания которых составляет 180-320 млрд на литр, в развитии кровяного сгустка огромна, поэтому начинать какие-либо исследования без предварительного определения их количества не имеет смысла.
Учебное видео расшифровки коагулограммы в норме и при отклонениях
— Рекомендуем посетить наш раздел с интересными материалами на аналогичные тематики «Профилактика заболеваний»
Признаки хронометрической нормокоагуляции что это
Свертываемость крови – защитный механизм человеческого организма, который помогает избежать больших кровопотерь при повреждениях тканей. Данный процесс очень сложный и состоит из нескольких этапов, поэтому исследование проводится сразу по нескольким параметрам.
Если в организме или на поверхности кожи есть повреждение, из которого течет кровь, организм моментально активирует систему коагуляции, которая закупоривает протекающий сосуд кровяным сгустком. Данный процесс называется каскад коагуляции – он зависит от ряда факторов. Отсутствие хоть одного из них может привести к очень серьезным последствиям, вплоть до летального исхода. Конечным результатом коагулятивной цепочки является образование нерастворимых нитей фибрина, которые соединяются в месте повреждения с тромбоцитами, вследствие чего возникает стабильный сгусток крови. Он предотвращает чрезмерную потерю крови и остается на месте до тех пор, пока поврежденная область не затянется рубцовой тканью. Затем активируются другие факторы, которые значительно замедляют свертывание крови, после чего растворяют сгусток. Спустя некоторое время он полностью исчезает.
Циркуляция крови в организме человека зависит от множества факторов, среди которых – скорость образования и рассасывания тромбов. Если они образуются чрезмерно, в итоге это приводит к закупориванию сосудов. Если же тромбы образуются в недостаточном количестве, это чревато развитием серьезных кровотечений. Тромбоз у беременных женщин очень опасен, ведь он может привести к отслойке плаценты и даже выкидышу. Если у человека наблюдается высокая свертываемость крови, это может привести к осложнениям ишемической болезни сердца и ряду других патологий.
У здоровых людей образование и удаление сгустков крови сбалансировано. Таким образом организм гарантирует, что кровотечение не приведет к чрезмерной потере крови, а также не станет причиной возникновения тромбоза из-за чрезмерного образования фиброзных сгустков. Если у человека наблюдаются проблемы со свертываемостью крови, это может привести к ряду серьезных последствий, ведь у них снижено количество тромбоцитов или факторов свертывания, что в итоге может привести к непредсказуемому результату даже при небольшом повреждении. В лабораторных условиях можно оценить основные этапы коагуляционного каскада. Исследование проводится с помощью специального компьютерного оборудования. Лаборант проверяет образец крови, добавляя туда особые вещества, после контакта с которыми биологический материал начинает процесс коагуляции. Засекается время, в течение которого образец сворачивается. Также измеряются белковые факторы, являющиеся неотъемлемой частью коагуляционного каскада. С помощью полученной информации можно диагностировать ряд дефектов или проблем с факторами свертывания.
На коагуляционный каскад могут повлиять такие факторы, как беременность, наличие воспалительных процессов или инфекционных заболеваний. Может увеличиться как кровоточивость, так и тромбообразование. Данное исследование очень популярно и проводится довольно часто. Основной его целью является оценка способности организма контролировать процесс свертывания крови в случае возможного кровотечения. Данное исследование обязательно в родах, при операции и в ряде других ситуаций. Также назначается пациентам для оценки имеющихся отклонений в коагуляционном каскаде на фоне имеющихся патологических состояний и заболеваний.
Коагулограмма расшифровка анализа
Для проведения анализа требуется проведение нескольких сложных биохимических реакций. Это может занять от 24 до 48 часов. Немаловажен и график работы медицинского заведения, а также то, является ли оно отдельной лабораторией или посредником.
Нормальные значения коагулограммы приведены в таблице ниже:
Коагулограмма
В системе гемостаза принимают участие факторы свертывающей, противосвертывающей (антикоагулянтной) и фибринолитической систем крови. Изменение функционального состояния одной из систем сопровождается компенсаторными сдвигами в деятельности другой. Нарушение функциональных взаимосвязей может привести к тяжелым патологическим состояниям организма, заключающимся или в повышенной кровоточивости, или во внутрисосудистом тромбообразовании.
Условия сдачи коагулограммы
Не допускается в течение 8 часов (желательно 12) до сдачи анализа прием пищи, в том числе, сок, чай, кофе, алкоголь. Можно пить простую воду. Если врач назначил сдачу анализа на фоне приема препаратов, влияющих на свертывание крови, отметьте это при сдаче анализа.
D-димер (продукт деградации фибрина, D-dimer, Fibrin degradation fragment)
Определение уровня Д-димера является высокоспецифичным и чувствительным маркером тромбообразования. Однако его уровень повышается и при патологических состояниях, сопровождающихся усиленным фибринолизом: геморрагические осложнения, инфекции, заживлении ран, при наличии в крови ревматоидного фактора и т.п. Тем не менее, определение Д-димера имеет важное диагностическое значение в диагностике тромбозов. Нормальный его уровень позволяет с точностью 98% исключить состояния, сопровождающиеся повышенным тромбообразованием.
Антитромбин III (Antithrombin III)
АТ III определяется по ингибированию тромбина. Дефицит AT III может быть наследственным или приобретенным. Наиболее частым клиническим проявлением наследственного дефицита AT III является развитие тромбоза глубоких вен и, как следствие этого, тромбоэмболии легкого. Вероятность развития тромботических осложнений у больных с дефицитом AT III увеличивается с возрастом.
Приобретенный дефицит AT III может быть обусловлен сниженным синтезом, повышенным потреблением или потерей белка. Во всех этих случаях наблюдается параллельное снижение концентрации и активности AT III. AT III синтезируется в печени, поэтому некоторые заболевания печени приводят к снижению уровня AT III. Если параллельно со снижением AT III происходит повышение тромбогенных свойств стенки сосудов и активация свертывания, то наблюдается дальнейшее снижение AT III обусловленное его потреблением, что встречается при ДВС-синдроме, вызванном различной патологией: при массивных травмах, сепсисе, воспалениях ран, змеиных укусах, осложненной беременности, раке и т.д.
Кроме того, снижение синтеза AT III наблюдается при терапии эстрогенами и синтетическими препаратами, обладающими эстрогенным действием, нефротическом синдроме и желудочно-кишечных заболеваниях, когда потеря белка превышает скорость его синтеза. В этих случаях наблюдается параллельное снижение AT III и альбумина.
Тромбиновое время (ТВ)
Дает общую оценку конечного этапа свертывания крови. Это показатель перехода фибриногена в фибрин, состояния антикоагулянтной системы. Не зависит от внутренней и внешней системы активации, но зависит от концентрации фибриногена, наличия аномального фибриногена, активности антитромбинов, процессов полимеризации и стабилизации фибрина.
В клинике определение ТВ используется для контроля за гепаринотерапией (особенно высомолекулярным гепарином) и фибринолитической терапией; для диагностики активации фибринолиза, косвенной диагностики гипо- и дисфибриногенемий.
Этот тест — один из основных для контроля лечения гепарином. У больных, получающих гепаринотерапию, АЧТВ удлиняется в 1,5–2 раза, что свидетельствует об эффективности лечения.
Определение АЧТВ позволяет окончательно решить вопрос о толерантности к гепарину: для этого проводят определение АЧТВ за 1 ч до очередного введения гепарина. Если АЧТВ окажется удлиненным более чем в 2,5 раза по сравнению с нормой, констатируют повышенную чувствительность к гепарину, снижают его дозу или увеличивают интервал между введениями.
Протромбиновое (тромбопластиновое) время (ПВ)
Путем ПВ с вычислением международного нормализованного отношения (МНО) и протромбинового индекса (ПИ) суммарно оценивают внешний механизм. Протромбиновое время зависит от содержания собственно протромбина — фактора II, а также V, VII, X факторов и фибриногена. Используют для диагностики тромбоэмболических и геморрагических состояний, для контроля за лечением антикоагулянтами непрямого действия.
Определение содержания фибриногена
Его концентрация определяется по времени образования сгустка в разведённой бестромбоцитной плазме при добавлении избытка высокоактивного тромбина (по Клауссу). Фибриноген синтезируется в печени, откуда поступает в кровь. Изменение концентрации фибриногена наблюдается при различных заболеваниях — в первую очередь, при нарушениях системы гемостаза и острых воспалениях.
Повышение количества фибриногена даже в пределах нормальных значений рассматривается как фактор риска при сердечно-сосудистых заболеваниях.
Антифосфолипидный синдром (АФЛ)
Это группа заболеваний, вызванных наличием антител к фосфолипидам. Антифосфолипидные антитела (АФЛ) — аутоантитела класса IgG и IgM, способные связываться с антигенными детерминантами фофолипидов- (кардиолипин, фосфатидилсерин, фосфатидилинозитол, фосфатидиловая кислота, фосфатидилхолин) и фосфолипид — связывающих белков. Связывание с кардиолипином происходит при обязательном участии кофактора — рг-гликопротена I.
Причины выработки АФЛ не установлены. Предположительно, длительная персистенция вирусов, тропных к эндотелию сосудов, вызывает: морфологические и функциональные изменения клеток эндотелиальной мембраны с развитием гиперкоагуляционного синдрома, стимуляцию В-лимфоцитов, которые при определенных условиях продуцируют АФЛ.
АФЛ связываются с фосфолипидами клеточных мембран, изменяя конформационную и метаболическую структуру клетки, что приводит к нарушению функции клеток с развитием стаза и тромбоза. В связи с тем, что поражаются сосуды различного калибра и различной локализации, спектр клинических проявлений АФС разнообразен — тромбозы, инсульты, акушерская патология, тромбоцитопении. Частота встречаемости АФЛ при различных патологических состояниях представлена ниже.
Основным критерием лабораторного диагноза АФС является наличие АФЛ (или антител к кардиолипину) и волчаночного антикоагулянта в 2-х или более исследованиях с интервалом не менее 6 недель.
Устаревшие методы исследования нарушений гемостаза и варианты их замены