Гастроэзофагеальная рефлюксная болезнь: новый подход к причинам и лечению
Гастроэзофагеальная рефлюксная болезнь: новый подход к причинам и лечению
Гастроэзофагеальная рефлюксная болезнь (ГЭРБ) — это состояние, при котором количество рефлюкса желудочного сока в пищевод превышает нормальный предел и вызывает или не вызывает симптомов повреждения слизистой оболочки пищевода. Это означает, что ГЭРБ не может вызывать недомогание пациента до тех пор, пока болезнь не обострится.
Патофизиология
В нормальных условиях (у здорового человека) содержимое желудочного сока с повышенной кислотностью периодически попадает в пищевод, но внутренние защитные механизмы либо снижают количество выделяемой кислоты до минимума, либо удаляют кислоту, которая быстро удаляется путем «очищения» пищевода. Поэтому симптомы кислотного раздражения пищевода не ощущаются или минимальны.
Механизмы, которые защищают пищевод от желудочной кислоты, включают нижний сфинктер пищевода (сфинктер) и нормальную перистальтику пищевода (моторику). Когда эти механизмы нарушаются, возникает рефлюкс и возникают симптомы ГЭРБ.
» data-medium-file=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/10/Гастроэзофагеальный-рефлюкс.jpg?fit=440%2C300&ssl=1″ data-large-file=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/10/Гастроэзофагеальный-рефлюкс.jpg?fit=806%2C550&ssl=1″ loading=»lazy» src=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/10/%D0%93%D0%B0%D1%81%D1%82%D1%80%D0%BE%D1%8D%D0%B7%D0%BE%D1%84%D0%B0%D0%B3%D0%B5%D0%B0%D0%BB%D1%8C%D0%BD%D1%8B%D0%B9-%D1%80%D0%B5%D1%84%D0%BB%D1%8E%D0%BA%D1%81.jpg?resize=900%2C614&ssl=1″ alt=»Гастроэзофагеальный рефлюкс» width=»900″ height=»614″ srcset=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/10/Гастроэзофагеальный-рефлюкс.jpg?w=900&ssl=1 900w, https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/10/Гастроэзофагеальный-рефлюкс.jpg?resize=440%2C300&ssl=1 440w, https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/10/Гастроэзофагеальный-рефлюкс.jpg?resize=806%2C550&ssl=1 806w, https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/10/Гастроэзофагеальный-рефлюкс.jpg?resize=768%2C524&ssl=1 768w» sizes=»(max-width: 900px) 100vw, 900px» data-recalc-dims=»1″/> Гастроэзофагеальный рефлюкс
Этиология: новый подход
Согласно преобладающей теории (с 1935 г.), ГЭРБ возникает, когда кислый желудочный сок выливается из желудка в пищевод, химически и механически повреждая слизистую оболочку пищевода, вызывая ее ожоги, раздражение, эрозии и, в конечном итоге, более серьезные последствия. Однако эта традиционная теория химического и механического раздражения слизистой оболочки пищевода не может полностью объяснить многие вещи, связанные с началом, симптомами и течением ГЭРБ.
В настоящее время появились сообщения о том, что ГЭРБ может быть иммунным воспалительным заболеванием, вызванным иммунными реакциями, а не прямым химическим повреждением слизистой оболочки пищевода желудочным соком. Гипотеза об этиологии иммунной ГЭРБ подтверждается одним из клинических исследований, проведенных в США. Результаты исследования были опубликованы в журнале American Medical Ассоциация.
Предварительные данные этого исследования показали, что Т-лимфоцитарный эзофагит, гиперплазия базальных клеток и клеток селезенки наблюдались у пациентов с тяжелой ГЭРБ, эффективно лечившихся ингибиторами протонной помпы (ИПП) после отмены ИПП, но с устойчивыми поверхностными клетками.
По словам руководителя исследования из Далласского медицинского центра ветеранов д-ра. Керри Данбар, это открытие предполагает, что патогенез рефлюксной болезни может быть связан больше с медиаторами воспаления и цитокинами, чем с химическим повреждением слизистой оболочки пищевода.
Воспалительная иммунная теория ГРЭБ могла бы легче и лучше объяснить не только начало и течение типичных симптомов этого заболевания, но и патофизиологию осложнений этойпатологии — метаплазию пищевода и слизистой оболочки Барретта.
» data-medium-file=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/10/Пищевод-Барретта.jpg?fit=450%2C259&ssl=1″ data-large-file=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/10/Пищевод-Барретта.jpg?fit=900%2C517&ssl=1″ loading=»lazy» src=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/10/%D0%9F%D0%B8%D1%89%D0%B5%D0%B2%D0%BE%D0%B4-%D0%91%D0%B0%D1%80%D1%80%D0%B5%D1%82%D1%82%D0%B0.jpg?resize=900%2C517&ssl=1″ alt=»Пищевод Барретта» width=»900″ height=»517″ srcset=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/10/Пищевод-Барретта.jpg?w=900&ssl=1 900w, https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/10/Пищевод-Барретта.jpg?resize=450%2C259&ssl=1 450w, https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/10/Пищевод-Барретта.jpg?resize=768%2C441&ssl=1 768w» sizes=»(max-width: 900px) 100vw, 900px» data-recalc-dims=»1″/> Пищевод Барретта
Недавние экспериментальные исследования на крысах также предполагают, что ГЭРБ более связана с иммунным, а не химическим кислотным поражением слизистой оболочки пищевода. Считается, что рефлюкс и химическое кислотное раздражение только инициируют иммунные воспалительные реакции в слизистой оболочке пищевода и, следовательно, играют менее важную роль.
Если иммуно-воспалительная теория этиопатогенеза ГЭРБ окажется верной, возможно, потребуется пересмотреть существующий режим лечения и профилактики рецидивов ГЭРБ. Не исключено, что расположение и роль антисекреторных препаратов (ИПП, блокаторы H2) могут измениться.
Предполагается, что иммунная теория рефлюксной болезни может более подробно объяснить причины и сущность не только типичных, но и недавно описанных атипичных форм (так называемых подтипов) ГЭРБ.
Исследователи предполагают, что ИПП и блокаторы H2 могут оставаться наиболее важными препаратами для лечения ГЭРБ, но схема лечения этого заболевания также должна включать препараты, влияющие на каскад иммунно-воспалительного ответа, особенно для более тяжелых и рефрактерных форм ГЭРБ.
Лечение гастроэзофагеальной рефлюксной болезни
Согласно действующим руководствам, ГЭРБ лечится поэтапно. Цель лечения: контролировать симптомы заболевания, лечить эзофагит, предотвращать рецидивы эзофагита и осложнения заболевания.
Лечение ГЭРБ состоит из следующих этапов:
Немедикаментозные меры предполагают следующее:
Частое питание через равные промежутки времени
» data-medium-file=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/10/Частое-питание-через-равные-промежутки-времени.jpg?fit=450%2C300&ssl=1″ data-large-file=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/10/Частое-питание-через-равные-промежутки-времени.jpg?fit=825%2C550&ssl=1″ loading=»lazy» src=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/10/%D0%A7%D0%B0%D1%81%D1%82%D0%BE%D0%B5-%D0%BF%D0%B8%D1%82%D0%B0%D0%BD%D0%B8%D0%B5-%D1%87%D0%B5%D1%80%D0%B5%D0%B7-%D1%80%D0%B0%D0%B2%D0%BD%D1%8B%D0%B5-%D0%BF%D1%80%D0%BE%D0%BC%D0%B5%D0%B6%D1%83%D1%82%D0%BA%D0%B8-%D0%B2%D1%80%D0%B5%D0%BC%D0%B5%D0%BD%D0%B8.jpg?resize=900%2C600&ssl=1″ alt=»Частое питание через равные промежутки времени» width=»900″ height=»600″ srcset=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/10/Частое-питание-через-равные-промежутки-времени.jpg?w=900&ssl=1 900w, https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/10/Частое-питание-через-равные-промежутки-времени.jpg?resize=450%2C300&ssl=1 450w, https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/10/Частое-питание-через-равные-промежутки-времени.jpg?resize=825%2C550&ssl=1 825w, https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/10/Частое-питание-через-равные-промежутки-времени.jpg?resize=768%2C512&ssl=1 768w» sizes=»(max-width: 900px) 100vw, 900px» data-recalc-dims=»1″/> Частое питание через равные промежутки времени
Медикаментозное лечение
Для лечения ГЭРБ используются несколько групп препаратов:
Антациды
До 1980-х годов антациды были стандартным средством лечения легкой формы ГЭРБ. Они по-прежнему используются для уменьшения симптомов легкого рефлюкса. Антациды принимают после каждого приема пищи и перед сном.
Прием антацидов перед сном
Прием антацидов перед сном
» data-medium-file=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/10/Прием-антацидов-перед-сном.jpg?fit=450%2C300&ssl=1″ data-large-file=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/10/Прием-антацидов-перед-сном.jpg?fit=825%2C550&ssl=1″ loading=»lazy» src=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/10/%D0%9F%D1%80%D0%B8%D0%B5%D0%BC-%D0%B0%D0%BD%D1%82%D0%B0%D1%86%D0%B8%D0%B4%D0%BE%D0%B2-%D0%BF%D0%B5%D1%80%D0%B5%D0%B4-%D1%81%D0%BD%D0%BE%D0%BC.jpg?resize=900%2C600&ssl=1″ alt=»Прием антацидов перед сном» width=»900″ height=»600″ srcset=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/10/Прием-антацидов-перед-сном.jpg?w=900&ssl=1 900w, https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/10/Прием-антацидов-перед-сном.jpg?resize=450%2C300&ssl=1 450w, https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/10/Прием-антацидов-перед-сном.jpg?resize=825%2C550&ssl=1 825w, https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/10/Прием-антацидов-перед-сном.jpg?resize=768%2C512&ssl=1 768w» sizes=»(max-width: 900px) 100vw, 900px» data-recalc-dims=»1″/> Прием антацидов перед сном
Антациды также полезны при побочных эффектах: они облегчают запор (алюминиевые антациды: ALternaGEL, Amphojel), могут усиливать жидкий стул (магниевые антациды: Phillips Milk of Magnesia). Гидроксид алюминия увеличивает pH содержимого желудка до >4 и подавляет протеолитическую активность пепсина, уменьшает симптомы расстройства желудка. Антациды не снижают частоту рефлюкса, но снижают кислотность текучего содержимого.
Гидроксид магния подавляет симптомы ацидоза, улучшает пищеварение. Антациды гидроксида магния осмотически задерживают жидкости в кишечнике, что растягивает стенки кишечника, стимулирует перистальтику кишечника и смягчает стул (слабительный эффект). При взаимодействии с соляной кислотой желудочного сока гидроксид магния превращается в хлорид магния.
Новые антациды и антирефлюксанты
Соли альгиновой кислоты используются в клинической практике для облегчения симптомов изжоги и эзофагита более 30 лет. Соли альгиновой кислоты обладают своеобразным механизмом действия: при взаимодействии с желудочной кислотой альгинаты выпадают в осадок и образуют гель, который покрывает слизистую пищевода защитным слоем и способствует ее восстановлению.
Исследования in vitro и in vivo показали, что альгинаты сочетают в себе углекислый газ и некоторые антацидные компоненты. Недавние кинетические исследования показали, что альгинаты обходят кислое содержимое и достигают пищевода раньше, чем содержимое пищевода, защищая слизистую оболочку органа от механического и химического раздражения соляной кислотой. Согласно клиническим исследованиям, альгинаты также действуют как физический барьер, тем самым более активно подавляя рефлюкс.
Альгинатные препараты содержат антациды, нейтрализующие кислоты, уменьшающие изжогу, но исследования не показали, что эффективность этих комбинированных препаратов зависит от их нейтрализующих свойств.
Клиническая эффективность альгинатных препаратов зависит от многих факторов: количества и проникновения выделяемого углекислого газа, особенностей молекулы, дополнительных ингредиентов (алюминий, кальций), обладающих положительным потенцирующим действием.
Альгинатные препараты остаются в желудке в течение нескольких часов, поэтому они действуют значительно дольше и более эффективны в подавлении симптомов ГЭРБ, чем традиционные антациды, они начинают действовать быстро и действуют долго. Альгинатные препараты полностью безопасны и поэтому используются для уменьшения симптомов рефлюкса у младенцев, детей и беременных женщин.
Например, один из таких п репаратов альгината магния Refluxaid применяется в европейских странах для уменьшения симптомов рефлюкса и ацидоза при ГЭРБ, язвенной болезни, эзофагите, функциональной диспепсии, других функциональных и воспалительных заболеваниях желудочно-кишечного тракта, проявляющихся изжогой, рефлюксом, дискомфортом в эпигастрии.
» data-medium-file=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/10/Препарат-Refluxaid.jpg?fit=434%2C300&ssl=1″ data-large-file=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/10/Препарат-Refluxaid.jpg?fit=796%2C550&ssl=1″ loading=»lazy» src=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/10/%D0%9F%D1%80%D0%B5%D0%BF%D0%B0%D1%80%D0%B0%D1%82-Refluxaid.jpg?resize=900%2C622&ssl=1″ alt=»Препарат Refluxaid» width=»900″ height=»622″ srcset=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/10/Препарат-Refluxaid.jpg?w=900&ssl=1 900w, https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/10/Препарат-Refluxaid.jpg?resize=434%2C300&ssl=1 434w, https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/10/Препарат-Refluxaid.jpg?resize=796%2C550&ssl=1 796w, https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/10/Препарат-Refluxaid.jpg?resize=768%2C531&ssl=1 768w» sizes=»(max-width: 900px) 100vw, 900px» data-recalc-dims=»1″/> Препарат Refluxaid
Альгинат магния в Rexluxaid — это натуральное вещество, извлеченное из морских водорослей. Препарат обладает высокой вязкостью, что увеличивает антирефлюксную эффективность и продолжительность действия. Обладает эмульсионными и набухающими свойствами.
Исследования показали, что высоковязкое соединение Refluxaid при попадании в желудок создает физический барьер, который связывает и нейтрализует желудочный сок, тем самым защищая пищевод от симптомов рефлюкса: изжоги, жжения за грудиной, боли в груди, дискомфорта в эпигастрии и т. д. Прием подобных лекарств ослабляет изжогу, срыгивание кислоты, уменьшается дисфагия и одинофагия (затруднение при глотании и болезненность), также подавляются экстразофагинитные симптомы ГЭРБ — кашель, охриплость голоса.
Refluxaid — это лекарство, отпускаемое по рецепту. Оно используется для эпизодического уменьшения симптомов ацидоза, рефлюкса и эзофагита, по запросу или в сочетании с антирефлюксными лекарствами (антисекреторными ИПП, блокаторами H2, прокинетиками).
Было обнаружено, что когда человек спит, альгинат магния может оставаться в желудке до 8 часов без разрушения — достаточно времени для пациента, чтобы хорошо выспаться. Прием рефлюкса перед сном может улучшить качество сна у пациента с ГЭРБ, поскольку симптомы, вызванные ночным рефлюксом, будут подавлены.
Антисекреторные препараты, блокаторы Н2-рецепторов
Это лечение первой линии при ГЭРБ легкой и средней степени тяжести и эзофагите I-II степени. В клинической практике обычно используются четыре блокатора H2: ранитидин, фамотидин, циметидин и низатидин. Они более эффективны в подавлении нестимулированной секреции желудочного сока с пищей и поэтому рекомендуются «натощак» или на ночь.
Н2-блокаторы эффективны при лечении легкого эзофагита (70-80% пациентов выздоравливают), а также в антирецессивном лечении и профилактике рецидивов. Эффективность блокаторов H2 снижается при длительном применении, что приводит к тахифилаксии. Блокатор H2 рекомендуется для пациентов, страдающих ночными симптомами рефлюкса, особенно в виске Барретта.
Ингибиторы протонной помпы (ИПП)
Это сильнейшие препараты, подавляющие желудочную секрецию. Клинические исследования показали, что они наиболее эффективны при лечении ГЭРБ. ИПП обычно хорошо переносятся, вызывая относительно мало побочных эффектов. Однако ИПП могут нарушать гомеостаз кальция, усугубляя существующие нарушения сердечной проводимости. ИПП повышают риск переломов бедренной кости у женщин в постменопаузе.
На основании множества клинических испытаний были сделаны выводы, что ИПП более эффективны, чем блокаторы H2, в контроле симптомов ГЭРБ в течение 4 недель. И более эффективны при лечении эзофагита в течение 8 недель. Также сообщается, что не обнаружено, что какой-либо препарат PSI более эффективен, чем другие, в борьбе с симптомами ГЭРБ в течение 8 недель.
Хотя ИПП являются наиболее эффективными антисекреторными препаратами, их применение, особенно в течение длительного периода времени, связано со многими побочными эффектами. Во-первых, у ИПП есть ограничения по применению: их нельзя применять детям до 1 года, беременным и кормящим женщинам. Было показано, что использование ИПП во время беременности увеличивает риск врожденных дефектов (пороков сердца).
Ограничения по применению ИПП
Ограничения по применению ИПП
» data-medium-file=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/10/Ограничения-по-применению-ИПП.jpg?fit=450%2C300&ssl=1″ data-large-file=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/10/Ограничения-по-применению-ИПП.jpg?fit=825%2C550&ssl=1″ loading=»lazy» src=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/10/%D0%9E%D0%B3%D1%80%D0%B0%D0%BD%D0%B8%D1%87%D0%B5%D0%BD%D0%B8%D1%8F-%D0%BF%D0%BE-%D0%BF%D1%80%D0%B8%D0%BC%D0%B5%D0%BD%D0%B5%D0%BD%D0%B8%D1%8E-%D0%98%D0%9F%D0%9F.jpg?resize=900%2C600&ssl=1″ alt=»Ограничения по применению ИПП» width=»900″ height=»600″ srcset=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/10/Ограничения-по-применению-ИПП.jpg?w=900&ssl=1 900w, https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/10/Ограничения-по-применению-ИПП.jpg?resize=450%2C300&ssl=1 450w, https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/10/Ограничения-по-применению-ИПП.jpg?resize=825%2C550&ssl=1 825w, https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/10/Ограничения-по-применению-ИПП.jpg?resize=768%2C512&ssl=1 768w» sizes=»(max-width: 900px) 100vw, 900px» data-recalc-dims=»1″/> Ограничения по применению ИПП
Исследования, проведенные в США, показывают, что чрезмерное использование ИПП имеет опасные последствия. Поэтому FDA США предупреждает врачей и пациентов о том, что в год не должно быть более трех 14-дневных курсов лечения. Длительное или частое использование ИПП связано с повышенным риском переломов костей, гиповитаминоза B12, электролитного дисбаланса (в первую очередь гипомагниемии), мышечных спазмов и даже судорог.
Чрезмерное подавление секреции желудочного сока при приеме ИПП может вызвать дискомфорт в эпигастрии, расстройство желудка, усиление кишечных инфекций (C. difficile и др.), Риск аспирационной пневмонии. Риск инфекционных осложнений еще выше, когда ИПП используются с блокаторами Н2-рецепторов.
Прокинетики
Прокинетики эффективны только при лечении легкой формыГЭРБ. Если ГЭРБ протекает тяжелее, помимо прокинетиков обычно назначают препараты, угнетающие секрецию желудочного сока.
Из прокинетиков в Европейских клиниках назначают метоклопрамид (10 мг/день перорально) — это наиболее часто назначаемая схема у взрослых с ГЭРБ. Длительное лечение прокинетиками может быть опасным, с серьезными, даже со смертельным исходом, осложнениями.
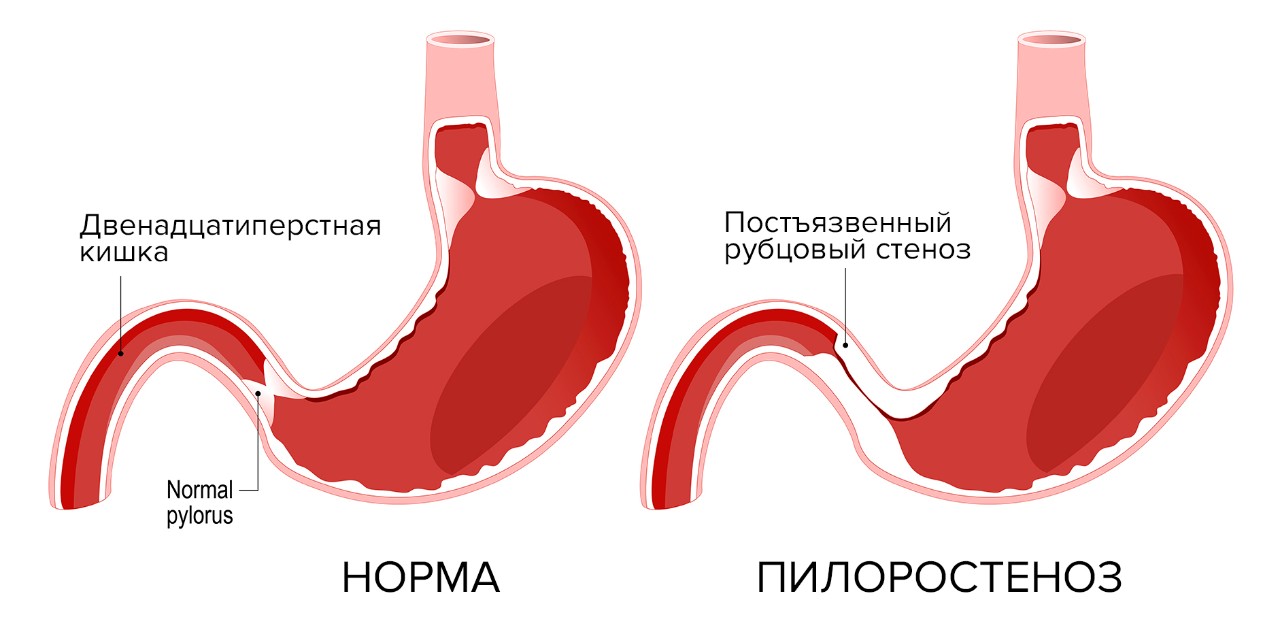
Пилоростеноз (высокая желудочно-кишечная непроходимость)
Главная угроза – полная невозможность прохождения пищи из желудка в нижележащие отделы ЖКТ и развитие истощения.
Постъязвенный рубцовый стеноз привратника (пилоростеноз) или двенадцатиперстной кишки – осложнение язвенной болезни выходного отдела желудка (пилорического отдела) или луковицы двенадцатиперстной кишки. На месте зажившей язвы образуется рубец, ткань в области рубца стягивается, прохождение пищи из желудка в двенадцатиперстную кишку затрудняется. Это место постоянно травмируется пищевыми массами, на него воздействует соляная кислота. Возникает хроническое воспаление, зона сужения прогрессирует, проход становится ещё уже. Затем развивается декомпенсация: пища проходит с большим трудом, желудок расширяется и теряет свою перистальтическую функцию. У пациентов с признаками декомпенсированной дуоденальной непроходимости желудок может достигать огромных размеров, пища перестает проходить дальше в кишку, процесс пищеварения останавливается. Возникает истощение.
Язва проявляется болями в брюшной полости. Это могут быть голодные боли или боли после еды. Сужение выходного отдела желудка проявляет себя тошнотой и чувством переполнения желудка после приёма пищи. В норме человек должен просыпаться утром с чувством голода, но пациент с высокой непроходимостью просыпается с чувством переполнения желудка. Декомпенсация стеноза характеризуется рвотой пищей, съеденной за 2-3 часа до этого. Декомпенсация – угрожающее жизни состояние, следует незамедлительно обратиться к врачу.
Для того, чтобы диагностировать постъязвенный рубцовый стеноз выходного отдела желудка, применяются компьютерная томография с водорастворимым контрастом и рентгенологическое исследование с водорастворимым контрастом или с барием. Чтобы понять, через какое время у пациента происходит эвакуация содержимого желудка в нижележащие отделы ЖКТ, врач даёт пациенту барий, делает рентгеновский снимок, и видит, куда барий распространился. Затем снимки делаются через 3, 6, 12 часов – это позволяет оценить динамику прохождения контраста и степень стеноза. В Ильинской больнице пациентам с подозрением на высокую кишечную непроходимость всегда выполняется эндоскопическая диагностика: с помощью эндоскопа врач точно локализует место стриктуры и определяет объем хирургической помощи.
Источник изображения: Designua / Shutterstock
Если степень желудочно-кишечной непроходимости не позволяет провести баллонную дилатацию, но серьёзной формы декомпенсации еще нет – хирурги Ильинской больницы выполняют пациенту лапароскопическую операцию – пилоропластику. Через небольшие разрезы на брюшной стенке (размером около 10 мм) в брюшную полость вводятся лапароскоп и хирургические манипуляторы. Одновременно через рот в просвет желудка вводится эндоскоп. С помощью лапароскопических инструментов хирург рассекает суженную зону двенадцатиперстной кишки и выходного отдела желудка в продольном направлении, а сшивает в поперечном, тем самым значительно расширяя место сужения и разрешая непроходимость. Второй хирург ассистирует ему из просвета желудка с помощью эндоскопа, обеспечивая максимальную безопасность манипуляций. Это малотравматичная операция, дающая устойчивый положительный эффект.
Современное представление о моторно-эвакуаторных нарушениях верхнего отдела желудочно-кишечного тракта (обзор литературы)
Нарушения моторно-эвакуаторной функции верхнего отдела желудочно-кишечного тракта приводят к часто встречающимся симптомам, таким как вздутие живота, тяжесть после приема пищи, изжога, тошнота и рвота. Это большинство случаев обращения больных к врачу, ос
Disorders in motor-evacuation function of the upper section of the gastrointestinal tract lead to frequent symptoms such as bloating, weight after a meal, heartburn, nausea and vomiting. These are the most common cases when patients go to see the doctor, especially in out-patient conditions.
Нарушения двигательной функции пищеварительного тракта являются актуальной проблемой современной медицины.
Эпидемиология
Часто встречающиеся симптомы гастроэнтерологических заболеваний, такие как отрыжка, изжога, тошнота, рвота, потеря аппетита, чувство раннего насыщения, тяжесть в эпигастрии, вздутие живота, возникают вследствие нарушений моторики. Данные нарушения могут носить первичный характер (функциональный) или вторичный (на фоне органических заболеваний) [1–3].
По данным некоторых авторов, от диспептических проявлений страдает от 25% до 40% лиц в популяции, а количество обращений с жалобами на диспепсию составляет около 5–7% всех обращений к врачам первичной помощи [4, 6–9]. У 18–50% обследованных при эндоскопическом исследовании обнаруживают моторные нарушения [1, 5, 23–25].
Моторно-эвакуаторная функция верхнего отдела пищеварительного тракта с точки зрения физиологии
Вне акта глотания пищевод представляет собой тонически напряженную мышечную трубку, не имеющую просвета. В акте глотания принимают участие более 20 мышц, синхронизированных между собой и деятельностью дыхательной системы. Проглатывание пищи представляет собой активную строго координированную деятельность сфинктеров и стенки пищевода. Поступление пищевого комка в просвет пищевода происходит при расслаблении верхнего пищеводного сфинктера. Задержка этого расслабления даже на 250 миллисекунд приводит к тяжелейшим случаям аспирационных пневмоний. После поступления пищи в пищевод инициируется первичная перистальтическая волна. Она движется по пищеводу со скоростью 2–4 см в секунду и проходит весь пищевод за 8–12 секунд. Причем сокращению стенки предшествует ее расслабление [3–5]. Холинергическая стимуляция на некоторое время тормозит собственную активность мускулатуры пищевода, поддерживающую его тонус. Затем после прекращения этой стимуляции стенка интенсивно сокращается. Через полсекунды после глотка начинается расслабление нижнего пищеводного сфинктера, которое длится от 7 до 12 секунд. За это время пища проходит в желудок. Если в пищеводе остается какое-то количество пищи, возникает вторичная перистальтическая волна, которая эти остатки удаляет. Нижний пищеводный сфинктер плотно закрывается каждый раз после прохождения пищи, препятствуя рефлюксу желудочного содержимого в пищевод. В дальнейшем он может время от времени расслабляться для удаления из желудка избытка воздуха. В том случае, когда количество этих эпизодов транзиторного расслабления превышает нормальное, развивается недостаточность сфинктера и появляются изжога, отрыжка, срыгивания. Двигательная активность желудка начинается с момента прохождения комка пищи через нижний пищеводный сфинктер [3, 6–8]. Моторика желудка осуществляется за счет сокращений гладких мышц средней оболочки его стенки. Тело и дно желудка обеспечивают депонирование, перетирание и перемешивание пищи; привратник осуществляет порционную эвакуацию химуса в 12-перстную кишку (ДПК).
Виды моторики желудка: тонические сокращения — длительное напряжение мышц разных отделов желудка; перистальтика — волнообразные сокращения дна и тела желудка, служат для перемешивания и продвижения содержимого желудка; распространяются от кардиальной части к пилорической (в кардиальной части расположены гладкомышечные клетки-водители ритма, обладающие автоматией); антральная систола — мощное сокращение антрального отдела желудка, распространяющееся в сторону тонкой кишки; играет главную роль в эвакуации пищи в ДПК [3, 9–12].
Режимы моторики желудка: «голодная моторика» — до приема пищи — включает в себя тонические сокращения (в пустом желудке стенки соприкасаются) и редкие перистальтические волны; рецептивная релаксация — расслабление желудка, возникающее при раздражении рецепторов ротовой полости и особенно после попадания первых порций пищи в желудок; создает резервуар для дальнейшего приема пищи; «сытая моторика» — после приема пищи — усиление тонуса и перистальтики, периодическое возникновение антральной систолы [13–15].
Поступление пищевого комка в желудок сопровождается рецептивным расслаблением дна и проксимальной части тела желудка. Рецептивное расслабление возникает при проглатывании любого количества пищи. В дальнейшем в зависимости от объема съедаемой пищи и выпиваемой жидкости начинается адаптивное расслабление дна и тела желудка. Назначение адаптивного расслабления — сохранить примерно постоянное давление в просвете органа независимо от объема пищи. В дистальной части тела и антральном отделе появляются интенсивные перистальтические волны, которые перемешивают содержимое и приводят к его измельчению. Подобные интенсивные сокращения возникают каждые 20 секунд. После прохождения по антруму перистальтические сокращения появляются в ДПК. Волны перистальтики в ДПК, слабые вначале, усиливаются при поступлении желудочного содержимого через пилорический сфинктер. Поступление происходит порциями, содержащими очень маленькие кусочки пищи. При этом именно эти порции активируют перистальтику ДПК. В ней поступающий химус смешивается с желчью, соком поджелудочной железы благодаря перистальтическим сокращениям. Эти перистальтические волны возникают координированно с деятельностью антропилорической зоны. Такая синхронизированная деятельность называется антродуоденальной координацией [14, 25–27].
В организации двигательной активности желудка непосредственную роль играют ионы кальция. Увеличение содержания Са 2+ ведет к сокращению, а снижение — к релаксации миоцита. Существует два основных пути поступления ионов Са 2+ в клетку: из внеклеточного пространства по медленным кальциевым каналам мембран, что приводит к тоническому сокращению и высвобождению Са 2+ из внутриклеточных депо, что вызывает фазовое сокращение. Стимуляция ацетилхолином мускариновых рецепторов способствует открытию натриевых каналов и входу Na+ в клетку, что сопровождается деполяризацией мембраны, открытием потенциалзависимых кальциевых каналов и проникновением Са 2+ внутрь клетки. Увеличение концентрации Са 2+ приводит к образованию комплекса кальций–кальмодулин, фосфорилированию миозина и сокращению миоцита. Снижение тонуса и сократительной активности миоцита происходит преимущественно при активизации симпатической нервной системы и стимуляции норадреналином a1-адренорецепторов, ассоциированных с депо Са 2+ на поверхности клетки, которое постоянно пополняется из внеклеточной среды. При этом происходит мобилизация Са 2+ из депо и открытие калиевых каналов. Последующий отток ионов К + вызывает закрытие кальциевых каналов, гиперполяризацию клеточной мембраны и релаксацию миоцита. Снижению концентрации Са 2+ внутри клетки (и соответственно расслаблению) способствует увеличение содержания внутриклеточного циклического аденозинмонофосфата (цАМФ), стимуляция его выхода цГМФ-зависимой протеинкиназой и активный транспорт Са 2+ при помощи кальциевого насоса — кальциевой АТФазы на внутренней поверхности мембраны. Роль ионов Са 2+ в регуляции основных функций желудка огромна. Они участвуют в процессах кислотообразования, синтезе и выделении протеаз, пролиферации желудочного эпителия, во всех компонентах желудочной моторики [16–20].
Нарушение каждого из компонентов двигательной активности пищевода, желудка может приводить к появлению соответствующей клинической симптоматики. Клинические проявления при замедленном опорожнении желудка: чувство тяжести и переполнения в эпигастрии после еды, эпигастральная боль, изжога, тошнота и рвота, чувство быстрого насыщения, сонливость после еды, отрыжка и регургитация, потеря веса. Клинические проявления при ускоренном опорожнении желудка: эпигастральная боль, тошнота, спазматические боли в животе, диарея, симптомы гипогликемии, симптомы гиповолемии. Нарушение рецептивного и адаптивного расслабления желудка вызывает чувство раннего насыщения, в ряде случаев тошноту и рвоту. Вследствие нарушения антродуоденальной координации появляются тяжесть в эпигастрии, вздутие живота, изжога, отрыжка, срыгивания [7, 21, 22, 28].
Регуляция моторно-эвакуаторных нарушений
1. Миогенная — за счет собственных свойств гладкомышечных клеток стенки желудка:
2. Нервная — осуществляется рефлекторно при раздражении рецепторов полости рта, пищевода, желудка, тонкой кишки:
3. Гуморальная — моторная функция желудочно-кишечного тракта (ЖКТ) у человека контролируется в основном гормонами, такими как гастрин, мотилин, панкреатический полипептид, секретин, холецистокенин и соматостатин. После приема пищи отмечается кратковременное повышение уровня мотилина и соматостатина в сыворотке крови, увеличение концентрации панкреатического полипептида при умеренном увеличении концентрации гастрина. Усиливает моторную функцию гастрин, тормозят секретин, холецистокенин. Несомненно, что в поддержании моторной деятельности ЖКТ, наряду с гормональной регуляцией, большое место занимает и нервная регуляция. Секреция мотилина, в свою очередь, регулируется нервной системой, и поэтому взаимодействие гуморальной и нервной регуляции — основное условие нормальной функции ЖКТ [3, 29–31].
Контроль продвижения пищи по желудочно-кишечному тракту осуществляется миогенной, нервной и гуморальной типами регуляции. Мышечная оболочка стенки пищеварительного тракта состоит из наружного продольного и внутреннего циркулярного мышечных слоев. Между ними располагается межмышечное нервное сплетение [30]. Снаружи органа к межмышечному нервному сплетению подходит экстрамуральная иннервация. Она представлена парасимпатической и симпатической частями. Согласованная, координированная деятельность парасимпатического и симпатического звеньев нервной регуляции создает условия для нормальной перистальтики. В парасимпатической системе контроль осуществляется через блуждающий нерв, который берет начало в продолговатом мозге. Волокна парасимпатической нервной системы приходят к ганглиям межмышечного нервного сплетения, инициируется так называемая первичная перистальтика пищевода, а затем открытие нижнего пищеводного сфинктера, рецептивное и адаптивное расслабление желудка. В адренергической системе контроль осуществляется через симпатические волокна, берущие начало в центрах спинного мозга. При этом симпатическая система уменьшает давление в нижнем пищеводном сфинктере, а также угнетает перистальтические движения тела желудка и его антрального отдела. В то же время двигательная активность может определяться самостоятельным функционированием межмышечного нервного сплетения, даже без участия вагусной регуляции [4, 31].
Характеристика моторно-эвакуаторных нарушений
Основные виды нарушений перистальтики желудка и ДПК хорошо известны. Однако, рассматривая изменения двигательно-эвакуаторной функции, необходимо разграничивать нарушение тонуса желудка, ДПК, работы сфинктерного аппарата (гипо- или атония, гипертонус или спазм, дисмоторика, при которой расстроена координация сократительной активности) и эвакуации (замедление или ускорение эвакуации, гастро- или дуоденостаз, ретроградная перистальтика, рефлюксы) [2, 14]. Данные нарушения могут сочетаться между собой в различных комбинациях. Так, например, спазм привратника может сочетаться с дуоденостазом и замедлением эвакуации при нормальной сократительной активности желудка, а снижение тонуса желудка — с повышенной сократительной активностью ДПК, дуоденогастральным рефлюксом и нормальной эвакуацией; дисфункция или спазм сфинктера Одди — с нормальной двигательно-эвакуаторной функцией желудка и ДПК [2, 5, 13, 16].
Характерные клинические проявления при замедленном опорожнении желудка: чувство тяжести и переполнения в эпигастрии после еды, эпигастральная боль, изжога, тошнота и рвота, чувство быстрого насыщения, сонливость после еды, отрыжка и срыгивания, потеря веса.
Основные причины задержки опорожнения желудка: функциональная диспепсия (дисмоторный вариант), кислотозависимые заболевания (пептические язвы, гастроэзофагеальная рефлюксная болезнь), гастриты (атрофический гастрит, антральный гастрит типа В), механические причины (рак желудка, препилорические, пилорические, дуоденальные язвы, идиопатический гипертрофический стеноз), метаболические расстройства (гиперкалиемия, гиперкальциемия), последствия оперативного лечения заболеваний желудка, лекарства (антихолинергические, опиаты, L-допа, трициклические антидепрессанты, соматостатин, холецистокинин, гидроокись алюминия, прогестерон), высокие дозы алкоголя, никотин; тяжелая физическая нагрузка [2, 20].
Характерные клинические проявления при ускоренном опорожнении желудка: эпигастральная боль, тошнота, спазматические боли в животе, диарея, симптомы гипогликемии, симптомы гиповолемии.
Основные причины ускорения опорожнения желудка: последствия оперативного лечения заболеваний желудка (демпинг-синдром, ваготомия с пилоропластикой), лекарства (эритромицин, цизаприд, метоклопрамид, домперидон), легкие физические упражнения [20].
Канадский ученый M. Horowitz и соавт. (2001) впервые выделяет атрофический гастрит, изменение слизистой и гастроэзофагеальный рефлюкс среди факторов, служащих причиной хронического замедления желудочной эвакуации [2, 21].
Особое внимание исследователи уделяют роли инфекционного агента Нelicobacter pylori (Hp) в развитии желудочной дисмоторики, поскольку в 30–89% случаев гастрит, выявляемый при обследовании пациентов с моторно-эвакуаторными расстройствами, ассоциируется с данной инфекцией [7, 8]. Тем не менее роль этой инфекции в развитии желудочной дисмоторики еще нуждается в дальнейшем изучении, так как выводы исследований по изучению этого вопроса довольно противоречивы [9]. В пользу Hp свидетельствуют данные об улучшении клинической симптоматики и качества жизни у пациентов после проведения эрадикационной терапии, что позволило рекомендовать ее проведение в Маастрихтском консенсусе-4 (2011) у пациентов обозначенной группы. Но непосредственно проведенные исследования эвакуаторной функции желудка у пациентов с признаками диспепсии не выявили достоверной зависимости показателей моторики желудка от наличия Hp [9].
Дуоденогастральный рефлюкс (ДГР), клиническими признаками которого являются эпигастральная боль и дискомфорт, отрыжка воздухом, также является важной клинической проблемой. В целом наличие ДГР определяют у 70% пациентов с диспептическими жалобами [9]. В развитии ДГР, как и при развитии замедленной желудочной эвакуации, значительная роль принадлежит нарушениям антродуоденальной координации и состоянию привратника, которые рассматриваются во взаимосвязи с состоянием нитрергической регуляции и дисбалансом гастроинтестинальных гормонов [8, 9, 19–21]. Некоторые авторы подчеркивают физиологическое значение ДГР, который по своему объему, продолжительности и регулярности не имеет признаков патологии. По их мнению, его возникновение после употребления жирной пищи способствует сохранению активности панкреатических ферментов, лучшему эмульгированию жиров [9]. Российские авторы отмечают физиологическую роль ДГР как фактора, регулирующего желудочную секрецию путем стимулирующего влияния на гастриновые рецепторы [29]. Тем не менее по другим данным повышение уровня гастрина способствует ослаблению моторной деятельности желудка и нарушению фаз сократительного цикла. Также выявлена связь структурной перестройки желудочной слизи с содержанием желчных кислот в желудке, а при эрозивных поражениях желудка под их влиянием происходит усиленный распад компонентов слизи [23]. Другие исследования свидетельствуют об ассоциации ДГР со структурной перестройкой слизистой оболочки желудка и развитием кишечной метаплазии, более высокой степенью колонизации тела желудка Hp [18, 24]. По данным российских ученых, на фоне ДГР любой степени выраженности чаще обнаруживают признаки антрального гастрита и эрозивные изменения [25]. Важными являются данные о мутагенном влиянии желчных кислот на слизистую оболочку желудка и пищевода [18, 26, 27].
Гастроэзофагеальный рефлюкс (ГЭР) — это хроническое рецидивирующее многосимптомное заболевание, обусловленное спонтанным, регулярно повторяющимся забросом в пищевод желудочного и/или дуоденального содержимого, приводящим к поражению нижнего отдела пищевода, проявляющееся изжогой, отрыжкой кислым, болью, жжением в эпигастральной области. Часто встречающееся проявление моторно-эвакуаторных нарушений [5]. Поскольку внутрибрюшное давление превышает внутригрудное, действует градиент давления, способствующий забросу содержимого желудка в пищевод, противостоит которому нижний пищеводный сфинктер. Несостоятельность последнего приводит к развитию патологического ГЭР, результат воздействия которого на слизистую оболочку пищевода определяется его составом (соляная кислота, пепсин, желчные кислоты), длительностью воздействия и собственной резистентностью слизистой оболочки. Помимо неэффективности нижнего пищеводного сфинктера, возникновению ГЭР способствует повышение внутрибрюшного (например, при ожирении, беременности) или внутрижелудочного давления (при желудочном или дуоденальном стазе функциональной или органической природы).
Коррекция моторно-эвакуаторных нарушений верхнего отдела желудочно-кишечного тракта
Коррекция нарушений моторики верхнего отдела ЖКТ сводится к решению трех задач:
Первопричиной функциональных нарушений чаще всего является нарушение нервной регуляции органов пищеварения, первая задача в этом случае должна решаться гастроэнтерологами в тесном контакте с невропатологами, психоневрологами и психологами после тщательного обследования пациента [5]. В случае первичной патологии органов пищеварения, например, при язвенной болезни, на первое место выходит лечение основного заболевания.
Вторая задача решается коррекцией питания, постуральной терапии и медикаментозными средствами. Для терапии пациентов с моторно-эвакуаторными нарушениями верхних отделов ЖКТ применяют лекарственные средства, регулирующие двигательную функцию — прокинетики, которые различаются между собой по механизму действия.
Прокинетики — препараты, усиливающие моторную активность органов пищеварительного тракта и препятствующие антиперистальтическим сокращениям гладкой мускулатуры [5, 15].
Стимулирующее влияние на моторику верхних отделов желудочно-кишечного тракта могут оказывать агонисты холинергических рецепторов (карбахолин, физостигмин), агонисты 5-НТ4-рецепторов (цизаприд, тегасерод), агонисты мотилиновых рецепторов (Эритромицин), антагонисты допаминовых рецепторов (метоклопрамид, домперидон) и др. Однако в реальной гастроэнтерологической практике карбахолин и физостигмин, а также Эритромицин (как прокинетик), цизаприд и тегасерод не применяются из-за выраженных нежелательных лекарственных реакций и развития осложнений. В настоящее время в качестве прокинетиков чаще всего применяются антагонисты допаминовых рецепторов, агонисты 5-НТ4-рецепторов и препарат с комбинированным механизмом действия — итоприда гидрохлорид (Ганатон) [5, 13].
Заключение
Таким образом, можно сделать вывод, что нарушение моторно-эвакуаторной функции верхних отделов пищеварительного тракта является важной медико-социальной проблемой современного общества. Предупреждение нарушения моторики и эвакуации способствует профилактике возникновения различной патологии со стороны желудочно-кишечного тракта.?
Литература
Е. А. Леушина 1
Е. Н. Чичерина, доктор медицинских наук, профессор
ГБОУ ВПО КГМА МЗ РФ, Киров