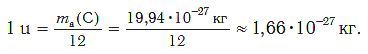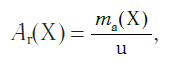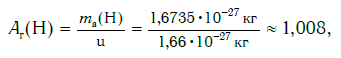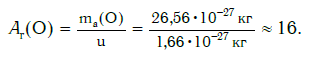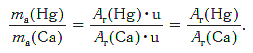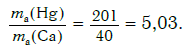Урок 2. Относительная атомная масса химических элементов
В уроке 2 «Относительная атомная масса химических элементов» из курса «Химия для чайников» рассмотрим разные способы выражения массы химических элементов. Напоминаю, что в прошлом уроке «Атомы и химические элементы» мы рассмотрели, кто и когда высказал идею о том, что все вокруг состоит из атомов; также выяснили, что из себя представляет химический элемент и каким образом обозначается.
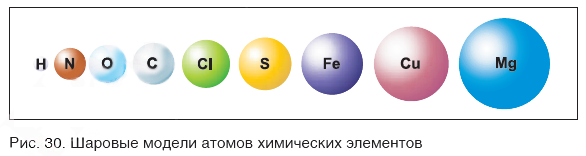
Чем различаются атомы разных элементов между собой? Вы уже знаете: массой, размерами и строением. На рисунке 30 показаны шаровые модели атомов некоторых химических элементов, конечно, не в реальных размерах, а многократно увеличенные. В действительности атомы настолько малы, что их невозможно рассмотреть даже в самые лучшие оптические микроскопы.
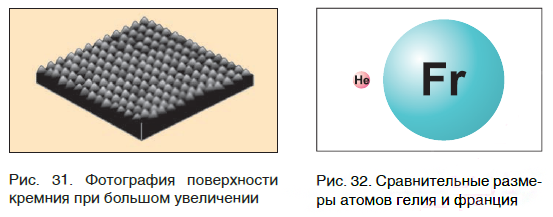
На заметку: В конце XX в. у ученых появились более совершенные микроскопы, позволяющие достигать увеличения в несколько десятков миллионов раз. Они называются туннельными микроскопами. На рисунке 31 показана фотография поверхности кремния. На ней отчетливо видны отдельные атомы, расположенные на поверхности этого вещества.
Размеры и масса атомов
Современная наука обладает методами, позволяющими определять размеры и массы атомов. Так, например, самый легкий атом — атом водорода. Его масса равна 0,0000000000000000000000000016735 кг. Самым маленьким является атом гелия He. Диаметр этого атома равен приблизительно 0,00000000098 м. Записывать и читать такие числа затруднительно, поэтому обычно их представляют в более удобном виде: 1,6735·10 −27 кг и 9,8·10 −10 м. Атомы большинства химических элементов по своим размерам значительно больше атома гелия. Самый большой из них — атом элемента франция Fr. Его диаметр в 7 раз больше диаметра атома гелия (рис. 32).
Еще больше различаются атомы разных элементов по массе. Масса атома обозначается символом ma и выражается в единицах массы СИ (кг). Так, например, масса атома углерода равна: ma(С) = 19,94·10 −27 кг, а атома кислорода — ma(О) = 26,56·10 −27 кг. Масса атома самого тяжелого из существующих на Земле элементов — урана U — почти в 237 раз больше массы атома водорода.
Атомная единица массы
Пользоваться такими маленькими величинами масс атомов при расчетах неудобно. К тому же, когда в XIX в. начало формироваться атомно- молекулярное учение, ученые еще не представляли реальных размеров и масс атомов. Поэтому на практике вместо истинных масс атомов стали применять их относительные значения. Они рассчитывались по массовым отношениям простых веществ в реакциях друг с другом. Химики предположили, что эти отношения пропорциональны массам соответствующих атомов. Именно так в начале XIX в. Дж. Дальтон ввел понятие относительной атомной массы, приняв за единицу сравнения массу самого легкого атома — водорода.
В настоящее время в качестве такой единицы сравнения используется 1/12 часть массы атома углерода (рис. 33). Она получила название атомной единицы массы (а. е. м.). Ее международное обозначение — u (от английского слова «unit» — единица):
Атомная единица массы — это 1/12 часть массы атома углерода, которая равна 1,66·10 −27 кг.
Относительная атомная масса
Сравнивая средние массы атомов различных элементов с атомной единицей массы, получают значения относительных атомных масс химических элементов.
Относительная атомная масса элемента — это физическая величина, которая показывает, во сколько раз масса атома данного химического элемента больше 1/12 части массы атома углерода.
Относительная атомная масса обозначается символами Ar ( А — первая буква английского слова «atomic» —атомный, r — первая буква английского слова «relative», что значит относительный), следовательно:
где Х — символ данного элемента.
Например, относительная атомная масса водорода:
В таблице Менделеева приведены относительные атомные массы всех элементов. В расчетах при решении задач мы будем пользоваться округленными до целых значениями этих величин (см. урок 1).
Внимание! Очень часто относительную атомную массу называют просто атомной массой. Однако следует отличать атомную массу — величину относительную (например, Ar(О) = 16) — от массы атома — величины, выражаемой в единицах массы — килограммах ( ma(O) = 26,56·10 −27 кг) или атомных единицах массы ( ma(O) = 16· u ).
Пример. Во сколько раз атом ртути тяжелее атома кальция?
Решение. Относительные атомные массы элементов равны: Ar(Hg) = 201 и Ar(Ca) = 40.
Масса атома ртути равна: ma(Hg) = Ar(Hg)·u (кг).
Масса атома кальция равна: ma(Са) = Ar(Са)·u (кг).
Другими словами, отношение масс атомов этих элементов равно отношению их относительных атомных масс. Следовательно, отношение масс атомов ртути и кальция равно:
Ответ: в 5,03 раза.
Краткие выводы урока:
Надеюсь урок 2 «Относительная атомная масса химических элементов» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии.
Относительная молекулярная масса – формула, примеры, таблица (химия, 8 класс)
Для химиков важно знать массы молекул исследуемых ими веществ. Измерять их в килограммах неудобно, поэтому ученые используют а. е. м. – атомные единицы массы.
Понятие атомной единицы массы
На сегодняшний день принята договоренность, что масса атома углерода (а точнее его изотопа углерод-12) в точности равна 12 а. е. м. По этой причине используемую химиками величину иногда называют углеродной единицей. Ранее ученые использовали другие единицы – водородную и кислородную, но они по ряду причин оказались неудобными. Опыты показывают, что 1 а. е. м. равна примерно 1,66•10 –27 кг.
Атомная масса показывает, какую массу имеет тот или иной атом. Найти ее можно в таблице Менделеева. Обычно в этой таблице масса записана как дробное число, очень близкое к какому-либо целому значению. Например, атомная масса водорода составляет 1,000797 а. е. м., у гелия она равна 4,0026 а. е. м., а у кислорода 15,9994 а. е. м. При решении практических задач принято округлять эти значения до целых чисел. То есть надо считать, что у водорода атомная масса равна 1 а. е. м, у гелия – 4 а. е. м., у кислорода – 16 а. е. м. Исключением является хлор, чью массу округляют до значения 35,5 а. е. м.
Важно понимать, что на самом деле у одного и того же элемента атомы могут иметь различную массу. Такие отличающиеся по массе атомы называются изотопами. У изотопов одного элемента одинаковое количество протонов, но различное количество нейтронов. При этом все изотопы одного элемента имеют одинаковые химические свойства.
В таблице Менделеева указан средний вес всех изотопов, при этом учитывается их распространенность в природе. Например, у кислорода есть три стабильных изотопа:
С учетом этого атомная масса кислорода, указанная в таблице Менделеева, рассчитывается так:
(15,9949•99,759 + 16,9991•0,037 + 17,9991•0,204)/100 = 15,9994 а. е. м.
Молекулярная масса
Зная атомные массы отдельных элементов, можно находить и молекулярные массы молекул. Для этого надо всего лишь сложить атомные массы тех атомов, которые входят в состав молекулы.
Например, рассмотрим молекулу метана, она имеет формулу СН4, то есть состоит из 1 атома углерода (который весит 12 а. е. м.) и 4 атомов водорода (каждый массой по 1 а. е. м.). Складываем атомные массы:
12 + 1 + 1 + 1 + 1 = 12 + 4•1 = 16 а. е. м.
Итак, молекула метана имеет молекулярную массу 16 а. е. м.
Заметим, что очень часто возникает путаница из-за молекул простых газов – водорода, кислорода, азота и т. д. Дело в том, что их молекулы состоят из двух атомов, поэтому и масса у них вдвое больше, чем масса атомов. Например, атомная масса элемента кислород – 16 а. е. м., а вот молекула кислорода, имеющая формулу О2, весит уже 16•2 = 32 а. е. м.
Молярная масса
Молекулярные массы веществ тесно связаны с понятием молярной массы. Молярная масса – это масса 1 моля вещества. Численно она совпадает с молекулярной массой, но измеряется в других величинах – в граммах на моль, или в г/моль.
Молярная масса позволяет определять, легче или тяжелее воздуха тот или иной газ. Для этого надо лишь сравнить молярную массу газа с молярной массой воздуха, составляющей 28,98 г/моль. Так, кислород оказывается тяжелее воздуха, так как его молярная масса – 32 г/моль. Азот же легче воздуха, ведь его масса равна 28 г/моль. Здесь следует уточнить, что воздух не является отдельным веществом в химическом смысле слова, то есть никаких «молекул воздуха» не существует (поэтому не существует и понятия «молекулярная масса воздуха»). В реальности воздух – это смесь нескольких газов, преимущественно азота и кислорода. При этом более тяжелые молекулы чаще встречаются в нижних слоях атмосферы, а легкие молекулы – на высоте. По этой причине (но отнюдь не только из-за нее) в горах тяжело дышать – на большой высоте воздух содержит меньше кислорода и больше азота.
Подведение итогов
Молекулярная масса показывает, какую массу имеет та или иная молекула. Для ее вычисления достаточно сложить массы входящих в молекулу атомов. Молекулярная масса численно равна молярной массе, и по ней можно оценить, какой газ легче воздуха, а какой – тяжелее.