Прибор нейродоктор что это
О приборе
Неудержимый рост заболеваемости населения во всём мире вынуждает врачей и ученых искать новые, более эффективные способы и средства восстановления и сохранения здоровья. Ряд открытий в квантовой физике и, разработанные на этой базе нанотехнологии, позволили исследователям вторгаться в недоступный доселе наномир живой материи, восстанавливать и регулировать жизненно важные процессы в организме человека.
Воплощением этих достижений стал уникальный прибор Нейродоктор, который создан российскими учёными и является новым поколением серии приборов квантовой медицины. Это простое с виду электронное устройство пришло на смену громоздкому стационарному оборудованию, которое использовалось в бывшем СССР во многих медицинских учреждениях страны.
Современные технологии позволили снизить вес прибора с 50 кг до 300 гр и сделать его общедоступным для применения в домашних условиях. Кроме того (в отличии от более ранних модификаций), новый прибор корректирует здоровье и омолаживает организм на клеточном уровне. Для большинства из нас это покажется фантастичным, но таковы реалии сегодняшнего дня: последние научные достижения способны решать задачи, которые несколько лет назад казались неразрешимыми.
Как работает Нейродоктор?
В приборе установлены два блока светодиодов и электронный блок управления. Импульсы света излучаются с определённой частотой, последовательностью и полярностью, в соответствии с выбранной вами программой (согласно прилагаемой инструкции). Это позволяет с высокой точностью устранять различные патологии в организма человека на атомно-молекулярном уровне.
Почему Нейродоктор нужен именно вам?*
Противопоказания
К ЧИСЛУ ОТНОСИТЕЛЬНЫХ ПРОТИВОПОКАЗАНИЙ ОТНОСИТСЯ ЭПИЛЕПСИЯ (ИСПОЛЬЗОВАНИЕ ПРИБОРА ДОПУСКАЕТСЯ ПОД НАБЛЮДЕНИЕМ ВРАЧА).
В остальных случаях применение прибора не только полезно, но и необходимо как для лечения, так и для профилактики, поскольку его воздействие на организм повышает иммунитет, энергетический потенциал и защитные силы организма.
*Администрация сайта уведомляет о том, что вся информация, содержащаяся в данном подразделе, не может быть использована как точные данные, т. к. основана на личном опыте покупателей аппарата Нейродоктор.
Аппараты для магнитотерапии: обзор
Магнитные поля обладают загадочным действием на организм, многие приписывают им лечебные свойства. Во многих программах реабилитации и санаторно-курортного лечения присутствуют данные процедуры и обещают мощный оздоровительный эффект. Так ли это на самом деле и в каких случаях магнитотерапия может помочь?
Магнитное поле земли оказывает на нас действие на протяжении всей жизни, поэтому для нашего организма это не является необычным. Так, по данным многочисленных исследований, вреда от магнитотерапии не зафиксировано, вне зависимости от её типа. Магнитотерапия одна из разновидностей физиотерапии, когда то или иное воздействие на организм должно привести к лечебному эффекту. Обычно курс магнитотерапии проходят в составе программы реабилитации. Её используют при:
Виды полей в магнитотерапии
Используются магнитные поля нескольких видов:
Общий лечебный эффект связан с неспецифическими реакциями нервной, иммунной и гуморальных систем регуляции, активируются резервы организма и компенсаторно-приспособительные механизмы. Возникает вопрос, а можно ли проводить подобные процедуры дома, без посещения лечебных учреждений?
Производители
Производители приборов для магнитотерапии дома:
Приборы

Противопоказания
Противопоказаниями для низкочастотной магнитной терапии являются:
Высокоинтенсивная магнитная терапия противопоказана пациентам с:
Сила эффекта
В исследованиях больший эффект магнитотерапия оказывает на нервную и сердечно-сосудистую систему. Основные эффекты были связаны с уменьшением боли, тревоги и улучшением качества жизни. То есть, если в составе проблемы есть один или несколько этих компонентов, возможно, будет отмечен положительный эффект.
Чтобы быть довольным результатом, нельзя предъявлять завышенных ожиданий. Так как механизм действия магнитного поля на организм достаточно сложен для восприятия, могут появляться заблуждения, формироваться образ «волшебной таблетки» или надежда на чудесное исцеление, когда врачи не смогли помочь. Физиотерапия всегда идет в комплексе, и хотя может являться важной частью лечения, но не будет единственной. Типичным примером может стать образ человека с избыточным весом и болью в коленях. Курсы противовоспалительных препаратов помогают с переменным успехом. Одна из ключевых причин избыточный вес, который приводит к болям. Покупка аппарата без корректировки образа жизни и снижения веса вряд ли даст нужный эффект.
Сначала следует получить консультацию специалиста, максимально выполнить рекомендации и потом со спокойной душой можно дополнить это магнитотерапией в домашних условиях.
Прибор нейродоктор что это
Нейрохирургическое лечение болезни Паркинсона
С 1950-х годов нейрохирургические стереотаксические деструкции (таламотомии, паллидотомии) были одним из основных методов коррекции наиболее существенных проявлений болезни Паркинсона (БП) — тремора, ригидности, брадикинезии, хотя часто приводили к серьезным осложнениям, таким как параличи. К 1969 г. в мировой печати были опубликованы результаты почти 40 000 стереотаксических операций [2,4]. После внедрения леводопы в клиническую практику начиная с 1967 г. количество стереотаксических деструкций значительно уменьшается. Однако по мере накопления опыта фармакотерапии БП возникли новые проблемы: лекарственные дискинезии и моторные флуктуации, поиски коррекции которых привели к своего рода «ренессансу» хирургического лечения БП, но уже на новом технологическом уровне.
Несмотря на то что положительное влияние нейростимуляции таламуса на тремор было известно давно, идея использования ее в терапевтических целях возникла только в 1987 г., когда французский нейрохирург A.Benabid опубликовал сообщение о результатах стимуляции вентрального промежуточного ядра таламуса (VIM) [6]. В 1992 г. L.V.Laitinen предложил использовать вместо паллидотомии (деструкции внутреннего сегмента бледного шара — GPI) стимуляцию этой структуры, сообщив, что нейростимуляция GPI вызывает уменьшение брадикинезии, ригидности, а также лекарственных дискинезий [12]. Стимуляция субталамического ядра (STN) для лечения БП была впервые выполнена в 1994 г. в Гренобле A.Benabid и соавт. [7].
Таким образом, с момента первого использования нейростимуляции глубинных структур головного мозга прошло уже более 20 лет. За это время проведено свыше 60 000 операций, и нейростимуляция подкорковых структур перешла из разряда экспериментальных методов в рутинные.
Стереотаксические деструкции (таламотомия, паллидотомия) продолжают выполняться в некоторых клиниках, однако в настоящее время в функциональной нейрохирургии наметилась тенденция к переходу к менее травматичной нейростимуляции. Деструктивные операции в настоящее время возможны только у больных с относительно изолированным, преимущественно односторонним тремором, а также в случаях, когда имеются противопоказания к стимуляции глубинных структур мозга (например, при высоком риске инфицирования) или когда стимуляция недостаточно эффективна.
В силу большей безопасности, отсутствия риска необратимого повреждения головного мозга, возможности двустороннего воздействия высокочастотная стимуляция глубинных структур мозга в последние годы стала предпочтительным вариантом нейрохирургического вмешательства.
Следует отметить, что пациентам, которым была выполнена паллидотомия, при снижении ее эффекта не исключается проведение нейростимуляции STN [13], а больных после таламотомии можно в последующем лечить нейростимуляцией STN либо GPI.
Система для нейростимуляции состоит из трех имплантируемых компонентов: четырехконтактного электрода, нейростимулятора и провода, соединяющего электрод с нейростимулятором (рис. 1). Методика операции заключается в имплантации в головной мозг с двух сторон электродов, которые соединяют с нейростимулятором, имплантируемым подкожно в подключичную область. Генератор импульсов представляет собой электрон-
ную микросхему для регулируемой генерации импульсов и батарею (в неперезаряжаемых моделях) либо аккумулятор (в перезаряжаемых моделях). Неперезаряжаемые стимуляторы имеют срок действия от 2 до 5 лет, после чего их необходимо заменить; достоинством перезаряжаемых стимуляторов является более длительный срок службы (примерно 9 лет), недостатком — необходимость регулярной подзарядки (несколько раз в неделю) [1].
Мишенями для нейростимуляции в настоящее время чаще всего служат STN, GPI и VIM. Точный механизм нейростимуляции до сих пор неизвестен, однако полагают, что высокочастотная стимуляция блокирует патологическую активность STN и GPI [5].
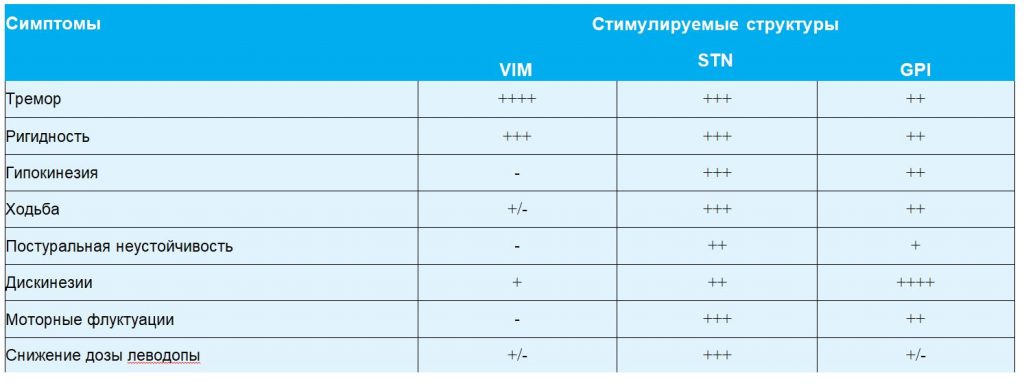
Воздействие на эти мишени по-разному влияет на основные симптомы БП (табл. 1). Выбор оптимальной точки мишени у каждого пациента осуществляется в специализированном центре совместно неврологом и нейрохирургом.
Стимуляция STN позволяет ослабить все основные двигательные проявления БП (тремор, ригидность, гипокинезию); сократить продолжительность и уменьшить тяжесть периода «выключения» (при оценке по III части шкалы UPDRS) на 45-65%, уменьшить выраженность лекарственных дискинезий на 67-83%, а также снизить дозу дофаминергических средств, прежде всего леводопы, в среднем на 50% [9, 14].
Стимуляция GPI наиболее эффективна при медикаментозных дискинезиях, которые уменьшаются на 66-90%. Однако влияние стимуляции GPI на тяжесть основных двигательных симптомов менее выражено (30-50%), и снизить дозу дофаминергических средств в такой степени, как при стимуляции STN не удается; кроме того, при длительном катамнестическом исследовании эффект стимуляции GPI не столь выражен, как при стимуляции STN [9, 14].
Стимуляция VIM показана больным с преимущественно дрожательной формой БП, поскольку уменьшает тремор на 90%, незначительно снижает ригидность и не влияет на остальные симптомы БП [16].
Успех нейрохирургического вмешательства определяется многими факторами, главными из которых являются правильный отбор больных, точно выполненная имплантация электродов, отсутствие интра- и послеоперационных осложнений, адекватно подобранная программа нейростимуляции, а также оптимальное ведение больных в отдаленные сроки, включающее коррекцию программы нейростимуляции и коррекцию фармакотерапии при прогрессировании заболевания.
Необходим комплексный индивидуальный подход к отбору больных, учитывающий не только показания и противопоказания к операции, но и большое количество других факторов, таких как возраст больного, длительность заболевания, скорость прогрессирования болезни, наличие или отсутствие немоторных симптомов.
Таблица 1 Эффекты, достигаемые при стимуляции глубинных структур мозга у больных БП
выраженные моторные флуктуации или дискинезии, не корригируемые оптимальной консервативной терапией, в том числе адекватной дозой дофаминергических средств;
Показаниями для выполнения нейрохирургического вмешательства больным с диагнозом БП (другие нозологические формы паркинсонизма должны быть исключены) являются:
плохая переносимость препаратов леводопы, не дающая возможности повысить ее дозу до оптимального уровня (прежде всего из-за дискинезий «пика дозы»); выраженный инвалидизирующий тремор покоя, который не удается корригировать с помощью медикаментозной терапии.
При отборе больных строго соблюдаются следующие критерии:
длительность заболевания не менее 5 лет; стадия заболевания по Хен-Яру не ниже 3-й; высокая эффективность леводопы при проведении фармакологической пробы;
высокая степень повседневной активности (не менее 60-70% по шкале Шваба-Ингланда) в периоде «включения».
Всем пациентам проводится однократная фармакологическая проба с назначением индивидуальной эффективной дозы леводопы в утренние часы после 12-часового ночного перерыва в приеме препарата. Сравнивают показатели по шкале UPDRS (учитывают суммарную оценку по II и III частям этой шкалы) в периодах «включения» и «выключения». Эффект леводопы оценивается как достаточно высокий, если разница показателей составляет 50%.
Как правило, оперативное вмешательство выполняют пациентам до 75 лет. По данным некоторых исследований, нейростимуляция STN у пожилых пациентов менее эффективна, чему относительно молодых [8, 17]. Кроме того, в более старшем возрасте чаще встречаются когнитивные нарушения, постуральные расстройства, а также сопутствующая соматическая патология, которые не дают проявиться положительному эффекту операции.
Важным условием направления на оперативное вмешательство служит отсутствие выраженных когнитивных или аффективных расстройств, в частности глубокой депрессии с суицидальными мыслями. Противопоказаниями к оперативному лечению являются также острый психоз, алкогольная и наркотическая зависимость, выраженная церебральная атрофия или очаговые поражения мозга (по данным МРТ), а также коагулопатия, сахарный диабет, иммуносупрессия, прием антикоагулянтов.
Нейрохирургическое вмешательство позволяет ослабить дискинезии и тремор, уменьшить клинические проявления в период «выключения». Однако оно не позволяет отказаться от лекарственной терапии, хотя создает условия для ее оптимизации. Кроме того, после оперативного вмешательства обычно не устраняются симптомы (например, нарушения ходьбы), которые сохраняются в период «включения».
Результаты хирургического лечения во многом зависят также от подбора программы стимуляции. Неадекватно подобранная программа электростимуляции способна не только свести к минимуму результаты операции, но и ухудшить клинические проявления заболевания [7, 12]. Программирование нейростимулятора производится неинвазивно с помощью специального программатора и требует от специалиста знания электроанатомии глубоких структур мозга. Цель программирования — найти наиболее эффективный электродный контакт, стимуляция которого обеспечивает максимальный клинический эффект при минимальных проявлениях побочных эффектов [1], для этого используются различные режимы стимуляции (монополярный, биполярный), а также различные значения параметров электростимуляции (амплитуды, длительности и частоты импульса).
Параллельно подбору параметров электростимуляции проводится коррекция медикаментозного лечения. Подбор терапии осуществляется эмпирически и зависит от степени клинического улучшения на фоне нейростимуляции. Нейростимуляция часто позволяет снизить дозу леводопы, при необходимости восполнив эффект за счет препаратов других фармакологических групп (агонисты дофаминовых рецепторов, ингибиторы МАО-В, препараты амантадина). Эффект стимулирующих вмешательств при БП может стойко сохраняться в течение многих лет.
Несмотря на то что электростимуляция глубинных структур головного мозга является более безопасной и менее инвазивной методикой по сравнению с деструктивными вмешательствами, тем не менее после нее на том или ином этапе лечения могут возникать осложнения. Их делят на несколько групп:
Осложнения, возникающие во время операции, включают интракраниальные гематомы, пневмоцефа- лию, смещение электрода, эпилептические припадки, дезориентацию, эмболию легочной артерии и др. Частота интракраниальных осложнений по сравнению с деструктивными операциями невысока и составляет в среднем от 1 до 5% [10, 11, 15].
Осложнения, возникающие в послеоперационном периоде: инфекционные осложнения (инфекции кожи, появление эрозий в месте вживления подкожного генератора); технические осложнения, связанные с неточным размещением электрода, его разрывом, смещением нейростимулятора или его неисправностью [6]. Частота инфекционных осложнений составляет от 3 до 10% [10, 15].
Осложнения, связанные с побочными эффектами стимуляции: стимуляционные дискинезии; аксиальные нарушения (дизартрия, постуральная неустойчивость, нарушения ходьбы); сенсорные нарушения в виде парестезий; двигательные нарушения (тоническое сокращение мышц лица или конечностей); вегетативные нарушения в виде ощущения жара, повышенного потоотделения; глазодвигательные нарушения, головокружения, приступы тревоги, эйфории, гипоманий. Эти побочные эффекты проходят при смене электродных контактов или коррекции параметров стимуляции.
Таким образом, электростимуляция глубоких структур мозга является современным, относительно безопасным и эффективным методом лечения БП, способным значительно улучшить качество жизни больного при своевременном направлении на нейрохирургическое вмешательство. В настоящее время продолжается поиск новых точек мишеней (педункулопонтинное ядро, каудальная часть неопределенной зоны [zona incerta]), способных уменьшать рефрактерные к терапии симптомы БП.
После первичного подбора программы нейростимуляции требуются повторные визиты для коррекции программы (примерно от 2 до 5 визитов в первые 6 месяцев), а затем по мере необходимости (примерно 1 раз
в 6-12 мес.) [3]. Несомненно, это привязывает пациентов к специализированным центрам, где работают специалисты, владеющие методикой программирования. До недавнего времени такие специалисты имелись в трех московских учреждениях, однако в последние годы в НИИ нейрохирургии им. Н.Н.Бурденко прошли обучение паркинсонологи из различных регионов России (Казань, Санкт-Петербург, Тюмень и др.), что позволило больным получать квалифицированную помощь независимо от того, где их прооперировали.
Исследование эффективности внутримозговой трансплантации дало неоднозначные результаты. С одной стороны, известны случаи приживления трансплантата и достижения выраженного стойкого улучшения. С другой, у значительной части больных возникли тяжелые, резистентные к терапии дискинезии. В связи с этим данный метод, так же как и методы, основанные на применении стволовых клеток, пока остается экспериментальным.
[1] Центр экстрапирамидных заболеваний, кафедра неврологии РМАНПО.
[2] Научно-исследовательский институт нейрохирургии им. акад. Н.Н.Бурденко.
Препараты для улучшения работы мозга
Работоспособность мозга зависит от его кровоснабжения. Из крови орган получает столь необходимый кислород. Если его не хватает, человек страдает от нарушений когнитивных функций. В условиях экстремальных нагрузок, требующих повышенной умственной активности, естественных ресурсов не хватает, и мозг требует подпитки. При наличии проблем с кровообращением эта потребность многократно возрастает.
В такой ситуации помогают препараты для повышения мозговой активности. Мы разберемся, как они действуют, кому их следует принимать и как их правильно выбрать.
Ноотропы: что это такое?
Ноотропы – это группа средств для улучшения высших функций головного мозга. Она объединяет в себе:
Им ошибочно приписывают несуществующее действие – развитие интеллектуальных способностей у детей и взрослых. Это заблуждение. От приема таблетки никто умнее не становится. Но если высшие психические функции начинают угасать, их можно вернуть на прежний уровень. Для этого нужно устранить причину – переутомление, гипоксию или иные мозговые нарушения. В этом и заключается назначение ноотропных препаратов.
Принцип действия препаратов для улучшения памяти
Для повышения активности ЦНС имеют значение и такие терапевтические эффекты этих препаратов:
Цель приёма ноотропов – в улучшении мозгового кровообращения и нормализации метаболических процессов в нервных клетках. Параллельно повышается скорость образования нейронных связей и наращивается их число. Это и приводит к активизации мозговой деятельности. То есть на фоне лечения нарушений ноотропы действуют как стимуляторы работы самого органа.
Что дает человеку повышение активности головного мозга
Ноотропы называют стимуляторами познавания. Прием таких лекарств или витаминов усиливает способности к обучению за счет комплексной активизации работы ЦНС:
В зависимости от действующего вещества, могут наблюдаться дополнительные эффекты. Одни обладают седативным действием, другие помогают выйти из депрессии. Есть лекарства, помогающие отрегулировать режим сна и бодрствования.
Стимуляторы активности головного мозга нередко объединяют в одну группу с нейропротекторами. Они защищают орган от тяжелых последствий нарушений кровообращения, препятствуют разрушению клеток, помогают притормозить деменцию.
Показания к приему
Ноотропные средства назначаются при диагностировании нарушений мозговой деятельности. Они могут быть связаны с травмами головы, проблемами с кровообращением, интоксикацией. Чаще всего ноотропы выписывают при:
В этих случаях речь идет о лекарственных препаратах. Для повышения умственной работоспособности можно обойтись хорошим витаминным комплексом.
Противопоказания к приему
Ноотропы считаются одними из самых безопасных лекарств. Абсолютных противопоказаний к их приему нет. Хотя врачи не рекомендуют употреблять их, если не диагностировано какое-либо нарушение мозговой активности. Не выписывают их беременным и младенцам.
Отдельные препараты имеют побочные эффекты. Их нежелательное появление и может стать относительным противопоказанием к приему. Сюда относят:
Так, если у человека наблюдается психомоторное возбуждение, лекарство для мозговой активности может лишь усугубить ситуацию. Сонливость проявляется не у всех. Перед тем как садиться за руль, стоит понаблюдать за своим состоянием после приема медикаментов.
Группы средств для улучшения работы мозга
Пирацетам был первым в мире ноотропом. Его разработали еще в 1963 году как замену психостимуляторам, выигрывающую за счет отсутствия побочных эффектов. Это вещество стало родоначальником группы рацетамов, улучшающих память.
В категории ноотропов также можно найти:
Нейропротекторы иногда отождествляют с ноотропами, но между ними есть различие. Нейропротекторы – это препараты смешанного действия. Они имеют более широкий спектр эффектов.
Рейтинг лучших препаратов для улучшения работы мозга
Несмотря на большой выбор препаратов ноотропного действия в аптеках, среди них есть прочно утвердившиеся лидеры. В первую очередь это упомянутый Пирацетам. Его выпускают в форме таблеток, капсул и инъекций.
Но есть еще много хороших средств аналогичного действия. Они отличаются действующими веществами и доминирующими эффектами. В первую пятерку вместе с Пирацетамом входят:
| Глицин | Одноименная аминокислота, помогающая справляться с проявлениями вегетососудистой дистонии и умственными перегрузками. |
| Кавинтон | Цереброваскулярный корректор винпоцетин, восстанавливающий кровообращение и нивелирующий последствия гипоксии. |
| Фенотропил | Психостимулятор, способствующий улучшению концентрации внимания, повышению работоспособности, легкий транквилизатор. |
| Семакс | Нейропептид, активизирующий процессы обучения и помогающий адаптироваться к недостатку кислорода. |
Витамины для улучшения работы мозга
Если серьезных нарушений в работе мозга не выявлено, злоупотреблять лекарствами не стоит. Решить задачу повышения концентрации внимания или способности к обучению можно с помощью витаминов:
Чудесной таблетки, которая разом решит все проблемы когнитивной сферы, не существует. Но правильно выявленная причина нарушений позволяет подобрать подходящее средство для их коррекции.
Болезнь Паркинсона: у больных появилась надежда
Боксер Мохаммед Али, политики Ясер Арафат и Мао Цзэдун, Папа Римский Иоанн Павел II, художник Сальвадор Дали, актер Майкл Джей Фокс (обаятельный Марти из фильма «Назад в будущее») – всех этих людей в разном возрасте объединила общая беда – болезнь Паркинсона. Еще несколько десятилетий назад это заболевание считалось приговором. Но, к счастью, сегодня появились средства, способные если не остановить болезнь, то по крайней мере значительно облегчить жизнь пациентов, страдающих этим хроническим неврологическим заболеванием.
Лекарства – по схеме
Поскольку причиной развития болезни является дефицит в головном мозге дофамина, больным требуется вводить его извне. К сожалению, доставить само это вещество невозможно – оно плохо проникает через гематоэнцефалический барьер и по пути распадается. Но зато можно ввести больному биологический предшественник дофамина – препарат, который, попав в кровь и достигнув мозга, уже на месте превратится в нужный нейромедиатор. Такой препарат применяется в неврологии уже около 40 лет. В конце 60‑х годов он совершил настоящую революцию, потому что эффект от его применения у пациентов был наиболее впечатляющий, особенно в первые годы приема. Это было похоже на чудо: человек, которого била дрожь и мертвой хваткой сковывал высокий мышечный тонус, выпивал таблетку и на глазах становился внешне практически здоровым.
После того как это лекарство стало широко применяться на практике, смертность людей с болезнью Паркинсона сократилась вдвое. Но, к сожалению, действие лекарства весьма непродолжительно – всего 1,5–3 часа, и оно вызывает ряд побочных эффектов. Дело в том, что в норме у человека дофамин выделяется равномерно, а при приеме лекарства – скачкообразно. Во время резкого повышения концентрации дофамина в организме, которое наступает спустя какое-то время после употребления таблетки, у больного начинается сильный приступ двигательной дискинезии, во время которого тело не слушается своего хозяина и совершает непроизвольные размашистые движения; и, наоборот, при резком снижении концентрации возникает обездвиженность. В связи с этим многие пациенты раньше опасались принимать это лекарство. Но врачи уверены, что бояться не нужно. Ведь сегодня можно успешно бороться побочными эффектами с помощью дополнительных препаратов, которые усиливают и продлевают лечебный эффект и сглаживают неприятные моменты. Эти лекарства в составе комплексной терапии очень эффективны, особенно у молодых пациентов.
Сегодня существует 7 групп противопаркинсонических средств, и в каждой из них имеются еще не менее 3–4 препаратов. Их выбор и схема лечения очень сложны, они зависят от возраста больного, формы, стажа заболевания и многих других обстоятельств. Поэтому врач, занимающийся ведением таких больных, должен быть очень знающим и опытным. Помимо своевременности лечения важна его непрерывность – лекарственные «каникулы» для больных очень вредны.
Нужна, как дырка в голове?
В последнее время появились более радикальные способы, которые находятся на стыке консервативного и нейрохирургического лечения.
Первые стереотаксические операции (таламотомия, паллидотомия и др.) на головном мозге были сделаны в 50–60‑х годах. Они проходили под местным наркозом. На голову больному надевался особый шлем, затем в нужном отделе черепа пациента высверливалось крошечное отверстие, через которое по точным расчетам вводилась тонкая канюля с проходившим через нее жидким азотом. Уничтожить «вредный» участочек в головном мозге можно было не только холодом, но и электрокоагуляцией или химическим способом. Это воздействие разрушало определенное ядро и тем самым прерывало поток патологической импульсации, в результате дрожание у пациента уходило буквально в ту же секунду. Но, увы, если делать операцию не на одной, а на двух сторонах головы (что чаще всего требуется при этой болезни), то в большинстве случаев возникают побочные явления: трудности с речью, проблемы с глотанием и пр. Поэтому область применения таких операций была не очень велика.
Но в начале 90‑х годов французский ученый Бенабид придумал метод глубокой электростимуляции мозга. В ходе этой операции под контролем специальной аппаратуры в те же структуры мозга, что и при деструктивных операциях, вводится электрод, стимулирующий нужное ядро. От этого электрода отходит провод, который проводится под кожей и заканчивается под ключицей пациента, где устанавливается источник питания. И с помощью небольшого наружного устройства (размером с мобильный телефон) врач программирует вживленный электрод на работу в определенном ритме. Самому пациенту достаточно нажимать 2–3 кнопки, чтобы включать и выключать устройство или поменять одну программу на другую, в зависимости от своего состояния. Если же случится сбой программы, необходимо обратиться к врачу, который проведет полноценное «перепрограммирование» (это случается, к счастью, не столь часто).
Операция эта очень сложная и долгая (двусторонняя длится около 8 часов), специалистов, владеющих этой методикой, – единицы. Зато эффект от нее столь же впечатляющий, как и при таламотомии, но без негативных последствий. Разве что в будущем нельзя будет проводить МРТ и другие магнитные процедуры. Хотя такая операция стоит порядка 1 миллиона рублей и по этой причине недоступна для большинства пациентов, но с недавних пор ее включили в перечень высокотехнологической медицинской помощи, поэтому при наличии квот в медицинских учреждениях это вмешательство всем нуждающимся проводят бесплатно. К сожалению, пока центров, где применяют этот метод, в нашей стране очень мало и все они расположены в Москве (Научный центр неврологии РАМН, Институт нейрохирургии им. Бурденко РАМН, Лечебно-реабилитационный центр Минздравсоцразвития).
В будущее – с оптимизмом!
Есть и немедикаментозные средства лечения этой болезни. Среди них – транскраниальная магнитная стимуляция (разновидность физиотерапии), а также правильно организованная лечебная физкультура, помогающая больным преодолевать скованность и нарушения равновесия. Для двигательной реабилитации пациентов с болезнью Паркинсона широко используются компьютерные программы и технологии виртуальной реальности, роботизированные устройства, тренажеры (обладающие низким сопротивлением) и другие высокотехнологичные аппараты.
На ранних этапах заболевания пациентам показаны занятия с определенными элементами бойцовских искусств и танцами, игры с мячом, передвижение по пересеченной местности (в том числе на лыжах), «мягкая» аэробика. На поздних этапах – ходьба (обычная и на месте), упражнения для стоп и подъем по ступенькам, имитация гребли на тренажере, плавание.
В связи с огромной значимостью этой медицинской проблемы в нашей стране около года назад было создано Национальное общество по изучению болезни Паркинсона и расстройств движений. Организация занимается обучением специалистов, разработкой сайта для пациентов, страдающих этим заболеванием, и их родственников (www.parkinsonizm.ru), регистром паркинсонизма в стране, а также проведением тематических конгрессов 1 раз в 2–3 года, выпуском специализированных бюллетеней для врачей и т. д. Организаторы общества надеются, что благодаря их работе диагноз «болезнь Паркинсона» вскоре перестанет быть приговором.
Впервые этот недуг описал английский врач Джеймс Паркинсон в 1817 году в своем «Эссе о дрожательном параличе». Средний возраст начала болезни – 55 лет. В то же время у 10% больных заболевание возникает в самом расцвете сил, до 40 лет – это так называемый ювенильный паркинсонизм.
Известно, что болезнь Паркинсона возникает из-за нарушения выработки дофамина – одного из нейромедиаторов (вещества, служащие для передачи импульсов в головном мозге). Это ведет к нарушению функций клеток в отделах мозга, отвечающих за движения. В результате у больных возникают непроизвольный тремор (дрожь в конечностях), заторможенность, затруднения при ходьбе, а затем и трудности при глотании.
Помимо первичного, ученые выделяют также паркинсонизм вторичный, который вызывают инфекции и другие заболевания головного мозга (например, энцефалит, атеросклероз сосудов мозга), а также повторные травмы головы. Известен токсический паркинсонизм. При нем страдают не одна, а сразу обе стороны тела. Эту разновидность болезни могут спровоцировать чрезмерный прием лекарств (в основном нейролептиков) или работа на вредном производстве (в том числе в сельском хозяйстве, где есть контакт с пестицидами, гербицидами и другими химическими удобрениями). В нашей стране, к сожалению, сильно распространен токсический паркинсонизм у молодых людей, связанный с избытком в их организме марганца. Эта разновидность болезни вызвана не профессиональными вредностями, а употреблением суррогатных наркотиков, в состав которых входит марганцовка.