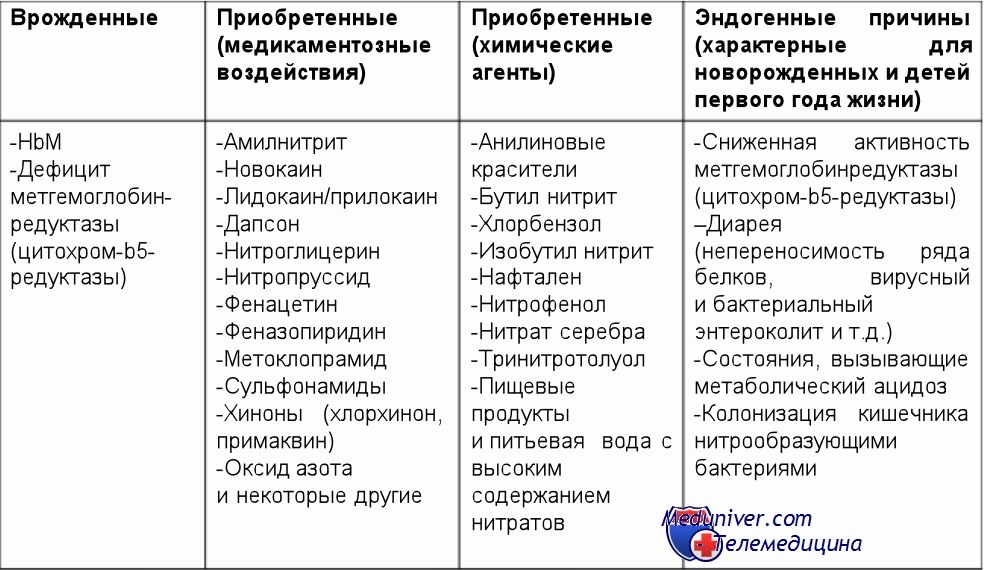
При избытке чего в воде и почве развивается метгемоглобинемия
При избытке чего в воде и почве развивается метгемоглобинемия
Метгемоглобинемии составляют разнородную группу наследственных или приобретенных заболеваний, которые характеризуются наличием в крови увеличенного количества метгемоглобина. Метгемоглобин (МетГб) это окисленная форма (Fe3+) гемоглобина, непригодного для выполнения ведущей функции переноса кислорода. С клинической точки зрения метгемоглобинемия проявляется цианозом, признаками недостатка кислорода, а иногда гемолитической анемией с тельцами Гейнца, или без таковых.
К этой группе заболеваний относятся как приобретенная метгемоглобинемия, при которой образование МетГб происходит под воздействием случайно вводимых в организм метгемоглобинизирующих веществ или медикаментов, так и наследственная метгемоглобинемия, в основу которой заложена генетическая аномалия структуры гемоглобина или набора ферментов эритроцита.
Первый случай наследственной метгемоглобинемии, за счет аномалии гемоглобина, описан Horlein и Weber в 1948 г. в одной немецкой семье. К тому времени молекулярные болезни еще не были известны и аномальный гемоглобин не вскрыт. Лишь в 1961 г. Gerald и Efron описали первые случаи гемоглобина М и механизм образования метгемоглобина в связи с структурной аномалией молекулы гемоглобина.
Этот факт сделал возможным не только дифференциацию приобретенной (токсической природы) и наследственной метгемоглобинемии, но и выделение в отдельные единицы метгемоглобинемии ферментативной природы и метгемоглобинемии за счет наличия гемоглобина М.
Причины (этиология) метгемоглобинемии
Наиболее часто встречается приобретенная метгемоглобинемия. Причины — многочисленны и разнообразны, они включают совокупность тех положений, когда в организм поступают химические метгемоглобинизирующие вещества в достаточно большом количестве и тем самым преодолевают восстановительную способность эритроцита.
Ниже приведены токсические агенты, наиболее часто встречающиеся на практике. При этом некоторые из них — средства текущей терапевтической практики, в то время как другие — вводятся в организм случайно. Наиболее активные — производные анилина, сульфонамиды, нитриты.
Потребление колодезной воды,зараженной нитритами (преобразуемыми кишечной флорой в нитраты) или случайное заглатывание карандаша или мела, содержащих анилиновые красители — относительно часто встречаются, особенно в педиатрии. Описан случай энтеро-генного цианоза с метгемоглобином и сульфгемоглобином после повышенного поглощения кишечником нитритов и соединений серы, видимо в связи с нарушением функции кишок.
II Приобретенные причины метгемоглобинемии:
А. Химические причины метгемоглобинемии:
— Нитриты (натрия, амила, этила)
— Нитраты (субнитрат висмута, нитрат аммония)
— Нитробензол
— Нитроглицерин, анилин, фенацетин, ацетиланилид, сульфамиды, сульфаниламид, сульфапиридин, сульфатиазол
Б. Разные причины метгемоглобинемии:
— Кишечная дисфункция (энторегенный цианоз)
— Заражение крови бациллой Clostridium welchii.
В основе наследственных метгемоглобинемий находится генетический механизм. В мировом плане показатель их частоты невелик, при этом не наблюдается расовый характер, хотя отмечается большая частота ферментативной метгемоглобинемий среди эскимосов Аляски, и наличие HbMIwate — среди нескольких семей в Японии. У нас в стране до настоящего времени диагностированы, в одной семье, недостаточность фермента, и в других трех — наличие ГбМ, причем в двух из них определен гемоглобин М вида HbMIwate.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Нитраты и метгемоглобинемия
Нитраты – это соли азотной кислоты. Их избыток в воде и почве обусловлен природными, а в большей степени еще и антропогенными факторами. Основной источник поступления нитратов в питьевую воду и продукты питания – стоки с полей, промышленных предприятий и использование азотосодержащих удобрений.
Регулярный анализ питьевой воды, контроль концентрации нитратов в овощах позволяет установить массовую долю токсичных веществ, сравнить ее с предельно допустимыми значениями и принять своевременные меры защиты. Важно также периодически исследовать воду из скважин, колодцев и родников, особенно в районах с развитым сельским хозяйством.
Опасность нитратов для здоровья людей
Избыток нитратов приводит к метгемоглобинэмии. Это патологическое состояние возникает после следующей цепочки реакций:
Метгемоглобинемия характеризуется следующими симптомами:
Особенно опасно заболевание для грудных недоношенных детей и малышей до 4 месяцев, употребляющих воду с повышенным содержанием нитратов.
При отсутствии лечения тяжелые формы метгемоглобинэмии могут закончиться летальным исходом. Прогрессирующее заболевание приводит к необратимым поражениям центральной нервной системы.
Меры профилактики
Контроль над концентрацией нитратов в питьевой воде и овощах является эффективной профилактической мерой против метгемоглобинэмии. Заказать исследование воды на содержание данных веществ можно в лаборатории «Веста». Мы четко соблюдаем регламент забора проб, располагаем современным оборудованием, используем современные методики тестирования, гарантируем достоверный результат анализов.
В нашей лаборатории проводится также анализ бутилированной воды для детей.
По результатам проверки воды из скважин, колодцев даются рекомендации по водоочистке. Эффективными средствами удаления нитратов являются системы обратного осмоса и ионообменная фильтрация.
Читайте также
Под аэроионами понимают три вида содержащихся в атмосфере частиц с положительным или отрицательным зарядом
Нормальное функционирование системы управления охраной труда (СУОТ) невозможно обеспечить без правильного распределения обязанностей и ответственности.
Каждый работодатель обязан проводить специальную оценку условий труда (СОУТ) в установленные законом сроки. В ее рамках рабочие места оцениваются на наличие вредных факторов, им присваивается класс условий.
МЕТГЕМОГЛОБИНЕМИЯ
МЕТГЕМОГЛОБИНЕМИЯ (methaemoglobinemia; метгемоглобин + греч. haima кровь) — повышенное содержание метгемоглобина в крови (больше 1 % от общего содержания Hb). М. возникает вследствие наследственной недостаточности восстанавливающих ферментных систем эритроцитов (метгемоглобинредуктаз, или мет-Hb-редуктаз) либо в результате превышения их функц, возможностей при попадании в организм больших доз нек-рых токсических агентов, являющихся метгемоглобинообразователями. Одной из причин М. может быть также наследственный дефект молекулы глобина — так наз. М-гемоглобинопатия (см. Гемоглобинопатии).
Содержание
Этиология и патогенез
Вторичные (приобретенные) М. делят на: 1) токсические М. экзогенного происхождения, возникающие при действии хим. агентов (окислителей, амидо- и нитропроизводных бензола, анилина, фенилгидразина, окислов азота, нитратов колодезной воды, хинонов, метилнитрофосов, нек-рых синтетических красок) или при отравлении лекарственными средствами (фенацетином, антипирином, нитритами, викасолом, сульфонами, нек-рыми сульфаниламидами и противомалярийными средствами); 2) токсические М. эндогенного происхождения, обусловленные нарушением продукции и всасывания нитратов при энтероколитах (так наз. энтерогенный цианоз).
В нек-рых случаях могут наблюдаться смешанные формы, напр, наследственная Энзимопеническая М., проявляющаяся у практически здоровых людей (гетерозиготных носителей генов) только после приема большой дозы сульфаниламидных препаратов.
Патогенез клин, проявлений М. обычно связан с хрон, гипоксией (см.), т. к. насыщение артериальной крови кислородом у больных снижено.
Наследственная Энзимопеническая М., наблюдаемая у гомозиготных носителей генов, является хрон, заболеванием, наследуется по аутосомно-рецессивному типу. В мировой литературе описано ок. 500 случаев, из них св. 50 в СССР (в т. ч. 40 в Якутской АССР). Эта форма М. обусловлена дефицитом активности метгемоглобинредуктазы, к-рый может носить изолированный или генерализованный характер; в первом случае дефицит выявляется в эритроцитах, а во втором (встречается реже) также в лейкоцитах и, возможно, имеется в клетках ткани головного мозга, что может обусловить замедление психического развития и умственную отсталость нек-рых больных.
Наследственная М-гемоглобинопатия передается по аутосомно-доминантному типу и встречается только у гетерозиготных носителей аномальных или нестабильных Hb.
Клиническая картина
Степень выраженности симптомов зависит от количества метгемоглобина в крови, скорости развития М. и компенсаторных способностей сердечно-сосудистой, дыхательной систем и гемопоэза в процессе адаптации к гипоксии. При содержании метгемоглобина в крови менее 20% от общего количества Hb симптомы М. обычно отсутствуют. При повышении его содержания в пределах 20—50% возникают общая слабость, недомогание, одышка при физической нагрузке, раздражительность, ослабление памяти, головные боли и головокружение.
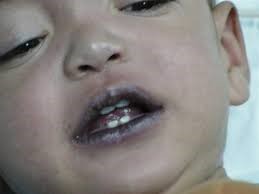
Наследственная Энзимопеническая М. у гомозитотных носителей генов выявляется в период новорожденности и характеризуется цианозом кожи и видимых слизистых оболочек, особенно заметным в области носогубного треугольника, мочек ушей, ногтевого ложа, полости рта. Окраска кожи и видимых слизистых оболочек варьирует от сероземлистого до темно-фиолетового. Цианоз (см.) усиливается при переохлаждении, приеме нек-рых лекарственных средств и пищевых продуктов, содержащих нитраты, а у беременных женщин при развитии токсикоза.
По данным М. С. Кушаковского (1968) и других исследователей, у больных имеются изменения гемодинамики (тахикардия, увеличение минутного объема сердца), носящие компенсаторный характер.
Нередко М. сочетается с другими врожденными аномалиями (атрезия влагалища и матки, недоразвитие кистей рук, изменения формы черепа, деформация и нарушение функции жел.-киш. тракта, талассемия, дефицит фермента глюкозо-6-фосфат дегидрогеназы и др.).
Венозная кровь необычно темного цвета с коричневатым оттенком, не алеет при встряхивании. Изменений гемограммы (см.) и морфологии эритроцитов не отмечается, однако у больных с относительно высоким содержанием метгемоглобина (более 20%) наблюдается вторичный компенсаторный эритроцитоз (до 6,0—7.0 млн. клеток в 1 мкл) с увеличением общего содержания H b до 17,0—24,0 г%, повышением вязкости крови и замедлением РОЭ. Количество активного Hb снижено, и даже при наличии эритроцитоза у больных выявляется кислородная недостаточность. Кривая диссоциации оксигемоглобина (см. Кровь) иногда сдвинута влево. У нек-рых больных отмечаются легкий ретикулоцитоз и повышение (до 1,5—2.0 мг%) непрямого билирубина сыворотки крови, что позволяет предположить наличие незначительного гемолиза; при интенсивном гемолизе метгемоглобин может присутствовать в моче (см. Метгемоглобинурия).
Больные альфа-цепочечными вариантами М-гемоглобинопатии синюшны с момента рождения, а при p-цепочечных вариантах цианоз развивается с 6-месячного возраста. Помимо выраженного цианоза, других симптомов не наблюдается.
Наследственная Энзимопеническая М. у гетерозиготных носителей генов (до попадания в организм сульфаниламидных препаратов) протекает бессимптомно; концентрация метгемоглобина в крови нормальная или слегка повышена (1—2%), активность метгемоглобинредуктазы снижена на 50%.
Токсическая М. экзогенного и эндогенного происхождения протекает остро или хронически и по симптоматике напоминает наследственную энзимопеническую М.; нередко сочетается с гемолизом (см.).
Диагноз
Лечение
Лечение больных токсической М. и гомозиготных носителей генов с наследственной энзимопенической М. со значительным (более 20%) содержанием метгемоглобина в крови и выраженной симптоматикой проводят специфическими лекарственными средствами, способствующими его восстановлению,— аскорбиновой к-той и метиленовым синим. Прием внутрь аскорбиновой к-ты (по 0,15—0,3 г 3 раза в день) уже в течение первых дней снижает концентрацию метгемоглобина в крови до 10% от общего количества Hb. Далее переходят на поддерживающие дозы (0,05—0,1 г 3 раза в день) в течение длительного времени (2—3 мес.); при этом необходимо делать перерывы продолжительностью 2—4 нед. Длительное лечение аскорбиновой к-той в таких больших дозах должно осуществляться под наблюдением врача с периодической проверкой функции поджелудочной железы, почек и измерением АД.
Метиленовый синий при внутривенном введении оказывает быстрый эффект и уже через 1 час относительная концентрация метгемоглобина в крови уменьшается до 1% и ниже. Его применяют в виде препарата «Хромосмон», вводят внутривенно медленно из расчета 1 мг на 1 кг массы тела или в капсулах (по 100 мг) 3—4 раза в день. Больные М-гемоглобинопатиями в лечении не нуждаются и резистентны к любой терапии.
Прогноз и Профилактика
Прогноз зависит от вида М. и тяжести клин, проявлений.
Профилактика. Необходимы медико-генетические консультации для исключения возможности вступления в брак гетерозиготных носителей М. Следует избегать контакта с хим. агентами — метгемоглобинообразователями как на производстве, так и в быту.
Метгемоглобинемия у новорожденных
У здоровых новорожденных в крови содержится приблизительно 0,5% метгемоглобина. У новорожденных чаще наблюдается М., связанная с незрелостью системы ферментов, восстанавливающих метгемоглобин (метгемоглобинредуктаз), и проявляющаяся повышенной чувствительностью к метгемоглобинобразователям. У таких новорожденных при контакте с пеленками, помеченными анилиновыми красителями, даче им колодезной воды, богатой нитратами, назначении фенацетина, новокаина и нек-рых других лекарственных средств появляется стойкий цианоз, одышка, что нередко трактуется врачами как проявление пневмонии или сердечно-сосудистой патологии. В тяжелых случаях присоединяются желтуха, судороги и ребенок может погибнуть.
Лечение: применяется хромосмон внутрь и внутривенно (0,1 мл 1% р-ра на 1 кг массы тела), метиленовый синий, аскорбиновая к-та.
Прогноз улучшается с возрастом.
Библиография: Андреева А. П. и др. Молекулярные основы нарушения функциональных свойств гемоглобина у больных энзимопенической метгемоглобинемией, Докл. АН СССР, т. 235, № 6, с. 1441, 1977; Бадалян Л. О., Таболин В. А. и Вельтищев Ю. Е. Наследственные болезни у детей, с. 152, М., 1971; Д e р в и з Г. В. Наследственная Энзимопеническая метгемоглобинемия, Клин, мед., т. 55, № 5, с. 8, 1977, библиогр.; Кушаковский М. С. Клинические формы повреждения гемоглобина, Л., 1968, библиогр.; Муромов А. Л. и Г л у-ховская Н. Я. Метгемоглобинемия в клинической токсикологии, в кн.: Острые отравления. Диагностика, клиника и лечение, под ред. И. И. Шиманко, с. 235, М., 1970; Тодоров Й. Клинические лабораторные исследования в педиатрии, пер. с болг., с. 138, 145, София, 1968; Токарев Ю. Н. Диагностика и лечение метгемоглобинемий, Тер. арх., т. 51, № 9, с. 79, 1979; Cartwright G. E. Methemoglobinemia, sulfhemoglobinemia, в кн.: Principles of intern, med., ed. by T. R. Harrison, p. 1310, N. Y. a. o., 1962, bibliogr.; Erslev A. J. a. Gabuzda T. G. Pathophysiology of blood, p. 70, Philadelphia, 1975; The metabolic basis of inherited disease, ed. by J. B. Stanbury a. o., N. Y. a. o., 1972.
Ю. H. Токарев; Л. H. Собеневская (пед.).
При избытке чего в воде и почве развивается метгемоглобинемия
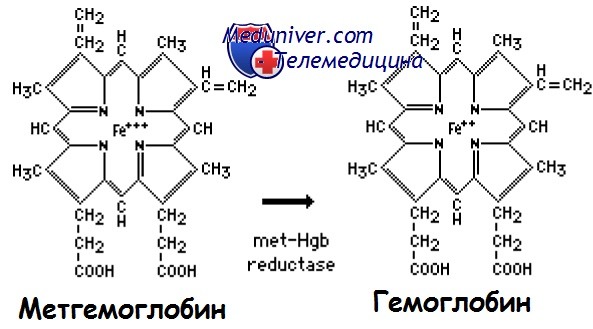
Метгемоглобин представляет собой форму окисленного гемоглобина. Последний отличается от нормального гемоглобина наличием в геме железа в состоянии Fe3+, вместо двухвалентного Fe2+, тем самым утрачивая способность обратимо связывать кислород и свойство дыхательного пигмента.
Ежедневно примерно 1% всего гемоглобина преобразовывается в метгемоглобин; в то-же время у лиц в норме, наблюдаются и цифры меньше 2%.
Сохранение метгемоглобина в физиологических пределах и его сокращение в виде функционального гемоглобина (гемоглобин-Fe2+) обеспечиваются ферментативными и иными механизмами защиты эритроцита:
2 гемоглобина — Fe2+ + Н2О2 2 гемоглобина — Fe3+ — ОН (метгемоглобин).
Основной ферментативный механизм образует метгемоглобинредуктазу, зависящую от НАД восстановл. (диафораза I), но существует и второй фермент — метгемоглобинредуктаза, зависящая от восстановленного НАДФ (диафораза II), которая, однако, в физиологических условиях мало активна. Восстановленный глютатион и аскорбиновая кислота участвуют в восстановлении метгемоглобина неферментатувным путем.
В крови метгемоглобин появляется при следующих трех обстоятельствах:
1) его чрезмерном образовании;
2) понижении функции восстановления метгемоглобина в гемоглобин;
3) структурной аномалии глобина с необратимым преобразованием Fe2+ в Fe3+. Метгемоглобин придает крови шоколадно-бурый оттенок, при том синюха развивается когда концентрация достигает примерно 15%, т.е. 2 г/100 мл крови.
Восстановление метгемоглобина в гемоглобин в норме
Приобретенная метгемоглобинемия наблюдается при чрезмерном образовании метгемоглобина под воздействием отдельных, поступающих в организм веществ. Восстановительный механизм эритроцита действует нормально, однако большая продукция метгемоглобина заглушает его. Развитие и резкость синюхи связаны с количеством и моментом проникновения в организм токсического метгемоглобинизирующего вещества.
На первых месяцах жизни синюха резко выражена даже при отностительно небольшом количестве токсического вещества, по причине более легкой метгемоглобинизации гемоглобина Ф, чем гемоглобина А.
Синюха, развивающаяся при наследственной метгемоглобинемии отличается некоторыми особенностями, которые связаны с механизмом образования метгемоглобина.
Генетический недостаток диафоразы I — основной редуктазы метгемоглобина — заложен в основу энзиматической метгемоглобинемии. Образующееся в организме количество метгемоглобина нормальное, однако оно накопляется по причине недостатка восстановительного фермента. Синюха наблюдается лишь у гомозиготов (рецессивная болезнь), уровень фермента которых нуль или приближается к нулю. Наличие синюхи отмечается непосредственно после рождения.
Тем не менее наличие относительно небольшого количества метгемоглобина (15—30%) даже при полном отсутствии диафоразы I объясняется компенсаторным действием остальных восстановительных механизмов — диафораза II, аскорбиновая кислота, восстановленный глютатион. У гетерозиготов не наблюдается синюха, поскольку невысокий но достаточный уровень фермента обеспечивает восстановление метгемоглобина и нормальную окраску покровов и слизистых оболочек.
Виды гемоглобина М при метгемоглобинемии
У родителей ребенка с метгемоглобинемией ферментативной природы вид нормалный, синюха не обнаруживается.
Отсутствуют доказательства, подтверждающие наличие наследственной метгемоглобинемии за счет недостатка диафоразы II или глютатиона. При наследственной болезни, обусловленной наличием гемоглобина М, образование метгемоглобина объясняется структурной аномалией глобина. Место сдвига находится на уровне связывания гема с глобином, или в непосредственной близости от него, в результате чего налаживаются стойкие связи между аномальной полипептидной цепью и железом гема, с его дальнейшим необратимым фиксированием в виде Fe3+.
Все случаи метгемоглобинемии за счет гемоглобина М представляют собой гетерозиготное состояние в отношение этого аномального гемоглобина. При этой болезни уровень метгемоглобина укладывается в пределы от 15 до 30%, причем объяснение явления следует искать в гетерозиготном состоянии и кодоминантном характере генетической аномалии. Следовательно, в крови подобного больного находится смесь функционального гемоглобина А (70—85%) и гемоглобина М в виде метгемоглобина (15—30%). Гомозиготная форма этого заболевания нежизнеспособна, поскольку все количество гемоглобина в организме оказалось бы нефункциональным — в виде метгемоглобина.
В таких случаях развитие цианоза зависит от структурной аномалии. Так, в случае гемоглобина М Iwate и гемоглобина М Boston, у которых структурня аномалия находится на цепях а, синюха появляется при рождении (цепи альфа включаются и в структуру гемоглобина Ф), в то время как при остальных гемоглобинах М со структурной аномалией на цепях бета, наличие синюхи отмечается на 3—4 месяце жизни, когда зрелый гемоглобин почти полностью заменяет гемоглобин Ф.
Признаки недостатка кислорода отмечаются, в принципе, либо при значительной концентрации метгемоглобина (30—40%), либо при осложнении основного заболевания другим патологическим состоянием, ведущим к уменьшению гемоглобина или его заниженной оксигенации в альвеолах легкого. Следует подчеркнуть, что, у страдающего метгемоглобинемией и показателем гемоглобина 12 г/100 мл крови по существу имеются лишь 7—8 г функционального гемоблобина (60—65%). Хронический тканевой недостаток кислорода объясняет компенсаторную полицитемию, наблюдаемую в отдельных случаях.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Метгемоглобинемия
МКБ-10
Общие сведения
Причины метгемоглобинемии
В процессе метаболических превращений в крови здоровых людей в очень небольших количествах образуются дисгемоглобины: карбоксигемоглобин, сульфгемоглобин, метгемоглобин (0,1-1 %). Вместе с тем, в эритроцитах содержится ряд факторов, которые поддерживают долю фракции метгемоглобина на уровне, не превышающем 1,0-1,5% от общего Hb. В частности, в реакции восстановления метгемоглобина в гемоглобин участвует фермент метгемоглобин-редуктаза. В отличие от оксигемоглобина (НbО2), содержащего восстановленное железо (Fe++), в метгемоглобине содержится окисленное железо (Fe+++), не способное переносить кислород. Поэтому при метгемоглобинемии, прежде всего, страдает кислородно-транспортная функция крови, следствием которой служит тканевая гипоксия.
Наследственные формы метгемоглобинемии представлены либо ферментопатиями (врожденной низкой активностью или отсутствием фермента метгемоглобин-редуктазы), либо М-гемоглобинопатиями (синтезом аномальных белков, содержащих окисленное железо).
В структуре приобретенных (вторичных) метгемоглобинемий выделяют токсические экзогенные и токсические эндогенные формы. Метгемоглобинемии экзогенного происхождения могут быть связаны с передозировкой лекарственных средств (сульфаниламидов, нитритов, викасола, противомалярийных препаратов, лидокаина, новокаина и др.) или отравлением химическими агентами (анилиновыми красителями, нитратом серебра, тринитротолуолом, хлорбензолом, питьевой водой и пищевыми продуктами с высоким содержанием нитратов и др.).
Повышенный уровень MtHb в крови наблюдается у недоношенных и доношенных новорожденных, что связано с низкой активностью фермента метгемоглобин-редуктазы и окислительным стрессом в родах. Однако даже при тяжелой гипоксии и желтухе новорожденных подъем MtHb не столь выражен и клинически значим, чтобы послужить причиной метгемоглобинемии. Однако при диарее, бактериальных и вирусных энтероколитах, в условиях метаболического ацидоза у детей первого года жизни может легко развиться приобретенная эндогенная метгемоглобинемия.
О смешанной форме патологии говорят в том случае, если метгемоглобинемия развивается под воздействием экзогенных факторов у здоровых лиц, являющихся гетерозиготными носителями генов наследственной формы заболевания.
Симптомы метгемоглобинемии
В зависимости от уровня фракции MtHb, выраженность проявлений врожденной и приобретенной метгемоглобинемии может значительно варьировать.
При концентрации MtHb в крови:
Для любых форм метгемоглобинемии характерна грифельно-серая окраска кожных покровов, однако отсутствуют характерные для сердечно-легочных заболеваний изменения ногтевых фаланг по типу «барабанных палочек». Акроцианоз усиливается при охлаждении, употреблении в пищу нитратосодержащих продуктов, при токсикозах беременности у женщин, а также приеме метгемоглобинобразующих медикаментов.
Диагностика метгемоглобинемии
Важным диагностическим признаком метгемоглобинемии служит темно-коричный цвет крови, которая, будучи помещенной в пробирку или на фильтровальную бумагу, не изменяет свой цвет на красный. При положительной пробе проводится спектроскопия, определение концентрации MtHb, активности НАД-зависимой метгемоглобинредуктазы, электрофорез гемоглобина.
В общем анализе крови может присутствовать компенсаторный эритроцитоз, увеличение Hb, ретикулоцитоз, уменьшение СОЭ. При исследовании биохимических показателей крови определяется незначительная билирубинемия, обусловленная увеличением непрямой фракции пигмента. Для хронической метгемоглобинемии типично появление в эритроцитах телец Гейнца-Эрлиха.
У больных с энзимопенической или токсической метгемоглобинемией показательна терапевтическая проба с внутривенным введением метиленового синего – после инъекции цианоз быстро исчезает, а кожа и видимые слизистые приобретают розовую окраску.
При анализе причин метгемоглобинемии важно выяснить, имел ли больной контакт с токсическими веществами, принимал ли метгемоглобинобразующие лекарственные препараты. При подозрении на врожденную метгемоглобинемию изучается родословная, проводится консультация генетика, определяется тип наследования патологии крови. Наследственные метгемоглобинемии требуют дифференциации с врожденными пороками сердца синего типа, аномалиями развития легких и другими состояниями, сопровождающимися гипоксией.
Лечение и профилактика метгемоглобинемии
Течение наследственной и лекарственной метгемоглобинемии, как правило, доброкачественное. Неблагоприятный исход возможен при тяжелых формах токсической метгемоглобинемии с высоким содержанием MtHb в эритроцитах. Пациентам с подобной патологией следует избегать контакта с метгемоглобинобразующими веществами, переохлаждений и других провоцирующих факторов. Профилактика врожденной метгемоглобинемии заключается в проведении медико-генетической консультации для выявления гетерозиготных носителей среди будущих родителей.