Общие сведения о работе надпочечников. Прегненолон
Прегненолон. Основы
Прегненолон, как и ДГЭА (дегидроэпиандростерон), это вырабатываемый телом человека стероидный гормон. Это гормон-прекурсор (предшественник), синтезируемый из холестерина, главным образом в надпочечных железах, но также и в печени, коже, головном мозге, яичках, яичниках и в сетчатке глаз.
Стероиды представляют собой большую семью биохимических веществ со сходной структурой, которые выполняют функцию определения пола, противовоспалительную функцию, а также регулируют процесс роста. На самом деле, прегненолон это крупный прекурсор, из которого образуются практически все остальные стероидные гормоны, в том числе ДГЭА, прогестерон, тестостерон, эстрогены и кортизол. Несмотря на свои мощные метаболиты (продукты обмена веществ), прегненолон не характеризуется каким бы то ни было серьёзным побочным действием, обладая минимальной или вовсе отсутствующей анаболической, эстрогенной или андрогенной активностью.
При проведении экспериментов на лабораторных мышах выяснилось, что прегненолон в 100 раз эффективнее улучшает память, чем другие стероиды или стероиды-прекурсоры. На данный момент прегненолон является самым действенным из всех известных средством улучшения памяти у животных. Людей же прегненолон делает не только умнее, но и счастливее, повышает работоспособность и вместе с тем усиливает ощущение благополучия. Также в отчетах о прегненолоне говорится, что он снижает утомление, вызванное сильным стрессом.
Также как и в случае со стероидным гормоном-прекурсором ДГЭА, уровень прегненолона снижается с возрастом. Многие врачи и учёные полагают, что восстановление прегненолона до юношеских уровней – это важный шаг в борьбе со старением и его симптомами. Прегненолон может быть одним из важнейших гормонов, поскольку обладает балансирующим эффектом. Это предшественник многих других гормонов, который способен при необходимости повышать или понижать их уровень.
К прочим положительным эффектам прегненолона можно отнести:
Прегненолон также действует как мощный нейростероид в головном мозге, модулируя передачу сигналов между нейронами и оказывая сильное влияние на процессы научения и памяти. Как и в случае с ДГЭА, уровень прегненолона естественным образом подскакивает в юности, после чего с годами начинает медленно, постепенно снижаться.
К 75-летнему возрасту наши тела продуцируют на 60% меньше прегненолона, чем в возрасте между 30-40 годами. По этой причине прегненолон считается одним из биомаркеров старения. Это как считать кольца на деревьях: измерив уровень прегненолона, в любой момент жизни человека, часто можно высказать обоснованную догадку о его/ее возрасте.
К гормонам, уровень которых с возрастом снижается, относятся:
Они также считаются биомаркерами старения. А поскольку прегненолон изначально предоставляет сырьё для производства всех прочих стероидных гормонов, параллельно со снижением его уровня будет снижаться и уровень этих гормонов.
По мере того как снижается запас гормонов молодости, прогрессирует и снижение качества нашей жизни. Мы постепенно начинаем испытывать спад, физический и умственный – прогрессирует потеря энергии, памяти, зрения и слуха, половой функции, артрит, сердечно-сосудистые заболевания и так далее. Дополнительный приём в небольших количествах этих нейрогормонов может замедлить эти процессы, связанные со старением, улучшая качество жизни путем омоложения организма до восстановления такого функционирования, которое характерно для организмов более молодых.
Прегненолон. Немного истории
Изучение прегненолона, как и его применение, началось с 1930-х гг. Исследования на людях проходили в 1940-х гг., в них участвовали заводские рабочие. Эти исследования были посвящены изучению действия прегненолона на предмет борьбы с утомлением и аутоиммунными нарушениями, в том числе ревматоидным артритом. Были получены хорошие результаты, отмечены улучшения. Однако, даже несмотря на доказательства того, что прогненолон был не только эффективным, но и безопасным, в 1949 г. его забраковали, когда появился новый лекарственный препарат – кортизон, выпущенный компанией Merck, который был назван панацеей от ревматоидного артрита.
Вскоре после того, как начали использовать кортизон и кортизол, появились синтетические стероидные гормоны – дексаметазон и позднее преднизон. Запомните, что эти стероиды в сотни раз мощнее, чем прегненолон (или ДГЭА, если уж на то пошло). Поскольку их можно было патентовать, фармацевтическим компаниям было выгоднее с политической и экономической точки зрения продвигать эти препараты, нежели прегненолон. Кроме того, по сравнению с прегненолоном, эти стероиды действовали очень быстро. И потребители, и врачи предпочитали сиюминутный результат. Тем не менее, было доказано, что у этих стероидных соединений есть серьёзные недостатки:
Помимо прочих тяжелых осложнений, они компрометируют иммунную систему и вызывают остеопороз.
Даже хотя кортизон и кортизол являются естественными для организма гормонами стресса, традиционно их применяют не в нормальном, естественном для тела количестве, а в фармакологических дозах. Фармакологические объёмы, в которых, как правило, назначают кортизон и кортизол, делают их приём таким же рискованным, как и приём синтетических гормонов.
Ученые многие годы изучали, как гормоны влияют на процессы научения и памяти. В ходе различных исследований было обнаружено, что прегненолон стимулирует мотивацию, способность к приобретению знаний и долговременную память. В 1940-х гг. исследовательская группа, состоящая из специалистов в области промышленной психологии, проводила испытания прегненолона на студентах и рабочих на предмет повышения производительности труда. Они обнаружили, что у студентов/рабочих существенно повышалась способность к обучению и запоминанию сложных заданий.
Также поразительно, что прегненолон не только повысил производительность труда студентов/рабочих – помимо этого, они испытывали душевный подъём, ощущение благополучия. Та же исследовательская группа провела испытания на заводских рабочих (занятых непосредственно на производстве), чтобы узнать, способен ли прегненолон улучшить и их производительность. Наиболее значительные показатели повышения производительности были отмечены у тех рабочих, чья работа в большей степени была сопряжена со стрессом – например, у тех, кто получал оплату за каждую произведенную единицу, чья зарплата напрямую зависела от продуктивности. Улучшение, хоть и менее выдающееся, было отмечено и у тех, чья зарплата была фиксированной и непосредственно от производительности не зависела. Прегненолон также не только повысил производительность, но и благоприятно сказался на настроении рабочих.
Как уже было упомянуто ранее, несмотря на положительную картину, изучение прегненолона было прекращено в 1950-х гг., когда стал доступен кортизон, немедленно названный средством от всех болезней. Поскольку прегненолон, в отличие от кортизона, невозможно было запатентовать, фармацевтические компании в продолжении исследований финансовой заинтересованности не выражали.
Очень жаль, что фармацевтические компании руководствуются такой финансовой системой и системой здравоохранения, которые накладывают определенные требования: любая молекула может приносить доход, только если ее можно запатентовать. Если бы прегненолон изучали хотя бы даже вполовину менее интенсивно, чем изучают патентуемые препараты, то терапевтический потенциал прегненолона мог бы иметь большие перспективы.
Где сосредоточен прегненолон?
Исследования, проводимые на людях, показывают, что концентрация прегненолона в нервной ткани значительно выше, чем в крови. Изучение прегненолона на животных показывает, что его концентрация в головном мозге в десять раз выше, чем концентрация других связанных со стрессом гормонов (в том числе ДГЭА).
Типичные причины подавления функции надпочечников
| Злость | Страх | Волнение/беспокойство |
| Депрессия | Вина | Переутомление/ физическое или умственное перенапряжение |
| Чрезмерные физические нагрузки | Недосыпание | Нарушение цикла дня и ночи |
| Поздний отбой | Хирургическое вмешательство | Травма/ранение |
| Хроническое воспаление | Хроническая инфекция | Хроническая боль |
| Экстремальные температуры | Отравления токсичными веществами | Мальабсорбция |
| Недостаточность пищеварения | Хроническое заболевание | Хронические тяжелые аллергии |
| Гипогликемия | Дефицит питательных веществ |
Связанные симптомы и последствия ухудшения функционирования надпочечных желёз
| Низкая температура тела | Слабость | Потеря волос неизвестной этиологии |
| Повышенная возбудимость | Сложности с набором мышечной массы | Раздражительность |
| Психическая депрессия | Сложности с набором веса | Настороженность |
| Гипогликемия | Неспособность сконцентрироваться | Резко усиленное чувство голода |
| Предрасположенность к воспалениям | Моменты замешательства | Несварение |
| Плохая память | Фрустрация | Чередующиеся диарея и запор |
| Остеопороз | Аутоиммунный гепатит | Аутоиммунные заболевания |
| Предобморочное состояние | Учащенное сердцебиение [трепетание, фибрилляция сердца] | Головокружение при вставании |
| Низкая сопротивляемость инфекциям | Низкое кровяное давление | Бессонница |
| Пищевые и/или аэрогенные аллергии | ПМС | Непреодолимая тяга к сладкому |
| Сухая и тонкая кожа | Головные боли | Скудное потоотделение |
| Непереносимость алкоголя |
Функции ДГЭА
Роль кортизола
Избыток кортизола
Сбалансированное питание для контроля уровня сахара в крови
Для поддержания нормальной функции надпочечников совершенно необходимо контролировать уровень сахара в крови, и следующие рекомендации вам в этом помогут:
Превышение нормы соотношения углеводов и белков приводит к повышенной секреции инсулина, что часто ведёт к периодической гипогликемии. В попытке нормализовать уровень сахара в крови тело запускает антагонистичный процесс, во время которого заставляет надпочечные железы вырабатывать повышенное количество кортизола и адреналина. Из этого следует, что чрезмерное потребление углеводов часто ведёт к чрезмерной секреции кортизола. Это вносит свой вклад в процесс истощения запасов кортизола и, следовательно, к истощению надпочечных желёз.
Для того чтобы стабилизировать уровень сахара в крови, необходимо поддерживать баланс двух гормонов – глюкагона и инсулина – которые вырабатываются поджелудочной железой. Белок, содержащийся в пище, индуцирует выработку глюкагона. А углеводы – выработку инсулина. Инсулин способствует накоплению жира (энергии). При чрезмерном потреблении углеводов тело вырабатывает много инсулина и мало глюкагона. Такой высокий уровень инсулина ведет к тому, что формируется и откладывается больше жира.
Когда уровень инсулина высокий, а уровень глюкагона низкий, надпочечные железы вынуждены производить много кортизола (из представленной далее в документе информации вы узнаете все о кортизоле) – это ответная мера, призванная помочь поднять уровень сахара в крови в отсутствие адекватного количества глюкагона. Всё это происходит за счёт надпочечников, что вносит свой вклад в процесс их истощения.
Сбалансированное питание
Оптимальное соотношение инсулина и глюкагона достигается при помощи диеты, в которой содержание углеводов и протеинов сбалансировано в пропорции примерно два к одному – т.е. в каждом приеме пищи или перекусе на один грамм белка и грамм жира должно приходиться два грамма углеводов.
Роль жиров
Для того чтобы контролировать количество поступающей в кровоток глюкозы (сахар крови), необходимо включать в каждый приём пищи небольшое количество (от 3/4 до 1 чайной ложки) жира (сливочного масла или растительного масла холодного отжима из овощей или семян).
Будет проще осуществлять такой гликемический контроль, если купить книги, в которых представлены таблицы питательной ценности, а также информация о гликемическом индексе. По таким таблицам вы сможете быстро определять, какие продукты вы хотели бы съесть, и будет ли ваше питание при употреблении таких продуктов должным образом сбалансированным.
Максимум пользы из сбалансированного питания
Поскольку нет такого баланса, который в точности подходил бы абсолютно всем людям, критически важно понимать роль каждого конкретного человека в разработке своего собственного идеального плана питания. Чтобы определить, насколько хорошо работает сбалансированная диета для поддержания уровня сахара в крови, нужно обращаться внимание на поведение собственного организма.
Прегненолон повышен у мужчин что это значит
Определение в крови концентрации одного из предшественников стероидных гормонов прегненолона, используемое для диагностики адреногенитального синдрома.
Иммуноферментный анализ (ИФА).
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
Общая информация об исследовании
Прегненолон – это один из предшественников синтеза стероидных гормонов, таких как кортизол, альдостерон и половые гормоны (тестостерон и эстрадиол). Его уровень исследуют при подозрении на адреногенитальный синдром.
Адреногенитальный синдром (другое название – врождённая гиперплазия коры надпочечников) – это группа наследственных нарушений синтеза стероидных гормонов, возникающих в результате дефицита одного из ключевых ферментов стероидогенеза. На сегодняшний день выявлено несколько мутаций в различных ферментах, приводящих к адреногенитальному синдрому. Наибольшее клиническое значение имеют следующие ферментопатии:
Хотя указанные ферментопатии имеют некоторые характерные клинические признаки, их дифференциальная диагностика опирается на лабораторное исследование, в ходе которого исследуют концентрацию нескольких стероидных гормонов и их предшественников. Чаще признаки адреногенитального синдрома выявляются в младенчестве или раннем детстве, однако известны случаи более поздней манифестации этой патологии.
На первом этапе подтверждают наличие адреногенитального синдрома и исключают наиболее часто встречающиеся ферментопатии (дефицит 21 и 11-гидроксилаз) с помощью исследования уровня кортизола, андростендиона и 17-гидроксипрогестерона. Если на основании полученных результатов указанные ферментопатии исключаются, переходят ко второму этапу исследования: исключение редких ферментопатий (дефицит 3-бета-гидроксистероиддегидрогеназы и 17-альфа-гидроксилазы) с помощью тестов на прегненолон и 17-гидроксипрегненолон. На основании результатов этих исследований и клинической картины удается установить точный диагноз. Характерные концентрации стероидных гормонов и некоторые другие диагностические признаки разных ферментопатий представлены в таблице:
21-гидроксилаза
11-бета-гидроксилаза
17-альфа-гидроксилаза
3-бета-гидроксистероиддегидрогеназы
Дисфункция надпочечников. Человек Уставший, продолжение.
Дисфункция – это как предболезнь. Заболевание еще не развилось, а жалобы есть, но они стертые, поэтому человеку плохо, но он не может понять, что с ним и с каким органом это состояние связать.
В современном обществе формируется неправильная тенденция социального поведения. Тебя постоянно подгоняют «еще, еще. больше работай, будь успешным, делай карьеру, но не забудь про семью, роди 2-3 детей (надо поднимать демографию страны), имей хобби, выучи языки, имей 2 образования, занимайся спортом, путешествуй, не забывай посещать театр (для кого-то ночной клуб, дискотеку), води машину и т.д.»
И как, скажите мне, человеку выдержать такой прессинг? Ни малейшего времени на передышку, на созерцание. Резервы организма ИМЕЮТ ПРЕДЕЛ, и у каждого свой срок «до срыва». И этим пределом часто является истощение функции надпочечников, одного из важнейших эндокринных органов.
Какими же симптомами дисфункция надпочечников может выражаться: (симптомы могут быть разной степени выраженности от минимальных до максимальных)
Как проверить работу надпочечников?
До 2015 года основным способом были: анализ крови на кортизол, АКТГ по часам 8:00- 24:00 (или еще промежуточно 13:00) и сбор суточной мочи на кортизол, кровь на ДГА-С. Это было крайне неудобно. Ни одна лаборатория, кроме расположенных в стационаре, кортизол в 24:00 не брала. А без этого показателя оценить функцию надпочечников правильно не возможно. Собирать суточную мочу не все соглашались, очень трудоемко и может быть не так достоверно.
С 2015-2016 года появился метод оценки кортизола слюны.
Собирается суточный профиль слюны на кортизол по 4 точкам 8:00- 13:00 и 17:00- 24:00.
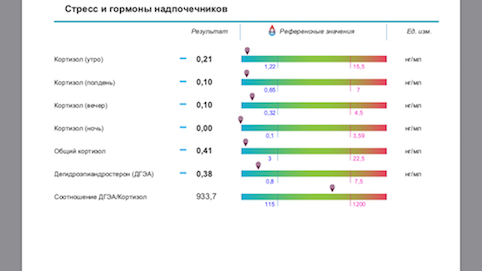
Ниже привожу материал лаборатории «CHROMOLAB» по исследованию состояния надпочечников и его интерпретации.
«Организм человека постоянно подвергается воздействию различных факторов внешней и внутренней среды. Это могут быть абиотические факторы, такие как холод, жара, атмосферное давление, влажность, недостаток кислорода. Избыток или дефицит поступающих в организм веществ (белков, углеводов, липидов), недостаток витаминов и микроэлементов, вирусная или микробная инфекция, токсины также оказывают определенное влияние. Негативные последствия имеют вредные привычки, физическая перегрузка, переедание, гиподинамия, нарушение ритма сна и бодрствования. Кроме того, к серьезным стрессорам относят техногенные и психологические воздействия: переизбыток компьютерной и телевизионной информации, монотонный труд, конфликты, чрезмерную рабочую нагрузку, эмоциональное истощение, завышенный уровень ответственности, общую неудовлетворенность и прочее. Все эти и многие другие причины ведут к постоянному напряжению физиологических резервов организма, который вынужден приспосабливаться (адаптироваться) к этим факторам или защищаться. Если воздействия носят интенсивный, внезапный или незнакомый («новый») характер, то организм отвечает на них универсальной (в формате «скорой помощи») физиологической реакцией, называемой СТРЕССОМ (стрессорной реакцией). Стрессорная реакция не связана с положительным или отрицательным восприятием внешних раздражителей, с которыми сталкивается человек. Она необходима для скорейшей адаптации организма с целью его защиты от гибели. Стресс – это защитная реакция организма. Однако длительная стрессорная реакция приводит к избыточному нерегулируемому ответу организма на повреждающий фактор и обратному эффекту. Вместо защитных процессов активируются деструктивные, что может стать пусковым механизмом для развития патологических состояний: сахарного диабета, тромбозов, инсультов, инфарктов, аритмии, бесплодия, эректильной дисфункции, аллергии, онкологических заболеваний, иммунодефицитов, ранней менопаузы, остеопороза, гипотиреоза, бессонницы, депрессии, ожирения, анорексии и многого другого. Стресс инициирует различные патологические состояния, и это зависит от провоцирующих факторов внешней и внутренней среды.»
Стадийность стрессорных реакций. Выделяют три стадии стресса (согласно Г. Селье):
Глубокое понимание механизмов регуляции стресса стало возможным благодаря исследованию процессов синтеза, обмена и метаболизма стероидных гормонов коры надпочечников: кортизола и дегидроэпиандростерона (ДГЭА), которые регулируют реализацию стрессорной реакции.
Согласно современным исследованиям, физиологический смысл этого феномена заключается в том, что ДГЭА – это мощный естественный антиглюкокортикоид, противостоящий кортизолу, уровень которого резко повышается при любом стрессе. Известно, что отношение ДГЭА к кортизолу следует рассматривать как ключевой маркер устойчивости организма к любому стрессу, для обеспечения которой в целях адекватной защиты в организме всегда должен превалировать уровень ДГЭА.
Оценку суточного ритма секреции кортизола по его концентрации в слюне (4-кратное определение в течение дня в разных порциях слюны) применяют для отличия стрессорной реакции от иных патологических состояний, связанных с дисфункцией секреции стероидных гормонов.
Оценка проводится только врачом.
Известно, что уровень кортизола – величина непостоянная, и он подвержен колебаниям в течение суток.
С 7 до 9 часов утра концентрация кортизола максимальна, в связи с чем утренний уровень этого гормона считается хорошим индикатором для определения функционального состояния надпочечников.
С 11 часов утра до 13 часов дня концентрация кортизола возвращается к среднему значению, что служит показателем адаптивной функции надпочечников.
С 15 до 17 часов дня уровень кортизола постепенно опускается.
С 22 часов вечера до полуночи концентрация гормона находится на самом низком уровне, что отражает нормальную надпочечниковую функцию.
Такое развернутое исследование надпочечников поможет определиться с диагнозом, нет ли здесь дебюта надпочечниковой недостаточности или это просто дисфункция и определиться с лечебной тактикой. Ведь кому-то надо будет отдохнуть и правильно питаться. А кому-то понадобится подобрать препараты гормонов надпочечников сроком от 1,5-3-х месяцев до пожизненной терапии при выявленной надпочечниковой недостаточности. Радует то, что надпочечниковая недостаточность встречается очень редко.
НО очень часто встречается дисфункция.
Особенную благодарность в идее составления этой статьи выражаю своему учителю Гострому Андрею Владимировичу.
Прегненолон повышен у мужчин что это значит
Исследование, направленное на определение в слюне концентрации прегненолона, который является одним из предшественников стероидных гормонов. Анализ используется в составе комплексной диагностики адреногенитального синдрома.
Высокоэффективная жидкостная хроматография с тандемной масс-спектрометрией.
Нг/мл (нанограмм на миллилитр).
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию
Общая информация об исследовании
Прегненолон является гормоном, синтез которого в организме осуществляется на основе холестерина в надпочечниках. Он играет роль промежуточного звена в реакциях биосинтеза стероидных гормонов: кортизола, альдостерона, половых гормонов (эстрогенов, прогестерона, тестостерона и др.). Кроме того, гормон синтезируется в определенных локализациях мозга, где проявляет самостоятельную биологическую активность в качестве нейростероида. Это позволяет принимать участие в процессах развития нейронов, миелинизации, оказывать нейропротективное действие.
Исследование слюны на прегненолон проводится методом высокоэффективной жидкостной хроматографии с тандемной масс-спектрометрией (ВЭЖХ). Этот современный метод позволяет выделить из образца соответствующий гормон на основе его физико-химических свойств, а затем подсчитать уровень его концентрации количественно. Анализ сочетает в себе простоту сбора материала с высокой точностью полученных результатов.
Для чего используется исследование?
Когда назначается исследование?
Что означают результаты?
Что может влиять на результат?
23 Кортизол в моче
8 17-гидроксипрогестерон (17-ОПГ)
42 Дегидроэпиандростерон-сульфат (ДЭА-SO4)
15 Тестостерон свободный
Кто назначает исследование
Эндокринолог, гинеколог, дерматовенеролог, педиатр, генетик, врач общей практики.