После диклофенака болит живот что делать
Как защитить желудок при длительном приёме НПВП
В каждой домашней аптечке лежит хотя бы одно нестероидное противовоспалительное средство (НПВП) – аспирин, диклофенак, ибупрофен и т.д. С их помощью можно быстро избавиться от боли, однако при длительном курсе лечения проявляется очень опасное побочное действие: эти лекарства вызывают поражение верхнего отдела пищеварительных путей, которое медики называют НПВП-гастропатией. Не все знают, как можно уберечь кишечник от этого заболевания.
Чем вызвано негативное влияние НПВП
Обезболивающие средства оказывают влияние на функционирование желудка: стимулируют выработку соляной кислоты и одновременно блокируют циклооксигеназу, защищающую стенки желудка. В результате желудочный сок начинает понемногу разъедать слизистую оболочку желудка и/или 12-перстной кишки, вызывая гастриты, эрозии, а впоследствии – язвенную болезнь этих отделов пищеварительного тракта. Поэтому врачи стараются не назначать нестероидные противовоспалительные лекарства курсом дольше месяца. Однако иногда без длительного приёма НПВП не обойтись, и тогда одновременно с этими лекарствами пациенты принимают гастроэнтеропротекторы.
Эффективная защита пищеварительного тракта
Гастроэнтеропротекторы используют для защиты желудка и кишечной стенки естественные механизмы, предусмотренные природой. В их функции входит:
стимуляция выработки простагландинов клетками слизистой оболочки, благодаря чему усиливается кровообращение в стенках желудка и кишечника;
Комплексный защитный эффект существенно снижает поражение тканей слизистых оболочек, поэтому очень важно принимать гастроэнтеропротекторы одновременно с НПВП.
Защита, которая не помогает
Некоторые пациенты считают, что не стоит тратиться на гастроэнтеропротекторы, когда можно защитить желудок простыми домашними средствами. К сожалению, защитный эффект оказывается недостаточным. Не пытайтесь заменить препарат, назначенный врачом, народными способами, в число которых входит:
Следует помнить, что у большинства лекарств есть побочные эффекты, и негативное действие нестероидных противовоспалительных средств сегодня могут купировать только гастроэнтеропротекторные препараты.
Как защитить желудок от НПВП — советы эксперта
Что вы делаете, когда болит голова, поднялась высокая температура или беспокоит боль в суставах? 90% опрошенных ответят: «Пью таблетку».
«Волшебные» пилюли
Существует группа препаратов, под общим названием нестероидные противовоспалительные (НПВП), которые мы все хотя бы раз в жизни, а многие регулярно, принимали. Это препараты, обладающие обезболивающим противовоспалительным и / или жаропонижающим действием. В качестве примера можно назвать Аспирин, Нурофен, Найс, Кетанов, Кетопрофен и прочие. Учитывая «волшебные эффекты» от их действия — снятие воспаления, боли и жара, — их назначают практически все, всем и всегда. Назначают травматологи, ревматологи, терапевты, лоры, стоматологи. Плюс, их можно совершенно свободно приобрести в любой аптеке. Но, наряду с «волшебными свойствами» эти лекарства обладают рядом побочных действий, которые можно разделить на 2 группы: кардиориски и гастро риски. Собственно о гастрорисках и пойдёт речь в данной статье.
НПВП-гастропатия
В научной литературе эта проблема называется «НПВП-гастропатия». Впервые термин был предложен в 1986 году для разграничения специфического поражения слизистой оболочки желудка, возникающего при длительном употреблении НПВП, от классической язвенной болезни.
Отличие НПВП-гастропатии от язвенной болезни можно проследить и по зоне поражения. Чаще всего язвы можно увидеть в желудке, а не в кишке. Плюс, изменения встречаются чаще у пожилых, а не у молодых людей.
Немного цифр
Немного статистики. В Великобритании назначается около 24 млн. НПВС в год. 70% лиц старше 70 лет принимают НПВС 1 раз в неделю, а 34% ежедневно. В США продается НПВС на сумму до 6 млрд. в год. Как следствие, риск развития желудочно-кишечных кровотечений (ЖКК) возрастает прободения — в 6 раз, риск смерти от осложнений до 8 раз. До всех случаев острых ЖКК связаны с НПВС.
Проблема эта актуальна и в нашей стране, к примеру по данным Научного Центра сердечно-сосудистой хирургии им. А.Н. Бакулева из 240 больных, ежедневно принимающих аспирин даже в малых дозах, на гастроскопии поражения желудка и 12 п.к выявлены у 30% (из них язвы — у 23,6%, эрозии — у 76,4%). Аналогичная картина у коллег из ВНИИ ревматологии РАМН — у 2126 пациентов, принимающих НПВС без «прикрытия» (защиты) желудка, эрозии и язвы гастродуоденальной зоны найдены в 33,8% случаев. Это очень впечатляющие и драматические цифры осложнений от приема НПВС, учитывая количество употребляющих эти препараты людей в развитых странах.
Как это работает?
Как же действуют эти препараты в наших желудках? Всё очень просто, негативное воздействие реализуется за счёт дисбаланса защитных и агрессивных сил. У нас в желудке существует ряд защитных механизмов, позволяющих противостоять натиску агрессоров. Среди последних:
Защищается желудок за счет мощного слоя слизи и бикарбонатов, которые нейтрализуют кислоту, адекватного кровоснабжения, способности очень быстро регенерировать. Когда мы используем НПВС препараты, баланс сил изменяется в сторону агрессивных механизмов и происходит поражение слизистого и подслизистого слоя желудка и кишки.
Диагностика
Для диагностики подобных изменений используется гастроскопия, являющаяся «золотым стандартом». Интересный факт, дело в том, что порядка 40% больных с эрозивно-язвенными изменениями, принимающих эти препараты длительно (более 6 недель) не ощущают никакого дискомфорта или неприятных, болезненных ощущений. Проблемы с желудком диагностируются лишь при походе к другим врачам, а не к гастроэнтерологу. И, наоборот, у 40% пациентов, на фоне жалоб, которые они предъявляют, ничего не находят.
Что же делать в таком случае?!
Алгоритм действий для пациентов, не имеющих проблем с желудком, и тех, у кого в анамнезе была язвенная болезнь или эрозивные изменения, различен. Для первой группы, при назначении нестероидных противовоспалительных препаратов более, чем на 5 дней, обязательно назначение препаратов из группы ингибиторов протонной помпы (ИПП). Таких как, омепразол, пантопразол, рабепразол и т. д. (на весь курс приема). Для второй группы, любые назначения из группы НПВС, независимо от срока приёма, требуют параллельного назначения ингибиторов протонной помпы. Так же обязателен прием ИПП пациентам, принимающих длительно аспирин.
Мифы, с которыми мы сталкиваемся в ежедневной практике
Миф 1. Использование НПВС препаратов в виде свечей является менее агрессивным для желудка, нежели приём таблеток
Это 100% миф. Патогенное, разрушительное действие лекарства реализуется через кровь, доставляющую его по сосудам в желудок.
Миф 2. В качестве «гастропротекторов» можно использовать лекарства из группы антацидов — Ренни, Маалокс, Фосфалюгель и H2-блокаторы (Ранитидин и Фамотидин)
В данном случае они не эффективны.
Миф 3. Принимать ингибиторы протонной помпы можно нерегулярно
Дело в том, что если пожилому человеку назначили на всю жизнь противовоспалительный препарат, абсолютно бессмысленно назначать гастропротекцию на месяц. В подобных случаях лекарства должны приниматься строго параллельно.
Миф 4. В качестве «гастропротекторов» могут выступать пищевые продукты (кисели и пр.)
Этот миф, как абсолютно фантастический, мы оставим без комментариев.
Как выбрать лекарство
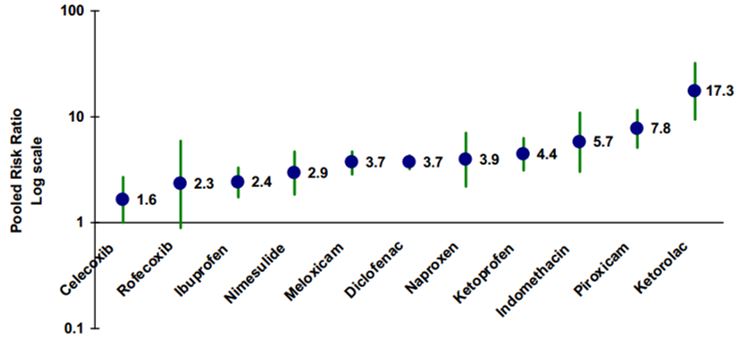
На самом деле, самым важным моментом является то, какие именно лекарства мы принимаем. На рисунке можно увидеть шкалу агрессивности различных препаратов из группы НПВС по отношению к желудку.
Самыми агрессивными препаратами являются Аспирин, Кеторолак, Пироксикам, Индометацин. По возможности рекомендуется использовать селективные препараты, которые обладают минимальными гастро-рисками. Их применение всегда более желательно, к ним относится Целекоксиб и Рофекоксиб. Но несмотря на их относительную безопасность, назначать их должен строго по показаниям лечащий доктор, не забывайте об этом.
Про Helicobacter pylori
Еще одним очень важным компонентом профилактики осложнений, является диагностика инфекции Helicobacter pylori у пациента планирующего длительно принимать НПВС (особенно аcпирин). Наличие бактерии увеличивает риски эрозивно-язвенных поражений ЖКТ и кровотечения в При её выявлении должна в обязательном порядке проводится эрадикация (уничтожение этой бактерии).
Резюме
Итак делаем выводы:
Защемление седалищного нерва
Защемление седалищного нерва – дискомфорт в нижней части тела, связанный со сдавливанием или раздражением самого нерва. Чаще всего недугу подвержены люди старше 30 лет.
Седалищный нерв – самый большой в нашем организме. Он охватывает большую часть тела – от пояснично-крестцового отдела позвоночника, далее проходит в ягодицу, по задней поверхности бедра и к нижней части ноги. Потому важно следить за его состоянием. Малейшее раздражение в одной части нерва приведет к боли по всему его участку. При отсутствии своевременного лечения постепенно теряется чувствительность и подвижность нижних конечностей.
Защемление может появиться из-за:
Поэтому специалисты разделяют недуг на два вида – первичный и вторичный. Первичный связан с пережатием нервного ствола поврежденной мышцей, а вторичный вызван патологией позвоночного столба, тазобедренных суставов, а возникает на фоне беременности или заболеваний органов малого таза.
Защемление нерва может развиваться быстрее при наличии лишнего веса. Также важно следить за поступлением необходимых витаминов и минералов в организм, так как их отсутствие или недостаток приводит к риску ускоренного развития заболевания.
Симптомы и лечение при защемлении седалищного нерва
Этот недуг довольно болезненный и бесследно не пройдет. Потому при появлении первых симптомов стоит показаться специалисту – неврологу, невропатологу или терапевту. Он назначит необходимое лечение и медицинские препараты.
Симптомы защемления седалищного нерва
Именно при наличии данных симптомов невропатологи, неврологи и терапевты диагностируют защемление седалищного нерва. Если у специалиста есть сомнения, то для полного прояснения ситуации пациента направляют на КТ или МРТ. По результатам процедур будут определены диагноз и лечение.
Симптомы у женщин при защемлении седалищного нерва
Недуг может возникнуть во время беременности. На втором или третьем триместре увеличенная матка давит на тазовые мышцы, тем самым вызывает спазм. У будущей мамы происходит перераспределение центра тяжести и смещаются поясничные позвонки. Также в области малого таза растущая голова плода сдавливает седалищный нерв.
На боли в пояснице жалуются от 40 до 80% беременных женщин. Однако не всегда причиной тому защемление седалищного нерва, оно наблюдается лишь в 5% случаев.
Врачи говорят, что недуг может пройти после родов. Однако терпеть боль до этого момента не стоит, лучше показаться специалисту, чтобы избежать серьезных последствий и усиления боли.
Лечение защемления седалищного нерва
Чаще всего боль настигает внезапно. Потому перед обращением к специалисту нужно проделать несколько простых шагов:
Неотложную медицинскую помощь необходимо вызывать при нестерпимой боли, которая не притупляется и не подавляется анальгетиками. В случаях более благоприятных тоже необходима медицинская помощь. Лучше всего обратиться к неврологу, невропатологу или терапевту. Как только боль будет купирована, обратитесь к врачу в местной клинике.
Как лечат защемление седалищного нерва?
После опроса о симптомах и осмотра врач направляет пациента на рентген, УЗИ, КТ, МРТ или общий и биохимический анализ крови. Процедуры необходимы для того, чтобы определить масштаб проблемы. Также на основе их результатов врач устанавливает причину защемления седалищного нерва и обнаруживает воспаления.
После чего специалисты прописывают противовоспалительные препараты, комплекс витаминов группы «В» и миорелаксанты. Также пациент может получить направление на физиотерапию и ЛФК. Обычно процедуры назначаются при нестерпимой боли, которая не уходит даже после комплексного лечения. В особых случаях доктор может прописать и дополнительные витаминные комплексы, антиоксиданты и обезболивающие средства. Таким образом будут сниматься не только симптомы недуга, но и начнется борьба с болезнью-возбудителем.
Дополнительно специалисты назначают и санаторно-курортное лечение, которое подразумевает бальнеологические процедуры, например, грязелечение.
При защемлении седалищного нерва к хирургическому вмешательству врачи обращаются редко. В таком случае показаниями будут запущенные формы остеохондроза, которые не поддаются терапии, или же объемные процессы в пораженной области – опухоли или абсцессы.
Сравнительная оценка влияния нимесулида на верхние отделы желудочно-кишечного тракта
Показано, что нимесулид оказывает значительно меньшее негативное влияние на верхние отделы желудочно-кишечного тракта, чем другие неселективные нестероидные противовоспалительные препараты (диклофенак, кетопрофен и индометацин).
Nimesulide has significantly less negative impact on the upper gastrointestinal tract than other non-selective non-steroidal anti-inflammatory drugs (diclofenac, ketoprofen and indomethacin).
Нимесулид — один из наиболее популярных в России представителей группы нестероидных противовоспалительных препаратов (НПВП). Это лекарство имеет в нашей стране репутацию эффективного и достаточно безопасного анальгетика и широко используется в различных отраслях медицины (прежде всего, в ревматологии, неврологии и травматологии), в которых имеется необходимость борьбы с острой или хронической болью [1–3].
Одной из главных особенностей российского опыта применения нимесулида является нередкое использование его продолжительными курсами. В большинстве стран мира нимесулид рассматривается прежде всего как ургентное обезболивающее средство; учитывая ограничения контролирующих органов, он назначается лишь на короткое время, обычно менее двух недель [4]. В нашей стране, напротив, нимесулид часто рекомендуют больным с хроническими заболеваниями, такими как остеоартроз (ОА), ревматоидный артрит (РА) и анкилозирующий спондилоартрит (АС). При этой патологии суммарный срок приема нимесулида у российских пациентов может достигать многих месяцев и даже лет.
Такая практика дает большой материал для оценки достоинств и недостатков лекарства, прежде всего, его безопасности.
Как известно, главной проблемой НПВП является риск развития побочных эффектов со стороны желудочно-кишечного тракта (ЖКТ) и сердечно-сосудистой системы [5, 6]. При этом основным достоинством нимесулида считается хорошая гастроинтестинальная переносимость, что, собственно, определяет основное преимущество этого препарата в сравнении со многими другими НПВП [1–4, 7].
Однако четких доказательств, подтверждающих низкий риск серьезных ЖКТ-осложнений (таких как кровотечения и клинически выраженные язвы) при использовании нимесулида, относительно немного. Имеются лишь немногочисленные работы, в которых специально изучалась частота таких опасных побочных эффектов, и отдельные исследования, организованные в соответствии с жесткими современными критериями «доказательной медицины», — двойные слепые, рандомизированные и контролируемые [7–9].
В этом случае большое значение приобретает анализ частоты осложнений, которые отмечаются в реальной клинической практике. Так, в клинику ФГБУ НИИР им. В. А. Насоновой РАМН ежегодно поступает для стационарного лечения большое число пациентов с различными ревматическими заболеваниями (РЗ) — ревматоидным артритом (РА), остеоартрозом (ОА), серонегативными спондилоартритами (ССА) и др., которые в течение длительного времени принимают НПВП, в т. ч. нимесулид. В данном учреждении функционирует собственный эндоскопический кабинет, основным направлением работы которого является выявление патологии верхних отделов ЖКТ. Результаты обследования больных РЗ, которые находятся в архиве кабинета эндоскопии, позволяют получить достаточно большой материал для оценки частоты патологии верхних отделов ЖКТ, возникающей на фоне приема НПВП.
Целью настоящего исследования было оценить сравнительную частоту и характер изменений верхних отделов ЖКТ у больных РЗ, регулярно принимавших нимесулид.
Материал и методы исследования
Мы провели ретроспективный анализ результатов всех эндоскопических исследований верхних отделов ЖКТ (эзофагогастродуоденоскопия (ЭГДС)), выполненных за период 2011–2013 гг. в клинике ФГБУ НИИР им. В. А. Насоновой РАМН больным РЗ, которые не менее 1 месяца до проведения данной процедуры получали нимесулид. В качестве контроля были использованы результаты ЭГДС, проведенных в тот же период всем больным, не менее месяца получавшим другие неселективные НПВП.
Все пациенты были направлены на эндоскопическое исследование лечащими врачами в связи с наличием определенных показаний: для исключения патологии верхних отделов ЖКТ из-за наличия симптомов гастроэзофагеального рефлюкса, гастралгии или диспепсии, наличия в анамнезе язвы желудка или двенадцатиперстной кишки (ДПК), для поиска источника анемии, для проведения онкопоиска, при необходимости взятия биопсии слизистой оболочки ДПК на амилоид и др.
Критериями отбора больных для проведения анализа являлся возраст старше 18 лет и зафиксированный в медицинской документации факт регулярного использования НПВП в течение не менее 1 месяца до момента до проведения ЭГДС.
В анализ не включались данные эндоскопического исследования у больных системными РЗ, при которых поражение ЖКТ может быть проявлением висцеральной патологии: системной склеродермией, поли/дерматомиозитом, системной красной волчанкой, болезнью Бехчета и системными васкулитами. В контрольную группу также не были включены пациенты, использовавшие мелоксикам, целекоксиб и эторикоксиб; принимавшие участие (на момент проведения ЭГДС) в клинических исследованиях, в которых изучалась безопасность НПВП; направленные на ЭГДС для контроля результатов курсового лечения язвы желудка, и/или ДПК, или эрозивного эзофагита.
Суммарно за три года ЭГДС была выполнена 1048 больным, соответствующим критериям отбора и принимавшим нимесулид, а также 816 больным, использовавшим другие неселективные НПВП. Этими препаратами были в основном диклофенак, кетопрофен, индометацин, ацеклофенак и ибупрофен; лишь единичные больные регулярно принимали пироксикам, теноксикам, кеторолак или метамизол.
Клиническая характеристика больных в исследуемых группах представлена в таблице.
Как видно, большинство пациентов были женщины среднего возраста, страдавшие ревматоидным артритом. В целом исследуемые группы были сопоставимы — правда, в контрольной группе было достоверно больше пациентов, страдающих ССА (преимущественно анкилозирующим спондилоартритом). Этот факт объясняет более высокую долю лиц мужского пола в контрольной группе. Следует отметить, что больные, принимавшие нимесулид, чаще имели язвенный анамнез, чаще принимали глюкокортикоиды (ГК) и достоверно реже — ингибиторы протонной помпы (ИПП).
При анализе результатов ЭГДС мы учитывали выявление эрозий, под которыми подразумевался поверхностный дефект слизистой, не имеющий видимой глубины, и язв — локального повреждения стенки ≥ 5 мм, имеющего видимую глубину. При обнаружении менее 10 эрозий они описывались как «единичные», а при выявлении ≥ 10 — как «множественные».
Электронная база данных была создана с помощью программы Microsoft Office Excel 2007, статистический анализ проводился с помощью программы SPSS 10.0. Приведенные в статье цифровые значения представлены в виде M ± m. Для оценки значимости отличия количественных параметров использован t-тест Стьюдента, для качественных параметров — χ 2 или точный тест Фишера.
Результаты
Общее число больных с эрозиями или язвами в группе 1 составило 244 (23,3%), в группе 2 — 272 (33,3%), р 65 лет) на частоту язв желудка и/или ДПК.
Оказалось, что язвы значительно чаще выявлялись у лиц, имевших язвенный анамнез. Так, в группе 1 у больных с этим фактором риска суммарная частота язв желудка и/или ДПК оказалась 11,5%, без — 3,1% (р 65 лет, принимавших нимесулид, частота язв составила 9,9%, более молодого возраста — 3,5% (р 65 лет) частота язв была намного ниже, чем в целом по группе. Тем не менее, язвы существенно чаще выявлялись в группе 2. Так, в группе 1 у 752 больных без факторов риска язвы были выявлены лишь у 16 (2,1%), а в контрольной группе — у 48 из 568 (8,5%), р 65 лет). Так, применение ИПП было отмечено у 16,2% больных из группы 1, имевших вышеуказанные факторы риска, и лишь у 5,3% не имевших; аналогично, в группе 2 эти препараты получали 26,2% и 5,6%.
Отдельным объектом нашего анализа стала оценка частоты патологии пищевода. Эрозивный эзофагит был выявлен лишь у небольшого числа больных (в сравнении с патологией желудка и ДПК). Тем не менее, эрозивный эзофагит достоверно реже выявлялся у пациентов в группе 1 — у 15 (1,4%), в сравнении с 26 (3,1%) в группе 2, р = 0,03.
Такие факторы риска, как пожилой возраст и ГК, не ассоциировались с более высокой частотой патологии пищевода ни в группе 1, ни в группе 2. В то же время эрозивный эзофагит достоверно чаще выявлялся у пациентов в группе 2, получавших НДА (но не в группе 1). Прием бисфосфонатов оказался однозначно важным фактором риска — и в группе 1, и группе 2, при использовании этих препаратов эрозивный эзофагит определялся достоверно чаще (p
А. Е. Каратеев, доктор медицинских наук, профессор
ФГБУ НИИР им. В. А. Насоновой РАМН, Москва
После диклофенака болит живот что делать
Первый Московский государственный медицинский университет им. И.М. Сеченова, Клиника пропедевтики внутренних болезней, гастроэнтерологии и гепатологии
Первый Московский государственный медицинский университет им. И.М. Сеченова, Клиника пропедевтики внутренних болезней, гастроэнтерологии и гепатологии
Профилактика желудочно-кишечных осложнений при приеме антитромбоцитарных препаратов
Журнал: Доказательная гастроэнтерология. 2012;(2): 77-82
Корнеева О. Н., Драпкина О. М. Профилактика желудочно-кишечных осложнений при приеме антитромбоцитарных препаратов. Доказательная гастроэнтерология. 2012;(2):77-82.
Korneeva O N, Drapkina O M. Prophylaxis of gastrointestinal complications associated with the intake of antiplatelet age. Russian Journal of Evidence-Based Gastroenterology. 2012;(2):77-82.
Первый Московский государственный медицинский университет им. И.М. Сеченова, Клиника пропедевтики внутренних болезней, гастроэнтерологии и гепатологии
Антитромбоцитарные препараты, служащие обязательным атрибутом современной терапии ишемической болезни сердца, ассоциируются с повреждением слизистой желудочно-кишечного тракта. Клинические исследования показали, что ингибиторы протонной помпы (ИПП) уменьшают число рецидивов желудочно-кишечных кровотечений у пациентов, относящихся к группе высокого кардиологического риска и получающих антитромбоцитарные средства. В связи с длительным приемом такими пациентами множества лекарственных средств встает вопрос об их взаимодействии. При назначении ИПП больному с кардиологической проблемой из группы риска по развитию гастропатии необходимо также учитывать безопасность препарата. Препаратом выбора среди ИПП может служить оригинальный пантопразол (Контролок, Никомед), обладающий свойством минимального лекарственного взаимодействия и доказанной высокой безопасностью и эффективностью.
Первый Московский государственный медицинский университет им. И.М. Сеченова, Клиника пропедевтики внутренних болезней, гастроэнтерологии и гепатологии
Первый Московский государственный медицинский университет им. И.М. Сеченова, Клиника пропедевтики внутренних болезней, гастроэнтерологии и гепатологии
В Российской Федерации распространенность сердечно-сосудистых заболеваний (ССЗ) достигла масштаба эпидемии. Пациенты с кардиологическими нарушениями преобладают на приеме не только у терапевтов, но и у врачей других специальностей. О каких больных из этой группы думает гастроэнтеролог? Конечно, речь идет о тех из них, кто принимает антитромбоцитарные препараты и нестероидные противовоспалительные средства. Согласно современным рекомендациям, с целью профилактики сердечно-сосудистых осложнений пациентам с ишемической болезнью сердца (ИБС) показано применение антитромбоцитарных препаратов (аспирин, клопидогрел, тиклопидин) [1]. Между тем для купирования боли, обусловленной сопутствующими заболеваниями (артриты, костно-мышечная патология и др.), больные зачастую бесконтрольно принимают множество самых разнообразных нестероидных противовоспалительных средств (НПВС).
Учитывая повсеместное назначение антитромбоцитарных препаратов для продолжительного приема, вопросы безопасности данной терапии становятся весьма актуальными. Использование антитромбоцитарных препаратов и НПВС ассоциируется с повреждением слизистой верхних отделов желудочно-кишечного тракта (ЖКТ), включая эрозивно-язвенные поражения, желудочно-кишечные кровотечения и перфорацию [2, 3].
У лиц, регулярно принимающих НПВС, в 25% случаев возникает язвенное поражение ЖКТ, а частота развития кровотечений и перфораций составляет 2-4% [4, 5].
Частота крупных желудочно-кишечных кровотечений при применении аспирина составляет от 1,8 до 3,7%, а при приеме двойной антитромбоцитарной терапии (аспирин и клопидогрел) от 3,0 до 4,9% в зависимости от дозы аспирина (75-325 мг) [6]. Развитие кровотечений верхних отделов ЖКТ на фоне малых доз аспирина составляет 0,5% в год (относительный риск (ОР) по сравнению с плацебо составляет 2,07; 95% ДИ 2,61-2,66) [7]. В семь раз увеличивается риск развития желудочно-кишечных кровотечений на фоне комбинации клопидогрела и аспирина (отношение шансов (ОШ): 7,4; 95% ДИ 3,5-15) по сравнению с монотерапией аспирином [8].
Оценка риска нежелательных эффектов НПВС и антитромбоцитарных препаратов на желудочно-кишечный тракт
Факторы риска негативного действия антитромбоцитарных средств и НПВС на ЖКТ сформулированы в рекомендациях, приведенных в American College of Gastroenterology, по предотвращению осложнений гастропатии, индуцированной НПВП. Выделены градации по степени риска негативного действия НПВС на ЖКТ: высокий, умеренный и низкий риск [9]. Кроме того, наличие инфекции пилорического хеликобактера служит независимым и дополнительным фактором риска, который необходимо рассматривать отдельно (см. таблицу).
Исходя из данных рекомендаций, многие пациенты кардиологического профиля даже при отсутствии язвенного анамнеза относятся к группе высокого риска по развитию желудочно-кишечных осложнений при приеме НПВС и антитромбоцитарных средств.
НПВС и аспирин чаще всего принимают пациенты старше 60 лет, из-за своего возраста сразу оказываясь в группе высокого риска. Повышенная частота развития желудочно-кишечного кровотечения и перфорации в пожилом возрасте по сравнению с более молодыми лицами объясняется возрастным уменьшением эндогенного синтеза простагландинов. Кроме того, доказано, что в пожилом возрасте непосредственно страдают защитные механизмы гастродуоденальной слизистой оболочки: снижаются кровоток, синтез муцина и секреция бикарбонатов. Старший возраст негативно влияет на течение язвенной болезни [10].
Более того, большинство пожилых пациентов вынуждено длительно принимать аспирин, клопидогрел, двойную, а иногда и тройную антитромбоцитарную терапию (аспирин, клопидогрел, варфарин). Не редкость и параллельный прием НПВС.
Ингибиторы протонной помпы: целесообразность профилактического назначения
Врачам-клиницистам приходится оценивать соотношение риск/польза и балансировать между положительными эффектами антитромбоцитарной терапии в предотвращении сердечно-сосудистых нарушений и соблюдением древнего врачебного принципа «не навреди».
Очевидно, что необходимо проводить профилактику НПВС-гастропатии и желудочно-кишечных кровотечений на фоне антитромбоцитарной терапии. Действенным способом снижения высокого риска желудочно-кишечных осложнений, обусловленного антитромбоцитарными препаратами, может служить дополнительное назначение ингибиторов протонной помпы (ИПП). Согласно международным рекомендациям, ИПП служат препаратами выбора для терапии и профилактики НПВС-индуцированных гастропатий и поражений ЖКТ на фоне антитромбоцитарной терапии.
Эффективность такого подхода продемонстрирована при лечении НПВС, при монотерапии аспирином и при двойной антитромбоцитарной терапии аспирином и клопидогрелом.
Так, риск язвенного поражения желудка и двенадцатиперстной кишки, индуцированного приемом НПВС, снижается на фоне применения ИПП (ОР 0,37; 95% ДИ 0,27-0,51) [11].
В исследовании А. Lanas и соавт. [12] с участием 2777 пациентов с кровотечениями из верхних отделов ЖКТ и 5532 из группы контроля прием ИПП ассоциировался со снижением риска кровотечений как для принимающих низкие дозы аспирина (ОШ 0,32; 95% ДИ 0,22-0,51), так и для принимающих клопидогрел (ОШ 0,19; 95% ДИ 0,07-0,49).
У пациентов с ИБС, получающих двойную антитромбоцитарную терапию аспирином и клопидогрелом, профилактическое назначение ИПП приводит к уменьшению частоты кровотечений из верхних отделов ЖКТ. Такие результаты были получены в ходе крупного плацебо-контролируемого рандомизированного исследования COGENT с участием больных в количестве 3761 человека, нуждающихся в длительной двойной антитромбоцитарной терапии (перенесших острый коронарный синдром или коронарное стентирование) [13].
Добавление омепразола в дозе 20 мг в сутки к комбинации аспирина и клопидогрела сопровождалось достоверным уменьшением риска желудочно-кишечных кровотечений на 45%. В группе больных, получавших ИПП, реже отмечались как любые желудочно-кишечные нарушения (ОР=0,34; 95% ДИ 0,18-0,63; р 
Как избежать лекарственного взаимодействия
В настоящее время в медицинском мире активно обсуждается вопрос о взаимодействии и безопасности сочетания клопидогрела с ИПП (особенно с омепразолом), так как ИПП потенциально способны уменьшить количество активного метаболита клопидогрела и выраженность его антитромбоцитарного действия. Определенный генетический полиморфизм, высокая вероятность лекарственных взаимодействий в системе цитохрома P-450 при добавлении ИПП может приводить к изменениям антитромбоцитарной эффективности клопидогрела ИПП [15].
Метаболизм клопидогрела и 2-оксо-клопидогрела в большой степени зависит от индукции или ингибирования CYP2C19, что обусловлено влиянием различных лекарственных препаратов, а также индивидуального генетического полиморфизма [16].
Применение ИПП может ингибировать превращение клопидогрела в активный метаболит за счет влияния на CYP2C19, приводя к ослаблению его антитромбоцитарной активности. Риск отсутствия эффективности лекарственного препарата возрастает, когда его концентрация зависит от изменчивой активности единственного пути метаболизма. Такой высокий фармакокинетический риск обнаружен у клопидогрела [17].
Другим объяснением влияния ИПП на активность клопидогрела может служить изменение внутрижелудочного рН на фоне приема ИПП, что меняет всасывание клопидогрела. ИПП блокируют протонную помпу париетальных клеток желудка, и восстановление внутрижелудочного рН возможно лишь с прекращением длительного терапевтического эффекта ИПП, через 12-24 ч.
Кроме того, фармакокинетическое и антитромбоцитарное тестирование активного метаболита клопидогрела показало, что концентрация и антитромбоцитарные эффекты препарата различаются в зависимости от генетического полиморфизма фермента CYP2C19. Аллель CYP2C19*1 обусловливает полностью функционирующий метаболизм клопидогрела. Аллели CYP2C19*2 и *3 не обеспечивают эффективного метаболизма клопидогрела. У пациентов с двумя аллелями сниженной активности (гомозиготы) наблюдается медленная метаболизация клопидогрела. Определенный генетический полиморфизм может приводить к увеличению сердечно-сосудистого риска на 50% и к трехкратному увеличению риска тромбоза стентов у больных, получающих клопидогрел [18].
Клиническая эффективность совместного применения ингибиторов протонной помпы и клопидогрела
Лишь одно рандомизированное клиническое исследование, упомянутое выше COGENT, было посвящено взаимосвязи между клопидогрелом и ИПП. Доказано отсутствие влияния ИПП на увеличение сердечно-сосудистого риска при параллельном статистически достоверном снижении риска желудочно-кишечных осложнений.
Возможности пантопразола в профилактике желудочно-кишечных осложнений на фоне антитромбоцитарных препаратов
На сегодняшний день последние рекомендации (ACCF/ACG/AHA 2010 Expert Consensus Document on the Concomitant Use of Proton Pump Inhibitors and Thienopyridines) не указывают на приоритетное назначение того или иного ИПП на фоне антитромбоцитарной терапии. Ретроспективное исследование (W. Ray, 2010) с участием 20 596 больных не показало значимого влияния ни одного из используемых ИПП (эзомепразол, лансопразол, омепразол, рабепразол, пантопразол) на увеличение частоты сердечно-сосудистых эпизодов [22].
Последний метаанализ S. Shukla и S. Guba не позволяет сделать вывод о том, что ИПП снижают активность клопидогрела. Но все же одновременно с клопидогрелом авторы рекомендуют назначать не омепразол, а пантопразол или рабепразол, поскольку последние не влияют на систему цитохрома 2C19.
Исходя из знаний фармакокинетических свойств ИПП и их влияния на систему цитохрома Р-450, можно говорить о преимуществах назначения пантопразола (Контролок, Никомед) пациентам с сердечно-сосудистой патологией, получающим антитромбоцитарные препараты.
Пантопразол имеет более низкую афинность к печеночной системе цитохрома Р-450, не влияет на ее активность и не дает клинически значимых реакций со многими лекарственными препаратами, в том числе с антитромбоцитарными средствами и НПВС. Это значительно расширяет область его применения, поскольку пантопразол больше подходит для назначения совместно с другими медикаментами, позволяя с большей уверенностью предположить, что их действие не изменится в сторону усиления, ослабления или извращения. В результате действие других лекарственных препаратов, метаболизирующихся с участием ферментных систем данного цитохрома, не ослабляется, что особенно актуально у пожилых больных с кардиологическими проблемами, вынужденных одновременно принимать несколько препаратов.
При более широком диапазоне рН пантопразол накапливается в париетальных клетках и вступает во взаимодействие с тиольной группой протонной помпы. Будучи более стабильным соединением, пантопразол с меньшей вероятностью прореагирует с тиольными группами белков вне париетальной клетки, что позволяет рассчитывать на его прогнозируемые фармакокинетические свойства [24].
Если говорить о лекарственном взаимодействии между антитромбоцитарными препаратами и пантопразолом, то последний обладает низкой способностью вступать в данное межлекарственное взаимодействие. Это связано с меньшей афинностью пантопразола по сравнению с другими ИПП к изоферментам CYP2C19 и CYP3A4.
В отличие от большинства продуктов, образующихся в фазе I биотрансформации других ИПП, первоначальный метаболит пантопразола 4-гидроксипантопразол, образуемый системой CYP, очень быстро покидает систему цитохрома Р-450, в результате чего нивелируется возможность конкуренции с разными лекарственными препаратами на уровне изоферментов CYP. 4-гидроксипантопразол затем биотрансформируется вторично (фаза II) посредством конъюгации с сульфатом в цитозоле. Эту реакцию конъюгации часто расценивают как причину более низкой способности пантопразола вступать в межлекарственные взаимодействия.
Заключение
Необходимость длительного приема антитромбоцитарных препаратов связана с повышением риска развития поражения желудочно-кишечного тракта. Дополнительный профилактический прием ИПП достоверно снижает риск желудочно-кишечных кровотечений, но вызывает противоречивые мнения по поводу ослабления антитромбоцитарной эффективности и по проблеме лекарственного взаимодействия. Метаболизм как ИПП, так и антитромбоцитарных средств изоферментами CYP печеночной системы цитохрома Р-450, а также индивидуальный генетический полиморфизм определяют эффективность и безопасность данной комбинации. Среди ИПП оригинальный препарат пантопразола (Контролок, Никомед) обладает наименьшей способностью межлекарственного взаимодействия и может служить препаратом выбора при назначении пациентам кардиологического профиля с высоким риском развития желудочно-кишечных осложнений, вынужденным постоянно получать антитромбоцитарную терапию.

_575.gif)

