Инструкция по применению препарата Полиоксидоний®, раствора для инъекций и местного применения
Полиоксидоний ®
Раствор для инъекций и местного применения
Инструкция по применению препарата Полиоксидоний ® раствор для инъекций и местного применения
Фармакологические свойства
Фармакодинамика
Фармакокинетика
Азоксимера бромид характеризуется быстрым всасыванием и высокой скоростью распределения в организме. Максимальная концентрация препарата в крови при внутримышечном введении достигается через 40 минут. Период полувыведения для разного возраста от 36 до 65 часов. Биодоступность препарата высокая: более 90 % при парентеральном введении.
Азоксимера бромид быстро распределяется по всем органам и тканям организма, проникает через гематоэнцефалический и гематоофтальмический барьеры. Кумулятивный эффект отсутствует. В организме Азоксимера бромид подвергается биодеструкции до низкомолекулярных олигомеров, выводится преимущественно почками, с фекалиями — не более 3 %.
Показания к применению
Применяется у взрослых и детей с 6 месяцев для лечения и профилактики инфекционно-воспалительных заболеваний (вирусной, бактериальной и грибковой этиологии), в стадии обострения и ремиссии.
Для лечения взрослых (в комплексной терапии):
Для лечения детей старше 6 месяцев (в комплексной терапии):
Для профилактики (монотерапия) у детей старше 6 месяцев и взрослых:
Противопоказания
С осторожностью
Применение при беременности и в период грудного вскармливания
Противопоказано применение препарата Полиоксидоний ® беременным и женщинам в период грудного вскармливания (клинический опыт применения отсутствует).
При экспериментальном изучении препарата Полиоксидоний ® у животных не выявлено влияния на генеративную функцию (фертильность) самцов и самок, эмбриотоксического и тератогенного действия, влияния на развитие плода, как при введении препарата в период всей беременности, так и в период грудного вскармливания.
Способ применения и дозы
Способы применения препарата Полиоксидоний ® : парентеральный (внутримышечно, внутривенно), интраназальный, сублингвальный. Способы применения, режим дозирования, необходимость и кратность проведения последующих курсов терапии выбираются врачом в зависимости от тяжести заболевания и возраста больного.
Для внутривенного капельного введения рассчитанную для пациента дозу препарата стерильно переносят из шприца во флакон/пакет с 0,9% раствором натрия хлорида. Приготовленный раствор для внутривенного введения хранению не подлежит.
Рекомендуемые схемы лечения взрослых:
– парентерально (внутримышечно или внутривенно): препарат назначают взрослым в дозах 6–12 мг 1 раз в сутки ежедневно, через день, или 1–2 раза в неделю в зависимости от диагноза и тяжести заболевания.
У онкологических больных:
Интраназально или сублингвально (смотри раздел «Правила применения при сублингвальном и интраназальном введении»):
Общий объем препарата в сутки 1 мл (20 капель) — шприц 6 мг/мл. Суточная доза препарата вводится интраназально или сублингвально за 3-4 приема в сутки.
Рекомендуемые схемы лечения у детей:
Парентерально (внутримышечно или внутривенно): назначают детям от 6 месяцев в дозе 0,1–0,15 мг/кг ежедневно, через день или 2 раза в неделю курсом 5–10 инъекций.
Интраназально или сублингвально (смотри раздел «Правила применения при сублингвальном и интраназальном введении»):
Для лечения дисбактериоза кишечника (применяется сублингвально) в сочетании с базисной терапией — в течение 10 суток.
Для детей с 6 месяцев до 18 лет рекомендуется применение шприцев с дозировкой 3 мг/мл.
Общий объем препарата в сутки назначается из расчета 1 капля (0,15 мг) на 1 кг веса.
При массе тела ребенка до 20 кг не более 20 капель (3 мг действующего вещества ).
При массе тела ребенка более 20 кг не более 40 капель (6 мг действующего вещества).
| Вес ребенка, кг | Количество капель в сутки | Объем вводимого раствора |
|---|---|---|
| 5 кг | 5 капель | 0,25 мл |
| 10 кг | 10 капель | 0,5 мл |
| 15 кг | 15 капель | 0,75 мл |
| 20 кг | 20 капель | 1 мл |
| > 20 кг | 1 капля на 1 кг веса, но не более 40 капель | не более 2 мл |
Суточная доза препарата вводится интраназально или сублингвально за 3–4 приема в сутки.
Продолжительность курса 5–10 дней.
Правила применения при сублингвальном и интраназальном введении.
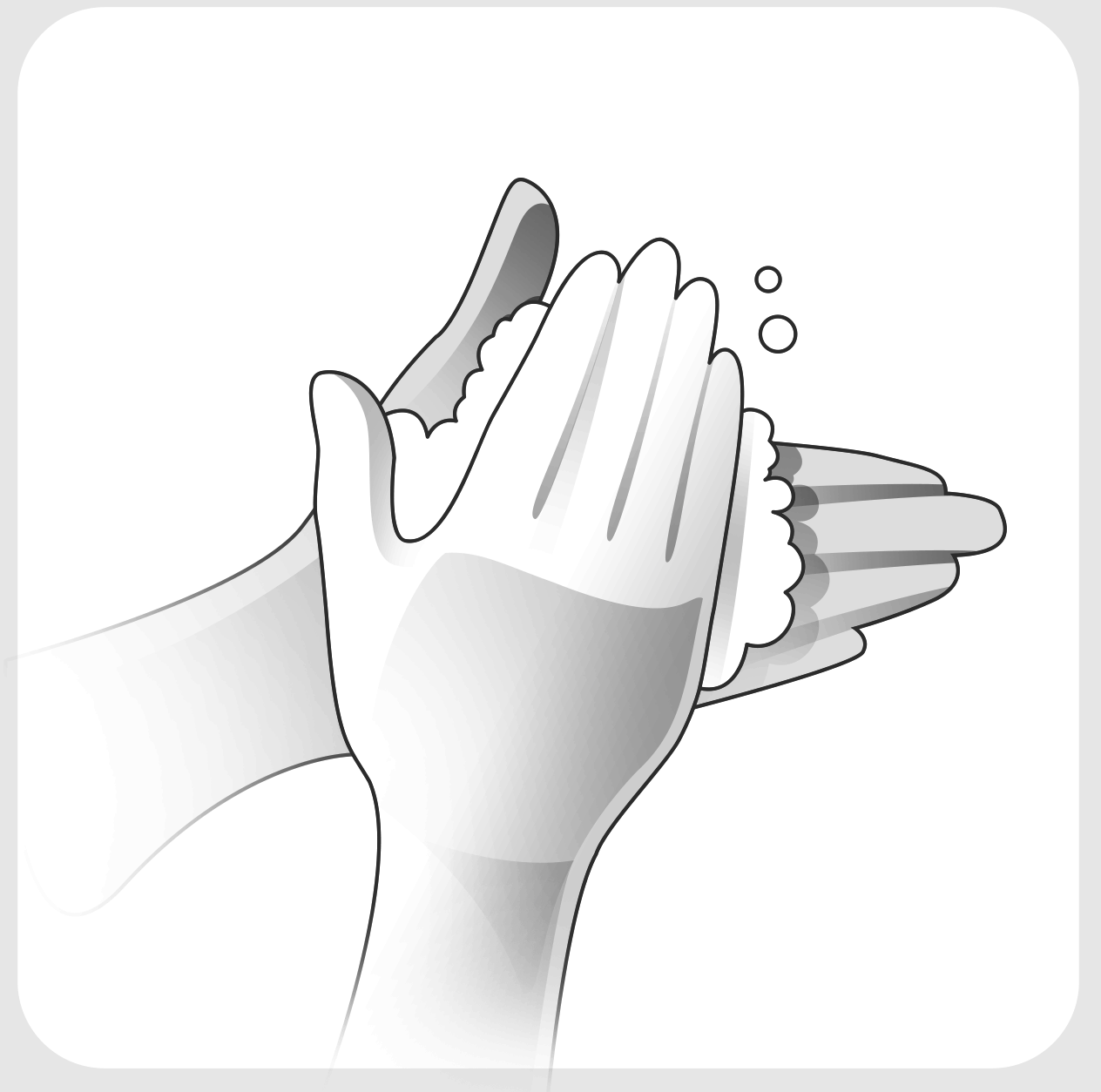 Рис.1 | 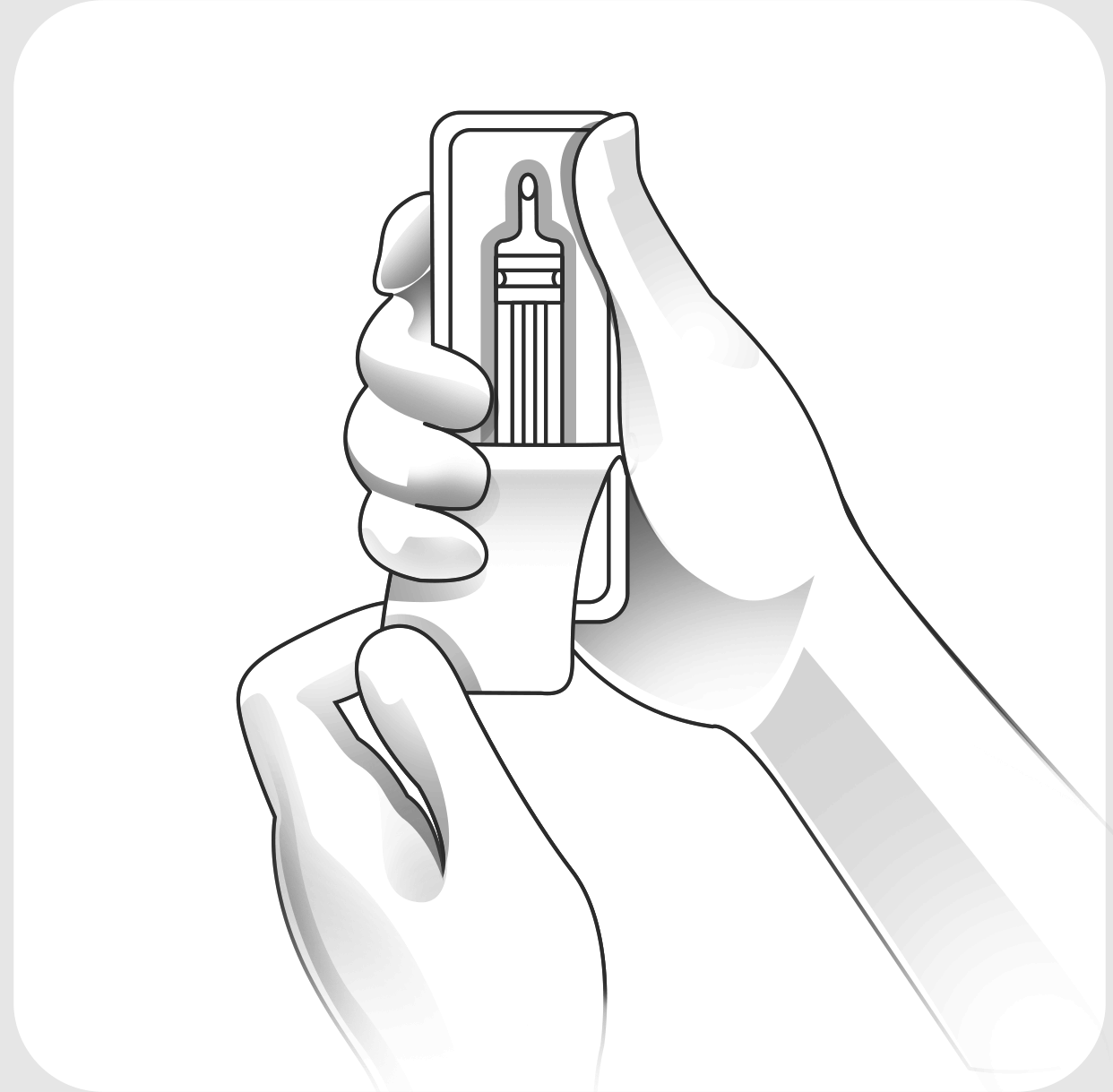 Рис.2 | 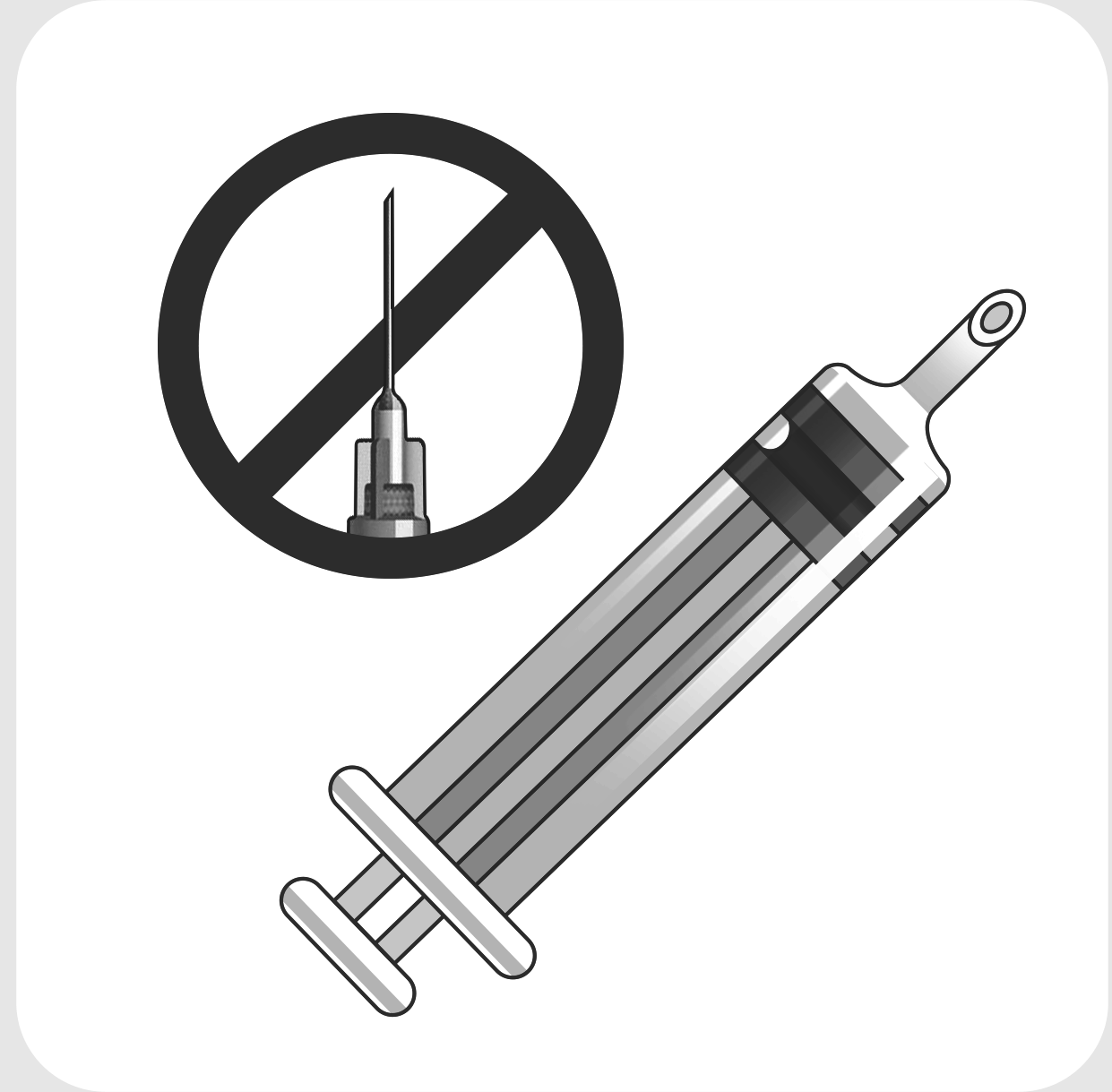 Рис.3 |
 Рис.4 | 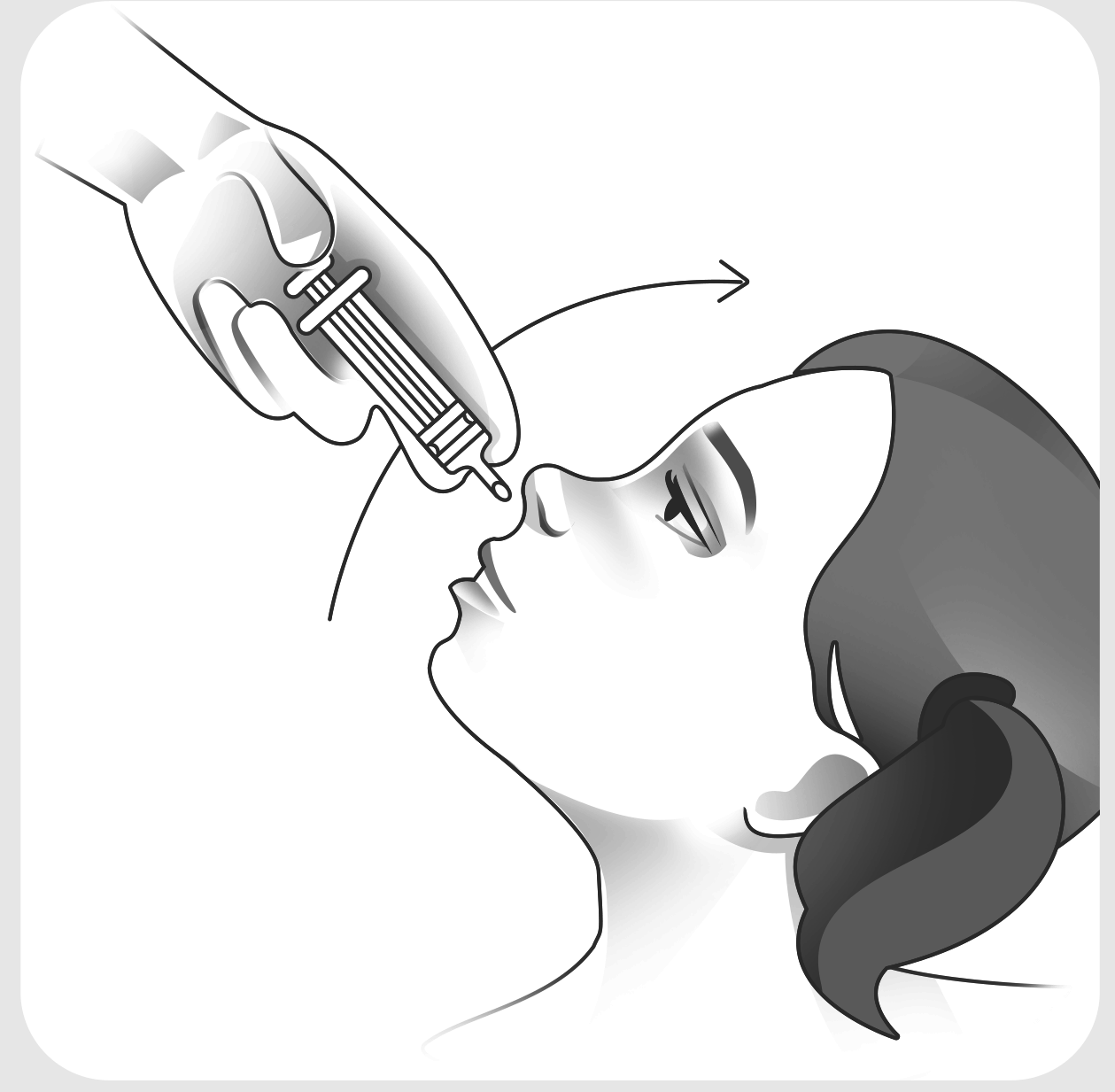 Рис.5 | 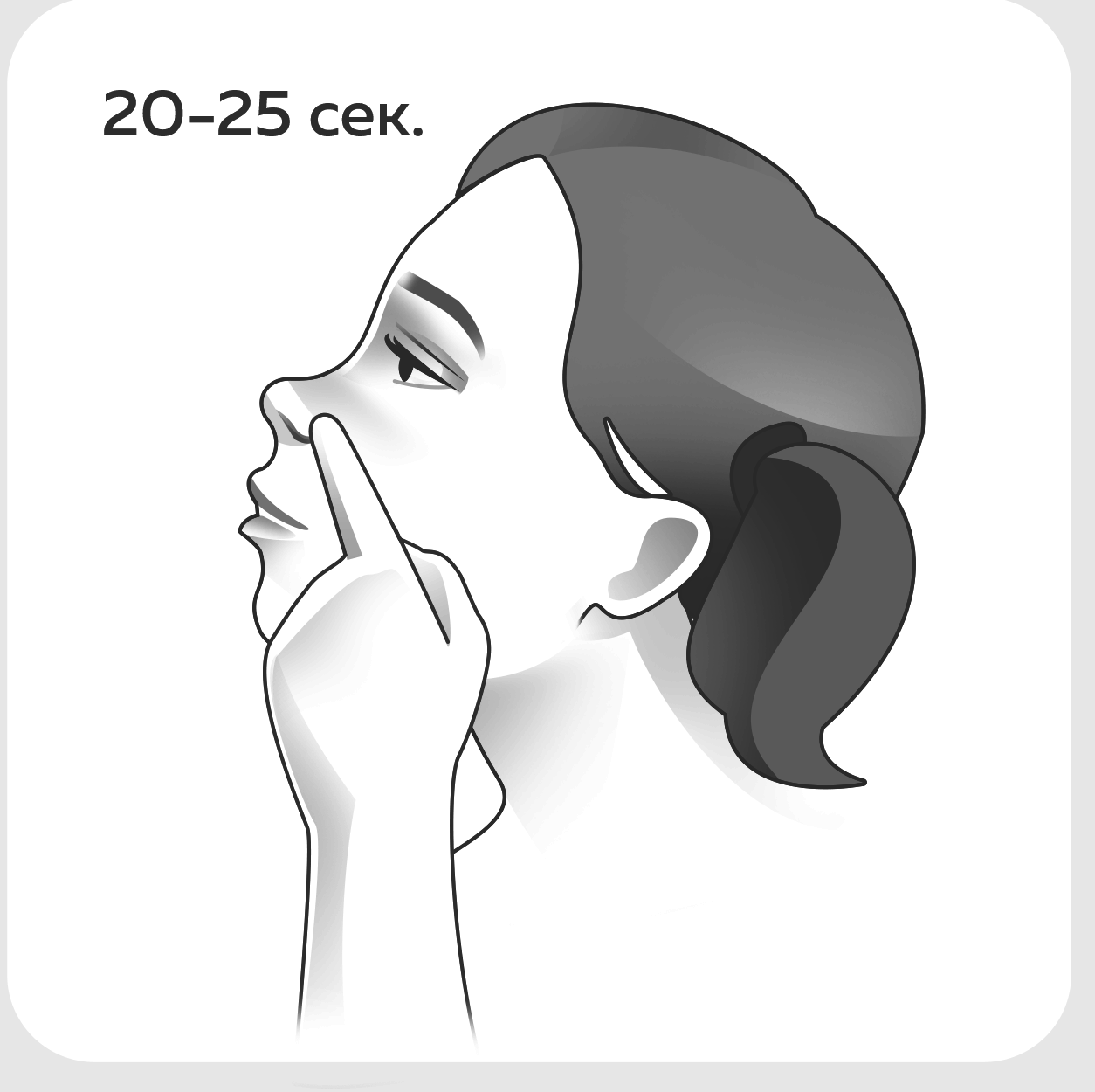 Рис.6 |
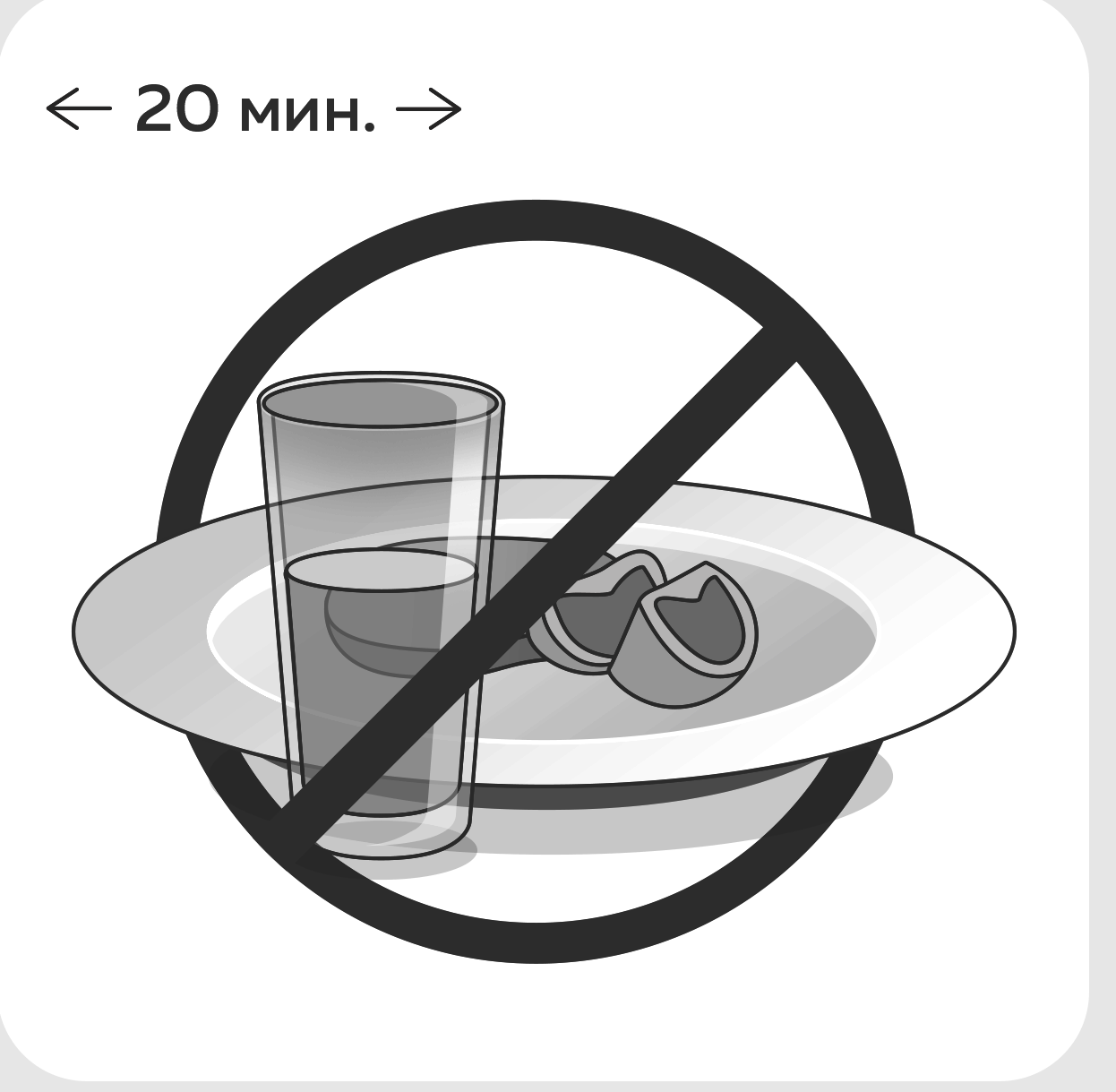 Рис.7 |  Рис.8 |  Рис.9 |
Подготовка к применению.
Для введения препарата в носовые ходы:
Для введения препарата под язык:
Закройте шприц колпачком. Вскрытый шприц при использовании препарата интраназально или сублингвально может храниться в холодильнике не более 7 дней.
Побочное действие
При применении препарата Полиоксидоний ® встречались следующие общие и местные реакции:
Влияние на способность управлять транспортными средствами и механизмами
Применение препарата Полиоксидоний ® не влияет на способность к выполнению потенциально опасных видов деятельности, требующих повышенной концентрации внимания и быстроты психомоторных реакций (в том числе управление транспортными средствами, работа с движущимися механизмами).
Форма выпуска
Раствор для инъекций и местного применения.
По 1,0 или 2,0 мл (для дозировки 3,0 мг/мл) в шприцы вместимостью 1 или 2 мл инъекционные одноразового применения из нейтрального стекла.
По 1,0 мл (для дозировки 6,0 мг/мл) в шприцы вместимостью 1 мл инъекционные одноразового применения из нейтрального стекла.
По 1,0 или 2,0 мл (для дозировки 3,0 мг/мл) или по 1,0 мл (для дозировки 6,0 мг/мл) во флаконы вместимостью 3 мл из бесцветного стекла.
По 1 шприцу c 1 одноразовой стерильной иглой в контурной ячейковой упаковке покрытой фольгой алюминиевой. По 5 флаконов в контурной ячейковой упаковке. По 1 контурной ячейковой упаковке в пачку из картона вместе с инструкцией по применению.
По 5 контурных ячейковых упаковок с 1 шприцем и 1 одноразовой стерильной иглой в пачку из картона вместе с инструкцией по применению.
По 5 шприцев c 5 одноразовыми стерильными иглами без контурной ячейковой упаковки в пачку из картона со вставкой из картона вместе с инструкцией по применению.
Срок годности
2 года. Не использовать по истечении срока годности.
Полиоксидоний® лиофилизат : инструкция по применению
Лекарственная форма
Лиофилизат для приготовления раствора для инъекций и местного применения, 3 мг и 6 мг
Состав
Один флакон содержит
вспомогательные вещества: маннитол, повидон, бетакаротен.
Описание
Пористая масса от белого цвета с желтоватым оттенком до желтого цвета. Препарат гигроскопичен и светочувствителен.
Фармакотерапевтическая группа
Фармакологические свойства
Полиоксидоний® обладает иммуномодулирующим действием, увеличивает резистентность организма в отношении локальных и генерализованных инфекций. Основой механизма иммуномодулирующего действия препарата Полиоксидоний® является прямое воздействие на фагоцитирующие клетки и естественные киллеры, а также стимуляция антителообразования.
Полиоксидоний® восстанавливает иммунитет при вторичных иммунодефицитных состояниях, вызванных различными инфекциями, травмами, ожогами, аутоиммунными заболеваниями, злокачественными новообразованиями, осложнениями после хирургических операций, применения химиотерапевтических средств, цитостатиков, стероидных гормонов.
Наряду с иммуномодулирующим действием, Полиоксидоний® обладает детоксикационной и антиоксидантной активностью, которая определяется структурой и высокомолекулярной природой препарата. Применение препарата Полиоксидоний® в комплексной терапии позволяет повысить эффективность и сократить продолжительность лечения, значительно уменьшить использование антибиотиков, бронхолитиков, глюкокортикостероидов, удлинить срок ремиссии.
Препарат хорошо переносится, не обладает митогенной, поликлональной активностью, антигенными свойствами, не оказывает аллергизирующего, мутагенного, эмбриотоксического, тератогенного и канцерогенного действия.
Показания к применению
Коррекция иммунитета у взрослых и детей от 6 месяцев.
У взрослых 6мг в комплексной терапии:
— хронических рецидивирующих инфекционно-воспалительных заболеваний, не поддающихся стандартной терапии в стадии обострения и в стадии ремиссии;
— острых и хронических вирусных и бактериальных инфекций (в том числе урогенитальных инфекционно-воспалительных заболеваний);
— острых и хронических аллергических заболеваний (в том числе поллиноза, бронхиальной астмы, атопического дерматита), осложненных хронической рецидивирующей бактериальной и вирусной инфекцией;
— ревматоидного артрита, длительно леченного иммунодепрессантами; при ревматоидном артрите, осложненном ОРВИ;
— для активации регенераторных процессов (переломы, ожоги, трофические язвы);
— для профилактики послеоперационных инфекционных осложнений;
— для профилактики гриппа и ОРВИ.
У детей от 6 месяцев 3мг в комплексной терапии:
— острых аллергических и токсико-аллергических состояний;
— бронхиальной астмы, осложненной хроническими инфекциями респираторного тракта;
— атопического дерматита, осложненного гнойной инфекцией;
— дисбактериоза кишечника (в сочетании со специфической терапией);
— для реабилитации часто и длительно болеющих;
— профилактики гриппа и ОРВИ.
Способ применения и дозы
Способы применения препарата Полиоксидоний®: парентеральный, интраназальный. Способы применения выбираются врачом в зависимости от тяжести заболевания и возраста больного.
Внутримышечно или внутривенно (капельно): препарат назначают взрослым в дозах 6-12 мг 1 раз в сутки ежедневно, через день, или 1-2 раза в неделю в зависимости от диагноза и тяжести заболевания.
Для внутримышечного введения содержимое флакона растворяют в 1,5-2 мл 0,9 % раствора натрия хлорида или воды для инъекций.
Для внутривенного (капельного) введения препарат растворяют в 2 мл 0,9% раствора натрия хлорида, затем стерильно переносят во флакон с указанными растворами объемом 200-400 мл.
Приготовленный раствор для парентерального введения хранению не подлежит.
Интраназально препарат назначают ежедневно в дозе 6 мг в сутки; дозу 6 мг растворяют в 1 мл (20 капель), 0,9 % раствора натрия хлорида, дистиллированной воды или кипяченой воды комнатной температуры. Приготовленный раствор хранят в холодильнике в течение 12 часов, перед употреблением согреть до комнатной температуры.
Рекомендуемые схемы лечения взрослых
При острых воспалительных заболеваниях: по 6 мг ежедневно в течение 3-х дней, далее через день общим курсом 5-10 инъекций.
При хронических воспалительных заболеваниях: по 6 мг через день инъекций, далее 2 раза в неделю курсом не менее 10 инъекций.
При туберкулезе: по 6-12 мг 2 раза в неделю курсом 10-20 инъекций.
У больных острыми и хроническими урогенитальными заболеваниями: по 6 мг через день курсом 10 инъекций в сочетании с химиопрепаратами.
При хроническом рецидивирующем герпесе: по 6 мг через день курсом 10 инъекций в сочетании с противовирусными препаратами, интерферонами и/или индукторами синтеза интерферонов.
Для лечения осложненных форм аллергических заболеваний: по 6 мг, курс 5 инъекций: две первые инъекции ежедневно, затем через день. При острых аллергических и токсико-аллергических состояниях вводить внутривенно по 6-12 мг в сочетании с противоаллергическими препаратами.
При ревматоидном артрите: по 6 мг через день 5 инъекций, далее 2 раза в неделю курсом не менее 10 инъекций.
У онкологических больных: до и на фоне химиотерапии для снижения иммунодепрессивного, гепато- и нефротоксического действия химиотерапевтических средств по 6-12 мг через день курсом не менее 10 инъекций; для профилактики иммунодепрессивного влияния опухоли, для коррекции иммунодефицита после химио- и лучевой терапии, после хирургического удаления опухоли длительное применение препарата Полиоксидоний® (от 2-3 месяцев до 1 года) по 6-12 мг 1-2 раза в неделю. Частота и длительность введения определяется врачом в зависимости от переносимости и длительности химио- и лучевой терапии.
У больных с острой почечной недостаточностью назначают не чаще 2 раз в неделю.
Интраназально назначают по 6 мг в сутки для лечения острых и хронических инфекций JIOP-органов, для усиления регенераторных процессов слизистых оболочек, для профилактики осложнений и рецидивов заболеваний, для профилактики гриппа и ОРВИ. По 3 капли в каждый носовой ход через 2-3 часа (3 раза в сутки) в течение 5-10 суток.
Способ применения и дозы для детей
Способы применения препарата Полиоксидоний® выбираются врачом в зависимости от диагноза, тяжести заболевания, возраста и массы тела больного: парентерально, интраназально, сублингвально.
Парентерально (внутримышечно или внутривенно капельно) препарат назначают детям от 6 месяцев в дозе 0,1-0,15 мг/кг ежедневно, через день или 2 раза в неделю в зависимости от тяжести заболевания, общим курсом 5-10 инъекций. Максимальная суточная доза 3 мг.
Расчет дозы в мл на массу ребенка указан в таблице (третий столбик).
Для внутримышечного введения препарат растворяют в 1 мл воды для инъекций или 0,9 % растворе натрия хлорида.
Для внутривенного капельного введения препарат растворяют в 1,5-2 мл стерильного 0,9 % раствора натрия хлорида, стерильно переносят во флакон с указанными растворами объемом 150-250 мл.
Приготовленный раствор для парентерального введения хранению не подлежит.
Сублингвально: ежедневно 1 раз в сутки в дозе 0,15 мг/кг в течение 10 дней.
Интраназально ежедневно в суточной дозе 0,15 мг/кг в течение 5-10 дней. Препарат вводят по 1-3 капли в каждый носовой ход через 2-3 часа, 2 раза в сутки до достижения суточной дозы, указанной ниже в таблице.
Полиоксидоний® (6 мг)
Инструкция
Торговое название
Международное непатентованное название
Лекарственная форма
Лиофилизат для приготовления раствора для инъекций и местного применения, 3 мг и 6 мг
Состав
Одна ампула или флакон содержит
активное вещество – азоксимера бромид 3 мг или 6 мг,
вспомогательные вещества: маннитол, повидон, бетакаротен.
Описание
Пористая масса от белого цвета с желтоватым оттенком до желтого цвета. Препарат гигроскопичен и светочувствителен.
Фармакотерапевтическая группа
Фармакологические свойства
Фармакокинетика
Фармакодинамика
Полиоксидоний® обладает иммуномодулирующим действием, увеличивает резистентность организма в отношении локальных и генерализованных инфекций. Основой механизма иммуномодулирующего действия препарата Полиоксидоний® является прямое воздействие на фагоцитирующие клетки и естественные киллеры, а также стимуляция антителообразования.
Полиоксидоний® восстанавливает иммунитет при вторичных иммунодефицитных состояниях, вызванных различными инфекциями, травмами, ожогами, аутоиммунными заболеваниями, злокачественными новообразованиями, осложнениями после хирургических операций, применения химиотерапевтических средств, цитостатиков, стероидных гормонов.
Наряду с иммуномодулирующим действием, Полиоксидоний® обладает детоксикационной и антиоксидантной активностью, обладает способностью выводить из организма токсины, соли тяжелых металлов, ингибирует реакции свободно-радикального окисления. Указанные свойства определяются структурой и высокомолекулярной природой препарата. Включение Полиоксидония® в комплексную терапию онкологических больных уменьшает интоксикацию, предупреждает развитие инфекционных осложнений и побочных эффектов в виде миелосупрессии, рвоты, диареи, цистита, колита и др, возникающих на фоне химио- и лучевой терапии, что в большинстве случаев позволяет проводить стандартную терапию без изменения схемы.
Применение препарата Полиоксидоний® на фоне вторичных иммунодефицитных состояний позволяет повысить эффективность и сократить продолжительность лечения, значительно уменьшить использование антибиотиков, бронхолитиков, глюкокортикостероидов, удлинить срок ремиссии.
Препарат хорошо переносится, не обладает митогенной, поликлональной активностью, антигенными свойствами, не оказывает аллергизирующего, мутагенного, эмбриотоксического, тератогенного и канцерогенного действия.
Показания к применению
Коррекция иммунитета у взрослых и детей от 6 месяцев.
У взрослых в комплексной терапии:
— хронических рецидивирующих инфекционно-воспалительных заболеваний, не поддающихся стандартной терапии в стадии обострения и в стадии ремиссии
— острых и хронических вирусных и бактериальных инфекций (в том числе урогенитальных инфекционно-воспалительных заболеваний)
— острых и хронических аллергических заболеваний (в том числе поллиноза, бронхиальной астмы, атопического дерматита), осложненных хронической рецидивирующей бактериальной и вирусной инфекцией
— ревматоидного артрита, длительно лечённого иммунодепрессантами; при ревматоидном артрите, осложненном ОРВИ
— для активации регенераторных процессов (переломы, ожоги, трофические язвы)
— для профилактики послеоперационных инфекционных осложнений
— для профилактики гриппа и ОРВИ
У детей в комплексной терапии:
— острых аллергических и токсико-аллергических состояний
— бронхиальной астмы, осложненной хроническими инфекциями респираторного тракта
— атопического дерматита, осложненного гнойной инфекцией;
— дисбактериоза кишечника (в сочетании со специфической терапией);
— для реабилитации часто и длительно болеющих
— профилактики гриппа и ОРВИ
Способ применения и дозы
Для взрослых:
Способы применения препарата Полиоксидоний®: парентеральный, интраназальный. Способы применения выбираются врачом в зависимости от тяжести заболевания и возраста больного.
Внутримышечно или внутривенно (капельно): препарат назначают взрослым в дозах 6-12 мг 1 раз в сутки ежедневно, через день, или 1-2 раза в неделю в зависимости от диагноза и тяжести заболевания.
Для внутримышечного введения содержимое ампулы или флакона растворяют в 1,5-2 мл 0,9 % раствора натрия хлорида или воды для инъекций.
Для внутривенного (капельного) введения препарат растворяют в 2 мл 0,9% раствора натрия хлорида, Реополиглюкина или 5% раствора декстрозы, затем стерильно переносят во флакон с указанными растворами объемом 200-400 мл.
Приготовленный раствор для парентерального введения хранению не подлежит.
Интраназально препарат назначают ежедневно в дозе 6 мг в сутки; дозу 6 мг растворяют в 1 мл (20 капель), 0,9 % раствора натрия хлорида, дистиллированной воды или кипяченой воды комнатной температуры.
Приготовленный раствор хранят в холодильнике в течение 12 часов, перед употреблением согреть до комнатной температуры.
Рекомендуемые схемы лечения взрослых
Парентерально:
При острых воспалительных заболеваниях: по 6 мг ежедневно в течение 3-х дней, далее через день общим курсом 5-10 инъекций.
При хронических воспалительных заболеваниях: по 6 мг через день 5 инъекций, далее 2 раза в неделю курсом не менее 10 инъекций.
При туберкулезе: по 6-12 мг 2 раза в неделю курсом 10-20 инъекций.
У больных острыми и хроническими урогенитальными заболеваниями: по 6 мг через день курсом 10 инъекций в сочетании с химиопрепаратами.
При хроническом рецидивирующем герпесе: по 6 мг через день курсом 10 инъекций в сочетании с противовирусными препаратами, интерферонами и/или индукторами синтеза интерферонов.
Для лечения осложненных форм аллергических заболеваний: по 6 мг, курс 5 инъекций: две первые инъекции ежедневно, затем через день. При острых аллергических и токсико-аллергических состояниях вводить внутривенно по 6-12 мг в сочетании с противоаллергическими препаратами.
При ревматоидном артрите: по 6 мг через день 5 инъекций, далее 2 раза в неделю курсом не менее 10 инъекций.
У онкологических больных:
У больных с острой почечной недостаточностью назначают не чаще 2 раз в неделю.
Интраназально назначают по 6 мг в сутки для лечения острых и хронических инфекций ЛОР-органов, для усиления регенераторных процессов слизистых оболочек, для профилактики осложнений и рецидивов заболеваний, для профилактики гриппа и ОРВИ. По 3 капли в каждый носовой ход через 2-3 часа (3 раза в сутки) в течение 5-10 суток.
Способ применения и дозы для детей
Способы применения препарата Полиоксидоний® выбираются врачом в зависимости от диагноза, тяжести заболевания, возраста и массы тела больного: парентерально, интраназально, сублингвально.
Парентерально (внутримышечно или внутривенно капельно) препарат назначают детям от 6 месяцев в дозе 0,1-0,15 мг/кг ежедневно, через день или 2 раза в неделю в зависимости от тяжести заболевания, общим курсом 5-10 инъекций. Максимальная суточная доза 3 мг.
Расчет дозы в мл на массу ребенка указан в таблице (третий столбик).
Для внутримышечного введения препарат растворяют в 1 мл воды для инъекций или 0,9% растворе натрия хлорида.
Для внутривенного капельного введения препарат растворяют в 1,5-2 мл стерильного 0,9 % раствора натрия хлорида, Реополиглюкина, или 5% раствора декстрозы, стерильно переносят во флакон с указанными растворами объемом 150-250 мл.
Приготовленный раствор для парентерального введения хранению не подлежит.
Сублингвально: ежедневно 1 раз в сутки в дозе 0,15 мг/кг в течение 10-20 дней.
Отечественные иммунотропные лекарственные средства последнего поколения и стратегия их применения
Введение Современная патология характеризуется ростом заболеваний, связанных с вторичной иммунологической недостаточностью. Она проявляется в частых, вялотекущих, рецидивирующих инфекционно-воспалительных заболеваниях дыхательного, желудочно
Современная патология характеризуется ростом заболеваний, связанных с вторичной иммунологической недостаточностью. Она проявляется в частых, вялотекущих, рецидивирующих инфекционно-воспалительных заболеваниях дыхательного, желудочно-кишечного и урогенитального трактов, кожи и мягких тканей. Применение антибактериальных лекарственных средств нередко бывает малоэффективным или вообще неэффективным. Становится очевидным, что без повышения иммунологической реактивности трудно (или невозможно) добиться хорошего клинического эффекта при различных хронических инфекционно-воспалительных процессах. Одним из главных методов коррекции иммунитета является применение иммунотропных лекарственных средств (ИТЛС). В настоящее время врач-иммунолог располагает достаточно большим набором таких препаратов. По происхождению их можно разделить на три группы: полимерные, экзогенные и эндогенные [20]. В данном обзоре представлены только те ИТЛС, которые разработаны и внедрены в клиническую практику за последнее десятилетие и являются новейшими достижениями отечественной науки.
К полимерным ИТЛС, полученным с помощью направленного химического синтеза, относится препарат полиоксидоний (выпускается в виде ампул по 3 мг). Он представляет собой N-оксидированное производное полиэтиленпиперозина с высоким молекулярным весом [13,15]. Препарат обладает широким спектром иммунофармакологического воздействия. Он стимулирует функциональную активность трех важнейших субпопуляций фагоцитов: подвижных макрофагов тканей, циркулирующих фагоцитов крови и оседлых фагоцитов ретикуло-эндотелиальной ткани. Это проявляется в повышенной способности фагоцитов поглощать и переваривать микробы, в образовании активных форм кислорода, повышении миграционной активности нейтрофилов. Результатом активации оседлых макрофагов ретикуло-эндотелиальной системы под влиянием полиоксидония является более эффективная элиминация из организма чужеродных частиц. Суммарным следствием активации факторов естественного иммунитета является повышение устойчивости животных к экспериментальным бактериальным и вирусным инфекциям. Полиоксидоний повышает также функциональную активность Т- и В-лимфоцитов, усиливая кооперативное взаимодействие между этими двумя важнейшими клеточными популяциями. При введении экспериментальным животным полиоксидония совместно с каким-либо антигеном наблюдается более чем десятикратное усиление антителообразования к этому антигену. Этот эффект отмечается к Т-зависимым и Т-независимым антигенам как животного, так и микробного происхождения. Полиоксидоний способен активировать иммунные реакции у животных с тяжелыми формами иммунодефицитов, в частности усиливать антителообразование у:
Кроме того, для полиоксидония характерно еще одно важное качество, не связанное с активацией иммунной системы: он обладает детоксицирующими свойствами. В силу своего молекулярного веса и наличия на поверхности молекулы большого количества различных активных групп он активно адсорбирует как растворимые токсические субстанции, так и микрочастицы, циркулирующие в крови. Полиоксидоний также обладает способностью снижать токсичность ряда лекарственных средств.
Препарат рекомендуется в качестве иммуномодулятора в комплексной терапии заболеваний или состояний, сопровождающихся угнетением иммунитета, так как при этих патологических процессах показал высокую клиническую эффективность. Он назначается внутримышечно, 5-7 инъекций на курс. ХНЗЛ были использованы две схемы лечения с разовыми дозами 6 мг (1-я) и 12 мг (2-я). При лечении полиоксидонием больных хроническим бронхитом в фазе ремиссии было отмечено удлинение сроков ремиссии и исчезновение астенического синдрома. Хороший эффект (быстрое купирование симптомов заболевания, сокращение сроков нетрудоспособности, достижение стойкой ремиссии, нормализация лабораторных показателей и др.) дали 1-я и 2-я схемы лечения в 63,6 и 77,8% случаев соответственно. Назначение в качестве препарата сравнения иммуномодулятора нуклеината натрия дает положительные результаты у 51,4% больных. Лечение полиоксидонием больных хроническим бронхитом в период обострения в комплексе с антибиотиками способствовало значительному улучшению их общего состояния, при этом уменьшались слабость, потливость, кашель и количество выделяемой мокроты, нормализовалась температура, исчезали хрипы в легких. Применение 1-й и 2-й схем лечения привело к хорошему эффекту у 66,6 и 87,5% больных соответственно. При лечении нуклеинатом натрия хороший эффект был только у 54,5%. При применении плацебо как в стадии ремиссии, так и в период обострения наблюдался только удовлетворительный эффект: купирование симптомов заболевания и положительная динамика в лабораторно-инструментальных данных.
У больных под воздействием полиоксидония происходила нормализация иммунонологических показателей: увеличение CD3 T-лимфоцитов, увеличение NK-активности, нормализация функциональной активности фагоцитарных клеток.
У пациентов с хроническим рецидивирующим фурункулезом в стадии ремиссии наблюдалось значительное удлинение ремиссии и снижение симптомов интоксикации. Хорошие результаты получены при применении 1-й и 2-й схем лечения у 60 и 81,8% больных соответственно. У больных, получавших нуклеинат натрия, наблюдался только удовлетворительный эффект (33,3%). У больных, получавших плацебо, положительной динамики клинической картины не выявлено. При применении полиоксидония в комплексе с антибиотиками у больных фурункулезом в стадии обострения происходила быстрая регрессия фурункулов, уменьшение их количества, уменьшение симптомов интоксикации. Хороший эффект при применении 1-й и 2-й схем лечения был у 80 и 90,9% больных соответственно. Положительная клиническая картина сопровождалась нормализацией иммунологических показателей.
Ярким примером клинической эффективности препарата являются результаты, полученные при лечении хирургических инфекций: сепсиса, перитонита, абсцессов и инфильтратов брюшной полости, гнойно-воспалительных процессов в малом тазу [11,18]. В группе, получавшей полиоксидоний, хорошие и отличные показатели наблюдались у 75 и 80% больных соответственно. В контрольной группе хороший и отличный результат был получен у 42% больных.
Хороший клинический эффект полиоксидония при хирургических инфекциях в значительной степени связан с его способностью усиливать процессы регенерации. Это проявлялось в быстром очищении раны от гнойно-некротических масс, ее эпителизации и сокращении сроков заживления (на 21%). Включение полиоксидония в комплексное лечение гнойно-раневых инфекций способствовало быстрому очищению раны от микроорганизмов.
У всех больных, имеющих в послеоперационный период гнойно-септические осложнения, наблюдались нарушения иммунного статуса, степень выраженности которых зависела от тяжести этого осложнения: снижалась функциональная активность фагоцитарных клеток, уменьшался уровень CD3 и CD4 T-лимфоцитов и IgG. Применение поолиоксидония существенно улучшало ряд биохимических и иммунологических параметров у хирургических больных. Во всех группах, получавших этот препарат, в отличие от контрольной группы снижалась активность печеночных ферментов (АСТ и АЛТ), уровень билирубина, креатинина и мочевины сыворотки крови, что, вероятно, связано с антиоксидантными и детоксицирующими свойствами полиоксидония.
К ИТЛС экзогенного происхождения относятся препараты бактериального и грибкового происхождения. К медицинскому применению разрешены такие средства микробного происхождения, как БЦЖ, пирогенал, продигиозан, нуклеинат натрия, рибомунил, бронхомунал и др. Все они обладают способностью усиливать функциональную активность нейтрофилов и макрофагов [7]. Как известно, микобактерии туберкулеза, входящие в состав полного адьюванта Фрейнда, обладают выраженной способностью стимулировать неспецифическую резистентность, клеточный и гуморальный иммунитет. Анализ компонентов микобактерий, ответственных за этот стимулирующий эффект, привел к открытию в составе пептидогликана клеточной стенки этих и практически всех других бактерий нового мощного иммуностимулятора — мурамилдипептида [22, 23]. Российские специалисты почти одновременно с французскими исследователями выделили из противоопухолевого препарата бластолизина — гидролизата клеточной стенки L.bulgaricus вещество, сходное по химической структуре, которое в дальнейшем было получено синтетическим путем [1]. Оно успешно прошло клинические испытания и получило фармакопейное название ликопид. Он выпускается в таблетированной форме по 10 мг и 1 мг. Препарат показал полную безвредность и высокую эффективность при ряде вторичных иммунодефицитных состояний [6]. Главной мишенью ликопида в организме являются клетки моноцитарно- макрофагального ряда. Он усиливает практически все функции клеток этой системы, в частности обеспечивает следующие процессы:
В ряде случаев ликопид эффективен и в виде монотерапии. Так, его своевременное применение по 1 мг. 3 раза в день в течение 10 дней в профилактических целях позволило существенно снизить (в 2,5 раза) сезонные острые респираторные заболевания. В самом начале развития патологического процесса ликопид оказывается эффективным (по 10 мг 1 раз в сутки в течение 10 дней) при папилломатозе шейки матки.
Применение его по той же схеме после хирургического лечения позволило свести практически к нулю рецидив папилломатоза. При использовании в качестве препарата сравнения нуклеината натрия эффективность лечения составила около 60%. Ликопид оказался также высокоэффективным при комплексной терапии острых и хронических герпетических инфекций всех локализаций. Схема лечения зависит от тяжести патологического процесса При легких и средней тяжести формах заболевания ликопид целесообразно принимать по 2 мг 3 раза в день, при тяжелых — по 10 мг 2-3 раза в день в течение 10 дней. Его комбинация с противовирусными средствами позволяет быстро купировать патологический процесс и вызвать стойкую ремиссию в течение года и более. Препарат хорошо взаимодействует не только с противовирусными средствами, но и с препаратами интерферона и их индукторами.
Высока клиническая эффективность ликопида и в комплексном лечении такого тяжелого заболевания, как туберкулез легких. Его назначение тремя курсами по 6-7 дней с интервалами в две недели с разовой дозой 10 мг ведет к более быстрому закрытию каверн и прекращению бациллоносительства.
Применение ликопида с целью профилактики хирургических инфекций позволило в несколько раз сократить частоту их развития. При наличии развившегося осложнения ликопид препятствует прогрессированию патологического процесса, возникновению новых осложнений, развитию пневмоний. Кроме того, он показал высокую клиническую эффективность практически при всех видах долго не заживающих ран, а также при трофических язвах.
Клинический эффект, как правило, сопровождается и выраженным улучшением иммунологических показателей. Наиболее четко это показано на примере хирургических инфекций [5,19,21]. Как при профилактике, так и при лечении этих инфекций ликопид оказывал положительное воздействие на гематологические, биохимические и иммунологические параметры. У больных, принимавших по 3 мг ликопида в течение 10 дней, по сравнению с больными, получавшими плацебо, были отмечены следующие статистически значимые положительные изменения:
В настоящее время в качестве ИТЛС эндогенного происхождения для профилактики и лечения вторичных иммунодефицитов применяются иммунорегуляторные пептиды, полученные из центральных органов иммунитета: тимуса и костного мозга и цитокины.
Из ИТЛС, полученных из костного мозга, достаточно широко распространен миелопид (выпускается в ампулах по 3 мг, разработка которого началась в начале 70-х годов, после того как было обнаружено, что костный мозг продуцирует группу биорегуляторных пептидных медиаторов, названных миелопептидами [14]. Эти биологически активные медиаторы обладают способностью стимулировать различные звенья иммунного ответа, особенно гуморальный иммунитет [10]. В состав миелопида входят шесть низкомолекулярных миелопептидов (МП) с молекулярной массой 500-3000 D, выделенных из супернатанта культуры клеток костного мозга свиньи методом твердофазной экстракции. Каждый миелопептид обладает определенным биологическим действием, совокупность которых и обусловливает его клинический эффект. МП-1 восстанавливает нормальный баланс активности Т-хелперов и Т-супрессоров. МП-2 подавляет пролиферацию злокачественных клеток и существенно снижает способность опухолевых клеток продуцировать токсические субстанции, подавляющие функциональную активность Т-лимфоцитов. МП-3 стимулирует активность фагоцитарного звена иммунитета и, следовательно, повышает антиинфекционный иммунитет. МП-4 оказывает влияние на дифференцировку гемопоэтических клеток, способствуя их более быстрому созреванию, т. е. обладает лейкопоэтическим эффектом.
Миелопид нашел применение в клинике для восстановления нормального функционирования иммунной системы при различных патологических состояниях.
Включение миелопида в комплексную терапию хронических неспецифических заболеваний легких существенно улучшает клиническое состояние больных и значительно увеличивает продолжительность ремиссии ( до одного года и более у 78%). Применение миелопида в комплексной терапии гнойно-воспалительных процессов позволяет добиться быстрой и полной санации очага инфекции и увеличивает эффективность действия антибиотиков. Так, у больных, перенесших различные операции на сердце, пневмония и нагноение раны с медиастинитом возникли в 15,5 и 18,9% случаев в контрольной группе, в опытной группе эти осложнения наблюдались у 6,7 и 10,8% соответственно. Следует отметить, что осложнения, развившиеся у больных, получавших миелопид, протекали на фоне менее выраженной интоксикации и лихорадки, умеренного лейкоцитоза и сопровождались незначительным гнойным отделяемым из раны. Клиническое улучшение у больных, получавших миелопид, наступало на 12-14-й день, у больных контрольной группы — на 17-21-й день после операции. Миелопид оказался также эффективным в комплексном лечении переломов нижней челюсти [17].
Иммунологическое исследование показало, что уже на первые-вторые сутки после операции у больных развивается выраженный иммунодефицит, при котором страдают практически все звенья иммунной системы. Проведение сразу после операции иммунотерапии с помощью миелопида приводило к значительному ускорению восстановления всех показателей иммунитета. Количество Т- и В-лимфоцитов и Т-хелперов у таких больных достигало нормальных значений уже на седьмые-восьмые сутки. Также происходило восстановление функциональной активности Т- и В-лимфоцитов, определяемое по способности синтезировать ИЛ-2 и иммуноглобулины соответственно [3].
Патологические состояния, при которых рекомендовано применение полиоксидония:
Патологические состояния, при которых рекомендуется применение ликопида:
Патологические состояния, при которых рекомендовано применение миелопида:
Патологические состояния, при которых применяется иммунофан:
Травма, так же как и оперативное вмешательство, ведет к развитию иммунодефицита, которое прежде всего проявляется в понижении уровня Т-клеток уже на следующие сутки. Без иммуностимуляции это иммунодефицитное состояние сохранялось в течение трех недель. Применение миелопида вело к существенному улучшению иммунологических показателей: количество Т-лимфоцитов возвращалось к норме на седьмой день. Восстановление иммунологических показателей четко коррелировало с улучшением клинической картины заболевания [17].
Из ИТЛС, полученных из тимуса, в клинической практике нашел применение целый ряд препаратов нескольких поколений. Толчком к их созданию стало открытие нового класса биологически активных соединений — пептидных гормонов тимуса [24]. К ним относится семейство тимозинов, тимопоэтинов и сывороточный тимический фактор — тимулин. Эти тимические пептиды при поступлении в кровь оказывают влияние на всю периферическую иммунную систему, стимулируя рост и пролиферацию лимфоидных клеток. Установление этого факта явилось мощным толчком к созданию ИТЛС тимического происхождения.
К ИТЛС первого поколения относятся препараты, полученные на основе экстрактов ткани тимуса: тактивин, тималин, тимоптин, тимактид и др. Из этих препаратов в хирургической практике наиболее часто используют тактивин, представляющий собой комплекс пептидов, экстрагированных из тимуса крупного рогатого скота [2]. Он является эффективным иммунокорригирующим средством, увеличиваеит число Т-лимфоцитов, которое, как правило, понижается при вторичных иммунодефицитных состояниях, усиливает их функциональную активность, определяемую по способности продуцировать цитокины, стимулирует активность естественных киллеров, стволовых гемопоэтических клеток и нормализует ряд других показателей, характеризующих напряженность Т-клеточного иммунитета [16].
Клиническая эффективность тимических препаратов первого поколения не вызывает сомнения. Но у них есть один недостаток: они представляют собой неразделенную смесь биологически активных пептидов и их достаточно трудно стандартизовать. Прогресс в области ИТЛС тимического происхождения шел по линии создания препаратов 2-го и 3-го поколения, представляющих собой синтетические аналоги естественных гормонов тимуса: альфа-один-тимозина и тимопоэтина или фрагментов этих гормонов, обладающих биологической активностью. Последнее направление оказалось наиболее продуктивным, особенно в отношении тимопоэтина. На основе одного из активных фрагментов, включающего аминокислотные остатки 32-36-тимопоэтина, создан препарат тимопентин, получивший на Западе разрешение на медицинское применение [25], и иммунофан [8], получивший разрешение на медицинское применение в России и представляющий собой синтетический гексапептид, аналог участка 32-36-тимопоэтина. Иммунофан выпускают в ампулах в виде 0,005% по 1 мл.
Изучение механизма действия показало [8], что иммунофан:
При проведении клинических испытаний иммунофан показал себя высоко эффективным средством в плане восстановления нарушенной иммунологической реактивности при хронических бактериальных и вирусных инфекциях, хирургических инфекциях, онкологических заболеваниях [8].
Его применение в комплексном лечении особенно тяжелых послеоперационных осложнений позволило существенно снизить летальность. Так, летальность у больных с нагноившейся гематомой печени, септической пневмонией и перитонитом, не получавших иммунофан, составила 100, 80 и 78%, при применении же в комплексном лечении этих больных иммунофана летальность составила 33, 33 и 50% соответственно. Как правило, у этих пациентов наблюдаются явления дезинтеграции всей иммунной системы. Она проявляется в понижении клеточного иммунитета (снижение всех популяций Т-лимфоцитов и их функциональной активности) и активации гуморального иммунитета (увеличение уровня IgG, IgM и циркулирующих иммунных комплексов) [9]. Применение иммунофана позволило быстро и эффективно нормализовать измененные параметры иммунологической реактивности.
Помимо стимуляции иммунологической реактивности иммунофан обладает выраженной способностью активировать антиоксидантную систему организма. Это проявляется в усилении активности каталазы и синтеза антиоксидантных белков — церулоплазмина и лактоферина. Эти два свойства имунофана позволили рекомендовать его в комплексной терапии онкологических больных не только для повышения иммунитета, но и для элиминации токсических свободнорадикальных и перекисных соединений. Его применение позволило существенно сократить лучевые реакции со стороны клеток белой крови и повысить их функциональную активность.
Как известно, ИТЛС редко используются в виде монотерапии. Основной их сферой применения являются вторичные иммунодефициты, при которых инфекционные агенты играют существенную роль в развитии заболевания. Поэтому в большинстве случаев для лечения этих иммунодефицитов применяются антибактериальные, противогрибковые и противовирусные препараты. Возникает вопрос, как и какие ИТЛС наиболее целесообразно применять в этих случаях? Здесь уместно напомнить, что в конечном итоге гибель большинства как внеклеточных, так и внутриклеточных микробов происходит в фагоцитарных клетках: нейтрофилах или макрофагах. Поэтому при лечении инфекционного компонента иммунодефицита целесообразно использовать те ИТЛС, которые усиливают функциональную активность фагоцитов. К ним относятся практически все основные современные препараты: ликопид, миелопид, полиоксидоний и др. Наиболее целесообразно при лечении инфекционного компонента иммунодефицита назначать ИТЛС одновременно с антибиотиками. При комплексном применении антибиотика и ИТЛС по возбудителю наносится двойной удар: антибиотик существенно подавляет функциональную активность возбудителя и делает его более чувствительным к киллерному эффекту фагоцита, а ИТЛС существенно стимулирует функциональную активность фагоцита, повышая его способность поглощать и убивать возбудителя. Аналогичная ситуация имеет место и при вирусной инфекции: ИТЛС (например, ликопид), повышая цитотоксические свойство макрофагов и NK- клеток, существенно усиливает их способность убивать вирусинфицированные клетки — главный путь диссеминации возбудителя в организме. Здесь также уместно сказать, что, помимо антибиотиков, ликопид хорошо взаимодействует и с препаратами интерферонового ряда и их индукторами. Нанесение тройного удара по возбудителю: противовирусное средство, ликопид и индуктор интерферона, по нашим наблюдениям, является исключительно эффективным при ряде хронических герпетических и цитомегаловирусных инфекциях.
Таким образом, главным принципом применения ИТЛС при лечении инфекционного компонента иммунодефицита является его одновременное назначение с антибактериальными средствами, что значительно повышает клинический эффект.
Суммируя представленный материал, следует отметить, что практически все ИТЛС, применявшиеся в лечебной практике, показали неплохой эффект в плане лечения и профилактики вторичных иммунодефицитов. Эра иммунокорригирующей терапии с помощью ИТЛС только началась, и широкое клиническое внедрение препаратов этого профиля в будущем позволит уточнить, дополнить и, может быть, значительно расширить (или ограничить) спектр их применения, схемы и дозировки. Как известно, практика — лучший критерий истины.
При применении ИТЛС с лечебной целью следует всегда помнить о двух правилах иммунокорригирующей терапии: она, как правило, входит в состав комплексного лечения и обязательным условием ее проведения является оценка иммунного статуса до и после лечения.
Наличие довольно большого числа ИТЛС не должно пугать практических врачей. Иммунная система состоит из ряда тесно связанных в функциональном плане компонентов, задача которых заключается в элиминации из организма чужеродных веществ антигенной природы. У каждого из компонентов этой системы могут быть свои относительно специфические агенты, модулирующие уровень их активности. В то же время следует помнить, что иммунная система работает по принципу системы мобилей [12]: активация одного из ее компонентов с помощью ИТЛС ведет к активации других участников системы, вследствие чего и получается положительный клинический эффект при использовании практически всех ИТЛС.


