Полинейропатия нижних конечностей что делать
Полинейропатия (ПНП)
При полинейропатии может происходить как изолированное поражение определенного типа нервных волокон, так и их сочетание, что приводит к появлению разнообразной клинической картины.
Важно как можно раньше уточнить причину полинейропатии, т.к. от этого зависит прогноз и тактика лечения.
В сложных диагностических случаях врач может рекомендовать проведение УЗИ периферических нервов, МРТ сплетений с контрастированием, диагностическую люмбальную пункцию, морфологическое исследование нерва (биопсия).
План обследования составляется индивидуально!
Важно помнить, что в каждом третьем случае после тщательного обследования уточнить причину полинейропатии не удается – в этом случае диагностируется идиопатическая полинейропатия.
Какие методы лечения разработаны при полинейропатии?
С позиций доказательной медицины не для всех полинейропатий разработано патогенетическое лечение.
Так, при диабетической полинейропатии, прежде всего, необходим тщательный контроль уровня глюкозы крови и соблюдение всех рекомендаций лечащего эндокринолога.
При токсической, например, алкогольной полинейропатии, лечение начинается с полного отказа от вредной привычки.
При обнаружении дефицитарной полинейропатии проводят витаминотерапию, а также устраняют причины, вызывающие развитие заболевания.
Патогенетическая терапия (т.е. терапия, направленная на коррекцию механизмов развития заболевания) является основной в лечении дизиммунных полинейропатии (синдром Гийена-Барре, хроническая воспалительная демиелинизирующая полинейропатия, парапротеинемические полинейропатии, мультифокальная моторная нейропатия и др.). В зависимости от типа дизиммунной нейропатии, в индивидуальном порядке, учитывая все нюансы заболевания, подбирается оптимальный метод лечения или их сочетание. Разработаны следующие методы патогенетической терапии дизиммунных нейропатий: гормонотерапия (применение высоких доз глюкокортикостероидных препаратов), высокообъемный плазмаферез, высокодозная внутривенная иммунотерапия, а также применение цитостатиков и препаратов моноклональных антител.
Симптоматическая терапия используется для устранения неприятных чувствительных ощущений (онемения, жжения, жгучей боли) при полинейропатии. Рекомендованы местные анестетики, антиконвульсанты, антидепрессанты, опиоидные анальгетики, а также психотерапия.
Восстановительно-реабилитационные методы лечения (чрескожная электронейростимуляция, акупунктура, биологическая обратная связь, интервенционные методы, массаж, физиотерапия, баланстерапия, роботизированная терапия) занимает важное место в коррекции неврологических нарушений при полинейропатии.
Если у вас есть симптомы полинейропатии или вам поставлен диагноз «Полинейропатия», вы можете пройти комплексное обследование в центре заболеваний периферической нервной системы ФГБНУ НЦН, где вам помогут уточнить диагноз, выявить причины поражения периферических нервов и назначат терапию с позиций доказательной медицины.
Для ФГБНУ НЦН данное направление издавна является одним из приоритетных. Здесь было создано первое в стране отделение нейрореанимации, которое славилось уникальной методологией ухода за пациентами с тяжелыми формами полинейропатий, нуждающимися в длительной искусственной вентиляцией легких. Несколько десятилетий назад были проведены уникальные работы по диагностике и лечению отдельных форм нейропатий: наследственных, дифтерийной, дизиммунных и др. Здесь впервые в СССР был внедрён плазмаферез как метод лечения аутоиммунных заболеваний нервной системы. Накоплен уникальный отечественный опыт лечения и реабилитации больных с синдромом Гийена-Барре, тяжелыми формами ХВДП и нейропатий другого генеза.
В состав центра заболеваний периферической нервной системы входит 13 специалистов, из них 10 неврологов и 3 эндокринолога. Все неврологи владеют методиками ЭНМГ-исследования.
Сотрудники центра заболеваний периферической нервной системы консультируют пациентов амбулаторно в рамках ОМС и на коммерческой основе.
ЗАПИСЬ НА ПРИЕМ И ЭНМГ/иЭМГ ПО МНОГОКАНАЛЬНОМУ ТЕЛЕФОНУ
+7 (495) 374-77-76
+7 (985) 931-60-24
Полинейропатия
Периферическая нервная система передает информацию от головного и спинного мозга (центральной нервной системы) к остальным частям тела. Периферическая нейропатия может быть результатом травматических повреждений, инфекций, нарушения обмена веществ, наследственных причин и воздействия токсинов. Одной из наиболее распространенных причин полинейропатии является сахарный диабет.
Пациенты с периферической нейропатией обычно описывают боли, как ощущения покалывания или жжения. Во многих случаях, симптомы снижаются, если возникает компенсация основного заболевания.
Каждый нерв в периферической нервной системе имеет определенную функцию, так что симптомы зависят от типа нервов, которые оказались повреждены. Нервы подразделяются на:
Симптомы
Симптомы полинейропатии, могут включать:
Если задействованы вегетативные нервы, симптомы могут включать:
Причины
Ряд факторов может привести к развитию невропатии, в том числе:
Осложнения полинейропатии могут включать
Диагностика
Врача при диагностике полинейропатии, в первую очередь, могут интересовать ответы на следующие вопросы
Врач может назначить обследование
Лечение
Целью лечения полинейропатии является лечение основного заболевания и минимизация симптомов. Если лабораторные тесты и другие методы обследования указывают на отсутствие основного заболевания, врач может рекомендовать выжидательную тактику, для того чтобы увидеть, есть самостоятельное уменьшение симптомов нейропатии. Если есть воздействие токсинов или алкоголя, врач будет рекомендовать избегать этих веществ.
Медикаментозное лечение
Лекарства, используемые для облегчения болей при полинейропатии включают в себя:
Кроме медикаментозного лечения могут применяться и другие методы лечения.
Нейропатия: необъяснимых болей не бывает
К группе периферических нервов относятся все, расположенные за пределами головного и спинного мозга. Они образуют широкую сеть, регулируют работу внутренних органов, сокращение мышц. Поэтому при возникновении нейропатии формируется большое количество симптомов, которые иногда ошибочно принимают за патологию определенного органа. Но лечение окажется безрезультатным, если не установить причину нарушений и не использовать методы комплексной терапии нерва.
Виды нейропатии
Разновидности нейропатии определяют в зависимости от количества пораженных нервов. Если в патологический процесс вовлекается только один нерв, говорят о мононейропатии. Такой тип заболевания, компрессионно-ишемическая нейропатия, чаще возникает в крупных нервных стволах – бедренном, седалищном, тройничном или лучезапятсном нерве. Патологию относительно легко диагностировать, симптомы появляются по направлению расположения нервного ствола в тканях.
Еще один вид – ишемическая нейропатия, но она затрагивает только зрительный нерв. По сути, это его инфаркт, приводящий к падению остроты зрения, вплоть до слепоты. Отдельно выделяют посттравматическую нейропатию, которая возникает в результате перелома, сдавления конечности, растяжения связок или других ранениях.
При полинейропатии поражаются целые группы периферических нервов. Заболевание может возникать одновременно в нескольких конечностях, часто симметрично на разных половинах тела, сопровождается большим количеством симптомов. В зависимости от причин, выделяют следующие виды полинейропатии:
Нейропатии делят на несколько типов, в зависимости от характера поражения нервного ствола. Они могут быть аксональные, когда повреждается внутренняя часть нерва, и демиелинизирующие, при которых разрушается оболочка и нарушается передача нервного импульса.
Причины болезни
Пациенты не всегда своевременно обращаются за помощью. Причиной тому являются многочисленные заблуждения, связанные с этим заболеванием. Так, многие уверены, что беспричинная боль пройдет сама. Но это не так, со временем патология прогрессирует, и лечение становится труднее.
Причиной нарушения функции нервов являются несколько факторов одновременно. При диабете повреждение возникает из-за нарушения кровоснабжения и метаболизма в нервной ткани, формировании отека и сдавления, синтезе антител к оболочке нервных стволов. В результате они атрофируются и приводят к появлению патологии.
Токсические и инфекционные поражения также связаны с разрушением внешней оболочки нервных волокон. При алкоголизме, дефиците витамина В12, избытке В6 и нарушениях питания в первую очередь разрушаются мелкие периферические нервные отростки – аксоны, что вызывает потерю чувствительности на кистях или стопах.
Атеросклероз сосудов, тромбоз мелких капилляров в совокупности с метаболическими нарушениями также становятся причиной нейропатии. По такому типу поражается зрительный нерв. У беременных полинейропатия связана с выработкой антител, нарушением питания нервов и токсическим повреждением собственными продуктами метаболизма.
Наследственные нейропатии характеризуются генетическими нарушениями, которые приводят к изменениям метаболизма и накоплению токсических веществ в тканях. Они повреждают миелиновую оболочку нерва. В некоторых случаях наследственное заболевание приводит к постепенной атрофии групп нервов и тяжелым двигательным, сенсорным нарушениям, которые не поддаются лечению.
Симптомы полинейропатии
Поводом для обращения к неврологу становятся беспричинные боли или чувство дискомфорта. Симптомы нейропатии зависят от типа заболевания, вовлечения в патологический процесс внутренней части нерва или только его оболочки.
Насторожить должны следующие симптомы:
Иногда появляется патологическая гиперчувствительность, когда слабое касание определенного участка тела вызывает сильную боль, а при значительном воздействии ощущения отсутствуют. Болевая чувствительность может полностью исчезать, поэтому, например, небольшая травма, порез не будет замечен. Но из-за нарушения иннервации такая рана долго заживает и часто переходит в форму трофической язвы.
В запущенных случаях появляются вегетативные нарушения, может повышаться или снижаться артериальное давление, изменяется работа пищеварительного тракта, ухудшается кровоснабжение кожи, она выглядит бледной, сухой и атрофичной.
Часто человек привыкает к этим ощущениям и из-за этого откладывает визит к врачу. Так повышается риск прогрессирования заболевания, ставшего причиной патологии нервной системы. А тем временем истощаются защитные ресурсы организма. При нейропатии может произойти безболевой инфаркт миокарда, так как из-за повреждения чувствительных нервов человек не будет чувствовать боль.
Раннюю диагностику этих состояний можно пройти на диагностическом комплексе Медмарвэл, которые установлены в медицинских кабинетах 36,6. Уже через 10 минут вы сможете узнать, если ли у вас ранние, начальные, еще не ставшие патологией, проявления нейропатии.
Как лечить нейропатию
Нет смысла самостоятельно искать лекарство от нейропатии. Это следствие, а не причина. Лечить нужно заболевание, которое ее вызвало. В каждом конкретном случае назначается своя терапия. Поэтому без помощи врача здесь не обойтись.
Поддержать состояние помогут вазоактивные препараты и витамины группы B, особенно при алкогольном или токсическом поражении. Не будут лишними средства для улучшения кровообращения, восстановления проводимости волокон и легкой седации.
Ошибка – заглушать ощущения обезболивающими. Они только избавляют от дискомфорта, но не лечат. А заболевание, ставшее первопричиной нейропатии, остается без внимания.
Не является альтернативой терапии и здоровый образ жизни. Изменить рацион, бросить курить и заняться спортом полезно, все это улучшает общее самочувствие. Но меры эти – второстепенные и лечения не заменяют.
Для лечения полинейропатии используются комплексные методы воздействия. В некоторых случаях необходимо наблюдение невролога и нескольких профильных специалистов – при диабете – у эндокринолога, при патологии почек – уролога, алкоголизме – нарколога.
Уменьшить неприятные болезненный ощущения, судорожные сокращения и чувство жжения помогают трициклические антидепрессанты, противосудорожные препараты. (Здесь нужна ссылка не на Финлепсин, а на Габапентин) При инфекционных причинах полинейропатии, особенно вызванной ВИЧ-инфекцией, полностью вылечиться от патологии невозможно, но при правильной терапии основного заболевания можно остановить ее прогрессирование.
Некоторым пациентам с аутоиммунными, токсическими или метаболическими расстройствами назначают плазмоферез. Очищение крови позволяет избавиться от веществ, которые вызывают повреждение нервных стволов. На этапе восстановления используют ЛФК, физиопроцедуры: электрофорез, магнитотерапию, лазеротерапию, акупунктуру.
Откладывать посещение невролога не стоит. Лучше, как можно раньше подобрать адекватное лечение, избавиться от неприятных симптомов и не допустить дальнейшего негативного влияния на организм.
Профилактика нейропатии
Предотвратить развитие некоторых форм нейропатии тяжело, предугадать формирование наследственного заболевания можно только при обследовании у генетика. Но возможно повлиять на развитие патологий, связанных с образом жизни.
Чтобы избежать болезни, необходимо снизить потребление алкоголя, а при склонности к алкоголизму – пройти специальное лечение. Часто нейропатия является следствием сахарного диабета. Но при хорошем контроле уровня глюкозы, поддержании его в пределах физиологических значений с помощью диеты или инъекций инсулина, можно избежать развития осложнений.
Для профилактики нейропатии необходимо избегать травм, при занятиях экстремальными видами спорта использовать качественную защиту и страховку. Беременным женщинам уменьшить вероятность патологии помогает правильная прегравидарная подготовка, применение комплекса поливитаминов до зачатия, лечение хронических заболеваний.
Будик Александр Михайлович, невролог, КМН, главный врач медицинских кабинетов 36,6
ИМЕЮТСЯ ПРОТИВОПОКАЗАНИЯ, ПЕРЕД ПРИМЕНЕНИЕМ НЕОБХОДИМО ПРОКОНСУЛЬТИРОВАТЬСЯ СО СПЕЦИАЛИСТОМ
Причины полинейропатии конечностей
Причины полинейропатии конечностей
Полинейропатия конечностей – это патология периферической нервной системы, при которой поражаются многочисленные нервные волокна, отвечающие за передачу команд от головного мозга к мышцам. При нормальном функционировании этой системы человек способен вести активную жизнедеятельность, но когда происходит малейшее нарушение – человек теряет способность полноценно пользоваться органами чувств и двигаться. В отличие от невропатии лицевого нерва, которая затрагивает только мышцы лица, данное заболевание может поразить как одну из верхних или нижних конечностей, так и несколько одновременно.
Как распознать полинейропатию конечностей?
На сегодняшний день врачи обращают внимание пациентов на то, что течение полинейропатии может отличаться не только у разных людей, но даже у одного и того же самого пациента при повторном проявлении. Развивается болезнь в некоторых случаях слабо, с постепенным нарастанием симптомов, а в некоторых – молниеносно. В первом случае речь идет о 4-5 неделях, во втором же прогресс происходит менее, чем за неделю.
Для того, чтобы поставить диагноз полинейропатия конечностей, требуется провести пациенту электромиографию – именно этот метод, а не субъективные симптомы, ощущаемые человеком, способен показать объективную картину состояния здоровья человека. Именно при помощи такого обследования не только удается обнаружить патологию на самых ранних этапах ее развития, но и определить тип, степень и уровень поражения, которому подверглись нервные волокна конечностей.
Причины возникновения заболевания и его симптомы
Существует целый ряд факторов, которые, по отдельности или в совокупности, способны привести к тому, что у человека будет развиваться полинейропатия. Это могут быть как соматические заболевания (аллергия, сахарный диабет, перенесенные инфекции, эндокринные нарушения), так и внешние факторы (интоксикация организма алкоголем, побочные действия антибиотиков, попадание в организм солей тяжелых металлов), а в некоторых случая – и наследственная предрасположенность.
Врачи утверждают, что причина, спровоцировавшая заболевание, не играет никакой роди в симптоматике. В любом случае, больной заметит у себя определенные признаки:
Перечисленные симптомы встречаются как поодиночке, так и сочетано, при этом чем сильнее запущено состояние, тем их больше и они явственнее. На поздних стадиях появляются болевые ощущения, — сперва на ногах, а впоследствии – и на верхних конечностях. Если попытаться выстроить из признаков цепочку, то она будет выглядеть примерно следующим образом: онемение конечностей-зябкость стоп-жжение-отеки рук и ног-образование язв.
Лечение полинейропатии
Не нужно обладать глубокими медицинскими познаниями для того, чтобы понять, что если полинейропатия спровоцирована каким-либо соматическим заболеванием, начинать терапию следует именно с его устранения. Помимо назначенной врачом терапии, направленной непосредственно на борьбу с заболеванием, не лишним будет принять курс поливитаминов, а также иммуномодуляторов. Умеренные физические нагрузки в этом случае тоже не помешают.
Следует помнить, что каждый день перенесенного заболевания – это угроза для нормального функционирования верхних и нижних конечностей, а потому чрезвычайно важно и на протяжении курса лечения, и некоторое время после него выполнять специальные физические упражнения.
Утерянные двигательные функции конечностей можно попытаться восстановить при помощи массажа. Обратите внимание на то, что массаж нужен именно лечебный, который назначает непосредственно лечащий врач. Начинать сеансы массажа можно на любой стадии полинейропатии, однако чем раньше это будет сделано, тем выше вероятность того, что функции конечностей будут полностью восстановлены. Курс лечебного массажа составляет не менее 30 процедур, при это во время одной процедуры массажу каждой конечности должно уделяться как минимум 5-10 минут.
Лечение болевой формы диабетической полинейропатии
Диабетическая дистальная симметричная сенсорно-моторная полинейропатия (ДПН) — самый частый вариант диабетической нейропатии, который выявляется более чем у 50% больных с сахарным диабетом (СД) 1-го и 2-го типа.
Диабетическая дистальная симметричная сенсорно-моторная полинейропатия (ДПН) — самый частый вариант диабетической нейропатии, который выявляется более чем у 50% больных с сахарным диабетом (СД) 1-го и 2-го типа [1]. ДПН является второй по частоте встречаемости причиной нейропатической боли (НБ). Распространенность ДПН варьирует в зависимости от используемых диагностических критериев. Частота нейропатии, диагностируемой на основании симптомов, составляет около 25%, а при проведении электронейромиографического исследования — 100% у больных СД [2].
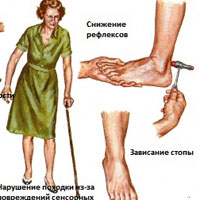
Диагноз ДПН основывается на тщательно собранном анамнезе, неврологическом обследовании, электрофизиологическом исследовании. Типичными симптомами являются ощущение «бегания мурашек», жжения, боли в голенях и стопах, ночные судороги мышц. При неврологическом обследовании выявляются ослабление ахилловых рефлексов, нарушение чувствительности по типу «носков» и «перчаток», снижение проприоцептивной чувствительности. При несвоевременно начатом лечении и неэффективности терапии развиваются такие осложнения ДПН, как язвы стоп, которые могут приводить к некрозу, гангрене (диабетическая стопа) и часто к ампутациям. Пациенты с СД нуждаются в ежегодном неврологическом и клиническом обследовании стопы [3].
Общепризнано, что основной причиной развития ДПН является повышенный уровень глюкозы [4]. Соответственно, единственным подтвержденным методом лечения, способным замедлять и даже в некоторой степени обращать прогрессирование ДПН, является хороший контроль уровня гликемии у больных с инсулинзависимым СД. У пациентов с интенсивной терапией СД (3 или более инъекции инсулина в день либо выполнение непрерывной подкожной инфузии инсулина с помощью дозатора инсулина (уровень HbA1c в диапазоне 6,5–7,5)) наблюдалось достоверное снижение риска развития микрососудистых осложнений и нейропатии [5]. Интенсивное лечение сульфонилмочевинами пациентов с инсулинонезависимым типом СД также приводило к снижению частоты и прогрессирования нейропатии [6]. Однако только достижение нормогликемии не способно быстро ликвидировать клинические проявления ДПН. В связи с этим требуется дополнительное патогенетическое и симптоматическое лечение, особенно для купирования болевого синдрома.
К препаратам патогенетического действия относится альфа-липоевая (тиоктовая) кислота (Эспа-липон, Тиоктацид, Тиогамма, Тиолепта). Эти препараты являются золотым стандартом патогенетического лечения ДПН. Альфа-липоевая кислота является мощным липофильным антиоксидантом. Тиоктовая кислота, накапливаясь в нервных волокнах, снижает содержание свободных радикалов; увеличивает эндоневральный кровоток; нормализует содержание NO, регулятора расслабления сосудистой стенки (если его много, как при СД, то он начинает действовать как свободный радикал); улучшает эндотелиальную функцию; снижает уровень общего холестерина, увеличивает уровень антиатерогенной фракции липопротеинов высокой плотности. В ряде исследований показано, что применение альфа-липоевой кислоты в дозе 600 мг/день в/в или перорально в течение от трех недель до шести месяцев уменьшает в клинически значимой степени главные симптомы ДПН, включая боль, парестезии и онемение [7, 8]. Оптимальным считается назначение в начале лечения внутривенного капельного введения альфа-липоевой кислоты (600 мг на 200 мл физиологического раствора) в течение 3 недель (15 капельниц) с последующим приемом 600 мг препарата в виде таблеток (один раз в день за 30–40 минут до еды) в течение 1–2 месяцев.
К препаратам, которые улучшают метаболизм пораженных нервных структур, традиционно относятся витамины группы B, что обусловлено их нейротропными свойствами. Витамин B1 участвует в синтезе ацетилхолина, а В6 — в синтезе нейромедиаторов, передаче возбуждения. Витамин В12 улучшает трофику периферических нервов. Показана высокая эффективность препарата Мильгамма драже в комплексном лечении ДПН. В его состав входят 100 мг бенфотиамина и 100 мг пиридоксина. Препарат назначается по одному драже 2–3 раза в сутки в течение 3–5 недель. Важно, что Мильгамма содержит бенфотиамин, липидорастворимость которого является причиной достижения высокой концентрации тиамина в крови и тканях.
Данные об эффективности и профиле безопасности позволяют рассматривать альфа-липоевую кислоту и бенфотиамин как препараты первой линии патогенетически ориентированной терапии диабетической полинейропатии [9].
В двух мультицентровых плацебо-контролируемых исследованиях 1335 пациентов с ДПН показано, что прием ацетил-L-карнитина в дозе 1000 мг 3 раза в день в течение 6 и 12 месяцев значительно уменьшал симптоматику ДПН [10].
Направление патогенетической терапии является чрезвычайно важным и во многом предопределяет прогноз. Однако лечение проводится длительными курсами и не всегда сопровождается быстрым очевидным клиническим улучшением. В то же время даже при негрубой ДПН может иметь место выраженный болевой синдром, приводя к нарушениям сна, депрессии, тревоге и социальной дезадаптации. Именно поэтому параллельно с патогенетической терапией чрезвычайно важно проводить своевременную симптоматическую терапию НБ.
Хочется сразу подчеркнуть, что простые анальгетики и нестероидные противовоспалительные препараты в лечении болей при ДПН не рекомендуются из-за их неэффективности [11]. К сожалению, в мире более 60% больных с НБ по-прежнему получают эти препараты, что недопустимо и чрезвычайно опасно при длительном применении (осложнения со стороны желудочно-кишечного тракта (ЖКТ), печени и крови). Основными группами препаратов для лечения НБ при ДПН являются: антидепрессанты, антиконвульсанты, опиоиды, антиаритмические средства, средства местного действия.
Трициклические антидепрессанты (ТЦА) стали одними из первых препаратов, которые продемонстрировали свою эффективность в лечении пациентов с НБ [12]. Тем не менее в России зарегистрирован только один ТЦА — амитриптилин, который используется для лечения НБ (постгерпетическая невралгия, ДПН). Считается, что обезболивающее действие ТЦА связано с ингибированием ими обратного захвата серотонина и норадреналина, следствием чего является усиление нисходящей активности норадренергических и серотонинергических систем, оказывающих тормозящее влияние на проведение болевых импульсов по ноцицептивным путям в ЦНС.
Помимо блокирования обратного захвата серотонина и норадреналина ТЦА блокируют альфа1-адренергические, Н1-гистаминовые, М-холинергические рецепторы, что обусловливает целый ряд противопоказаний и побочных эффектов, ограничивающих их применение. Среди побочных эффектов наблюдаются нарушение зрения, сухость во рту, синусовая тахикардия, запор, задержка мочи, спутанность сознания и/или нарушение памяти (антихолинергические эффекты); седативный эффект, сонливость, увеличение веса (Н1-гистаминовые эффекты); ортостатическая гипотензия, головокружение, тахикардия (альфа1-адренергические эффекты) [13]. ТЦА противопоказаны больным с острым и подострым инфарктом миокарда, с нарушением внутрижелудочковой проводимости, с закрытоугольной глаукомой, принимающими ингибиторы моноаминоксидазы (ИМАО). Эти препараты следует применять с осторожностью пациентам с ишемической болезнью сердца (ИБС), аритмией, артериальной гипертонией, после инсульта, а также с задержкой мочи или вегетативной недостаточностью. Данное обстоятельство существенно ограничивает применение ТЦА в общемедицинской практике.
Эффективность применения ТЦА (амитриптилин, дезипрамин, кломипрамин, имипрамин) при лечении болевой формы ДПН показана в ряде рандомизированных плацебо-контролируемых исследований [14]. Наиболее распространенными препаратами этой группы, применяемыми для лечения болевых полинейропатий, являются амитриптилин и имипрамин [15]. Наиболее широко используется амитриптилин. Начальная доза препарата составляет 10–12,5 мг на ночь, затем дозу постепенно увеличивают на 10–25 мг каждые 7 дней до достижения эффекта (максимально до 150 мг/сут). Суточную дозу принимают однократно на ночь или дробят на 2–3 приема. При сопутствующей депрессии обычно требуется назначение более высоких доз препарата. При непереносимости амитриптилина возможно назначение других ТЦА, например имипрамина или кломипрамина. Пробное лечение антидепрессантами должно продолжаться как минимум 6–8 недель, при этом максимально переносимую дозу пациент должен принимать не менее 1–2 недель. Хотя амитриптилин эффективен примерно у 70% больных с НБ, выраженные побочные эффекты ограничивают его применение. Перед назначением любого ТЦА обязательно предварительное проведение ЭКГ, особенно у лиц старше 40 лет.
При плохой переносимости ТЦА возможно применение тетрациклических антидепрессантов (например, мапротилина, 25–100 мг/сут) или селективных ингибиторов обратного захвата серотонина и норадреналина (СИОЗСН) (венлафаксина, 150–225 мг/сут, или дулоксетина, 60–120 мг/сут) [16]. Эффективность венлафаксина неоднократно доказана в ходе исследований, включавших пациентов с ДПН [17, 18], при этом у него отсутствуют постсинаптические эффекты, свойственные для ТЦА (действие на М-холинорецепторы, альфа-адренергические и гистаминовые рецепторы). Это делает препарат более безопасным, чем ТЦА. Наступление противоболевого эффекта отмечено уже на второй неделе терапии [19].
Таким образом, венлафаксин является эффективным, безопасным, хорошо переносимым лекарственным средством при лечении ДПН. В трех мультицентровых рандомизированных двойных слепых плацебо-контролируемых исследованиях длительностью от 12 до 13 недель показана эффективность применения дулоксетина в дозе от 60 до 120 мг/сут у больных с болевой ДПН. В результате исследований обнаружено 50% снижение интенсивности боли при лечении дулоксетином (вне зависимости от применяемой дозы) у 41% больных, по сравнению с 24% пациентов, принимавших плацебо [20].
Селективные ингибиторы обратного захвата серотонина (СИОЗС) (флуоксетин, пароксетин, сертралин, циталопрам, эсциталопрам) вызывают меньше побочных действий, но оказывают менее отчетливый противоболевой эффект, что, возможно, объясняется отсутствием прямого влияния на норадренергическую передачу. Они показаны, главным образом, в тех случаях, когда боль связана с депрессией, а больной плохо переносит другие антидепрессанты [16].
Поскольку НБ часто сопровождается депрессией, актуальным является выбор препарата, эффективно воздействующего на это психопатологическое состояние и обладающего хорошим профилем безопасности. Одним из таких препаратов является пипофезин (Азафен) [21]. Механизм антидепрессивного действия основан на неизбирательном ингибировании обратного захвата серотонина и норадреналина, что приводит к увеличению их концентрации в ЦНС. Препарат не обладает кардиотоксическими свойствами. В связи с отсутствием холинолитического действия Азафен можно назначать больным глаукомой и другими заболеваниями, при которых противопоказано применение препаратов, обладающих холинолитической активностью, в том числе имипрамина и амитриптилина. Отсутствие выраженных побочных явлений позволяет назначать препарат больным с соматическими заболеваниями и лицам пожилого возраста, прежде всего, в амбулаторной практике.
Среди антиконвульсантов, применяемых при лечении болевой ДПН, наиболее эффективными являются габапентин (Нейронтин) и прегабалин (Лирика) [22, 23]. Механизм действия габапентина и прегабалина, по-видимому, основан на способности связываться с альфа-2-дельта-субъединицами потенциалзависимых кальциевых каналов периферических сенсорных нейронов. Это приводит к снижению входа кальция в пресинаптический нейрон, в результате чего уменьшается высвобождение главных медиаторов боли (глутамата, норадреналина и субстанции Р) перевозбужденными нейронами, что сопровождается редукцией болевого синдрома. Оба препарата обладают хорошей переносимостью и высокой эффективностью, наблюдаемой уже на 1-й неделе лечения. Наиболее частыми побочными эффектами являются головокружение и сонливость. Начальная доза габапентина — 100–300 мг на ночь. Затем суточную дозу постепенно увеличивают каждые 3–5 дней на 100–300 мг, переходя на трехкратный прием.
Средняя эффективная доза составляет 1800 мг/сут (600 мг 3 раза в день), максимальная — 3600 мг/сут. На титрование дозы габапентина может уйти от 2 до 8 недель. Прежде чем делать вывод о неэффективности препарата, его максимально переносимую дозу следует принимать 1–2 недели. По показателям эффективности и безопасности прегабалин примерно соответствует габапентину, но в отличие от габапентина обладает линейной фармакокинетикой, что обеспечивает предсказуемость изменений концентрации препарата в плазме крови при изменении дозы. Диапазон суточных доз преагабалина — 150–600 мг/сут в 2 приема.
При лечении болевой ДПН стартовая доза может составлять 150 мг/сут. В зависимости от эффекта и переносимости дозу можно увеличить до 300 мг/сут через 3–7 дней. При необходимости можно увеличить дозу до максимальной (600 мг/сут) через 7-дневный интервал. В соответствии с опытом применения препарата, при необходимости прекращения приема рекомендуется постепенно снижать дозу в течение недели. Прегабалин быстрее всасывается в кровь и обладает более высокой биодоступностью (90%) по сравнению с габапентином (33–66%). Вследствие этого препарат эффективен в меньших дозах и обладает меньшей частотой и выраженностью побочных эффектов, в особенности седации [22, 23].
Использование опиоидов для лечения болевых синдромов возможно только при отсутствии эффекта от других препаратов. Среди опиоидов наиболее эффективными при лечении болевой ДПН оказались оксикодон в дозе 37–60 мг/сут [24] и трамадол (препарат, обладающий низкой аффинностью к опиоидным μ-рецепторам и одновременно являющийся ингибитором обратного захвата серотонина и норадреналина). Лечение трамадолом начинают с дозы 50 мг на ночь (или 25 мг 2 раза в день), спустя 5–7 дней дозу увеличивают до 100 мг/сут. При необходимости дозу повышают до 100 мг 2–4 раза в день. Пробное лечение трамадолом должно продолжаться не менее 4 недель [25]. Опиоиды ценятся за их болеутоляющие свойства, но препараты этого класса вызывают в организме и чрезвычайно выраженные и опасные побочные эффекты.
Комбинация трамадола с парацетамолом (Залдиар) позволяет снизить дозу трамадола и тем самым риск побочного действия, не жертвуя анальгетическим эффектом [26]. При комбинации двух указанных препаратов, обладающих разным механизмом действия (механизм анальгетического эффекта парацетамола может быть связан с ингибирующим эффектом на центральный синтез простагландинов, возможно, за счет торможения ЦОГ-3), возникает эффект синергизма. Адекватное обезболивание при приеме комплекса препаратов наблюдается в 1,5–3 раза чаще, чем при применении каждого из соединений в соответствующих дозах.
Кроме того, для парацетамола и трамадола характерен взаимодополняющий фармакокинетический профиль, благодаря которому препарат быстро начинает действие — уже через 15–20 минут (за счет парацетамола) и длительное время поддерживает анальгетический эффект (за счет трамадола) [26]. В состав Залдиара входит низкая доза трамадола (в одной таблетке содержится 37,5 мг трамадола и 325 мг парацетамола), поэтому побочные эффекты при его применении возникают реже, чем при применении трамадола. Назначение препарата не требует длительного титрования дозы, лечение может быть начато с дозы 1–2 таблетки в день, в последующем доза может быть повышена до 4 таблеток в сутки.
Пероральный антиаритмический препарат мексилетин также относится к анестетикам. Считается, что мексилетин блокирует натриевые каналы, таким образом стабилизируя мембрану нейронов и блокируя передачу болевых импульсов. Испытания по применению мексилетина при НБ дают противоречивые результаты. В ряде случаев мексилетин значительно уменьшает боль, особенно при его применении в высоких дозах. Однако при этом чаще возникают побочные эффекты, в частности со стороны ЖКТ. Препарат следует применять с осторожностью при наличии в анамнезе сердечной патологии или выявлении нарушений при ЭКГ-исследовании [27].
В ряде исследований было показано, что применение местных анестетиков (кремов, гелей и пластыря (Версатис) с 5-процентным содержанием лидокаина или препаратов на основе экстрактов жгучего перца — капсаицина) было эффективным при лечении болевой формы ДПН [27, 28]. Эффект лидокаина основан на блокировании транспорта ионов натрия через мембрану периферических нейронов, в результате чего происходит стабилизация клеточной мембраны, замедляется распространение потенциала действия, а следовательно, уменьшается боль. Из побочных эффектов может наблюдаться местное раздражение кожи в области нанесения, которое чаще всего незначительно и быстро проходит. Действие препаратов капсаицина основано на истощении запасов субстанции Р в терминалях сенсорных волокон. Жжение, покраснение и зуд в месте нанесения являются наиболее частыми побочными эффектами, часто отмечается усиление боли при первом нанесении препарата.
Тем не менее ни одно лекарственное средство нельзя рассматривать в качестве единственного препарата для лечения боли при ДПН [29]. Нередки случаи, когда применение любого из перечисленных выше средств оказывается недостаточно эффективным и возникает потребность в комбинации препаратов. Поэтому хотя число одновременно принимаемых пациентом лекарственных средств по общему правилу следует стараться ограничивать, но в большинстве случаев НБ при ДПН удается адекватно контролировать лишь с помощью комбинации двух и более препаратов. Нерационально сразу же назначать комбинацию нескольких средств: первоначально следует испробовать один препарат, и лишь убедившись, что в переносимых данным пациентом дозах он оказывает лишь частичный эффект, к нему следует присоединить следующее средство, которое, как правило, обладает иным механизмом действия.
В клинической практике часто комбинируют антидепрессант с антиконвульсантом, антиконвульсант с трамадолом или Залдиаром. Рекомендуется избегать сочетания трамадола (особенно больших доз) с ИМАО, СИОЗС и СИОЗСН, так как подобная комбинация может спровоцировать серотониновый синдром. С осторожностью трамадол следует назначать в комбинации с трициклическими антидепрессантами (учитывая риск серотонинового синдрома) [30].
Нефармакологические методы лечения ДПН включают в себя психотерапию, бальнеотерапию, гипербарическую оксигенацию (1,2–2 атм.), фототерапию, магнитотерапию, электрофорез, диадинамические токи, электростимуляцию паретичных мышц, чрескожную электронейростимуляцию, иглорефлексотерапию. Противопоказанием к их применению является тяжелое состояние больного, обусловленное соматической патологией и/или тяжелая декомпенсация метаболизма. Рядом авторов показана высокая эффективность электростимуляции спинного мозга, используемой для лечения болевой диабетической нейропатии [31]. Как правило, имплантацию стимуляторов производят у пациентов с рефрактерными к фармакотерапии болевыми синдромами.
В заключение следует заметить, что лечение каждого пациента должно быть индивидуальным с учетом клинических особенностей, а также наличия коморбидных заболеваний (тревоги, депрессии, заболеваний внутренних органов и т. д.). При выборе лекарственных препаратов, помимо непосредственного анальгетического эффекта, должны быть учтены другие положительные эффекты выбранного препарата (уменьшение уровней тревоги, депрессии, улучшение сна и настроения), а также его переносимость и возможность развития серьезных осложнений.
Ряд авторов в качестве препаратов первого ряда при лечении болевых форм полинейропатий рекомендуют ТЦА и габапентин или прегабалин. К препаратам второго ряда относят СИОЗСН — венлафаксин и дулоксетин. Они обладают меньшей эффективностью, но более безопасны, имеют меньше противопоказаний по сравнению с ТЦА, и им должно быть отдано предпочтение при лечении больных с сердечно-сосудистыми факторами риска. Препараты третьей линии включают в себя опиоиды. К препаратам с более слабым эффектом относятся капсаицин, мексилетин, окскарбазепин, СИОЗС, топиромат, мемантин, миансерин [32].
Литература
*Первый МГМУ им. И. М. Сеченова, **МОНИКИ им. М. Ф. Владимирского, Москва