Полиморфная палочка в мазке у женщин что
Что говорит о здоровье женщины результат мазка на флору
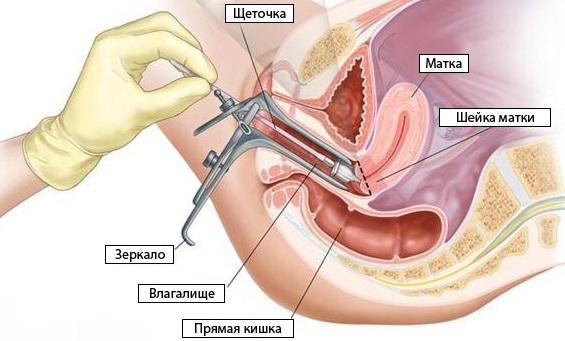
У всех пациенток врач-гинеколог во время приема берет мазки со слизистой половых путей. Однако разобраться в результатах анализа достаточно сложно. Что же означают странные термины, указанные на бланке с результатами: палочковая, кокковая и коккобациллярная флора, и хорошо это или плохо, если флоры нет совсем.
Палочковая флора
Такая запись – признак женского здоровья. У пациентки в половых путях живут лактобациллы (палочки Додерлейна), синтезирующие молочную кислоту и поддерживающие кислую среду, не дающую развиваться патогенным бактериям. Получив такой результат, можно не волноваться – в вашем организме всё хорошо.
Однако если вместо палочек Додерлейна найдена кишечная палочка – это совсем другая история. Этот микроорганизм должен находиться в кишечнике, а его попадание в соседние органы приводит к воспалительным процессам – кольпитам, циститам и уретритам. Причины обнаружения возбудителя – ношение грязного белья, несоблюдение гигиены женщиной или ее партнером. Для лечения назначают антибиотики.
Кокковая флора
В мазке могут обнаруживаться диплококки, сарцины, стрептококки, стафилококки, энтерококки. Единичные кокки считаются вариантом нормы, но большое количество этих бактерий указывает на воспалительный процесс. Энтерококки, как и кишечная палочка, проникают в вагинальную среду из прямой кишки, и без лечения могут вызвать эндоцервицит – воспаление слизистой шейки матки.
Но самые неприятные представители кокковой флоры – гонококки, появляющиеся при заражении гонореей. Выявление даже единичных возбудителей требует срочного лечения. Женщины часто являются носителями гонококка, но при этом сами не испытывают симптомов половой инфекции. Не зная о своей болезни, они заражают партнеров, у которых возникает гонорейный уретрит.
В этом случае женщине показано антибактериальное лечение и обследование на других возбудителей ЗППП. Чаще всего для этого проводится ПЦР-реакция, обнаруживающая минимальное количество патогенных микробов и простейших.
Обнаружение кокковой флоры – плохой знак, указывающий на инфекционные воспалительные процессы, требующие лечения и повторного контроля после антибиотикотерапии.
Коккобациллярная флора
К этой категории относятся бациллы, находящиеся по своему строению между палочками и кокками – гарднерелла, хламидии, гемофильная палочка. Обнаружение таких возбудителей указывает на вагинальный дисбактериоз (дисбиоз), вызванный заражением, бесконтрольным приемом антибиотиков или частыми спринцеваниями. Коккобациллярная флора часто «расцветает» на фоне падения иммунитета.
Возбудители меняют среду с кислой на щелочную, убирая барьер на пути других инфекций. На фоне дисбиоза часто развивается молочница и в мазках обнаруживается мицелий гриба.
При обнаружении большого количества коккобацилл, в бланке результатов указывается, что коккобациллярная форма обильная. Если таких бактерий немного, врач напишет, что она скудная или умеренная.
В результатах мазка можно увидеть и другие обозначения выявленной флоры – грамвариабельная или полиморфная. Запись свидетельствует об обнаружении в анализах разной грамположительной и грамотрицательной флоры.
При таких результатах женщине придется долго лечиться, чтобы избавиться от патогенных микробов, проникших в ее интимную зону. Поскольку у таких пациенток часто обнаруживаются скрытые половые инфекции, женщину направляют на ПЦР-диагностику. Показано УЗИ малого таза, ведь наличие гноеродных микробов свидетельствует о воспалительных процессах в малом тазу, которые надо выявить и вылечить.
Если флоры нет совсем
Отсутствие микроорганизмов в мазке свидетельствует о неправильной подготовке к сдаче анализа. Чаще всего такая ситуация возникает, если женщина перед приемом у врача использовала антибактериальные свечи или спринцевалась. Некоторые пациентки применяют спринцевания, поскольку считают, что к врачу надо идти «чистой». Но такая чистота делает взятие анализов бессмысленным.
Вторая причина отсутствия флоры – прием антибиотиков. Современные антибактериальные препараты убивают полезные бактерии во всём организме. Если не принять мер, у женщины разовьется дисбиоз и вместо нормальной флоры появится патогенная, чаще всего коккобациллярная. Поэтому пациенткам назначают пробиотики в свечах, лечащие дисбиоз.
Однако отсутствие флоры не свидетельствует об отсутствии скрытых ЗППП. В таких случаях, наоборот, часто выявляются разные венерические болезни, поэтому нужно пройти ПЦР-исследование и пересдать мазок.
Обнаружение в анализах трихомонад, уреаплазм, микоплазм и хламидий ничего хорошего не сулит. Такой женщине требуется серьезное обследование и длительное лечение с повторной сдачей анализов.
Четыре степени чистоты вагинальной слизистой
В результатах мазка указывается степень чистоты, к примеру II или III. Дело в том, что все анализы делятся по степени чистоты обнаруженной флоры на четыре категории:
По окончанию лечения женщина должна записаться на прием к гинекологу и сдать мазок повторно. Если медикаментозная терапия была подобрана успешно, показатели должны улучшиться. Однако при запущенных формах воспалительных процессов для достижения результата потребуется длительное лечение.
О врачах
Можно доверять! Данная статья проверена врачом и носит общий информационный характер, не заменяет консультацию специалиста. Для рекомендаций по диагностике и лечению необходима консультация врача.
Полиморфная палочка в мазке у женщин. Что это такое, лечение при беременности
Люди живут в мире бактерий, некоторые живут в организме человека постоянно, другие приходят извне. Одна из них – полиморфная палочка, часто встречающаяся в мазке у женщин.
Что такое полиморфная палочка
Бактерии существуют в различных формах. Одни имеют круглую или овальную, они называются кокки. Другие приобретают палочковидную форму, это бациллы. Третьи – существуют в виде спирали, называются спирохетами. Бактериальные формы не ограничиваются только этими 3 типами. Некоторые из них полиморфны, что означает существование в различных состояниях.
Такие бактерии не имеют определённой формы или отличаются от трёх известных стереотипных форм. Полиморфные бактерии видоизменяются, приспосабливаясь к геному человека. Полиморфная палочка, в мазке у женщин встречающаяся нередко, относится к бациллам, которые изменяют свою форму и имеют разные типы.
Патогенное воздействие полиморфной палочки
Нормальная микрофлора женского организма – это качественное и количественное соотношение микробных популяций, которые колонизировали определённую систему организма. Колонии бактерий участвуют в поддержании здоровья. Когда начинают преобладать патогенные микроорганизмы, нарушается баланс микрофлоры. Среди патогенов есть как палочковые формы, так и кокки.
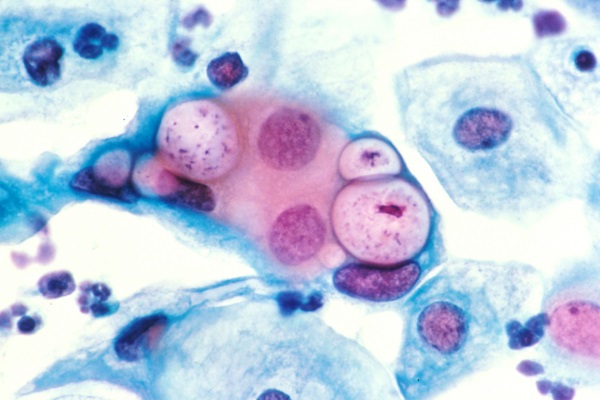
Влагалище женщины имеет кислую среду, потому что в ней содержится много молочной кислоты, вырабатываемой под воздействием эстрогена. Около 97% бактерий, населяющих микрофлору, относятся к молочно-кислым бактериям. Одновременно в микрофлоре присутствуют условно-патогенные организмы, кокки, палочки, бациллы.
Их количество не должно в норме превышать 10,3 КОЕ/мл. Превышение этого параметра говорит о начавшемся бактериальном заболевании. Увеличение кокков сопровождается разрастанием другой условно-патогенной формы – полиморфной палочки.
Причины появления полиморфной палочки
Полиморфная палочка в мазке у женщин – это микроскопический организм, который создаёт болезнетворную среду во влагалище, шейке матки или цервикальном канале. Под микрофлорой влагалища подразумевают совместное проживание разных бактерий.
Одни из них присутствуют в организме нормально, не вызывая никаких последствий. Кишечная палочка мирно живёт в желудке и принимает участие в процессе переваривания пищи. Так же и в половой сфере, многие бактерии трудятся на благо здоровья.
Но это разделение условное, среда микрофлоры делится на 3 категории:
За чистоту микрофлоры отвечают палочки Дедерлейна, поддерживающие кислую среду.
Они же принимают участие в создании антител к различным инфекциям, поддерживают влажность влагалища, сдерживают размножение патогенных микробов в допустимых нормах. Полиморфная палочка является микробом патогенным, способным в любой момент атаковать человека, поразить шейку матки, цервикальный канал.
Палочки Дедерлейна выступают антагонистом этому микробу, не давая полиморфам размножаться сверх меры. При уменьшении количества палочек Дедерлейна их место занимает полиморфная палочка, что указывает на образование дисбактериоза.
В крови начинает увеличиваться количество лейкоцитов, которые отвечают за борьбу с плохими микробами. Их усиленное размножение сигнализирует, что в организме начался инфекционный или воспалительный процесс.
Причины, по которым повышается количество полиморфов в микрофлоре:
Диагностика полиморфной палочки
Полиморфная палочка в мазке у женщины определяется с помощью бактериологического анализа. Для проведения диагностики сдают мазок на микрофлору. С помощью мазка трудно определить конкретный вид бактерий, которые преобладают в микрофлоре.
Для этого и проводится бактериологический посев, на основе которого не только определяют вид поселившейся бактерии, но и определяют чувствительность её к антибиотикам. Полученные результаты дают возможность врачу диагностировать гинекологические заболевания: кольпит, вагиноз. Часто большое скопление полиморфных палочек указывает на развитие вагинального дисбактериоза.
Влияние микробов на микрофлору:
| Состояние микрофлоры | Нарушения | Формы расстройств |
| Нормальное | Отсутствие отрицательной микрофлоры, преобладание лактобактерий | Нормальное состояние влагалищной среды |
| Промежуточное состояние | Количество лактобактерий умеренное, присутствие палочек, грамположительных и грамотрицательных кокков. Имеются лейкоциты и макрофаги. | Нормальное состояние у здоровых женщин, девочек-подростков, без объективных жалоб. |
| Влагалищный дисбиоз | Лактобактерий мало или они отсутствуют совсем. Многочисленная колония полиморфных палочек и кокков. Количество лейкоцитов колеблется. | |
| Вагинит | Просматривается увеличенное количество макрофагов, лейкоцитов, имеются гонококки, споры, мицелий. | Неспецифический или микотический вагинит, гонорея. |
Во время беременности преобладание полиморфной палочки отрицательно сказывается на здоровье женщины и будущего ребёнка. Анализы можно сдать в поликлиниках, где стоимость мазка не превышает 300 руб. Бактериологический посев стоит от 600 до 800 руб.
Когда необходимо обратиться к врачу
При появлении признаков, которые доставляют дискомфорт, следует обратиться к врачу — гинекологу:
Профилактика появления полиморфной палочки
Чтобы избежать расстройства микрофлоры:
Методы лечения полиморфной палочки
Для коррекции микрофлоры следует установить первопричину возникновения дисбиоза. Если не планируется беременность, гинекологическая операция, то можно обойтись без лекарственных препаратов, ожидая, пока равновесие не восстановится самостоятельно. При наличии отягчающих симптомов требуется медикаментозное лечение.
Полиморфная палочка, размножившаяся в микрофлоре, о чём свидетельствует мазок, взятый у женщины, лечится в 2 этапа.
Вначале предполагается применение антибактериальных и антисептических препаратов, которые подавляют размножение патогенов. На 2 этапе – используются препараты, восстанавливающие микрофлору. Между 1 и 2 этапом лечения назначаются лекарства, разрушающие биоплёнку, которую создают патогены для снижения активности клеток, защищающих организм.
Терапия антибактериальными препаратами имеет побочные эффекты в виде гибели естественной флоры и не всегда эффективна, вследствие того, что патогенные организмы принимают разнообразные формы. Многие бактерии имеют повышенное противодействие ко многим препаратам.
Лекарственные препараты
Антибактериальные препараты:
Лекарства на основе лактобактерий улучшают действие антибактериальной терапии:
Препарат, разрушающий бактериальную биоплёнку:
Прочие методы
Лечение предусматривает применение биопрепаратов, восстанавливающих биоценоз вагинальной микрофлоры.
Это препараты зубиотики:
Народные методы
Полиморфная палочка в мазке у женщин, обнаруженная во время посещения врача, может быть признаком вагинального дисбактериоза, который лечится домашними средствами.
Лечение с помощью тампонов:
Яблочный уксус является хорошим восстановителем рН среды. Его можно добавить в тёплую ванну для купания и посидеть в ней 30 мин.
Травы, обладающие лечебными свойствами:
Настои из трав используют для спринцевания, примочек, ванночек.
Возможные осложнения
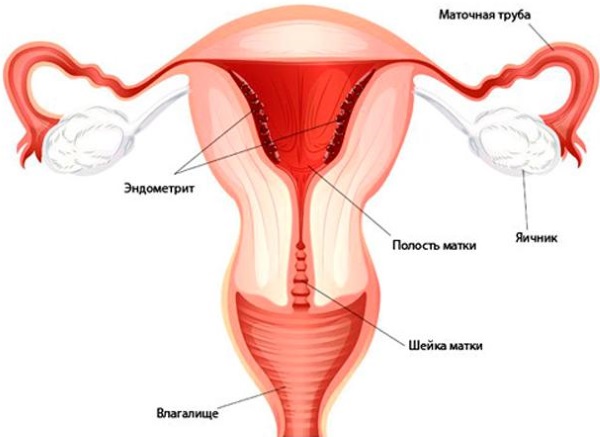
Образование больших колоний патогенных бактерий во влагалище грозит воспалением влагалищных стенок, шейки матки. Со временем бактерии проникнут в саму матку, что приведёт к развитию эндометрита, аднексита. Воспаление может затронуть мочеиспускательный канал и мочевой пузырь.
Скопление бактерий, пониженная готовность организма сопротивлению, приводит к половым инфекциям: вирусу герпеса, гонококкам, хламидиям.
Нарушение нормальной микрофлоры у женщин, одной из причин которой является полиморфная палочка, обнаруженная в мазке, совсем не безобидное заболевание. Не следует откладывать визит к врачу, потому что дисбиоз влагалища ведёт к серьёзным проблемам.
Автор: Беляева Анна
Видео о причинах появления и методах лечения полиморфной палочки у женщин
О нарушении микрофлоры:
Как расшифровать результаты мазка на флору:
Полиморфная палочка в мазке у женщин что
Исследование на микробиоценоз влагалища с микроскопией, урогенитальный мазок на микрофлору.
Синонимы английские
Gram’s Stain. Bacterioscopic examination of smears (vaginal, cervical, urethral).
Какой биоматериал можно использовать для исследования?
Мазок из половых путей женщины.
Как правильно подготовиться к исследованию?
Женщинам рекомендуется сдавать анализ до менструации или через 2-3 дня после ее окончания.
Общая информация об исследовании
Микроскопическое исследование мазка у женщин позволяет полуколичественно оценить общую микробную обсемененность, состояние эпителия влагалища, наличие и выраженность воспаления (по лейкоцитарной реакции), состав микрофлоры, а также выявить молочницу, трихомониаз и гонорею. Этот метод является «золотым стандартом» для диагностики бактериального вагиноза (чувствительность – 100 %). Норма мазка на флору определяется следующими показателями:
Для чего используется исследование?
Когда назначается исследование?
Что означают результаты?
Референсные значения для различных видов микроорганизмов зависят от их локализации (точки взятия биологического материала).
На основании микроскопической картины выделяют 4 типа микробиоценоза влагалища.
Тип микробиоценоза
Общая информация об исследовании
Доминирование лактобацилл, отсутствие грамотрицательной микрофлоры, спор, мицелия и псевдогифов, наличие единичных лейкоцитов и «чистых» эпителиальных клеток. Такой тип мазка у женщин является вариантом нормы.
Умеренное или сниженное количество лактобацилл, наличие грамположительных кокков и грамотрицательных палочек, лейкоцитов, моноцитов, макрофагов, эпителиальных клеток. Этот тип мазка на флору часто наблюдается у здоровых женщин и редко сопровождается явными симптомами.
Незначительное количество или полное отсутствие лактобацилл, обильная полиморфная грамотрицательная и грамположительная палочковая и кокковая микрофлора, наличие «ключевых» клеток, вариабельное количество лейкоцитов, отсутствие или незавершенность фагоцитоза. Вместе с этим часто обнаруживаются гарднереллы, микоплазмы, уреаплазмы, вибрионы рода Mobiluncus, анаэробные кокки.
Полимикробная картина мазка с большим количеством лейкоцитов, макрофагов, эпителиальных клеток, с выраженным фагоцитозом и практически полным отсутствием лактобацилл. При обнаружении возбудителей специфических инфекций (гонококков, трихомонад, псевдогифов споры) можно предполагать наличие гонореи, трихомониаза или кандидозного вагинита.
Что может влиять на результат?
Местное применение антисептиков, антибактериальных, противогрибковых и противозачаточных препаратов.
Гинекологический мазок «на флору»: на что смотреть, и как понять
Большинству женщин мазок «на флору» знаком, как самый «простой» гинекологический анализ. Однако исследование куда «полезнее», чем может казаться. И всего несколько (а то и одно) отклонений способны подсветить значимые проблемы, еще до появления каких-либо симптомов. Так как же понять полученные результаты? Рассказываем по пунктам.
1. Эпителий
Как известно, любой живой объект в природе имеет ограниченный срок жизни, по истечении которого он погибает «от старости».
Эпителий в гинекологическом мазке – это и есть слущенные «старые» клетки слизистой оболочки влагалища, цервикального или уретры (в зависимости от оцениваемого локуса). Которые могут присутствовать в материале в умеренных количествах.
Превышение нормативных пределов («много» или «обильно») может указывать на:
Уменьшение или отсутствие эпителия в мазке – на атрофические изменения, недостаток эстрадиола или избыток андрогенов.
Кроме того, ввиду зависимости эпителия от уровня половых гормонов, его количество в материале может сильно меняться в зависимости от дня цикла, начиная с единичного «в поле зрения» в самом начале – до умеренного и даже большого количества ближе к овуляции и во время нее.
А появление в мазке так называемых «ключевых клеток» (эпителий, «облепленный» мелкими кокковыми бактериями) – является маркером бактериального вагиноза.
2. Лейкоциты
«Норма» лейкоцитов в мазке также сильно зависит от стадии цикла и уровня половых гормонов, а также исследуемого локуса.
Так, за «максимум» для:
Повышение показателя – очевидно, свидетельствует о воспалении, а полное отсутствие может иметь место в норме в самом начале цикла.
Слизь
Результат «отсутствует», «мало» или «умеренно» для этого показателя является нормой, что тоже связано с индивидуальными особенностями гормонального фона и циклом.
А вот «много» слизи в мазке – может свидетельствовать о том, что мазок взят в середине цикла, дисбиотических изменениях или избытке эстрогенов. Поэтому требует внимания специалиста или, как минимум, контроля в динамике.
Флора
Преобладающей флорой женских половых путей в норме у женщин репродуктивного возраста, как известно, являются лактобактерии (или палочки Дедерлейна). Количество которых может быть от умеренного до обильного, в том зависимости, в том числе, от фазы менструального цикла.
Патологические элементы
Присутствия мицелия грибов, трихомонад, диплококков (в том числе и возбудитель гонореи), лептотрикса, мобилункуса и прочих патогенных микроорганизмов в нормальном мазке не допускается, даже в минимальном количестве. А их выявление – серьезный повод незамедлительно обратиться за лечением.
Вагиниты, вызванные условно-патогенной микрофлорой: рекомендации для практикующих врачей
Сведения об авторе:
Пустотина Ольга Анатольевна, доктор медицинских наук, профессор кафедры акушерства, гинекологии и репродуктивной медицины ФПК МР РУДН Адрес: 117198 Москва, ул. Миклухо-Маклая д. 6, телефон 8 (495) 787-38-27, email: rudn@rudn.ru Pustotina Olga Anatolievna, Doctor of Medicine, Professor of The department of Obstetrics, Gynecology and Reproductive Health, Peoples’ Friendship University of Russia. Address: 117198 Moscow, Mikluho-Maklaya str, 6. Phone 8(495)7873827
Нормальная микрофлора женских половых органов
Таким образом, во влагалище здоровых женщин репродуктивного возраста общая численность бактерий составляет 105-106 КОЕ/мл выделений, 95% которых представлены лактобактериями и только 5% формируется представителями других видов аэробных и анаэробных УПМ.
Вагиниты, вызванные УПМ
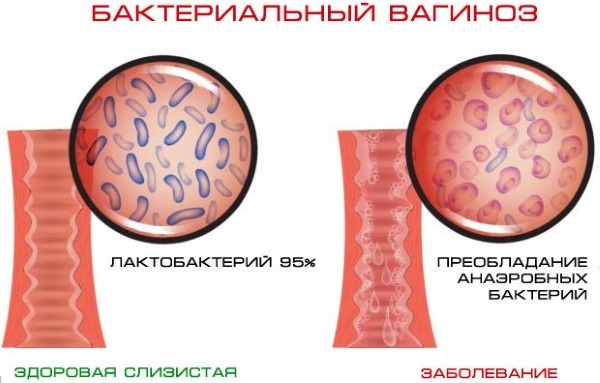
Вагиниты бывают воспалительного и невоспалительного характера. Воспалительные вагиниты в зависимости от вида возбудителя разделяют на неспецифические и специфические. К специфическим относятся трихомонадный, хламидийный, гонококковый и грибковый вагинит (вагинальный кандидоз), при обнаружении любых других УПМ вагинит является неспецифическим. Невоспалительный вагинит называется бактериальным вагинозом. Бактериальный ваги- ноз, неспецифический вагинит и вагинальный кандидоз объединяют вагиниты, вызванные УПМ.
Бактериальный вагиноз не относится к инфекциям, передаваемым половым путем (ИППП), но связан с сексуальной активностью женщины и может вызывать симптомы уретрита у мужчин. Происходящие во влагалищном биотопе изменения облегчают восходящее инфицирование ИППП: гонококками, хламидиями, трихо- монадами, ВИЧ-инфекцией и др. Кроме того, накапливаясь в большом количестве, УПМ проникают в полость матки, вызывая хроническую воспалительную реакцию, приводя к бесплодию, невынашиванию беременности и снижению эффективности программ ЭКО [7, 8].
Вагинальный кандидоз-это воспаление слизистой оболочки влагалища, вызванное дрожжевыми грибами рода СапсНс1а, которое встречается у 5-10% женщин репродуктивного периода. Развитие кандидоза в основном расценивают как вторичную эндогенную инфекцию, резервуаром которой является желудочно-кишечный тракт. Основными причинами, способствующими проникновению грибов из аногенитальной области во влагалище и их интенсивному размножению, является прием антибиотиков, глюкокортикоидов, потребление пищи с большим количеством углеводов. Предрасполагающими к заболеванию факторами служат ожирение, сахарный диабет и нарушение правил личной гигиены 10.
Факторы риска вагинитов, вызванных УПМ
Устойчивость экосистемы влагалища определяется факторами эндогенного и экзогенного происхождения. К развитию дисбиотических процессов в вагинальном микроценозе наиболее часто приводят: стресс, лечение антибиотиками, гормональная терапия, эндокринные и аллергические заболевания, снижение иммунной защиты организма, хронические запоры, инфекция мочевых путей. Уменьшение доли лактобацилл и повышение рН в содержимом влагалища происходит при повреждениях эпителиального покрова в результате полового акта, трещин, расчесов, при чрезмерной гигиене наружных половых органов. Нередко женщины при появлении неприятного запаха из половых путей прибегают к спринцеванию. Спринцевание не имеет ни гигиенического, ни профилактического, ни лечебного эффекта, а усугубляет дис- биоз и является фактором риска воспалительных заболеваний органов малого таза. Нарушение экосистемы влагалища может возникать после полового акта вследствие действия спермы с высоким уровнем рН, при частой смене половых партнеров, во время аногенитальных контактов, при использовании некоторых спермицидов. Длительное маточное кровотечение, инородные тела во влагалище (тампоны, пессарии, швы при истмико-цервикальной недостаточности) нередко также сопровождаются патологическими выделениями из половых путей [4, 6, 7, 9].
Клиника и диагностика вагинитов, вызванных УПМ
В основе вагинитов, вызванных УПМ, лежит уменьшение колоний лактобактерий, в результате которого изменяется рН вагинальной среды с кислой на щелочную и создаются условия для разрастания УПМ и их адгезии на освобождающийся эпителий слизистой оболочки влагалища.
Все происходящие изменения вагинального биотопа объединяются диагностическими критериями Амселя: появление специфических белей из половых путей, увеличение рН вагинального отделяемого, «рыбный» запах и наличие «ключевых клеток», представляющих собой эпителиальные клетки, порытые сплошным слоем различных микроорганизмов. По последним данным, даже наличие двух критериев из четырех позволяет установить нарушение вагинального микробиоценоза [5].
Кроме того, возбудители ИППП, такие как хламидии, трихомонады, гонококк и Мусор1а5та депйаПит, также могут колонизировать генитальный тракт, не нарушая нормальный рост лактобактерий и не изменяя рН влагалищного содержимого, в следствие чего до 90% случаев инфицирования ИППП протекают бессимптомно. Поэтому международные и отечественные эксперты 15 рекомендуют дополнительно к микроскопическому исследованию, обладающему низкими диагностическими возможностями в отношении облигатных патогенов, использовать метод полимеразной цепной реакции (ПЦР) для выявления антигенов хламидий, трихо- монад, гонококка и Мусор1а5та депИаИит в отделяемом половых путей.
Таким образом, окончательный диагноз вагинитов, вызванных УПМ, устанавливается при наличии у женщины жалоб на патологические вагинальных выделения и данных микроскопического исследования, и только после исключения ИППП методом ПЦР.
Лечение вагинитов, вызванных УПМ
Первый этап: Противомикробная терапия.
Препаратами выбора для лечения бактериального вагиноза являются производные нитроимидазола и линкозамиды, которые наиболее активно подавляют размножение анаэробной микрофлоры:
Исследования показали, что ни у одной из схем нет преимуществ в эффективности терапии [7], однако при местном использовании значительно реже возникают побочные эффекты [16].
Для лечения неспецифического вагинита рекомендуется использовать клин- дамицин (300 мг 2 р/сут 7 дней, вагинальный крем 2% 5г 7 дней, свечи 100 мг вагинально 3 дня). В сравнении с производными нитроимидазола (метронидазол, тинидазол, орнидазол), он имеет более широкий спектр действия, включающий не только анаэробные, но и аэробные грамположительные и грамотрицательные бактерии [3, 12, 13, 17, 18].
В последние годы опубликованы результаты крупных рандомизированных контролируемых исследований, показавших высокую эффективность лечения нарушений вагинального микробиоценоза еще двумя антибиотиками широкого спектра действия: рифаксимина (250 мг вагинально 5 сут) [19] и нифуратела (250 мг вагинально 10 сут) [20].
Следует отметить, что все выше представленные антибактериальные средства, обладая выраженной подавляющей активностью в отношении УПМ, не влияют на жизнедеятельность полезных молочно-кислых бактерий [15, 19, 20].
Терапия вагинального кандидоза проводится антимикотиками, среди которых препаратами первой линии являются азолы для интравагинального применения (имидазолы):
и азолы для приема внутрь (триазолы):
При остром неосложненном вагинальном кандидозе, вызванном СапсМс1а а1Ысап5, все препараты местного и системного действия одинаково эффективны.
В случаях рецидивирования процесса длительность и количество курсов увеличивается, при этом необходимо идентифицировать вид кандидозной инфекции и исключить возможные факторы риска [10,12-14].
Антисептики:
В настоящее время получено множество доказательств эффективности терапии вагинитов, вызванных УПМ, различными антисептическими средствами, такими как:
Все антисептики обладают широким неспецифическим спектром действия и подавляют рост аэробных и анаэробных микроорганизмов, а также грибов рода СапсМс1а, при этом не влияя на жизнедеятельность колонии лактобактерий [15].
Наибольшая доказательная база (уровень доказательности 1А) продемонстрирована для деквалиния хлорида (флуомизина). В крупномасштабных многоцентровых рандомизированных зарубежных [21 ] и отечественных исследованиях (БИОС-1/М) [18, 22, 24] с участием 321 и 640 пациенток, соответственно, деквалиния хлорид показал сопоставимую эффективность с действием клиндамицина при лечении вагинитов, вызванный УПМ, при значительно лучшей переносимости и меньшей частоте развития кандидоза. Кроме того, вагинальные таблетки деквалиния хлорида обладают хорошей всасываемостью и меньшей текучестью в сравнении с хлоргексидином, поэтому назначаются один раз в сутки, не вызывая аллергических и других побочных эффектов, характерных для повидон-йода, при этом более эффективно уменьшая количество «ключевых клеток» и ПЯЛ в вагинальном мазке [18, 22].
Второй этап: восстановление микробиоценоза
Одной из причин хронизации процесса являются бактериальные пленки, формирующие невосприимчивость микроорганизмов к действию антибактериальных и антисептических средств [23]. В результате уровень излеченности через 3 мес составляет 60-70% и еще ниже через 6 мес [6]. Значительное повышение эффективности терапии вагинитов происходит после проведения второго этапа, направленного на восстановление нормального микробиоценоза [22, 23, 25].
Наилучшие результаты продемонстрировало применение пробиотиков, содержащих живые лактобактерии. Они не только подавляют рост УПМ, ассоциированных с бактериальным вагинозом и неспецифическим вагинитом, за счет образования молочной кислоты, перекиси водорода и бактериоцинов, но и способны разрушать образованные ими биопленки, а также модулируют иммунный ответ и способствуют размножению колоний эндогенных лактобактерий [4, 12, 19, 24, 26, 27].
В качестве дополнительного фактора, улучшающего состояние вагинального микробиоценоза после антимикробной терапии, является применение вагинальных таблеток аскорбиновой кислоты. [28]. В то же время, применение исключительно пробиотиков и/или закисления вагинальной среды без предшествующей антимикробной терапии для лечения вагинитов, вызванных УПМ, недостаточно [7].
Лечение вагинитов, вызванных УПМ, у беременных
Нарушение вагинального микробиоценоза у беременных достоверно сопряжено с повышенным риском преждевременных родов, восходящего инфицирования плода и послеродовых гнойно-септических осложнений [1,8, 29-31 ].
Согласно зарубежным рекомендациям [12, 13] терапия бактериального вагино- за и неспецифического вагинита у беременных женщин не отличается от таковой у небеременных. Препаратом первой линии считается метронидазол для системного и местного применения. При осложненном течении беременности и высоком риске преждевременных родов более эффективным считается назначение клиндамицина, обладающего более широким спектром активности 35. При этом терапию нарушений биоценоза влагалища необходимо проводить с самых ранних сроков беременности [36].
В отечественных рекомендациях [14] антибиотики из группы нитроимидазола и линкозамидов противопоказаны в первом триместре, их применение возможно только местно после 12 нед беременности. Поэтому препаратами выбора для беременных являются вагинальные антисептики широкого спектра действия. Среди антисептических средств только у деквалиния хлорида безопасность применения на любом сроке беременности и в период грудного вскармливания подтверждена в масштабных многоцентровых исследованиях [18, 21, 22, 24]. Беременным с вагинальным кандидозом показано местное применение азолов (клотримазол, миконазол, терканозол и др.) 13. В случаях неэффективности терапии предусмотрено интравагинальное назначение полиенов (натамицин, нистатин) 13. В дальнейшем для профилактики рецидивов вагинальных выделений беременным назначаются пробиотики и средства, подкисляющие вагинальную среду [28, 36].
В заключение хочется отметить, что вагинальный микробиоценоз напрямую связан с состоянием здоровья женщины. Любые нарушения гомеостаза могут сопровождаться патологическими выделениями из половых путей, которые нередко бывают кратковременными, и после нормализации общего состояния самостоятельно проходят. В случаях рецидивирования процесса основной задачей врача является не поиск и идентификация возможных возбудителей, которых при вагинитах, вызванных УПМ, как правило множество, а выяснение причин, приведших к длительному течению заболевания. Для постановки правильного диагноза достаточно простой микроскопии вагинального мазка и метода ПЦР для исключения строгих патогенов. При рецидивирующих патологических вагинальных выделениях необходим также тщательный сбор анамнеза для выявления всех возможных факторов риска, только после устранения которых достигается полноценное восстановление вагинального микробиоценоза.
Список использованной литературы
1. Гуртовой Б.Л., Кулаков В.И., Воропаева С.Д. Применение антибиотиков в акушерстве и гинекологии. – М.: Триада-Х, 2004. – 176с.
2. Sweet RL, Gibbs RS. Infectious diseases of the female genital tract. – 5th ed. Lippincott Williams Wilkins, 2009. 469p.
4. Радзинский В.Е. Бактериальный вагиноз. В кн. Шейка матки, влагалище, вульва. Физиология, патология, кольпоскопия, эстетическая коррекция: руководство для практикующих врачей / Под ред. С.И. Роговской, Е.В. Липовой. – М.: Издат журнала StatusPraesens, 2014. – С.249-280.
5. Mittal V, Jain A, Pradeep Y. Development of modified diagnostic criteria for bacterial vaginosis at peripheral health centres in developing countries/ J Infect Dev Ctries. 2012; 6(5): 373-377.
6. Verstraelen H, Verhelst R. Bacterial vaginosis: an update on diagnosis and treatment/ Expert Rev Anti Infect Ther. 2009;7:1109–1124.
7. Donders GG, Zodzika J, Rezeberga D. Treatment of bacterial vaginosis: what we have and what we miss/ Expert Opin Pharmacother. 2014;15(5): 645-657.
8. Leitich H, Bodner-Adler B, Brunbauer M. et al. Bacterial vaginosis as a risk factor for preterm delivery: a meta-analysis/ Am J Obstet Gynecol. 2003;189: 139–147.
9. Filler SG. Insights from human studies into the host defense against candidiasis/ Cytokine. 2012; 58(1): 129-132.
10. Байрамова Г.Р. Рецидивирующий вульвовагинальный кандидоз: автореф. дис. докт.мед.наук.– М., 2013.
11. Роговская С.И., Липова Е.В., Яковлева А.Б. Вульвовагинальные микозы. В кн. Шейка матки, влагалище, вульва. Физиология, патология, кольпоскопия, эстетическая коррекция: руководство для практикующих врачей / Под ред. С.И. Роговской, Е.В. Липовой. – М.: Изд-во журнала StatusPraesens, 2014. – С.281-308.
12. CDC. Sexually Transmitted Diseases Treatment Guidelines 2010. http://www.cdc.gov/std/treatment/2010/pid.htm
13. Sherrard J, Donders G, White D. European (IUSTI/WHO) Guideline on the management of vaginal discharge in women reproductive age. 2011.
14. Клинические рекомендации РОАГ. Акушерство и гинекология. – 4-е изд./ под ред. В.Н. Серова, Г.Т. Сухих. – М.: ГЭОТАР-Медиа, 2014. – 1024с.
15. Профилактика, диагностика и лечение инфекций, передаваемых половым путем: рук-во для дерматовенерологов, акушеров-гинекологов, урологов и семейных врачей. – М.:Институт здоровья семьи, 2008.
16. Mikamo H, Kawazoe K, Izumi K, et al. Comparative study on vaginal or oral treatment of bacterial vaginosis / Chemotherapy. 1997; 43:60-68.
17. Практическое руководство по антиинфекционной химиотерапии// Под ред. Л.С. Страчунского, Ю.А. Белоусова, С.Н. Козлова. – М., 2007. – 462с.
18. Подзолкова Н.М., Никитина Т.И. Сравнительная оценка различных схем лечения больных с бактериальным вагинозом и неспецифическим вульвовагинитом // Рос вестник акуш гинекол, 2012.- №4. – С.75-81.
19. Donders GG, Guaschino S, Peters K, et al. A multicenter, double-blind, randomized, placebocontroled study of rifaximin for the treatment of bacterial vaginosis/ Int J Gynaecol Obstet. 2013; 120:131-136.
21. Weissenbacher ER, Donders G, Unzeitig V. et al. Fluomizin Study Group. A comparison of dequalinium chloride vaginal tablets (Fluomizin®) and clindamycin vaginal cream in the treatment of bacterial vaginosis: a single-blind, randomized clinical trial of efficacy and safety. Gynecol Obstet Invest.
2012; 73: 8–15.
23. Swidsinski A, Verstraelen H, Loening-Baucke V. et al. Presence of a polymicrobial endometrial biofilm in patients with bacterial vaginosis/ PLoS One. 2013;8:e53997.
25. McMillan A, et al. Disruption of urogenital biofilms by lactobacilli / Colloids Surf B Biointerfase,2011; 86(1): 58-64.
26. Larsson PG, Stray-Pedersen B, Ryttig KR, Larsen S. Human lactobacilli as supplementation of clindamycin to patients with bacterial vaginosis reduce the recurrence rate; a 6-month, double-blind, randomized, placebo-controlled study./ BMC Women Health, 2008;15(8):3.
27. Ya W, Reifer C, Miller L E. Efficacy of vaginal probiotic capsules for recurrent bacterial vaginosis: a double blind, randomized, placebo-controlled study. Am J Obstet Gynecol. 2010; 203:1200–1208.
28. Zodzika J, Rezerberga D, Donders G. et al. Impact of vaginal ascorbic acid on abnormal vaginal microflora / Arch Gynecol Obstet 2013; 288: 1039-1044.
29. Bothuyne-Queste E, et al. Is the bacterial vaginosis risk factor of prematurity? Study of a cohort of 1336 patients in the hospital of Arras/ J Gynecol Obstet Biol Reprod. 2012; 41(3): 262-270.
30. Pustotina OA, Bubnova NI, Yezhova LS. Pathogenesis of hydramnios and oligohydramnios in placental infection and neonatal prognosis /J mat-fetal&neonat med. 2008; 21(1): 267-271.
31. Pustotina OA. Urogenital infection in pregnant women: clinical signs and outcome /J Perinat Med, 2013; 41:135.
32. Simcox R, Sin WT, Seed PT, et al. Prophylactic antibiotics for the prevention of preterm birth in women at rick: a meta-analysis/ Aust N-Z J Obstet Gynaecol. 2007; 47: 368-377.
33. McDonald HM, Brocklehurst P, Gordon A. Antibiotics for treating bacterial vaginosis in pregnancy/Cochr Database Syst Rev. 2007. N1.P.CD000262.
34. Lamont RF, Duncan SLB, Mandal D, et al. Intravaginal clindamycin to reduce preterm birth in women with abnormal genital tract flora/ Obstet Gynecol. 2003;101:516–522.