Подострый
Смотреть что такое «Подострый» в других словарях:
подострый — под острый (мед.) … Русский орфографический словарь
ПОДОСТРЫЙ — (subacute) данный термин применяется для описания заболевания, которое прогрессирует быстрее, чем хроническое, но не переходит в острую форму … Толковый словарь по медицине
Подострый лимфоцитарный тиреоидит — МКБ 10 E06.106.1 МКБ 9 245.1245.1 DiseasesDB … Википедия
Подострый тиреоидит — МКБ 10 E06.106.1 МКБ 9 245.1245.1 DiseasesDB … Википедия
Подострый склерозирующий панэнцефалит — (ПСПЭ) протекает по типу медленной инфекции. Вызывается вирусом кори или близким к нему вирусом. (Источник: «Словарь терминов микробиологии») … Словарь микробиологии
Подострый делирий — Смотри синоним: Состояние спутанности сознания подострое. Краткий толковый психолого психиатрический словарь. Под ред. igisheva. 2008 … Большая психологическая энциклопедия
Подострый психоорганический синдром — Смотри синоним: Состояние спутанности сознания подострое. Краткий толковый психолого психиатрический словарь. Под ред. igisheva. 2008 … Большая психологическая энциклопедия
подострый склерозирующий панэнцефалит — — [Англо русский глоссарий основных терминов по вакцинологии и иммунизации. Всемирная организация здравоохранения, 2009 г.] Тематики вакцинология, иммунизация EN subacute sclerosing panencephalitis … Справочник технического переводчика
Подострый (Subacute) — данный термин применяется для описания заболевания, которое прогрессирует быстрее, чем хроническое, но не переходит в острую форму. Источник: Медицинский словарь … Медицинские термины
ТИРЕОИДИТ ПОДОСТРЫЙ — мед. Подострый тиреоидит длительно протекающий тиреоидит, характеризующийся десквамацией и дегенерацией тироцитов, замещающихся клетками соединительной ткани, наличием гигантских многоядерных клеток и гранулём, а также увеличением содержания в… … Справочник по болезням
Подострая стадия что это
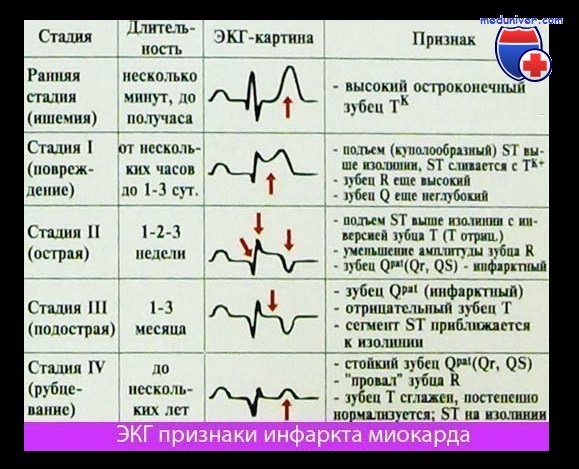
Третья (подострая) стадия отражает изменения на ЭКГ, связанные с наличием зоны некроза, в которой происходят в это время процессы рассасывания, пролиферации, репарации и организации, и с наличием «зоны ишемии», изменения в которой обусловлены в незначительной степени недостаточностью кровоснабжения миокарда и главным образом воспалительной реакцией вследствие контакта с рассасывающимся очагом некроза. Зоны повреждения на этом этапе развития инфаркта обычно уже нет. На ЭКГ в отведениях с положительным электродом над инфарктом отмечается увеличенный зубец Q и отрицательный симметричный зубец Т.
Длительность подострой стадии колеблется от 1 до 2 мес в зависимости от величины инфаркта и течения болезни. На протяжении этого периода на ЭКГ постепенно уменьшается глубина зубца Т в связи с уменьшением «зоны ишемии».
Четвертая стадия — стадия зубца, образовавшегося на месте инфаркта. На ЭКГ имеются изменения только комплекса QRS. Главным из них является увеличенный зубец О, что обусловлено уменьшением электродвижущей силы данной области вследствие замещения миокарда электрически неактивной рубцовой тканью. Кроме того, на ЭКГ отмечаются сниженный или расщепленный зубец R в отведениях над рубцом и высокий зубец Р в противоположных позициях. Сегмент S—Т на изолинии, а зубец Т, как правило, отрицательный. Иногда зубец Т положительный.
Увеличенный зубец Q обычно определяется на ЭКГ в течение многих лет, часто всю жизнь. Однако он может и уменьшиться. Иногда зубец Q довольно быстро (в течение нескольких месяцев) или постепенно (на протяжении нескольких лет) уменьшается до нормальных размеров. В этих случаях на ЭКГ не отмечается никаких признаков перенесенного инфаркта миокарда.
Такую возможность следует иметь в виду, чтобы не ошибиться в сложных случаях. Обычно полное исчезновение электрокардиографических признаков инфаркта наблюдается при относительно небольшом рубце или при расположении его в областях, малодоступных обычным отведениям ЭКГ. Причина такого постепенного уменьшения патологического зубца Q на ЭКГ в динамике, возможно, связана с компенсаторной гипертрофией мышечных волокон внутри рубца или циркулярно по периферии рубца.
Приведенная динамика ЭКГ по стадиям развития инфаркта миокарда имеет практическое значение, так как позволяет правильно определить время возникновения инфаркта и провести в каждом случае сопоставление динамики течения болезни и ЭКГ.
В зависимости от преимущественного поражения той или иной области сердца различают следующие основные локализации инфаркта миокарда:
I. Инфаркты передней стенки левого желудочка:
а) распространенный инфаркт передней стенки левого желудочка с вовлечением передней части межжелудочковой перегородки и боковой стенки (распространенный передний инфаркт);
б) инфаркт передней стенки, прилежащих участков боковой стенки и верхушки левого желудочка (переднебокоЕой инфаркт);
в) инфаркт передней части межжелудочковой перегородки;
д) инфаркт верхних отделов передней стенки (высокий передний инфаркт);
е) распространенный инфаркт верхних отделов передней и боковой стенок левого желудочка (высокий переднебоковой инфаркт).
II. Инфаркты задней стенки левого желудочка:
а) инфаркт нижнеправых отделов задней стенки левого желудочка, обычно с вовлечением задней межжелудочковой перегородки (заднедиафрагмальный инфаркт);
б) инфаркт нкжнелевых отделов задней стенки и боковой стенки левого желудочка (заднебоковой инфаркт);
в) инфаркт верхних отделов задней стенки левого желудочка (заднебазальный инфаркт).
III. Глубокий инфаркт межжелудочковой перегородки и прилегающих отделов передней и задней стенок желудочка (глубокий перегородочный инфаркт).
IV. Инфаркты боковой стенки левого желудочка:
а) обширный инфаркт преимущественно нижних отделов боковой стенки левого желудочка (боковой инфаркт);
б) инфаркт, ограниченный верхними отделами боковой стенки левого желудочка (высокий боковой инфаркт).
V. Субэндокардиальный мелкоочаговый инфаркт левого желудочка (одной из локализаций, указанных в п. I, II, III, IV).
VI. Интрамуральный мелкоочаговый инфаркт левого желудочка (одной из локализаций, указанных в п. I, II, III, IV).
VII. Инфаркт правого желудочка.
VIII. Инфаркт предсердий.
Подострый тиреоидит (E06.1)
Версия: Справочник заболеваний MedElement
Общая информация
Краткое описание
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
Этиология и патогенез
Эпидемиология
Факторы и группы риска
— женщины в возрасте 30-50 лет, переболевшие вирусной инфекцией;
— носители гена HLA-BW 35 (восприимчивые к вирусным заболеваниям).
Клиническая картина
Cимптомы, течение
При развитии заболевания характерна смена фаз функционального состояния ЩЖ.
1. Тиреотоксическая стадия продолжается до 1-1.5 мес (как правило, легкой или средней степени тяжести), обусловдена выбросом в кровь большого количества гормонов ЩЖ (Т3 и Т4) из разрушенных фолликулов, вызывая развитие тиреотоксикоза. Клинически характеризуется появлением тахикардии, увеличением пульсового давления, повышением температуры тела, похуданием, раздражительностью, плаксивостью.
ЩЖ увеличена, резко болезненна при пальпации, в отдельных участках уплотнена, не спаяна с окружающими тканями, подвижна, кожа над железой гиперемирована. Подчелюстные и шейные лимфатические узлы не увеличены.
2. Эутиреоидная стадия характеризуется снижением уровня тиреоидных гормонов до нормы, вследствие нарушения их синтеза и истощения запасов Т3 и Т4 в ЩЖ.
Диагностика
Диагноз подострого тиреоидита устанавливается на основании следующих данных:
1. Анамнез : повышение температуры тела до 38-39 градусов С через 5-6 недель после перенесенной вирусной инфекции, отчетливая сезонность в течение заболевания (осень-зима).
Лабораторная диагностика
Дифференциальный диагноз
— острый гнойный тиреоидит;
— кровоизлияние в кисту ЩЖ;
— диффузный токсический зоб (ДТЗ) легкой и средней степени тяжести;
— аутоиммунный тиреоидит, гипертиреоидная фаза;
— недифференцированный рак ЩЖ;
— флегмона шеи;
— средний отит;
— острый фарингит;
— синдром височно-нижнечелюстного сустава;
— эзофагит;
— десневой или парадонтальный абсцесс.
Осложнения
Лечение
Цели лечения:
— купировать болевой синдром;
— купировать воспалительную реакцию (нормализация температуры тела и показателей ОАК);
— восстановить функциональное состояние ЩЖ.
2. Глюкокортикоиды (ГКС) рекомендовано применять в большинстве случаев: преднизолон 30-40 мг внутрь после еды 1 раз/сут., до ликвидации клинических проявлений (1-3 нед.), с последующим уменьшением дозы на 5 мг в неделю. Общая продолжительность лечения составляет 2-3 мес. При быстром снижении ГКС болевой синдром усиливается.
3. Для устранения симптомов тиреотоксикоза назначают бета-адреноблокаторы: пропроналол 20-40мг 3-4 р./сут., до ликвидации клинических проявлений.
В случае развития первичного гипотиреоза при многократных тяжелых рецидивах назначается заместительная гормонотерапия левотироксином натрия (дозы подбираются индивидуально).
Антитиреоидные препараты не показаны.
В случае отсутствия лечения следует отметить, что подострый тиреоидит длится до 4-6 месяцев.
Инфаркт миокарда
Основные причины инфаркта миокарда
Основной причиной инфаркта миокарда принято считать сужение просвета коронарных артерий, вызванное атеросклеротическими изменениями. Повышенная свёртываемость крови ведёт к образованию тромбов, нарушающих процессы кровообращения в области сердечной мышцы. Ткани жизненно важного органа страдают от недостатка питательных веществ. Спровоцировать инфаркт миокарда могут сильное эмоциональное и физическое перенапряжение, наличие ишемической болезни сердца или стенокардии, а также сахарный диабет, ожирение, пристрастие к алкогольным напиткам и курению.
Стадии заболевания и основные признаки инфаркта миокарда
В своём развитии инфаркт миокарда проходит несколько стадий. Длительность и выраженность каждой зависит от размеров очага поражения, состояния сосудов, сопутствующих заболеваний и осложнений, а также правильности выбранной тактики лечения. Выделяют острый, подострый период, периоды рубцевания и постинфарктный период. Многие пациенты отмечали, что острому периоду предшествовали некоторые признаки нестабильной работы сердца – стенокардия, аритмия.
Острый период может длиться до 10 суток. Это самое сложное для пациента время, когда возникают всевозможные осложнения и вероятность смертельного исхода довольно велика. Характерная клиническая картина острого периода инфаркта миокарда – сильные боли в области грудной клетки с иррадиацией в левое плечо, ключицу, шею, ухо, лопатки. Ощущения спазма могут быть разными – режущими, колющими, давящими, жгущими. Такое состояние при инфаркте миокарда продолжается от тридцати минут до нескольких часов. Приступ при инфаркте миокарда протекает волнообразно. Боли могут усиливаться или ослабевать. Купировать их нитроглицерином невозможно. Одновременно при инфаркте миокарда пациент испытывает сильную слабость, чувство нехватки воздуха, беспокойство. Отмечаются также бледность кожи, синюшность (акроцианоз) носогубного треугольника, аритмия, обильный липкий пот. Возможно повышение артериального давления.
Подострый период инфаркта миокарда характеризуется исчезновением болевых ощущений. Их сохранение свидетельствует о присоединении перикардита (воспаление наружной оболочки сердца). Некротические процессы в зоне воспаления могут вызывать лихорадку с подъёмом температуры тела. Пациента беспокоит стойкое пониженное давление.
Период рубцевания при инфаркте миокарда характеризуется постепенным заживлением поражённого участка посредством образования рубцов. Длительность процесса составляет от нескольких недель до нескольких месяцев. Состояние больного значительно улучшается. Болевые симптомы исчезают.
Постинфарктный период – время восстановления и возвращения к обычному образу жизни. При этом рекомендуется избегать самостоятельного перемещения тяжестей, отказаться от алкоголя и курения, соблюдать диету, следить за массой тела, контролировать пульс и давление, избегать долгого пребывания на солнце.
Важно знать, что встречаются атипичные формы инфаркта миокарда, при которых признаки угрожающего жизни состояния не всегда очевидны. Они затрудняют диагностику и своевременное оказание медицинской помощи. Среди наиболее распространённых:
Записаться на обследование при инфаркте миокарда
Осложнения инфаркта миокарда
В первые часы инфаркта миокарда могут возникнуть различные осложнения, которые утяжеляют состояние пациента. Это появление аневризмы аорты, разрыв миокарда, кардиогенный шок, прекращение сердечной деятельности (асистолия), отёк лёгких. Последствия инфаркта могут сопровождать больного пожизненно. Это сбои сердечного ритма, кардиосклероз и другие проблемы, связанные с нарушением работы сердечно-сосудистой системы. Специалисты не гарантируют абсолютного выздоровления после перенесённого инфаркта и рекомендуют соблюдать все предписания врача-кардиолога для того, чтобы избежать рецидива. Следующий приступ грозит появлением новой области некроза. Компенсировать такие последствия для сердца практически невозможно.
Диагностика и лечение инфаркта миокарда
Помимо клинической картины инфаркта миокарда и составления подробного анамнеза для подтверждения такого серьёзного диагноза используется ряд дополнительных исследований:
При подозрении на инфаркт необходимо вызвать бригаду скорой помощи для срочной госпитализации в кардиологическую реанимацию. Пациенту с инфарктом миокарда предписывается строгий постельный режим, покой и диетическое питание с исключением продуктов, возбуждающих нервную и сердечно-сосудистую системы. Терапия направлена на купирование болевого синдрома, устранение аритмий и сердечной недостаточности, восстановление нормального кровообращения и борьбу с образованием тромбов. Для этого применяются анальгетики, нейролептики, антиаритмические препараты, тромболитики. Список лекарств индивидуален для каждого пациента. Он соответствует обширности текущего заболевания, общему самочувствию больного и наличию сопутствующих осложнений. Помимо медикаментов, по особым указаниям, используются хирургические методы лечения – шунтирование, иссечение аневризмы аорты, имплантация водителей ритма (прибор, задающий правильный сердечный ритм).
Стоимость консультации при инфаркте миокарда?
Что делать при инфаркте миокарда до приезда скорой помощи?
До приезда врачей необходимо помочь больному:
Профилактика инфаркта миокарда
Несмотря на все усилия современной медицины, смертность от инфаркта продолжат оставаться довольно высокой. Чтобы снизить вероятность возникновения данной патологии, необходимо знать, как предотвратить недуг. Рекомендации специалистов:
Диссеминированное внутрисосудистое свёртывание крови (ДВС-синдром)
Диссеминированное внутрисосудистое свёртывание крови (ДВС-синдром) – это один из наиболее распространённых в интенсивной терапии и представляющих большую опасность для больных вид патологии гемостаза. ДВС-синдром в настоящее время является важной проблемой медицины, так как осложняет течение практически любого заболевания, может являться причиной их развития и нередко предопределяет прогноз заболевания. Данный синдром универсален и может протекать как молниеносно с развитием смертельного исхода, так и латентно. При ДВС-синдроме возможно свёртывание крови в сосудистом русле, так и регионарные и органные тромбозы.
ДВС-синдром является полиэтиологическим заболеванием и может развиваться при различных заболеваниях и патологических процессах, которые приведены в таблице 1.
Заболевания системы крови
Острый промиелоцитарный лейкоз
Хронический мегакориоцитарный лейкоз
Серповидноклеточная анемия (гемолитический криз)
Эмболия околоплодными водами
Конфликт матери и плода по АВО и резус-фактору
Заболевания сосудистой стенки и сосудов
Тромбоэмболия лёгочной артерии
Тромботическая тромбоцитопеническая пурпура
Шок (травматический, ожоговый, септический)
Массивные поражения тканей (краш-синдром, большие операции)
Синдром массивных трансфузий
Переливание несовместимой крови
Отравления и интоксикации (лекарственные, змеиные яды)
В основе патогенеза ДВС-синдрома лежит преобладание активирующих свёртывающую систему механизмов над антикоагулянтной системой.
Развитие тяжёлого ДВС-синдрома начинается в результате массивной и длительной активации свёртывающей системы в под воздействием внешнего фактора. В результате этого развивается состояние гиперкоагуляции, что приводит к повсеместному образованию мелких сгустков, которые оседают в микроциркуляторном русле.
Обязательным элементом ДВС-синдрома является агрегация тромбоцитов. В результате гиперкоагуляции тромбоциты склеиваются между собой. Постепенно количество тромбоцитов уменьшается, в связи с чем развивается тромбоцитопения потребления.
В патогенезе ДВС-синдрома центральное место занимают образование в сосудистом русле тромбина и истощение механизмов, препятствующих свёртыванию крови и агрегации тромбоцитов. В процессе развития ДВС-синдрома может происходить снижение уровня основного физиологического антикоагулянта – антитромбина III в плазме. В результате запущенного патологического процесса в крови накапливается огромное количество активированных факторов свёртывания, что приводит к истощению системы фибринолиза и образовавшиеся сгустки практически перестают лизиироваться. Развивается блокада микроциркуляции, приводящая к нарушению кровоснабжения почек, печени, лёгких, слизистых оболочек кишечника, что создаёт предпосылки к развитию полиорганной недостаточности (ПОН).
Основными типичными клиническими проявлениями ДВС-синдрома являются геморрагии и/или тромбозы и ПОН. ПОН развивается в результате тромбогеморрагических поражений органов, имеющих богатую микроциркуляторную сеть. К данным органам относятся лёгкие, почки, головной мозг, кожа, надпочечники и печень.
Первыми признаками поражения лёгких является одышка и падение артериальной оксигенации. Нарушение микроциркуляции под воздействием вазоактивных субстанций приводит к развитию острой дыхательной недостаточности с нарастающей одышкой, цианозом, ателектазами в лёгких и прогрессирующим отёком лёгких.
Отложение фибрина в сосудах почечных клубочков может привести к почечной недостаточности. В клинической картине наблюдается олигоурия, рефрактерная к диуретикам, микро-и макрогематурия, высокие показатели мочевины и креатинина сыворотки крови.
Нарушения микроциркуляции головного мозга приводит к энцефалопатии, нарушению психики, потери сознания. В случае тяжёлого течения ДВС-синдрома возможно кровоизлияние в головной мозг.
Для ДВС-синдрома характерно образование стрессовых, гипоксических эрозий и язв слизистой желудочно-кишечного тракта, осложняющихся диффузным кровотечением.
При ДВС-синдроме отмечается геморрагический синдром, который носит смешанный гемотомно-петехиальный характер. На коже спонтанно или при незначительных воздействиях появляются синяки. Течение геморрагического синдрома сопровождается носовыми, десневыми кровотечениями и кровотечениями из места инъекций.
Кровотечения, геморрагический синдром и внутрисосудистый гемолиз приводят к развитию анемического синдрома. Анемический синдром сопровождается снижением уровня гемоглобина, эритроцитов.
В результате нарушения микроциркуляции, наличия гематом и повышения проницаемости слизистой оболочки желудочно-кишечного тракта создаются благоприятные условия для развития генерализованной инфекции – сепсиса.
По клиническому течению ДВС-синдрома выделяют:
Острый ДВС-синдром характерен для акушерской патологии, сепсиса, массивного краш-синдрома, обширных ожогов, массивного распада опухолей, переливания несовместимой крови. Для острого ДВС-синдрома характерна диффузная кровоточивость из операционной раны, носовые, десневые, постинъекционные кровотечения.
Подострое течение ДВС-синдрома наблюдается при аутоиммунных заболеваниях, хронических инфекциях и при всех перечисленных выше патологических состояниях. Длительность подострого течения занимает от нескольких недель до месяцев.
Хронический ДВС-синдром может длительное время не проявляться клинически. Возникновение ДВС-синдрома связано с прогрессированием основного заболевания. Хронический ДВС-синдром встречается при терапевтической патологии, например при сердечной недостаточности, хроническом гломерулонефрите, септическом эндокардите.
Рецедивирующий ДВС-синдром проявляется необильными носовыми кровотечениями, синяками на коже в период обострения основного заболевания.
В настоящее время в течение ДВС-синдрома выделяют три стадии:
I стадия – гиперкоагуляции. Для стадии гиперкоагуляции характерно повышение агрегации тромбоцитов и тромбообразование. При остром течении ДВС-синдрома данная стадия кратковременна и быстро переходит в стадию гипокоагуляции.
II стадия – нормокоагуляция. В этой стадии наблюдается субкомпенсация гемостаза.
III стадия – гипокоагуляция, при которой развивается выраженная кровоточивость, являющаяся следствием истощения фибринолиза.
ДВС-синдром является вторичным проявлением патологического процесса. Поэтому главной задачей является устранение провоцирующего фактора или своевременное лечение основного заболевания.
Лечение ДВС-синдрома включает в себя:
Использование гепарина оправдано на любой стадии ДВС-синдрома. В стадии гиперкоагуляции ДВС-синдрома гепарин применяется в суточной дозе 500-800 ЕД/кг. Доза гепарина подбирается в соответствии с лабораторными показателями гемостаза. Считается, что исходное время свертывания по Ли-Уайту должно увеличиться в 2 раза. Определёнными преимуществами обладают препараты фракционированного гепарина (фраксипарин, клексан, фрагмин), которые можно вводить 1-2 раза в сутки без значительных колебаний времени свертывания. В стадии гипокоагуляции гепарин вводят вместе со свежезамороженной плазмой (СЗП). В данном случае доза гепарина составляет 2500-5000 ЕД. Введение гепарина перед СЗП повышает активность антитромбина-III (AT-III) по отношению к факторам Ха и IХа, обрывает процесс внутрисосудистого свёртывания и тем самым не даёт развиться коагулопатии потребления.
Заместительная терапия предназначена для восстановления гемостаза больного. К заместительной терапии относится переливание СЗП, которая содержит достаточную концентрацию необходимых компонентов гемостаза. На начальных этапах лечения ДВС-синдрома доза СЗП составляет 800-1600 мл/сут. В стадии гипокоагуляции доза СЗП увеличивается до 15-20 мл/кг/сут.
Эффективно применение криопреципитата, содержащего более высокие концентрации фибриногена, фактора Виллебранда, фибронектина и фактора ХIII. Криопреципитат показан при остром или молниеносном течении ДВС-синдрома.
Для восстановления объёма циркулирующей крови используются растворы кристаллоидов, альбумина и коллоидов. В I стадии применяется растворы гидроксиэтилкрахмала, что способствует улучшению микроциркуляции.
При снижении уровня гемоглобина ниже 70-80 г/л, гематокрита менее 25% показано переливание отмытых эритроцитов, а при их отсутствии — эритроцитной массы. Тромбоцитарный концентрат переливают при снижении уровня тромбоцитов до 50•109/л.
В стадии гипокоагуляции показано введение ингибиторов протеаз: контрикала или апротинина (трисалол). Контрикал в водят внутривенно в начальной дозе 350000 АтрЕ и затем в поддерживающей дозе 140000 АтрЕ каждые 4 ч до нормализации показателей гемостаза. Начальная доза трасилола составляет 500000 КИЕ и поддерживающая – 50000 КИЕ/ч.
Одним из компонентов терапии ДВС-синдрома является использование препаратов улучшающих микроциркуляцию и дезагрегантов.
Важным компонентом комплексной терапии ДВС-синдрома являются методы экстракорпоральной детоксикации. Методы экстракорпоральной детоксикации повышают эффективность лечения ДВС-синдрома и его осложнений, что позволяет снизить летальность.
Плазмаферез (ПФ) позволяет удалять продукты паракоагуляции, активаторы свёртывания, циркулирующие иммунные комплексы, крупномолекулярные соединения. ПФ необходимо проводить в максимально ранние сроки ДВС-синдрома. Для достижения клинического эффекта необходимо, чтобы объём удаляемой плазмы за один сеанс ПФ был не менее 50% объёма циркулирующей плазмы. Замещение должно производиться СЗП в объёме, равном объёму удаляемой плазмы.
Развитие ПОН и в частности острого повреждения почек является показанием для проведения заместительной почечной терапии (ЗПТ): гемодиализ, гемофильтрация, гемодиафильтрация. ЗПТ удаляет низко- и среднемолекулярные токсины, медиаторы воспаления, снижает объём жидкости, улучшает кислородтранспортную функцию крови.
Прогноз при ДВС-синдроме определяется степенью его выраженности, распространенностью и характером течения. Опыт современной медицины даёт основание говорить о возможности эффективного лечения больных с острыми вариантами ДВС-синдрома, однако летальность может составлять 50 %.