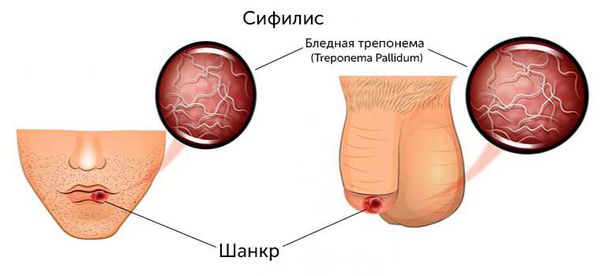
Как выглядит выпавшая кишка 4 27 1 689 1 192
Энтероптоз (K63.4)
Версия: Справочник заболеваний MedElement
Общая информация
Краткое описание
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
13-15 октября, Алматы, «Атакент»
600 брендов, более 150 компаний-участников из 20 стран.
Новинки рынка стоматологии. Цены от производителей
Классификация
Общий спланхноптоз:
Этиология и патогенез
Этиология энтероптоза неизвестна. В настоящее время рассматриваются 3 основных теории:
1. Энтероптоз является следствием гипотрофии.
2. Энтероптоз является следствием слабости соединительной и мышечной ткани.
3. Энтероптоз является вариантом нормы.
Патофизиология
Чаще всего энтероптоз поражает наиболее подвижные в анатомическом плане части кишечника, например, ободочную кишку. Опускающаяся ободочная кишка приобретает U-образную форму, что затрудняет пассаж пищи и газов.
В вертикальном положении пациента, при выраженном энтероптозе пассаж может почти прекратиться, что вызывает клинику частичной кишечной непроходимости.
Гистологически энтероптоз представлен признаками катарального воспаления и/или атрофии стенки кишечника (в зависимости от стадии). Инфильтрация подслизистой и атрофия слизистой вследствие хронического воспаления сочетаются с гибелью подавляющего большинства ганглиев и деструктивными изменениями межмышечных нервных сплетений.
Эпидемиология
Возраст: преимущественно взрослый
Признак распространенности: Крайне редко
Соотношение полов(м/ж): 0.3
Истинная распространенность энтероптоза неизвестна.
Заболевание может протекать без клинической симптоматики или в субклинической форме, не требующей применения методов визуализации и, следовательно, не диагностируемой при жизни или диагностируемой случайно.
Пол. Большинство авторов сходятся во мнении о значительном преобладании лиц женского пола.
Факторы и группы риска
Клиническая картина
Клинические критерии диагностики
Cимптомы, течение
Чаще всего энтероптоз протекает бессимптомно.
Дополнительные (редкие) симптомы (симптомы так называемой «эндогенной интоксикации»):
Обычно наблюдается опущение тех или иных отделов толстой кишки с различной клинической картиной:
1. Опущение слепой кишки наблюдается редко (15% от всех случаев энтероптоза). Сопровождается запорами, периодическим вздутием живота и ощущением полноты в правой подвздошной области. При чрезмерно подвижной слепой кишке в ней застаиваются фекальные массы, нередки приступы болей, напоминающие приступ аппендицита, иногда возникает кишечная непроходимость вследствие перегибов и перекручивания слепой кишки.
Диагностика
Диагностика энтероптоза основана почти исключительно на методах визуализации.
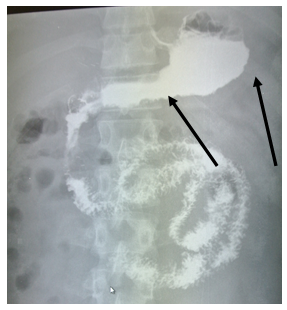
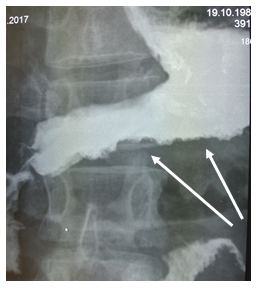
1. Обзорная рентгенография только в отдельных случаях может предположить диагноз энтероптоза, не разграничивая его признаки с кишечной непроходимостью.
3. Пассаж кишечника иногда определяют с помощью рентгеновского наблюдения за проглоченными маленькими металлическими кольцами (около 20 штук) или пассажем бария (энтерография).
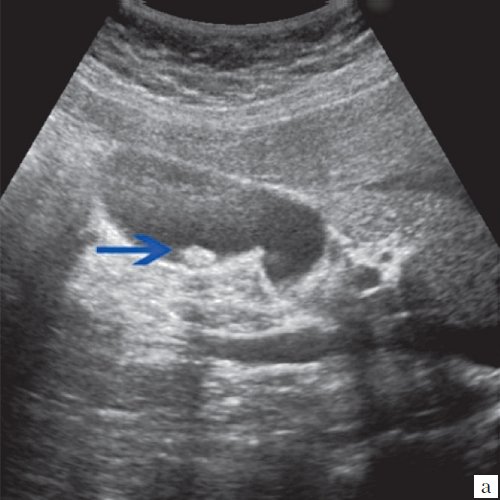
6. УЗИ органов брюшной полости является обязательным исследованием в плане ассоциированной патологии.
Лабораторная диагностика
Дифференциальный диагноз
Энтероптоз дифференцируется со всеми заболеваниями, имеющими хроническую боль в животе, задержку стула и газов, интоксикацию, замедление пассажа по кишечнику.
Основными различиями являются:
— отсутствие симптомов раздражения брюшины;
— отсутствие каловых масс в прямой кишке при ректальном исследовании;
— хронический характер патологии;
— изменение интенсивности симптомов при ношении бандажа и в положении лёжа;
— отсутствие в кале и других исследуемых субстанциях каких-либо изменений также говорит в пользу энтероптоза.
Окончательная дифференциальная диагностика проводится с учетом данных колоноскопии и радиологического обследования.
Осложнения
Вопрос об осложнениях энтероптоза претерпевал значительные изменения по мере накопления данных.
Лечение
Единого мнения нет. Лечение энтероптоза зависит от стадии развития и, соответственно, клинических проявлений.
В тактике лечения борются два подхода:
1. Обязательная «стартовая» консервативная терапия, которая включает в себя:
— диета (клетчатка, жидкость, дробное питание);
— ношение бандажа;
— слабительные и средства, смягчающие стул (в редких случаях, по показаниям);
— лечебная физкультура (избегая бега, поднятия тяжестей и любых упражнений, повышающих внутрибрюшное давление).
Оперативное вмешательство производят в основном при различных осложнениях. Как плановый этап лечения, оперативное вмешательство не рекомендуется.
Приведенный ниже перечень лекарств предназначен для проведения оперативного вмешательства или подготовки к нему или послеоперационного ведения.
Что такое выпадение прямой кишки? Причины возникновения, диагностику и методы лечения разберем в статье доктора Хитарьяна Александра Георгиевича, проктолога со стажем в 31 год.
Определение болезни. Причины заболевания
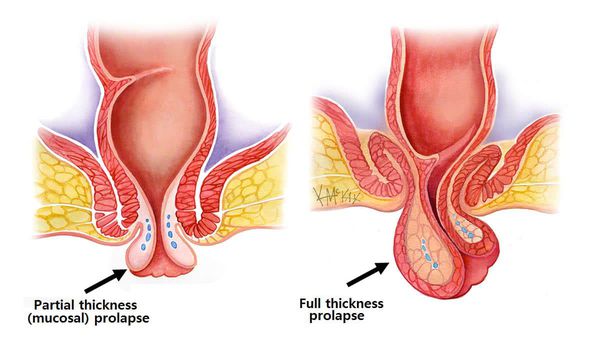
Ректальный пролапс — частичное или полное выпадение прямой кишки за пределы ануса. Выпадение может быть внутренним или в виде инвагинации прямой кишки, под которой понимают внедрение вышележащего участка кишечника в нижележащий, но не выходящее через анальное отверстие. В подавляющем большинстве случаев данное заболевание является полиэтиологичным, т. е. причин возникновения несколько, и их сочетание приводит к выпадению. [1] [2] [3]
Среди причин развития принято выделять неконтролируемые:
Часто заболевание связано и с наличием длительно существующих нарушений акта дефекации, травматических или иных приобретенных нарушений иннервации кишечника, заболеваний дыхательной системы, сопровождающихся кашлем в течение продолжительного времени, тяжелой физической активностью, [4] а также многоплодной беременностью и различными гинекологическими факторами.
Симптомы выпадения прямой кишки
Зачастую диагностирование данного заболевания не представляет сложностей, если речь идет о наружном ректальном пролапсе. При данном состоянии больные жалуются на чувство инородного тела и неполного опорожнения. Явным признаком является выпячивание кишки через задний проход. [5]
Также больные в некоторых случаях отмечают необходимость ручного вправления, после чего наступает облегчение. При внутренней инвагинации больные, как правило, предъявляют жалобы на затрудненную дефекацию, боли, выделение слизи и крови, необходимость введения пальцев через анальное отверстие. [6] [7] [8]
Патогенез выпадения прямой кишки
Вышеуказанные причины приводят к ослаблению мышечно-связочного аппарата прямой кишки, а также мышц тазового дна и промежности и вместе с повышением внутрибрюшного давления приводят к перемещению слоев кишечной стенки друг относительно друга, вызывая наружное или внутреннее выпадение.
Классификация и стадии развития выпадения прямой кишки
В ГНЦК создана классификация выпадения прямой кишки, используемая большинством отечественных специалистов. [7] [8] В данную классификацию входит 3 стадии в зависимости от условий, которые привели к выпадению:
1-я стадия — во время опорожнения кишечника;
2-я стадия — при физической активности;
3-я стадия — выпадение при ходьбе.
Помимо стадий, данная классификация описывает степень компенсации мышечного аппарата тазового дна:
Кроме того, данная классификация описывает степень недостаточности анального сфинктера:
1-я степень — невозможность удерживать кишечные газы;
2-я степень — невозможность удерживать жидкую часть стула
3-я степень — невозможность удерживать любые каловые массы.
Иностранные специалисты придерживаются Оксфордской классификации, основанной на результатах рентгенологического исследования. В данной классификации выделяют:
1. высокая ректальная инвагинация;
2. низкая ректальная инвагинация;
3. высокая анальная инвагинация;
4. низкая анальная инвагинация;
5. выпадение прямой кишки. [9]
Осложнения выпадения прямой кишки
Самым опасным осложнением выпадения прямой кишки является ущемление выпавшего участка кишки. Как правило, при выпадении прямой кишки ущемление происходит при несвоевременном вправлении или при попытке грубого вправления. При ущемлении отмечается наличие нарастающей ишемии, развитие отека, в связи с чем вправить выпавший участок становится всё сложнее. При несвоевременном обращении за специализированной медицинской помощью может возникнуть некроз (омертвение) ущемленного участка.
Еще одним осложнением при частом выпадении прямой кишки является образование солитарных язв, которое связано с нарушением трофики кишечной стенки. Длительно существующие язвы могут приводить к кровотечениям, перфорациям и т. д.
Диагностика выпадения прямой кишки
Как правило, диагностика ректального пролапса не составляет особых трудностей. Если при ректальном осмотре видимого выпадения не выявляется, но при этом больной настаивает на выпадении, то его располагают в коленно-локтевую позу и просят натужиться. В некоторых случаях выпадение прямой кишки можно принять за выпадение геморроидальных узлов. Наличие концентрического характера складок будет говорить о выпадении прямой кишки, тогда как при выпадении геморроидальных узлов расположение складок будет радиальным.
«Золотым стандартом» в обследовании колопроктологических больных является рентгенологическая дефекография. [10] [11] Данное исследование проводят при помощи рентген-контрастного вещества, которым заполняется просвет прямой кишки. Результаты проведенного исследования оцениваются, исходя из положения контрастированной кишки от лонно-копчиковой линии в покое и при натуживании. Выполнение дефекографии также позволяет выявить у больных ректо-, сигмо- и цистоцеле.
При внутренней инвагинации важное значение имеет ректороманоскопия, выполнение которой позволяет выявить наличие избыточных складок слизистой и заполнение просвета ректоскопа кишечной стенкой. Ректороманоскопия также позволяет выявить язвенные дефекты слизистой, отличительными особенностями которых является гиперемия участка слизистой с белым налетом. Примерно у половины больных отмечается изъязвление язвы, у четверти — полиповидные разрастания. [12] [13] Немаловажным является выполнение видеоколоноскопии или ирригоскопии для выявления опухолей толстого кишечника.
Лечение выпадения прямой кишки
При ректальном пролапсе и тем более внутренней инвагинации одним из ведущих методов лечения является хирургический, однако на начальных стадиях курс лечения нужно начинать с консервативных мероприятий. Основными направлениями терапии является нормализация стула и пассажа кишечного содержимого. С этой целью первым этапом назначаются диета, богатая клетчаткой, а также обильное питье. Следующим этапом является назначение слабительных препаратов, увеличивающих объем калового содержимого, а также усиление перистальтики кишечника. Широкое распространение получили лекарственные препараты семян подорожника, например «Мукофальк». Последний назначают по 1 пакетику или 1 чайной ложке до 5-6 раз в сутки.
К консервативным методам лечения ректального пролапса относят и методы нейростимуляции. К таким методам относится БОС-терапия и тибиальная нейромодуляция. Данная терапия направлена на нормализацию иннервации. Метод биологической обратной связи основан на моделировании нормальных режимов работы мышц промежности и тазового дна. Методика представляет собой визуализацию сигналов от датчиков, расположенных в прямой кишке и на коже промежности. Данные выводятся на монитор или в виде аудиосигнала. Пациент, в зависимости от режима или запланированной программы, волевым усилием способен контролировать сокращения мышц. Регулярные процедуры позволяют получить положительный эффект у 70% больных с нарушением иннервации мышц тазового дна. Методика тибиальной нейромодуляции заключается в стимуляции тибиального нерва с целью укрепления мышц промежности и анального сфинктера. Два электрода устанавливаются на область медиальной лодыжки. Импульсы подаются с периодами расслабления и напряжения.
Консервативные методы утрачивают свою эффективность при дальнейшем развитии заболевания. В этих случаях необходимо прибегать к хирургическим методам коррекции. Все хирургические вмешательства в зависимости от доступа подразделяются на промежностные и трансабдоминальные, которые, в свою очередь, можно разделить на открытые и лапароскопические.
Несмотря на положительный эффект консервативных методов лечения, наиболее эффективным является применение хирургических методов коррекции ректального пролапса. [14] В настоящее время в мировой практике описано множество методик оперативного лечения выпадения прямой кишки. Все описанные методики возможно разделить в зависимости от применяемого доступа через промежность или через брюшную полость. Промежностные варианты лечения более предпочтительны для больных с имеющейся тяжелой сопутствующей патологией, поскольку такие операции менее травматичны. Наряду с меньшей травматичностью, стоит отметить высокую частоту рецидивов, а также послеоперационных осложнений.
Среди промежностных вмешательств выделяют такие операции, как:
Суть операции по Делорма заключается в том, что слизистый слой рассекают по всей окружности на два сантиметра проксимальнее гребешковой линии. Далее после препаровки от подлежащего слоя иссекается выпадающий участок. На мышечный слой накладываются швы в продольном направлении для создания валика, после чего ушивается слизистый слой. Преимущества данной операции в небольшой травматичности и достоверном повышении функции анального сфинктера, что ведет к улучшению функцию удержания компонентов кала. Однако, исходя из данных различных исследований, встречаемость рецидивов выше, чем при операциях через брюшную полость, а частота осложнений, таких как острая задержка мочи, послеоперационные кровотечения и нарушение пассажа кишечного содержимого, достигают 15%.
При ректосигмоидэктомии или операции Альтмайера необходимо рассечь слизистый слой прямой кишки по всей окружности на два сантиметра выше зубчатой линии как при операции Делорма. Следующим этапом является мобилизация сигмовидной и прямой кишки и лигирование сосудов до уровня отсутствия избыточной подвижности. Далее отсекают избыточную слизистую, после чего необходимо наложить аппаратный или ручной анастомоз. Положительной стороной данного оперативного вмешательства является низкий процент кровотечений из линии анастомоза, его несостоятельностей, а также малое число гнойных осложнений в клетчатке таза. Рецидив заболевания составляет до 30%, которые, по данным исследований, уменьшаются в 3-4 раза, если дополнить данную операцию пластикой мышц леваторов.
Операция по Лонго, называемая еще трансанальной проктопластикой, подразумевает применение циркулярных сшивающих аппаратов. При данной операции на слизистую по передней и задней ее поверхности накладываются полукисетные швы. Далее поочередно на головке сшивающего аппарата затягивают сначала передний полукисетный шов с иссечением избытка слизистой, затем затягивают швы по задней полуокружности на головке сшивающего аппарата и отсекают избыток слизистой аналогично передней полуокружности. Операция по Лонго также может быть выполнена через брюшную полость, что расширяет возможности данной операции, позволяя применять ее у более широкого круга пациентов, в том числе с сопутствующей патологией. Частота послеоперационных осложнений достигает 47%.
Несмотря на минимальную травматичность промежностных вмешательств, высокий процент рецидивов обуславливает их ограниченную применимость. В последние годы все больший процент оперативных вмешательств выполняется через брюшную полость, а большинство предложенных методик являются либо модификациями описанных операций, либо представляют лишь исторический интерес и в настоящий момент не используются.
Минимальный процент рецидивов и лучшие, в сравнении с промежностными операциями, функциональные результаты обуславливают более широкое внедрение трансабдоминальных вмешательств. Стоить отметить, что из-за высокого процента послеоперационных осложнений у данного вида операций ограничивается его применение к пациентам пожилого возраста с тяжелой сопутствующей патологией.
Из наиболее распространенных вмешательств стоит отметить:
При ректопексии прямая кишка фиксируется выше мыса крестца. Зачастую, первым этапом выполняют резекцию прямой кишки, при этом анастомоз располагают выше мыса крестца. Данный метод отличается относительно низким процентом рецидивов, достигающим 5%, тогда как послеоперационные осложнения встречаются примерно в 20%. Также некоторые исследования указывают на улучшение транзита по кишечнику.
Ряд авторов убеждены в необходимости субтотальной резекции кишечника, однако последние исследования указывают на отказ от расширенного объема у пациентов с анальной инконтиненцией, поскольку у больных происходит ухудшение функции анального сфинктера.
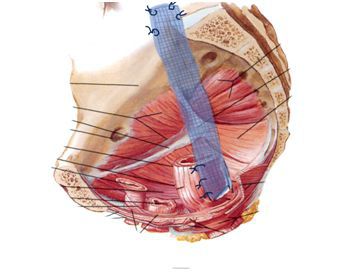
Ректопромонтофиксацию начинают с мобилизации прямой кишки справа от нее по задней и боковой полуокружности вплоть до латеральной связки. У женщин при наличии пролапса ректовагинальной перегородки последнюю рассекают и мобилизуют до анального сфинктера. У мужчин мобилизация проводится до границы средней и нижней трети ампулярного отдела прямой кишки по задней полуокружности. Далее к выделенной стенке кишки фиксируется сетчатый протез. При ректоцеле дополнительно фиксируется задний свод влагалища. Другой конец протеза фиксируют к промонториуму.
Схема ректопромонториофиксации
Обзор исследований с большим количеством пациентов выявил появление рецидивов в 3,5% случаев, тогда как послеоперационные осложнения встречались в 25%. Нарушения пассажа кишечного содержимого встречалось в среднем в 15% случаев.
Оперативный метод по Уэллсу заключается в рассечении брюшины над мысом крестца вплоть до тазовой брюшины и прямой кишки с обеих ее сторон. Далее выделяют кишку до мышц леваторов по задней и боковым полуокружностям, к которым фиксируют сетчатый протез. Другой конец протеза фиксируют к мысу крестца поперек оси последнего. Частота появления рецидивов после данного вида вмешательства достигает 6%, запоры встречаются у 20%, а признаки анальной инконтиненции встречаются примерно в 40% случаев.
Оперативный метод по Зеренину-Кюммелю заключается во вскрытии брюшины до Дугласового пространства спереди от прямой кишки, последнюю выделяют до леваторов. Далее от мыса и ниже накладывают швы, включая продольную связку, и продолжают линию швов на переднюю стенку прямой кишки. При затягивании швов происходит ротация на 180 градусов, производят ликвидацию глубокого кармана Дугласа. Рецидив, по данным литературы, встречается примерно у 10% больных.
Прогноз. Профилактика
При оперативном лечении ректального пролапса рецидивы наблюдаются в среднем примерно у 30% больных, при этом большая часть таких пациентов перенесли промежностные вмешательства. [15] Нарушения транзиторной функции толстого кишечника встречаются в среднем у трети пациентов. [16] Очень часто больные обращаются в довольно поздние сроки, когда выпадение прямой кишки является очевидным и имеются выраженные нарушения функции. Чем длительнее существует заболевание, тем более неблагоприятным является дальнейший прогноз. При этом увеличивается риск развития осложнений, угрожающих жизни, таких как толстокишечная непроходимость и некроз участка кишки.
С целью профилактики данного заболевания необходимо исключить описанные предрасполагающие факторы, которые возможно корригировать.
Стадии рака ободочной кишки
Ободочная кишка, состоящая из четырех отделов: восходящей, поперечной, нисходящей и сигмовидной кишки, занимает около 4/5 от длины толстой кишки. В любом из этих отделов может развиваться злокачественная опухоль.
Рак ободочной кишки обычно диагностируется в возрасте 50-75 лет, одинаково часто возникает как у мужчин, так и женщин. В половине случаев опухоль развивается в сигмовидной ободочной кишке, около 10-12% от всех злокачественных опухолей ободочной кишки приходится на восходящую часть, в 2% случаев злокачественное образование поражает сразу несколько отделов.
Задать вопросы и записаться на консультацию можно
по телефону: 222-10-87
или заполните форму ниже
Спасибо, ваш вопрос успешно отправлен, скоро мы с вами свяжемся!
Классификация
В зависимости от размеров первичной опухоли, степени ее прорастания, распространения на другие структуры организма, различают несколько стадий рака ободочной кишки. Установленная при первичном обследовании, стадия в дальнейшем не изменяется, даже если опухоль уменьшается или увеличивается. В течении рака ободочной кишки различают 4 стадии.
| Стадия | Характеристика опухоли |
|---|---|
| I | опухоль размером не более 1,5 см, локализована в пределах слизистого слоя |
| II | II A — размер опухоли превышает 1,5 см, раковые клетки распространяются на субсерозный слой; II B — клетки опухоли проникают в соседние структуры; III C — опухоль не более 1,5 см, но раковые клетки поражают близлежащие лимфоузлы; |
| III | III А — опухоль распространяется более, чем на половину окружности кишки, выходит за пределы кишечной стенки; II В — опухоль может быть любого размера, имеются множественные метастазы; |
| IV | процесс распространяется на отдаленные органы, независимо от размера первичной опухоли и степени прорастания кишечной стенки. |
Стадирование необходимо для выбора тактики лечения и составления прогноза. Для определения стадии проводится обследование, куда входят различные методы диагностики, позволяющие оценить локализацию патологического очага и степень распространения злокачественных клеток по организму. В нашей клинике пациентам доступны все современные и эффективные методы обследования: колоноскопия, томография, ультрасонография, различные исследования крови, в том числе на онкомаркеры и др.
Основные симптомы
На начальном этапе рака ободочной кишки какие-либо симптомы отсутствуют. Однако с ростом опухоли появляются различные признаки. На что стоит обратить внимание, чтобы распознать заболевание своевременно?
Стоит учитывать, что не бывает одинаковых пациентов с идентичными симптомами, появление признаков при раке ободочной кишки зависит от локализации опухоли. Например, болевой синдром чаще появляется при расположении опухоли в правых отделах кишечника. Отрыжка, дискомфорт в животе чаще беспокоит пациентов при опухоли поперечной ободочной кишки. Запоры, диарея, метеоризм, как правило, появляются в первую очередь при злокачественном образовании в левых отделах кишки. Сигмовидная кишка чаще дает о себе знать появлением слизи и крови в испражнениях. Поэтому при любом недомогании лучше обратиться к специалисту.
Однако существуют симптомы, которые появляются независимо от локализации опухоли. Необъяснимая слабость, потеря аппетита, резкое снижение веса, повышение температуры, которую сложно снижать — эти симптомы связаны с интоксикацией организма, что происходит при запущенной стадии рака любой локализации.
Осложнения
При отсутствии лечения существует риск развития осложнений. Опухоль, достигшая больших размеров, может перекрывать просвет кишки, становясь причиной кишечной непроходимости. В этом случае пациент нуждается в немедленной госпитализации. Помимо ухудшения состояния, существует риск некроза и развития перитонита, что представляет угрозу здоровью пациента.
Непрекращающееся кровотечение может стать причиной анемии, что также способно ухудшить состояние больного. При распространении метастазов в печень возможно нарушении оттока желчи и развитие желтухи. Одним из признаков тяжелой стадии рака также является скопление жидкости в брюшной полости — асцит. Подобные осложнения ухудшают прогноз при раке ободочной кишки.
Лечение
Основным методом лечения рака ободочной кишки является операция, цель которой — удаление опухоли. В ходе оперативного вмешательства вместе с опухолью удаляется часть приводящей и отводящей кишки, регионарные лимфатические узлы и окружающая клетчатка. Методика подбирается в зависимости от локализации опухоли. Существуют следующие виды оперативных вмешательств:
В том случае, если оперативное лечение противопоказано или не может быть проведено, проводится паллиативная операция, целью которой является устранение симптомов заболевания и облегчение состояния больного.
Как проводится операция
Операция выполняется в несколько этапов.
Постоянная колостома накладывается, если опухоль является неоперабельной. В таком случае проходимость кишки восстанавливается с использованием стента. Такая операция относится к паллиативным.
Мой подход к лечению пациентов с раком ободочной кишки
Я подбираю тактику лечения, учитывая результаты обследования, возраст пациента и наличие сопутствующих заболеваний. Если это возможно, я всегда отдаю предпочтение органосохраняющему и малоинвазивному лечению. При опухоли на ранней стадии может быть проведена резекция, при этом дистальный и проксимальный края резекции находятся на достаточном расстоянии от очага патологии, чтобы при микроскопическом исследовании отсутствовали опухолевые клетки; таким образом достигается радикальность операции.
Для диссекции на протяжении многих лет я использую технологию мезоколонэктомии по собственной оригинальной методике. Использование современных ультразвуковых ножниц и аппарата электротермического лигирования тканей «LigaSure» (США) позволяет провести быстро и бескровно мобилизацию кишки в правильном слое, без необходимости применения хирургических клипс и нитей.
При мобилизации правых отделов кишки для более безопасной диссекции тканей (вблизи печеночного изгиба, между фасцией Тольди и Герота) я использую оригинальный комбинированный латерально-медиальный доступ. Этот прием дает возможность безопасно выделить мочеточник и двенадцатиперстную кишку, после чего лигировать крупные сосуды, проходящие на этом участке кишки.
В большинстве случаев на этапе реконструкции я формирую анастомоз, что позволяет сохранить качество жизни пациента на прежнем уровне. При создании межкишечного соустья я использую сшивающие аппараты последнего поколения, их применение позволяет снизить количество таких осложнений после операции, как несостоятельность швов анастомоза или стриктура.
Удаление кишки, клетчатки, лимфоузлов проводится единым блоком. При этом удаляемые ткани предварительно помещаются в специальный пластиковый контейнер, что предупреждает попадание клеток опухоли на здоровые ткани, в противном случае высок риск рецидива. Весь биологический материал, удаленный в ходе операции, отправляется на гистологическое обследование — для верификации диагноза.
При проведении операции важным этапом является профилактика тромбоза и тромбоэмболии, для этого используется компрессионный трикотаж и управляемая интраоперационная прерывистая пневматическая компрессия SCD Response (Tyco Healthcare/Kendall).
Преимущества лапароскопии
В большинстве случаев я провожу операцию методом лапароскопии: все действия выполняются через несколько небольших проколов на передней брюшной стенке. Современное эндоскопическое оборудование, используемое в ходе операции, оснащено минивидеокамерой, что позволяет выполнять все действия точно и максимально бережно. Среди преимуществ лапароскопии также можно выделить:
Короткий период реабилитации позволяет пациентам в ближайшее время после операции приступить к химиотерапии, что важно для предотвращения рецидива. Кроме того, ранняя активизация пациента после лапароскопии рекомендована в целях предупреждения тромбоэмболии.
Прогноз
Продолжительность жизни больных после операции зависит от ряда факторов, основным из которых является своевременное начало лечения. Например, при опухоли 1-2 стадии выживаемость в течение первых пяти лет после лечения превышает 90%. Прогноз при раке ободочной кишки 3 стадии составляет около 30%. Ухудшает выживаемость наличие метастазирования в отдаленные органы, для пациентов с 4 стадией рака ободочной кишки прогноз неблагоприятный, показатель составляет не более 10%.
Впрочем, эти цифры весьма приблизительны. На эффективность лечения влияет тип опухоли, ее степень дифференцировки, а также наличие сопутствующих заболеваний. Кроме того, во многом излечение зависит от адекватности терапии. Существующие сегодня методы лечения, как хирургического, так и химиотерапевтического, позволяют добиться положительных результатов даже в тех случаях, которые еще недавно считались безнадежными. Но для этого обращаться за медицинской помощью следует в клинику, где есть современное оборудование и опытный персонал.
Лечением онкологических пациентов я занимаюсь на протяжении нескольких десятков лет. Я владею четырьмя узкими специализациями, одной из которых является колопроктология. Мною лично проведено более 300 хирургических вмешательств при заболеваниях ободочной кишки. Результаты обобщены в монографии «Малоинвазивная хирургия толстой кишки». Я также регулярно провожу семинары и мастер-классы, посвященные хирургическому лечению заболеваний кишечника, которые посещают специалисты клиник и центров, курсанты постдипломного образования.
Выпадение прямой кишки у женщин, детей, мужчин — причины, лечение, степени
На выпадение прямой кишки приходится всего 0,5% от всех проктологических заболеваний у взрослых, поэтому эта проблема считается редкой. В медицине ее называют ректальным пролапсом и относят к серьезным патологиям, требующим комплексной терапии. Выражается это заболевание частичным или полным выпадением прямой кишки из ануса.
Вероятность возникновения пролапса прямой кишки различна. В США, например, им страдают преимущественно женщины старше 50 лет, в то время как в странах постсоветского пространства у женщин выпадение диагностируется в 5 раз реже, чем у мужчин.
Что такое выпадение прямой кишки и чем оно опасно
Ректальный пролапс не является опасным для жизни состоянием, но привносит массу неудобств в жизнь больного: постоянный физический и психологический дискомфорт, невозможность заниматься привычными делами и т.д. Состояние характеризуется ослаблением и растяжением терминального отдела кишечника (сигмовидной и прямой кишок) и повышения их подвижности.
Иногда при выпадении прямой кишки происходит резкое натяжение брыжейки, соединяющей переднюю и заднюю брюшные стенки. В этот момент больной испытывает сильную боль, которая может стать причиной возникновения болевого шока или коллапса. Такие состояние угрожают жизни и требуют срочного врачебного вмешательства.
У взрослых пациентов выпадение прямой кишки напрямую связывают с инвагинацией кишечника, когда одна его часть опускается и внедряется в просвет расположенной ниже кишки.
При этом дискомфорт сопровождается появлением в анальном отверстии округлых образований, которые вполне можно принять за геморроидальные узлы, если не знать особенностей, характерных для пролапса. При прогрессировании болезни происходит выпадение слизистой прямой кишки из ануса, а при прогрессировании — подслизистого и мышечного слоя.
Если вовремя не начать лечение ректального пролапса, существует риск столкнуться с осложнениями:
Чтобы не доводить состояние до критического, при подозрении на выпадение прямой кишки не следует ждать, что болезнь пройдет самостоятельно. Еще опаснее применять нетрадиционное лечение в домашних условиях. Единственный способ избавиться от ректального пролапса — обратиться к проктологу и пройти комплексную терапию болезни.
Симптомы пролапса и его стадии
Основные симптомы ректального пролапса разнятся в зависимости от стадии болезни. Общими для всех этапов прогрессирования заболевания называют:
Интенсивность указанных симптомов изменяется в зависимости от стадии болезни. Чем глубже изменения, тем сильнее они проявляются.
Есть и другие признаки, по которым врач может определить, как далеко зашел ректальный пролапс:
Признаки этой болезни похожи на проявления геморроя, поэтому их часто путают. Единственный способ, как отличить, выпадение прямой кишки или геморрой — внимательно осмотреть выпавшее из ануса образование. Рассмотреть подробно, как выглядит выпадение прямой кишки и геморрой, и чем они отличаются, поможет фото ниже.
Если складки на нем расположены продольно, а цвет телесный или бледно-розовый, это геморроидальный узел, в то время как поперечные складки и ярко красный цвет образования свидетельствуют о пролапсе прямой кишки.
Причины патологии
Основная причина возникновения пролапса прямой кишки — инвагинация кишечника. однако не только она играет роль в развитии заболевания. Было выяснено, что основными провокаторами болезни выступают анатомические или генетические особенности организма:
Перечисленные причины относятся к врожденным патологиям, однако они могут иметь и травматическую природу. Так, ослабление мышц тазового дна и анального сфинктера может произойти после родов (только естественных) у женщин. Повлиять на удерживающие способности мышц и связок могут хирургические вмешательства, травмы передней брюшной стенки, промежности, прямой кишки или ануса.
Ослабление сфинктера и удерживающих прямую кишку связок может произойти и при регулярных занятиях анальным сексом.
По статистике у мужчин выпадение чаще происходит из-за анатомических особенностей организма и вследствие чрезмерных физических нагрузок. Среди женского населения причины возникновения ректального пролапса связаны с повышением нагрузки на мышцы тазового дна при беременности и их растяжение во время родов. Причем патологические изменения становятся заметны не сразу, а спустя несколько лет или даже десятилетий, так как большая часть пациенток с таким диагнозом находится в возрасте 50 лет и старше.
Диагностика заболевания
Диагностика ректального пролапса включает первичный осмотр, во время которого врач (чаще всего это проктолог) оценивает состояние ануса и прямой кишки визуально. Помимо этого проводится простой тест: пациента просят присесть на корточки и немного натужиться, как во время дефекации. Если при этом происходит раскрытие сфинктера и прямая кишка выходит наружу, приступают к комплексному инструментальному обследованию, которое включает:
По результатам обследования и выяснения анамнеза проктолог сможет выяснить причины возникновения ректального пролапса и подобрать лечение.
Как лечить пролапс прямой кишки у взрослых
Для устранения выпадения прямой кишки применяют консервативное и хирургическое лечение. Больным рекомендуют соблюдать диету для нормализации стула, выполнять комплекс упражнений для укрепления мышц тазового дна, анального сфинктера и промежности. Чтобы избежать прогрессирования болезни, полностью исключают физические нагрузки.
Медикаментозная терапия
Консервативное лечение эффективно на первых стадиях ректального пролапса, когда прямая кишка самостоятельно втягивается, а заболевание возникло не более 3-х лет до обращения к проктологу. Цели терапии:
перечень лекарственных препаратов при таком заболевании немногочисленный. В большинстве случаев назначают регулирующие стул препараты, например, слабительные свечи или пероральные препараты (таблетки, порошки для приготовления напитков). При сильных болях возможно применение обезболивающих препаратов. Этот вопрос желательно обсудить с проктологом.
Важно! Использовать слабительные средства нужно крайне осторожно и только с разрешения лечащего врача. Попытки смягчить ими стул без наличия хронического запора могут привести к повышению нагрузки на прямую кишку и ректальный сфинктер.
Если выпадение прямой кишки наблюдается у женщины при беременности, к выбору лекарств подходят с особой осторожностью. Этой категории больных противопоказана большая часть препаратов. Для восстановления стула будущим мамам рекомендуется применять масляные клизмы или микроклизму «Микролакс» и препараты для нормализации функции толстой кишки (Дюфалак, Фитомуцил). Для подбора терапии рекомендована консультация специалиста.
Также при ректальном пролапсе применяется склерозирование прямой кишки. Метод относится к консервативным и применяется преимущественно для лечения молодых людей и детей. В ходе процедуры врач вводит склерозирующий препарат на основе 70% этилового спирта в околопрямокишечную клетчатку, в результате чего она частично рубцуется и лучше удерживает этот отдел кишечника.
Дополнительно больным назначают комплекс витаминов с железом. Это помогает восстановить общее самочувствие и укрепить иммунитет.
Хирургическое вмешательство
Оперативное лечение применяется на 3 и 4 стадиях ректального пролапса, а также при неэффективности консервативной терапии. Существует несколько методов закрепления прямой кишки в физиологически правильном положении, и ни один врач не скажет, какая именно операция самая эффективная. Все они делятся на несколько групп и отличаются по принципу воздействия на органы.
Методы оперативного лечения тотального выпадения прямой кишки:
Из всего многообразия предложенных различными авторами хирургических методов лечения, проверку временем прошло лишь несколько, из-за высокого процента рецидивов в одних случаях, большой травматичности и множества осложнений в других. На сегодняшний день наиболее часто при выпадении прямой кишки выполняются:
Операция Кюммеля-Зеренина
Выполняется лапаротомия (т.е. разрез на передней брюшной стенке). Натянутую кверху прямую кишку подшивают узловыми серозно-мышечными швами к продольной связке мыса крестца.
Задняя петлевая ректопексия по Walles
Задняя петлевая ректопексия с помощью сетки предложена E.H.Wells в 1959 г. Операция может быть выполнена как обычным способом, т.е. с лапаротомией, так и лапароскопически. После мобилизации прямой кишки и ее подтягивания выполняется фиксация задней стенки кишки к крестцу с помощью полипропиленовой сетки. По данным разных авторов, количество рецидивов после операции составляет от 2% до 8%.
Операция Микулича
Представляет собой промежностное иссечение выпадающей части прямой кишки. Операция Микулича относительно проста в техническом исполнении, малотравматична, операционный риск при ее проведении минимален, однако дает большое количество рецидивов, по данным разных авторов до 60%. С учетом преимуществ и недостатков выполняется в основном пожилым больным.
Операция Делорма (Склифосовского-Юварра-Рен-Делорм-Бира)
Основана на принципе удаления слизистой оболочки выпадающей прямой кишки и последующей пликации оголенной кишечной стенки для формирования как бы мышечной муфты, предупреждающей последующее выпадение. Эта операция также малотравматична, операционный риск при ее проведении минимален, возможно ее проведение под местной анестезией. Недостаток у нее тот, же, что и у предыдущей операции — дает большое количество рецидивов (по данным разных авторов до 40%), хотя и существенно меньше, чем операция Микулича. Также выполняется в основном пожилым больным.
После хирургического вмешательства применяют местные анестетики и пероральные анальгетики для уменьшения боли, противовоспалительные и заживляющие препараты (свечи, мази или гели).
В послеоперационный период больному важно соблюдать строгую диету, чтобы не допустить возникновения запора или диареи.
В течение года после проведения хирургического вмешательства пациент должен регулярно приходить на прием к проктологу.
Диета
В рацион больного включают продукты с грубыми растительными волокнами: фрукты и овощи, крупы, цельнозерновой хлеб (желательно подсушенный), кисломолочные продукты. Они должны стать основой диеты. Питание должно быть регулярным, обязательно без переедания. В день должно быть не менее 5 приемов пищи.
Нежелательно включать в рацион продукты и блюда, которые раздражают кишечник и вызывают запор:
Отказаться стоит и от алкоголя, кофе, газированных напитков. Они раздражают кишечник не меньше, чем перечисленные выше продукты. Пить лучше натуральные ягодные морсы и компоты, кисели, травяной чай и воду. Минимальный объем жидкости, который следует употреблять в день, составляет 2 литра.
Народные средства
Средства народной медицины не особенно эффективны при ректальном пролапсе. Они помогают устранить неприятные симптомы и избежать появления необратимых изменений прямой кишки. Улучшить состояние помогут сидячие ванночки с отварами трав:
Полезными будут примочки из выпаренного сока айвы, настойки манжетки или пастушьей сумки. Также лечение в домашних условиях подразумевает прием растительных препаратов внутрь. Как правило, эти средства обладают регулирующими стул свойствами. Неплохим эффектом обладают отвары корней аира и побегов манжетки.
Важно! Народная медицина не является альтернативой стандартных терапевтических методов. Использовать упомянутые средства можно только с одобрения лечащего врача!
ЛФК и другие способы
Если причиной возникновения ректального пролапса стала слабость мышц анального сфинктера или тазового дна, проктологи рекомендуют ежедневно выполнять комплекс специальных упражнений:
Дополнительно может использоваться пальцевый массаж прямой кишки. Он проводится только специалистом, и помогает повысить тонус мышц прямой кишки и удерживающих ее мышц и связок.
На время терапии пациент должен соблюдать тщательную гигиену промежности. После дефекации желательно использовать мягкую, слегка увлажненную бумагу. Идеальный вариант — подмываться слегка прохладной водой.
Последствия и профилактика выпадения прямой кишки
При отсутствии своевременного лечения пролапс прямой кишки может осложниться некрозом тканей, ишемическим колитом, трофическими язвами, проктитом и даже гангреной. Такие заболевания наблюдаются при длительном протекании болезни с частыми выпадениями прямой кишки. В отдельных случаях на фоне осложненного выпадения образуются полипы, которые затем могут переродиться в раковую опухоль.
Единственный способ избежать таких проблем — профилактика возникновения пролапса. Она включает исключение факторов, приводящих к перенапряжению передней брюшной стенки и повышению внутрибрюшного давления:
Если избежать болезни не удалось, необходимо лечить ее под наблюдением проктолога и соблюдать все его рекомендации.
Основная информация о пролапсе прямой кишки, о риске ее возникновения и способах лечения смотрите в видео.
Выпадение прямой кишки у взрослых. Клинические рекомендации.
Выпадение прямой кишки у взрослых
Оглавление
Ключевые слова
Список сокращений
ИМТ – индекс массы тела
МКБ – международная классификация болезней
СОП – синдром опущения промежности
СОД – синдром обструктивной дефекации
СРК – синдром раздраженного кишечника
УЗИ – ультразвуковое исследование
ЖКТ – желудочно-кишечный тракт
ФГБУ – Федеральное Государственное бюджетное учреждение
ГНЦК – Государственный научный центр колопроктологии
МЗ – Министерство здравоохранения
РФ – Российская Федерация
Термины и определения
Синдром опущения промежности – совокупность заболеваний, возникающих вследствие опущения или выпадения органов таза. Эти заболевания могут существовать как отдельные нозологические формы (ректоцеле, выпадение прямой кишки, энтероцеле).
Синдром обструктивной дефекации – нарушение опорожнения прямой кишки, обусловленное анатомическими изменениями заднего отдела тазового дна, такими как ректоцеле, внутренняя инвагинация и выпадение прямой кишки, энтероцеле и сигмоцеле в сочетании с дискоординацией и/или атрофией мышц тазового дна.
1. Краткая информация
1.1 Определение
Выпадение прямой кишки – выпячивание или выход всех слоёв прямой кишки наружу через заднепроходное отверстие [1, 2, 3, 4, 5, 6].
Синоним: ректальный пролапс.
Внутреннее выпадение прямой кишки – интраректальная инвагинация прямой и/или сигмовидной кишки без выхода наружу, т.е. стенка прямой кишки пролабирует в ее просвет, но не выпадает через задний проход [7, 8].
Синоним: внутренняя (интраректальная) инвагинация прямой кишки.
1.2 Этиология и патогенез
Наружное и внутреннее выпадение прямой кишки развиваются вследствие слабости связочно-мышечного аппарата органов таза. Эти заболевания принято считать нозологическими формами синдрома опущения промежности, возникающего чаще у женщин. Соответственно, выпадение прямой кишки чаще отмечается у представительниц женской половины населения. Однако у мужчин, подвергавшихся в течение жизни воздействию характерных факторов риска, может развиваться опущение тазового дна с выпадением или внутренней инвагинацией прямой кишки.
Риск развития заболевания у женщин увеличивается при осложненном течении беременности и родов, в том числе при хирургических пособиях при родах, при стремительных родах, разрывах промежности, родах крупным плодом [9].
Развитию синдрома опущения промежности способствует тяжелый физический труд и интенсивные занятия спортом, причем не только сопровождающиеся поднятием тяжестей. В основе влияния этих факторов лежит повышение внутрибрюшного давления, а также резкие вертикальные нагрузки, ведущие к смещению органов таза в сагиттальной плоскости [10].
Следующим фактором риска, провоцирующим опущение тазовых органов с последующим выпадением прямой кишки, можно считать хронические заболевания кишечника и легких. Хронический запор, провоцирующий частое и интенсивное натуживание и упорный кашель, приводят к многократному резкому повышению внутрибрюшного давления и как следствие – перерастяжению мышечно-фасциальных структур тазового дна, обеспечивающих нормальное положение органов.
К особенностям конституции организма и строения прямой кишки, которые могут послужить причиной развития выпадения прямой кишки, относят большую глубину прямокишечно-маточного углубления у женщин и прямокишечно-пузырного у мужчин, диастаз порций леватора, недостаточную фиксацию прямой кишки к крестцу, слабость анального сфинктера [11, 12, 13, 14].
1.3 Эпидемиология
Частота заболеваемости выпадением прямой кишки составляет в среднем 9% от всех колопроктологических заболеваний или от 0,3% до 5,2% среди пациентов общехирургических стационаров [24, 25].
Женщины в возрасте старше 50 лет в 6 раз чаще мужчин страдают выпадением прямой кишки [26, 27, 28]. Традиционно считается, что ректальный пролапс является следствием тяжёлых многократных родов, однако около 1/3 пациенток с данным заболеванием являются нерожавшими. Пик заболеваемости приходится на седьмое десятилетие у женщин, однако у мужчин эта проблема может развиться в возрасте 40 лет и ранее. Ректальный пролапс, возникающий в молодом возрасте, чаще всего диагностируется на фоне аутизма, задержки психомоторного развития, а также различных психических заболеваний, требующих длительного приёма нейролептиков [29]. У 31% больных заболевание развивается на фоне тяжёлого физического труда [30].
1.4 Код по МКБ-10
Другие болезни кишечника (К62).
K62.2 Выпадение заднего прохода.
K62.3 Выпадение прямой кишки.
K62.6 Язва заднего прохода и прямой кишки.
1.5 Классификация
Оксфордская рентгенологическая классификация:
1) высокая ректо-ректальная инвагинация (выпадение остаётся выше пуборектальной линии);
2) низкая ректо-ректальная инвагинация (пролапс на уровне пуборектальной линии);
3) высокая ректо-анальная инвагинация (пролапс доходит до анального канала);
4) низкая ректо-анальная инвагинация (пролапс в анальном канале, но не выходит за анальную складку);
5) наружное выпадение прямой кишки [31].
Классификация ГНЦ колопроктологии:
Стадии выпадения прямой кишки:
Фазы компенсации функции мышц тазового дна:
Степени недостаточности анального сфинктера:
2. Диагностика
2.1 Жалобы и анамнез
Пациент предъявляет жалобы на наличие выпадения, выворачивания прямой кишки через задний проход, вправляемого самостоятельно или требующего ручного пособия. Выпавшая часть прямой кишки может иметь разную форму, размеры и длину [34].
При внутреннем выпадении прямой кишки отмечаются следующие жалобы:
Примерно 50-75% пациентов с выпадением прямой кишки жалуются на недержание кала, а 25-50% на запоры [35, 36, 37, 38].
2.2 Физикальное обследование
На этапе постановки диагноза:
2.3 Лабораторная диагностика
На этапе постановки диагноза:
2.4 Инструментальная диагностика
На этапе постановки диагноза:
Коментарий: Кроме этого, при ректороманоскопии можно обнаружить солитарную язву, уточнить её расположение и произвести биопсию для морфологического подтверждения диагноза
Солитарная язва чаще представляет собой участок гиперемированной слизистой оболочки небольшого размера с белым налётом. Приблизительно у 57 % пациентов с солитарной язвой встречается изъязвление дефекта, а полиповидные разрастания в области язвы выявляются в 25 % [49, 50, 51].
Таблица1. Нормальные показатели дефекографии [48].
Положение кишки относительно лобково-копчиковой линии (см.)
Время опорожнения прямой кишки (сек.)
Коментарий: Данные дефекографии позволяют сделать заключение о степени СОП, выявить внутреннюю инвагинацию прямой кишки и сопутствующие ей изменения, такие как ректоцеле, сигмоцеле и диссинергия тазовых мышц
Коментарий: Профилометрия определяет исходное состояние запирательного аппарата прямой кишки, которое может отличаться от нормальных значений при выпадении прямой кишки [55, 56]. Исследование осуществляется с помощью катетера, введенного в прямую кишку, по которому устанавливается скорость перфузии жидкости равная 1 мл/мин. Затем катетер вытягивается из прямой кишки со скоростью 5 мм/сек, при этом регистрируется давление на всем протяжении его перемещения (Таблица 2). Анализ данных проводится компьютерной программой с построением графика, на котором отражается распределение давления в анальном канале [56].
Таблица 2. Показатели профилометрии в норме (мм.рт.ст.) [56].
Показатели профилометрии
Анальный канал в целом:
Коэффициент асимметрии (ед)
Зона высокого давления*
*Зона высокого давления соответствует проекции внутреннего и глубокой порции наружного сфинктера (УДД 3, УУР С).
Коментарий: Исследование выполняют при помощи стимуляции специальным электродом дистальных ветвей половых нервов в точке их входа в седалищно-прямокишечную ямку у седалищных остей. С электродом соединён датчик, который регистрирует вызванный моторный ответ. Время проведения импульса оценивается как латентность полового нерва. В норме она составляет 2,0±0,2 мс.
Пациенты с увеличением латентности половых нервов, могут иметь более высокую степень недержания кала после хирургической коррекции пролапса, хотя прямой корреляционной зависимости этих состояний не обнаружено.
Таблица 3. Показатели электромиографии в норме (мкВ).
Фоновая электрическая активность, мкВ
Произвольная электрическая активность, мкВ
Рефлекторные реакции на пробы с повышением внутрибрюшного давления (кашель, напряжение мышц передней брюшной стенки)
Коментарий: Это позволяет определить функциональные особенности толстой кишки – преобладание медленно-транзитного запора или эвакуаторных нарушений.
2.5 Дифференциальная диагностика
Распространённым заблуждением является ошибочное выявление ректального пролапса при выпадении геморроидальных узлов. Как правило, эти состояния легко дифференцировать при клиническом осмотре. Направление складок на выпадающих тканях показывает, что в случае полнослойного выпадения они всегда ориентированы концентрически, в то время как при выпадении геморроидальных узлов или слизистой оболочки прямой кишки наблюдается их радиальное расположение[10, 32].
3. Лечение
3.1 Консервативное лечение
Коментарий: Лечение следует начинать с мероприятий, заключающихся в подборе режима питания с включение в рацион высоковолокнистых продуктов и большого количества жидкости. Ежедневный прием 25 граммов волокон увеличивает частоту стула у пациентов с хроническими запорами [63].
Макрогол образует водородные связи с молекулами воды в просвете кишки, увеличивает содержание жидкости в химусе, стимулирует механорецепторы и улучшает перистальтику кишечника. Рекомендуется ежедневный прием 20 г. макрогола [64].
Прукалоприд – прокинетик, селективный антогонист 5-НТ4-серотониновых рецепторов, что объясняет его действие на моторику кишечника. Рекомендуемая доза – 2 мг. в день. В результате семи плацебо-контролируемых исследований установлено, что прокинетики увеличивают частоту опорожнения толстой кишки по сравнению с группой, принимавшей плацебо [66]. Сочетание препаратов, увеличивающих объем кишечного содержимого (макрогол) и усиливающих кишечную перистальтику (прукалоприд) часто дает эффект в лечении хронических запоров [64, 65].
Лактулоза оказывает осмотическое, слабительное действие, стимулирует размножение молочнокислых бактерий и усиливает перистальтику толстой кишки. Максимальная доза для взрослых — 60 мл в сутки. Кратность приема может составлять 1–2 (реже 3) раза в день. Курс лактулозы назначают на 1–2 месяца, а при необходимости — и на более длительный срок. Отменяют препарат постепенно под контролем частоты и консистенции стула [65].
Рекоменуется сравнительная оценка действия мукофалька (фитомуцила), который является более эффективным средством, обеспечивающий лучшую консистенцию стула и дает меньше побочных реакций по сравнению с лактулозой и другими слабительными [67].
Кроме указанных препаратов для улучшения функции толстой кишки могут применяться другие слабительные средства, такие как магния гидроксид, бисакодил и т.д. (УДД 3, УУР С) [65, 68].
По разным данным эффект от биофидбек-терапии отмечается у 70% пациентов с диссинергией мышц тазового дна, а у 50% эффект сохраняется в отдалённом периоде [72, 73].
3.2 Хирургическое лечение
Хирургический метод является основным для лечения выпадения прямой кишки. Существует множество способов коррекции ректального пролапса.
В зависимости от доступа они подразделяются на промежностные и трансабдоминальные вмешательства. Выбор операции зависит от возраста пациента, наличия тяжёлых сопутствующих заболеваний, состояния моторно-эвакуаторной функции кишечника, предпочтений хирурга и его опыта [74].
3.2.1. Трансабдоминальные операции
Трансабдоминальные вмешательства имеют лучшие функциональные результаты и низкую частоту рецидивов по сравнению с трансперинеальными, что делает их операциями выбора при лечении ректального пролапса [74, 75, 76]. Практически все трансабдоминальные операции могут выполняться как открытым, так и лапароскопическим способом [74, 77, 78, 79].
Коментарий: Показания: наружное или внутреннее выпадение прямой кишки. Методика. Справа от прямой кишки на уровне мыса крестца вскрывается тазовая брюшина. Разрез продлевается вниз до дна Дугласова кармана, огибая кишку спереди. Производится мобилизация прямой кишки по задней и правой боковой полуокружностям до леваторов. Затем, начиная от мыса крестца, в дистальном направлении накладываются 3-4 шва нерассасывающимся материалом (полиамид), захватывая продольную связку крестца. Этими же швами, начиная с нижнего, прошивается передняя стенка прямой кишки. При завязывании швов происходит ротация кишки на 1800 с её фиксацией к крестцу. Тазовая брюшина ушивается над кишкой с созданием дубликатуры для того, чтобы ликвидировать глубокий Дугласов карман.
По данным литературы, частота рецидивов после шовной ректопексии составляет от 3% до 9% [80, 81]. Эта методика может вызвать возникновение запоров или усиление уже существующих нарушений транзита в отдалённые сроки после операции у 50% оперированных больных [24].
Коментарий: Показания: наружный или внутренний пролапс, сочетание выпадения кишки с ректоцеле и сигмоцеле. Методика. После рассечения тазовой брюшины справа от прямой кишки производится её мобилизация по передней и правой боковой полуокружностям до латеральной связки. У мужчин по передней полуокружности кишка мобилизуется до границы средне- и нижнеампулярного отделов. У женщин при сопутствующем ректоцеле операция выполняется с расщеплением ректовагинальной перегородки и мобилизацией передней стенки кишки до анального сфинктера. Синтетический имплант (полипропиленовая сетка размерами 10х3 см.) подшивается тремя-четырьмя не рассасывающимся швами (полиамид) ко всей поверхности мобилизованной передней стенки прямой кишки. У женщин двумя дополнительными швами к сетке фиксируется задний свод влагалища. Затем свободный конец сетки крепится к надкостнице 1-го крестцового позвонка двумя нерассасывающимся швами (полиамид), и операция завершается ушиванием тазовой брюшины над сеткой.
Коментарий: Показания: наружное или внутреннее выпадение прямой кишки. Методика. Рассекают тазовую брюшину с обеих сторон от прямой кишки, обнажая мыс крестца. Кишку мобилизуют по задней и боковым полуокружностям до уровня леваторов. К крестцу двумя швами с использованием не рассасывающегося материала (полиамид) подшивается в поперечном к оси крестца направлении сетчатый имплант (полипропиленовая сетка) размерами 8х3 см. Мобилизованная кишка без избыточного натяжения помещается на аллотрансплантат, и свободные края сетки фиксируются нерассасывающимся материалом (полиамид) к боковым стенкам кишки (2 шва с каждой стороны). Тазовая брюшина ушивается над сеткой.
Коментарий: Показания: наружное или внутреннее выпадение прямой кишки в сочетании с хроническим толстокишечным стазом (время транзита более 96 часов за счёт задержки в левых отделах). Методика. Выполняется стандартная резекция левых отделов ободочной кишки с наложением анастомоза конец в конец. Затем прямая кишка фиксируется к крестцу при помощи одного из вышеописанных методов таким образом, что сигмо-сигмоидный анастомоз находится на 2-3 см выше мыса крестца.
Процент рецидивов после использования данного метода колеблется от 2% до 5%, а частота осложнений достигает 20% [74, 8]По данным некоторых авторов, у пациентов с нарушением транзита по толстой кишке после выполнения резекции кишки с ректопексией происходит нормализация стула [74, 88,89]. Другие авторы утверждают, что удаление левых отделов является неадекватным объёмом резекции, и у пациентов с хроническим толстокишечным стазом должна выполняться ректопексия с субтотальной колэктомией. Отмечено, что выполнение резекции кишки в сочетании с ректопексией у пациентов с признаками анальной инконтиненции снижает вероятность улучшения анального держания в послеоперационном периоде по сравнению с изолированной ректопексией
В литературе появляется все больше доказательств того, что резекцию левых отделов ободочной кишки можно выполнять только в случаях нарушения транзита по левым отделам ободочной кишки, а при преобладании симптомов недержания выполнение данного оперативного вмешательства противопоказано [90,91].
Коментарий: Показания: внутреннее выпадение прямой кишки, осложнённое солитарной язвой с рубцовой деформацией стенки кишки, нарушающей кишечную проходимость. Методика. Производят разрез брюшины в области корня брыжейки сигмовидной кишки. Затем разрез продлевают на тазовую брюшину, огибая прямую кишку в виде лиры. Выполняют мобилизацию сигмовидной и прямой кишки до нижнеампулярного отдела. Граница резекции прямой кишки проходит ниже края солитарной язвы, сигмовидную кишку резецируют на уровне дистальной трети. Анастомоз накладывают конец в конец с использованием циркулярного сшивающего аппарата.
По результатам ретроспективных исследований установлено, что частота рецидивов выпадения прямой кишки после передней резекции растёт с течением времени и через 2, 5 и 10 лет после операции составляет до 3%, 6% и 12%, соответственно [92]. Послеоперационные осложнения развиваются в 29% случаев [92]. Важно отметить, что низкое наложение анастомоза у больных с недержанием может привести к полной потере контроля над дефекацией
3.2.2. Промежностные операции
Выполнение хирургических вмешательств промежностным доступом менее травматично для пациента. Однако высокая частота рецидивов и плохие функциональные результаты определяют их применение лишь у пожилых пациентов или у больных с тяжёлыми сопутствующими заболеваниями [32,75,76].
Коментарий: Показания: наружное выпадение прямой кишки у пожилых пациентов с наличием тяжёлых сопутствующих заболеваний, повышающих риск трансабдоминальных вмешательств. Методика. Трансанально, отступя 2 см от зубчатой линии, циркулярно рассекают слизистую оболочку прямой кишки. Последняя отпрепаровывается от мышечного слоя выпавшей части кишки и отсекается. На мышечную стенку прямой кишки накладывается 4-5 вертикальных швов для создания мышечного валика, затем восстанавливается целостность слизистой оболочки.
Положительной стороной данного вмешательства является малая травматичность. Однако вероятность развития рецидива пролапса после этого метода выше, чем при трансабдоминальных операциях, и составляет 10%-15% [94, 95, 96, 97]. Воспалительные осложнения, задержка мочеиспускания, кровотечение и запоры встречаются в послеоперационном периоде в 4-12% случаев.
Коментарий: Показания: наружное выпадение прямой кишки у пациентов, страдающих тяжёлыми заболеваниями сердечно-сосудистой и дыхательной систем. Методика. На 2 см. выше зубчатой линии производят циркулярный разрез всей толщи кишечной стенки. Трансанально мобилизуют прямую кишку и дистальный отдел сигмовидной с перевязкой кровеносных сосудов в максимальной близости от кишечной стенки до уровня, когда дальнейший пролапс кишки невозможен. После пересечения ободочной кишки и удаления препарата накладывают анастомоз ручным швом или с помощью сшивающего аппарата.
Частота осложнений после операции Лонго варьирует от 15 до 47% [104, 105, 106, 107]. Чаще всего встречается императивный позыв на дефекацию (40%), однако спустя год он сохраняется лишь у 10% пациентов [108].
4. Реабилитация
5. Профилактика и диспансерное наблюдение
6. Дополнительная информация, влияющая на течение и исход заболевания
Отрицательно влияют на исход лечения:
Отказ от приема препаратов, улучшающих функцию толстой кишки и облегчающих опорожнение;
Физические нагрузки, приводящие к повышению внутрибрюшного давления;
Обострения хронических заболеваний легких, сопровождающихся длительным и натужным кашлем;
Присоединения инфекционных осложнений.
6.1. Область применения рекомендаций
Клинические рекомендации предназначены врачам-терапевтам, врачам общей практики (семейным врачам), гастроэнтерологам, колопроктологам, хирургам, эндоскопистам, организаторам здравоохранения, медицинским работникам со средним медицинским образованием, врачам-экспертам медицинских страховых организаций, в том числе при проведении медико-экономической экспертизы. Консервативное может проводиться в амбулаторных условиях при участии врача-колопроктолога или врача-хирурга. Хирургическое лечение проводится в условиях круглосуточного стационара, необходимо применение КСГ 75 – операции на кишечнике и анальной области (уровень 3), или, в зависимости от метода лечения и характера течения заболевания оказания высокотехнологичной медицинской помощи по профилю «Абдоминальная хирургия» перечня видов высокотехнологичной медицинской помощи, не включенных в базовую программу обязательного медицинского страхования, финансовое обеспечение которых осуществляется за счет средств, предоставляемых федеральному бюджету из бюджета Федерального фонда обязательного медицинского страхования в виде иных межбюджетных трансфертов.
6.2. Ограничение применения рекомендаций.
Клинические рекомендации отражают мнение экспертов по наиболее спорным вопросам. В клинической практике могут возникать ситуации, выходящие за рамки представленных рекомендаций, поэтому окончательное решение о тактике ведения каждого пациента должен принимать лечащий врач, на котором лежит ответственность за его лечение.
Критерии оценки качества медицинской помощи
Критерии качества
Уровень достоверности доказательств
Уровень убедительности рекомендаций
Как выглядит выпавшая кишка 4 27 1 689 1 192
TNM классификация рака толстой кишки и его стадии
Система TNM широко распространена (системы Дюкс и Астлер-Колер не используются): Т = первичная опухоль, N = вовлечение лимфоузлов, М = отдаленные метастазы. Ниже представлена TNM классификация рака толстой кишки.
а) Первичная опухоль
Тx Первичная опухоль не может быть оценена
Т0 Признаки первичной опухоли отсутствуют
Tis Рак in situ: интраэпителиальный или с инвазией в собственную пластинку
Т1 Опухоль прорастает в под слизистый слой
Т2 Опухоль прорастает в собственную мышечную оболочку
Т3 Опухоль прорастает через мышечную оболочку в субсерозный слой или в неперитонизированные параколические/параректальные ткани
Т4 Опухоль прорастает висцеральную брюшину или непосредственно прорастает в соседние органы
б) Регионарные лимфатические узлы (N)
Nx Региональные лимфатические узлы не могут быть оценены
N0 Нет метастазов в региональные лимфатические узлы
N1 Метастазы в 1-3 региональных лимфатических узлах
N2 Метастазы в >4 региональных лимфатических узлах
в) Отдаленные метастазы (М)
Mx Наличие отдаленных метастазов не может быть оценено
M0 Отдаленных метастазов нет
Ml Отдаленные метастазы
г) Протяженность резекции
Rx Наличие резидуальной опухоли не может быть оценено
R0 Резидуальной опухоли нет
R1 Резидуальная опухоль определяется микроскопически
R2 Резидуальная опухоль определяется макроскопически
д) Модификаторы
р Патоморфологическая оценка
с Клиническая оценка
и Ультрасонографическая оценка
у Оценка после химиолучевой терапии
е) Клиническое стадирование, основанное на наиболее значимом компоненте TNM
— Стадия I М0 + N0 =>Т1 или Т2
— Стадия II М0 + N0 => Т3 или Т4
IIА Т3 N0 М0
IIВ Т4 N0 М0
— Стадия III М0 => N+, любая Т
IIIА Т1-Т2 N1 М0
IIIВ Т3-Т4 N1 М0
IIIС любая Т N2 М0
— Стадия IV M1, любая Т, любая N
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Расшифровка результатов 1 скрининга при беременности
Комбинированный пренатальный скрининг проводится на 11-14 неделе беременности при размере эмбриона не менее 45 мм и не более 84 мм. Это комплексное обследование плода для оценки параметров его развития. Основная его задача – раннее выявление пороков развития плода, профилактика детской инвалидности, снижение младенческой и детской смертности.
Первый скрининг состоит из инструментальной части – проведение УЗИ и лабораторной – анализ крови на определение концентрации хорионического гонадотропина (βХГЧ) и ассоциированного с беременностью протеина А (РАРР-А). Совокупные результаты этих показателей позволяют спланировать тактику ведения беременности.
Почему обследование проводится на сроке 11-14 недель
Первый триместр – это период формирования всех органов и структур организма. К концу первого триместра заканчивается эмбриональный и начинается фетальный период развития плода. Именно в сроке от 11 недель 1 дня до 13 недель 6 дней беременности наиболее хорошо визуализируются эхографические маркеры хромосомных аномалий.
Кому нужно пройти обследование
По результатам исследования можно судить о риске рождения детей с хромосомными болезнями и врожденными пороками развития, поэтому рекомендуется внимательно отнестись к вопросу и обследоваться всем беременным. Показаниями к обязательному пренатальному скринингу первого триместра являются:
Как подготовиться
Подготовка к первому скринингу выражается в щадящей диете. Погрешности питания могут сказаться на общем состоянии женщины и снизить точность результатов. За неделю до обследования:
За сутки до скрининга:
Желательно соблюдать умеренную физическую активность, если для этого нет противопоказаний. Также важны прогулки, полноценный отдых.
Проведение обследования
Анализ крови и УЗИ выполняются в один день, чтобы избежать погрешностей из-за разницы срока.
Только по расшифровке результатов УЗИ и анализа на гормоны делается вывод о возможных рисках.
Что показывает УЗИ
На скрининге при беременности производится фетометрия плода – определение размеров частей тела и оцениваются все анатомические структуры.
Полученные результаты сравниваются со статистической таблицей, в которой указан процентиль попадания в выборку нормативных значений. При показателях менее 5 и более 95 назначаются дополнительные обследования.
Во время ультразвукового исследования в 1 триместре оценивают следующие параметры: кости свода черепа и головной мозг, позвоночник, передняя брюшная стенка, конечности плода, структуры лица, органы грудной клетки и брюшной полости, а также основные эхографические маркеры хромосомных аномалий.
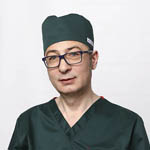
Толщина воротникового пространства (ТВП)
Область между внутренней поверхностью кожи плода и наружной поверхностью мягких тканей, покрывающих шейный отдел позвоночника. ТВП считается наиболее важным маркером хромосомных аномалий.
Это пространство после 13 недели начинает уменьшаться, поэтому возможность его оценить есть только на первом скрининге.
| Срок беременности | Толщина воротниковой зоны в мм | ||
| Процентиль 5 | Процентиль 50 | Процентиль 95 | |
| 11 недель | 0,8 | 1,6 | 2,4 |
| 12 недель | 0,7 | 1,6 | 2,5 |
| 13 недель | 0,7 | 1,7 | 2,7 |
Несоответствие результатов нормативным значениям говорит о повышенном риске развития хромосомных патологий. В зависимости от сформировавшегося набора хромосом, это могут быть синдром Дауна, Патау, Эдвардса, Шерешевского-Тернера. Для уточнения диагноза в этом случае могут быть назначены биопсия хориона или плаценты, анализ пуповинной крови, околоплодных вод. Только после проведения дополнительных исследований можно поставить точный диагноз.
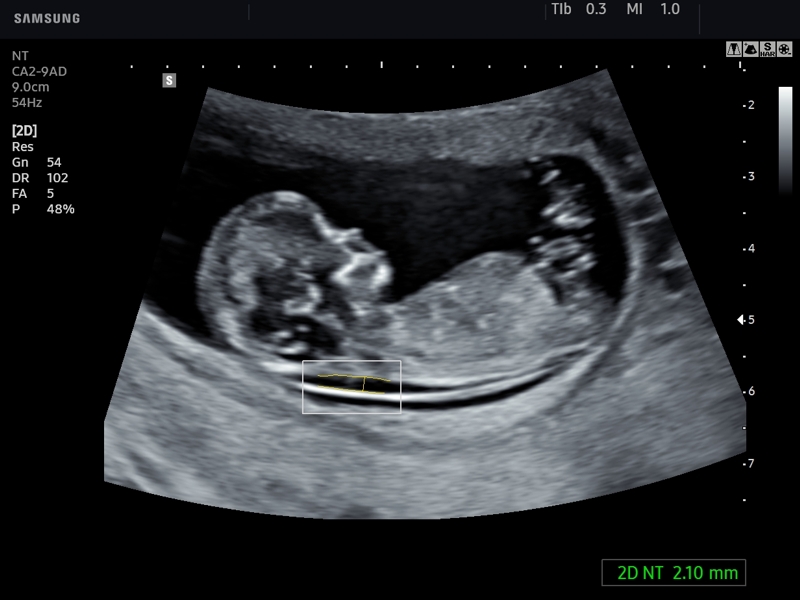
Копчико-теменной размер (КТР)
Показывает расстояние между копчиковой и теменной костями. По этому параметру на УЗИ определяют точный срок гестации, а также устанавливают соотношение массы плода к его КТР.
Незначительное отклонение от норм говорит об особенностях телосложения и не является поводом для беспокойства.
| Срок беременности | Копчико-теменной размер в мм | ||
| Процентиль 5 | Процентиль 50 | Процентиль 95 | |
| 11 недель | 34 | 42 | 50 |
| 12 недель | 42 | 51 | 59 |
| 13 недель | 51 | 63 | 75 |
Если скрининг при беременности показал результаты, превышающие нормы, это указывает, что плод достаточно крупный. Показатель существенно меньше говорит либо о неправильно определенном сроке гестации (в этом случае проводится повторное обследование через 1-1,5 недели), либо о замедлении развития вследствие внутриутробной гибели, нарушенного гормонального фона или инфекционного заболевания матери, генетических отклонений.
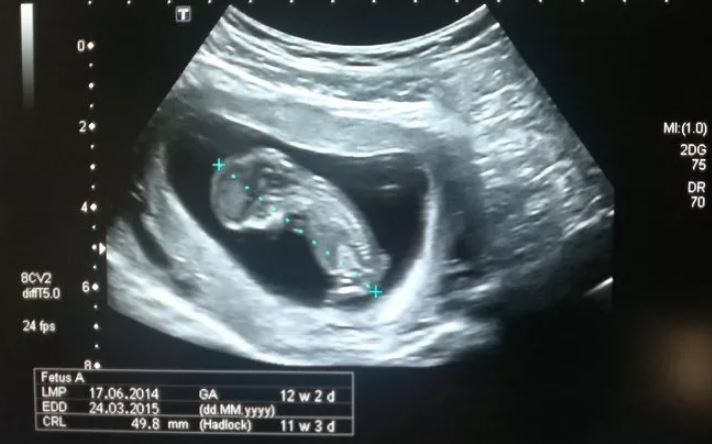
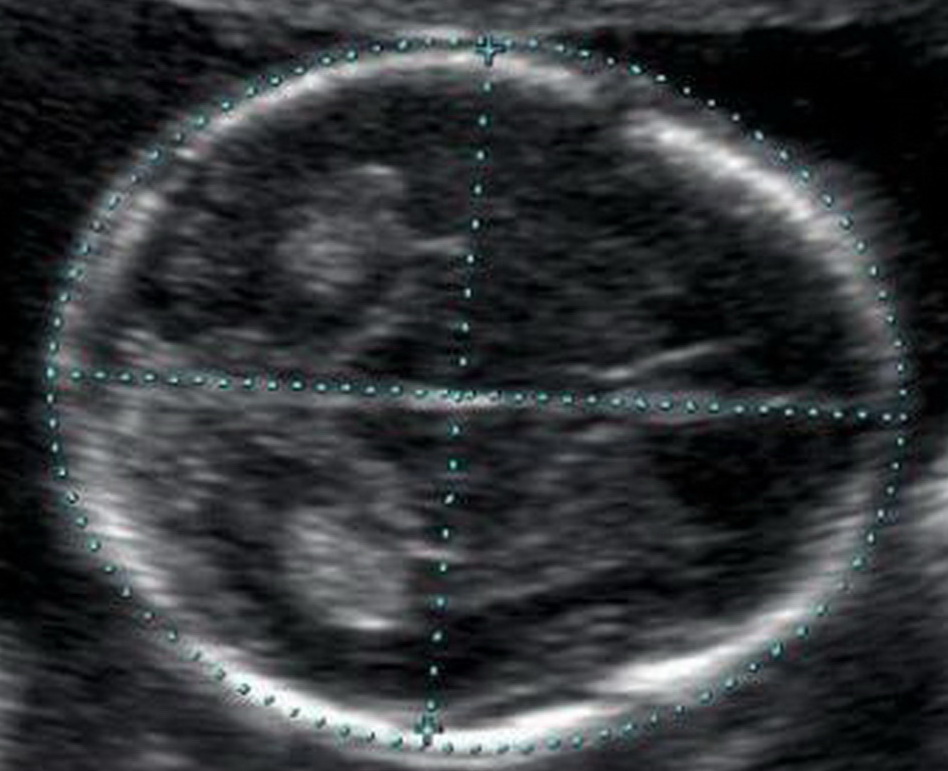
Кости свода черепа и головной мозг
Уже с 11 недели при УЗ-исследовании можно обнаружить дефекты костей черепа, что говорит о тяжелых пороках развития плода, несовместимых с жизнью. Оценка головного мозга основана на изучении так называемой «бабочки» – сосудистых сплетений боковых желудочков. Четкая визуализация и ее симметричность говорит о нормальном развитии головного мозга.
| Срок беременности | БПР, ЛЗР в мм | ||
| Процентиль 5 | Процентиль 50 | Процентиль 95 | |
| 11 недель | 13,19 | 17,21 | 21,23 |
| 12 недель | 19,22 | 21,24 | 24,26 |
| 13 недель | 20,26 | 24,29 | 28,32 |
Носовая кость
К концу триместра она должна быть сформирована, четко визуализироваться.
| Срок беременности | Носовая кость в мм | ||
| Процентиль 5 | Процентиль 50 | Процентиль 95 | |
| 11 недель | визуализируется, не измеряется | визуализируется, не измеряется | визуализируется, не измеряется |
| 12 недель | 2 | 3,1 | 4,2 |
| 13 недель | 2 | 3,1 | 4,2 |
Патологией носовой кости считается ее отсутствие, гипоплазия (очень маленькие размеры) и изменение ее эхогенности.
Диаметр грудной клетки, окружность головы и живота, длина бедренной кости также позволяют судить о пропорциональности развития.
Состояние сердца
При исследовании сердца оценивается его расположение, устанавливается наличие четырех камер сердца – два предсердия и два желудочка и оценивается их симметричность. Измеряется частота сердечных сокращений.
| Срок беременности | Частота сердечных сокращений в ударах за минуту | ||
| Процентиль 5 | Процентиль 50 | Процентиль 95 | |
| 11 недель | 153 | 165 | 177 |
| 12 недель | 150 | 162 | 174 |
| 13 недель | 147 | 159 | 171 |
Венозный проток (ВП) – прямая коммуникация между пупочной веной и центральной венозной системой. При нормально развивающейся беременности кровоток в ВП представляет собой трехфазную кривую. Появление реверсного кровотока может говорить о наличии патологии плода.
Что показывает анализ крови
Результаты УЗИ сопоставляются с показателями ассоциированного с беременностью протеина А из плазмы матери (PAPP-A) и хорионическим гонадотропином человека (ХГЧ). Значения приведены в таблице:
| Срок беременности | ХГЧ в нг/мл | PAPP-A в мЕд/л |
| 11 недель | 17,4 – 130,4 | 0,46 – 3,73 |
| 12 недель | 13,4 – 128,5 | 0,79 – 4,76 |
| 13 недель | 14,2 – 114,7 | 1,03 – 6,01 |
Отличия от референсных значений может говорить о патологиях матери или плода.
Интерпретация обследования
Первое исследование оценивается только по совокупности всех показателей. Отдельно взятый параметр не может стать основанием для точного заключения. В протоколе фиксируются данные УЗИ, анализа на гормоны, отражаются риски вероятных заболеваний и комплексный медианный коэффициент MoM. Он указывает совокупное отклонение полученных результатов от средних значений. Коэффициент должен находиться в интервале от 0,5 до 2,5. Рассчитывается он специализированными программами.
Что может повлиять на результат
Современное диагностическое оборудование позволяет оценить более 15 параметров плода, построить его объемную реконструкцию для исследования органов на ранних периодах развития, рассчитать возможные риски с высокой точностью. Обращайтесь в хорошо оснащенные клиники и доверяйте специалистам с подтвержденной квалификацией.
Методы функциональной диагностики сердечно-сосудистых заболеваний
Пред — и послеоперационное ведение пациента врачом дерматокосметологом
Лучевая диагностика патологии желчного пузыря и желчевыводящих путей
УЗИ аппарат HM70A
Экспертный класс по доступной цене. Монокристальные датчики, полноэкранный режим отображения, эластография, 3D/4D в корпусе ноутбука. Гибкая трансформация в стационарный сканер при наличии тележки.
Введение
Натощак желчный пузырь содержит 30-80 мл желчи, но он может концентрировать печеночной желчи в 5-10 раз больше. При застое желчи в пузыре ее количество может увеличиваться. У женщин желчный пузырь в состоянии функционального покоя имеет несколько больший объем, чем у мужчин, но сокращается быстрее. С возрастом сократительная функция желчного пузыря снижается.
Ультрасонография является одним из самых информативных и доступных инструментальных методов диагностики заболеваний желчного пузыря 4.
Акустические свойства ультразвука позволяют выявлять мельчайшие эхогенные структуры, находящиеся в желчном пузыре.
Полипы в желчном пузыре имеются у 6% всего населения. В 80% случаев полипы в желчном пузыре отмечаются у рожавших женщин в возрасте после 30 лет. Так как полипы клинически себя никак не проявляют, диагностика их чаще всего случайна и происходит при проведении УЗИ у пациента по совершенно другим причинам 10.
Хотя причины появления полипов на стенках в желчного пузыря не установлены, а симптомы неочевидны, известны четыре типа таких образований. Наиболее часто по статистике в желчном пузыре у пациентов сегодня встречаются следующие типы [4, 5, 9].
Нередко врачи также ставят диагноз аденомы желчного пузыря. Так происходит потому, что это своего рода доброкачественная опухоль в виде полиповидного разрастания железистой ткани желчного пузыря больного.
Также следует отметить папиллому или полипоз желчного пузыря у некоторых пациентов. Такая папиллома представляет собой доброкачественную опухоль слизистой оболочки пузыря в виде различных по виду и структуре своеобразных папиллом или сосочковых разрастаний.
К самому распространенному типу относят так называемый холестериновый полип желчного пузыря, который представляет собой возвышение слизистой оболочки пузыря с холестриновыми отложениями на ней. Холестероз достаточно часто встречается среди пациентов, направленных на операцию с клиническим диагнозом «полипы» или «полипоз желчного пузыря», по некоторым данным от 42 до 95% случаев.
Ультрасонография является эффективным средством выявления полиповидной формы холестероза 8. Традиционной считается следующая сонографическая характеристика холестериновых полипов: неподвижные гиперэхогенные структуры, которые не дают акустической тени и прикрепляются к стенке желчного пузыря. Контуры таких образований, как правило, ровные, а размеры таких образований различны, чаще не превышают 10 мм (рис. 2).
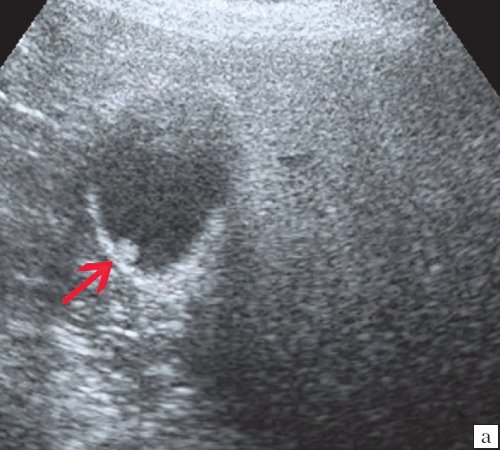
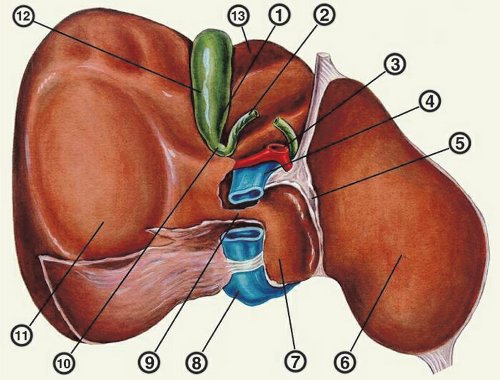
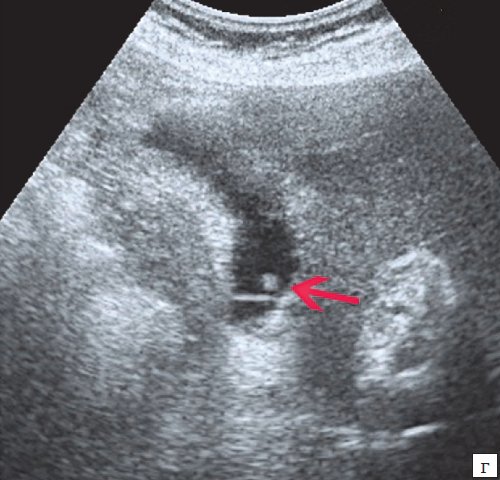
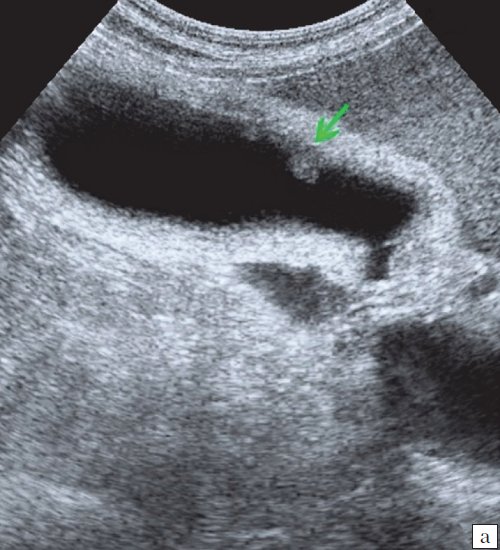
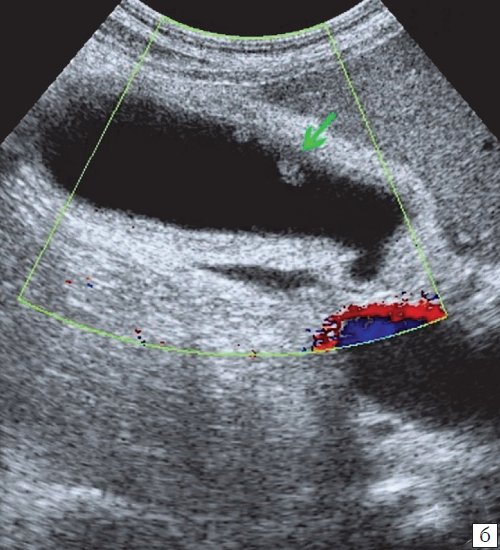
a) Одиночный полип в желчном пузыре (гиперэхогенное пристеночное неподвижное образование, с ровными контурами, без акустической тени).
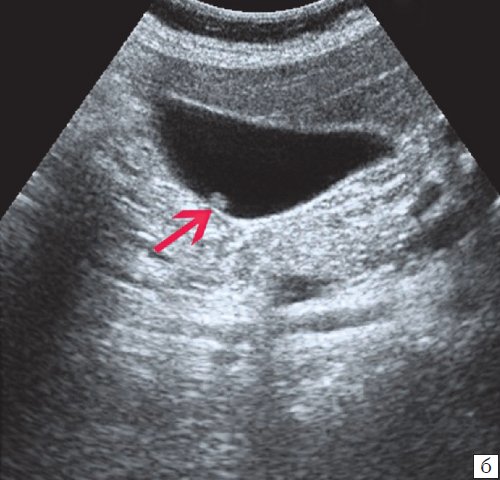
б) Одиночный полип в желчном пузыре.
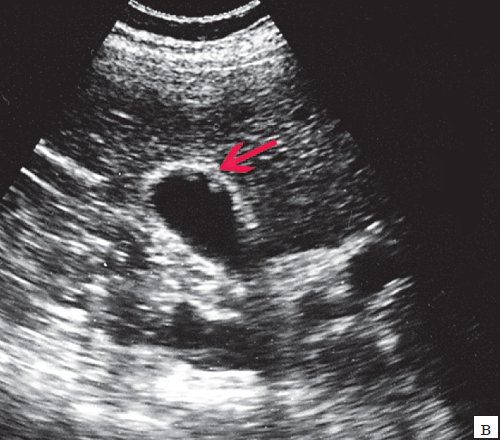
в) Полиповидно-сетчатая форма холестероза, полипы размерами до 5 мм, повышенной эхогенности.
г) Одиночный полип в желчном пузыре.
Однако, по некоторым данным, размеры холестериновых полипов могут быть более 20 мм. Кроме того, полипы больших размеров (в 7% от общего числа) могут иметь пониженную эхогенность и фестончатый контур.
Мелкие холестериновые включения, образующие диффузную сеточку в толще подслизистого слоя размерами 1-2 мм, выглядят как локальное утолщение или уплотнение стенки желчного пузыря и в некоторых случаях (см. рис. 2) вызывают реверберацию (эхографический симптом «хвост кометы»).
При распространенном холестерозе визуализируются множественные гиперэхогенные образования, дающие картину «земляничного» желчного пузыря (рис. 3).
а) Множественные полипы в желчном пузыре, картина «земляничного» желчного пузыря.
б) В режиме цветного допплеровского картирования кровоток не регистрируется.
Характер ножки полипа традиционно учитывается в онкологической практике как признак, ассоциированный со злокачественной природой образования. Вероятность возможной малигнизации больше, если у него имеется широкое основание, а не тонкая ножка. Однако необходимо принимать во внимание возможность ложноположительной диагностики широкого основания при полипах больших размеров из-за их ограниченной смещаемости в просвете желчного пузыря. Дрожание, напоминающее пламя свечи, наблюдается у полипов небольших размеров и вытянутой формы, и указывает на их тонкую ножку 9.
Существует два основных механизма образования желчных камней: печеночнообменный и пузырно-воспалительный. Печеночно-обменный механизм заключается в формировании желчных камней вследствие таких факторов, как несбалансированное питание с преобладанием в рацио не грубодисперсных животных жиров (свиного, бараньего, говяжьего) в ущерб растительным; нейроэндокринные нарушения, например, связанные с дисфункцией эндокринной системы возрастного характера и гипофункцией щитовидной железы; поражения печеночной паренхимы токсического и инфекционного генеза; гиподинамия и застой желчи. В результате печень продуцирует литогенную желчь, т. е. способную образовывать холестериновые или смешанные камни. При пузырно-воспалительном механизме желчные камни формируются под влиянием воспалительного процесса в желчном пузыре, приводящего к физико-химическим сдвигам в составе желчи (дисхолии). Изменение рН желчи в кислую сторону, характерное для любого воспаления, приводит к уменьшению защитных свойств коллоидов, в частности белковых фракций желчи, переходу мицеллы билирубина из взвешенного состояния в кристаллическое. При этом образуется первичный кристаллизационный центр с последующим наслоением других ингредиентов желчи, слизи, эпителия и др.
Клиническая картина желчнокаменной болезни многообразна [5-6, 10]. Условно выделяют хроническую болевую, хроническую рецидивирующую, диспептическую, стенокардитическую и ряд других клинических форм. Характерным ультразвуковым признаком конкремента в желчном пузыре является его акустическая тень. Такая тень возникает из-за высокой плотности камня по сравнению с мягкими тканями. Наличие или отсутствие тени помогает отличить камень от полипа желчного пузыря (рис. 4).
а) Одиночный конкремент желчного пузыря (подвижная гиперэхогенная структура, дающая четкую теневую дорожку).
Острая кишечная непроходимость у взрослых
Общая информация
Краткое описание
I. ВВОДНАЯ ЧАСТЬ
Название протокола: Острая кишечная непроходимость у взрослых.
Код протокола:
Код по МКБ 10:
К56.0 – паралитический илеус.
К56.1 – инвагинация кишечника.
К56.2 – заворот кишок.
К56.3 – илеус, вызванный желчным камнем.
К56.4 – другой вид закрытия просвета кишечника.
К56.5 – паралитический илеус.
К56.6 – другая и неуточнённая кишечная непроходимость.
К56.7 – паралитический илеус.
К91.3 – послеоперационная кишечная непроходимость.
Дата разработки протокола: 11.09.2013
Категория пациентов: взрослые пациенты от 18 лет
Пользователи протокола: врачи хирурги, анестезиологи, реаниматологи, визуальной диагностики, медицинские сёстры.
Острая кишечная непроходимость может быть вызвана многочисленными причинами, которые принято делить на предрасполагающие и производящие.
К предрасполагающим причинам относят: анатомо-морфологические изменения в желудочно-кишечном тракте – спайки, сращения, способствующие патологическому положению кишечника, сужение и удлинение брыжейки, приводящие к чрезмерной подвижности кишечника, различные образования, исходящие из стенки кишки, соседних органов или находящиеся в просвете кишечника, карманы брюшины и отверстия в брыжейке. К предрасполагающим причинам относят и нарушение функционального состояния кишечника в результате длительного голодания. В таких случаях прием грубой пищи может вызвать бурную перистальтику и кишечную непроходимость («болезнью голодного человека»). Роль предрасполагающих причин сводится к созданию избыточной подвижности петель кишечника, или, наоборот, его фиксации. В результате кишечные петли и их брыжейка смогут занимать патологической положение, при котором пассаж кишечного содержимого нарушается.
Примечание: в данном протоколе используются следующие классы рекомендаций и уровни доказательств:
Уровень I – Доказательства, полученные в ходе по крайней мере от одного должным образом разработанного случайного контролируемого исследования или мета-анализа
Уровень II – Доказательства, полученные в ходе по крайней мере от одного хорошо разработанного клинического испытания без надлежащей рандомизации, от аналитического когортного или исследования типа случай-контроль (предпочтительно из одного центра) или от полученных драматических результатов в неконтролируемых исследованиях.
Уровень III – Доказательства, полученные от мнений авторитетных исследователей на основе клинического опыта.
Класс А – Рекомендации, которые были одобрены по согласованию по крайней мере 75% процентов мультисекторной группы экспертов.
Класс B – Рекомендации, которые были несколько спорны и не встречали согласие.
Класс C – Рекомендации, которые вызвали реальные разногласия среди членов группы.
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
13-15 октября, Алматы, «Атакент»
600 брендов, более 150 компаний-участников из 20 стран.
Новинки рынка стоматологии. Цены от производителей
Классификация
Клиническая классификация
В Казахстане и других странах СНГ наиболее распространены следующие классификации:
По Оппелю В.А.
1. Динамическая непроходимость (паралитическая, спастическая).
2. Гемостатическая непроходимость (тромбофлебетическая, эмболическая).
3. Механическая с гемостазом (ущемление, поворот).
4. Механическая простая ( закупорка, перегиб, сдавление).
По Чухриенко Д.П.
по происхождению
1. врожденную
2. приобретенную
по механизму возникновения:
1. механическая
2. динамическая
по наличию или отсутствию расстройств кровообращения:
1. обтурационная
2. странгуляционная
3. сочетанная
по клиническому течению:
1. частичная
2. полная (острая, подострая, хроническая, рецедивирующая)
По морфологической природе:
динамическая
1. паралитическая
2. спастическая.
механическая
1. странгуляционная
2. обтурационная
3. смешанная
По уровню обструкции
1. тонкокишечная (высокая)
2. толстокишечная (низкая)
По стадиям:
1 стадия (до12-16 часов) – нарушение кишечного пассажа
2 стадия (16-36 часов) – стадия острых расстройств внутристеночной кишечной гемоциркулляции
3 стадия (свыше 36 часов) стадия перитонита.
Диагностика
II. МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
Перечень основных и дополнительных диагностических мероприятий:
1. Общий анализ крови
2. Общий анализ мочи
3. Определение глюкозы крови
4. Микрореакция
5. Определение группы крови
6. Определение резус-фактора
7. Определение билирубина
8. Определение АСТ
9. Определение АЛТ
10. Определение тимоловой пробы
11. Определение креатинина
12. Определение мочевины
13. Определение щелочной фофатазы
14. Определение общего белка и белковой фракции
15. Определение амилаза крови
16. Коагулограмма (протромбиновый индекс, время свёртываемости, время кровотечения, фибриноген, АЧТВ)
17. Кровь на ВИЧ
18. ЭКГ
19. Обзорная рентгенография органов брюшной полости
20. Обзорная рентгенография органов грудной клетки
21. УЗИ органов брюшной полости
22. Компьютерная томография органов брюшной полости
23. Диагностическая лапароскопия
24. Контрастное исследование желудочно-кишечного тракта
25. Консультация реаниматолога
26. Консультация анестезиолога
27. Консультация онколога
28. Консультация терапевта
Диагностические критерии
Жалобы и анамнез
ОКН характеризуется многообразием предъявляемых жалоб больными, однако главными и наиболее достоверными из них можно назвать следующую триаду жалоб: боли в животе, рвота, задержка стула и газов [1, 3, 6, 7, 8, 9].
1. Боли в животе обычно возникают внезапно, вне зависимости от приема пищи, в любое время суток, без предвестников. Для кишечной непроходимости наиболее характерны схваткообразные боли, что связано с перистальтикой кишечника. Четкой локализации болей в каком – либо отделе брюшной полости не отмечается. При обтурационной кишечной непроходимости боли вне схваткообразного приступа обычно исчезают. В случае странгуляционной кишечной непроходимости боли бывают стойкими, резко усиливающимися во время приступа. Стихают боли лишь на 2-3 сутки, когда наступает истощение перистальтики кишечника. Прекращение болей при наличии кишечной непроходимости служит плохим прогностическим признаком [1, 7]. При паралитической кишечной непроходимости боли постоянные, распирающие, умеренной интенсивности.
2. Рвота вначале носит рефлекторный характер, при продолжающейся непроходимости развивается рвота застойным содержимым, в позднем периоде при развитии перитонита рвота становится неукротимой, беспрерывной, а рвотные массы имеют каловый запах. Чем выше непроходимость, чем выраженнее рвота. В промежутках между рвотой больной испытывает тошноту, его беспокоит отрыжка, икота. При низкой локализации препятствия наблюдается рвота с большими промежутками.
3. Задержка стула и газов наиболее выражена при низкой кишечной непроходимости. При высокой кишечной непроходимости в начале заболевания у некоторых больных может быть стул. Это происходит за счет опорожнения кишечника, расположенного ниже препятствия. При кишечной непроходимости на почве инвагинации из заднего прохода иногда наблюдаются кровянистые выделения из заднего прохода, что может служить причиной диагностической ошибки, когда ОКН ошибочно принимают за дизентерию [7, 8].
Анамнез заболевания: необходимо обращать внимание на прием обильного количества пищи (особенно после голодания), появление болей в животе при физической нагрузке, сопровождающейся значительным повышением внутрибрюшного давления, жалобы на снижение аппетита и явления кишечного дискомфорта (периодически появление болей и вздутие живота; запоры, сменяющиеся диареей; патологические примеси в кале);
Анамнез жизни имеет также важно значение. Перенесенные операции на органах брюшной полости, открытые и закрытые травмы живота, воспалительные заболевания нередко являются предпосылкой возникновения кишечной непроходимости.
Физикальные обследования:
1. Общее состояние больного может быть средней тяжести или тяжелым в зависимости от формы, уровня или времени, прошедшего от начала ОКН.
2. Температура в начальный период заболевания не повышается. При странгуляционной непроходимости, когда развиваются коллапс и шок, температура снижается до 36°С. В дальнейшем, при развитии перитонита, температура повышается до субфебрильной.
3. Пульс в начале заболевания не изменяется, при нарастании явлений непроходимости появляется тахикардия. Обращает на себя внимание расхождение между низкой температурой и частым пульсом [9].
4. Кожные покровы и слизистые: по их оценке можно судить о степени обезвоживания: сухость кожных покровов и слизистых, снижение тургора кожи, сухость языка.
6. Пальпация живота болезненна. Напряжение мышц брюшной стенки нет. Симптом Щеткина-Блюмберга отрицательный. При странгуляционной непроходимости бывает положительным симптом Тевенара – резкая болезненность при надавливании на два поперечных пальца ниже пупка по средней линии, то есть там, где проходит корень брыжейки. Этот симптом особенно характерен для заворота тонкого кишечника. Иногда при пальпации живота иногда удается определить опухоль, тело инвагината, воспалительный инфильтрат, послужившие причиной непроходимости. При легком сотрясении брюшной стенки можно услышать «шум плеска» – симптом Склярова. Этот симптом указывает на наличие перерастянутой паретичной петли кишки, переполненной жидким и газообразным содержимым [1, 6, 7].
7. Перкуссия живота выявляет ограниченные участки зон притупления, что соответствует местоположению петли кишки, наполненной жидкостью и непосредственно прилегающей к брюшной стенке. Эти участки притупления не меняют своего положения при поворотах больного, чем и отличаются от свободного выпота. Притупление перкуторного звука выявляется также над опухолью, воспалительным инфильтратом или инвагинатом кишки.
9. Ректальное пальцевое исследование может выявить опухоль прямой кишки, каловый завал, головку инвагината и следы крови. Ценным диагностическим признаком, характерным для низкой кишечной непроходимости, является атония сфинктера и баллонообразное вздутие пустой ампулы прямой кишки (симптом Обуховской больницы) и малая вместимость дистального отдела кишечника (симптом Цэге-Мантефейля). При этом в прямую кишку удается ввести не более 500 – 700 мл воды, при дальнейшем введении вода будет вытекать обратно [1, 8].
Лабораторные исследования:
— общий анализ крови (могут наблюдаться лейкоцитоз, палочкоядерный сдвиг, ускорение СОЭ, признаки анемии);
— коагулограмма (могут наблюдаться признаки гиперкоагуляции);
— биохимический анализ крови (нарушение водно-электролитного и кислотно-щелочного равновесия).
Инструментальные исследования
2. Ультразвуковое исследование брюшной полости
При механической кишечной непроходимости:
— расширение просвета кишки более 2 см с наличием феномена «секвестрации жидкости» в просвет кишки;
— утолщение стенки тонкой кишки более 4 мм;
— наличие возвратно-поступательных движений химуса по кишке;
— увеличение высоты керкринговых складок более 5 мм;
— увеличение расстояния между керкринговыми складками более 5 мм;
— гиперпневматизация кишечника в приводящем отделе
при динамической кишечной непроходимости:
— отсутствие возвратно-поступательных движений химуса по кишке;
— феномен секвестрации жидкости в просвет кишки;
— невыраженный рельеф керкринговых складок;
— гиперпневматизация кишечника во всех отделах [2].
3. Контрастное исследование желудочно-кишечного тракта применяется реже и только при затруднениях в диагностике кишечной непроходимости, стабильном состоянии больного, интерметтирующем характере кишечной непроходимости. Больному дают выпить 50 мл бариевой взвеси и проводят динамическое исследование пассажа бария. Задержка его до 4-6 часов и более дает основание заподозрить нарушение двигательной функции кишечника.
4. Диагностическая лапароскопия (применяется только при малой информативности предыдущих методов инструментальной диагностики).
Показания для консультаций специалистов:
— Реаниматолог: для определения показаний для лечения больного в условиях реанимационного отделения, для согласования тактики ведения больного в части ликвидации нарушений водно-электролитного и кислотно-щелочного равновесия.
— Анестезиолог: для определения типа анестезия при необходимости оперативного вмешательства, а также согласование тактики ведения предоперационного периода.
— Онколог: при подозрении на опухоли брюшной полости, ставшие причиной ОКН.
— Терапевт: выявление сопутствующей соматической патологии, которая осложняет течение ОКН, а также может осложнить течение операции и послеоперационный период.
Дифференциальный диагноз
Лечение
Цели лечения: ликвидация кишечной непроходимости; полное восстановление пассажа кишечного содержимого; ликвидация причины, вызвавшей ОКН (по возможности).
Тактика лечения
Медикаментозное лечение:
| Фармакологическая группа | МНН | Дозировки, кратность введения, путь введения |
| Спазмолитики | Дротаверин | 0,04/2 мл р-р * 3 р/д (в/м или в/в) |
Перечень основных лекарственных средств:
1. Спазмолитические препараты
2. Антибактериальные препараты (цефалоспорины II-III поколения)
3. Анальгетические препараты
4. Кристаллоидные растворы для инфузии
Профилактические мероприятия
В целях профилактики острой кишечной непроходимости необходимо вовремя находить и удалять опухоли кишечника. К профилактике кишечной непроходимости также относится борьба с запорами. Пища больного должна содержать продукты, богатые на содержание клетчатки и растительного масла. Животные жиры требуют резкого ограничения.
Требуется исключить из своего рациона: творог, сыр, печенье, сушки. Рис можно употреблять в сочетании с различными овощами. Также необходим прием слабительных средств (бисакодил таблетки и суппозитории, трава сенны). Необходимо, чтобы стул был не менее одного раза в три дня, а если его нет, то требуется увеличение дозы слабительного препарата, его замена, очистительная клизма или срочная консультация врача-хирурга.
Профилактика осложнений у оперированных больных с диагнозом «острая кишечная непроходимость» сводится в адекватном и правильном ведении послеоперационного периода (см. п. 15.6).
Индикаторы эффективности лечения:
1. Устранение симптомных проявлений заболевания (отсутствие болей в животе, отсутствие тошноты и рвоты);
2. Положительная рентгенологическая динамика;
3. Восстановление проходимости кишечника (регулярное отхождение стула и газов через искусственные (колостома, илеостома) или естественные отверстия;
4. Заживление операционной раны первичным натяжением, отсутствие признаков воспаления послеоперационной раны.
Диагностика и лечение рака прямой кишки в Юсуповской больнице
Рак прямой кишки – злокачественное новообразование, связанное с повышенным риском местного рецидива. Большая сложность объясняется непростыми анатомическими особенностями прямой кишки:
Это ухудшает прогноз после лечения заболевания.
Врачи Юсуповской больницы проводят диагностику рака прямой кишки, ранних метастазов и рецидивов с помощью новейшей аппаратуры ведущих мировых производителей. Онкохирурги выполняют радикальные операции, иссекают опухоль в пределах здоровых тканей.
После операции назначают новейшие химиотерапевтические препараты, которые уничтожают раковые клетки. Первичный очаг и пути метастазирования облучают с помощью современных аппаратов для радиотерапии. Всё это в комплексе позволяет улучшить прогноз выживаемости после операции по поводу рака прямой кишки 2,3 и 4 стадии.
Особенности лечения рака прямой кишки
Врачи Юсуповской больницы проводят мультидисциплинарное лечение рака прямой кишки. Проводится радикальное или местное лечение, выполняются сфинктеросохраняющие операции или брюшно-промежностная экстирпация прямой кишки с открытого доступа или лапароскопическим путём. Для прогноза заболевания имеют значение следующие факторы:
Хирурги Юсуповской больницы имеют большой опыт выполнения оперативных вмешательств на прямой кишке, виртуозно выполняют все разработанные сегодня операции. До начала хирургического лечения проводится комплексное обследование пациента. Оно включает анализ жалоб и истории развития болезни, пальцевое исследование прямой кишки, ректороманоскопию. Для определение регионарных и отдалённых метастазов выполняют ультразвуковое исследование, компьютерную и магнитно-резонансную томографию.
В соответствии с рекомендациями Национального Института Рака проводят предоперационную или послеоперационную лучевую терапию, в основном в комбинации с химиотерапевтическим лечением. Она улучшает локальный контроль над опухолью, несмотря на то, что не всегда увеличивает общую выживаемость при раке прямой кишки.
Для того чтобы улучшить прогноз выживаемости при раке прямой кишки в Юсуповской больнице во время операции определяют проксимальную границу прямой кишки (место слияния теней). Эндоскопическое определение наиболее важно для назначения неоадъювантной терапии в случае, если опухоль находится на расстоянии 15 см над краем анального канала по отметкам на ригидном ректоскопе.
Классификация рака прямой кишки tnm
В России принята TNM классификация рака прямой кишки. Выделяю 4 стадии рака прямой кишки.
Критерий Т обозначает «опухоль». Тx устанавливают в том случае, когда недостаточно данных для оценки первичной опухоли. Tis – это преинвазивная карцинома. При T1опухоль распространяется в подслизистый слой стенки кишки. Т2 обозначает, что новообразование распространяется на мышечный слой прямой кишки и не прорастает её стенку. Если опухоль прорастает все слои стенки кишки с распространением в жировую клетчатку без поражения соседних органов, онкологи применяют обозначение Т3. Для новообразований, расположенных в верхнеампулярном отделе прямой кишки и ректосигмоидном отделах ободочной кишки (покрытых брюшиной), символ Т3 характеризует распространение раковой опухоли до субсерозного слоя. Она не прорастают серозную оболочку.
На стадии Т4 новообразование прорастает в окружающие органы и ткани или серозную оболочку при локализации в верхнеампулярном отделе прямой кишки и ректосигмоидном отделах ободочной кишки (покрытых брюшиной). Т4а обозначает прорастание висцеральной брюшины, Т4б – прорастание в другие органы.
Критерий N – лимфатический узел. Nх говорит о том, что недостаточно данных для оценки регионарных лимфатических узлов. Если нет поражения регионарных лимфатических узлов, состояние обозначают как N0. При N1имеются метастазы в 1-3 регионарных лимфатических узлах:
Критерий M обозначает наличие метастазов:
Нулевая стадия рака прямой кишки устанавливается в случае Тis, N0, M0. Первая стадия определяется как T, N0, M0. При IIA стадии ситуация выглядит как Т3, N0, M0, IIB –Т4а, N0, M0, IIC – Т4б, N0, M0. Рак прямой кишки 3 стадия имеет 3 варианта течения:
Диагноз «рак прямой кишки 4 степени» устанавливается при любом размере опухоли независимо от количества поражённых лимфатических узлов в случае наличия отдалённых метастазов. Для адекватного стадирования опухоли в Юсуповской больнице проводят исследование как минимум 12-15 лимфоузлов в удалённом препарате, но меньшее число после облучения.
Симптомы рака прямой кишки
На начальной стадии заболевания рак прямой кишки имеет бессимптомное течение. Его выявляют во время рутинного обследования. Наиболее частыми признаками злокачественной опухоли прямой кишки являются следующие симптомы:
Боль в прямой кишке полости таза является грозным симптомом. На поздней стадии развития рака прямой кишки возникают осложнения:
Лимфоваскулярная инвазия, периневральная инвазия, наличие депозитов опухоли вне лимфоузлов относятся к отрицательным прогностическим факторам. При раке прямой кишки 4 стадии продолжительность жизни небольшая.
Прогноз выживаемости при раке прямой кишки
Определение стадии рака прямой кишки имеет первостепенное значение для выработки показаний к оперативному вмешательству, поскольку лучшего способа лечения не существует. Для локализованных опухолей вероятность излечения выше. Вовлечение в патологический процесс регионарных лимфатических узлов резко снижает благоприятный прогноз. Важными показателями являются размер новообразования и глубина его прорастания. Некоторые факторы взаимосвязаны: чем больше размер опухоли, тем более вероятен риск метастазирования в регионарные лимфоузлы.
При выявлении рака прямой кишки первой стадии, или стадии IIA вероятность полного излечения составляет 90%. При стадии II B прогноз пятилетнее выживаемости ухудшается до 70%. Если диагностирован рак прямой кишки 3 стадия, излечиваются 50% больных. Даже при наличии опухоли четвёртой стадии имеют шанс излечиться от 10% до 20% больных. Если вторичные очаги поражения образовались в лёгких или костях, прогноз будет чрезвычайно неблагоприятным. Рак прямой кишки обычно распространяется сначала в лимфатические узлы, а затем – в печень. Если в печени определяется единственный метастаз, его удаляют хирургическим путём. Когда у пациента выявлена высокодифференцированная аденокарцинома прямой кишки, прогноз оптимистичный.
Лечение рака прямой кишки
Когда диагноз и стадия рака прямой кишки не вызывают сомнений, профессора и врачи высшей категории на заседании экспертного совета принимают решение о тактике лечения. Применяют хирургическое лечение, облучение новообразования до и после операции. Химиотерапию проводят в соответствии с международными общепринятыми стандартами.
Пациентам Юсуповской больницы доступны все самые современные методы лечения рака прямой кишки, включая такие, как брюшно-промежностная экстирпация прямой кишки лапаротомическим или лапароскопическим методом, колостомия, хирургическое удаление метастазов в печени.
Брюшно-промежностная экстирпация прямой кишки выполняется под общей анестезией. Сначала хирург-онколог выполняет рассечение передней брюшной стенки и производит отсечение сигмовидной кишки на 10-15 см выше новообразования. Затем нисходящий участок сигмовидной кишки выводит наружу и подшивает к брюшной стенке, формируя колостому для последующего вывода каловых масс.
Затем накладывает швы на рану и выполняет доступ через промежность. Сначала выполняется круговой разрез тканей вокруг заднего прохода, потом удаляет прямую кишку и окружающие её ткани. Промежность наглухо ушивает. После операции прогноз пятилетней выживаемости хороший.
Колостомия – операция, при которой формируется специальное отверстие, которое называется колостома. Через него из организма удаляются каловые массы. Оперативное вмешательство производится после удаления прямой кишки. При необходимости, выполняется пластика прямой кишки. Операции проводят (в абсолютном большинстве случаев) малотравматичным лапароскопическим методом.
Паллиативные резекции выполняются при наличии отдалённых метастазов рака. Они помогают предупредить в послеоперационном периоде такие осложнения, как кровотечения из распадающейся опухоли, выраженный болевой синдром, зловонные, раздражающие ткани кишечные выделения. Тем самым улучшается качество жизни запущенных онкологических больных.
Химиотерапия является одним из методов комбинированного лечения рака прямой кишки. Пациентам проводят адъювантную (дополнительную) химиотерапию после операции при поражении опухолью регионарных лимфатических узлов. Иммуномодулирующая терапия заключается в назначении пациентам после хирургического лечения при отсутствии метастазов в регионарных лимфоузлах цитостатика и иммуномодулятора.
Лучевая терапия используется в качестве предоперационного метода лечения рака прямой кишки (для уменьшения стадийности рака). Облучение проводят после операции для сокращения частоты рецидивов. Радиотерапию используют в качестве основного метода лечения местнораспространённого неоперабельного рака прямой кишки.
Полную информацию о диагностике и лечении этого вида рака Вам предоставят специалисты контакт центра. Звоните по телефону Юсуповской больницы, клиника работает ежедневно и круглосуточно. Вас запишут на консультацию онколога в удобное для вас время.
Как выглядит выпавшая кишка 4 27 1 689 1 192
Смертность от онкологических заболеваний занимает второе место после болезней сердечно-сосудистой системы. В 2017 г. в России выявлено почти 541 тыс. онкобольных, а умерло 290,7 тыс., что составило 15,9% в общей структуре смертности [1, с. 3].
В последние годы отмечается тенденция к снижению заболеваемости раком желудка (РЖ), тем не менее в структуре заболеваемости злокачественными новообразованиями населения России РЖ занимает 4-е место у мужчин (7,6%) и 5-е место у женщин (4,7%) [1, с. 9, 10]. Пик заболеваемости приходится на возраст старше 50 лет. Злокачественные новообразования желудка занимают вторую позицию в структуре смертности у мужчин и женщин. Ежегодно в РФ регистрируют около 36 тыс. новых случаев РЖ, и более 34 тыс. больных умирает от этого заболевания. Этиология заболевания до конца не выяснена [2, с. 6].
Имеется связь возникновения патологии с определенными факторами риска. Их можно разделить на немодифицируемые: пол (мужчины страдают чаще), возраст (по мере увеличения возраста увеличивается частота возникновения РЖ), генетическая предрасположенность (5–10% пациентов, страдающих РЖ, имеют отягощенный семейный анамнез); и модифицируемые: инфекция Helicobacter Pylori (HP), характер рациона, ожирение, курение, алкоголь, профессиональная деятельности [3, с. 4-6].
В настоящее время установлено, что почти 90% случаев РЖ в мире обусловлено инфицированием бактерией HP. При этом средства лечения HP-инфекции существуют, но широко не применяются из-за недостатка подтвержденных данных эффективности в профилактике рака желудка и высокой стоимости [5, с. 22]. К возникновению РЖ могут привести фоновые заболевания: хронический атрофический гиперпластический гастрит, аденоматозные полипы, пернициозная анемия, состояния после резекции желудка, болезнь Менетрие [2, с. 6]. Различают три гистологических типа РЖ (по Lauren, 1965 г.): кишечный, диффузный, смешанный. При диффузном раке опухоль представлена слабоорганизованными группами или одиночными клетками с большим содержанием муцина (перстневидные клетки). Для данного типа характерен диффузный инфильтративный рост [2, с. 7].
Перстневидно-клеточный рак желудка содержит не менее половины клеток с признаками внутриклеточного образования слизи. Скапливающаяся в цитоплазме слизь сдвигает ядро к периферии, и клетка приобретает сходство с перстнем [6, с. 589]. Согласно результатам клинических наблюдений неблагоприятный прогноз при диффузном раке желудка связывают с низкой выявляемостью на ранних стадиях, быстрым течением, более злокачественным потенциалом опухолевых клеток и ранним метастазированием [7].
Приводим случай летального исхода пациента с перстневидно-клеточным раком желудка, диагностированным на последней стадии.
Клиническое наблюдение. Пациент В., 28 лет, поступил в гастроэнтерологическое отделение клинической медико-санитарной части г. Перми 14.11.2017 г. с жалобами на постоянные боли в области правого фланка живота, преимущественно в нижней части; интенсивные боли в правом подреберье и правом боку при глубоком дыхании; тошноту, рвоту желчью, вздутие живота, Также пациента беспокоили отсутствие аппетита, отвращение к пище, жидкий стул 2–3 раза в сутки без примесей. Отмечались выраженная общая слабость, повышение температуры тела до 37,4°С. За 1 месяц больной похудел на 13 кг.
Анамнез. В начале сентября 2017 г. больной получал терапию антибактериальными и нестероидными противовоспалительными препаратами (НПВП) по назначению стоматолога (после экстракции зуба) в течение 7 дней. В начале октября 2017 г. были вновь назначены антибактериальная терапия и НПВП по поводу гайморита. На фоне приема препаратов появились боли в эпигастрии, изжога, неустойчивый стул. Больной обратился в поликлинику по месту жительства, где обследовался у участкового терапевта. 7 октября 2017 г. выполнена фиброгастродуоденоскопия (ФГДС), на которой выявлены множественные язвы желудка (6 дефектов), язва двенадцатиперстной кишки (ДПК) в стадии эпителизации, застойная гастропатия, дуоденогастральный рефлюкс. Уровень антител к HP составил 1,44. Получал терапию ингибиторами протонной помпы (ИПП), антацидами без эффекта – сохранялись тошнота и абдоминальный болевой синдром с локализацией в эпигастрии.
Участковым терапевтом дано направление на экстренную госпитализацию в терапевтическое отделение городской больницы с диагнозом: Множественные язвы желудка и язва луковицы ДПК, ассоциированные с HP. Гастринома? Синдром Золлингера–Эллиссона?, где больной находился с 12.10.2017 г. по 24.10.17 г. При обследовании в общем анализе крови (ОАК) от 13.10.2017 г.: гемоглобин – 157 г/л; умеренное повышение лейкоцитов до 11х10 9 /л; ускоренная скорость оседания эритроцитов (СОЭ) – 40 мм/час. В биохимическом анализе крови от 13.10.2017 г. общий белок, амилаза, холестерин, печеночные тесты, электролиты крови в пределах нормальных значений. На ультразвуковом исследовании органов брюшной полости (УЗИ) от 13.10.2017 г. выявлены признаки диффузных изменений видимых участков поджелудочной железы. Кал на скрытую кровь – слабоположительный.
23.10.2017 г. выполнена повторная ФГДС: слизистая желудка диффузно гиперемирована с выраженным отеком, утолщена, сосудистый рисунок смазан. Слизистая оболочка в области привратника отечна, гиперемирована. По всем стенкам множественные точечные лимфоидные высыпания. Заключение: Диффузный катаральный гастрит выраженной степени активности. Дуоденогастральный рефлюкс. Диффузный катаральный бульбит выраженной степени активности. Косвенные признаки панкреатита. Гистологическое исследование не проводилось.
В стационаре по результатам обследований был поставлен диагноз: Язвенная болезнь желудка, луковицы ДПК. Множественные острые язвы желудка в активной стадии. НПВП-ассоциированная гастропатия. Язва луковицы ДПК в стадии эпителизации. Больной получал терапию спазмолитиками, ИПП 40 мг в сутки, антацидами.
На фоне лечения отмечалась положительная клиническая и эндоскопическая динамика в виде уменьшения болевого синдрома и эпителизации язвенных дефектов. Пациент был выписан из стационара с рекомендациями продолжить прием ИПП в дозе 40 мг в сутки и явиться на прием к участковому терапевту.
После выписки боли в эпигастрии усилились, появилась острая боль справа в боку в области ребер. Участковый терапевт назначил прием прокинетика, антацидных препаратов, НПВП внутримышечно (в/м) № 3. 4.11.2017 г. у пациента внезапно возникла острая боль в области верхнего левого фланка живота и межреберьях, связанная с дыханием. Больной обратился в приемное отделение клинической больницы, где был поставлен диагноз: Межреберная невралгия. Проведена терапия НПВП в/м, и больной был отпущен домой под наблюдение невролога и терапевта с рекомендациями приема НПВП. Далее по назначению гастроэнтеролога поликлиники принимал висмута трикалия дицитрат, спазмолитики, даларгин без эффекта – сохранялись абдоминальный болевой синдром, неустойчивый стул; также появились выраженное вздутие живота, рвота, отвращение к пище, прогрессирующее похудание. 13.11.2017 г. выполнена ректороманоскопия: стенка прямой кишки с трудом расправлялась воздухом, с эрозиями, утолщенными складками, сосудистый рисунок смазан. Заключение: эрозивно-катаральный проктосигмоидит.
14.11.2017 г. пациент был экстренно госпитализирован в гастроэнтерологическое отделение клиники для дальнейшего обследования и лечения.
Из анамнеза жизни известно, что пациент рос и развивался соответственно возрасту. Курил в течение 8 лет по 10 сигарет в день. Профессиональных вредностей не было. Со слов больного, ранее лечился по поводу мочекаменной болезни. Наследственность по заболеваниям органов пищеварения не отягощена.
При физическом исследовании обращала на себя внимание бледность кожных покровов с сероватым оттенком. Кожа чистая, отеков не отмечалось. Пульс – 92 удара в минуту, ритмичный. Тоны сердца ясные, ритм правильный. Дополнительные шумы не выслушивались. Дыхание везикулярное, ослаблено в нижних отделах, хрипы не выслушивались. Перкуторный звук несколько притуплен в нижних отделах легких. ЧДД – 16 в минуту.
Язык обложен бело-желтым налетом у корня, влажный. Живот плотный, увеличен за счет вздутия и асцита; пальпация резко болезненная в эпигастрии, в области правого фланка живота, по ходу толстой кишки. Ординаты Курлова 10х8х7 см. Стул оформленный, чередующийся с кашицеобразным, без патологических примесей, 1–2 раза в сутки. Со стороны почек и мочевого пузыря без видимой патологии.
Результаты лабораторно-инструментальных исследований представлены ниже.
ОАК: эритроциты 4,7х10 9 /л, гемоглобин 140 г/л, среднее содержание гемоглобина (ССГ) 29%, тромбоциты 307х10 9 /л, лейкоциты 8,4х/л, палочкоядерные нейтрофилы 7%, сегментоядерные нейтрофилы 75%, лимфоциты 15%, моноциты 3%, повышение СОЭ до 43 мм/час.
ОАМ: цвет – желтый, мутная, pH 6,0, умеренная протеинурия 0,39 г/л, лейкоциты 4–6 в поле зрения (п/з), эритроциты 0–1 в п/з, эпителий 2–3 в п/з, слизь +.
Биохимический анализ крови от 15.11.2017 г.: глюкоза 4,8 ммоль/л, Ca 2,29 ммоль/л, AСТ/АЛТ 16/18 Ед/л, ГГТП 84 Ед/л, ЩФ 285 Ед/л, общий белок 54 г/л, альбумины 27 г/л, билирубин общий 12 мкмоль/л, прямой 4,1 мкмоль/л, холестерин общий 3,7 мкмоль/л, калий 4,5 ммоль/л, натрий 134 ммоль/л, креатинин 51 ммоль/л, резкое повышение С-реактивного белка (СРБ) 105 мг/л, снижение железа сыворотки до 4,5 мкмоль/л, повышение общей железосвязывающей способности сыворотки до 75, незначительное повышение прокальцитонина до 0,2 нг/мл. При форезе белков выявлены снижение альбумина до 37,95% и повышение α1-глобулинов до 8,77%, α2-глобулинов до 13,28%, β-глобулинов до 18,5 3%, γ-глобулин 21,47%.
Коагулограмма от 15.11.2017 г.: протромбиновое время 14,9 секунд (11–15 секунд), тромбиновое время – 17,2 секунд, активированное частичное протромбиновое время – 28 секунд (24–35 секунд), резкое повышение фибриногена до 9,56 г/л.
Копрограмма от 16.11.2017 г.: консистенция жидкая, цвет темно-коричневый, переваренные мышечные волокна 0–1–2 в п/з, неизмененные мышечные волокна 0–1 в п/з, форменные элементы крови 0–1 в п/з, лейкоциты 10–20 в п/з, эпителий плоский – единичный в п/з, нейтральных жиров нет, жирных кислот нет, крахмал внеклеточно скудно, йодная флора +, детрит +++.
ФГДС от 14.11.2017 г.: складки желудка гипертрофированные, отечные. Слизистая желудка ярко гиперемирована, плотная при инструментальной пальпации, ранимая при контакте с линейными рубцами неправильной формы. Луковица ДПК деформирована, рыхлая с увеличенными эрозированными фолликулами, на верхушках – фибрин. Заключение: Болезнь Крона? Дуоденогастральный рефлюкс. Косвенные признаки панкреатита. Выполнена биопсия.
Результаты патогистологического исследования слизистой желудка (20.11.2017 г.): в слизистой оболочке пилородуоденальной области очаговое скопление крупных клеток округлой и овальной формы, со светлой слизьсодержащей цитоплазмой, периферически расположенными уплощенными ядрами, единичные клетки с гиперхромными ядрами, скудной цитоплазмой. Диагноз: недифференцированный аденогенный рак с образованием перстневидных клеток.
16.11.2017 г. выполнена КТ органов брюшной полости. Выявлен выпот в реберно-диафрагмальные синусы с обеих сторон. Желудок в области тела и антрального отдела с неравномерно утолщенными стенками до 0,8 см. Большой сальник в области эпигастрия уплотнен, с узловыми образованиями. В брюшной полости большое количество свободного выпота. Заключение: Признаки двустороннего гидроторакса, инфильтративных изменений стенок желудка. Большой сальник в эпигастральной области уплотнен с узловыми образованиями (канцероматоз брюшины). Асцит. Аденопатия гепатодуоденальных лимфатических узлов.
На рентгеноскопии пищевода, желудка, ДПК с бариевой взвесью диагностировано стойкое сужение просвета тела, синуса, выходного отдела желудка (рис. 1) с неровными фестончатыми контурами, атипичным рельефом слизистой (рис. 2). Заключение: Рентгенологические признаки инфильтративного поражения желудка.
Рис. 1. Рентгенологическое исследование желудка пациента В., 28 лет: сужение просвета тела, синуса, выходного отдела желудка
Рис. 2. Рентгенологическое исследование желудка пациента В., 28 лет: неровность и фестончатость контуров, атипичный рельеф слизистой
В условиях стационара проводилась инфузионная, антибактериальная, спазмолитическая, обезболивающая терапия. Амитриптилин 6,25–12,5 мг на ночь. Больной выписан из отделения 22.11.2017 г. с диагнозом:
Основной: Недифференцированный аденогенный рак выходного отдела желудка IV ст. Сопутствующий: Эрозивно-катаральный проктосигмоидит.
Осложнения: Канцероматоз брюшины. Аденопатия гепатодуоденальных лимфоузлов. Асцит. Двусторонний гидроторакс. Дефицит железа.
Пациенту выдано направление в онкологический диспансер. Даны рекомендации приема Амитриптилина 25 мг на ночь; Прегабалина 75 мг 1 раз в день; Нейробиона по 1 табл. 3 раза в день.
С 23.11.2017 г. по 30.11.2017 г. пациент находился в краевом онкологическом диспансере, где был подтвержден диагноз: Злокачественное новообразование желудка (ЗНО) IV ст. Т4NxMx».
Проведен 1 курс полихимиотерапии (ПХТ). После выписки, несмотря на проводимое лечение, состояние пациента прогрессивно ухудшалось. 18.12.2017 г. проведена эвакуация 10 литров асцитической жидкости в условиях стационара. 20.12.2017 г. – консультативный прием в онкологическом диспансере. Диагноз: Злокачественное новообразование желудка IV ст. Т4NxMx. Тотальное поражение. Канцероматоз брюшины. Прогрессирование. Кахексия. Асцит. Было рекомендовано продолжить симптоматическую терапию по месту жительства, а также попытка проведения гастростомии. Учитывая тяжесть состояния, ПХТ не показана.
22.12.2017 г. больной отметил появление одышки. На следующий день самостоятельно обратился в приемное отделение краевой больницы и был госпитализирован в отделение торакальной хирургии. На КТ органов грудной клетки (23.12.2017 г.) выявлен двусторонний гидроторакс. По легочным полям определялись очаги уплотнения по типу «матового стекла».
23.12.2017 г. и 25.12.2017 г. – плевральная пункция – эвакуирован 1 л серозно-геморрагического отделяемого. 26.12.2017 г. состояние больного тяжелое, с отрицательной динамикой. Появились рвота темной кровью, боли в эпигастрии, слабость, сухость во рту. На ФГДС – кровотечение интрагеморрагическое. Эрозивный эзофагит. Гемостаз системой EndoClot.
27.12.2017 г. состояние было крайне тяжелым. Сохранялась рвота темной кровью. Пациент переведен в ОРИТ, где проводилась инфузионная терапия, получал Метоклопрамид, Трамадол, Кетопрофен, Верошпирон, Транексам, Нексиум. При обследовании нарастала тромбоцитопения – 11569-41-19х10 9 л, показатели очищения: мочевина 20,01 ммоль/л; креатинин 140,9 ммоль/л; гипопротеинемия 46,4 г/л.
27.12.2017 г. в 22:15 – асистолия. Реанимационные мероприятия в полном объеме – без эффекта.
Основное заболевание: Злокачественное новообразование желудка: низкодифференцированная аденогенная карцинорма G3-4 (перстневидно-клеточный вариант – гистологически) с метастазами в парааортальные, периэзофагальные лимфоузлы, легкие, надпочечники; канцероматоз плевральных полостей и брюшины рТ4N3M1b.
Осложнение основного заболевания: Отек головного мозга. Двусторонний гидроторакс (1200/1200 мл). Асцит 3500 мл. Кахексия. Венозное полнокровие и паренхиматозная дистрофия миокарда, печени, почек.
Сопутствующие заболевания: Хронический пиелонефрит, ремиссия.
Обсуждение. В структуре заболеваемости РЖ возрастает доля молодого контингента больных (до 45 лет) с преобладанием низкодифференцированных и сложных форм, характеризующихся крайне плохим прогнозом [7, 8]. В настоящее время показатели несвоевременной диагностики рака желудка (IV стадия) являются одними из лидирующих, составляя в России 39,9% [9, с. 10].
Врач первичного звена является первой линией защиты в борьбе с онкопатологией. Первичная профилактика направлена на выявление и устранение влияния неблагоприятных факторов окружающей среды (канцерогенов) на процесс возникновения злокачественной опухоли, а также на устранение модифицируемых факторов риска [10]. У описанного нами пациента к факторам риска можно отнести длительный стаж курения и инфекцию НР.
Вторичная профилактика направлена на выявление и устранение предраковых заболеваний и диагностирование злокачественного новообразования на ранней стадии процесса при помощи ряда лабораторных и инструментальных методов обследования, включая полное гистологическое и молекулярно-генетическое исследование. При этом важно помнить о «симптомах тревоги» [10]. У пациента имели место снижение массы тела и повышение СОЭ, что должно было насторожить врачей. В течение 1,5 месяцев пациента вели с диагнозом «НПВП-гастропатия» с назначением ИПП, которые могли маскировать клинику рака желудка. Кроме того, отсутствие анамнестических данных о наличии фоновых заболеваний желудка и наследственной предрасположенности, молодой возраст пациента, неспецифическая симптоматика в начале заболевания, а также несвоевременное гистологическое исследование слизистой желудка послужили причиной поздней диагностики.
Заключение. Важно помнить, что рак желудка может быть диагностирован и в молодом возрасте, имея при этом крайне агрессивное течение. Необходимо выделять группы риска и своевременно проводить скрининг онкологических заболеваний. Регулярное диспансерное наблюдение является важнейшей массовой и высокоэффективной медицинской технологией сбережения здоровья и снижения преждевременной смертности населения.
Эпителиальный копчиковый ход у взрослых. Клинические рекомендации.
Эпителиальный копчиковый ход у взрослых
Оглавление
Ключевые слова
рандомизированное клиническое исследование
эпителиальный копчиковый ход
Список сокращений
Термины и определения
Эпителиальный копчиковый ход – представляет собой узкий канал, выстланный эпителием, содержащий волосяные луковицы, сальные железы, и открывающийся на коже межъягодичной складки одним или несколькими точечными (первичными) отверстиями.
1. Краткая информация
1.1 Определение
Эпителиальный копчиковый ход (ЭКХ) – представляет собой узкий канал, выстланный эпителием, содержащий волосяные луковицы, сальные железы, и открывающийся на коже межъягодичной складки одним или несколькими точечными (первичными) отверстиями [1, 2].
1.2 Этиология и патогенез
ЭКХ может длительное время протекать бессимптомно и люди, страдающие этой аномалией развития, чувствуют себя практически здоровыми. Нередко его обнаруживают случайно при профилактическом обследовании. По мнению Ю.В. Дульцева, болезнью ЭКХ можно считать с момента его первых клинических проявлений [3]. В 80-90% случаев заболевание манифестирует с образования острого абсцесса в крестцово-копчиковой области, что как правило, является поводом для обращения пациента за медицинской помощью [1, 4].
Полость копчикового хода сообщается с внешней средой через первичные свищевые отверстия, они же являются и «входными воротами» для инфекции, что приводит к возникновению воспалительного процесса в крестцово-копчиковой области, формированию абсцесса [1, 5, 6, 7, 8, 9, 10]. Предрасполагающими для этого факторами является травматизация крестцово-копчиковой области (езда на автомобиле, мотоцикле, велосипеде, верховая езда т.п.), избыточное скопление пота в межъягодичной складке, переохлаждение и повышенное развитие волосяного покрова в этой области [3, 11]. В результате воздействия этих неблагоприятных факторов возникает закупорка первичных свищевых отверстий, нарушается их дренажная функция, что ведет к развитию воспалительного процесса. L.A. Buieв 1944г., отметив высокий рост заболеваемости среди солдат, ввел специальный термин «Jeepdisease» (автомобильная болезнь), подчеркивая, что длительная травматизация крестцово-копчиковой области и плохая гигиена, способствуют появлению клинических симптомов заболевания [12]. В случаях, когда проходимость свищевых ходов не нарушена и сохраняется их дренажная функция, заболевание может длительное время протекать бессимптомно, либо проявляться периодически возникающим дискомфортом в крестцово-копчиковой области и скудными слизисто-гнойными выделениями через свищевые отверстия [1, 5, 7,13].
Дискуссии относительно этиологии и патогенеза ЭКХ ведутся с середины XVIII века. И.А. Лурин и И.В. Цема (2013) [14], в своей работе, обобщили теории этиопатогенеза ЭКХ и подразделили их следующим образом: 1) Нейрогенная теория, предложена в 1887 г. F. Tourneaux и G. Hermann. Согласно этой теории, копчиковый ход является рудиментарным остатком спинной хорды. В дальнейшем это теоретическое предположение не имело широкого распространения. В своей монографии Ю. В. Дульцев и В. Л. Ривкин (1988г.) отмечают, что доказанный факт существования каудального мозгового остатка в области копчика еще не означает что именно он дает начало кожной инвагинации. 2) Теория эктодермальной инвагинации, была разработана O. Lannelongue и L. Ashoff в 90-х годах ХХVIII века. Авторы предположили, что неравномерный рост позвоночного столба и спинного мозга в эмбриональном периоде приводят к фиксации кожи у верхушки копчика, что ведет к развитию заболевания. Одним из вариантов теории эктодермальной инвагинации, является теория «тракционного дивертикула», предложенная H.L. Newell в 1935 году. Причину тракции автор видел в натяжении filiumterminale (дистальный отдел спинного мозга, ставший тонкой связкой на определенном этапе развития человеческого зародыша), что приводит к вентральному смещению копчика и натяжению кожи на дне межъягодичной складки в области фиксации к этой связке. Сюда же можно отнести и ставшую наиболее популярной, теорию «хвостовой связки», разработанную L. Tait в 1924 г. Автор выявил, что у эмбриона имеется 9 копчиковых позвонков. В процессе внутриутробного развития происходит уменьшение количества позвонков до 3-5. В результате нарушения процессов редукции происходит возникновение подкожного копчикового хода. В отечественной медицине подобную теорию развития заболевания описывал в своих трудах С.Б. Раменский (1961г.) [12]. В 1903г. Н. Н. Петровым высказана мысль, что ЭКХ является врожденной аномалией развития, связанной с неполной редукцией мышечных и соединительнотканных элементов хвоста у человека, что и в наши дни поддерживается рядом авторов [1, 3, 7, 13, 15]. Впоследствии, данное положение в своих научных трудах подтвердил В. Л. Ривкин, который на основании исследований 500 трупов, показал, что в некоторых случаях редукция хвостовых позвонков происходит не до конца [16]. 3) Теории развития копчикового хода как приобретенного заболевания основаны на ретроградном врастании, «погружении» волос в подкожно-жировую клетчатку с образованием свищевых ходов. Впервые, предположение о том, что волосы играют важную роль в развитии заболевания, высказал еще R.M. Hodges в 1880г. Автором было указано, что волосы попадают в копчиковые ходы извне, а не закладываются там изначально. Однако ответить на ключевой вопрос о причинах первичного происхождения эпителиальных ходов, автор не смог. Данная теория на долгие годы была забыта и лишь в 1958г. D.H. Patey и R.W. Scarff вернулись к ней [17]. Авторы дополнили теорию приобретенного трихогенного происхождения ЭКХ, впервые описав помповый механизм проникновения волос в подкожно-жировую клетчатку. Исследователи предположили, что при ходьбе в межъягодичной складке, за счет напряжения и расслабления ягодичных мышц, периодически создается отрицательное давление. Благодаря этому происходит изменение направления роста волос, которые начинают врастать вглубь кожи. Впоследствии вокруг волос формируется соединительнотканная капсула, которая эпителизируется за счет врастания эпителия кожи по ходу волоса. Таким образом формируются первичные свищевые отверстия, давая начало развитию заболевания. Следует отметить, что в отечественной медицине очень мало исследований, посвященных такому механизму развития болезни. Можно выделить лишь работу С. З. Оганесяна, который в 1971г. подробно описал механизм попадания волос в эпителиальные копчиковые ходы извне [18, 19]. Однако, объяснить почему волосы в копчиковом ходе встречаются лишь в половине случаев автор не смог. В свое время, его теория так же не приобрела должного числа сторонников. Более подробно и стадийно трихогенно-помповый механизм развития заболевания описал в своих трудах J. Bascom в 1980 г. Формирование первичного свищевого отверстия автор объясняет с начинающегося воспаления волосяного фолликула и образованием микроабсцесса, который прорывается в глубину мягких тканей. После стихания воспаления на месте пораженного фолликула образуется углубление в виде воронки, стенки которого покрываются кожным эпителием, препятствующим заживлению. Таким образом происходит формирование первичного свищевого отверстия. Далее посредством помпового механизма, через первичное свищевое отверстие в глубину мягких тканей попадают волосы и инфекция. Закупоривание первичных отверстий и нарушение их дренажной функции приводит к повторному воспалению и абсцедированию, что влечет самопроизвольное или хирургическое вскрытие последнего с формированием уже вторичных свищевых отверстий [9].
Таким образом, все теории этиопатогенеза ЭКХ условно можно подразделить на две основные группы – врожденные и приобретенные. При этом в России взгляды на возникновение ЭКХ кардинально отличаются от взглядов зарубежных ученых. Так, традиционно, в отечественной литературе ЭКХ считается врожденным заболеванием, тогда как большинство зарубежных исследователей, в настоящее время, склоняются к приобретенной этиологии данного заболевания. Несмотря на множество проведенных исследований, единой теории возникновения копчикового хода подтвержденной достоверными данными в настоящее время не существует.
1.3 Эпидемиология
Заболевание в общей популяции встречается у 26 на 100000 человек [3, 20]. В проктологических стационарах больные с гнойными осложнениями эпителиального копчикового хода занимают четвертое место после геморроя, парапроктита и анальной трещины [3]. ЭКХ встречается преимущественно у лиц молодого возраста с преобладанием мужского пола над женским в соотношении 3:1 [3, 21]. Клинические проявления болезни, в основном, выявляются в возрасте от 15 до 30 лет [11, 16, 20, 22]. Некоторые авторы отмечают, что заболевание более часто встречается у кавказских народностей и наоборот является редким у людей негроидной расы. Процентное соотношение при их сопоставлении составляет 97,7% к 2,3% [23]. Ряд исследователей в развитии данного заболевания отмечают наследственную предрасположенность, которая по разным данным варьирует от 10,4% до 38% [24, 25]. DollD. (2009), установил, что ЭКХ встречается по первой линии родства у 68 (12%) из 578 пациентов [26].
1.4 Кодирование по МКБ-10
Пилонидальная киста (L05):
1.5 Классификация
1.5.1. Неосложнённый ЭКХ (без клинических проявлений).
1.5.2. Острое воспаление ЭКХ:
Определение стадии рака по системе TNM
2.58 (Проголосовало: 12)
Стадирование опухоли основано на трех критериях: глубина врастания опухоли в стенку кишки (Т), наличие распространения опухолевых клеток по лимфатическим узлам (N) и, наконец, наличие или отсутствие метастазов (M). Эти три составляющих образуют систему TNM для стадирования колоректального рака (см. таблицы ниже).
Стадия Т (tumor) – глубина врастания опухоли в стенку кишки. Чем меньше значение это стадии, тем менее инвазивный рост опухоли. Опухоль стадии Т0 можно еще считать достаточно доброкачественной, так как рост этой опухоли ограничен только слизистой оболочкой кишки. Опухоль стадии Т4 обозначает то, что опухоль проросла не только все слои кишечной стенки, но и соседние с ней органы.
Стадия N (lymphnodes) – обозначает количество лимфатических узлов, в которых были обнаружены раковые клетки. Стадия N0 обозначает, что при патологоанатомическом исследовании ни в одном из лимфатических узлов не были обнаружены клетки рака. Стадия Nx обозначает, что количество пораженных лимфатических узлов неизвестно. Это может быть на стадии обследования до операции, когда невозможно определить поражены лимфатические узлы или нет. Пока не проведено патологоанатомическое исследование, стадия считается как Nx.
Стадия М (metastases) – обозначает, имеются ли у опухоли отдаленные отсевы – метастазы.
Стадия опухоли по системе TNM
| T | N | M |
| is – рост опухоли в пределах слизистой | 0 – нет данных за поражение лимфатических узлов | 0 – нет данных за наличие отдаленных метастазов |
| 1 |
опухоль врастает, но не прорастает подслизистый слой кишки
поражение от 1 до 3 лимфатических узлов
наличие отдаленных метастазов опухоли
опухоль врастает, но не прорастает мышечный слой кишки
поражение больше, чем 3 лимфатических узлов
неизвестно, имеются ли метастазы
опухоль прорастает через мышечный слой в окружающие ткани
неизвестно, поражены ли лимфатические узлы
опухоль врастает в окружающие органы
Общая стадия опухоли
| T | N | M | |
|---|---|---|---|
| Стадия | 1,2 | 0 | 0 |
| Стадия | 3,4 | 0 | 0 |
| Стадия | Любая | 1,2 | 0 |
| Стадия | Любая | Любая | 1 |
Чтобы понять, как устанавливается стадия, найдите в таблице заголовки T, Nи M. В каждом столбце имеются цифры или слово «любая». Вторая строка в таблице соответствует стадии I, в столбцах имеются следующие данные: стадия Т 1 или 2, стадии Nи M – 0. Это означает, что если опухоль врастает только в стенку кишки (стадия Т1 или Т2) и ни в одном лимфоузле нет раковых клеток (стадия N0), и нет отдаленных метастазов (стадия M0), то опухоль будет классифицироваться, как рак I стадии. Опухоль, которая прорастает через кишечную стенку (стадия Т3 или T4), но при этом нет пораженных лимфатических узлов и отдаленных метастазов, имеет стадию II, и так далее.
Стадирование играет очень важную роль для определения тактики лечения. Для лечения опухолей I стадии обычно достаточно только хирургической операции, а опухоли III стадии обычно лечат, применяя и операцию, и химиотерапию. Таким образом, стадирование опухоли – это очень важный этап предоперационной диагностики. Для того, чтобы определить стадию до операции, может потребоваться выполнение многих исследований. Компьютерная томография (КТ), рентген грудной клетки, ультразвуковое исследование (УЗИ), магнитно-резонансная томография (МРТ) и позитронно-эмиссионная томография (ПЭТ) являются очень информативными исследованиями, помогающими определить степень распространения опухоли. Тем не менее, самым точным методом определения стадии опухоли является исследование удаленной во время операции части кишки с помощью микроскопа.
Очень важно, чтобы пациенты понимали принципы определения стадии опухоли, и имели представление о том, как это делается, чтобы грамотно обсуждать варианты и прогноз лечения с врачом.
Непроходимость двенадцатиперстной кишки (K31.5)
Версия: Справочник заболеваний MedElement
Общая информация
Краткое описание
Стеноз ДПК – это сужение ее просвета, наблюдающееся в течение длительного времени и не устраняющееся самопроизвольно. Стеноз может быть органическим и функциональным.
Функциональный стеноз возникает вследствие спазма мышц ДПК или отёка ее стенки. Наиболее часто появляется в период обострения язвенной болезни, устраняется при проведении адекватного лечения.
Функциональное сужение имеет схожую с органическим стенозом симптоматику. Отличие заключается в том, что проявления функционального стеноза исчезают по мере заживления язвы и исчезновения воспалительного инфильтрата.
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
13-15 октября, Алматы, «Атакент»
600 брендов, более 150 компаний-участников из 20 стран.
Новинки рынка стоматологии. Цены от производителей
Классификация
Анатомически можно выделить высокую и низкую (когда препятствие находится в области связки Трейтца) хроническую непроходимость ДПК.
Этиология и патогенез
Эпидемиология
Признак распространенности: Редко
Факторы и группы риска
Клиническая картина
Клинические критерии диагностики
Cимптомы, течение
Хроническая низкая непроходимость ДПК
Основные проявления: боли в животе (наиболее часто локализуются в надчревной области), рвота и похудание.
При прогрессирующем резком расширении желудка отмечаются вздутие живота и боли во всех его отделах, которые могут быть ошибочно приняты за кишечную непроходимость, особенно при наличии рвоты.
Рвота является обязательным симптомом хронической низкой непроходимости ДПК. В начале заболевания рвота непостоянная и скудная. В дальнейшем частота рвоты увеличивается, иногда отмечается рвота фонтаном. Рвота приносит облегчение, в результате чего, при усилении распирающих болей в животе, больные могут вызывать ее искусственно.
В рвотных массах присутствует большое количество желчи и пищи, съеденной накануне. При значительной примеси желчи в желудочном содержимом следует предполагать наличие механического препятствия дистальнее большого сосочка ДПК.
Диагностика
В вертикальном положении пациента при низкой хронической непроходимости ДПК, как правило, отмечаются:
— расширение желудка и ДПК до перехода ее влево от позвоночника;
— расширение промежутков между складками слизистой оболочки ДПК, их четкая циркулярная очерченность;
— обрыв тени просвета кишки в виде вертикальной линии, параллельной левому контуру позвоночника;
— в некоторых случаях наблюдается прохождение небольшой порции контрастирующей массы в тощую кишку.
Лабораторная диагностика
Лабораторные критерии диагностики непроходимости ДПК отсутствуют.
Изменения показателей могут быть обусловлены следующими причинами:
— проявление язвенной болезни желудка и ДПК;
— нарушение питания вследствие хронической непроходимости ДПК
— осложнения хронической непроходимости ДПК.
В таблице приведены изменения, характерные для выраженной формы непроходимости без кровотечения.
Что такое сифилис? Причины возникновения, диагностику и методы лечения разберем в статье доктора Агапова Сергея Анатольевича, венеролога со стажем в 39 лет.
Определение болезни. Причины заболевания
Сифилис (Syphilis) — хроническое инфекционное заболевание, вызванное бледной трепонемой (Treponema pallidum), которое характеризуется специфическим системным поражением кожи, слизистых оболочек, нервной системы, внутренних органов и опорно-двигательного аппарата. Передаётся преимущественно половым путём. Активное течение заболевания чередуется с латентными периодами.
Заболеваемость сифилисом
Возбудитель сифилиса
Причиной заболевания является инфицирование бледной трепонемой (Treponema pallidum) — небольшим микроорганизмом спиралевидной формы, который в естественных условиях способен существовать и размножаться только в организме человека. Бледная трепонема практически мгновенно погибает во внешней среде вследствие высыхания, легко разрушается при кипячении и воздействии антисептиков и этилового спирта. Помимо типичной спиралевидной формы существует в виде цист и L-форм, в которые она реорганизуется для выживания в неблагоприятной для неё среде.
Как передаётся сифилис. Можно ли заразиться бытовым путем
Условия, при которых происходит заражение:
Факторы риска
Риск заражения сифилисом повышен, если:
Заразность сифилиса
Контагиозность сифилиса зависит от стадии заболевания: как правило, особенно контагиозными являются первичная и вторичная формы, скрытый сифилис может распространяться трансплацентарно и трансфузионно.
Инкубационный период
После внедрения спирохеты наступает инкубационный период — промежуток времени между первичным инфицированием и появлением первых симптомов. Инкубационный период продолжается от 9 до 90 дней (в среднем 21 день).
Сифилис во время беременности
Поражаются ли внутренние органы при сифилисе
Симптомы сифилиса
Через какое время после контакта проявляются первые признаки
Первые симптомы сифилиса появляются в среднем через 21 день, но срок может удлиниться до трёх месяцев.
Внешние признаки сифилиса
Первичная сифилома (твёрдый шанкр) — симптом первичного периода сифилиса, признаком которого является эрозия или язва, возникающие на месте внедрения бледных трепонем в кожу или слизистые оболочки. Формирование шанкра начинается с возникновения небольшого красного пятна, через несколько дней оно превращается в узелок с коркой, при отторжении которой происходит обнажение безболезненной при пальпации эрозии или язвы овальной или округлой формы с чёткими границами.
Размеры твёрдых шанкров:
Чаще шанкр является одиночным, но при многократных половых актах с инфицированным партнёром могут появляться множественные высыпания. К множественным шанкрам относят «биполярный» шанкр, при котором язвы возникают одновременно на разных частях тела, и «целующийся» шанкр на соприкасающихся поверхностях.
В 90-95 % случаев шанкр расположен в любой области половых органов. Тот факт, что его часто обнаруживают на основании полового члена, свидетельствует о неполной эффективности презерватива для предохранения от сифилиса. Крайне редко шанкры могут появляться внутри уретры, во влагалище и на шейке матки. Атипичной формой шанкра в области гениталий является индуративный отёк в виде обширного безболезненного уплотнения крайней плоти или больших половых губ.
Сифилитическая лимфаденопатия (увеличение лимфатических узлов) — является симптомом первичного и вторичного периодов сифилиса.
Сифилитическая розеола (пятнистый сифилид) — проявление вторичного раннего врождённого и реже третичного периода сифилиса, возникающее у 50-70 % больных.
Папулёзный сифилид — симптом вторичного и раннего врождённого сифилиса, появляется при рецидиве заболевания в 12-34 % случаев. Представляет собой высыпания изолированных плотных узелков (папул) полушаровидной формы с гладкой поверхностью от розово-красного до медного или синюшного цвета. Зуда и болезненных ощущений нет, но если надавить на центр папулы, больные отмечают резкую болезненность (симптом Ядассона).
Сифилитическая ангина — симптом вторичного сифилиса, признаком которой является появление розеол и (или) папул на слизистой оболочке рта, зева, мягкого нёба. Если папулы локализуются на голосовых связках, появляется характерный «хриплый» голос. Иногда сифилитическая ангина — это единственное клиническое проявление болезни, и тогда она опасна в плане возможности полового (во время орального секса) и бытового инфицирования из-за высокого содержания трепонем в элементах сыпи.
Бугорковый сифилид (третичная папула) — основной симптом третичного периода сифилиса, который может появиться уже спустя 1-2 года с момента инфицирования. Но как правило возникает через 3-20 лет. Характеризуется появлением изолированных буровато-красных уплотнений размером до 5-10 мм, которые возвышаются над уровнем кожи и имеют гладкую и блестящую поверхность. Исходом существования бугорка всегда становится формирование рубца.
Симптомы нейросифилиса
Симптомы раннего врожденного сифилиса:
Симптомы позднего врождённого сифилиса:
Может ли сифилис проходить бессимптомно
Скрытая стадия сифилиса — это период, когда видимые признаки сифилиса отсутствуют. Без лечения инфицированный человек продолжает болеть сифилисом, даже если при этом нет никаких симптомов.
Патогенез сифилиса
После внедрения спирохеты наступает скрытый (инкубационный период) — промежуток времени между первичным инфицированием и появлением первых клинических симптомов, продолжающийся от 9 до 90 дней (в среднем 21 день). Удлинению инкубационного периода в первую очередь способствует приём антибиотиков в дозах, недостаточных для излечения.
Первичная стадия
В 90-95 % случаев по окончанию инкубационного периода в месте внедрения трепонем возникает первичный очаг — сифилитический твёрдый шанкр. В 5-10 % случаев заболевание протекает первоначально скрыто — без его образования (обезглавленный сифилис). Через 7-10 дней появления шанкра начинают увеличиваться региональные лимфатические узлы. Спустя 1-5 недель шанкр самопроизвольно регрессирует. Промежуток между появлением шанкра и его исчезновением принято называть первичным периодом сифилиса.
Вторичная стадия
Через 1-5 недель после образования первичного шанкра вследствие распространения трепонем по всему организму появляется кожная сыпь, которая существует в течение 2-6 недель, после чего самопроизвольно исчезает. Через определённое время сыпь может рецидивировать. Такое волнообразное течение сифилиса связано с активизацией трепонем или угнетением их размножения вследствие иммунного ответа организма. Промежуток между первым появлением сыпи и появлением третичных сифилидов принято называть вторичным периодом сифилиса, а промежутки между рецидивами — скрытым периодом сифилиса. Вторичный сифилис с рецидивами отмечается у 25 % больных.
Следует отметить, что в достаточном количестве случаев сифилис может изначально существовать в скрытой форме, переходить в неё после первичного периода или после первого эпизода вторичного сифилиса и протекать далее бессимптомно. В таких случаях различают ранний скрытый сифилис с давностью заболевания менее двух лет и поздний скрытый с давностью заболевания свыше двух лет после инфицирования. Вторичный и скрытый сифилис могут продолжаться в течение нескольких лет и даже десятилетий.
Третичная стадия
Приблизительно у 15 % больных с нелеченым сифилисом через 1-45 лет после заражения появляется кожная сыпь в виде бугоркового или гуммозного сифилидов, что свидетельствует о переходе заболевания в третичный период. Как и при вторичном сифилисе, сыпь может исчезать и рецидивировать.
Нейросифилис и сифилис глаза
Врождённый сифилис
Врождённый сифилис возникает в результате инфицирования плода через пупочную вену и лимфоузлы пуповины от больной матери. Заражение возможно уже с 10-12 недели беременности. Может протекать скрыто или с клиническими проявлениями.
Классификация и стадии развития сифилиса
Согласно Международной классификации болезней 10 пересмотра (МКБ-10) существуют следующие виды сифилиса [25] :
1. Ранний врождённый сифилис:
2. Поздний врождённый сифилис:
3. Врождённый сифилис неуточнённый;
4. Ранний сифилис:
5. Поздний сифилис:
6. Другие и неуточнённые формы сифилиса:
Осложнения сифилиса
Различают следующие осложнения при первичной стадии сифилисе:
Риск заражения ВИЧ
Неврологические проблемы
Без лечения сифилис может привести к менингиту, прогрессирующему параличу и спинной сухотке (дегенерации спинного мозга).
Сердечно-сосудистые проблемы
Сифилис может стать причиной:
Смерть от сифилиса наступает вследствие поражения внутренних органов. Наиболее частой причиной является разрыв аорты вследствие сифилитического аортита.
Диагностика сифилиса
Когда следует обратиться к врачу
К врачу необходимо обратиться при появлении первых симптомов сифилиса — язвы и сыпь на половых органах. Также посетить доктора следует, если сифилис обнаружен у вашего сексуального партнёра или человека, с которым был тесный бытовой контакт.
Подготовка к посещению врача
Кровь на наличие антител нужно сдавать натощак. Эрозии и язвы не следует обрабатывать антисептиками в течение суток до посещения доктора.
Для диагностики сифилиса применяются микроскопические, молекулярные, иммуногистохимические, серологические и инструментальные методы.
Материал для исследования:
Показания для обследования:
Положительная реакция без сифилиса
Возможны ложноположительные серологические реакции на сифилис — положительные результаты серологических реакций у лиц, не болеющих и не болевших ранее сифилисом. Причины могут быть следующими:
Ложноотрицательные серологические реакции на сифилис могут быть при вторичном сифилисе вследствие «феномена прозоны» и у лиц с выраженным иммунодефицитом и некоторыми инфекциями (ВИЧ, туберкулез).
Клиническая оценка серологических реакций
Исследование спинномозговой жидкости проводится для диагностики нейросифилиса. Оно показано:
Лечение сифилиса
Можно ли вылечить сифилис
Сифилис можно вылечить антибиотиками, правильно подобранными лечащим врачом. Однако в запущенных случаях лечение может не исправить того вреда, который уже нанесла инфекция.
Что такое превентивное лечение
Превентивное, или предупредительное, лечение проводят лицам, находившимся в половом и тесном бытовом контакте с больными ранними формами сифилиса, если с момента контакта прошло не более двух месяцев.
Предупредительное лечение врождённого сифилиса проводят:
Лечение антибиотиками
Специфическое лечение направлено на элиминацию (выведение) возбудителя заболевания и назначается всем больным с клиническими и скрытыми формами инфекции.
Превентивное лечение заключается в назначении препаратов больным, которые имели сексуальный или тесный бытовой контакт с больным ранними формами сифилиса, если с момента контакта прошло не более двух месяцев.
Дополнительное лечение назначается лицам с серорезистентностью после адекватного лечения.
Физиопроцедуры
Физиотерапия при сифилисе не проводится.
Последующее наблюдение после начала лечения сифилиса
Последующее наблюдение в зависимости от стадии заболевания длится от 1 года до 5 лет. В течении первого года анализ крови необходимо проводить каждые три месяца.
Мифы и заблуждения о лечении сифилиса
Домашние средства лечения (стоит ли пытаться вылечить самостоятельно)
Вылечить сифилис без применения антибактериальной терапии не получится. Препараты для лечения сифилиса назначает врач-венеролог.
Прогноз. Профилактика
Если начать лечение сифилиса своевременно, то прогноз будет благоприятен.
Как снизить риск заболевания
Профилактика заболевания заключается в санитарно-просветительской работе, скрининге декретированных групп населения, которые находятся в группе риска, в осуществлении полноценных специфических лечебных мероприятий и последующем клинико-серологическом контроле.
Для профилактики врождённого сифилиса необходимо трёхкратное серологическое обследование при беременности (при постановке на учёт, в 28-30 недель и 35-37 недель), адекватное специфическое и профилактическое лечение при выявлении сифилиса у беременных и профилактическое лечение детей, рождённых от недолеченной или больной матери.
Что делать, если у члена семьи сифилис
После первой инъекции антибиотика больной сифилисом не опасен для окружающих. Если ранее был тесный бытовой контакт, то назначается серологический и клинический контроль в течении трёх месяцев или предупреждающее лечение.
Можно ли заразиться сифилисом повторно
Перенесённый ранее сифилис не защитит от повторного заражения.
Как выглядит выпавшая кишка 4 27 1 689 1 192
Согласно классификации 2019 г., в группу доброкачественных эпителиальных новообразований толстой кишки вошли зубчатая дисплазия, аденоматозные полипы и железистая интраэпителиальная неоплазия. Зубчатая дисплазия (МКБ-О 8213/0 и 8213/2) представляет собой бывшие зубчатые образования. Происходит ожидаемое изменение терминологии: вместо вызывающего огромное количество дискуссий термина «sessile serrated polyp/adenoma» предлагается использовать термин «sessile serrated lesion» (SSL, сидячее зубчатое образование). В сравнении с классификацией 2010 г. более четко прописаны критерии TSA: щелевидная зубчатость и высокие вытянутые клетки с выраженной эозинофильной цитоплазмой и длинным карандашевидным ядром (spencillate). Традиционные аденомы в классификации переименованы: вместо термина «аденомы» принят «аденоматозные полипы», который по-прежнему включает тубулярную, тубуловорсинчатую и ворсинчатую аденомы. Критерии аденом остались прежними (по площади, занимаемой ворсинчатыми структурами). В 5-м издании введен отдельный большой раздел, посвященный дисплазии, ассоциированной с воспалительной болезнью толстой кишки, которая определяется как явные неопластические изменения в эпителии, ограниченные базальной мембраной. Диагноз может применяться только при специфических поражениях, таких как колит Крона и язвенный колит.
ФГБОУВО «Московский государственный университет им. М.В. Ломоносова», Москва, Россия
ГУНУ «Факультет фундаментальной медицины МГУ им. М.В. Ломоносова»;
ГБОУ ДПО «Российская медицинская академия последипломного образования», Москва
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздрава РФ;
ГБОУ ДПО «Российская медицинская академия последипломного образования», Москва
Новая классификация опухолей толстой и прямой кишки WHO 2019, 5-е издание [1, 2] выглядит довольно стройной, чрезвычайно краткой и включает в себя только эпителиальные новообразования, разделенные на две группы: доброкачественные и злокачественные новообразования. Наша публикация посвящена только классификации доброкачественных образований (табл. 1).

В группу доброкачественных образований в классификации WHO 2019 г. вошли зубчатая дисплазия, аденоматозные полипы и железистая интраэпителиальная неоплазия.
Зубчатая дисплазия. Зубчатая дисплазия (приведено два кода МКБ-О — 8213/0 и 8213/2) представляет собой бывшие зубчатые образования. Бросаются в глаза чрезмерная краткость рубрики зубчатая дисплазия и большое количество форм, описанных в тексте WHO 2019, которые не нашли отражение в официальной классификации МКБ-О. Так, к группе зубчатых дисплазий относятся:
1. гиперпластический полип (hyperplastic polyp, HP) микровезикулярного и богатого бокаловидными клетками типа;
2. сидячее зубчатое образование (sessile serrated lesion, SSL);
3. традиционная зубчатая аденома (traditional serrated adenoma, TSA);
4. неклассифицируемая зубчатая аденома.
Происходит ожидаемое изменение терминологии: вместо вызывающего огромное количество дискуссий термина «sessile serrated polyp/adenoma» предлагается использовать термин «sessile serrated lesion» (SSL, сидячее зубчатое образование), что исключает дальнейшие рассуждения относительно истинности опухолевой природы такого новообразования.
Коды МКБ-О указаны не для всех образований, а только для TSA (8213/0) и неклассифицируемой зубчатой аденомы (8213/0), в связи с чем может возникнуть путаница: какие коды использовать в практической работе врача? Складывается впечатление, что код 8213/2 следует использовать только для SSL с дисплазией, однако это в тексте не прописано однозначно. Зубчатый путь канцерогенеза сильно расширен (рис. 1)

1) метилирование гена MLH1 с последующим развитием высокого уровня метиляторного фенотипа (CIMP) и колоректальной карциномы с дефектной системой репарации ДНК (MMR — mismatch repair);
2) мутация TP53 с развитием карциномы с сохранными генами группы MMR.
TSA могут развиваться de novo, из SSL или богатых бокаловидными клетками HP, прогрессируют через BRAF- или KRAS-путь до high grade дисплазии и карциномы без метилирования промоторов генов группы MMR. Активация WNT-пути характерна для всех вышеописанных моделей на этапе развития дисплазии.
В качестве предопухолевых поражений рассматриваются воспалительные изменения толстой кишки и традиционные и зубчатые образования, однако в 5-м издании отсутствует такое понятие, как «очаг аберрантных крипт» ни диспластического, ни гиперпластического типа. Источники HP или традиционной аденомы не определены, явного подтверждения исключения из оборота термина «очаг аберрантных крипт» нет, однако в тексте «очаги аберрантных крипт» не встречаются. С одной стороны, у этих изменений отсутствовали четкие критерии, и патологи могли довольно вольно трактовать термин по своему усмотрению, с другой стороны, «очаг аберрантных крипт» как термин вносил некую ясность в патогенез образований и определялся как первая стадия будущего образования. Теперь в отсутствие понятия «очаг аберрантных крипт» складывается впечатление, что и HP, и SSL, и традиционные аденомы формируются de novo (за исключением SSL из HP).
Морфологические критерии описанных образований принципиально не изменились (табл. 2).


Для SSL достаточно установить наличие одного из четырех признаков нарушения архитектоники крипты (рис. 3):

1) горизонтальный рост крипт вдоль мышечной пластинки;
2) расширение базальных отделов крипт;
3) зубчатость крипт, доходящая до базальных отделов (в нижней трети);
4) асимметричная пролиферация.
Все эти изменения являются структурной основой формирования ямок II-O типа по эндоскопической классификации Kudo [3]. В новой классификации четко обозначено, что наличие даже одной крипты с явными признаками SSL считается достаточным для постановки диагноза. Следует учесть, что нарушение архитектоники этой крипты должно быть явным, в противном случае расценивать данные изменения как SSL не рекомендуется, равно как и умеренная дилатация базальных отделов крипт не считается достаточным критерием SSL. Введенное уточнение является чрезвычайно важным аспектом для практической работы и направлено на снижение вариабельности классифицирования новообразований. Особо подчеркнуто, что никакие клинические данные, такие как размер, локализация, эндоскопическая картина не могут быть основанием для постановки диагноза SSL. Выпячивание слизистой оболочки (mucosal herniation) является диагностической трудностью и «ловушкой» для SSL. Зубчатые крипты могут пролабировать через мышечную пластинку слизистой оболочки в подслизистый слой, часто в окружении жировой ткани или лимфоидных агрегатов, поскольку гладкомышечные волокна искажают архитектонику крипты. Наличие выпячивания слизистой оболочки важно отличать от инвазии, особенно в новообразованиях с дисплазией. Описанный в других источниках [4] пролапс слизистой оболочки толстой кишки (рис. 4),

Отмечено, что дисплазия в SSL обычно четко отграничена и имеет бóльшую гетерогенность по сравнению с традиционными аденомами. Структурные изменения SSL с дисплазией включают (рис. 5):

Цитологически, дисплазия может быть трех типов:
1) кишечная дисплазия, напоминающая дисплазию в традиционных аденомах;
2) зубчатая дисплазия — круглые атипичные ядра, выраженные ядрышки, множество митозов, эозинофильная цитоплазма;
3) крайне невыраженная цитологическая атипия, включая гипермуцинозные изменения (очень редкий вариант).
В случаях, когда диспластические изменения в SSL неявные и вызывают сомнения, помочь может уточняющее ИГХ-определение с антителами к MLH1: диспластические крипты, как правило, отрицательны в сравнении с окружающей слизистой оболочкой. Подразделение дисплазии в SSL на low и high grade не рекомендуется, поскольку, с одной стороны, это крайне затруднительно ввиду гетерогенности морфологических проявлений, а с другой стророны, из-за со слабой корреляции в связи с потерей MLH1-экспрессии.
В сравнении с классификацией 2010 г. теперь более четко прописаны критерии TSA: щелевидная зубчатость, подобная щелям между ворсинками нормальной слизистой оболочкой тонкой кишки; высокие вытянутые клетки с выраженной эозинофильной цитоплазмой и длинным карандашевидным ядром (spencillate).
Эктопические крипты, представляющие собой грыжеподобные выпячивания, перпендикулярно отходящие от крипты и не достигающие мышечной пластинки слизистой оболочки (рис. 6),

Введена новая подрубрика — неклассифицируемая зубчатая аденома. Эта подрубрика может быть использована, если полип с зубчатой архитектоникой трудно дифференцировать между TSA и SSL с дисплазией. Целесообразность подрубрики вызывает вопросы, поскольку указывается, что вблизи 50% TSA обнаруживается любой другой предшественник — HP или SSL.
Все многообразие образований и относительно четко прописанные диагностические критерии не нашли отражения в их кодировании по МКБ-О, ввиду чего к большинству зубчатых образований (дисплазий) применяется код 8312/0. Размер полипов более 1 см считается фактором развития зубчатого полипоза, при этом имеется риск возникновения колоректальной карциномы, однако на кодировании эти факторы также не отражаются. В связи с этим возникает логичный вопрос в целесообразности деления зубчатых образований на подтипы с учетом всех вышеприведенных критериев. Также остается неясно, как кодировать HP. В классификации HP включены, прописаны под рубрикой зубчатые дисплазии, с кодом МКБ-О 8213/2, однако собственного кода МКБ-О не имеют. Возможно, авторы подчеркивают их неопухолевую природу, и в диагнозе HP должен стоять без кода, что более вероятно, но, с другой стороны, рекомендован код 8213/2, что странно, поскольку дисплазия в HP не встречается.
Аденоматозные полипы. Традиционные аденомы в классификации переименованы, термин «аденомы» заменен на «аденоматозные полипы» [5] и по-прежнему включает тубулярную, тубуловорсинчатую и ворсинчатую аденомы, однако в 5-м издании для каждой аденомы непосредственно в классификацию введена степень дисплазии, что влияет на финальный код по МКБ-О (см. табл. 1). Критерии аденом остались прежними (количество площади, занимаемой ворсинчатыми структурами).
Прогрессивная аденома (advanced adenoma) значилась в предыдущей версии, но не была вынесена в отдельную рубрику. Ее критериями обозначены: размер более 10 мм; тубуловорсинчатая или ворсинчатая структура и/или high grade дисплазия, или внутриэпителиальная аденокарцинома.
Отмечается, что эта группа является собирательной и введена специально для международного сравнения скрининговых программ колоректального рака, поскольку прогрессивные аденомы ассоциированы с более высоким риском развития синхронных, или метахронных аденом (дословный перевод).
Дисплазия, ассоциированная с воспалительной болезнью толстой кишки. В 5-м издании введен отдельный большой раздел, посвященный дисплазии, ассоциированной с воспалительной болезнью толстой кишки. Соответствующие коды в классификации (8148/0 и 8148/2) значились и ранее, но критерии постановки, а также характер процессов были прописаны достаточно расплывчато, в связи с чем дополнения и конкретика в этом вопросе были ожидаемы.
Авторы приводят статистику: при язвенном колите дисплазия наблюдается в левых отделах ободочной и дистальных отделах кишки, при болезни Крона — в зонах сегментарного поражения, а 44—72% дисплазий приходится на ректосигмоидный отдел, совпадая с локализацией колоректальных раков, ассоциированных с язвенным колитом.
Описанные ограничения кажутся не совсем корректными, так как понятие «воспалительная болезнь толстой кишки» не ограничивается только язвенным колитом и колитом Крона. С точки зрения патогенеза, неясно, почему в других (неспецифических) вариантах не может развиться дисплазия эпителия, а главное, как ее кодировать, или авторы имеют в виду гиподиагностику язвенного колита и болезни Крона, которые должны быть при наличии дисплазии, ассоциированной с воспалительной болезнью толстой кишки? Отсутствует в тексте новой классификации и упоминание о так называемом воспалительном полипе/псевдополипе, который прямо описывается в классических руководствах как вариант выбора в сложных диагностических ситуациях и, кроме того, содержится в МКБ-11 (DB35.1).
Морфологически дисплазия может быть двух типов: 1) кишечной (аденоматозной) или 2) зубчатой, каждая из которых градируется как low и high grade по признакам цитологической атипии и изменениям гистоархитектоники крипты. При low grade дисплазии крипты тубулярные/ворсинчатые или зубчатые со слабым почкованием и скученностью; ядра увеличены, вытянуты, увеличено ядерно-цитоплазматическое соотношение, отмечаются гиперхромия, стратификация, ограниченная базальной частью цитоплазмы клетки, и множественные мелкие ядрышки или агрегированный хроматин.
В зубчатой дисплазии диспластические клетки характеризуются гиперэозинофильной, бедной муцином цитоплазмой или микровезикулярным эпителием, похожим на спорадические зубчатые образования (рис. 7).

В high grade дисплазии клетки значительно увеличены, часто плеоморфны, с гиперхромными ядрами, явной потерей полярности и стратификацией, которая распространяется на всю цитоплазму. Фигуры митозов, как типичные, так и нетипичные, часто наблюдаются в верхних отделах крипт и поверхностном эпителии. High grade дисплазия часто дополняется значительными нарушениями архитектуры, такими как скученность желез, формирование криброзных структур, почкование и ветвление. Могут встречаться внутрипросветные некрозы. Нет единого мнения относительно количества high grade диспластических крипт в биоптате для постановки диагноза high grade диwсплазии, но большинство авторов сходятся во мнении, что при наличии хотя бы одного фокуса, соответствующего high grade, дисплазия должна классифицироваться как тяжелая (high grade).
Описаны также другие, более редкие типы дисплазии — муцинозный тип с эозинофильной цитоплазмой, выраженным истощением бокаловидных клеток и криптоклеточный тип (cryptcell), представленный эпителиальными клетками с атипичным ядром и сохранной цитопазмой. Муцинозная дисплазия часто присутствует в тубуловорсинчатом паттерне, эпителий имеет маленькие, гиперхромные, базально-ориентированные ядра с минимальной цитологической атипией. Количество бокаловидных клеток снижено, но цитоплазма имеет отчетливую муцинозную дифференцировку.
Заключение
Новая классификация 2019 г. ликвидирует ряд накопившихся проблем в терминологии зубчатых образований толстой кишки, но при этом она не является полностью логичной. Имеются трудности в навигации, поскольку названия, приведенные в классификационной таблице, не соответствуют указанным разделам с описанием. Неясно, как соотносятся разновидности традиционных аденом и зубчатых образований с аденоматозными полипами и зубчатой дисплазией. Странно, что гиперпластические полипы и аденомы с дисплазией low grade отнесены к группам дисплазии high grade. Считаем, что возврат к термину «аденоматозный полип» в новой классификации при сохранении термина «аденома» вносит значительную путаницу и будет затруднять взаимодействие врачей-гастроэнтерологов, эндоскопистов и медиков других клинических специальностей.
Работа выполнена в рамках госзадания ФГБОУ ВО МГУ им. М.В. Ломоносова с использованием оборудования, приобретенного по Программе развития ФГБОУ ВО МГУ им. М.В. Ломоносова до 2020 г.
Сведения об авторах
Автор, ответственный за переписку: Олейникова Нина Александровна — е-mail: noleynikova@mc.msu.ru
1 Еще не введена в действие ни за рубежом, ни в Российской Федерации (ожидается введение в действие с 01.01.22).
Общий анализ кала
Копрограмма (общий анализ кала)
Подготовка к исследованию
Подробное описание анализа

Копрограмма имеет важное значение при диагностировании и клиническом разграничении патологических процессов, протекающих в желудочно-кишечном тракте. Ее результаты позволяют практикующему специалисту поставить предварительный диагноз и определить тактику дальнейшего обследования. С помощью копрологического исследования возможно быстро обнаружить инфекционных возбудителей – это особенно важно в случаях, когда требуется изолировать пациента.
Поводом для проведения общего анализа кала является наличие:
Нужно ли соблюдать диету перед проведением копрограммы?
В большинстве случаев перед забором образца биологического материала не обязательно придерживаться особого питания. Специальную диету должны соблюдать пациенты, у которых предполагают внутреннее кровотечение. Искажение результатов копрологического исследования могут спровоцировать мясные и рыбные продукты, яйца, томаты, шпинат, тыква, клубника, малина, ежевика, ревень, свекла, черника, ботат, черная смородина, сельдерей – их необходимо исключить из рациона питания за 48 часов до собирания кала. Также перед анализом пациенту нужно отменить прием препаратов магния, железа и висмута, отказаться от чистки зубов – во время гигиенической процедуры можно зубной щеткой травмировать десны, что приводит к попаданию в пищеварительный тракт крови и получению недостоверных итоговых данных исследования.
Методика выполнения анализа кала на копрограмму
В первую очередь образец экскрементов подвергается визуальному изучению, оцениванию качественно-количественных параметров и выявлению патологических включений различного происхождения. Затем, используя химические реагенты, проводят химические пробы, в ходе которых определяется наличие примесей. Третьим этапом исследования является микроскопия нативного препарата и препаратов с глицерином, растворами Люголя, Гента, метиленового синего и Судана.
Фекалии здорового человека представляют собой однородную оформленную густую массу, имеющую цилиндрическую форму, коричневый оттенок, выраженный запах и минимальное количество непереваренной пищи, однако в которой отсутствуют примеси слизи, крови и гноя, яйца, личинки и фрагменты гельминтов. Физические характеристики кала зависят от особенностей рациона питания пациента и применения некоторых медикаментозных средств – связанные с ними небольшие отклонения считаются допустимыми.
Нормальные результаты анализа и их интерпретация
Микроскопия позволяет изучить патологические примеси в испражнениях, а также сделать вывод о степени перевариваемости продуктов питания в каждом из отделов ЖКТ.
Таблица 1. Микроскопия кала.
| № | Патологические примеси | Норма | Отклонения |
| 1. | Не перевариваемые мышечные волокна, перевариваемые мышечные волокна и соединительные волокна | Отсутствует | Их наличие указывает на недостаточность переваривания пищи в желудке, патологии поджелудочной железы. |
| 2. | Жир нейтральный | Отсутствует | Может выявляться при недостаточности выработки пищеварительных ферментов поджелудочной железой. |
| 3. | Жирные кислоты, мыло | Отсутствует | Их обнаружение указывает на обструкцию желчевыводящих путей, замедленное пищеварение в тонком кишечнике. |
| 4. | Растительная перевариваемая клетчатка | Отсутствует | Выявляется при обструкции желчевыводящих путей, гнилостных процессах, нарушении пищеварения в тонком кишечнике и ускоренном продвижении пищи по толстому, колите. |
| 5. | Крахмал, йодофильная флора | Отсутствует | |
| 6. | Слизь | У взрослых отсутствует, допускается небольшое количество у детей до 5 мес. | Наличие в кале указывает на развитие колита, хронического запора, повышенной секреции толстого кишечника. |
| 7. | Лейкоциты | Отсутствует | Обнаруживаются при распаде новообразований, изъявлениях кишечных слизистых. |
| 8. | Эритроциты | Отсутствует | Их наличие может свидетельствовать о злокачественных опухолях в кишечнике или желудке, полипах, анальных трещинах и геморрое. |
| 9. | Яйца гельминтов и простейшие | Отсутствует |
При химическом исследовании проводят реакции на скрытую кровь, белок и билирубин, которые должны быть отрицательными. Реакция на стеркобилин должна быть положительной.
Поджелудочная железа: размеры, норма
В пищеварительную систему входит такой орган, как поджелудочная железа. Она способствует перевариванию пищи. Имеется в виду жирная, углеводистая, белковая еда. Благодаря такому органу происходит регуляция углеводного обмена в организме. При развитии различных патологических процессов или заболеваниях повышается риск серьезного последствия для поджелудочной железы.
Форма
Во время ультразвукового исследования определяется форма и отклонение от нормы. При отсутствии каких-либо проблем, орган будет иметь S образную форму. В некоторых ситуация можно выявить патологию, которая выражается в нарушенной форме. Орган может быть кольцевидной, спиральной, расщепленной, добавочной формы. Аномалия, которая выявлена с помощью узи, это изолированный дефект поджелудочной или часть тяжелого патологического процесса.
В большинстве случаев, ультразвуковое исследование способно выявить только косвенные симптомы. Речь идет о сужении или дополнительном протоке. В такой ситуации врач может назначить другое исследование, чтобы исключить иди подтвердить отклонение.
Размер
Диагностическое ультразвуковое исследование заключается также в измерении параметров поджелудочной железы. У взрослого человека норма размера варьируется от 14 до 22 сантиметров. Весит такая поджелудочная железа около 75 грамм. Орган состоит из головки, где расположен крючковидный отросток (длина такого отростка приблизительно три сантиметра), тела (длина колеблется от 1.5 до 1.7 сантиметра) и хвоста (размер около двух сантиметров).
Головку охватывает двенадцатиперстная кишка. Локализацией является уровень первого и начало второго поясничного позвонка. У протока поджелудочной железы ровная гладкая стенка. Ее диаметр не превышает один миллиметр в теле и двух миллиметров в головке. Колебание параметров может происходить как в меньшую, так и в большую сторону.
Каждый вид патологического процесса отличается различной картиной, которая видна во время ультразвукового исследования. Воспалительный процесс, который сопровождается отечностью, характеризуется увеличением участка от головки до хвоста. При наличии опухоли будут увеличиваться отдельные пораженные части. К примеру, злокачественное образование более чем в 55 процентах случаев расположено в головке поджелудочной железы. В таком случае голова органа увеличиться более 4 сантиметров. Около 15 процентов случаев диагностируют онкологию тела поджелудочной железы. Будет увеличено тело органа.
Контур
Норма это наличие ровных и четко очерченных контуров. Имеются в виду все составляющие органа (головка, тело, хвост). При расплывчатых очертаниях можно предположить, что развивается воспалительный процесс в поджелудочной железе. Часто встречается, что отечность спровоцирована органом, который расположен рядом. К примеру, возникновение реактивного отека поджелудочной связано с гастритом, язвой желудка и двенадцатиперстной кишки.
Киста и абсцесс способствуют появлению выпуклых и гладких контуров на отдельных участках органа. Неровности границы являются последствием панкреатита и опухоли, размер которой не превышает один сантиметр, и которая расположена на поверхности. Внешние границы могут измениться, если сформировалось крупное новообразование, размер которого превышает два сантиметра.
Структура
С помощью ультразвукового исследования определяется структура поджелудочной железы, учитывая плотность. Нормой является зернистая структура, средняя плотность, которая похожа на плотность печени или селезенки. На мониторе определяется наличие равномерной эхогенности с небольшим вкраплением. Если изменена плотность органа, будет изменяться отражение ультразвуковых волн.
Может наблюдаться увеличение (гиперэхогенность) или уменьшение (гипоэхогенность) плотности. Визуализация гиперэхогенности связана с хроническим панкреатитом. Наличие частичной гиперэхогенности говорит о камне или опухоли. Выявить гипоэхогенность можно во время острого панкреатита, отечности и злокачественных новообразованиях. Киста или абсцесс характеризуется наличием эхонегативных участков, когда не происходит отражения ультразвуковых волн. В таком случае на мониторе видны белые участки. Практика показывает, что во время ультразвукового исследования выявляется смешанная эхогенность, когда совмещается гиперэхогенная и гипоэхогенная область.
Как расшифровывают результаты
Когда окончено ультразвуковое исследование, квалифицированный врач оценит полученные данные, на основании которых выносится заключение. В нем происходит полная расшифровка результата обследования поджелудочной железы. Наличие какой-либо болезни или подозрение на нее характеризуется совокупностью нескольких изменений.
При незначительных отклонениях поджелудочной железы от стандартного показателя нет необходимости ставить точный диагноз. Расшифровку врач проводит после ультразвукового исследования, на это потребуется приблизительно 15 минут.
Клинические формы хронической Эпштейн-Барр-вирусной инфекции: вопросы диагностики и лечения
Какие заболевания могут вызвать вирус Эпштейна-Барра? Какие симптомы типичны для ВЭБ-инфекции? Существуют ли строго специфичные для ВЭБ изменения лабораторных показателей? Что включает в себя комплексная терапия ВЭБ-инфекции?
Какие заболевания могут вызвать вирус Эпштейна-Барра? Какие симптомы типичны для ВЭБ-инфекции?
Существуют ли строго специфичные для ВЭБ изменения лабораторных показателей?
Что включает в себя комплексная терапия ВЭБ-инфекции?
В последние годы наблюдается рост числа больных, страдающих хроническими рецидивирующими герпес-вирусными инфекциями, которые во многих случаях сопровождаются выраженным нарушением общего самочувствия и целым рядом терапевтических жалоб. Наиболее широко распространены в клинической практике лабиальный герпес (чаще вызывается Herpes Simplex I), опоясывающий лишай (Herpes zoster) и генитальный герпес (чаще вызывается Herpes simplex II); в трансплантологии и гинекологии часто встречаются заболевания и синдромы, вызванные цитомегаловирусом (Cytomegalovirus). Однако о хронической инфекции, вызванной вирусом Эпштейна-Барр (ВЭБ), и ее формах врачи общей практики осведомлены явно недостаточно.
ВЭБ был впервые выделен из клеток лимфомы Беркетта 35 лет назад. Вскоре стало известно, что вирус может вызывать у человека острый мононуклеоз и назофарингеальную карциному. В настоящее время установлено, что ВЭБ ассоциирован с целым рядом онкологических, преимущественно лимфопролиферативных и аутоиммунных заболеваний (классические ревматические болезни, васкулиты, неспецифический язвенный колит и др.). Кроме того, ВЭБ может вызывать хронические манифестные и стертые формы заболевания, протекающие по типу хронического мононуклеоза [1, 3, 6, 9,12]. Вирус Эпштейна—Барр относится к семейству герпес-вирусов, подсемейство гамма-герпес-вирусов и род лимфокриптовирусов, содержит две молекулы ДНК и обладает способностью, как и другие вирусы этой группы, пожизненно персистировать в организме человека [6, 8]. У части больных на фоне иммунной дисфункции и наследственной предрасположенности к той или иной патологии ВЭБ может вызывать различные заболевания, о которых упоминалось выше. ВЭБ инфицирует человека, проникая через интактные эпителиальные слои путем трансцитоза в нижележащую лимфоидную ткань миндалин, в частности В-лимфоциты [7]. Проникновение ВЭБ в В-лимфоциты осуществляется через рецептор этих клеток CD21 — рецептор к С3d-компоненту комплемента. После инфицирования число пораженных клеток увеличивается посредством вирус-зависимой клеточной пролиферации. Инфицированные В-лимфоциты могут значительное время находиться в тонзиллярных криптах, что позволяет вирусу выделяться во внешнюю среду со слюной.
С инфицированными клетками ВЭБ распространяется по другим лимфоидным тканям и периферической крови. Созревание В-лимфоцитов в плазматические клетки (что происходит в норме при их встрече с соответствующим антигеном, инфектом) стимулирует размножение вируса, а последующая гибель (апоптоз) этих клеток приводит к выделению вирусных частиц [7] в крипты и слюну. В инфицированных вирусом клетках возможно два вида размножения: литический, то есть приводящий к гибели, лизису, клетки-хозяина, и латентный, когда число вирусных копий небольшое и клетка не разрушается. ВЭБ может длительно находиться в В-лимфоцитах и эпителиоцитах назофарингеальной области и слюнных желез. Кроме того, он способен инфицировать другие клетки: Т-лимфоциты, NK-клетки, макрофаги, нейтрофилы, эпителиоциты сосудов [1, 6, 8, 9]. В ядре клетки-хозяина ДНК ВЭБ может формировать кольцевую структуру — эписому, либо встраиваться в геном, вызывая хромосомные нарушения [14].
При острой или активной инфекции преобладает литическая репликация вируса.
Активное размножение вируса может происходить в результате ослабления иммунологического контроля, а также стимуляции размножения клеток, инфицированных вирусом под действием целого ряда причин: острой бактериальной или вирусной инфекции, вакцинации, стрессов и др.
По данным большинства исследователей, сегодня примерно 80—90% населения инфицировано ВЭБ. Первичная инфекция чаще возникает в детском или молодом возрасте. Пути передачи вируса различны: воздушно-капельный, контактно-бытовой, трансфузионный, половой, трансплацентарный. После заражения ВЭБ репликация вируса в организме человека и формирование иммунного ответа могут протекать бессимптомно либо проявляться в виде незначительных признаков ОРВИ. Но при попадании большого количества инфекта и/или наличии в данный период значимого ослабления иммунной системы у пациента может развиться картина инфекционного мононуклеоза. Возможно несколько вариантов исхода острого инфекционного процесса:
Ближайший и отдаленный прогноз для больного с острой инфекцией, вызванной ВЭБ, зависит от наличия и степени выраженности иммунной дисфункции, генетической предрасположенности к тем или иным ВЭБ-ассоциированным заболеваниям (см. выше), а также от наличия ряда внешних факторов (стрессы, инфекции, операционные вмешательства, неблагоприятное воздействие окружающей среды), повреждающих иммунную систему. Было обнаружено, что ВЭБ обладает большим набором генов, дающим ему возможность в определенной мере ускользать от иммунной системы человека. В частности, ВЭБ вырабатывает белки — аналоги ряда человеческих интерлейкинов и их рецепторов, изменяющих иммунный ответ [5]. В период активного размножения вирус продуцирует ИЛ-10-подобный белок, который подавляет Т-клеточный иммунитет, функцию цитотоксических лимфоцитов, макрофагов, нарушает все этапы функционирования естественных киллеров (то есть важнейших систем противовирусной защиты). Другой вирусный белок (BI3) также может подавлять Т-клеточный иммунитет и блокировать активность клеток-киллеров (через подавление интерлейкина-12). Еще одно свойство ВЭБ, как и других герпес-вирусов, высокая мутабельность, позволяет ему на определенное время избегать воздействия специфических иммуноглобулинов (которые были наработаны к вирусу до его мутации) и клеток иммунной системы хозяина. Таким образом, размножение ВЭБ в организме человека может явиться причиной усугубления (возникновения) вторичного иммунодефицита.
Клинические формы хронической инфекции, вызванной вирусом Эпштейна—Барр
Хроническая активная ВЭБ-инфекция (ХА ВЭБИ) характеризуется длительным рецидивирующим течением и наличием клинических и лабораторных признаков вирусной активности [9]. Пациентов беспокоят слабость, потливость, нередко — боли в мышцах и суставах, наличие кожных высыпаний, кашель, затрудненное носовое дыхание, дискомфорт в горле, боли, тяжесть в правом подреберье, прежде нехарактерные для данного больного головные боли, головокружение, эмоциональная лабильность, депрессивные расстройства, нарушение сна, снижение памяти, внимания, интеллекта. Часто наблюдаются субфебрильная температура, увеличение лимфоузлов, гепатоспленомегалия различной степени выраженности. Нередко эта симптоматика имеет волнообразный характер. Иногда больные описывают свое состояние как хронический грипп.
У значительной части больных с ХА ВЭБИ наблюдается присоединение других герпетических, бактериальных и грибковых инфекций (герпес-лабиалис, генитальный герпес, молочница, воспалительные заболевания верхних дыхательных путей и желудочно-кишечного тракта).
ХА ВЭБИ характеризуется лабораторными (косвенными) признаками вирусной активности, а именно относительным и абсолютным лимфомоноцитозом, наличием атипичных мононуклеаров, реже моноцитозом и лимфопенией, в ряде случаев анемией и тромбоцитозом. При исследовании иммунного статуса у больных ХА ВЭБИ наблюдаются изменение содержания и функции специфических цитотоксических лимфоцитов, естественных киллеров, нарушение специфического гуморального ответа (дисиммуноглобулинемия, длительное отсутствие наработки иммуноглобулина G (IgG) или так называемое отсутствие сероконверсии к позднему нуклеарному антигену вируса — EBNA, что отражает несостоятельность иммунологического контроля размножения вируса. Кроме того, по нашим данным, более чем у половины больных снижена способность к стимулированной продукции интерферона (ИФН), повышено содержание сывороточного ИФН, имеют место дисиммуноглобулинемия, нарушение авидности антител (их способности прочно связываться с антигеном), уменьшено содержания DR+лимфоцитов, нередко повышены показатели циркулирующих иммунных комплексов и антител к ДНК.
У лиц с выраженной иммунной недостаточностью возможно возникновение генерализованных форм ВЭБ-инфекции с поражением центральной и периферической нервной систем (развитие менингита, энцефалита, мозжечковой атаксии, полирадикулоневритов), а также с поражением других внутренних органов (развитие миокардита, гломерулонефрита, лимфоцитарного интерстициального пневмонита, тяжелых форм гепатита). Генерализованные формы ВЭБ-инфекции нередко заканчиваются летальным исходом [10, 15].
ВЭБ-ассоциированный гемофагоцитарный синдром характеризуется развитием анемии или панцитопении. Часто сочетается с ХА ВЭБИ, инфекционным мононуклеозом и лимфопролиферативными заболеваниями. В клинической картине преобладают интермиттирующая лихорадка, гепатоспленомегалия, лимфоаденопатия, панцитопения или выраженная анемия, печеночная дисфункция, коагулопатия. Гемофагоцитарный синдром, развивающийся на фоне инфекционного мононуклеоза, характеризуется высокой летальностью (до 35%). Вышеописанные изменения объясняют гиперпродукцией провоспалительных цитокинов (ФНО, ИЛ1 и ряда других) Т-клетками, инфицированными вирусом. Эти цитокины активируют систему фагоцитов (размножение, дифференцировку и функциональную активность) в костном мозге, периферической крови, печени, селезенке, лимфоузлах. Активированные моноциты и гистиоциты начинают поглощать клетки крови, что приводит к их разрушению. Более тонкие механизмы этих изменений находятся в стадии изучения.
Стертые варианты хронической ВЭБ-инфекции
По нашим данным, ХА ВЭБИ нередко протекает стерто или под масками других хронических заболеваний.
Можно выделить две наиболее часто встречающиеся формы латентной вялой ВЭБ-инфекции. В первом случае больных беспокоит длительный субфебрилитет неясного генеза, слабость, боли в периферических лимфоузлах, миалгии, артралгии. Характерна также волнообразность симптоматики [11]. У другой категории больных помимо вышеописанных жалоб имеют место маркеры вторичного иммунодефицита в виде ранее нехарактерных для них частых инфекций дыхательных путей, кожи, желудочно-кишечного тракта, гениталий, которые на фоне терапии полностью не проходят или же быстро рецидивируют. Наиболее часто в анамнезе этих пациентов имеют место длительные стрессовые ситуации, чрезмерные психические и физические перегрузки, реже — увлечение голоданием, модными диетами и т. д. Нередко вышеописанное состояние развивалось после перенесенной ангины, ОРЗ, гриппоподобного заболевания. Характерными для этого варианта инфекции также являются устойчивость и длительность симптоматики — от шести месяцев до 10 и более лет. При повторных обследованиях обнаруживают ВЭБ в слюне и/или лимфоцитах периферической крови. Как правило, повторные углубленные обследования, проводимые у большинства этих пациентов, не позволяют обнаружить других причин длительного субфебрилитета и развития вторичного иммунодефицита.
Очень важен для постановки диагноза ХА ВЭБИ является и тот факт, что в случае устойчивого подавления вирусной репликации удается достичь длительной ремиссии у большинства пациентов. Диагностика ХА ВЭБИ затруднена из-за отсутствия специфических клинических маркеров заболевания. Определенный «вклад» в гиподиагностику вносит и недостаточная информированность практических врачей о данной патологии. Тем не менее, учитывая прогрессирующий характер ХА ВЭБИ, а также серьезность прогноза (риск развития лимфопролиферативных и аутоиммунных заболеваний, высокая летальность при развитии гемофагоцитарного синдрома), при подозрении на ХА ВЭБИ необходимо проводить соответствующее обследование. Наиболее характерный клинический симптомокомплекс при ХА ВЭБИ — это длительный субфебрилитет, слабость и снижение работоспособности, боли в горле, лимфаденопатия, гепатоспленомегалия, печеночная дисфункция, психические нарушения. Важным симптомом является отсутствие полного клинического эффекта от проведения общепринятой терапии астенического синдрома, общеукрепляющей терапии, а также от назначения антибактериальных препаратов.
При проведении дифференциальной диагностики ХА ВЭБИ в первую очередь следует исключить следующие заболевания:
Лабораторные исследования в диагностике ВЭБ-инфекции
Как уже упоминалось выше, все перечисленные изменения не являются строго специфичными для ВЭБ-инфекции (их можно обнаружить и при других вирусных инфекциях).
По нашим данным, в иммунном статусе при ВЭБ-инфекции встречаются два вида изменений: повышенная активность отдельных звеньев иммунной системы и/или дисбаланс и недостаточность других. Признаками напряженности противовирусного иммунитета могут быть повышенные уровни ИФН в сыворотке крови, IgА, IgМ, IgЕ, ЦИК, нередко — появление антител к ДНК, повышение содержания естественных киллеров (CD16+), Т-хелперов (CD4+) и/или цитотоксических лимфоцитов (CD8+). Система фагоцитов может быть активирована.
В свою очередь, иммунная дисфункция/недостаточность при этой инфекции проявляется снижением способности к стимулированной продукции ИФН альфа и/или гамма, дисиммуноглобулинемией (снижение содержания IgG, реже IgА, повышение содержания Ig М), снижением авидности антител (их способности прочно связываться с антигеном), снижением содержания DR+лимфоцитов, CD25+ лимфоцитов, то есть активированных Т-клеток, уменьшением числа и функциональной активности естественных киллеров (CD16+), Т-хелперов (CD4+), цитотоксических Т-лимфоцитов (CD8+), снижением функциональной активности фагоцитов и/или изменением (извращением) их реакции на стимулы, в том числе на иммунокорректоры.
Специфические IgM-АТ появляются в острой фазе заболевания или в период обострения и через четыре–шесть недель, как правило, исчезают. IgG-АТ к ЕА (ранние) также появляются в острой фазе, являются маркерами активной репликации вируса и при выздоровлении снижаются за три–шесть месяцев. IgG-АТ к VCA (ранние) определяются в остром периоде с максимумом ко второй–четвертой неделе, затем их количество снижается, и пороговый уровень сохраняется длительное время. IgG-АТ к EBNA выявляются спустя два — четыре месяца после острой фазы, и их выработка сохраняется в течение всей жизни.
По нашим данным, при ХА ВЭБИ более чем у половины больных в крови определяются «ранние» IgG-АТ, в то время как специфические IgM-АТ определяются значительно реже, при этом содержание поздних IgG-АТ к EBNA колеблется в зависимости от стадии обострения и состояния иммунитета.
Надо отметить, что проведение серологического исследования в динамике помогает в оценке состояния гуморального ответа и эффективности противовирусной и иммунокорригирующей терапии.
Использование данного метода в клинической практике для выявления того или иного внутриклеточного агента из-за слишком высокой его чувствительности нередко затруднено, так как нет возможности отличить здоровое носительство (минимальное количество инфекта) от проявлений инфекционного процесса с активным размножением вируса. Поэтому для клинических исследований используют ПЦР-методику с заданной, более низкой чувствительностью. Как показали наши исследования, применение методики с чувствительностью 10 копий в пробе (1000 ГЭ/мл в 1 мл образца) позволяет выявлять здоровых носителей ВЭБ, в то время как снижение чувствительности метода до 100 копий (10000 ГЭ/мл в 1 мл образца) дает возможность диагностировать лиц с клинико-иммунологическими признаками ХА ВЭБИ.
Мы наблюдали больных с наличием клинических и лабораторных данных (в том числе результатов серологических исследований), характерных для вирусной инфекции, у которых при первичном обследовании анализ на ДНК ВЭБ в слюне и клетках крови был отрицательным. Важно отметить, что в этих случаях нельзя исключить репликацию вируса в желудочно-кишечном тракте, костном мозге, коже, лимфоузлах и др. Только повторное обследование в динамике может подтвердить или исключить наличие или отсутствие ХА ВЭБИ.
Таким образом, для постановки диагноза ХА ВЭБИ помимо проведения общеклинического обследования необходимы исследование иммунного статуса (противовирусного иммунитета), ДНК, диагностика инфекции в различных материалах в динамике, серологические исследования (ИФА).
Лечение хронической Эпштейн—Барр-вирусной инфекции
В настоящее время общепринятых схем лечения ХА ВЭБИ не существует. Однако современные представления о влиянии ВЭБ на организм человека и данные об имеющемся риске развития серьезных, нередко фатальных заболеваний показывают необходимость проведения терапии и диспансерного наблюдения у больных, страдающих ХА ВЭБИ.
Данные литературы и опыт нашей работы позволяют дать патогенетически обоснованные рекомендации по терапии ХА ВЭБИ. В комплексном лечении данного заболевания используют следующие препараты:
Другие группы лекарств, как правило, играют вспомогательную роль.
До начала лечения желательно обследовать членов семьи больного на предмет выделения вирусов (со слюной) и возможности повторного инфицирования пациента, при необходимости подавление вирусной репликации проводят и у членов семьи.
Препаратом выбора является интерферон-альфа, в среднетяжелых случаях назначаемый в виде монотерапии [14]. Хорошо зарекомендовал себя (в том, что касается биологической активности и переносимости) отечественный рекомбинантный препарат реаферон, при этом стоимость его существенно ниже, чем у зарубежных аналогов. Используемые дозы ИФН-альфа различаются в зависимости от веса, возраста, переносимости препарата. Минимальные дозы — 2 млн. ЕД в сутки (по 1 млн. ЕД два раза в день внутримышечно), первую неделю ежедневно, затем три раза в неделю в течение трех–шести месяцев. Оптимальные дозы — 4–6 млн. ЕД (по 2—3 млн. ЕД два раза в день).
ИФН-альфа, как провоспалительный цитокин, может вызвать гриппоподобную симптоматику (лихорадка, головные боли, головокружение, миалгии, артралгии, вегетативные расстройства — изменение АД, ЧСС, реже диспептические явления).
Выраженность указанных симптомов зависит от дозы и индивидуальной переносимости препарата. Это преходящие симптомы (исчезают через 2—5 дней от начала лечения), и часть из них контролируется назначением нестероидных противовоспалительных средств. При лечении препаратами ИФН-альфа могут возникать обратимые тромбоцитопения, нейтропения, кожные реакции (зуд, сыпи разнообразного характера), редко — алопеция. Длительное применение ИФН-альфа в больших дозах может привести к иммунной дисфункции, клинически проявляющейся фурункулезом, другими гнойничковыми и вирусными поражениями кожи.
В среднетяжелых и тяжелых случаях, а также при неэффективности препаратов ИФН-альфа к лечению необходимо подключать аномальные нуклеодиты — валацикловир (валтрекс), ганцикловир (цимевен) или фамцикловир (фамвир).
Курс лечения аномальными нуклеотидами должен составлять не менее 14 дней, первые семь дней желательно внутривенное введение препарата.
В случаях тяжелого течения ХА ВЭБИ в комплексную терапию включают также препараты иммуноглобулинов для внутривенного введения в дозе 10—15 г. При необходимости (по результатам иммунологического обследования) — назначают иммунокорректоры с Т-активирующей способностью или замещающие тимические гормоны (тимоген, иммунофан, тактивин, и др.) в течение одного-двух месяцев с постепенной отменой или переходом на поддерживающие дозы (два раза в неделю).
Лечение ВЭБ-инфекции необходимо проводить под контролем клинического анализа крови (один раз в 7—14 дней), биохимического анализа (один раз в месяц, при необходимости чаще), иммунологического исследования — через один-два месяца.
К противовирусной терапии препаратами ИФН-альфа и аномальными нуклеотидами в первую очередь подключают системные кортикостероиды в дозах: парентерально (в пересчете на преднизолон) 120–180 мг в сутки, или 1,5–3 мг/кг, возможно использование пульс-терапии метипредом 500 мг в/в капельно, или внутрь по 60–100 мг в сутки. Внутривенно вводят плазму и/или препараты иммуноглобулинов для внутривенного введения. При выраженной интоксикации показаны введение детоксицирующих растворов, плазмаферез, гемосорбция, назначение антиоксидантов. В тяжелых случаях применяют цитостатики: этопозид, циклоспорин (сандиммун или консупрен).
Лечение назначают при появлении клиники ВЭБ-инфекции или при формировании признаков ВИД.
Проведение комплексной терапии с включением указанных выше препаратов позволяет добиться ремиссии заболевания у части пациентов с генерализованной формой заболевания и при гемофагоцитарном синдроме. У больных со среднетяжелыми проявлениями ХА ВЭБИ и в случаях стертого течения заболевания эффективность терапии выше (70—80%) помимо клинического эффекта часто удается добиться подавления репликации вируса.
После подавления размножения вируса и получения клинического эффекта важно продлить ремиссию. Показано проведение санаторно-курортного лечения.
Больных следует информировать о важности соблюдения режима труда и отдыха, полноценного питания, ограничения/прекращения приема алкоголя; при наличии стрессовых ситуаций необходима помощь психотерапевта. Кроме того, при необходимости проводят поддерживающую иммунокорригирующую терапию.
Таким образом, лечение больных с хронической Эпштейн—Барр-вирусной инфекцией является комплексным, проводится под лабораторным контролем и включает применение препаратов интерферона-альфа, аномальных нуклеотидов, иммунокорректоров, заместительных иммунотропных препаратов, глюкокортикоидных гормонов, симптоматических средств.
Литература
И. К. Малашенкова, кандидат медицинских наук
Н. А. Дидковский, доктор медицинских наук, профессор
Ж. Ш. Сарсания, кандидат медицинских наук
М. А. Жарова, Е. Н. Литвиненко, И. Н. Щепеткова, Л. И. Чистова, О. В. Пичужкина
НИИ физико-химической медицины МЗ РФ
Т. С. Гусева, О. В. Паршина
ГУНИИ эпидемиологии и микробиологии им. Н. Ф. Гамалеи РАМН, Москва
Клиническая иллюстрация случая хронической активной ВЭБ-инфекции с гемофагоцитарным синдромом
Больная И. Л., 33 лет, обратилась в лабораторию клинической иммунологии НИИ ФХМ 20.03.97 с жалобами на длительный субфебрилитет, выраженную слабость, потливость, боли в горле, сухой кашель, головные боли, одышку при движении, учащенное сердцебиение, нарушения сна, эмоциональную лабильность (повышенную раздражительность, обидчивость, плаксивость), забывчивость.
Из анамнеза: осенью 1996 года после тяжелой ангины (сопровождавшейся сильной лихорадкой, интоксикацией, лимфоаденопатией) возникли вышеуказанные жалобы, длительно сохранялись увеличение СОЭ, изменения лейкоцитарной формулы (моноцитоз, лейкоцитоз), была выявлена анемия. Амбулаторное лечение (антибиотикотерапия, сульфаниламиды, препараты железа и др.) оказалось неэффективным. Состояние прогрессивно ухудшалось.
При поступлении: t тела — 37,8°С, кожные покровы повышенной влажности, выраженная бледность кожи и слизистых. Лимфоузлы (подчелюстные, шейные, подмышечные) увеличены до 1-2 см, плотноэластической консистенции, болезненные, не спаяны с окружающими тканями. Зев гиперемирован, отечен, явления фарингита, миндалины увеличены, рыхлые, умеренно гиперемированы, язык обложен бело-серым налетом, гиперемирован. В легких дыхание с жестким оттенком, рассеянные сухие хрипы на вдохе. Границы сердца: левая увеличена на 0,5 см влево от среднеключичной линии, тоны сердца сохранены, короткий систолический шум над верхушкой, ритм неправильный, экстрасистолия (5—7 в мин), ЧСС — 112 в мин, АД — 115/70 мм рт ст. Живот вздут, умеренно болезненный при пальпации в правом подреберье и по ходу толстой кишки. По данным УЗИ органов брюшной полости, незначительное увеличение размеров печени и — в несколько большей степени — селезенки.
Из лабораторных анализов обращали на себя внимание нормохромная анемия со снижением Hb до 80 г/л с анизоцитозом, пойкилоцитозом, полихроматофилией эритроцитов; ретикулоцитоз, нормальное содержание сывороточного железа (18,6 мкм/л), отрицательная реакция Кумбса. Кроме того, наблюдались лейкоцитоз, тромбоцитоз и моноцитоз с большим количеством атипичных мононуклеаров, ускорение СОЭ. В биохимических анализах крови отмечались умеренное повышение трансаминаз, КФК. ЭКГ: ритм синусовый, неправильный, предсердная и желудочковая экстрасистолия, ЧСС до 120 в минуту. Электрическая ось сердца отклонена влево. Нарушение внутрижелудочковой проводимости. Снижение вольтажа в стандартных отведениях, диффузные изменения миокарда, в грудных отведениях наблюдались изменения, характерные для гипоксии миокарда. Также был существенно нарушен иммунный статус — повышено содержание иммуноглобулина М (IgМ) и снижено иммуноглобулинов А и G (IgА и IgG), наблюдалось преобладание продукции низкоавидных, то есть функционально неполноценных антител, дисфункция Т-звена иммунитета, повышение уровня сывороточного ИФН, снижение способности к продукции ИФН в ответ на многие стимулы.
В крови были повышены титры IgG-антител к ранним и поздним вирусным антигенам (VCA, EA EBV). При вирусологическом исследовании (в динамике) методом полимеразной цепной реакции (ПЦР) в лейкоцитах периферической крови была обнаружена ДНК ВЭБ.
В эту и последующие госпитализации проводились углубленное ревматологическое обследование и онкологический поиск, были исключены также другие соматические и инфекционные заболевания.
Больной были поставлены следующие диагнозы: хроническая активная ВЭБ-инфекция, умеренная гепатоспленомегалия, очаговый миокардит, соматогенно обусловленная персистирующая депрессия; вирусассоциированный гемофагоцитарный синдром. Иммунодефицитное состояние; хронический фарингит, бронхит смешанной вирусно-бактериальной этиологии; хронический гастрит, энтерит, дисбиоз кишечной флоры.
Несмотря на проведенную беседу, от введения глюкокортикоидов и препаратов интерферона-альфа больная категорически отказалась. Было проведено лечение, включающее противовирусную терапию (виролекс внутривенно в течение недели, с переходом на зовиракс 800 мг 5 раз в день per os), иммунокорригирующую терапию (тимоген по схеме, циклоферон 500 мг по схеме, иммунофан по схеме), заместительную терапию (октагам по 2,5 г два раза внутривенно капельно), детоксикационные мероприятия (инфузии гемодеза, энтеросорбция), антиоксидантную терапию (токоферрол, аскорбиновая кислота), использовали препараты-метаболики (эссенциале, рибоксин), назначалась витаминотерапия (поливитамины с микроэлементами).
После проведенного лечения у больной нормализовалась температура, уменьшились слабость, потливость, улучшились некоторые показатели иммунного статуса. Однако полностью подавить репликацию вируса не удалось (ВЭБ продолжал определяться в лейкоцитах). Клиническая ремиссия продолжалась недолго — через полтора месяца наступило повторное обострение. При исследовании помимо признаков активации вирусной инфекции, анемии, ускорения СОЭ были выявлены высокие титры антител к сальмонелле. Проводилось амбулаторное лечение основного и сопутствующего заболевания. Тяжелое обострение началось в январе 1998 года после острого бронхита и фарингита. По данным лабораторных исследований, в этот период отмечались утяжеление анемии (до 76 г/л) и нарастание количества атипичных мононуклеаров в крови. Отмечалось нарастание гепатоспленомегалии, в мазке из зева найдены Chlamidia Trachomatis, золотистый стафилококк, стрептококк, в моче — Ureaplasma Urealiticum, в крови обнаружено существенное повышение титров антител к EBV, CMV, вирусу простого герпеса 1-го типа (HSV 1). Таким образом, у больной увеличивалось число сопутствующих инфекций, что также свидетельствовало о нарастании недостаточности иммунитета. Проводилась терапия индукторами интерферона, заместительная терапия Т-активаторами, антиоксидантами, метаболиками, длительная детоксикация. Заметный клинический и лабораторный эффект был достигнут к июню 1998 года, пациентке рекомендовано продолжить метаболическую, антиоксидантную, иммунозаместительную терапию (тимоген и др.). При повторном исследовании осенью 1998 года в слюне и лимфоцитах ВЭБ не определялся, хотя сохранялись умеренная анемия и иммунная дисфункция.
Таким образом, у больной И., 33 лет, острая ВЭБ-инфекция приняла хроническое течение, осложнилась развитием гемофагоцитарного синдрома. Несмотря на то что удалось достигнуть клинической ремиссии, больная нуждается в динамическом наблюдении с целью как контроля репликации ВЭБ, так и своевременной диагностики лимфопролиферативных процессов (учитывая высокий риск их развития).