Синдром раздражённого кишечника
Классификация синдрома раздражённого кишечника
Причины синдрома раздражённого кишечника
Считается, что неправильная работа нервной системы играет важную роль в возникновении синдрома раздражённого кишечника. Под влиянием психологического стресса, у некоторых людей слизистая оболочка кишки становится очень чувствительной. При этом интенсивность восприятия боли становится не адекватной вызывающему ее стимулу. Болевые импульсы от кишки приходят в головной мозг. В ответ на полученный сильный импульс возникает нарушение двигательной активности кишки, проявляющееся болями в животе, вздутием, поносами или запорами.
У некоторых пациентов инфекция и воспаление могут играть ключевую роль в появлении симптомов СРК. Эти симптомы могут длиться в течение месяцев и лет после того, как инфекция и воспаление уменьшатся.
К возможным причинам развития СРК также относятся избыточный рост бактерий, некачественное питание, употребление большого количества газообразующих продуктов, жирная пища, избыток кофеина, злоупотребление алкоголем, недостаток в рационе продуктов с пищевыми волокнами, переедание. Жир животного или растительного происхождения является сильным биологическим стимулятором двигательной активности кишечника.
Таким образом, СРК в настоящее время рассматривается как результат взаимодействия разнообразных биологических и психосоциальных факторов. Нарушение моторики, повышенная чувствительность слизистой оболочки кишечника, нарушения регуляции желудочно-кишечного тракта со стороны центральной нервной системы, вегетативные и гормональные нарушения, генетические факторы, последствия инфекций и психологические проблемы разной степени тяжести могут спровоцировать симтомы СРК.
Симптомы синдрома раздражённого кишечника
Синдром раздражённого характеризуется многообразием клинических проявлений.

Вздутие живота обычно возрастает в течение дня, достигая максимума к вечеру, и заметно усиливается после еды.
Диарея. При диарее стул чаще всего отмечается в утренние часы, после завтрака. Количество опорожнений кишечника может достигать до 5 раз в день, с небольшими временными промежутками. Позывы на дефекацию могут возникать после каждого приёма пищи. Характерно также появление позывов на дефекацию в ситуациях, когда ее совершение не представляется возможной, например, на совещание, во время поездки в транспорте, во время экзамена, при стрессовых ситуациях. Количество кала остаётся нормальной, и, как правило, не превышает 200 граммов в сутки. Часто остаётся чувство неполного опорожнения кишечника. В стуле могут присутствовать слизь, непереваренные кусочки пищи. Перед актом дефекации отмечается усиление болей и значительное уменьшение их после него.
По мимо основных симптомов при СРК, может быть ощущение кома в горле при глотании, боли в эпигастральной области, чувство быстрого насыщения, тошнота и боли в правом подреберье, боли в левой половине грудной клетки, в мышцах, в суставах, в спине, головные боли, сердцебиение, ощущение перебоев в работе сердца, учащённое мочеиспускание, снижение веса, шум в ушах, чувство слабости и сухость во рту.
При СРК часто возникает сильный дискомфорт и недомогание, что очень сильно раздражает больного. Но не смотря на это, этот синдром не наносит сильного вреда кишечнику, не вызывает кишечное кровотечение, рак или воспалительные заболевания, такие как болезнь Крона или неспецифический язвенный колит.
Диагностика синдрома раздражённого кишечника
Диагноз СРК является диагнозом исключения. Больные предъявляют жалобы, которые могут сопровождать течение неблагоприятных органических заболеваний. Исключив их врач может остановиться на диагнозе синдрома раздражённого кишечника.
Процесс диагностики СРК проходит в несколько этапов.
В начале проводятся ряд диагностических тестов, которые включают в себя клинический и биохимический анализы крови, копрологическое исследование с анализом кала на яйца глистов и цисты лямблий, ЭГДС, УЗИ органов брюшной полости и малого таза, сигмо– или колоноскопию и ирригоскопию.
При болевой форме наибольшую ценность могут иметь такие диагностические исследования, как электрогастроэнтерография, манометрия, баллонно–дилатационный тест, при диарейной форме – лактозотолерантный тест, аспирация содержимого тонкой кишки для исследования бактериальной флоры, при запорах – радиоизотопное исследование транзита, электрогастроэнтерография, изучение аноректальных функций, включающее аноректальную манометрию.
После предварительной постановки диагноза назначают первичный курс лечения, по результатам которого вновь обращаются к диагностическим исследованиям. При эффективности лечения может быть выставлен окончательный диагноз СРК, при неэффективности – проводится дополнительное обследование.
Лечение синдрома раздражённого кишечника
Следует хорошо пережёвывать пищу. Необходимо выяснить, нет ли какой-либо сильной непереносимости некоторых пищевых продуктов, которые вызывают дискомфорт в кишечнике. К ним относятся: кофе, черный чай, матэ, напитки, содержащие кофеин, и сигареты.
Необходимо привести нервную систему в равновесие. Для этого можно принимать гармонизирующий чай, состоящий из корней валерьяны, листочков мелиссы и ромашки. Для раздражённого кишечника благотворны также хмель и страстоцвет (пассифлора), которые предлагаются в основном в готовых препаратах, таблетках, каплях, чае.
Врачи относят синдром раздражённого кишечника к рубрике K58, синдром раздражённого кишечника с диареей к рубрике К58.0, синдром раздражённого кишечника без диареи к К58.9 в Международной классификации болезней МКБ-10.
СИНДРОМ РАЗДРАЖЕННОГО КИШЕЧНИКА
МГМСУ им. А.И. Евдокимова
Синдромом раздраженного кишечника ежегодно заболевает около 1% населения мира. Подчас этот синдром ощутимо снижает качество жизни пациентов, особенно если учесть частое его сочетание с другими функциональными заболеваниями, например c функциональной диспепсией и/или синдромом раздраженного мочевого пузыря.
Согласно Римским критериям последнего, IV пересмотра (2016 г.), синдром раздраженного кишечника — это функциональное расстройство кишечника, которое сопровождается периодическими болями в животе со средней частотой не реже 1 дня в неделю за последние 3 месяца, при условии, что эти боли отвечают ≥ 2 следующим критериям:
Еще одно обязательное условие соответствия указанных признаков синдрому раздраженного кишечника (СРК) — их наличие у пациента на протяжении последних 3 месяцев при общей продолжительности жалоб ≥ 6 месяцев.
В зависимости от типа стула выделяют 4 вида (типа) заболевания:
Коды СРК по МКБ 10:
ЭПИДЕМИОЛОГИЯ
Начало развития СРК зачастую приходится на молодые годы, затем его распространенность снижается. Отметим, что диагноз СРК сомнителен в случае возникновения патогномоничных симптомов у людей старше 60 лет, что диктует необходимость исключения органической патологии.
Во многих странах мира у женщин симптомы СРК наблюдаются чаще (примерно в 2 раза), чем у мужчин. Заболевание чаще встречается у городских жителей.
ЭТИОЛОГИЯ
Этиопатогенетические предпосылки возникновения СРК недостаточно изучены; предположительно они представляют собой совокупность множества факторов.
Большую роль в этиологии СРК играет психоэмоциональный фактор. Известный американский психиатр G. Engel предложил биопсихосоциальную модель болезни. По этой теории главный механизм развития СРК — нарушение координации между ЦНС и автономной нервной системой кишечника, обусловленное хроническим воздействием факторов внешней среды, стрессов при генетической предрасположенности пациента к этому расстройству. Отмечено, что у трети пациентов с клиническими проявлениями СРК ближайшие родственники имеют сходную симптоматику. У однояйцевых близнецов конкордантность в развитии СРК достигает 33%, в то время как у разнояйцевых — 13%.
Считается, что СРК во многих случаях является своеобразной формой невроза, при которой ведущими клиническими симптомами становятся кишечные расстройства (табл. 1).
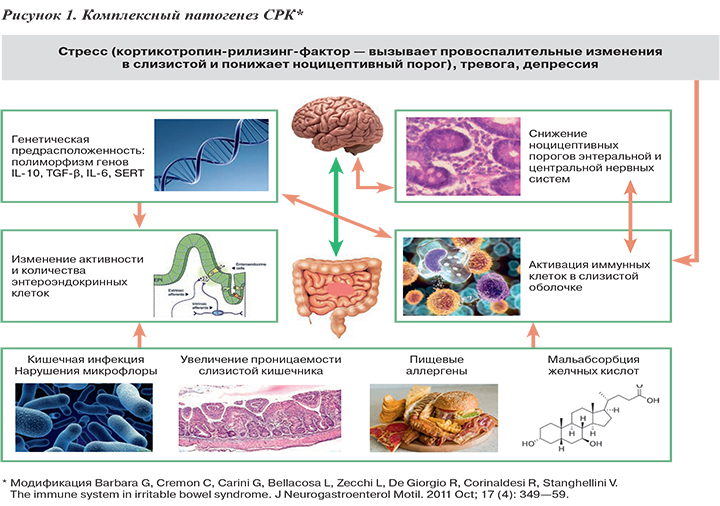
Повышение сократительной активности мышечного слоя стенки кишечника, спастическая активность является основной причиной возникновения болей в животе при СРК, и она связана с висцеральной гиперчувствительностью рецепторного аппарата. В основе гиперсенситивности при СРК лежат дисфункционально-дисрегуляторные нарушения, которые наблюдаются в корковых и подкорковых центрах, вегетативной нервной системе, периферическом нейрорецепторном аппарате кишечника с системой нейротрансмиттеров и биологически активных веществ (рис. 1).
Продолжают изучаться взаимосвязи возникновения СРК с перенесенными кишечными инфекциями («постинфекционный СРК»), нарушенной бактериальной флорой. Изменение микробного биоценоза — важный патогенетический механизм в развитии синдрома. Так, у пациентов с СРК имеется избыточная микробная контаминация в тонком кишечнике (68%) и дисбиоз в толстой кишке (98%). Вследствие возникающих дисбиотических процессов в толстый кишечник поступает химус, обладающий агрессивными свойствами. Это способствует расстройству моторно-секреторной функции ободочной и прямой кишки. Доказано, что серьезным фактором риска развития СРК служат острые бактериальные гастроэнтериты, т.к. по различным данным у 7—33% пациентов после кишечной инфекции развивается клиническая картина, подобная СРК-Д.
Вероятность развития СРК возрастает в 6 раз после острых желудочно-кишечных инфекций при наличии следующих факторов риска:
ДИАГНОСТИКА
Клинические проявления СРК включают:
Отметим, что в Римских критериях IV (2016 г.) по сравнению с Римскими критериями III (2006 г.) определение клинико-диагностических признаков СРК претер.
Синдром раздраженного кишечника у детей: основные причины и подходы к терапии
Синдром раздраженного кишечника (СРК) является самым распространенным функциональным заболеванием кишечника у взрослых и представляет значимую социальную проблему, влияя на качество жизни. В основе развития СРК лежит взаимодействие двух основных патогенетических механизмов: психосоциального воздействия и нарушения моторной функции толстой кишки, что проявляется повышением висцеральной чувствительности и изменением двигательной активности кишки.
В развитие заболевания имеют значение личностные и психологические аспекты, генетическая предрасположенность, факторы питания, изменение висцеральной гиперчувствительности, нарушения моторной активности и нейроэндокринной системы (ось «головной мозг — кишечник»), повышение проницаемости кишки, нарушение состава кишечной микробиоты. Качественные и количественные изменения микрофлоры оказывают влияние на функцию кишечника, выступая в качестве причины нарушений его двигательной активности, чувствительности и нейроиммунных взаимоотношений, включая нарушение экспрессии рецепторов слизистой оболочки и изменения функции гипоталамо-гипофизарно-надпочечниковой системы. В педиатрической практике возможности использования медикаментозных препаратов значительно ограничены возрастом пациентов. В терапии предпочтение необходимо отдавать селективным препаратам, влияющим на висцеральную чувствительность и пробиотикам с доказанной эффективностью и безопасностью штаммов.
Сведения об авторах:
Захарова Ирина Николаевна – д.м.н., профессор, заведующая кафедрой педиатрии им. Г.Н. Сперанского ФГБОУ ДПО «Российская медицинская академия непрерывного профессионального образования» Минздрава России; +7 (495) 496-52-38; e-mail: kafedra25@yandex.ru.
Сугян Нарине Григорьевна – кандидат медицинских наук, доцент кафедры педиатрии педиатрии им. Г.Н. Сперанского ФГБОУ ДПО «Российская медицинская академия непрерывного профессионального образования» Минздрава России;
Бережная Ирина Владимировна — кандидат медицинских наук, доцент кафедры педиатрии педиатрии им. Г.Н. Сперанского ФГБОУ ДПО «Российская медицинская академия непрерывного профессионального образования» Минздрава России.
Ключевые слова: дети, синдром раздраженной кишки, прокинетики, тримебутин, необутин, пробиотики, максилак.
Синдром раздраженного кишечника (СРК) является самым распространенным функциональным заболеванием кишечника у взрослых, представляя значимую социальную проблему с негативным влиянием на качество жизни. В большинстве стран мира частота встречаемости СРК составляет в среднем около 20%, варьируя от 9 до 48%. Мало информации о распространенности СРК у детей, например, в США по данным разных авторов частота составляет от 1,2 до 2,9% [1]. Оценить распространенность СРК в популяции трудно, т. к. статистические данные значимо различаются даже в разных регионах одной страны. Эпидемиологические показатели, обобщенные по данным опросников в разных странах мира, показывают, что чифры колеблются от 10 до 25%. По данным мета-анализа, суммарная распространенность заболевания оказалась около 11,2% (95% ДИ, 9,8–12,8) с различием в регионах земного шара: от самой низкой в Южной Азии (7%) до самой высокой в Южной Америке (21%). Показано, что первые несколько месяцев после установки диагноза «СРК» больные переносят до 4 атак с выраженной болью в животе. В дальнейшем у 30–40% увеличиваются светлые промежутки между обострениями. Примерно у половины пациентов с СРК (45%) развиваются хронические заболевания верхних отделов ЖКТ (диспепсия, хронический гастрит, ГЭРБ и др.) через несколько лет течения СРК.
Функциональные нарушения ЖКТ одна из самых загадочных проблем современной медицины, так как, несмотря на огромный спектр диагностических процедур, до конца понять этиологию и патогенез не представляется возможным. Уже около 30 лет мы используем клинические рекомендации, известные под названием Римские критерии. В 2016 году вышла новая редакция клинических рекомендаций функциональных нарушений ЖКТ – Рим IV, в которые входят разделы функциональных гастроинтестинальных расстройств ФГИР) у взрослых, детей и подростков. Появившаяся доказательная база в течение последних 10 лет обеспечила основу для рекомендаций «Рим IV пересмотра». При некоторых расстройствах органов пищеварения комитет использовал клинический опыт и консенсус членов комитета, все еще не имея достоверных научных данных, для этих разделов. В научной литературе можно встретить разные интерпретации перевода «functional gastrointestinal disorders» — функциональные гастроинтестинальные расстройства (ФГИР), функциональные расстройства органов пищеварения (ФРОП) и другие. ФРОП более полно отражает проблему, так как консенсус охватывает функциональные нарушения верхних и нижних отделов ЖКТ и расстройства билиарного тракта.
В критериях Рима III подчеркивалось, что для установления функциональных нарушений нужно исключить органическое заболевание. В Римских критериях IV пересмотра фраза «нет доказательств в пользу воспалительного, анатомического, метаболического или неопластического процесса, объясняющего симптомы у субъекта» был удален из диагностических критериев [2]. Вместо этого добавлено «после соответствующего медицинского обследования, симптомы не могут быть отнесены к другому заболеванию». Это изменение позволяет выборочное обследование для подтверждения положительного диагноза ФРОП. Также отмечено, что ФРОП могут сосуществовать с другими органическими и хроническими воспалительными заболеваниями [3]. Точно так же у одного пациента могут быть разные ФРОП. В последней версии рекомендаций международного консенсуса Римские критерии-IV (Rome-IV), опубликованной в 2016 г., функциональные кишечные расстройства рассматриваются как спектр кишечных симптомов в 6 категориях, которые определяются как расстройства взаимодействия «кишка — головной мозг» («ЖКТ — ЦНС (центральная нервная система») (disorders of gut-brain interaction) [4].
В новую редакцию Римских критериев IV (2016) включены новые расстройства, это функциональная тошнота и функциональная рвота. Изменена формулировка «боль в животе, связанная с функциональными желудочно-кишечными расстройствами» на «функциональные абдоминальные болевые расстройства». В эту группу внесен новый термин — функциональная абдоминальная боль (иным образом «FAP-NOS») для описания детей абдоминальной болью, диагностические критерии которых недостаточны для включения под определенное расстройство, например, СРК, функциональная диспепсия или абдоминальная мигрень.
Термин «дискомфорт» в новой редакции Римских критериях IV изъят из определения, поскольку сложно проводить грань между дискомфортом и абдоминальной болью у детей. Кроме того, как диагностический критерий, отсутствуют такие жалобы, как вздутие, растяжение или другие ощущения пациента [5].
В основе ФРОП лежат комбинированные физиологические и морфологические отклонения, связанные с висцеральной гиперчувствительностью, нарушениями моторики ЖКТ, защитного слизистого барьера, иммунной функции и состава кишечной микробиоты, а также расстройствами со стороны ЦНС.
В развитии ФРОП у детей в раннем возрасте немаловажную роль играют такие факторы, как морфофункциональная незрелость, недостаточная активность панкреатических и гастроинтестинальных ферментов, нарушение микробиоценоза, недостаточность мукозального иммунитета. В более старшем возрасте висцеральная гиперчувствительность обусловлена совокупностью факторов: социальными взаимоотношениями, стрессом, переутомлением, нарушением режима дня, отдыха.
В основе развития СРК лежит взаимодействие двух основных патогенетических механизмов: психосоциального воздействия и нарушения моторной функции толстой кишки, что проявляется повышением висцеральной чувствительности и нарушением двигательной функции кишки (таблица 1).
Таблица 1. Диагностические критерии СРК для детей (признаки должны присутствовать не менее 2 месяцев) [1].
Должны присутствовать следующие симптомы:
1. Абдоминальная боль не менее 4 дней в месяц, ассоциированная с 1 или более из следующих симптомов:
а. связано с дефекацией;
б. ассоциирована изменением частоты опорожнения;
c. ассоциирована с изменением формы (внешнего вида) стула.
2. При СРК с запором боль не проходит после опорожнения (если боль проходит после опорожнения, то у ребенка функциональный запор, а не СРК).
3. После соответствующей оценки симптомы не могут быть отнесены под другое заболевание.
Боль может быть различной интенсивности, локализуется, как правило, внизу живота, хотя может отмечаться и в других его отделах. Она часто усиливается при погрешностях в диете, психоэмоциональной нагрузке, переживаниях, также при физической нагрузке. Важно отметить, что абдоминальная боль исчезает в ночное время, когда ребенок спит.
Если боль проходит после опорожнения, то в этом случае, скорее всего, у ребенка имеет место функциональный запор, а не СРК с запором. Установлено, что у 75% детей, страдающих запором, присутствует абдоминальная боль, что подпадает под критерии СРК. Но и пациенты с СРК длительно наблюдаются с диагнозом функциональный запор не получая эффективной медицинской помощи. Комитет рекомендует пациентам с запором и абдоминальной болью на начальном этапе проводить лечение только от запора. Если боль в животе проходит после лечения запора, то у пациента функциональный запор. Если боль не проходит, вероятно, у ребенка имеет место СРК с запором. Аналогично, в случае возможного СРК с диареей. На первом этапе нужно исключить кишечную инфекцию с рецидивирующим, хроническим течением, целиакию, мальабсорбцию углеводов и реже воспалительное заболевание кишечника. Важно обратить внимание на тревожные сигналы («симптомы тревоги», «красные флаги»), при наличии которых нужно исключить органическую патологию органов ЖКТ. Указывается, что чем больше присутствует тревожных симптомов, тем выше вероятность органического заболевания (Таблица 2). Определение фекального кальпротектина все чаще используется как неинвазивный скрининг для исключения воспалительного заболевания кишечника (ВЗК) [6].
Таблица 2. Симптомы тревоги у пациентов с ФРОП.
| Семейный анамнез воспалительного заболевания кишечника, целиакии или язвенная болезнь; |
| Постоянная боль в правом верхнем или правом нижнем квадранте; |
| Дисфагия, одинофагия; |
| Рецидивирующая рвота; |
| Кровотечения из органов желудочно-кишечного тракта; |
| Ночная диарея; |
| Артрит; |
| Периректальные поражения; |
| Немотивированное похудание, потеря веса, недостаточность питания; |
| Задержка полового созревания; |
| Необъяснимая лихорадка; |
У детей, как и у взрослых, СРК можно разделить на разные типы, отражающие преобладающий характер стула (СРК с запор, СРК с диареей, СРК с запором и диарея и неуточненный СРК) и эти типы теперь включены в Рим IV [7].
Таблица 3. Функциональные расстройства органов пищеварения: нарушение взаимодействия ЖКТ и ЦНС по данным Римских критериев IV (коды Рим IV и МКБ-10).
С. Кишечные расстройства
С.1 Синдром раздраженного кишечника (СРК)
СРК с преобладанием запора (СРК-3)
СРК с преобладанием диареи (СРК-Д)
СРК смешанного типа (СРК-См)
Неклассифицируемый СРК (СРК-Н)
Формулировка
Коды Рим IV
МКБ-10
K59.0 запор
K58.2 Синдром раздраженного кишечника с преобладанием запоров
K59.1 Функциональная диарея
K58.1 Синдром раздраженного кишечника с преобладанием диареи
Функциональное абдоминальное вздутие/растяжение
R14 Метеоризм и родственные состояния
K59.9 Функциональное нарушение кишечника неуточненное
K58.8 Другой или неуточненный синдром раздраженного кишечника
Неспецифическое функциональное кишечное расстройство
K59.2 Неврогенная возбудимость кишечника, не классифицированная в других рубриках
K58.3 Синдром раздраженного кишечника со смешанными проявлениями
K59.0 Запор
Сложность этио-патогенеза заболевания у детей объясняется совокупностью факторов: личностные психологические аспекты, генетическая предрасположенность, факторы питания, развитие висцеральной гиперчувствительности, нарушения моторной активности, изменения в нейроэндокринной системе (ось «головной мозг — кишечник»), повышение проницаемости кишечника, нарушение состава кишечной микробиоты.
В научных исследованиях показано, что висцеральная гиперчувствительность может быть связана с детским психологическим стрессом (тревога, депрессия, импульсивность, гнев) [8].
У детей с СРК могут наблюдаться повышенный уровень стресса, беспокойства, депрессии и эмоциональных проблем, о которых они сообщают сами [9]. Тяжелые заболевания, требующие медицинского инвазивного вмешательства в раннем возрасте (например, операция) связаны с более высоким риском развития ФРОП у детей, включая СРК [10].
Патофизиология СРК включает воздействие внешних раздражающих факторов (стресс, высокая эмоциональная нагрузка, недостаток сна и т. д.), что возбуждает ЦНС, вегетативный ответ, с воздействием на нейроэндокринную систему кишечника, включая гипоталамо-гипофизарно-надпочечниковую (кортизол) систему. Это нарушает двигательную активность кишечника, усиливает спазм гладкой мускулатуры, нарушает пассаж кишечного содержимого. С другой стороны, изменения двигательной активности кишечника приводят к перевозбуждению внутрикишечных нервных волокон, клеток Кахаля, усиливая спазм гладких мышц, изменяется микробиота, что влияет на среду и синтез КЖК. Таким образом, возникает порочный круг (таблица 4).
Таблица 4. Патофизиология развития СРК: связь «головной мозг – кишка» [11].
Нарушение функционирования оси «головной мозг – кишка»
Кортикотропин-релизинг-фактор (CRF)
Активация энтеральной нервной системы
Изменение микробиоты
Активирует CRF-1 рецепторы → усиление моторики при стрессе
Провоспалительная активность → увеличение синтеза ИЛ-1 и ИЛ-2
Усиление ответа на эндотоксины
Повышение уровня кортизола и адреналина
Повышение сенситивности кишечных нервов
Нейротрансмиттеров → нарушение перистальтики
Повышенная дегрануляция тучных клеток → нарушение серотонинового сигнального каскада
Дисбаланс синтеза провоспалительных и воспалительных медиаторов
Повышение проницаемости кишечного барьера
Нарушение местного иммунитета
Экспрессия синтеза нейротрансмиттеров
(серотонин, ГАМК, гистамин, ацетилхолин, мелатонин и др.)
Нарушение слизистого барьера
и микробной биопленки
Модуляция кишечной чувствительности
афферентных волокон
Часто СРК развивается после перенесенной острой кишечной инфекции, отмечено повышение содержания провоспалительных цитокинов в слизистой оболочке ЖКТ и развивается постинфекционный СРК [12]. Систематический обзор, опубликованный в 2015 году, показал частоту регистрации постинфекционной функциональной диспепсии и СРК в популяции, включая детей 10,0% (ФД, n = 976; ОГЭ, n = 9737) и 13,1% (СРК, n = 1128; ОГЭ, n = 8624), соответственно. Так же указано длительное сохранение расстройств, установлено, что через 1 год после перенесенного о. гастроэнтерита постинфекционная функциональная диспепсия сохранилась у 13,5 % пациентов (n = 380; ОГЭ n = 2807) и синдром раздраженной кишки у 38,9% детей (n = 86 ; ОГЭ n = 221) [13].
В другом исследовании указана роль паразитарной инфекции (Balantidiumcoli, Strongyloidesstercoralis, Ascarislumbricoides, Necatoramericanus, Ancylostomaduodenale, Taeniasolium, Taeniasaginataи Hymenolepisnana) в развитии постинфекционных ФРОП, в частности в развитии СРК (OР составил: 1,69), функционального запора (Oр: 4,13) [14].
Роли кишечной микробиоты в патофизиологии СРК в настоящее время посвящено большое количество экспериментальных и клинических исследований. Были продемонстрированы изменения в микробиоме кишечника, хотя неясно, являются ли эти изменения причиной или результатом СРК и его симптомов [15].
Установлено, что качественные и количественные изменения микрофлоры оказывают влияние на функцию кишечника, выступая в качестве причины нарушений его двигательной активности, чувствительности и нейроиммунных взаимоотношений, включая нарушение экспрессии рецепторов слизистой оболочки и изменения функции гипоталамо-гипофизарно-надпочечниковой системы. Известно, что кишечная микрофлора утилизирует нерастворимые углеводы и выделяются метаболиты, среди них важное значение имеют короткоцепочечные жирные кислоты (уксусная, пропионовая и масляная кислоты). Именно эти короткоцепочечные жирные кислоты (КЦЖК) в разных отделах толстой кишки оказывают противоположное влияние на моторную ее активность, через стимуляцию определенных рецепторов, вырабатывающих биологически активные вещества. В проксимальных отделах толстой кишки КЦЖК стимулируют рецепторы L-клеток, которые вырабатывают регуляторный полипептид PYY, замедляющий двигательную активность не только толстой, но и тонкой кишки. А в дистальных отделах КЦЖК стимулируют рецепторы Ecl-клеток, вырабатывающих гистамин, который, действуя на 5-HT 4-рецепторы афферентных волокон блуждающего нерва, инициирует рефлекторное ускорение моторики. Среди КЦЖК, важное значение для колоноцитов имеет масляная кислота (бутират), которая является важнейшим энергетическим источником для колоноцитов, синтеза липидов мембран, защитного барьера и проницаемости слизистой оболочки толстой кишки, подавления окислительного стресса, воспаления, колоректального канцерогенеза, восстановления водно-электролитного баланса. Кроме этого, масляная кислота (бутират) оказывает регулирующее влияние на кишечную моторику [16].S.A.Vanhoutvin с соавт. изучали влияние масляной кислоты (бутирата) на висцеральную гиперчувствительность у здоровых добровольцев. Участникам исследования ректально вводили масляную кислоту. Результаты исследования показали, что введение масляной кислоты повышало порог болевой чувствительности и снижало боль и дискомфорт, вызванные раздуванием ректального баллона, что оценивалось по аналоговой шкале. При этом отмечено, что введение бутирата имело дозозависимый эффект, чем выше была доза бутирата, тем больше снижалась висцеральная чувствительность [17].
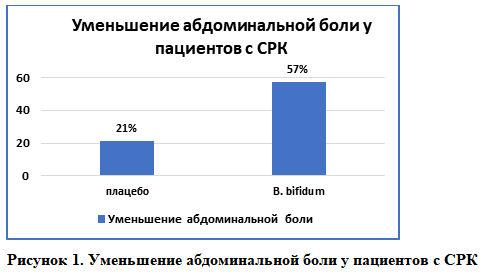
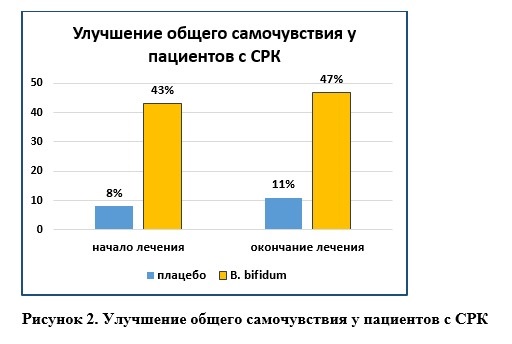
Применение одного из штаммов Bifidobacterium bifidum у пациентов с симптомами СРК приводило к значимому снижению таких симптомов как боль/дискомфорт в животе, метеоризм, нарушение пищеварения у 57% пациентов по сравнению с 21% в группе плацебо [19].
В метаанализе проводилась оценка результатов 24 клинических исследований с участием 2001 пациентов с СРК. Результаты анализа показали достоверное уменьшение симптомов боли и общих симптомов у пациентов при применении мультиштаммовых пробиотиков. Мультиштаммовые пробиотики оценивались в 12 РКИ с участием 1197 пациентов со значительным влиянием на симптом абдоминальной боли (ОР = 0,81; 95% ДИ 0,67–0,98, р 8 КОЕ, а также пребиотический компонент фруктоолигосахарид. Инновационная капсула DRcaps™, в свою очередь, нейтрализует негативное воздействие кислого содержимого желудка, солей желчных кислот и пищеварительных ферментов.
Ведущую роль в структуре абдоминального болевого синдрома наиболее часто играет спастическая висцеральная боль, в основе которой лежит непроизвольное сокращение гладких мышц кишечника, не сопровождающееся их немедленным расслаблением. Селективные миотропные спазмолитики имеют возрастные ограничения у детей. По клинической эффективности тримебутин сопоставим с такими спазмолитиками, как пинаверия бромид и мебеверин в терапии боли в животе при СРК у взрослых [27].
Проведена сравнительная оценка эффективности терапии препаратами, координирующими моторику кишечника (тримебутин) как монотерапии, так и в комбинации с пробиотиками у детей в возрасте 5-17 лет с симптомами СРК. В первой группе (n=15) проводилась терапия тримебутином в возрастной дозировке курсом 1 месяц, во второй группе (n=15) проводилась комбинированная терапия тримебутин + пробиотики. Авторы определяли уровень фекального кальпротектина (белка, отражающего выраженность воспалительного процесса), как показателя воспаления в кишечнике. Уровень кальпротектина у пациентов с СРК был исходно повышен у 27,3% детей, средний уровень показателя превышал нормальные показатели в 2 раза.
Полученные результаты показали высокую эффективность тримебутина (у 82% детей) при монотерапии, и наилучший результат (до 98%) при комбинации тримебутина с пробиотиком. В группе плацебо купирование абдоминальной боли наблюдалось у 22 % детей. Нормализация стула у 99% детей второй группы и 15% группы плацебо [29].
В другом исследовании оценивали распространенность СРК у детей и эффективность тримебутина в коррекции клинической симптоматики. Были включены 345 детей и подростков от 4-18 лет. Распространенность СРК в соответствии с критериями Рима III у детей и подростков составила 22,6%, причем преобладающим подтипом был СРК с запором. 78 детей и подростков с нормальными лабораторными показателями и установленным диагнозом СРК были рандомизированы на две группы: 39 пациентов получали тримебутин 300 мг в сутки три недели, 39 пациентов не получали медикаментозного лечения. Клиническое улучшение наблюдалось у 94,9% пациентов, принимавших тримебутин против 20,5% в группе, не применявшей медикаментозное лечение (P