Ребенок первых недель жизни защищен в основном за счет
Процент CD3 Т-лимфоцитов в крови пуповины несколько ниже, чем в периферической крови старших детей и взрослых, но в силу большего общего числа лимфоцитов абсолютное количество этих клеток у новорожденных достаточно велико. Кроме того, отношение CD4- к CD8-лимфоцитам в крови пуповины выше (3,5—4:1), чем в крови детей старшего возраста и взрослых (1,5-2:1). Практически все Т-лимфоциты пуповинной крови несут на своей поверхности изоформу CD45 — CD45RA. Преобладание CD45RA над CD45RO Т-лимфоцитами сохраняется на протяжении первых 2-3 лет жизни. Затем число клеток с разными изоформами CD45 постепенно уравнивается.
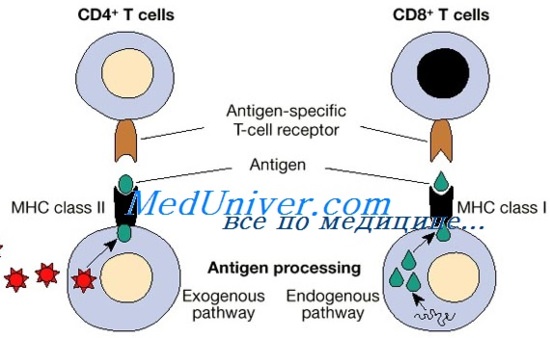
В зависимости от продуцируемых цитокинов Th-клетки разделяют на две группы. Тh1-клетки выделяют ИЛ-2 и ИФН-у, которые активируют цитотоксические Т-лимфоциты и способствуют развитию аллергических реакций замедленного типа, тогда как Тh2-клетки продуцируют ИЛ-4, ИЛ-5, ИЛ-6 и ИЛ-13, стимулирующие В-лимфоциты и сенсибилизирующие организм к аллергенам. Т-лимфоциты пуповинной крови нормально реагируют на ФГА и Кон А и участвуют в смешанной лейкоцитарной реакции. Т-лимфоциты новорожденных способны реагировать на специфические антигены. Так, у ребенка, вакцинированного БЦЖ уже в первый день жизни, через несколько недель развивается сильная реакция на туберкулин. Поскольку тяжелый дефицит Т-лимфоцитов у маленьких детей может оставаться нераспознанным, все вводимые им препараты крови следует облучать.
В-лимфоциты и иммуноглобулины новорожденного ребенка. Поскольку новорожденные не получают от матери IgM-антител (которые представляют собой термостабильные опсонины), восприимчивость к грамотрицательным микроорганизмам у них повышена. Уровень термолабильного опсонина, С3b, в сыворотке новорожденных также ниже, чем у взрослых. По-видимому, именно это определяет неспособность нейтрофилов новорожденных фагоцитировать некоторые бактерии. Термостабильными опсонинами для большинства грамполо-жительных бактерий служат проникающие через плаценту IgG-антитела; они же обеспечивают защиту новорожденного от вирусов.
Однако из-за относительного дефицита IgG2 защита от инкапсулированных полисахаридных антигенов может быть недостаточной. Поскольку в крови недоношенных детей к моменту рождения содержится мало IgG, опсонизирующая активность их крови снижена по отношению ко всем микроорганизмам.
Процент В-лимфоцитов в пуповинной крови слегка ниже, чем в крови старших детей и взрослых, но их абсолютное число значительно выше. Однако при стимуляции PWM или анти-СD40 в сочетании с ИЛ-4 или ИЛ-10 они синтезируют менее разнообразные иммуноглобулины (в основном, IgM) и в гораздо меньшем количестве, чем В-лимфоциты старших детей и взрослых.
Скорость синтеза антител класса IgM в ответ на стимуляцию бесчисленным количеством антигенов после рождения быстро увеличивается. То же происходит, по-видимому, и у недоношенных детей. Концентрация IgM в сыворотке крови резко возрастает примерно к 6-му дню после рождения и продолжает увеличиваться до годовалого возраста, достигая уровня, характерного для взрослых. В сыворотке пуповинной крови IgA практически отсутствует. Впервые его удается определить около 13-го дня после рождения. Далее его концентрация постепенно нарастает и к 6-7-му году достигает «взрослого» уровня. Концентрация IgG в сыворотке пуповинной крови сравнима с таковой в сыворотке матери или даже несколько превышает ее.
В течение первых 6-8 мес. жизни материнский IgG постепенно исчезает из сыворотки ребенка; одновременно увеличивается скорость синтеза собственного IgG (причем на первом году жизни уровень IgGl и IgG3 нарастает быстрее, чем IgG2 и IgG4), пока к 7-8 годам общее содержание IgG не достигнет «взрослого» уровня. Первыми этого уровня достигают концентрации IgGl и IgG4, затем — IgG3 (в 10 лет) и IgG2 (в 12 лет). Наименьшая суммарная концентрация иммуноглобулинов отмечается примерно в 3-4-месячном возрасте. Уровень IgE, как правило, изменяется параллельно содержанию IgA. В дальнейшем концентрации трех основных иммуноглобулинов у здорового человека остаются практически постоянными. К моменту рождения имеется способность продуцировать специфические антитела к белковым антигенам. Однако продукция антител к полисахаридным антигенам, как правило, начинается лишь после 2-летнего возраста, если только полисахарид не связан с белковым носителем, как в конъюгированных вакцинах против Haemophilus influenzae типа b или Streptococcus pneumoniae.
NK-клетки новорожденного. Процент NK-клеток в крови пуповины обычно ниже, но абсолютное их число примерно такое же, как в крови старших детей и взрослых. Активность NK-клеток у новорожденных, оцениваемая как по их числу, так и по антителозависимой клеточной цитотоксичности, примерно на 1/3 ниже активности этих клеток у взрослых людей.
Развитие лимфоидных органов новорожденного. Лимфоидная ткань у новорожденных достаточно развита и продолжает быстро созревать в постнатальном периоде. У плода величина тимуса по отношению к телу максимальна; к моменту рождения его абсолютная масса лишь на 1/3 меньше, чем у годовалого ребенка. Максимальной величины тимус достигает непосредственно перед периодом полового развития, а затем подвергается постепенной инволюции. К первому году жизни все лимфоидные структуры оказываются гистологически зрелыми. Абсолютное число лимфоцитов в периферической крови также достигает максимума на первом году жизни. В грудном и раннем детском возрасте общий объем периферической лимфоидной ткани быстро увеличивается, достигая максимума примерно к 6 годам.
Половое развитие сопровождается инволюцией этой ткани. Однако селезенка в этом периоде продолжает увеличиваться и достигает окончательной величины лишь в зрелые годы. Количество пейеровых бляшек при рождении в среднем вдвое меньше, чем у взрослых людей; оно постепенно увеличивается и достигает максимума в подростковом возрасте.
Особенности иммунной системы новорожденных
Врач лабораторной диагностики Шульга Л.П.
Централизованная иммунно-токсикологическая
лаборатория
Первый критический период — это период новорожденности (до 29 дней жизни), когда организм ребенка защищен почти исключительно материнскими антителами, полученными через плаценту и с грудным молоком. Чувствительность новорожденного ребенка к бактериальным и вирусным инфекциям в этот период очень высока. Группу повышенного риска развития инфекций среди новорожденных составляют недоношенные, а среди них — маловесные дети, страдающие наиболее выраженными и стойкими иммунологическими дефектами.
Второй критический период (4-6 мес. жизни) характеризуется утратой полученных от матери антител. Способность к продукции собственных антител в этот период ограничивается слабым синтезом только иммуноглобулинов M, в то время как иммуноглобулины G являются главными защитными антителами. Недостаточность местной защиты слизистых связана с более поздним накоплением секреторного иммуноглобулина A. В связи с этим чувствительность ребенка ко многим воздушно-капельным и кишечным инфекциям в этот период очень высока.
Третий критический период (2-й год жизни), когда значительно расширяются контакты ребенка с внешним миром и с возбудителями инфекций.
Четвертый критический период (6-7й годы жизни), когда в крови у ребенка уменьшается абсолютное и относительное количество лимфоцитов.
Пятый критический период — подростковый возраст (у девочек с 12-13 лет, у мальчиков с 14-15 лет), когда скачок роста сочетается с относительным уменьшением массы лимфоидных органов, а начавшаяся секреция половых гормонов служит причиной угнетения клеточных механизмов иммунитета
В каждом из этих периодов иммунная система ребенка характеризуется рядом особенностей.
При рождении в крови ребенка преобладают нейтрофилы. К концу первой недели жизни происходит выравнивание количества нейтрофилов и лимфоцитов — так называемый «первый перекрест» — с последующим нарастанием количества лимфоцитов, которые в последующие 4-5 лет жизни остаются преобладающими клетками среди лейкоцитов крови ребенка. «Второй перекрест» происходит у ребенка в возрасте 6-7 лет, когда уменьшается абсолютное и относительное количество лимфоцитов и лейкоцитарная формула приобретает вид, характерный для взрослых. При оценке данных клинического анализа крови у детей необходимо учитывать эти «перекресты».
Повышенное количество гранулоцитов в крови новорожденных в какой-то степени компенсирует недостаточную активность их защитных функций. Абсолютное количество моноцитов крови у новорожденных выше, чем у детей более старшего возраста, но они также отличаются низкой защитной активностью.
Содержание антибактериального фермента лизоцима в сыворотке крови новорожденного превосходит уровень материнской крови уже при рождении, он нарастает в течение первых дней жизни, а к 7-8-ому дню жизни несколько снижается и достигает уровня взрослых людей. А в слезной жидкости новорожденных содержание лизоцима ниже, чем у взрослых, с чем связана повышенная частота конъюнктивитов у новорожденных.
У новорожденных детей резко ослаблены все основные механизмы неспецифической защиты организма от патогенных бактерий и вирусов, чем объясняется высокая чувствительность новорожденных и детей первого года жизни к бактериальным и вирусным инфекциям. Дефекты фагоцитирующих клеток в наибольшей степени выражены у недоношенных новорожденных и детей с задержкой внутриутробного развития. Для таких детей характерно затяжное течение инфекций (например, пневмонии) и низкая эффективность антибиотикотерапии.
После рождения иммунная система ребенка получает сильнейший стимул быстрого развития в виде потока чужеродных (микробных) антигенов, поступающих в организм ребенка через кожу, слизистые дыхательных путей, желудочно-кишечного тракта, активно заселяемые микрофлорой в первые часы после рождения. Проникающие через желудочно-кишечный тракт микроорганизмы являются основными двигателями созревания всей иммунной системы ребенка. Быстрое развитие иммунной системы проявляется увеличением массы лимфатических узлов, которые заселяются Т- и В-лимфоцитами. После рождения ребенка абсолютное количество лимфоцитов в крови резко повышается уже на 1-й неделе жизни (первый перекрест в формуле белой крови). Физиологический возрастной лимфоцитоз сохраняется на протяжении 5-6 лет жизни и может рассматриваться как компенсаторный.
Относительное количество Т-лимфоцитов у новорожденных понижено по сравнению со взрослыми, но в связи с возрастным лимфоцитозом абсолютное количество Т-лимфоцитов в крови новорожденных даже выше, чем у взрослых. Особенности Т-лимфоцитов новорожденных связаны с выходом в кровоток недозрелых предшественников. Слабость клеточных механизмов защиты делает детей особенно чувствительными к вирусным и грибковым инфекциям, защита от которых требует участия функционально полноценных Т-лимфоцитов.
Иммуноглобулин A в крови новорожденных либо отсутствует, либо присутствует в незначительном количестве (0,01 г/л), и лишь в значительно более старшем возрасте достигает уровня взрослых (после 10-12 лет). Секреторные иммуноглобулины А отсутствует у новорожденных, а появляются в секретах после 3-го месяца жизни.
Резервные возможности защиты организма новорожденного связаны с грудным вскармливанием. С молоком матери в организм ребенка попадают готовые антибактериальные и антивирусные антитела — секреторные иммуноглобулины A и G. Секреторные антитела поступают непосредственно на слизистые желудочно-кишечного и респираторного трактов и защищают эти слизистые ребенка от инфекций. Благодаря наличию специальных рецепторов на слизистой желудочно-кишечного тракта новорожденного, иммуноглобулины G проникают из желудочно-кишечного тракта ребенка в его кровяное русло, где пополняют запас материнских антител, ранее поступивших через плаценту. Повышение резервов иммунной системы и профилактика инфекций у новорожденных достигается грудным вскармливанием. Женское молоко содержит не только комплекс необходимых ребенку пищевых компонентов, но и важнейшие факторы неспецифической защиты и продукты специфического иммунного ответа в виде секреторных иммуноглобулинов класса А. Поступающий с грудным молоком секреторный IgA улучшает местную защиту слизистых желудочно-кишечного, респираторного и даже мочеполового тракта ребенка. Грудное вскармливание за счет введения готовых антибактериальных и антивирусных антител класса SIgA существенно повышает устойчивость детей в отношении кишечных инфекций, респираторных инфекций, среднего отита. Поступающие с грудным молоком иммуноглобулины и лимфоциты матери стимулируют иммунную систему ребенка, обеспечивая долговременный антибактериальный и противовирусный иммунитет. На фоне грудного вскармливания повышается иммунный ответ детей на вводимые вакцины. Грудное вскармливание препятствует развитию аллергических заболеваний и аутоиммунного заболевания — целиакии.
По мере созревания иммунной системы ребенка, совершенствования механизмов специфического иммунного ответа повышается степень риска чрезмерного реагирования его иммунной системы на контакт с антигенами окружающей среды и развития аллергических реакций.
Особенности иммунитета у детей разного возраста
Фрейдлин И.С., чл.-корр. РАМН, профессор, доктор медицинских наук НИИ экспериментальной медицины РАМН
Развитие иммунной системы организма продолжается на протяжении всего периода детства. В процессе развития иммунной системы ребенка выделяют «критические» периоды, т.е. периоды максимального риска развития инфекционных заболеваний, связанных с недостаточностью функций иммунной системы.
Первый критический период — это период новорожденности (до 29 дней жизни), когда организм ребенка защищен почти исключительно материнскими антителами, полученными через плаценту и с грудным молоком. Чувствительность новорожденного ребенка к бактериальным и вирусным инфекциям в этот период очень высока. Группу повышенного риска развития инфекций среди новорожденных составляют недоношенные, а среди них — маловесные дети, страдающие наиболее выраженными и стойкими иммунологическими дефектами.
Второй критический период (4-6 мес. жизни) характеризуется утратой полученных от матери антител. Способность к продукции собственных антител в этот период ограничивается слабым синтезом только иммуноглобулинов M, в то время как иммуноглобулины G являются главными защитными антителами. Недостаточность местной защиты слизистых связана с более поздним накоплением секреторного иммуноглобулина A. В связи с этим чувствительность ребенка ко многим воздушно-капельным и кишечным инфекциям в этот период очень высока.
Третий критический период (2-й год жизни), когда значительно расширяются контакты ребенка с внешним миром и с возбудителями инфекций. Иммунный ответ ребенка на инфекционные антигены остается неполноценным. Местная защита слизистых все еще остается несовершенной из-за низкого уровня секреторного IgA. Чувствительность ребенка к респираторным и кишечным инфекциям все еще высока.
Четвертый критический период (6-7й годы жизни), когда в крови у ребенка уменьшается абсолютное и относительное количество лимфоцитов. В этот период уровни иммуноглобулинов М и G в крови ребенка приближаются к уровням взрослых, но уровень иммуноглобулина A все еще остается более низким, с чем связана слабая местная защита слизистых. Содержание иммуноглобулина E, напротив, достигает максимального уровня в связи с высоким уровнем глистных инвазий, чем объясняется повышенная чувствительность к аллергическим реакциям у детей данной возрастной группы. Чувствительность детей этого возраста к инфекциям все еще высока.
Пятый критический период — подростковый возраст (у девочек с 12-13 лет, у мальчиков с 14-15 лет), когда скачок роста сочетается с относительным уменьшением массы лимфоидных органов, а начавшаяся секреция половых гормонов служит причиной угнетения клеточных механизмов иммунитета. В этом возрасте резко возрастают внешние, часто неблагоприятные, воздействия на иммунную систему. Дети этого возраста характеризуются высокой чувствительностью к вирусным инфекциям.
В каждом из этих периодов иммунная система ребенка характеризуется рядом особенностей.
При рождении в крови ребенка преобладают нейтрофилы. К концу первой недели жизни происходит выравнивание количества нейтрофилов и лимфоцитов — так называемый «первый перекрест» — с последующим нарастанием количества лимфоцитов, которые в последующие 4-5 лет жизни остаются преобладающими клетками среди лейкоцитов крови ребенка. «Второй перекрест» происходит у ребенка в возрасте 6-7 лет, когда уменьшается абсолютное и относительное количество лимфоцитов и лейкоцитарная формула приобретает вид, характерный для взрослых. При оценке данных клинического анализа крови у детей необходимо учитывать эти «перекресты».
Повышенное количество гранулоцитов в крови новорожденных в какой-то степени компенсирует недостаточную активность их защитных функций. Абсолютное количество моноцитов крови у новорожденных выше, чем у детей более старшего возраста, но они также отличаются низкой защитной активностью.
Содержание антибактериального фермента лизоцима в сыворотке крови новорожденного превосходит уровень материнской крови уже при рождении, он нарастает в течение первых дней жизни, а к 7-8-ому дню жизни несколько снижается и достигает уровня взрослых людей. А в слезной жидкости новорожденных содержание лизоцима ниже, чем у взрослых, с чем связана повышенная частота конъюнктивитов у новорожденных.
Низкое содержание основных компонентов системы комплемента в крови новорожденных является причиной недостаточной вспомогательной активности сыворотки крови при фагоцитозе. Только ко второму году жизни окончательно созревает продукция компонентов системы комплемента.
В крови новорожденных содержание естественных киллеров значительно ниже, чем у взрослых. Естественные киллеры детской крови отличаются сниженной цитотоксической и секреторной активностью.
Как видно из выше сказанного, у новорожденных детей резко ослаблены все основные механизмы неспецифической защиты организма от патогенных бактерий и вирусов, чем объясняется высокая чувствительность новорожденных и детей первого года жизни к бактериальным и вирусным инфекциям. Дефекты фагоцитирующих клеток в наибольшей степени выражены у недоношенных новорожденных и детей с задержкой внутриутробного развития. Для таких детей характерно затяжное течение инфекций (например, пневмонии) и низкая эффективность антибиотикотерапии. Предпринятые в последние годы попытки применения у таких детей комбинированного лечения с использованием иммуномодулятора Ликопида показали, что клинические признаки улучшения состояния детей, сокращения сроков заболевания сочетаются с исправлением дефектных функций фагоцитирующих клеток.
После рождения иммунная система ребенка получает сильнейший стимул быстрого развития в виде потока чужеродных (микробных) антигенов, поступающих в организм ребенка через кожу, слизистые дыхательных путей, желудочно-кишечного тракта, активно заселяемые микрофлорой в первые часы после рождения. Проникающие через желудочно-кишечный тракт микроорганизмы являются основными двигателями созревания всей иммунной системы ребенка. Быстрое развитие иммунной системы проявляется увеличением массы лимфатических узлов, которые заселяются Т- и В-лимфоцитами. После рождения ребенка абсолютное количество лимфоцитов в крови резко повышается уже на 1-й неделе жизни (первый перекрест в формуле белой крови). Физиологический возрастной лимфоцитоз сохраняется на протяжении 5-6 лет жизни и может рассматриваться как компенсаторный.
Относительное количество Т-лимфоцитов у новорожденных понижено по сравнению со взрослыми, но в связи с возрастным лимфоцитозом абсолютное количество Т-лимфоцитов в крови новорожденных даже выше, чем у взрослых. Особенности Т-лимфоцитов новорожденных связаны с выходом в кровоток недозрелых предшественников. Именно в связи с дефектностью клеточных механизмов защиты на протяжении всего периода детства сохраняется высокая степень риска заболевания туберкулезом в связи с широкой циркуляцией возбудителя туберкулеза. Слабость клеточных механизмов защиты делает детей особенно чувствительными к вирусным и грибковым инфекциям, защита от которых требует участия функционально полноценных Т-лимфоцитов. Среди детей в возрасте от 1 до 6 лет нередко выделяют группу «часто и длительно болеющие» острыми респираторными вирусными инфекциями (ОРВИ). При иммунологическом обследовании таких детей у них, как правило, выявляются дефекты основных защитных механизмов. Такие находки явились основанием для проведения предупредительной иммунокоррекции, при которой дети получали иммуномодулятор Ликопид® вне периода обострения заболевания. Эффективность такого способа иммунокоррекции контролировалась по частоте и длительности эпизодов ОРВИ и по изменениям иммунологических показателей. Частота заболеваний в группе детей, получавших вне обострения Ликопид®, снизилась в два раза. При этом было отмечено значимое повышение в слюне детей этой группы содержания секреторного иммуноглобулина А, который является важнейшим фактором защиты слизистых оболочек от бактерий и вирусов.
Поэтому в течение первых трех лет жизни проводится плановая вакцинация детей против всех наиболее опасных и частых инфекционных заболеваний: туберкулеза, полиомиелита, дифтерии, столбняка, коклюша, кори, вирусного гепатита.
В этом возрасте иммунная система организма отвечает на вакцинацию (убитыми или ослабленными возбудителями, их антигенами, их обезвреженными токсинами) формированием долгоживущих Т-клеток памяти, которые обеспечивают при заражении инфекционным агентом быстрый и эффективный защитный ответ. Именно в детстве, в период расцвета функций тимуса формируется специфический противомикробный иммунитет и соответствующая иммунологическая память, которой должно хватить на всю последующую жизнь.
Абсолютный и относительный лимфоцитоз в крови детей отражает процесс накопления лимфоцитов, имеющих специфические рецепторы для распознавания разных чужеродных антигенов. Этот процесс завершается, в основном, к 5-7 годам, что проявляется изменением формулы крови: лимфоциты перестают доминировать и начинают преобладать нейтрофилы.
Лимфатические узлы ребенка раннего возраста отвечают на любую инфекцию, на любой воспалительный процесс выраженным увеличением размеров (припухлостью). Для детей первых лет жизни характерен аналогичный ответ на инфекции увеличением объема лимфоидной ткани, связанной со слизистыми, например, гортани, с чем связана повышенная частота и опасность быстрого развития отека в области гортани у детей при инфекциях и аллергических реакциях. Лимфоидная ткань, ассоциированная с желудочно-кишечным трактом, у детей первых лет жизни остается незрелой, с чем связан высокий риск кишечных инфекций.
Иммуноглобулин A в крови новорожденных либо отсутствует, либо присутствует в незначительном количестве (0,01 г/л), и лишь в значительно более старшем возрасте достигает уровня взрослых (после 10-12 лет). Секреторные иммуноглобулины А отсутствует у новорожденных, а появляются в секретах после 3-го месяца жизни. Характерные для взрослых уровни секреторного иммуноглобулина A в секретах слизистых достигаются к возрасту 2-4 года. До этого возраста местная защита слизистых у детей остается резко ослабленной. При грудном вскармливании недостаточность местного иммунитета слизистых частично компенсируется поступлением секреторного иммуноглобулина A с молоком матери.
Резервные возможности защиты организма новорожденного связаны с грудным вскармливанием. С молоком матери в организм ребенка попадают готовые антибактериальные и антивирусные антитела — секреторные иммуноглобулины A и G. Секреторные антитела поступают непосредственно на слизистые желудочно-кишечного и респираторного трактов и защищают эти слизистые ребенка от инфекций. Благодаря наличию специальных рецепторов на слизистой желудочно-кишечного тракта новорожденного, иммуноглобулины G проникают из желудочно-кишечного тракта ребенка в его кровяное русло, где пополняют запас материнских антител, ранее поступивших через плаценту. Повышение резервов иммунной системы и профилактика инфекций у новорожденных достигается грудным вскармливанием. Женское молоко содержит не только комплекс необходимых ребенку пищевых компонентов, но и важнейшие факторы неспецифической защиты и продукты специфического иммунного ответа в виде секреторных иммуноглобулинов класса А. Поступающий с грудным молоком секреторный IgA улучшает местную защиту слизистых желудочно-кишечного, респираторного и даже мочеполового тракта ребенка. Грудное вскармливание за счет введения готовых антибактериальных и антивирусных антител класса SIgA существенно повышает устойчивость детей в отношении кишечных инфекций, респираторных инфекций, среднего отита. Поступающие с грудным молоком иммуноглобулины и лимфоциты матери стимулируют иммунную систему ребенка, обеспечивая долговременный антибактериальный и противовирусный иммунитет. На фоне грудного вскармливания повышается иммунный ответ детей на вводимые вакцины. Грудное вскармливание препятствует развитию аллергических заболеваний и аутоиммунного заболевания — целиакии. Один из компонентов грудного молока — лактоферрин участвует в стимуляции иммунологических функций, будучи способен проникать в иммунокомпетентные клетки, связываться с ДНК, индуцируя транскрипцию генов цитокинов. Непосредственной антибактериальной активностью обладают такие компоненты грудного молока, как специфические антитела, бактериоцидины, ингибиторы бактериальной адгезии. Все выше сказанное требует большого внимания в профилактической работе с беременными женщинами к разъяснению преимуществ грудного вскармливания. Полезными являются специальные образовательные программы, вовлекающие не только женщин, но и их мужей, родителей и других лиц, способных повлиять на принятие женщиной единственно верного решения о грудном вскармливании ребенка.
По мере созревания иммунной системы ребенка, совершенствования механизмов специфического иммунного ответа повышается степень риска чрезмерного реагирования его иммунной системы на контакт с антигенами окружающей среды и развития аллергических реакций. Даже внутриутробный контакт плода с вдыхаемыми матерью пыльцовыми аллергенами приводит к последующему развитию у новорожденного атопических реакций и заболеваний. Высокий риск развития атопических реакций у детей первых лет жизни связан с преобладанием у них дифференцировки T-хелперов 2, контролирующих синтез иммуноглобулина E и повышенную секрецию гистамина базофилами и тучными клетками. Низкий уровень секреторного IgA на слизистых у детей способствует беспрепятственному проникновению аллергенов через слизистые респираторного и желудочно-кишечного тракта. Особенностью атопических реакций у детей первых лет жизни можно считать более высокую частоту пищевой и более низкую частоту пылевой/пыльцовой аллергии по сравнению со взрослыми. У детей нередко проявляется аллергия к коровьему молоку (2-3% детей в индустриально развитых странах). Коровье молоко содержит более 20 компонентов белковой природы, а многие из них способны вызвать синтез иммуноглобулина Е. Широкое распространение такой аллергии затрудняет искусственное вскармливание детей, заставляя искать адекватные заменители (например, соевые продукты).
Описанные проявления иммунодефицита у детей первых лет жизни обычно оцениваются как «физиологические», т.е. не выходящие за пределы возрастных норм. Однако обусловленная этими возрастными иммунологическими дефектами повышенная чувствительность к инфекциям заставляет искать пути иммунокоррекции. Выше мы рассмотрели примеры применения иммуномодулятора Ликопид®, в том числе, и с целью иммунокоррекции. Многократно доказано иммунокорректирующее действие сбалансированного питания ребенка, мер по закаливанию организма, дозированной физической нагрузки.