Многоликий АИТ (часть 1)
В структуре эндокринной патологии значительный удельный вес принадлежит аутоиммунной тиреопатологии, одним из основных представителей которой является аутоиммунный тиреоидит (АИТ).
Эта заметка скорее попытка для врачей описать варианты течения такого остающегося до сих пор загадочным заболеванием как АИТ. Это не руководство к действию для пациентов.
Сколько я не пыталась найти, ни в одном учебнике или монографии нет полного, подробного описания вариантов течения АИТ. Поэтому не все ещё понятно и раскрыто в этом процессе. Нет единой, общепринятой классификации АИТ. Патогенетическая терапия не разработана, а симптоматическая не имеет доказательной базы.
Проведу анализ вариантов течения АИТ, на основе наиболее известных классификаций и клинических наблюдений.
1. АИТ «классическая», критерии который были приняты ВОЗ в 2000 году, ранее была единственным определением АИТ: критерием диагноза АИТ могла быть только совокупность данных симптомов (отсутствие же одного из них делала диагноз АИТ предположительным.
УЗИ картина АИТ предполагает:
Косвенным признаком АИТ является увеличение лимфатических узлов у нижних полюсов обеих долей щитовидной железы.
Но, как показали годы наблюдений, в «чёткие» рамки только этой характеристики АИТ не укладывается, картина его течения оказалась более разнообразной.
2. По классификации национального руководства по эндокринологии под редакцией Дедова И.И.
Наиболее часто встречающиеся формы тиреоидита:
Сроки наступления/чередования фаз тоже могут быть разными. Например, начало послеродового тиреоидита может быть через полгода или даже через год после родов. а не через 3 месяца.
3. Более редкие формы АИТ:
Есть ещё классификация Davies T. 1993 года, по которой были попытки «состыковать» структурные аномалии и функцию щитовидной железы, которая более подробно отражает варианты течения АИТ.
Есть ещё УЗ- классификация АИТ по В.П. Харченко (1999 года) при которой АИТ бывает 4-х УЗИ – типов:
АИТ часто сопровождает «обычный» коллоидный узловой зоб, суть в том, что если при «изолированном» коллоидном зобе после оперативного удаления одной доли щитовидной железы функция оставшейся доли сохраняется и лечение гормонами не требуется, то сочетании с АИТ – вторая доля «не тянет» функцию удалённой доли и требуется, как правило, пожизненное лечение гормонами.
Реже встречается, гипотиреоз после таких операций транзиторный (преходящий), с последующим восстановлением в эутиреоз функции оставшейся доли без гормонозаместительной терапии (ГЗТ).
Не исключено сочетание АИТ с раком щитовидной железы, поэтому проведение пункции узлов (ТАБ = аспирационной тонкоигольной биопсии), так же необходимо при узлах более 1 см, как и при коллоидном зобе.
Причины появления АИТ до сих пор до конца не ясны, есть предположения о наследственной предрасположенности, особенно по женской линии, вирусной теории, теории переизбытка йода в окружающей среде, сочетании с другими иммунными заболеваниями, проблемами с экологией и т.д.
Аутоиммунный тиреоидит (АИТ, тиреоидит Хашимото)
Что такое аутоиммунный тиреоидит?
Причина аутоиммунного тиреоидита кроется в неправильной работе иммунной системы пациента. При аутоиммунном тиреоидите, встречающемся чаще всего у женщин, иммунная система, в норме обеспечивающая «полицейские» функции в организме и занимающаяся уничтожением чужеродных клеток и организмов, начинает проявлять агрессию по отношению к собственному органу – щитовидной железе. Ткань щитовидной железы пропитывается лейкоцитами, деятельность которых приводит к развитию воспаления железы – тиреоидит (его называют аутоиммунным тиреоидитом, чтобы подчеркнуть, что причиной заболевания является сбой в работе собственной иммунной системы организма). Со временем из-за воспаления часть клеток щитовидной железы погибает, а оставшихся в живых начинает не хватать для выработки необходимого количества гормонов. Развивается гормональная недостаточность – гипотиреоз.
Симптомы аутоиммунного тиреоидита (АИТ)
Симптомы аутоиммунного тиреоидита легко спутать с повседневным состоянием очень многих наших соотечественников: пациента беспокоит слабость, сонливость, быстрая утомляемость, депрессия, ухудшение настроения, иногда – отеки. Образно говоря, жизнь начинает терять свои краски. Многих пациентов с аутоиммунным тиреоидитом беспокоит и замедление мыслительной деятельности («не собраться с мыслями»), часто активно выпадают волосы.
Диагностика АИТ
Аутоиммунный тиреоидит на УЗИ щитовидной железы
При ультразвуковом исследовании при АИТ обычно отмечается понижение эхогенности железы и появление выраженных диффузных изменений. Переводя на «человеческий» язык, можно сказать, что при аутоиммунном тиреоидите щитовидная железа выглядит на экране УЗИ-аппарата темной и имеет очень неоднородную структуру – в одних местах ткань более светлая, в других – более темная. Нередко врачи ультразвуковой диагностики обнаруживают при болезни Хашимото в ткани щитовидной железы и узлы. Следует отметить, что зачастую эти уплотнения настоящими узлами не являются и представляют собой просто очаги с резко выраженным воспалительным процессом, их еще называют «псевдоузлами». Чаще всего квалифицированный врач ультразвуковой диагностики может отличить псевдоузел при аутоиммунном тиреоидите от узла, однако в некоторых случаях сделать это непросто. Именно поэтому врачи нередко пишут заключение примерно так: «Признаки АИТ. Узлы (псевдоузлы?) щитовидной железы», чтобы подчеркнуть свою неуверенность в оценке характера изменений. При выявлении в ткани щитовидной железы на фоне аутоиммунного тиреоидита образований диаметром 1 см и более пациенту рекомендуется проведение биопсии для уточнения их природы. В ряде случаев после получения результатов исследования становится понятно, что исследованный узел является псевдоузлом на фоне АИТ (ответ цитолога обычно в таких случаях краток: «Аутоиммунный тиреоидит» или «Тиреоидит Хашимото»). Вместе с тем, на фоне аутоиммунного тиреоидита возможно выявление и узлов коллоидного (доброкачественного) строения, и злокачественных новообразований.
Лечение аутоиммунного тиреоидита
Лечение причины аутоиммунного тиреоидита – неправильной работы иммунной системы – в настоящее время невозможно, поскольку подавление работы иммунной системы приводит к снижению защищенности организма от вирусов и бактерий, что может быть опасно. Именно поэтому врачам приходится лечить не причину аутоиммунного тиреоидита, а его следствие – нехватку гормонов, вернее одного гормона – тироксина, который вырабатывается щитовидной железой из йода, поступающего с пищей. Революция в лечении АИТ свершилась, когда врачи получили возможность использовать гормоны щитовидной железы свободно. На наше счастье, фармацевтами была синтезирована точная копия человеческого гормона тироксина, совершенно не отличающаяся от оригинала. При выявлении АИТ и связанного с этим недостатка гормонов врач-эндокринолог назначает пациенту искусственный тироксин, который позволяет привести уровень гормонов в норму. При правильном назначении тироксин не вызывает никаких побочных эффектов. Единственное неудобство такого лечения – его следует продолжать в течение всей жизни пациента, поскольку раз начавшись, аутоиммунный тиреоидит (АИТ) никогда не проходит, и лекарственная поддержка требуется пациенту постоянно.
Гнойный тиреодит
Тиреоидит Риделя
Гипофизарный нанизм (карликовость)
Подострый тиреоидит (тиреоидит де Кервена)
Подострый тиреоидит является воспалительным заболеванием щитовидной железы, возникающим после перенесенной вирусной инфекции и протекающий с разрушением клеток щитовидной железы. Наиболее часто подострый тиреоидит возникает у женщин. Мужчины болеют подострым тиреоидитом значительно реже женщин – примерно в 5 раз.
Аутоиммунный полигландулярный синдром
Пангипопитуитаризм
Хроническая надпочечниковая недостаточность
Надпочечниковая недостаточность (недостаточность коры надпочечников) является одним из наиболее тяжелых заболеваний эндокринной системы, которое характеризуется снижением выработки гормонов корой надпочечников (глюкокортикоидов и минералокортикоидов)
Классы аппаратов для выполнения УЗИ щитовидной железы
Описание различных классов УЗИ-оборудования, применяемого для проведения УЗИ щитовидной железы
Гормон Т3
Гормон Т4
Эндокринная офтальмопатия (офтальмопатия Грейвса)
Диффузный эутиреоидный зоб
Гипотиреоз
Гипотиреозом называется состояние, отличающееся недостатком гормонов щитовидной железы. При длительном существовании нелеченного гипотиреоза возможно развитие микседемы («слизистого отека»), при котором развивается отечность тканей пациента в сочетании с основными признаками недостаточности гормонов щитовидной железы.
Заболевания щитовидной железы
В настоящее время изучению заболеваний щитовидной железы уделяется настолько серьезное внимание, что был выделен особый раздел эндокринологии – тиреоидология, т.е. наука о щитовидной железе. Врачей, занимающихся диагностикой и лечением заболеваний щитовидной железы, называют тиреоидологами.
Гормоны щитовидной железы
Гормоны щитовидной железы делятся на два различных класса: йодитиронины (тироксин, трийодтиронин) и кальцитонин. Из двух этих классов гормонов щитовидной железы тироксин и трийодтиронин регулируют основной обмен организма (тот уровень энергозатрат, который необходим для поддержания жизнедеятельности организма в состоянии полного покоя), а кальцитонин участвует в регуляции обмена кальция и развития костной ткани.
Псевдогипопаратиреоз
Анализы в СПб
Одним из важнейших этапов диагностического процесса является выполнение лабораторных анализов. Чаще всего пациентам приходится выполнять анализ крови и анализ мочи, однако нередко объектом лабораторного исследования являются и другие биологические материалы.
Анализ на гормоны щитовидной железы
Консультация эндокринолога
Специалисты Северо-Западного центра эндокринологии проводят диагностику и лечение заболеваний органов эндокринной системы. Эндокринологи центра в своей работе базируются на рекомендациях Европейской ассоциации эндокринологов и Американской ассоциации клинических эндокринологов. Современные диагностические и лечебные технологии обеспечивают оптимальный результат лечения.
Экспертное УЗИ щитовидной железы
УЗИ щитовидной железы является главным методом, позволяющим оценить строение этого органа. Благодаря своему поверхностному расположению, щитовидная железа легко доступна для проведения УЗИ. Современные ультразвуковые аппараты позволяют осматривать все отделы щитовидной железы, за исключением расположенных за грудиной или трахеей.
УЗИ шеи
Консультация детского эндокринолога
Очень часто на прием к специалистам Северо-Западного центра эндокринологии обращаются пациенты, не достигшие 18 лет. Для них в центре работают специальные врачи – детские эндокринологи
Отзывы
Истории пациентов
Видеоотзывы: опыт обращения в Северо-Западный центр эндокринологии
Псевдоузлы щитовидной железы что это
Нетоксический зоб представляет собой увеличение щитовидной железы. Зоб может быть спорадическим или эндемическим (в районах с дефицитом йода). При аутопсии, узлы щитовидной железы обнаруживают примерно у 50% умерших. По всей видимости, этиология зоба многофакторная, задействованы как генетические факторы, так и факторы окружающей среды.
Показатели ТТГ у пациентов с зобом обычно находятся в пределах нормы, поэтому, по всей видимости, заболевание не зависит от ТТГ. Нетоксический зоб чаще встречается у женщин, часто болеют несколько членов семьи. Очень крупный зоб может причинять физические неудобства, но в большинстве случаев зоб протекает бессимптомно. Иногда зоб может смещать трахею, пищевод и сосуды шеи, становится причиной стридора и дисфагии.
В последние годы как бессимптомный зоб, так и рак щитовидной железы стали диагностироваться гораздо чаще. Связано это с разработкой и внедрением методов компьютерной томографии (КТ), магнитно-резонансной томографии (МРТ), дуплексного сканирования сонных артерий. Узлы щитовидной железы в популяции встречаются достаточно часто. В районах с достаточным содержанием йода пальпируемые узлы щитовидной железы обнаруживаются у 5% женщин и 1% мужчин. «Инсиденталомы» щитовидной железы представляют собой непапильпируемые лимфоузлы, которые, тем не менее, обнаруживаются на УЗИ высокого разрешения.
Они встречаются у 19-67% населения. Меньшая их часть, 5-15%, являются злокачественными; большинство же представляет собой простые доброкачественные узлы. И хотя заболеваемость раком щитовидной железы возросла, увеличения смертности за этим не последовало. Вероятно, это связано с тем, что рак часто обнаруживается на ранней стадии, когда размер первичной опухоли невелик. Дифференцированный рак щитовидной железы, к которому относится папиллярный и фолликулярный рак, составляет около 90% всех злокачественных опухолей щитовидной железы.
В период с 1973 по 2002 гг. заболеваемость раком щитовидной железы возросла более чем в 2,4 раза, в первую очередь за счет увеличения заболеваемости папиллярным раком.
Сбор анамнеза и осмотр помогают уточнить природу опухоли. Признаками, указывающими на злокачественность, являются мужской пол, пожилой возраст, отягощенный семейный анамнез по раку щитовидной железы. Также риск рака щитовидной железы возрастает у пациентов, подвергшихся в детстве воздействию ионизирующего излучения: лучевое лечение акне, лимфогранулематоза, облучение тимуса. Риск повышен у лиц, находившихся вблизи очагов ядерных аварий, например, на Чернобыльской АЭС. Также на злокачественную природу опухоли указывают ее быстрый рост, лимфоаденопатия, парез/паралич голосовых складок.
Учитывая высокую распространенность в популяции узлов щитовидной железы и очень благоприятный прогноз при папиллярных микрокарциномах, узлы размером менее 1 см в большинстве случаев обследования не требуют, кроме случаев, когда присутствует дополнительная клиническая симптоматика. Как правило, у пациентов с раком щитовидной железы содержание тиреоидных гормонов в крови находится на нормальном уровне, но риск рака несколько выше у пациентов с болезнью Грейвса. На рисунке ниже изображен алгоритм действий врача при обнаружении узлов щитовидной железы.
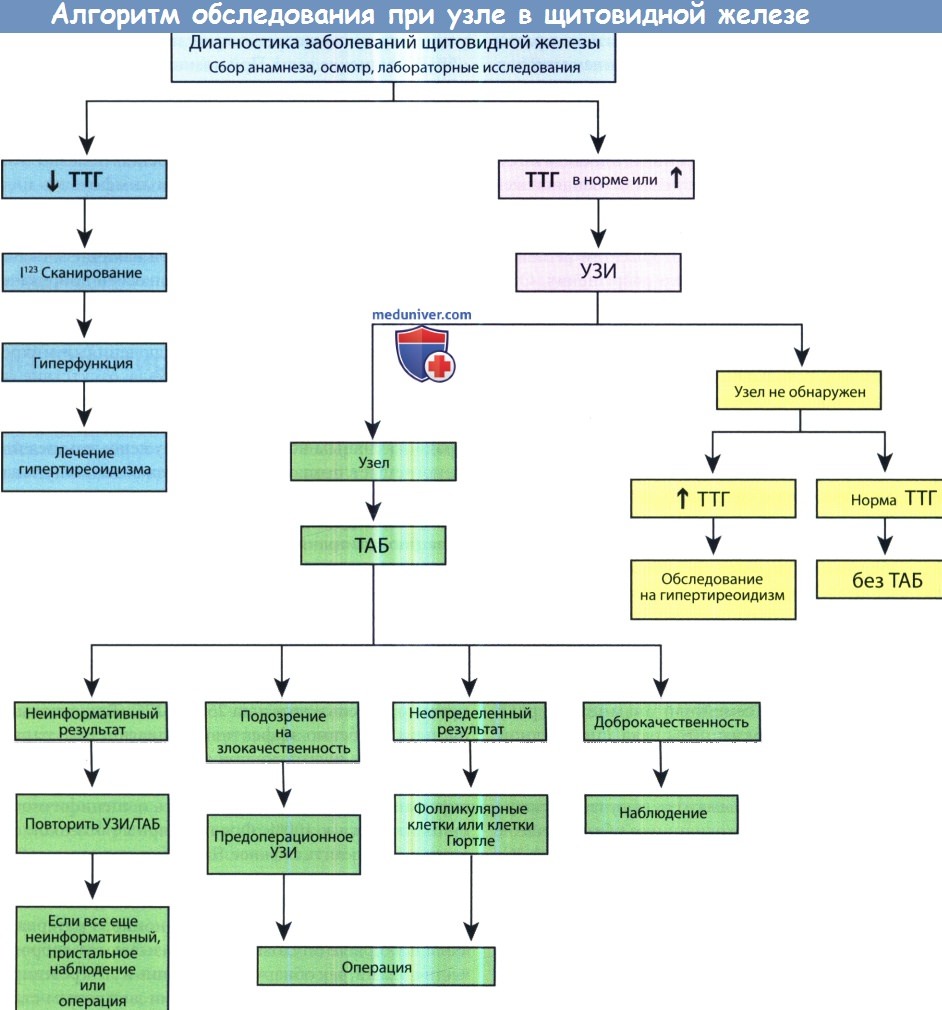
ТАБ — тонкоигольная аспирационная биопсия; ТТГ—тиреотропный гормон.
а) Дополнительные методы обследования при узле щитовидной железы. При помощи УЗИ можно обнаружить узлы даже совсем небольших размеров. Согласно данным одного исследования, у 65% пациентов при ультразвуковом исследовании щитовидной железы обнаружились ее узлы. При помощи УЗИ можно определить гетерогенную эхоструктуру псевдоузлов при тиреоидите Хашимото, а допплерография позволяет обнаружить усиление кровотока в тканях железы при болезни Грейвса. Особенно полезно УЗИ в описании ткани самой железы и лимфоузлов шеи.
УЗИ является методом выбора при обследовании пациента с узлами щитовидной железы, а определенные признаки позволяют предположить наличие злокачественного новообразования. Признаками доброкачественности являются гиперэхогенность и кистозная структура узла. Признаками малигнизации являются гипоэхогенный узл, особенно с включениями микрокальцификатов; неровными края узла; отсутствие гало; превышение вертикального размера узла над горизонтальным. Если при исследовании с радиоактивным йодом 131 обнаружено, что узел йод не поглощает, показана аспирационная тонкоигольная биопсия узла под контролем УЗИ.
При обнаружении узла, подозрительного на малигнизацию, выполняется его тонкоигольная биопсия. Данный метод диагностики, особенно при выполнении его под контролем УЗИ, имеет превосходные чувствительность и специфичность, превышающие 90%. Метод прост в исполнении, безопасен, не доставляет дискомфорта пациенту. В материале должно содержаться как минимум 10-15 клеток, полученных за 3-6 вколов. Как правило, используется игла 25 или 27G. Тонкоигольная биопсия особенно эффективна в диагностике папиллярного рака, поскольку при цитологическом исследовании раковые клетки характеризуются четкими изменениями в ядрах; чувствительность и специфичность приближаются к 100%.
Фолликулярные опухоли, напротив, определить сложнее. Часто биоптат оказывается неинформативным, и для постановки окончательного диагноза требуется удаление пораженной доли железы с последующим изучением операционного материала. Фолликулярные опухоли часто оказываются доброкачественными, рак обнаруживают лишь в 20% резецированных желез. Недавно коммерчески доступным стало исследование на мутацию BRAF. Данная мутация часто встречается при папиллярном и фолликулярном раке, выявление BRAF помогает спланировать лечение при получении неинформативного биоптата.
Риск обнаружении рака у пациентов с множественными узлами такой же, что и у пациентов с единичным узлом. Согласно рекомендациями Американского общества щитовидной железы, биопсии подлежат лимфоузлы размером более 1 см и имеющие признаки злокачественности при УЗИ. Если при УЗИ крупный узел выглядит доброкачественным, рекомендуется повторное выполнение УЗИ. При увеличении узла на 50% или на 2 мм и больше в двух измерениях необходимо выполнение биопсии.
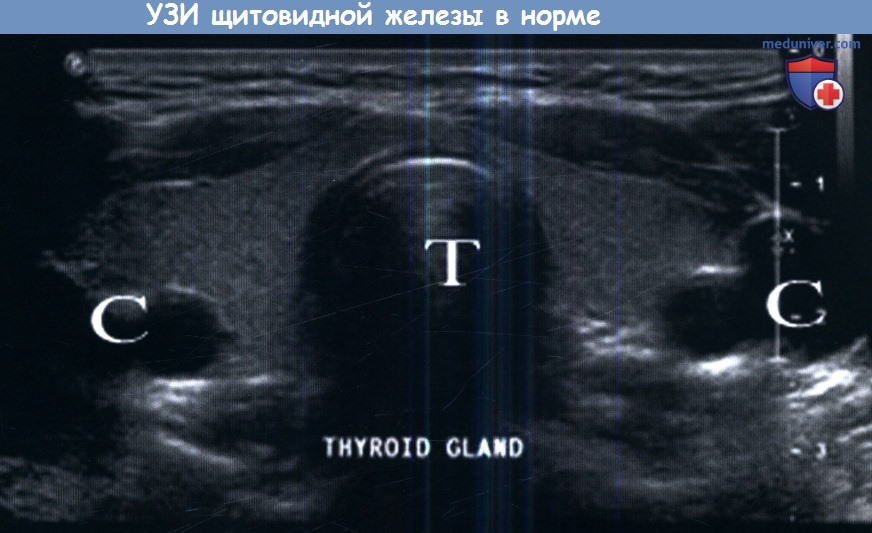
Железа лежит над и вокруг трахеи, а также над сонными артериями.
Т, treachea — Т, трахея; С, carotid artery — С, сонные артерии; Thyroid gland — Щитовидная железа.
б) Эпидемиология (частота) рака щитовидной железы. В большинстве случаев рак щитовидной железы представлен дифференцированными формами. 80% всех злокачественных опухолей щитовидной железы составляет папиллярный рак, 15% — фолликулярный рак. Медуллярный рак, нейроэндокринная опухоль вырабатывающих кальцитонин клеток щитовидной железы, встречается в 3% случаев и может быть связана с множественной эндокринной неоплазией II типа. Анапластический рак, отличающийся агрессивным течением, составляет 1-2% от всех злокачественных опухолей щитовидной железы. Иногда на фоне тиреоидита Хашимото развивается лимфома щитовидной железы, заподозрить ее нужно при появлении новообразования, быстро увеличивающегося в размерах.
в) Классификация и стадирование рака щитовидной железы. Рак щитовидной железы сталируется на основании его формы, размера опухоли, распространения за пределы железы, наличия метастазов в лимфатические узлы, возраста пациента.
Опухоли Т1а имеют размер 1 см и меньше, T1b — 1-2 см.
Т2 — опухоль 2-4 см, не распространяется за пределы железы.
Т3 — опухоль более 4 см без распространения за пределы железы, либо любые опухоли с ограниченным ростом за пределы опухоли (в грудино-щитовидную мышцу или окружающие железу мягкие ткани).
Т4а — опухоль любого размера, распространяющаяся в гортань, трахею, пищевод, возвратные гортанные нервы или подкожную клетчатку.
Т4b — опухоль прорастает в превертебральную фасцию или включает в себя сонную артерию. Описанная выше система стадирования относится ко всем формам рака, за исключением анапластического.
Любой анапластический рак считается опухолью Т4: Т4а — опухоль ограничена пределами железы, Т4b — опухоль распространяется за пределы железы.
N1a — поражение лимфоузлов VI уровня (предтрахеальные, паратрахеальные, предгортанные).
N1b — поражение шейных, заглоточных или верхних медиастинальных лимфоузлов с обеих, либо с одной стороны.
Папиллярный и фолликулярный рак. У пациентов моложе 45 лет выставляется стадия I, за исключением наличия отдаленных метастазов, при которых выставляется II стадия. У пациентов старше 45 лет опухоль Т1 соответствует I стадии, опухоль Т2 соответствует II стадии. Стадия III — Т3 с№), либо Т1-Т3сN1а. Стадия IVA — Т1-Т3 с N1b, либо опухоль Т4а. Стадия IVB — опухоль Т4b без отдаленных метастазов. При наличии отдаленных метастазов выставляется стадия IVC.
Медуллярный рак. Стадия I — первичная опухоль Т1. Стадия II — Т2-Т3 без метастазов в лимфоузлы. Стадия III — Т1-Т3 с лимфоузлами Nla. Стадия IVA — Т1-Т3 с N1b, либо опухоль Т4а. Стадия IVB-все опухоли Т4b. Стадия IVC выставляется при наличии отдаленных метастазов.
Анапластический рак. Любой анапластический рак щитовидной железы соответствует IV стадии заболевания. Стадия IVA—Т4а, стадия IVB — Т4b. Стадия IVC выставляется при наличии отдаленных метастазов.
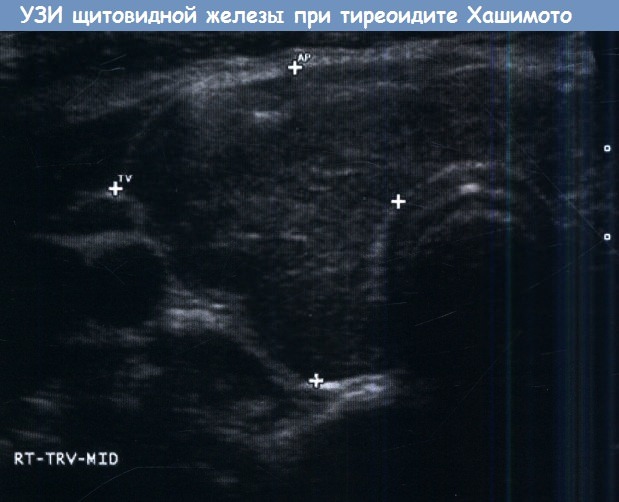
характерные для тиреоидита Хашимото. 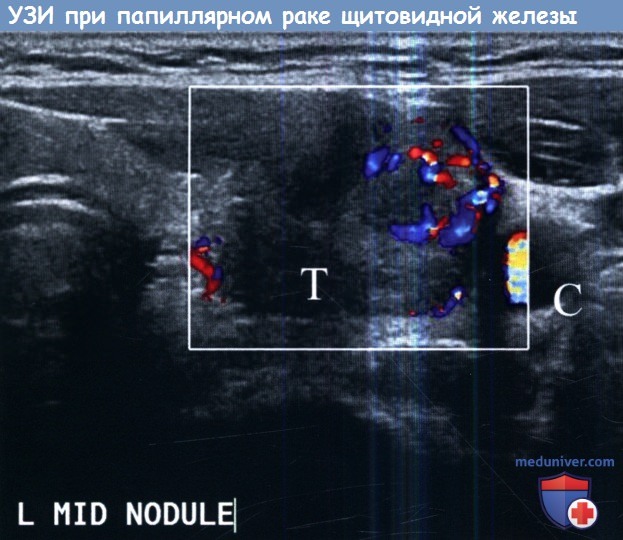
Визуализируются нечеткие границы опухоли, микрокальцификаты, повышенное кровенаполнение тканей при допплерографии.
Т — трахея; С — сонные артерии.
г) Лечение рака щитовидной железы. Основой лечения рака щитовидной железы является хирургическая резекция. Выполняется тиреоидэктомия, а при наличии показаний и шейная лимфодиссекция. При опухолях размером менее 1 см и отсутствии других угрожающих признаков возможно выполнение лобэктомии. Тиреоидэктомия также показана при неопределенном состоянии узла, выраженной атипии при цитологическом исследовании, отягощенном семейном анамнезе по раку щитовидной железы, воздействии ионизирующего облучения. Перед операцией рекомендуется выполнение УЗИ щитовидной железы и лимфатических узлов шеи. Для подтверждения метастазов в лимфоузлы выполняется их тонкоигольная биопсия под контролем УЗИ. После хирургического лечения прогноз и наблюдения основываются на стадии заболевания по системе TNM.
д) Послеоперационное лечение при раке щитовидной железы. В зависимости от результатов гистологического исследования, перенесшим тиреоидэтомию пациентам может быть показана терапия радиоактивным йодом. При низком риске рецидива дополнительное лечение обычно не требуется, оно проводится больным с опухолями большого размера, либо с распространением первичной опухоли за пределы железы. Абляция небольшого количества остаточной нормальной щитовидной ткани после тиреоидэктомии может способствовать раннему обнаружению рецидива на основе определения концентрации тиреоглобулина плазмы. Согласно последним данным, при малом риске рецидива низкие дозы радиоактивного йода обладают такой же эффективностью, что и более высокие дозировки.
Терапия высокими дозами может использоваться у пациентов с гистологически агрессивными формами рака (высококлеточный, инсулярный рак). Пациентам, которым проводится терапия радиоактивным йодом, может быть показана отмена левотироксина до достижения уровня ТТГ в 30 мМЕ/л, также они должны придерживаться диеты с низким содержанием йода. Иногда вместо отмены левотироксина можно назначать рекомбинантный ТТГ, показавший в исследованиях аналогичный краткосрочный риск рецидива. Через неделю после курса терапии радиоактивным йодом проводится посттерапевтическое сканирование всего тела с целью обнаружения отдаленных метастазов.
Дифференцированные раковые клетки щитовидной железы экспрессируют рецепторы к ТТГ, поэтому в ответ на стимуляцию ТТГ они начинают интенсивно делиться, а также продуцируют некоторые специфические белки. Для подавления продукции ТТГ и снижения риска рецидива проводится терапия левотироксином. У пациентов со средним и высоким риском рецидива рекомендуется подавление уровня ТТГ ниже 0,1 мМЕ/л. Пациентам с низким риском рецидива допустимо поддерживать уровень ТТГ на уровне нижней границы нормы или чуть меньше (0,1-0,5 мМЕ/л).
При дифференцированном раке щитовидной железы необходимо длительное наблюдение. Пациентам, которым не выполнялась тотальная ларингэктомия и терапия радиоактивным йодом 131, в послеоперационном периоде необходим контроль уровня тиреоглобулина и антител к тиреоглобулину, а также УЗИ органов шеи. Антитела к тиреоглобулину (АТ-ТГ), обнаруживаемые примерно у 25% пациентов с раком щитовидной железы, могут приводить к ложному занижению показателей тиреоглобулина. Примерно 20% пациентов без симптомов заболевания, у которых на фоне гормональной супрессии ТТГ уровни тиреоглобулина плазмы находятся на уровне ниже 1 нг/мл, через год после проведения операции на фоне стимуляции ТТГ показатели тиреоглобулина плазмы достигнут определяемых значений.
Примерно у одной трети данных пациентов возникнет рецидив или персистирование рака, в то время как у других 2/3 показатели стимулированного тиреоглоубилина постепенно снизятся, либо останутся на прежнем уровне. При появлении рецидива опухоли в лимфоузлах или мягких тканях шеи, необходимо повторное оперативное вмешательство.
е) Ключевые моменты:
• Тонкоигольная биопсия является чувствительным и специфичным методом диагностики папиллярного рака щитовидной железы. После анализа операционного материала только 20% всех фолликулярных образований щитовидной железы оказываются злокачественными.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021

