Патогенетический подход к лечению различных вариантов мастопатии
Доброкачественные заболевания молочных желез принято объединять термином «мастопатия». По определению ВОЗ (гистологическая классификация 1984 г.), мастопатия — фиброзно-кистозная болезнь, которая характеризуется широким спектром пролиферативных и регресс
Доброкачественные заболевания молочных желез принято объединять термином «мастопатия». По определению ВОЗ (гистологическая классификация 1984 г.), мастопатия — фиброзно-кистозная болезнь, которая характеризуется широким спектром пролиферативных и регрессивных изменений тканей молочных желез с ненормальным соотношением эпителиального и соединительно-тканного компонентов. Мастопатия наиболее часто встречается в возрасте 30–45 лет. Распространенность ее составляет 30–45% в популяции, а у женщин с различными гинекологическими заболеваниями — 70–95% (Л. М. Бурдина, 1993).
Общность мастопатии и рака молочной железы определяется суммой схожих этиологических факторов, сочетанием этих заболеваний в большом числе наблюдений, близостью некоторых морфологических форм мастопатии к раку, схожестью нарушений как в гормональном, так и в метаболическом звене гомеостаза (Л. Н. Сидоренко, 1991).
Расстройства гормонального гомеостаза в организме женщины могут наблюдаться в различных его звеньях. Причиной этих сдвигов являются самые разнообразные неблагоприятные факторы: нервно-психические нарушения, заболевания в генитальной сфере, заболевания печени, щитовидной железы и др. Расстройства различных звеньев гормонального гомеостаза чаще приводят к одному и тому же результату — гиперэстрогенизации организма женщины. Гиперэстрогенизация с действием гонадотропных гормонов выступает в качестве основного фактора, вызывающего образование дисгормональных пролифератов в молочных железах. Необходимо отметить, что гиперэстрогенизация может быть следствием не только абсолютного, но и относительного избытка эстрогенов (Т. А. Пантюшенко, 1985; Л. Н. Сидоренко, 1991).
Риск возникновения рака молочной железы увеличивается при наличии кистозных изменений и зависит от степени протоковой и внутридольковой пролиферации эпителия и наличия признаков кальцификации (Л. Ю. Дымарский, 1970; и др.). При резко выраженной пролиферации малигнизация может наступить в 31,4% случаев (О. Сепп и соавт., 1975).
С этих позиций своевременная диагностика и лечение мастопатии являются основой вторичной профилактики рака молочной железы. Согласно современным концепциям, больные дисгормональной гиперплазией молочных желез подлежат включению в диспансерную группу наблюдения (Е. В. Кира и соавт., 2000).
Особенности патогенетических механизмов возникновения мастопатии у каждой конкретной больной обусловливают разнообразие проявлений этого заболевания, что затрудняет создание единой классификации.
В практическом плане принято выделять две основные формы мастопатии: диффузную и узловую. Больные с узловой формой мастопатии подвергаются, как правило, оперативному лечению и последующей лекарственной терапии в условиях онкологических учреждений. При диффузной мастопатии наблюдение и лечение часто осуществляются врачами различных специальностей: онкологами, акушерами-гинекологами, хирургами, терапевтами. Это делает необходимым знакомство с этой патологией широкой медицинской аудитории.
При диффузной мастопатии ткани пораженных молочных желез мало изменены. У женщин, страдающих этой формой дисгормональной гиперплазии, отмечается преобладание различных функциональных расстройств. В анамнезе относительно частыми являются нарушения менструальной функции, многочисленные аборты, кратковременная лактация, отсутствие беременностей или патологическое их течение. Среди жалоб преобладают боли в одной или обеих молочных железах, иррадиирующие в смежные части тела (ключицу, плечо, лопатку, подреберье, шею). Боли, как правило, появляются перед наступлением менструации. С ее окончанием они уменьшаются или совсем исчезают. При осмотре каких-либо изменений в молочных железах выявить не удается. Пальпаторно обнаруживаются различные по величине и протяженности болезненные, без четких границ уплотнения. Поверхность их зернистая или дольчатая.
В терапии больных мастопатией ведущая роль принадлежит системному подходу, охватывающему многообразие факторов, которые способствуют развитию заболевания, с учетом гормонального статуса и процессов метаболизма. Системный подход базируется на знании личностных особенностей больной, факторов окружающей среды, психологических взаимоотношений на работе, индивидуальных нюансов семейных отношений. Основой патогенетической терапии фиброзно-кистозной мастопатии является коррекция выявленных изменений функций нейроэндокринных органов (Л. Н. Сидоренко, 1991).
Препараты, применяемые для лечения больных с дисгормональными гиперплазиями молочных желез, довольно многочисленны, целесообразно выделить три основных комплекса:
Первый комплекс представляет собой наиболее обширную группу и включает разнообразные средства:
Препараты первого комплекса можно назначить на этапе обследования в ожидании результатов дополнительных методов обследования.
Назначение гормональных препаратов, на наш взгляд, допустимо только после тщательного исследования уровней гормонов в сыворотке крови и глубокого анализа клинической картины. В практике нашли применение:
Клинические варианты диффузной мастопатии и методы лечения
Комплексное углубленное обследование больных, оценка эффективности проводимых лечебных воздействий, анализ литературы позволяют выделить клинические варианты диффузной мастопатии:
Определение вариантов диффузной мастопатии позволяет более патогенетически подойти к выбору необходимых лекарственных средств, терапевтических подходов.
Аденоз молочных желез молодого возраста
Этот клинический вариант мастопатии характерен для пациенток в возрасте от 16 до 30 лет. При обращении больные предъявляют жалобы на боли в области молочных желез, усиливающиеся, как правило, в предменструальный период. Пальпаторно выявляются болезненные диффузные или локальные уплотнения, «нагрубания» ткани молочных желез. При ультразвуковом исследовании имеет место диффузное усиление эхоплотности или отсутствие каких-либо патологических признаков.
У ряда пациенток могут быть светлые выделения из сосков.
При цитологическом исследовании мазков отмечается отсутствие клеточных элементов.
Анамнестические сведения и результаты гинекологического обследования позволяют диагностировать у части больных неустановившийся менструальный цикл и склонность к персистированию фолликула.
Терапевтический эффект при данном клиническом варианте мастопатии достигается длительным приемом 0,25% раствора йодистого калия (1 чайная ложка 2–3 раза в день), витаминов группы А, Е. Продолжительность лечения от 3 до 6 мес. В ряде случаев в течение года назначаются повторные курсы лечения, седативная терапия.
Назначение андрогенов в молодом возрасте не показано, так как, обладая ингибирующим действием на гонадотропную функцию гипоталамо-гипофизарной системы, они не только не способствуют нормализации процессов овуляции, но и отягощают имеющиеся нарушения.
Диффузный аденоз и диффузный фиброаденоматоз на фоне дисменореи
Возраст больных при этом клиническом варианте мастопатии составляет от 25 до 45 лет. Заболевание проявляется болевым синдромом различной интенсивности. Пальпаторно определяется диффузное или локальное нагрубание молочных желез, грубодольчатая структура и фиброзная тяжистость ткани желез. На маммограммах выявляется различной распространенности затемнение неоднородной структуры. При ультразвуковом исследовании отмечается диффузный фиброз ткани молочных желез, наличие мелкокистозных образований. При цитологическом исследовании выделений, наблюдаемых у части больных, определяется наличие эпителиальных клеток и псевдомолозивных телец (клетки с выраженной апокринизацией).
Характерным для этого варианта мастопатии является наличие у больных дисменореи различного генеза. Наиболее частыми причинами дисменореи являются персистирование фолликула, атрезия фолликулов.
Лечение данной группы больных необходимо проводить совместно с гинекологом. При персистировании фолликула целесообразным является назначение в соответствии со второй фазой менструального цикла гестагенных препаратов (норколут, дюфастон) (Г. В. Бабаева, 1986; Т. Е. Самойлова, 1986).
При атрезии фолликулов наиболее оптимально назначение эстрогенов (синестрол, микрофоллин) и гестагенных препаратов (климонорм, дивина) в соответствии с фазами менструального цикла в обычных терапевтических дозах. У ряда больных положительный терапевтический эффект оказывают комбинированные эстроген-гестагенные препараты (климодиен, мерсилон, овидон, фемоден), назначаемые 21-дневными курсами с недельными перерывами. Продолжительность лечения до 6 мес. После купирования симптомов заболевания целесообразен профилактический прием гормональных препаратов в течение 3 мес дважды в год (Е. Ф. Кира и соавт., 2000).
Диффузная мастопатия зрелого возраста, периода предменопаузы
Этот клинический вариант диффузной мастопатии характерен для женщин 40–50 лет. Часто у них имеет место патология в гинекологической сфере (хронические андекситы, кисты яичников, фибромиома матки и т. д.). Основными жалобами являются боли в области молочных желез, мало связанные с менструальным циклом. При пальпации выявляются признаки начальной жировой инволюции молочных желез: железы мягкоэластической консистенции с липоматозными дольками различной величины, выраженной на этом фоне фиброзной тяжистостью. На маммограммах определяются округлые тени с ровными контурами до 1 см в диаметре или сочетание участков уплотнения с участками просветления. При ультразвуковом исследовании отмечаются участки фиброза на фоне пониженной эхоплотности. Выделения из сосков, как правило, отсутствуют.
Терапевтический эффект достигается назначением седативных препаратов (бром-валериановая смесь в форме микстуры Мильмана) и синтетических прогестинов (норколут с 16-го по 25-й дни менструального цикла). При начальных проявлениях климактерического синдрома и сохраненной менструальной функции возможно также назначение во второй половине цикла андрогенных препаратов (метилтестостерон в суточной дозе 10 мг). Положительный эффект у данной категории больных может быть достигнут при применении комбинированных эстроген-гестагенных препаратов: климена, климонорма (А. Б. Ильин, 1998).
Кистозная и фиброзно-кистозная мастопатия
Особенностью этого клинического варианта мастопатии является наличие выделений молозивного типа. Цитологическое исследование выделений выявляет наличие молозивных телец, эпителиальных клеток, иногда со склонностью к пролиферации. Болевой синдром выражен незначительно. Пальпаторно участки уплотнения в молочных железах обычно не определяются, фиброзная тяжистость ткани имеет различную степень выраженности.
На маммограммах выявляется наличие узких линейных теней, образующих крупнопетлистую сетку на светлом фоне. Ультразвуковое исследование свидетельствует о наличии диффузного незначительного фиброза, расширенных гипоэхогенных зон, расширенных протоков.
Клинические и анамнестические данные позволяют говорить о базальной гиперпролактинемии при отсутствии достаточного функционального подъема синтеза пролактина: наряду с наличием выделений у большинства больных в момент обращения или в анамнезе была эрозия шейки матки с рецидивирующим течением, продолжительность лактации редко достигала 6 мес, были случаи временной аменореи (М. Г. Стуруа, 1983). Наличие гиперпролактинемии подтверждается данными лабораторных исследований.
Больным этой группы проводится дегидратирующая терапия (хлористый аммоний, магнезия в порошках, легкие салуретики).
Лечебный эффект чаще достигается назначением парлодела — препарата, снижающего активность пролактина. Доза составляет 5–7,5 мг/сут, при плохой переносимости суточная доза снижается до 2,5 мг. При отсутствии эффекта от одного препарата возможна комбинация во второй половине цикла парлодела с гестагенными средствами. Недопустимо сочетание парлодела с эстрогенными и комбинированными эстроген-прогестиновыми препаратами. В последние годы широкое применение нашел агонист дофамина мастодинон, назначаемый по 30 капель 2 раза в день в течение 3–6 мес.
Мастодигения на фоне жировой инволюции молочных желез
Этот клинический вариант диффузной мастопатии определен нами на основании публикаций S. Z. Halsman, G. Shyamala (1981), которые показали, что жировая инволютивная ткань молочной железы отличается большим содержанием эстрогеновых рецепторов.
Тесты на гормональную насыщенность у этой категории больных показывают высокую эстрогеновую активность, хотя у большинства из них имеет место менопауза 5 и более лет.
Заболевание проявляется болевым синдромом в области молочных желез. Клинически и рентгенологически отмечается жировая инволюция молочных желез. Молочные железы с выраженными липоматозными дольками, фиброзной тяжистостью, умеренно болезненны при пальпации. На маммограммах имеются обширные просветления с тяжевым фиброзным рисунком. Эта группа женщин требует проведения дифференциального диагноза между мастодигенией и болевым корешковым синдромом, обусловленным остеохондрозом грудного отдела позвоночника.
Лечение мастодигении на фоне жировой инволюции молочных желез проводится поэтапно. В начале назначаются бромкамфора и нестероидные противовоспалительные препараты (напроксен, диклофенак, индометацин). При отсутствии эффекта от приема этих препаратов, используются андрогены (метилтестостерон 10 мг/сут, тестостерон) в течение 10 дней с 20-дневным перерывом. Длительность лечения при этом составляет от 3 до 6 мес. Рекомендации, касающиеся режима назначения андрогенов, разработаны Л. Г. Тумилович, Т. Е. Самойловой (1988).
При неэффективности андрогенотерапии возможно применение антиэстрогенного препарата тамоксифена. Суточная доза составляет 0,01 г, длительность приема от 1 до 3–6 мес (C. S. Gaset, 1985).
Фиброзная мастопатия негенитального генеза
Возраст больных при этом варианте заболевания составляет 20–40 лет. Больных беспокоят сильные боли в области молочных желез, не связанные с менструальным циклом. При пальпации определяются диффузное уплотнение ткани молочных желез, грубая фиброзная тяжистость при отсутствии выделений. На маммограммах отмечается наличие затемнений, характерных для выраженного диффузного фиброза.
Клинические, рентгенологические данные, результаты ультразвукового исследования говорят о резком преобладании в ткани молочных желез фиброзных компонентов. Патологии со стороны гениталий, как правило, не отмечается. У части больных имеют место слабоположительные ревмопробы.
Улучшение при этом клиническом варианте мастопатии достигается благодаря назначению нестероидных противовоспалительных препаратов (диклофенак, напроксен, индометацин). Положительный терапевтический эффект проявляется в купировании болевого синдрома и уменьшении выраженности фиброза молочных желез. При сильных болях и упорном течении заболевания назначаются кортикостероиды (полькортолон, 8–16 мг/ сут) до улучшения состояния больных. Отмена кортикостероидов производится постепенно на фоне приема нестероидных противовоспалительных средств. Больные этой группы в большинстве своем в течение года получают повторное лечение, включающее индометацин, комплекс витаминов (веторон Е, ревивона, триовит, витрум циркус, сана-сол), биостимуляторы (ФИБС, стекловидное тело).
В заключение следует отметить, что определение клинического варианта диффузной мастопатии позволяет патогенетически подойти к подбору лекарственных средств. Многосторонность клинического проявления заболевания порой затрудняет определение его клинического варианта. Это обусловливает необходимость тщательного углубленного обследования больных, длительного наблюдения и проведения продуманного поэтапного лечения.
По вопросам литературы обращайтесь в редакцию.
В. С. Кириллов Воронежский областной клинический онкологический диспансер, Воронеж
А если это рак молочной железы? (опасные симптомы и признаки)
Рак груди – что это?
Что такое рак молочной железы сегодня ответить сложно. Это большая социальная проблема, больных становится с каждым годом все больше, чаще болеют молодые женщины.
Почему возникает рак груди?
Причин много, это и стресс в нашей жизни, и ритм жизни, все куда-то спешат, торопятся, не знают, что будет завтра. Плюс, раньше женщина была хранительницей домашнего очага, матерью, а сегодня у всех работа, карьера и о семье и детях задумываются после 35-40 лет. Но все нужно в жизни делать во время, нужно успевать и детей рожать и воспитывать и делать карьеру.
Какие формы злокачественых образований (рака) в молочной железе выделяют?
Злокачественные образования молочной железы подразделяются на эпителиальные и неэпителиальные опухоли молочной железы.
Неэпителиальные опухоли – это саркома молочной железы, которая встречается в 0,6-4% случаев всех злокачественных образованиях молочной железы. По морфологическим признакам выделяют: липосаркрму, фибросаркому, ангиосаркому, гемосаркому, хондриостеоидную саркому, ретиноклеточную саркому, лимфосаркому, стромальную саркому Берга и пр. Саркомы молочной железы характеризуются медленным ростом, опухоли безболезненны, с довольно четким контуром, местами бугриты. Поначалу опухоли не инфильтрируют и не фиксируют кожу, но когда они достигают больших размеров, в 43% случаев наблюдается спаянность опухолевого узла с кожей, а также расширение подкожной венозной сети. Особенность сарком в том, что они не поражают лимфатические узлы, для них характерно гематогенное метастазирование в легкие и кости. Прогноз более благоприятен, чем при раке, и зависит от распространенности опухоли, степени ее дифференцировки и гистологического типа. Саркомы лечат хирургическим методом, химиолучевому лечению они поддаются плохо.
Также к неэпителиальным опухолям относится лимфома молочной железы (0,1-0,17% всех злокачественных опухолей) – это опухоль лимфоидной ткани, имеющая первичный очаг, подобно солидным опухолям, однако способная не только к метастазированию, но и к диссеминации по всему организму одновременно с формированием состояния, напоминающего лимфоидные лейкозы. Диагноз как правило, устанавливается по результатам гистологического исследования уплотнения. Данная патология лечится успешно химиотерапевтическими методами.
К эпителиальным формам относятся протоковый и дольковый раки молочной железы с различной степенью инвазии.
Чаще встречается односторонний РМЖ, двухсторонний (3-15%) рак возникает одновременно или чаще через 3-7-12-20 и более лет.
В зависимости от сроков развития опухоли во второй молочной железе, а также по некоторым другим признакам выделяют следующие типы рака второй молочной железы:
В зависимости от распространенности рак подразделяют на две формы — узловую и распространенную (диффузную).
Выделяют особую форму рака молочной железы – это рак Педжета, или рак соска. Он развивается из эпителия сосков и распространяется на ареолу и кожу, напоминая экзему, что затрудняет диагностику, т. к. часто такие пациенты сначала обращаются к дерматологу, а не к онкологу. На поздних стадиях опухоль прорастает ткань железы и протекает как обычная карцинома.
В каких случаях женщине нужно «бить тревогу» и экстренно идти к доктору, если она не посещала его регулярно до этого? (самодиагностика, выделения, боль).
Если женщина обнаружила у себя какое-либо образование в молочной железе, необходимо сразу же идти к врачу, причем хочется отметить, что 80% образований в молочной железе, женщины находят самостоятельно, и, только у 20% пациенток ставится диагноз злокачественного образования, в остальных случаях это доброкачественные процессы. Если появились какие-то изменения в состоянии молочных желез, это могут быть деформация, увеличение размеров железы, изменение кожных покровов железы, в этих ситуациях необходимо обращаться к специалистам. В отношении выделений из соска, следует обращать внимание на цвет выделений, если они становятся бурыми, кровянистыми, следует незамедлительно идти к врачу. Прозрачные, или желтоватые выделения могут иметь место при кистозном фиброаденоматозе. При появлении жалоб на боль в молочной железе, следует также обратиться к врачу. Причиной болевого синдрома может быть не только молочная железа, часто боли в наружных квадрантах желез обусловлены патологией позвоночника, например распространенным остеохондрозом. Но всегда, первоначально исключается патология молочных желез.
Основными признаками наличия патологии молочных желез, которые может выявить женщина самостоятельно, являются:
Эти признаки могут быть симптомами не только злокачественных опухолей молочной железы, но и ряда других заболеваний, в связи с чем, появление хотя бы одного из них требует обязательной консультации со специалистом.
Диагностика рака молочной железы основывается на данных трех основных методов — клинического, радиологического и патоморфологического. Клиническое обследование включает осмотр и пальпацию молочных желез и регионарных лимфатических узлов. Следует отметить, что каждая женщина должна ежемесячно проводить обследование молочных желез, т. к. до 80% образований в молочных железах женщины обнаруживают самостоятельно.
Если при выполнении процедуры самообследования женщина нашла какое-либо уплотнение в молочных железах, необходимо сразу обратиться к специалисту – онкологу-маммологу. После осмотра врач назначает дополнительное обследование: это может быть радиологическое обследование — маммография, которая чаще выполняется у женщин после 35 лет, или ультразвуковое исследование молочных желез (и регионарных зон, в зависимости от конкретной ситуации). Возможно сочетание этих двух методов, поскольку они дополняют друг друга и позволяют доктору поставить точный диагноз. В сложных клинических ситуациях помогает установить диагноз компьютерная томография или магнитно-резонансная маммография. Одним из важных моментов обследования при постановке диагноза – является получение гистологического подтверждения данного заболевания. Патоморфологический диагноз устанавливается с помощью трепан-биопсии новообразования молочной железы. По материалу, полученному при трепан-биопсии, устанавливается патоморфологическая форма опухоли и определяются дополнительные характеристики образования, необходимые для планирования лечения: степень злокачественности опухоли, рецепторы эстрогена и прогестерона, наличие гиперэкспрессии гена HER2new. При невозможности выполнения трепан-биопсии можно выполнить аспирационную биопсию (пункцию) новообразования молочной железы. Эта процедура дает цитологическое подтверждение диагноза, но, к сожалению, в этой ситуации отсутствует информация о рецепторном статусе опухоли и степени дифференцировки. Также возможно получение гистологического подтверждения диагноза интраоперационно – выполняется срочное гистологическое исследование удаленного образования во время операции, и определяется дальнейшая тактика лечения, возможно с расширением объема оперативного вмешательства.
Какие существуют методы лечения рака груди, от чего это зависит?
Существует следующие методы лечения рака молочной железы:
Интересно отметить, что в России, по данным последнего статистического отчета, только операция выполнена 23.8% пациенток, у подавляющего большинства (74.7% больных) применяются комбинированные и комплексные методы лечения. Успех лечения напрямую зависит от стадии заболевания, чем раньше выявлено заболевание и начато лечение, тем лучше результат. Плюс, следует помнить, что при начальных формах заболевания, возможно выполнить органосохраняющее лечение и пластику молочной железы, ведь сохранить молочную железу женщина хочет в любом возрасте, это очень важный психологический аспект лечения. Большое значение имеет психологический настрой пациента, степень его доверия врачу.
Предопухолевая патология молочной железы
Международные названия
Содержание
Дольковая (лобулярная) неоплазия молочной железы
Наиболее сложным в патологической анатомии является вопрос дифференциальной диагностики гиперпластических процессов, которые возникают на фоне гормональной стимуляции, прежде всего гиперэстрогении, и начальных форм РМЖ.
Дольковая неоплазия наиболее часто развивается у женщин в предменопаузальный период (в возрасте 45–47 лет) и составляет 1–3,8% всех эпителиальных патологических процессов молочной железы. В 0,5–4% материала биопсий, взятых по поводу доброкачественных заболеваний молочной железы, выявляют дольковую неоплазию разной степени дифференцировки. В 85% случаев дольковая неоплазия возникает мультицентрично и в 30–67% — билатерально.
Для лобулярной неоплазии характерна пролиферация мелкого эпителия, расположенного в просвете долек, со слабым межклеточным соединением, с педжетоидной реакцией или без нее. Происходит дольковая неоплазия из эпителия концевой (терминальной) протоково-дольковой единицы молочной железы. Выраженность атипии, степень пролиферации, количество атипических митозов зависят от степени дифференцировки неоплазии. Выделяют два типа клеток дольковой неоплазии: тип А и тип В. Тип А состоит из мономорфных эпителиальных клеток, тип В — из крупных полиморфных клеток с выраженными признаками атипии. Хотя клетки крупные, они гораздо мельче эпителия протоков.
Может быть смешанный тип, представленный сочетанием в разной пропорции клеток типа А и В.
Согласно Классификации РМЖ ВОЗ (2003) рекомендуется пользоваться термином «дольковая неоплазия», подразделяя ее на три степени и термин «дольковый рак in situ ».
Деление на степени дифференцировки дольковой неоплазии происходит в зависимости от выраженности клеточного полиморфизма, наличия некрозов, признаков атипии и количества митозов.
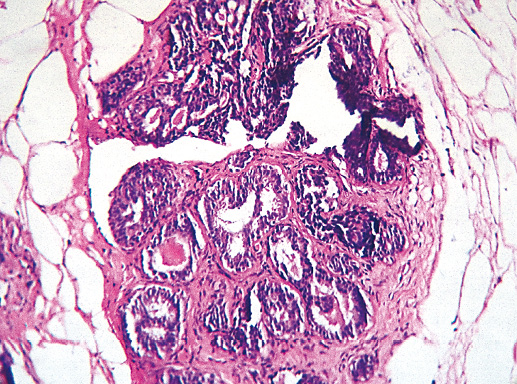
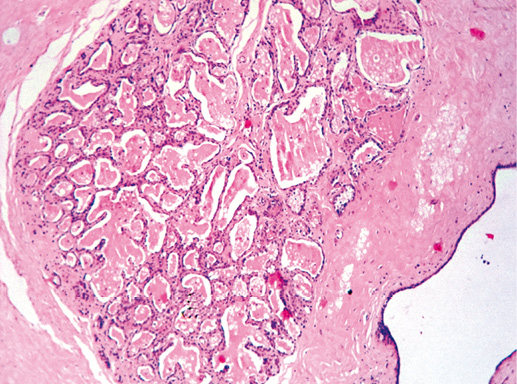
Легкая степень дольковой неоплазии (первая степень неоплазии) характеризуется сохранением альвеолярной архитектоники, пролиферацией в одной или нескольких дольках мелких мономорфных эпителиальных клеток, слабо сцепленных между собой (клетки типа А). Как правило, клетки в очаге пролиферации имеют округлое, нечетко отграниченное ядро и скудную цитоплазму. Некрозы, митозы и кальцинаты редки. Иногда отмечают очаги пролиферации и полиморфизма клеток, появляются скопления крупных клеток, но эти признаки представлены незначительно. В единичных дольках могут быть признаки апокриновой неоплазии (фото 3).
Фото 3. Легкая степень дольковой неоплазии. Общее строение дольки сохранено, однако количество долек значительно увеличено, отмечается выработка секрета, эпителий мелкий мономорфный. Гематоксилин-эозин, х 100
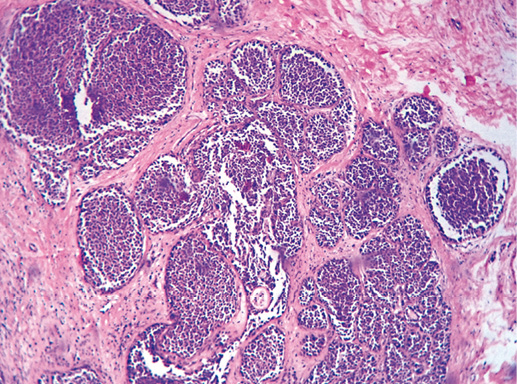
Умеренная дольковая неоплазия (вторая степень неоплазии) характеризуется нарастанием полиморфизма эпителия долек, появлением большего количества крупных клеток с неправильной формой ядра и обильной цитоплазмой, отмечают единичные митозы и отдельные перстневидные клетки. Миоэпителиальные клетки чаще располагаются вдоль базальной мембраны, но могут вытесняться из обычного места расположения и примешиваться к эпителиальному пролиферату. Базальная мембрана сохранна на всем протяжении (фото 4, 5).
Фото 4. Умеренная степень дольковой неоплазии. Отмечается пролиферация и формирование многорядного эпителия, очаги секреции. Гематоксилин-эозин, х 200
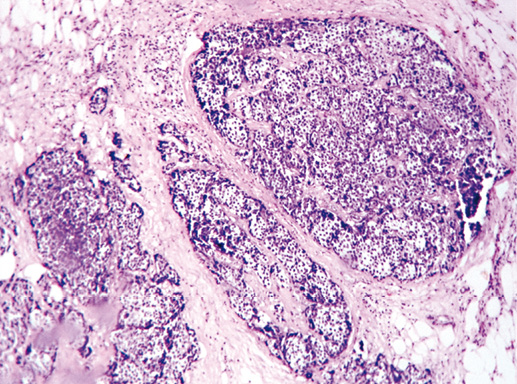
Фото 5. Умеренная степень дольковой неоплазии. Эпителий полиморфный, формирует сосочки, миоэпителиальные клетки местами вытесняют эпителиальные. Гематоксилин-эозин, х 400
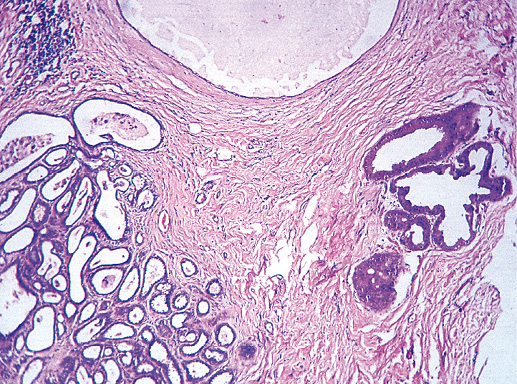
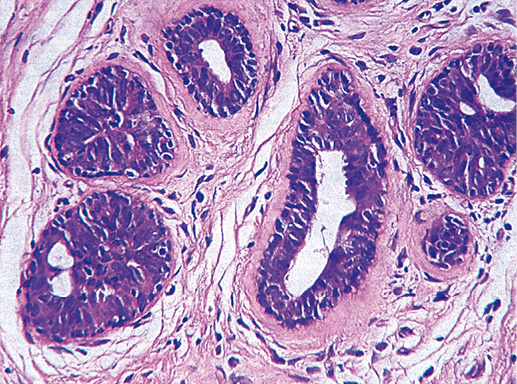
Фото 6. Тяжелая степень дольковой неоплазии. Дольки расширены, просвет полностью заполнен эпителиальными клетками. Гематоксилин-эозин, х 100
Фото 9. Простая протоковая гиперплазия. Некоторые протоки расширены в виде кист, в отдельных протоках видны признаки апокриновой секреции, однако общее строение протоков сохранено. Гематоксилин-эозин, х 100
Для описания атипической дольковой неоплазии часто используют термин «дольковый рак in situ ». Все эти процессы имеют один морфологический код в Международном классификаторе онкологических заболеваний — 8520/2.
Рак in situ часто ассоциирован с микроинвазивным раком в окружающих участках, поэтому его исследование требует особой ответственности и внимания при установлении диагноза. Необходимо изучить большое количество срезов и края резекции. В сложных случаях для исключения инвазивного рака необходимо исследовать базальную мембрану для выявления ее целостности и доказать отсутствие нарушения миоэпителиального слоя и базальной мембраны.
Важным условием диагностики дольковой неоплазии является отсутствие инвазии опухолевыми клетками базальной мембраны. Для исключения инвазии применяют антитела, выявляющие коллаген IV типа и гладкомышечный актин.
Через довольно длительный промежуток времени у некоторых женщин на фоне рака in situ возникают инвазивные формы рака, но следует отметить, что дольковый рак in situ не обязательно является предраком инфильтративных форм.
Внутрипротоковые пролиферативные поражения
К ним относят простую протоковую гиперплазию, гиперплазию со слабо выраженной пролиферацией эпителия, атипическую протоковую гиперплазию и протоковый рак in situ (трех степеней дифференцировки).
Существуют два классификационных подхода к оценке эпителиальных пролиферативных поражений протоков. Касательно молочной железы одновременно используют две классификационные схемы.
Простая протоковая гиперплазия
Простая протоковая гиперплазия
Слабо выраженная протоковая атипия
Протоковая интраэпителиальная неоплазия Grade1А
Атипическая протоковая гиперплазия
Протоковая интраэпителиальная неоплазия Grade1В
Протоковый рак in situ Grade1
Протоковая интраэпителиальная неоплазия Grade1С
Протоковый рак in situ Grade2
Протоковая интраэпителиальная неоплазия Grade2
Протоковый рак in situ Grade3
Протоковая интраэпителиальная неоплазия Grade3
Левый столбик отражает взгляды большинства экспертов ВОЗ, терминологию, представленную справа, используют преимущественно в Северной Америке.
Нам кажется, что классификация ВОЗ более отражает сущность опухолевой трансформации, кроме того эта схема более воспроизводима и более наглядна для восприятия в реальных практических условиях.
Популяционный маммологический скрининг требует выделения патологических состояний, имеющих чрезвычайно высокий риск развития инвазивного рака молочной железы. Результаты дальнейших клинических исследований показали, что различные внутрипротоковые пролиферации с различной частотой переходят в рак in situ и инвазивный рак. Так, риск развития инвазивного РМЖ из простой протоковой гиперплазия составляет 1,5%, из атипической протоковой гиперплазии 4–5% и рака in situ 8–10% [1].
Термин «интраэпителиальная неоплазия» широко используют для описания патологии не только молочной железы, но и предстательной железы, шейки матки.
Простая (обычная) протоковая гиперплазия часто возникает на фоне мастопатии и выглядит как пролиферация эпителия с признаками некоторого полиморфизма внутри протоков. Протоки располагаются неравномерно, их размеры разные. Характерно изменение нормальной структуры протоков, формирование расширенных, неправильной формы протоков вокруг долек нормального строения. Протоки ветвятся в виде ручейков от центра участка гиперплазии к периферии. Клеточные пролифераты могут формировать солидные участки, криброзные структуры, мостики.
Фото 10. Простая протоковая гиперплазия. Участок апокриновой метаплазии. Гематоксилин-эозин, х 100
Фото 11. Протоковая неоплазия со слабо выраженной атипией. Гематоксилин-эозин, х 100
Критерии простой протоковой гиперплазии
Цитологические. Вариабельность форм ядер с гиперхромными округлыми и овальными ядрышками, ассиметричными нуклеолами.
Интерцеллюлярные расстояния отличаются по размеру и форме, часто отмечают щелеподобные структуры.
Риск развития инвазивного рака из простой протоковой гиперплазии составляет 2,6% за период наблюдения около 14 лет. Следует отметить, что такой процент инвазивного рака на фоне атипической протоковой гиперплазии формируется за 8,3 года [61]. В другом исследовании указывается, что в 4% случаев простая протоковая гиперплазия транформировалась в инвазивный РМЖ за 15 лет наблюдения [62]. Однако риск развития рака на фоне этой гиперплазии значительно ниже, чем при других вариантах гиперплазий.
Обычная протоковая гиперплазия является одним из морфологических проявлений гормональных изменений в организме женщины.
Морфофункциональные изменения, возникающие в различные периоды менструального цикла и беременности, могут симулировать обычную протоковую гиперплазию, поэтому патологоанатом должен иметь информацию о состоянии женщины, ее возрасте, наличии эндокринных и гинекологических заболеваний. Обязательно следует выдерживать сроки взятия биопсии или проведения операции в соответствии с менструальным циклом.
Протоковая неоплазия со слабо выраженной атипией
В данном варианте протоковой неоплазии по сравнению с предыдущим более выражена пролиферация эпителия, клетки формируют в протоке от 1 до 3–5 рядов, более существенно проявление атипии клеток. Папиллярные, криброзные, солидные пролифераты отсутствуют. Часто отмечают секрецию эпителия (цитоплазма клеток становится обильной светлой пенистой, ядро расположено ассиметрично, ближе к базальному краю) и секрет в просвете протоков (фото 12–14). Возможны микрокальцинаты. Морфологическая картина при этой патологии соответствует протоковой интраэпителиальной неоплазии Grade 1А.
Фото 12. Протоковая неоплазия со слабо выраженной атипией. Гематоксилин-эозин, х 200
Фото 13. Протоковая неоплазия со слабо выраженной атипией. Эпителий протоков формируют микропапиллярные структуры и сосочки. Гематоксилин-эозин, х 200
Фото 14. Атипическая протоковая гиперплазия. Эпителий протоков полиморфный с гиперхромными ядрами. Гематоксилин-эозин, х 200
Риск развития инвазивного рака на фоне простой протоковой атипии выше, чем на фоне простой протоковой гиперплазии.
Атипическая протоковая гиперплазия
Это заболевание характеризуется более выраженной пролиферацией эпителия, усилением признаков клеточного полиморфизма и появлением атипии разной степени выраженности. Заболевание характеризуется умеренным риском развития инвазивного рака молочной железы.
В протоках отмечают равномерное распределение мономорфных клеток с округлым ядром. Эпителиальные клетки формируют папиллярные структуры, солидные группы, пучки, аркады, криброзные структуры внутри протоков. Морфологическая картина соответствует протоковой интраэпителиальной неоплазии Grade 1В, местами протоки похожи на рак in situ G- 1. Для атипической протоковой гиперплазии обязательны участки простой протоковой гиперплазии. Для исключения рака in situ общим требованием является взятие на исследование ткани через каждый 1 мм и исследование серийных срезов гистологического блока.
Микрокальцинаты могут отсутствовать, быть представленными фокально или на большом протяжении. Это не является ведущим фактором для установления диагноза (фото 15–19).
Фото 15. Атипическая протоковая гиперплазия. Некроз и кальцинаты в протоках. Гематоксилин-эозин, х 200
Фото 16. Атипическая протоковая гиперплазия. Эпителий протоков полиморфный с гиперхромными ядрами, формирует криброзные структуры, слева отмечается очаг некроза, во многих протоках явления секреции. Гематоксилин-эозин, х 200
Фото 17. Атипическая протоковая гиперплазия. Атипичный эпителий в протоках формирует солидные пласты, однако нет инвазии стромы. Гематоксилин-эозин, х 200
Фото 19. Экспрессия гладкомышечного актина (клон HHF35, производство DAKO). Иммуногистохимическое окрашивание, система визуализации EnVision, хромоген DAB. Миоэпителиальные клетки в виде непрерывной линии вдоль базальной мембраны. х 200
Атипическая протоковая гиперплазия имеет довольно высокий риск развития инвазивного РМЖ. По данным различных авторов инвазивный рак развивается в 3,7–22% случаев атипической протоковой гиперплазии [66, 67].
Важнейшим отличительным признаком любой формы протоковой интраэпителиальной неоплазии является наличие непрерывной базальной мембраны и слоя миоэпителиальных клеток. В зависимости от степени протоковой интраэпителиальной неоплазии количество эпителиальных клеток отличается.
Наиболее важная и сложная задача патологоанатома — не пропустить инвазию опухолевыми клетками базальной мембраны. Эта задача может быть выполнена только в результате кропотливого исследования большого количества срезов, отбора наиболее подозрительных на малигнизацию участков и проведения дополнительных методов окраски базальной мембраны и миоэпителиальных клеток. Неоценимую помощь в этом оказывает иммуногистохимический метод исследования. Для маркировки миоэпителиальных клеток мы часто применяем антитела к гладкомышечному актину, которые дают четкое окрашивание, и реакция легко воспроизводима.
Внутрипротоковая папиллома
Эти образования возможны в любом месте в пределах системы протоков от соска до терминальной дольково-протоковой единицы. Бывают доброкачественные варианты (внутрипротоковая папиллома), атипические (атипическая папиллома) и злокачественные (внутрипротоковый папиллярный рак).
Среди внутрипротоковых папиллом в зависимости от локализации выделяют центральные и периферические варианты. Центральная внутрипротоковая папиллома — это одиночное образование, располагающееся, как правило, в субареолярной зоне, часто в кистозно-расширенном протоке. Периферические внутрипротоковые папилломы чаще множественные. Большинство исследователей считают, что одиночные внутрипротоковые папилломы не имеют тенденции к малигнизации. Множественные папилломы, особенно в периферических отделах дольково-протоковой системы, склонны к озлокачествлению. Большие затруднения возникают при диагностике центральных внутрипротоковых папиллом, так как они могут клинически сопровождаться кровянистыми выделениями из соска [5].
Диагностика папиллом включает обязательно маммографию, ультразвуковое исследование (УЗИ), а также цитологическое исследование выделений из соска.
Внутрипротоковая папиллома — округлое образование с четкой границей размером 3–4 см, но возможны процессы, занимающие несколько сантиметров в диаметре. Внутрипротоковая папиллома представлена сосочковыми разрастаниями, состоящими из фиброваскулярной ножки, покрытой эпителием и миоэпителием (фото 20). Часто отмечают апокринизацию эпителия [5].
Фото 20. Внутрипротоковая папиллома. Гематоксилин-эозин, х 200
Фото 21. Внутрипротоковая папиллома. Видны отдельные сосочки с фиброзной стромой и однорядной эпителиальной выстилкой. Гематоксилин-эозин, х 200
Фото 22. Периферическая внутрипротоковая папиллома. Гематоксилин-эозин, х 200
Фото 23. Атипическая внутрипротоковая папиллома. Сосочки имеют грубоволокнистую соединительнотканную основу, миоэпителиальный компонент и один или несколько слоев эпителиальных клеток с гиперхромными ядрами. Гематоксилин-эозин, х 200
Термин «папилломатоз» молочной железы эксперты ВОЗ рекомендуют избегать и использовать термин «множественные внутрипротоковые папилломы».
Все внутрипротоковые папилломы имеют общий морфологический код в Международном классификаторе онкологических заболеваний — 8503/0.
Центральная внутрипротоковая папиллома
Гистологическое строение центральной и периферической внутрипротоковой папилломы одинаковое. Однако, учитывая большие размеры центральной папилломы, в ней можно отметить участки двух видов: протоковый и папиллярный. Папиллярные образования представлены фиброваскулярной ножкой, покрытой двумя слоями эпителия. Протоковый компонент имеет строение описанных выше протоковых гиперплазий. Опухоли, в которых преобладает протоковый компонент и склероз стромы, обычно называют «склерозирующая папиллома».
В центральных внутрипротоковых папилломах могут быть представлены участки пролиферации миоэпителия, апокринизация эпителия, плоскоклеточная, хрящевая и костная метаплазия, внутрипротоковая пролиферация эпителия, воспалительная инфильтрация. Отсутствие клеточной атипии, инвазии стромы позволит диагностировать центральную внутрипротоковую папиллому. Особенно кропотливой работы требуют папилломы с участками, имитирующими микроинвазию. Большую помощь в таких случаях оказывает иммуногистохимическое исследование компонентов базальной мембраны и миоэпителия. Чаще для этих целей применяют антитела, выявляющие коллаген IV типа и гладкомышечный актин.
Периферическая внутрипротоковая папиллома
В отличие от центральной внутрипротоковой папилломы, эта опухоль развивается у женщин более молодого возраста. Клиническое течение чаще протекает скрыто. Большие размеры папиллом могут пальпироваться. Маммография выявляет чаще множественные узловые образования с четкими контурами, возможны микрокальцинаты.
Характерный мультицентричный рост периферической внутрипротоковой папилломы может быть на фоне внутрипротоковой гиперплазии, карциномы in situ или инвазивного рака.
Термин «микропапиллома» применяют к малым формам периферической внутрипротоковой папилломы. Часто микропапилломы выявляют в больших фокусах аденоза молочной железы.
Атипическая внутрипротоковая папиллома
Эта форма внутрипротоковой папилломы выделена из-за ее важного прогностического значения, поскольку именно на фоне атипической внутрипротоковой папилломы чаще возникают инвазивные карциномы.
Внутрипротоковый папиллярный рак лишен (почти на всем протяжении) миоэпителиального клеточного слоя и характеризуется пролиферацией атипичного эпителия (фото 24). Часто бывает мультицентричный рост.
Фото 24. Внутрипротоковый папиллярный рак. Часть сосочков не имеет соединительной ткани в своей основе и состоит из атипичных эпителиальных клеток. Гематоксилин-эозин, х 400
Эта опухоль имеет свой морфологический код в Международном классификаторе онкологических заболеваний — 8503/2.