Материалы конгрессов и конференций
23-й ежегодный симпозиум «Рак молочной железы»
Сан Антонио, США, 2000 год
САН-АНТОНИО 2000: гормонотерапия рака молочной железы
В последние годы целый ряд новых гормональных агентов для лечения рака молочной железы (чистые антиэстрогены, ингибиторы ароматазы и агонисты гонадотропин-рилизинг-гормонов) интенсивно изучаются у женщин с гормонозависимыми опухолями. Эти препараты сравниваются с «золотым» стандартом тамоксифеном, а также друг с другом в больших клинических исследованиях.
Тамоксифен vs Анастрозол при диссеминированном раке молочной железы.
Сравнение эффективности ингибитора ароматазы анастрозола с тамоксифеном в качестве гормонотерапии первой линии проведено в двух больших мультицентровых исследованиях, имевших сходный дизайн: Европейском и Северо-Американском. [1,2]. Эти исследования продемонстрировали небольшое повышение эффективности анастрозола по сравнению с тамоксифеном, а также увеличение времени до прогрессирования, особенно у больных с положительными рецепторами к эстрогену.
Аналогичные результаты получены также в исследовании испанских авторов, в котором анастрозол сравнивался с тамоксифеном при проведении гормонотерапии первой линии у больных с положительными рецепторами к эстрогену [3] (табл.4).
Таблица 4.
Анастрозол vs Тамоксифен: Барселонское исследование.
| Тамоксифен | Анастрозол | р | |
|---|---|---|---|
| Кол-во больных | 117 | 121 | |
| Суточная доза | 40 мг | 1 мг | |
| Эффективность | 23% | 34% | Нет данных |
| Среднее время до прогр. | анастрозол | Анастрозол > Там | |
| Кол-во больных | 74 | 85 | |
| Эффективность | 8% | 9% | |
| Стабилизация >24 нед. | 52% | 41% |
Полученные данные свидетельствуют о существенной активности анастрозола у больных с прогрессированием на фоне приема тамоксифена и наоборот. Это несомненно является обнадеживающим для больных с гормоночувствительными опухолями молочной железы. Однако, проведение перекреста не позволяет сделать вывод о том, какой же из двух препаратов обеспечил улучшение выживаемости в этих исследованиях.
При среднем сроке наблюдения 2 года никаких существенных изменений содержания холестерина, липопротеидов низкой и высокой плотности, а также триглицеридов не было отмечено ни среди больных, принимавших тамоксифен, ни в группе пациенток, принимавших анастрозол [5].
Летрозол в сравнении с Тамоксифеном при лечении распространенного и раннего рака молочной железы.
Второй ингибитор ароматазы летрозол также является объектом пристального внимания исследователей. Результаты двух больших исследований представлены компанией Новартис. В первом (двойном слепом, перекрестном) сравнивалась эффективность летрозола и тамоксифена при проведении гормонотерапии первой линии у больных в менопаузе с положительными или неизвестными рецепторами [6]. Полученные результаты представлены в табл. 6.
Таблица 6.
Летрозол в сравнении с тамоксифеном при распространенном раке молочной железы.
| Летрозол | Тамоксифен | Р | |
|---|---|---|---|
| Суточная доза | 2,5 мг | 20 мг | |
| Кол-во больных | 453 | 454 | |
| Средний возраст | 65 лет | 64 года | |
| РЭ+ и/или РП+ | 66% | 67% | |
| РЭ/РП неизвестны | 34% | 33% | |
| Предшествующая терапия тамоксифеном | 20% | 18% | |
| Ср. время до прогрессирования | 9,4 мес. | 6,0 мес. | 0,0001 |
| Эффективность | 30% | 20% | 0,0006 |
| Длительность эффектов | 23 мес. | 23 мес. | >0,05 |
| Ощущение приливов | 18% | 15% |
В этом исследовании летрозол обеспечивал лучшую непосредственную эффективность и более продолжительное время до прогрессирования по сравнению с тамоксифеном. Данные относительно выживаемости отсутствуют. Оба вида лечения переносились больными сравнительно хорошо. Летрозол оценен в сравнении с тамоксифеном также у больных в менопаузе с ранним раком молочной железы [7]. В исследование включались больные, которым планировалось органосохраняющее лечение, с гормонозависимыми опухолями. Продолжительность неоадъювантной гормонотерапии составляла 4 мес., после чего больные подвергались хирургическому лечению. Полученные результаты представлены в табл. 7.
Таблица 7.
Летрозол в сравнении с тамоксифеном в качестве предоперационной гормонотерапии рака молочной железы.
| Летрозол | Тамоксифен | Р | |||||
|---|---|---|---|---|---|---|---|
| Суточная доза | 2,5 мг | 20 мг | |||||
| Кол-во больных | 154 | 170 | |||||
| РЭ+ | 88% | 87% | |||||
| РП+ | 66% | 60% | |||||
| HER2+ | 12% | 16% | |||||
| Эффективность | 55% | 36% | 24 нед. | 24% | 29% | 25% | 19% |
| Длит. эффекта | 14,3 мес. | 14,0 мес. | 19,3 мес. | 10,5 мес. | |||
| Приливы | 18% | 17% | 24% | 24% |
В целом не было выявлено каких-либо существенных различий в частоте объективных эффектов или времени до прогрессирования между фулвестрантом и анастрозолом. Небольшое различие в длительности эффекта было отмечено в Северо-Американском исследовании.
Экземестан в сравнении с Тамоксифеном в качестве первой линии терапии диссеминированного рака молочной железы.
Экземестан в отличие от анастрозола и летрозола имеет стероидную структуру и необратимо блокирует ароматазу. Сравнение эффективности экземестана и тамоксифена проведено в рамках рандомизированного исследования, в котором приняли участие больные диссеминированным раком молочной железы в менопаузе с положительными РЭ и/или РП [10]. Основные результаты исследования приведены в табл. 9.
Таблица 9.
Экземестан vs Тамоксифен при диссеминированном раке молочной железы.
| Экземестан | Тамоксифен | |
|---|---|---|
| Суточная доза | 25 мг | 20 мг |
| Кол-во больных | 56 | 56 |
| Эффективность | 44% | 14% |
| Стаб. >24 недель | 11% | 25% |
В этом исследовании экземестан продемонстрировал лучшие непосредственные результаты лечения по сравнению с тамоксифеном.
Экземестан в неоадъювантной терапии местно-распространенного рака молочной железы. Роль экземестана в предоперационной терапии рака молочной железы оценена в небольшом исследовании II фазы [11], в которое включены 13 больных постменопаузального возраста с РЭ+. Участницы исследования получали экземестан в суточной дозе 25 мг в течение 3 месяцев перед хирургическим лечением. В среднем отмечено уменьшение опухолевой массы на 85%, и 83% больных ответили на лечение. В результате изучения биоптатов молочных желез было показано, что экземестан снижает циркуляцию периферических и синтез внутриопухолевых эстрогенов.
Итак, несколько рандомизированных исследований были посвящены сравнению тамоксифена и ингибиторов ароматазы в первой линии гормонотерапии диссеминированного рака молочной железы у больных в менопаузе. В целом, ингибиторы ароматазы отличались более благоприятным спектром токсичности по сравнению с тамоксифеном. В большинстве исследований ингибиторы ароматазы продемонстрировали сравнимую с тамоксифеном, а иногда и превосходящую его эффективность. Полученные результаты свидетельствуют о том, что ингибиторы ароматазы могут рассматриваться, наряду с тамоксифеном, как препараты выбора для лечения больных постменопаузального возраста с РЭ+, правда пока нет четких данных об улучшении выживаемости при использовании ингибиторов ароматазы. Нерешенным остается и вопрос об оптимальной последовательности назначения ингибиторов ароматазы и тамоксифена.
Выключение функции яичников или химиотерапия в качестве адъювантного лечения.
Возрождается интерес к проблеме аменореи/овариоэктомии у женщин пременопаузального возраста с гормонозависимой болезнью. Полагают, что эффект адъювантной химиотерапии частично реализуется через индуцируемую аменорею; исследования по изучению этой проблемы признаны сегодня приоритетными [12]. В частности, в исследовании ZEBRA с участием пациенток пременопаузального (
Заместительная гормональная терапия для мужчин с возрастным андрогенным дефицитом
Специализация: урология, андрология
Синдром возрастного андрогенодефицита у мужчин — это нарушение биохимического баланса, возникающее в зрелом возрасте по причине недостаточности андрогенов в сыворотке крови, нередко сопровождающейся снижением чувствительности организма к андрогенам. Как правило, это приводит к значительному ухудшению качества жизни и неблагоприятно сказывается на функциях практически всех систем организма. Естественно, что огромный интерес вызывают вопросы терапии андрогенного дефицита, поскольку именно она ставит сложную задачу перед врачом-клиницистом: выбрать из широкого арсенала методов и препаратов гормональной терапии наиболее оптимальный, сочетающий в себе качество, эффективность, а также удобство в применении.
В настоящее время врачи-урологи и андрологи наиболее часто применяют заместительную терапию тестостероном. Данный метод позволяет решить целый ряд задач: снизить симптомы возрастного андрогенодефицита путем повышения либидо, общей сексуальной удовлетворенности, уменьшить выраженность либо полностью ликвидировать вегетососудистые и психические расстройства. Кроме того, если заместительная терапия тестостероном применяется более 1 года, у пациентов наблюдается повышение плотности костной массы, снижение выраженности висцерального ожирения, а также нарастание мышечной массы. Также после длительного курса лечения нормализуются лабораторные параметры: наблюдается повышение уровня гемоглобина или количества эритроцитов, снижение уровня ЛПОНП (липопротеинов очень низкой плотности) и ЛПНП (липопротеинов низкой плотности) при неизмененном уровне ЛПВП (липопротеинов высокой плотности). Многие авторы считают, что такого эффекта можно достичь, добившись восстановления концентрации тестостерона в крови до нормального уровня (10–35 нмоль/л). Следует также учитывать, что *17α-алкилированные препараты тестостерона флуоксиместеролон и метилтестостерон обладают выраженной гепатотоксичностью, оказывая токсическое и канцерогенное влияние на печень, а также отрицательно воздействуют на липидный спектр крови (резкое повышение уровня атерогенных и снижение уровня антиатерогенных липопротеидов). Поэтому применение этих производных тестостерона в клинической практике было прекращено.
В настоящее время из пероральных препаратов предпочтение отдается тестостерону ундеканоату (Андриол). Указанный эфир тестостерона не подвергается первичному печеночному метаболизму, так как всасывается в лимфатическую систему, минуя печень. После гидролиза тестостерона ундеканоата в лимфатической системе в системный кровоток поступает тестостерон, который оказывает лечебное действие как сам по себе, так и через свои основные метаболиты – дигидротестостерон (ДГТ) и эстрадиол, обусловливающие полный спектр андрогенной активности тестостерона. Таким образом, тестостерона ундеканоат сохраняет свою активность при пероральном применении. Вместе с этим, минуя систему воротной вены и прохождение через печень, тестостерона ундеканоат не оказывает гепатотоксического и гепатоканцерогенного действия. Период полувыведения препарата из плазмы составляет 3–4 часа. В связи с этим режимом дозировки тестостерона ундеканоата является 2-кратный прием в течение суток, это не всегда удобно для пациентов. Исходя из собственного опыта, мы считаем, что Андриол является достаточно мягким препаратом и помогает только в случаях начальных и минимальных проявлений возрастного андрогенного дефицита.
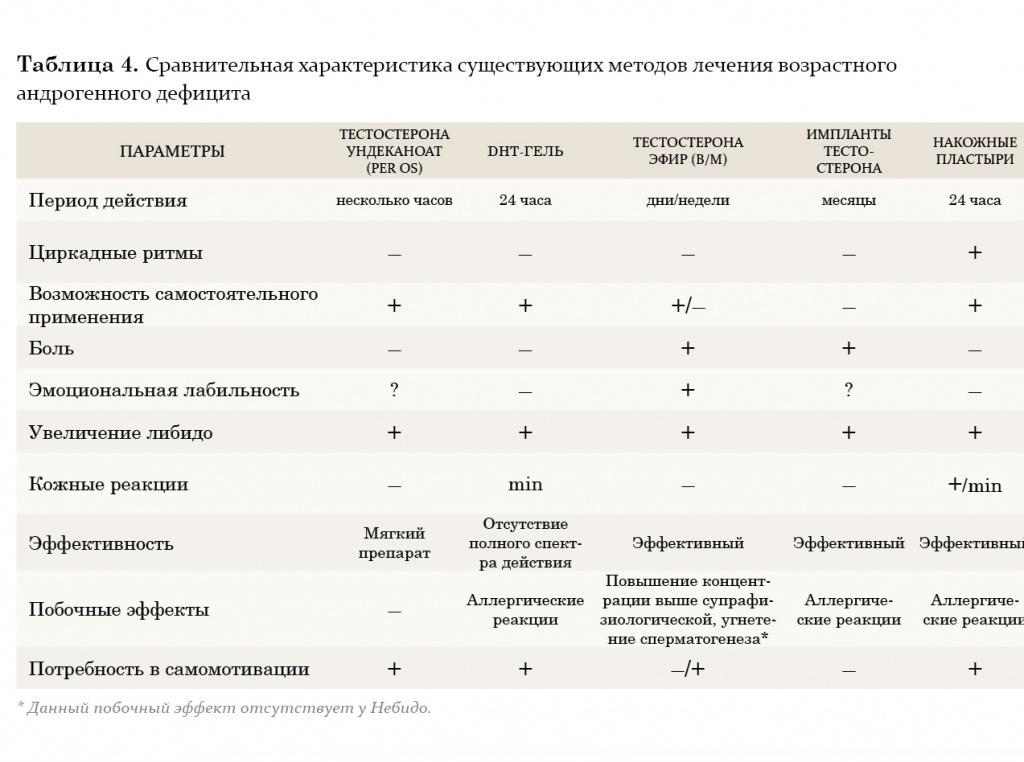
Внутримышечные инъекции пролонгированных эфиров тестостерона также являются широко применяемым методом заместительной терапии у мужчин с гипогонадизмом. Два наиболее известных эфира тестостерона – тестостерона ципионат и тестостерона энантат, имеют похожую фармакокинетику. При внутримышечном введении этих препаратов создается депо, из которого препарат высвобождается в кровеносное русло. В течение первых 2–3 дней после введения уровень тестостерона повышается до супрафизиологических цифр, а затем медленно снижается на протяжении последующих 2 недель до субнормальных значений. Положительной стороной этих препаратов является длительность терапевтического действия. Тем не менее резкие изменения в уровне тестостерона, зачастую ощущаемые самим пациентом в виде подъемов и снижения либидо, общего самочувствия, эмоционального статуса, являются нежелательными качествами данных препаратов. В связи с этим большие надежды возлагаются на новый препарат Небидо (Шеринг), фармакокинетика которого значительно отличается от других эфиров тестостерона. Небидо представляет собой тестостерона ундеканоат и является препаратом, не обладающим пиком повышения концентрации.
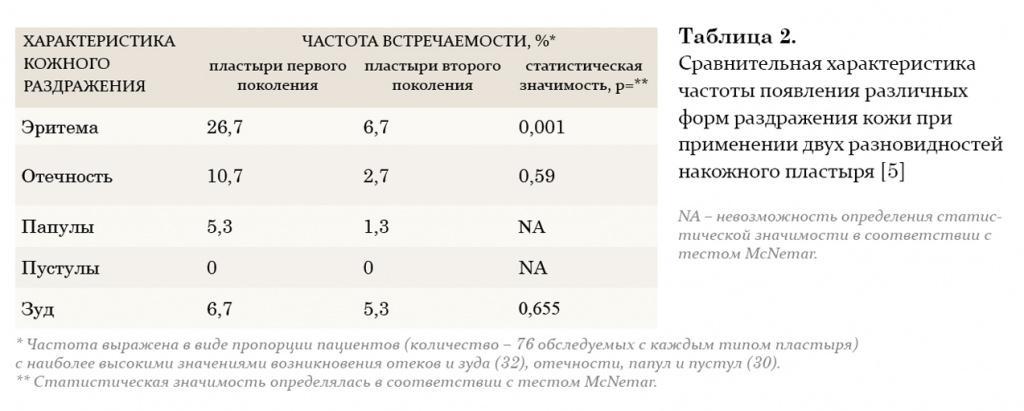
На протяжении двух последних десятилетий большое внимание уделяется исследованию преимуществ трансдермального применения препаратов тестостерона. Мошоночные пластыри обладают эффективным действием, и некоторые пациенты считают их наиболее удобным методом лечения. Накожные пластыри наиболее хорошо воспринимаются пациентами и дают эффективный уровень тестостерона в сыворотке крови. Тем не менее существуют некоторые различия между этими двумя разновидностями пластырей относительно их аллергогенного потенциала: при применении накожных пластырей отмечается гораздо большая частота возникновения аллергических реакций и раздражения кожи, чем при применении мошоночных пластырей.
Гель тестостерона обладает всеми преимуществами пластырей и не вызывает развития кожных реакций. Единственный его недостаток заключается в наличии возможности контакта геля с партнершей и недостаточном количестве долговременных исследований по его применению.
Трансдермальный путь введения тестостерона позволяет избежать его первичного метаболизма в печени и инактивации, как это происходит при применении пероральных андрогенных препаратов, а также позволяет имитировать циркадные ритмы высвобождения физиологического немодифицированного тестостерона и его естественных метаболитов, эстрадиола и ДГТ. К тому же терапию с использованием пластырей и геля в случае необходимости можно легко прервать. К положительным моментам этого метода лечения также относится низкий риск возникновения лекарственной зависимости.
Европейский препарат 5-α-дигидротестостерон-гель (ДГТ) хотя и признан эффективным, однако неизвестно, оказывает ли изолированное применение неароматизированного андрогена, каким является ДГТ, такое же действие, как тестостерон, в связи с тем, что метаболиты тестостерона включают эстрадиол. По мнению многих авторов, применение препарата не рекомендуется, так как ДГТ вследствие невозможности превращения в эстрадиол не обладает полным спектром терапевтических свойств тестостерона (например, влиянием на костную ткань и сердечно-сосудистую систему).
Некоторые из препаратов заместительной терапии, такие как тестостерона ундеканоат, ДГТ-гель и мошоночные пластыри, вызывают существенное увеличение концентрации ДГТ в сыворотке крови. ДГТ известен как главный андроген простаты, и в связи с этим проводилось много дискуссий по поводу способности его вызывать заболевания предстательной железы. Однако, несмотря на эти предположения, в последнее 10-летие не зафиксировано данных в пользу увеличения частоты возникновения патологии простаты при назначении препаратов ДГТ.
Таким образом, существует множество препаратов заместительной андрогенотерапии, однако все они имеют те или иные побочные эффекты, а также обладают угнетающим действием на сперматогенез. В последнее время появляется все больше работ, демонстрирующих вторичный характер возрастного андрогенного дефицита. Согласно материалам ВОЗ, получены данные о сохранении секретирующей функции клетками Лейдига у пожилых мужчин, что позволило ученым предложить принципиально новый подход в лечении возрастного андрогенного дефицита, основанный на стимуляции синтеза эндогенного тестостерона.
Однако не стоит забывать, что наряду с абсолютными противопоказаниями для заместительной терапии андрогенами (рак грудной и предстательной желез) существуют и дополнительные (доброкачественная гиперплазия предстательной железы с выраженной обструкцией, пролактинома, полицитемия). К относительным противопоказаниям относятся нарушения сна в виде апноэ, обструктивные заболевания легких, интенсивное курение.
К побочным эффектам андрогенов относятся усиление ночного апноэ, полицитемия, гинекомастия, приапизм, задержка жидкости, повышение АД, отеки, увеличение размеров простаты, торможение сперматогенеза.
То есть сегодня существуют методы лечения возрастного андрогенного дефицита, которые можно разделить на две группы, принципиально различающиеся по механизму действия:
заместительная терапия экзогенными андрогенными препаратами; терапия, стимулирующая синтез эндогенного тестостерона.
Таким образом, можно сказать, что оптимального для всех средства для лечения возрастного андрогенного дефицита у мужчин не существует. И к выбору препарата следует подходить строго индивидуально, учитывая возраст пациента, индекс массы тела, необходимость сохранения сперматогенеза, показатели гематокрита и сопутствующие заболевания.
Сравнительный фармакоэкономический анализ применения анастрозола, летрозола и экземестана при адъювантной терапии рака молочной железы
Полный текст:
Аннотация
Актуальность. В данной статье отражены результаты анализа эффективности затрат, сравнивающего альтернативные схемы гормональной терапии рака молочной железы (РМЖ) ингибиторами/инактиваторами ароматазы. Цель: сравнительная фармакоэкономическая оценка терапии анастрозолом, летрозолом и экземестаном пациенток с I–II стадиями РМЖ в условиях российской системы здравоохранения. Методология: Марковское моделирование, анализ эффективности затрат. Результаты. При анализе эффективности затрат инициальной адъювантной терапии при РМЖ наиболее экономически эффективным препаратом является летрозол. При анализе эффективности затрат при переключении с продолжением терапии тамоксифеном при РМЖ наиболее экономически эффективным препаратом является экземестан. Вывод. Все три препарата: анастрозол, летрозол и экземестан более чем в 2 раза меньше установленного «порога готовности платить», поэтому могут быть рекомендованы для включения в список ЖНВЛП (кроме анастрозола, который уже присутствует там) и для применения в системе государственного возмещения.
Ключевые слова
##article.ConflictsofInterestDisclosure##:
##article.articleInfo##:
Депонировано (дата): 06.06.2018
##article.reviewInfo##:
##article.editorialComment##:
Для цитирования:
Белоусов Д.Ю., Афанасьева Е.В., Зырянов С.К. Сравнительный фармакоэкономический анализ применения анастрозола, летрозола и экземестана при адъювантной терапии рака молочной железы. Качественная Клиническая Практика. 2012;(2):45-55.
Введение
Рак молочной железы (РМЖ) – занимает первое место среди злокачественных новообразований у женщин и является одной из главных причин смертности женского населения во всём мире. Заболеваемость РМЖ увеличивается с возрастом. Как правило, опухоли возникают после 35-40 лет, пик заболеваемости регистрируют у женщин в возрасте 60-65 лет [14].
В России в структуре заболеваемости злокачественными новообразованиями РМЖ занимает 1-ое место (18,1%). Распространённость РМЖ в 2011 г. на 100 000 населения – 369,5 человек. В 2011 г. выявлено 57 379 больных РМЖ женщин, из них 55 184 поставлено на учёт. Удельный вес больных с диагнозом, подтверждённым морфологически, от числа больных с впервые в жизни установленным диагнозом РМЖ – 96,6%. Удельный вес больных с опухолевым процессом I стадии от числа больных с впервые в жизни установленным диагнозом РМЖ – 18,5%, II стадии – 46,5%, III стадии – 24,8%, IV стадии – 9,1% [19].
Радикальное лечение РМЖ получило 36 469 женщин [19], в том числе:
Пятилетняя выживаемость в 2011 г. составила 57,6%. Индекс накопления контингентов больных с РМЖ – 9,5. Одногодичная летальность с момента установления РМЖ – 8,7% [19].
Как уже было сказано выше, среди женщин с впервые выявленным РМЖ в 65% случаев диагностируют I-II стадии заболевания [19]. Преобладающее большинство этих больных, после завершения хирургического этапа лечения, нуждается в проведении адъювантной лекарственной терапии. Одними из основных критериев выбора метода лекарственной терапии (использование цитостатиков, средств гормонотерапии) служит наличие или отсутствие экспрессии рецепторов эстрогенов, прогестерона и Her2-new в ткани опухоли, а так же состояние менструальной функции у женщины. Перечисленные факторы являются не только прогностическими, но и предсказательными в отношении чувствительности опухолевых клеток к тому или иному виду лечения и, в частности, гормонотерапии.
До настоящего времени ингибиторы/инактиваторы ароматазы третьего поколения служат краеугольным камнем гормонотерапии метастатического рака молочной железы, а сегодня всё шире используются для проведения адъювантной терапии у больных операбельным раком молочной железы в менопаузе. Последнее стало возможным после анализа результатов трёх крупных рандомизированных исследований, показавших, что использование ингибиторов/инактиваторов ароматазы III поколения: анастрозола, летрозола, экземестана в монорежиме или последовательно, после завершения 2-5 лет терапии тамоксифеном увеличивает длительность безрецидивного периода в сравнении с использованием тамоксифена [1, 2, 10-12].
Полученные данные кардинально изменили подходы к адъювантной гормонотерапии больных РМЖ в менопаузе.
Современные принципы адъювантной гормонотерапии больных РМЖ были сформулированы на совещании экспертов, состоявшемся в марте 2007 года в St. Gallen. А именно:
Изменение ранее существовавшей клинической практики проведения адъювантной терапии у больных РМЖ в менопаузе вызвало целый ряд вопросов у клиницистов:
Если обратиться к результатам ранее завершённых клинических исследований, нестероидные ингибиторы ароматазы III поколения (анастрозол и летрозол) и стероидный инактиватор (экземестан) снижают уровень эстрогенов в сыворотке крови более чем на 98%. Поэтому мы предположили, что любой из препаратов равно эффективен в режиме адъювантной терапии при гормоночувствительном РМЖ, любой режим терапии (моно или последовательно) в равной мере снижает абсолютный риск рецидива и риск смерти, и нет различий в побочных эффектах между лекарственными препаратами.
Очевидно, что для окончательного суждения о преимуществах или недостатках того или иного препарата и режиме его назначения, эффективности и безопасности терапии, сходстве и различиях между ингибиторами/инактиваторами ароматазы необходимы дальнейшие исследования. В современных условиях одним из основных критериев выбора схемы лечения, наряду с клинической эффективностью, переносимостью и безопасностью, является анализ эффективности затрат (cost effectiveness analysis / CEA). Любое различие по показателю «затраты-эффективность» (cost effectiveness ratio / CER) может оказаться существенным аргументом в пользу выбора того или иного лекарственного препарата и режима его назначения, поскольку даже при условиях схожей противоопухолевой эффективности ингибиторов/инактиваторов ароматазы, различные режимы терапии могут отличаться между собой по показателю CER.
В настоящее время в Российской Федерации требуется проведение оценки клинической и экономической эффективности медицинских технологий (ОМТ). Это является результатом осознания того, что решения, связанные с распределением ресурсов в стране с бюджетной системой финансирования здравоохранения, должны быть подкреплены информацией о стоимости лечения и об относительной эффективности медицинского вмешательства.
В данной статье отражены результаты анализа эффективности затрат, сравнивающего альтернативные схемы гормональной терапии рака молочной железы ингибиторами/инактиваторами ароматазы.
Цель исследования
Целью данной работы являлась сравнительная фармакоэкономическая оценка терапии анастрозолом, летрозолом и экземестаном пациенток с I-II стадиями РМЖ в условиях российской системы здравоохранения.
Задачи исследования
Популяция больных
Женщины, находящиеся в менопаузе, с I-II стадией рака молочной железы, находящиеся на гормональной адъювантной терапии ингибиторами/инактиваторами ароматазы.
Методология исследования
При проведении фармакоэкономического анализа был использован применяемый в РФ Отраслевой стандарт «Клинико-экономического исследования» [17]. Были использованы следующие методы экономического анализа:
Марковское моделирование. Для прогнозирования вероятности развития событий при лечении РМЖ и ассоциированных с ними прямых медицинских затрат за определённый период времени при использовании различных терапевтических стратегий была разработана Марковская модель, которая выбрана из-за длительного течения РМЖ. Её структура позволяет следующее:
Модель представлена на рис. 1 и табл. 1, продолжительность цикла модели 1 год (всего 5 циклов), включает следующие состояния [5]:
Рис. 1
Марковская модель прогрессирования рака молочной железы
Таблица 1
Матрикс Марковской модели рака молочной железы с переходом из одного состояния в другое
Для проведения клинико-экономического анализа разработан алгоритм принятия возможных решений при развитии рецидива заболевания (рис. 2).
Рис. 2
Алгоритм принятия возможных решений при развитии рецидива РМЖ («древо» решений)
Стоимость прямых медицинских затрат. По Стандарту оказания медицинской помощи больным со злокачественными новообразованиями молочной железы [20] были рассчитаны прямые медицинские затраты на использование медицинских ресурсов при оказании медицинской помощи больным РМЖ на:
Прямые медицинские затраты. Для расчётов ценовых показателей стоимости медицинских услуг мы использовали Прейскурант на оказание медицинских услуг клиник ПМГМУ им. И.М. Сеченова [18], ФГБУ «Российский научный центр рентгенорадиологии» за 2012 г. г. Москва [24]; цены на препараты сравнения были рассчитаны как средние розничные в аптеках г. Москвы [13].
Показатель эффективности затрат. Так как у сравниваемых стратегий разные показатели эффективности и затрат был проведён анализ показателя эффективности затрат (cost—effectiveness ratio – CER). Наиболее фармакоэкономически приемлемым считался наименьший показатель CER, который рассчитывался по следующей формуле:
CER = DC ÷ Ef, где
DC – прямые медицинские затраты (равно CoI – стоимости болезни);
Ef – эффективность (действенность), выраженная в показателях безрецидивной выживаемости (DFS – disease—free survival).
Вероятность перехода в состояние и эффективность препаратов. Вероятность перехода из одного состояния здоровья в другое и эффективность сравниваемых препаратов оценивалась по результатам контролируемых клинических исследований: ATAC [10, 11], ARNO 95 [6], BIG 1-98 [1, 2, 12], IES [3], на которых и обосновывался данный модельный фармакоэкономический анализ.
Вероятность перехода из одного состояния в другое
Исследование ATAC – оценка эффективности терапии анастрозолом по сравнению с тамоксифеном в качестве инициальной адъювантной терапии I-II стадии РМЖ (табл. 3) [10, 11].
Таблица 3
Вероятность перехода в исследовании ATAC из одного состояния в другое [10, 11]


