Простакор : инструкция по применению
Состав
Описание
Лиофилизированный порошок или пористая масса, уплотненная в таблетку белого или белого с желтоватым оттенком цвета.
Фармакотерапевтическая группа
Средство лечения хронического простатита.
Способствует уменьшению отека, лейкоцитарной инфильтрации и тромбоза венул предстательной железы, нормализует секреторную функцию эпителиальных клеток, увеличивает количество лецитиновых зерен в секрете ацинусов, стимулирует мышечный тонус мочевого пузыря.
Уменьшает тромбообразование, обладает антиагрегатной активностью.
Показания к применению
Хронический простатит, осложнения после операций на предстательной железе.
Противопоказания
Способ применения и дозировка
Внутримышечно по 5-10 мг один раз в сутки в течении 5-10 дней.
Перед введением препарат растворяют в 1 мл 0,25-0,5 % раствора новокаина, раствора натрия хлорида 0,9 % или воды для инъекций.
При необходимости проводят повторный курс (через 1-6 месяцев).
Побочное действие
Форма выпуска
Условия хранения
В сухом, защищенном месте от света и недоступном для детей месте при температуре от 2 до 10 °С.
Срок годности
3 года.
Не применять по истечении срока годности, указанного на упаковке.
Условия отпуска из аптек
Производитель/организация, принимающая претензии
ФГУП «НПО «Микроген», Россия
115088, г. Москва, ул. 1-ая Дубровская, д. 15,
450014, г. Уфа, ул. Новороссийская, д. 105
Простакор
Заказать Простакор в аптеках Москвы.
Инструкции:
Простакор, Раствор для внутримышечного введения
Торговое название
Латинское название
Регистрационный номер
Фармакологическая группа
Средство для лечения хронического простатита.
G04BX Прочие препараты для лечения урологических заболеваний
Лекарственная форма
Раствор для внутримышечного введения.
Описание
Прозрачный раствор светло-желтого цвета со слабым специфическим запахом.
Состав
Форма выпуска и упаковка
Раствор для внутримышечного введения, 5 мг/мл.
В ампулах по 1 мл.
10 ампул вместе с инструкцией по применению и скарификатором ампульным в коробке из картона.
5 ампул в контурной ячейковой упаковке. 2 контурные ячейковые упаковки вместе с инструкцией по применению и скарификатором ампульным в пачке из картона.
При упаковке ампул, имеющих кольцо излома или точку для вскрытия, скарификатор ампульный не вкладывают.
Условия хранения
Хранить в сухом, защищенном от света, недоступном для детей месте, при температуре от 4 до 8 °С.
Срок годности
2 года. Не применять после истечения срока годности, указанного на упаковке.
Условия отпуска
Владелец РУ
МИКРОГЕН ФГУП научно-производственное объединение, Россия
Производитель
МИКРОГЕН, ФГУП НПО, Россия
Представительство
МИКРОГЕН ФГУП научно-производственное объединение, Россия
Фармакологические свойства
Показания
Показания для применения препарата Простакор:
— хронический простатит;
— осложнения после операций на предстательной железе.
Противопоказания
— гиперчувствительность к компонентам препарата Простакор;
— детям и подросткам до 18 лет.
С осторожностью
Относительные противопоказания для препарата Простакор не описаны.
Способ применения и дозы
Передозировка
Случаи передозировки препарата Простакор не описаны.
Побочное действие
Особые указания и меры предосторожности
Мальтоза, содержащаяся в препарате Простакор, может оказывать влияние на показатели содержания глюкозы в крови и моче при лабораторном определении.
Взаимодействие
Клинически значимых последствий взаимодействия препарата Простакор с другими лекарственными средствами не выявлено.
Простакор ® (Prostacor)
Владелец регистрационного удостоверения:
Лекарственная форма
Форма выпуска, упаковка и состав препарата Простакор ®
Лиофилизат для приготовления раствора для в/м введения в виде порошка или пористой массы белого или белого с желтоватым оттенком цвета.
| 1 амп. | |
| экстракт простаты животных* | 5 мг |
* препарат полипептидной природы, получаемый путем экстракции из предстательной железы крупного рогатого скота.
Вспомогательные вещества: глицин.
Фармакологическое действие
Лекарственное средство животного происхождения. Обладает органотропным действием на предстательную железу. Уменьшает степень отека, лейкоцитарной инфильтрации предстательной железы, нормализует секреторную функцию эпителиальных клеток, увеличивает число лецитиновых зерен в секрете ацинусов, стимулирует мышечный тонус мочевого пузыря. Уменьшает тромбообразование, обладает антиагрегантной активностью, препятствует развитию тромбоза венул в предстательной железе. Нормализует параметры предстательной железы и эякулята.
Фармакокинетика
Как пептидное вещество, расщепляется клеточными протеазами до аминокислот. Не обладает кумулятивным действием.
Показания активных веществ препарата Простакор ®
Хронический простатит; доброкачественная гиперплазия предстательной железы; состояния до и после оперативных вмешательств на предстательной железе.
Режим дозирования
Предназначен для применения у взрослых мужчин.
Внутрь, в/м, ректально. Доза и схема применения зависят от показаний и используемой лекарственной формы.
Побочное действие
Противопоказания к применению
Повышенная чувствительность к активному веществу; возраст до 18 лет.
Применение при беременности и кормлении грудью
Применение у детей
Противопоказано применение в возрасте до 18 лет.
Особые указания
До начала лечения хронического простатита и, при необходимости, в процессе лечения рекомендуется проводить анализ секрета предстательной железы.
В период применения препарата для лечения доброкачественной гиперплазии предстательной железы следует регулярно проводить стандартный контроль данного заболевания. Перед началом лечения необходимо убедиться, что патология носит доброкачественный характер.
Лекарственное взаимодействие
Совместим с антибактериальными препаратами, применяемыми для лечения простатита.
Простакор р-р д/ин. 5мг/мл 1мл n10
Доставим в одну из 2397 аптек вашего региона
Доставим в течение 1-2 дней, бесплатно
Оплата в аптеке при получении товара
Инструкция по применению Простакор р-р д/ин. 5мг/мл 1мл n10
Состав
Фармакологическое действие
Способствует уменьшению отека, лейкоцитарной инфильтрации и тромбоза венул предстательной железы, нормализует секреторную функцию эпителиальных клеток, увеличивает количество лецитиновых зерен в секрете ацинусов, стимулирует мышечный тонус мочевого пузыря.
Уменьшает тромбообразование, обладает антиагрегантной активностью.
Показания
хронический простатит;
осложнения после операций на предстательной железе.
Способ применения и дозировка
Внутримышечно по 5-10 мг один раз в сутки в течение 5-10 дней.
При необходимости проводят повторный курс (через 1-6 месяцев).
Побочные действия
Противопоказания
гиперчувствительность;
детям и подросткам до 18 лет.
С осторожностью: относительные противопоказания не описаны.
Передозировка
Случаи передозировки препарата Простакор не описаны.
Особые указания
Мальтоза, содержащаяся в препарате Простакор, может оказывать влияние на показатели содержания глюкозы в крови и моче при лабораторном определении.
Взаимодействие с другими препаратами
Клинически значимых последствий взаимодействия препарата Простакор с другими лекарственными средствами не выявлено.
Современные возможности медикаментозного лечения доброкачественной гиперплазии ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ
К числу наиболее распространенных урологических заболеваний у пациентов пожилого возраста относится доброкачественная гиперплазия предстательной железы (ДГПЖ) [2].
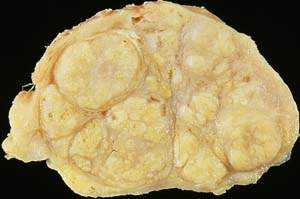 |
| Рисунок 1. Доброкачественная гиперплазия предстательной железы (макропрепарат) |
К числу наиболее распространенных урологических заболеваний у пациентов пожилого возраста относится доброкачественная гиперплазия предстательной железы (ДГПЖ) [2]. Около 80% мужчин старше 80 лет страдают этим заболеванием. Другая статистика свидетельствует, что из всех заболеваний, которым подвержены мужчины старше 50 лет, на долю доброкачественной гиперплазии простаты приходится 36% [1]. Эти сведения настолько общеизвестны, что ухудшение качества мочеиспускания часто рассматривается как естественное явление.
Клинически данное заболевание проявляется различными симптомами, связанными с нарушением пассажа мочи по нижним мочевым путям. При значительно выраженной инфравезикальной обструкции, как правило, прибегают к хирургическому вмешательству. Оперативное лечение по поводу ДГПЖ показано 30% больных в возрасте от 50 до 80 лет [4]. Однако в последние годы все большую популярность завоевывает медикаментозная терапия доброкачественной гиперплазии предстательной железы. Это, с одной стороны, объясняется вполне логичным желанием врача и пациента по возможности избежать операции, с другой — развитием представлений о патогенезе расстройств мочеиспускания при доброкачественной гиперплазии предстательной железы.
До недавнего времени патогенез расстройств мочеиспускания при доброкачественной гиперплазии предстательной железы рассматривали с позиции классических представлений о механической инфравезикальной обструкции и развитии вторичных структурно-функциональных изменений детрузора (компенсация, декомпенсация). За последние два десятилетия получены принципиально новые данные о природе повышенного внутриуретрального сопротивления. Его перестали отождествлять исключительно с механическим сдавлением шейки мочевого пузыря и задней уретры. Обнаружен динамический компонент обструкции, который состоит в повышении тонуса указанных анатомических структур за счет активности a-адренорецепторов. Появились также иные трактовки происхождения ирритативных симптомов. Их считают проявлением первичного нестабильного мочевого пузыря и не связывают напрямую с обструкцией [5].
Результаты нашей работы свидетельствуют, что при ДГПЖ клиническая симптоматика развивается вследствие недостаточности энергетического метаболизма и гипоксии детрузора в условиях повышенного уретрального сопротивления [3]. Об этом свидетельствуют:
Причины нарушений энергетического метаболизма и функций детрузора крайне многообразны. В частности, к таким нарушениям могут привести повышение активности симпатической нервной системы, расстройства органного кровообращения, авитаминоз (группа В), хронические заболевания дыхательной и сердечно-сосудистой систем, влияние приема ряда фармакологических препаратов, угнетающих дыхательную цепь, и, естественно, обструктивные нарушения уродинамики и т. д. Весьма важно, что нарушения гипоксического характера в гладкомышечной ткани могут иметь и первичный митохондриальный генез (первичные нарушения энергетического метаболизма детрузора [3].
Необходимо отметить, что у больных ДГПЖ в нижнем отделе мочевого тракта протекают два параллельных процесса — формирование уретральной обструкции и нарушение энергетического метаболизма детрузора (митохондриальная недостаточность).
Подобное представление патогенеза расстройств мочеиспускания открывает широкие возможности для фармакотерапии. Сокращения и расслабления детрузора можно достичь с помощью средств метаболической терапии, прямого улучшения снабжения детрузора кислородом и т. д. Наиболее значимые расстройства основных функций мочевого пузыря все же опосредованы расстройствами кровообращения. И если процесс обратим, то до или после хирургического вмешательства можно существенно влиять на функциональное состояние мочевого пузыря с помощью вазоактивных препаратов, к которым в первую очередь относятся a1-адреноблокаторы.
При определении критериев отбора пациентов для медикаментозной терапии ДГПЖ мы воспользовались рекомендациями IV Международного консультативного комитета по ДГПЖ.
Основу настоящего исследования составили собственные клинические наблюдения за 1724 пациентами (средний возраст 61,4 года), страдающими ДГПЖ и получавшими различные варианты медикаментозного лечения. Нами применялись препараты всех групп, использующихся в настоящее время для лечения ДГПЖ: a-адреноблокаторы, блокаторы 5-a-редуктазы, препараты растительного происхождения и их комбинации. Схемы проведенного лечения и характеристика групп пациентов приведены в табл. 1.
Из наиболее многочисленной и популярной сегодня группы препаратов для медикаментозного лечения ДГПЖ — селективных a-адреноблокаторов мы использовали альфузозин, теразозин, доксазозин и тамсулозин. Общее число пациентов, получавших a-адреноблокаторы, составило 1408. Финастерид был взят нами как классический представитель блокаторов 5-a-редуктазы. Из препаратов растительного происхождения мы использовали пермиксон и таденан.
В пяти группах общей численностью 1305 человек проводилась терапия селективными a-адреноблокаторами в течение длительного периода времени по стандартным схемам и в стандартных дозах. Результаты лечения приведены в табл. 2.
Улучшение качества мочеиспускания отметили в среднем 86,74% пациентов. Суммарный балл I-PSS сократился на 38,68% к окончанию первого года лечения и на 43,4% к окончанию курса терапии. Балл QOL уменьшился на 29,04% и 35,58% соответственно. Максимальная скорость потока мочи увеличилась на 45,25% к окончанию первого года лечения и стабилизировалась на достигнутом уровне. Количество остаточной мочи сократилось в среднем на 57,6%. Процент пациентов, по тем или иным причинам выбывших из исследования, был тождествен во всех группах и равнялся 14,38%.
Особо следует остановиться на препарате тамсулозин (омник, Yamanouchi) — пока единственном простатселективном a1А-адреноблокаторе на отечественном рынке. Этот препарат обладает рядом свойств, которые позволяют его использовать в различных функциональных тестах. Прежде всего это возможность назначения единой терапевтической дозы (один раз в сутки по 0,4 мг). А отсутствие выраженного влияния на артериальное давление и сердечную деятельность избавляет от необходимости титрования дозы. Мы согласны с рядом авторов, которые считают возможным применение коротких курсов терапии тамсулозином в качестве прогностических тестов эффективности лечения a1-адреноблокаторами, что может иметь решающее значение при выборе того или иного метода медикаментозного лечения ДГПЖ [4].
Части больных (группа А5) проведена проверка возможности разрешения острой задержки мочеиспускания (ОЗМ) приемом альфузозина по 5 мг два раза в сутки. Эта терапия проводилась пациентам с впервые возникшей ОЗМ и отсутствием симптомов нарушения мочеиспускания в анамнезе. Положительный эффект был достигнут у 8 из 14 пациентов (57,1%), которым параллельно приему альфузозина производилось кратковременное (трое суток) дренирование мочевого пузыря катетером. Единовременный прием суточной дозы альфузозина (10 мг) способствовал восстановлению самостоятельного мочеиспускания лишь у одного из четырех пациентов, которым проводилась подобная терапия. Вероятно, это объясняется гипотонией детрузора, усугубляющейся в ситуации длительного перерастяжения мочевого пузыря на фоне задержки мочеиспускания.
Для изучения эффективности и безопасности комбинированной медикаментозной терапии ДГПЖ препаратами разных групп, а также для уточнения целесообразности проведения терапии нами были созданы три группы.
В первой группе (К1) пациенты получали проскар по 5 мг/сут. параллельно с приемом теразозина по 5-10 мг/сут. Обращало на себя внимание значительное повышение показателей максимальной скорости потока мочи (+40%), характерное для группы монотерапии a-адреноблокаторами, и постепенное, на протяжении курса лечения, снижение объема предстательной железы (-20,4%), характерное для группы монотерапии финастеридом. Очевидно, что положительные изменения показателей мочеиспускания в этой группе являются следствием воздействия обоих препаратов. Тем не менее процент выбывших пациентов в этой группе был крайне высоким — 32,3%. Основной причиной прекращения комбинированной терапии ДГПЖ пациенты называли неприемлемо высокую стоимость лечения.
В третьей группе комбинированной терапии (К3) лечение проводилось финастеридом по 5 мг/сут. в сочетании с пермиксоном по 160 мг два раза в сутки. Через два года после начала лечения 50% пациентов покинули группу, приводя причиной отказа от дальнейшей терапии высокую стоимость лечения при отсутствии быстрого улучшения качества мочеиспускания. При сравнении полученных данных с результатами в других группах очевидно, что эффективность лечения в третьей существенно ниже.
Таким образом, эффективность медикаментозной терапии больных ДГПЖ при соблюдении показаний и противопоказаний к ее назначению, правильном выборе препарата и схемы его назначения высока и достигает в среднем 80,2%. При этом эффективность монотерапии a-адреноблокаторами составляет 86,7%, блокаторами 5a-редуктазы — 69,4%, препаратами растительного происхождения — 69,3% и при комбинированной терапии — 95,45%. Комбинированная медикаментозная терапия a-адреноблокаторами в сочетании с блокаторами 5a-редуктазы эффективнее монотерапии этими препаратами. С целью снижения стоимости лечения возможен переход на монотерапию блокаторами 5a-редуктазы после достижения выраженного регресса обструктивной симптоматики. Медикаментозная терапия a-адреноблокаторами является эффективным способом консервативного лечения острой задержки мочеиспускания. Терапия должна проводиться на фоне кратковременного (трое суток) дренирования мочевого пузыря уретральным катетером.
Литература
1. Гориловский Л. М. Эпидемиология и факторы риска развития доброкачественной гиперплазии предстательной железы. В кн.: Доброкачественная гиперплазия предстательной железы / Под ред. Н. А. Лопаткина. М., 1997, с. 10-18.
2. Лопаткин Н. А., Перепанова Т. С. Клинический опыт лечения больных доброкачественной гиперплазией предстательной железы a1-адреноблокатором альфузозином // Урол. и нефрол., 1997, № 5, с. 14-17.
3. Лоран О. Б., Вишневский Е. Л., Вишневский А. Е. Лечение расстройств мочеиспускания у больных доброкачественной гиперплазией простаты a-адреноблокаторами. Монография. М., 1998.
4. Сивков А. В. Медикаментозная терапия доброкачественной гиперплазии предстательной железы. В кн.: Доброкачественная гиперплазия предстательной железы / Под ред. Н. А. Лопаткина. М., 1997, с. 67-83.
5. McConnell J. D. Prostatic growth: new insights into hormonal regulation // Br. J. Urol. 1995. Vol.76.(suppl.1). P. 5-10.

