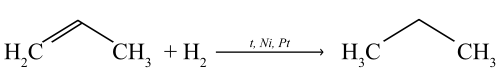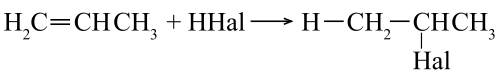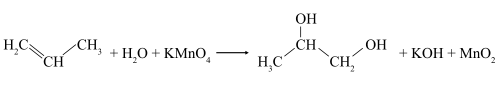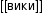Пропилен
| Пропилен | |
 | |
 | |
| Общие | |
|---|---|
| Химическая формула | C3H6 |
| Физические свойства | |
| Молярная масса | 42.08 г/моль |
| Плотность | 0.695@-47 °C г/см³ |
| Термические свойства | |
| Температура плавления | − 185.2 °C |
| Температура кипения | − 47.6 °C |
| Классификация | |
| Рег. номер CAS | 115-07-1 |
| SMILES | C=CC |
Содержание
Физические свойства
Химические свойства
Обладает значительной реакционной способностью. Его химические свойства определяются двойной углерод-углеродной связью. p-связь, как наименее прочная и более доступная, при действии реагента разрывается, а освободившиеся валентности углеродных атомов затрачиваются на присоединение атомов, из которых состоит молекула реагента. Все реакции присоединения протекают по двойной связи и состоят в расщеплении π-связи алкена и образовании на месте разрыва двух новых σ-связей.
Чаще реакции присоединения идут по гетеролитическому типу, являясь реакциями электрофильного присоединения.
Присоединение галогенов (галогенирование)
Реакцию галогенирования обычно проводят в растворителе при обычной температуре. Галогены легко присоединяются по месту разрыва двойной связи с образованием дигалогенопроизводных. Легче идет присоединение хлора и брома, труднее — йода. Фтор взаимодействует со взрывом.
Присоединение водорода (реакция гидрирования)
Присоединяя водород в присутствии катализаторов (Pt, Pd, Ni), пропен переходит в предельный углеводород — пропан.
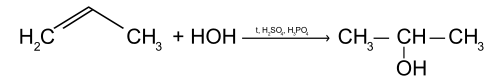
Присоединение воды (реакция гидратации)
Пропилен реагирует с водой с образованием одноатомного спирта изопропанола, при этом двойная связь раскрывается.
Присоединение галогеноводородов (HHal)
Происходит по правилу Марковникова. Водород кислоты HHal присоединяется к наиболее гидрированному атому углерода при двойной связи. Соответственно остаток Hal связывается с атомом углерода, при котором находится меньшее число атомов водорода.
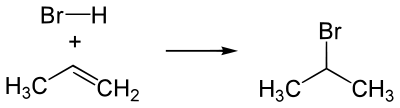
Пример гидрогалогенирования — получение бромпроизводного пропана при реакции бромоводорода и пропилена.
Горение на воздухе
При поджигании горит на воздухе: 2СН2=СНСН3 + 9О2 → 6СО2 + 6Н2О.
С кислородом воздуха газообразный пропилен образует взрывчатые смеси.
В слабощелочной или нейтральной водной среде пропилен окисляется перманганатом калия, что сопровождается обесцвечиванием раствора KMnO4 и образованием гликолей (соединений с двумя гидроксильными группами при соседних атомах углерода). Эта реакция получила название реакции Вагнера.
Полимеризация
Условия реакции: нагревание, присутствие катализаторов. Соединение молекул происходит путем расщепления внутримолекулярных π-cвязей и образования новых межмолекулярных σ-cвязей.
Окисление кислородом воздуха в пропиленоксид
При нагревании в присутствии серебряных катализаторов:
Получение
В лаборатории
1. Отщепление галогеноводорода от галогеналкилов при действии на них спиртового раствора щелочи:
2. Гидрирование пропина в присутствии катализатора (Pd):
3. Дегидратация изопропилового спирта (отщепление воды). В качестве катализатора используют кислоты (серную или фосфорную) или Аl2O3:
4. Отщепление двух атомов галогена от дигалогеноалканов, содержащих галогены при соседних атомах С. Реакция протекает под действием металлов (Zn и др.):
В промышленности
Обычно пропилен выделяют из газов нефтепереработки (при крекинге сырой нефти в кипящем слое (процесс фирмы BASF), пиролизе бензиновых фракций) или попутных газов, а также из газов коксования угля. Существует несколько видов пиролиза пропилена: пиролиз в трубчатых печах, пиролиз в реакторе с кварцевым теплоносителем (процесс фирмы Phillips Petroleum Co.), пиролиз в реакторе с коксовым теплоносителем (процесс фирмы Farbewerke Hoechst), пиролиз в реакторе с песком в качестве теплоносителя (процесс фирмы Lurgi), пиролиз в трубчатой печи (процесс фирмы Kellogg), процесс Лавровского — Бродского, автотермический пиролиз по Бартоломе. В промышленности пропилен получают также дегидрированием алканов в присутствии катализатора (Сr2О3, Аl2О3).
Промышленным способом получения пропилена наряду с крекингом служит дегидратация пропанола над оксидом алюминия:
Применение
Для производства оксида пропилена, получения изопропилового спирта и ацетона, для синтеза альдегидов, для получения акриловой кислоты и акрилонитрила, полипропилена, пластмасс, каучуков, моющих средств, компонентов моторных топлив, растворителей.
Производство
Большая часть производственных мощностей по пропилену сосредоточена в Европе, Северной Америке и Азии. В настоящее время за год в мире производится более 50 миллионов тонн пропилена полимерного и химического сортов (PG/CG). Большая часть выпуска пропилена этих сортов приходится на долю установок пиролиза, где пропилен — побочный продукт производства этилена. Установками термического крекинга вырабатывается более 60 % такого пропилена. Нефтеперерабатывающими FCC-предприятиями выпускается 34 %. При дегидрогенизации или метатезисе пропана производится 3 % пропилена (в данном случае пропилен является целевым продуктом).
Пропилен нефтехимической чистоты (RG) производится на нефтеперерабатывающих предприятиях мира в количестве, равном 31,2 миллионам тонн. Большая часть такого пропилена вырабатывается на FCC-предприятиях, где пропилен — побочный продукт производства бензина и дистиллятов. Половина этих пропиленовых мощностей интегрирована с нефтехимическими предприятиями, на которых происходит алкилирование пропилена или смешивание LPG и пропана.
Источники
Примечания
Ссылки
Полезное
Смотреть что такое «Пропилен» в других словарях:
ПРОПИЛЕН — Газообразное углеводородное тело, входящее в состав светильного газа. Словарь иностранных слов, вошедших в состав русского языка. Чудинов А.Н., 1910. ПРОПИЛЕН бесцветный газ углеводородного состава., находящейся в светильном газе; под сильным… … Словарь иностранных слов русского языка
Пропилен — – вещество, представляющее собой бесцветный горючий газ со слабым запахом. Химическая формула СH2=СН–CH3. Пропилен является одним из важнейших видов промышленного химического сырья. Содержится в газах крекинга нефтепродуктов. Широко… … Нефтегазовая микроэнциклопедия
ПРОПИЛЕН — (пропен), бесцветный алифатический УГЛЕВОДОРОД, СН2СН:СН2, получаемый термическим КРЕКИНГОМ ЭТИЛЕНА. Используется в производстве широкого ряда химических веществ, включая виниловую и акриловую смолы. Свойства: температура кипения 48 °С;… … Научно-технический энциклопедический словарь
пропилен — сущ., кол во синонимов: 3 • олефин (5) • пропен (1) • углеводород (77) Словарь синонимов ASIS … Словарь синонимов
ПРОПИЛЕН — (пропен CH2 = CHCH3) непредельный (ненасыщенный) углеводород ряда этилена; бесцветный горючий газ со слабым запахом. Получают пиролизом нефтепродуктов и дегидрогенизацией пропана. Является важным сырьем химической промышленности … Российская энциклопедия по охране труда
пропилен — (C3Н6) [http://slovarionline.ru/anglo russkiy slovar neftegazovoy promyishlennosti/] Тематики нефтегазовая промышленность EN propylene … Справочник технического переводчика
ПРОПИЛЕН — (пропей), (СH2=CH СH3) ненасыщенный углеводород ряда этилена, горючий газ без цвета, но со слабым запахом; обладает высокой реакционной способностью. П. содержится в газах, образующихся при (см.) нефти; широко применяется для производства… … Большая политехническая энциклопедия
пропилен — а; м. Органическое соединение газ, выделяемый из попутных газов нефтедобычи и нефтепереработки (используется в производстве моторных масел). ◁ Пропиленовый, ая, ое. П ая смесь. * * * пропилен (пропен), СН3СН=СН2, бесцветный газ, tкип 47,7°C.… … Энциклопедический словарь
пропилен — propenas statusas T sritis chemija formulė CH₂=CHCH₃ atitikmenys: angl. propene; propylene rus. пропен; пропилен ryšiai: sinonimas – propilenas … Chemijos terminų aiškinamasis žodynas
Пропилен (пропен), получение, свойства, химические реакции
Пропилен (пропен), получение, свойства, химические реакции.
Пропилен (пропен), C3H6 – органическое вещество класса алкенов. Пропилен имеет двойную углерод-углеродную связь и поэтому относится к ненасыщенным или непредельным углеводородам.
Пропилен (пропен), формула, газ, характеристики:
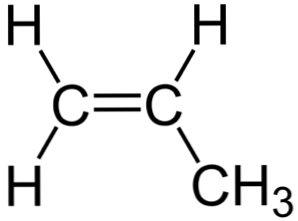
Химическая формула пропилена C3H6, рациональная формула H2CCHCH3, структурная формула CH2=CH-CH3. Изомеров не имеет.
Пропилен – бесцветный газ, без вкуса, со слабым запахом.
Пожаро- и взрывоопасен.
Пропилен по токсикологической характеристике относится к веществам 4-го класса опасности (малоопасным веществам) по ГОСТ 12.1.007, но оказывает вредное воздействие на человека более сильным, чем этилен (этен).
Физические свойства пропилена (пропена):
| Наименование параметра: | Значение: |
| Цвет | без цвета |
| Запах | со слабым запахом |
| Вкус | без вкуса |
| Агрегатное состояние (при 20 °C и атмосферном давлении 1 атм.) | газ |
| Плотность (при 20 °C и атмосферном давлении 1 атм.), кг/м 3 | 1,184 |
| Плотность (при 0 °C и атмосферном давлении 1 атм.), кг/м 3 | 1,9149 |
| Температура плавления, °C | -185,25 |
| Температура кипения, °C | -47,6 |
| Температура вспышки, °C | 107,8 |
| Температура самовоспламенения, °C | 410 |
| Критическая температура*, °C | 91,4 |
| Критическое давление, МПа | 4,6 |
| Взрывоопасные концентрации смеси газа с воздухом, % объёмных | от 2,3 до 11,1 |
| Удельная теплота сгорания, МДж/кг | 45,694 |
| Молярная масса, г/моль | 42,08 |
* при температуре выше критической температуры газ невозможно сконденсировать ни при каком давлении.
Химические свойства пропилена (пропена):
Пропилен — химически активное вещество. Так как в молекуле между атомами углерода имеется двойная связь, то одна из них, менее прочная, легко разрывается, и по месту разрыва связи происходит присоединение, замещение, окисление, полимеризация молекул.
Химические свойства пропилена аналогичны свойствам других представителей ряда алкенов. Поэтому для него характерны следующие химические реакции:
В результате данной химической реакции образуется пропан.
Водород кислоты HBr присоединяется к наиболее гидрированному атому углерода при двойной связи. Соответственно остаток Br связывается с атомом углерода, при котором находится меньшее число атомов водорода.
Реакция происходит в присутствии минеральных кислот (серной, фосфорной). В результате данной химической реакции образуется изопропанол (изопропиловый спирт).
В результате горения пропилена происходит разрыв всех связей в молекуле, а продуктами реакции являются углекислый газ и вода.
В результате образуется полипропилен.
Получение пропилена (пропена). Химические реакции – уравнения получения пропилена (пропена):
Пропилен получают как в лабораторных условиях, так и в промышленных масштабах.
Обычно пропилен получают при пиролизе углеводородного сырья и каталитическом крекинге нефтяных фракций.
В промышленных масштабах пропилен получают, например, в результате следующей химической реакции:
Пропилен в лабораторных условиях получается в результате следующих химических реакций:
Применение и использование пропилена (пропена):
– как сырье в химической промышленности для органического синтеза различных органических соединений: оксида пропилена, изопропилового спирта, ацетона, альдегидов, акриловой кислоты, акрилонитрила, полипропилена,
Примечание: © Фото //www.pexels.com, //pixabay.com

как получить пропилен реакция ацетилен пропен 1 2 вещество пропилен кислород водород связь является углекислый газ бромная вода
уравнение реакции масса объем полное сгорание моль молекула смесь превращение горение получение пропилена
напишите уравнение реакций пропилен
Мировая экономика
Справочники
Востребованные технологии
Поиск технологий
О чём данный сайт?
Настоящий сайт посвящен авторским научным разработкам в области экономики и научной идее осуществления Второй индустриализации России.
Он включает в себя:
– экономику Второй индустриализации России,
– теорию, методологию и инструментарий инновационного развития – осуществления Второй индустриализации России,
– организационный механизм осуществления Второй индустриализации России,
– справочник прорывных технологий.
Мы не продаем товары, технологии и пр. производителей и изобретателей! Необходимо обращаться к ним напрямую!
Мы проводим переговоры с производителями и изобретателями отечественных прорывных технологий и даем рекомендации по их использованию.
О Второй индустриализации
Осуществление Второй индустриализации России базируется на качественно новой научной основе (теории, методологии и инструментарии), разработанной авторами сайта.
Конечным результатом Второй индустриализации России является повышение благосостояния каждого члена общества: рядового человека, предприятия и государства.
Вторая индустриализация России есть совокупность научно-технических и иных инновационных идей, проектов и разработок, имеющих возможность быть широко реализованными в практике хозяйственной деятельности в короткие сроки (3-5 лет), которые обеспечат качественно новое прогрессивное развитие общества в предстоящие 50-75 лет.
Та из стран, которая первой осуществит этот комплексный прорыв – Россия, станет лидером в мировом сообществе и останется недосягаемой для других стран на века.
Химическая структура, свойства и применение пропилена
пропилен или пропен при комнатной температуре и при атмосферном давлении находится в газообразном состоянии и, как и другие алкены, бесцветен. Он имеет запах, похожий на масло, но менее интенсивный. Он имеет дипольный момент, поскольку, хотя ему не хватает сильной полярной связи, его молекула асимметрична.
Также пропилен является структурным изомером циклопропана (они имеют одинаковую химическую формулу C)3H6). Это происходит в природе как следствие процессов вегетации и брожения. Искусственно встречается при переработке ископаемых видов топлива, таких как нефть, природный газ и, в меньшей степени, углерод.
Аналогичным образом, этилен и пропилен являются продуктами переработки нефти в процессе расщепления больших углеводородных молекул с образованием небольших углеводородов, пользующихся высоким спросом..
Пропилен также может быть получен с использованием различных методологий:
— Реагирует обратимо на этилен и бутен, где двойные связи разрываются и переформулируются для получения пропилена.
— Через процесс дегидрирования (потери водорода) пропана.
— В рамках программы по производству олефинов из метанола (МТО), пропилен был произведен из метанола. Это было пропущено через цеолитный катализатор, который способствует его дегидратации и приводит к образованию этилена и пропилена..
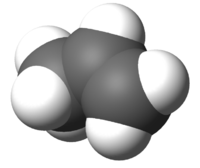
Химическая структура
На изображении выше видна химическая структура пропилена, в которой выделяется его асимметрия (правая сторона отличается от левой). Его углеродный скелет, не считая атомов H, можно наблюдать как бумеранг.
Этот бумеранг представляет ненасыщенность или двойную связь на одной из его сторон (C1) и, следовательно, он плоский из-за sp-гибридизации 2 атомов углерода.
Однако другая сторона занята метильной группой (-CH3), чья гибридизация является sp 3 и он имеет тетраэдрическую геометрию. Таким образом, если смотреть спереди, бумеранг плоский с атомами H, выступающими из этого на 109,5º приблизительно.
В газовой фазе молекула слабо взаимодействует с другими силами дисперсии. Кроме того, метильная группа предотвращает взаимодействие между двойными связями (π-π) двух молекул пропилена..
Это приводит к уменьшению их межмолекулярных сил, что отражается на их физических свойствах. Только при очень низких температурах пропилен может принять твердую структуру, в которой бумеран остается сгруппированным со своими слабыми взаимодействиями.
свойства
Это бесцветный газ с ароматическим запахом. Он транспортируется в виде сжиженного газа и, когда он выходит из контейнеров, в которых он находится, он делает это в форме газа или жидкости. При низких концентрациях он образует взрывоопасную и легковоспламеняющуюся смесь с воздухом, плотность пропилена выше, чем у воздуха.
Разница между пропиленом и полипропиленом
Пропилен является органическим соединением и углеводородом. Это второй самый простой алкен в серии алкенов. Пропилен является ненасыщенным из-за наличия двойной связи. При комнатной температуре это г
Содержание:
Ключевые области покрыты
1. Что такое пропилен
— определение, использование, производство
2. Что такое полипропилен
— Определение, Тактичность, Использование
3. Какова связь между пропиленом и полипропиленом
4. В чем разница между пропиленом и полипропиленом
— Сравнение основных различий
Ключевые слова: углерод, крекинг, гибридизация, полимер, полимеризация, полипропен, полипропилен, пропен, пропилен, тактичность.
Что такое пропилен
Пропилен представляет собой углеводород, имеющий химическую формулу C3ЧАС6, ИЮПАК название пропилена пропен, Это второй самый простой алкен, имеющий три атома углерода, связанных друг с другом. Это ненасыщенное соединение, имеющее двойную связь. Следовательно, существует два типа углерод-углеродных связей; Связь C = C и связь C-C. Следовательно, это соединение имеет два типа атомов углерода; два зр 2 гибридизованные атомы углерода и один зр 3 гибридизированный атом углерода.
Рисунок 1. Структура пропилена с шариковой ручкой
Использование пропилена для производства других химических веществ
Производство пропилена
Пропилен производится из ископаемого топлива, включая нефтяное масло, природный газ и уголь. Он образуется как побочный продукт переработки сырой нефти и переработки природного газа. Пропилен производится в основном двумя методами крекинга:
Эти реакции крекинга производят пропилен вместе со многими другими продуктами в виде смеси. Поэтому пропилен отделяют от этой смеси фракционной перегонкой. Однако каталитический крекинг дает больше пропилена по сравнению с паровым крекингом.
Что такое полипропилен
Рисунок 2: Повторяющаяся единица полипропилена
Полипропилен является дешевым, потому что это один из самых доступных для переработки пластиков. В отличие от мономера, полипропилен не имеет двойных связей в своей структуре полимера. Следовательно, это насыщенная структура.
тактичность полимера представляет собой расположение боковых групп / боковых групп (-CH3) вдоль полимерной цепи. Есть три типа тактик, которые можно наблюдать в полипропилене; Изотактический, Атактический и Синдиотактический. Изотактический полимер Структура состоит из полимерных цепей, содержащих боковую группу на одной стороне. Атактический полимер Структура состоит из полимерных цепей, содержащих метильную группу случайным образом. В синдиотаксическая структураметильные группы присоединены в чередующемся порядке.
Наиболее благоприятные свойства полипропилена включают низкую плотность, хорошую прозрачность, возможность повторного использования и растяжимость. Некоторые общие области применения полипропилена включают производство пленок для упаковки пищевых продуктов, текстильной промышленности (для производства ковров и т. Д.), Производства товаров народного потребления и т. Д.
Отношения между пропиленом и полипропиленом
Разница между пропиленом и полипропиленом
Определение
пропилен: Пропилен представляет собой углеводород, имеющий химическую формулу C3ЧАС6.
Состав
насыщение
пропиленПропилен является ненасыщенным соединением из-за наличия двойной связи.
Полипропилен: Полипропилен является насыщенным соединением и имеет двойные или тройные связи.
Гибридизация атомов углерода
пропилен: Пропилен имеет оба sp 2 и зр 3 гибридизованные атомы углерода.
Полипропилен: Полипропилен имеет только зр 3 гибридизованные атомы углерода.
Молярная масса
пропилен: Молярная масса пропилена составляет 42,08 г / моль.
Полипропилен: Полипропилен имеет молярную массу 42,08 г / моль для одного повторяющегося звена.
Тактичность
пропилен: Тактичность отсутствует в пропилене.
Полипропилен: Тактичность присутствует в полипропилене.
Основное использование
пропиленПропилен в основном используется в качестве мономера для производства полимеров и других соединений, таких как пропеновая кислота, пропенонитрил и т. Д.
Полипропилен: Полипропилен используется в качестве пленки для упаковки пищевых продуктов, в текстильной промышленности (для производства ковров и т. Д.), В производстве товаров народного потребления и т. Д.
Заключение
Ссылка:
1. Лазонби, Джон. «Пропен (пропилен)». Основная химическая промышленность онлайн,