Современные подходы к лечению больных гипертрофической кардиомиопатией
Полувековая история изучения проблемы гипертрофической кардиомиопатии (ГКМП) отражает значительную эволюцию знаний в области этиологии, патогенеза, диагностики, клинического течения, прогноза и вариантов лечения этого заболевания. За указанный период тол
Полувековая история изучения проблемы гипертрофической кардиомиопатии (ГКМП) отражает значительную эволюцию знаний в области этиологии, патогенеза, диагностики, клинического течения, прогноза и вариантов лечения этого заболевания. За указанный период только в англоязычных изданиях опубликованы более 1000 крупных научных работ. ГКМП — одна из основных и, вероятно, наиболее распространенных форм кардиомиопатий, заболеваний миокарда, сопровождающихся его дисфункцией (Report of the 1995 WHO/ISFC Task Force on the Definition and Classification of Cardiomyopathy) [1].
В 2003 г. создан Международный комитет (ACC/ESC), объединивший американских и европейских экспертов по ГКМП, и опубликовано сообщение, суммировавшее основные положения, включая стратегию лечебных мероприятий [2].
Определение заболевания носит описательный характер. Так, по современным представлениям, ГКМП является преимущественно генетически обусловленным заболеванием мышцы сердца, характеризующимся комплексом специфических морфофункциональных изменений и неуклонно прогрессирующим течением с высокой угрозой развития тяжелых, жизнеугрожающих аритмий и внезапной смерти (ВС). ГКМП характеризуется массивной гипертрофией миокарда левого и/или реже правого желудочка, чаще асимметричного характера за счет утолщения межжелудочковой перегородки (МЖП), нередко с развитием обструкции (систолического градиента давления) выходного тракта ЛЖ при отсутствии видимых причин (артериальная гипертония, пороки и специфические заболевания сердца). Основным методом диагностики остается эхокардиографическое исследование. В зависимости от наличия или отсутствия градиента систолического давления в полости ЛЖ, ГКМП разделяют на обструктивную и необструктивную, что имеет важное практическое значение при выборе тактики лечения. При этом различают 3 гемодинамических варианта обструктивной ГКМП: с субаортальной обструкцией в покое (так называемой базальной обструкцией); с лабильной обструкцией, характеризующейся значительными спонтанными колебаниями внутрижелудочкового градиента давления без видимой причины; с латентной обструкцией, которая вызывается только при нагрузке и провокационных фармакологических пробах (в частности, вдыханием амилнитрита, при приеме нитратов или внутривенном введении изопротеренола).
Типичными являются морфологические изменения: аномалия архитектоники сократительных элементов миокарда (гипертрофия и дезориентация мышечных волокон), развитие фибротических изменений мышцы сердца, патология мелких интрамиокардиальных сосудов [3, 4].
В настоящее время наблюдается повсеместный рост числа зарегистрированных случаев этой патологии как за счет внедрения в практику современных методов диагностики, так и, вероятно, в связи с истинным увеличением числа больных ГКМП [8, 9]. Согласно данным последних исследований, распространенность заболевания в общей популяции является более высокой, чем считалось ранее, и составляет 0,2% [10, 11]. ГКМП может диагностироваться в любом возрасте, от первых дней до последней декады жизни, однако преимущественно заболевание выявляется у лиц молодого трудоспособного возраста [12, 13]. Ежегодная смертность больных ГКМП колеблется в пределах от 1 до 6%: у взрослых больных составляет 1–3% [14, 15], а в детском и подростковом возрасте у лиц с высоким риском ВС — 4–6% [16, 17].
Общепризнанна концепция о преимущественно наследственной природе ГКМП [18, 19]. В литературе широкое распространение получил термин «семейная гипертрофическая кардиомиопатия». К настоящему времени установлено, что более половины всех случаев заболевания являются наследуемыми [20, 21], при этом основной тип наследования — аутосомно-доминантный. Оставшиеся приходятся на так называемую спорадическую форму; в этом случае у пациента нет родственников, болеющих ГКМП или имеющих гипертрофию миокарда. Считается, что большинство, если не все случаи спорадической ГКМП, также имеют генетическую причину, т. е. вызваны случайными мутациями.
ГКМП — это генетически гетерогенное заболевание, причиной которого являются более 200 описанных мутаций нескольких генов, кодирующих белки миофибриллярного аппарата [2, 22]. К настоящему времени известны 10 белковых компонентов сердечного саркомера, выполняющих контрактильную, структурную или регуляторную функции, дефекты которых наблюдаются при ГКМП. Причем в каждом гене множество мутаций могут становиться причиной заболевания (полигенное мультиаллельное заболевание).
Наличие той или иной ассоциированной с ГКМП мутации признается «золотым» стандартом диагностики заболевания. При этом описанные генетические дефекты характеризуются разной степенью пенетрантности, выраженностью морфологических и клинических проявлений. Тяжесть клинической картины зависит от присутствия и степени гипертрофии. Мутации, которые ассоциируются с высокой пенетрантностью и плохим прогнозом, выражаются большей гипертрофией левого желудочка и толщиной МЖП, чем те, которые характеризуются низкой пенетрантностью и имеют хороший прогноз. Так, было показано, что лишь отдельные мутации ассоциированы с плохим прогнозом и высокой частотой ВС. К ним относятся замены Arg 403 Gln, Arg 453 Cys, Arg 719 Trp, Arg 719 Gln, Arg 249 Gln в гене тяжелой цепи β-миозина, InsG 791 в гене миозин-связывающего белка С и Asp 175 Asn в гене α-тропомиозина [23, 24, 25, 26]. Для мутаций в гене тропонина Т характерна умеренная гипертрофия миокарда, однако прогноз достаточно неблагоприятен, а вероятность внезапной остановки сердца высока [27]. Другие генетические аномалии, как правило, сопровождаются доброкачественным течением и благоприятным прогнозом или занимают промежуточное положение по тяжести вызываемых ими проявлений.
Таким образом, ГКМП характеризуется крайней гетерогенностью вызывающих ее причин, морфологических, гемодинамических и клинических проявлений, разнообразием вариантов течения и прогноза, что существенно затрудняет выбор адекватных и наиболее эффективных лечебных подходов по контролю и коррекции имеющихся нарушений. При этом отчетливо выделяются 5 основных вариантов течения заболевания и исходов:
Вариабельность прогноза определяет необходимость детальной стратификации риска фатальных осложнений заболевания, поиск доступных прогностических предикторов и критериев оценки проводимого лечения.
По современным представлениям, лечебная стратегия определяется в процессе разделения больных на категории в зависимости от описанных выше вариантов течения и прогноза (рис.).
Все лица с ГКМП, включая носителей патологических мутаций без фенотипических проявлений болезни и пациентов с бессимптомным течением заболевания, нуждаются в динамическом наблюдении, в ходе которого оцениваются характер и выраженность морфологических и гемодинамических нарушений. Особое значение имеет выявление факторов, определяющих неблагоприятный прогноз и повышенный риск ВС (в частности, скрытых прогностически значимых аритмий).
К общим мероприятиям относятся ограничение значительных физических нагрузок и запрещение занятий спортом, способных вызывать усугубление гипертрофии миокарда, повышение внутрижелудочкового градиента давления и риска ВС. Для предупреждения инфекционного эндокардита в ситуациях, связанных с развитием бактериемии, при обструктивных формах ГКМП рекомендуется антибиотикопрофилактика, аналогичная таковой у больных с пороками сердца.
До настоящего времени окончательно не решен вопрос о необходимости проведения активной медикаментозной терапии у наиболее многочисленной группы больных с бессимптомной или малосимптомной формами ГКМП и низкой вероятностью ВС. Противники активной тактики обращают внимание на то, что при благоприятном течении заболевания продолжительность жизни и показатели смертности не отличаются от таковых в общей популяции [28, 29]. Некоторые же авторы указывают на то, что использование в этой группе пациентов β-адреноблокаторов и антагонистов кальция (верапамил) может приводить к сдерживанию гемодинамических нарушений и клинической симптоматики [30, 31]. При этом никто не оспаривает тот факт, что выжидательная тактика в случаях бессимптомного или малосимптомного течения ГКМП возможна лишь при отсутствии признаков внутрижелудочковой обструкции, обмороков и серьезных нарушений сердечного ритма, отягощенной наследственности и случаев ВС у близких родственников.
Следует признать, что лечение ГКМП, генетически обусловленного заболевания, обычно распознаваемого на поздней стадии, пока может быть в большей степени симптоматическим и паллиативным. Тем не менее к основным задачам лечебных мероприятий относятся не только профилактика и коррекция основных клинических проявлений заболевания с улучшением качества жизни пациентов, но и положительное влияние на прогноз, предупреждение случаев ВС и прогрессирования заболевания.
Основу медикаментозной терапии ГКМП составляют препараты с отрицательным инотропным действием: β-адреноблокаторы и блокаторы кальциевых каналов (верапамил). Для лечения весьма распространенных при этом заболевании нарушений сердечного ритма используются также дизопирамид и амиодарон.
β-адреноблокаторы стали первой и остаются и по сей день наиболее эффективной группой лекарственных средств, применяемых в лечении ГКМП. Они оказывают хороший симптоматический эффект в отношении основных клинических проявлений: одышки и сердцебиения, болевого синдрома, включая стенокардию, не менее чем у половины больных ГКМП [32, 33, 34], что обусловлено, в основном, способностью этих препаратов уменьшать потребность миокарда в кислороде. Благодаря отрицательному инотропному действию и уменьшению активации симпатоадреналовой системы при физическом и эмоциональном напряжении, β-блокаторы предотвращают возникновение или повышение субаортального градиента давления у больных с латентной и лабильной обструкцией, существенно не влияя на величину этого градиента в покое. Убедительно показана способность β-блокаторов улучшать функциональный статус пациентов в условиях курсового и длительного применения [35]. Хотя препараты не оказывают прямого влияния на диастолическое расслабление миокарда, они могут улучшать наполнение ЛЖ косвенно — за счет уменьшения частоты сердечных сокращений и предупреждения ишемии сердечной мышцы [36]. В литературе имеются данные, подтверждающие способность β-блокаторов сдерживать и даже приводить к обратному развитию гипертрофии миокарда [37, 38]. Однако другие авторы подчеркивают, что вызываемое β-блокаторами симптоматическое улучшение не сопровождается регрессией гипертрофии ЛЖ и улучшением выживаемости больных [39]. Хотя эффект этих препаратов в отношении купирования и предупреждения желудочковых и суправентрикулярных аритмий и внезапной смерти не доказан, ряд специалистов все же считают целесообразным их профилактическое назначение больным ГКМП высокого риска, включая пациентов молодого возраста с отягощенным случаями внезапной смерти семейным анамнезом [40].
Предпочтение отдается β-блокаторам без внутренней симпатомиметической активности. Наибольший опыт накоплен по применению пропранолола (обзидан, анаприлин). Его назначают начиная с 20 мг 3-4 раза в день, с постепенным увеличением дозы под контролем пульса и артериального давления (АД) до максимально переносимой в большинстве случаев 120–240 мг/сут. Следует стремиться к применению возможно более высоких доз препарата, так как отсутствие эффекта терапии β-блокаторами, вероятно, связано с недостаточной дозировкой. При этом нельзя забывать о том, что повышение дозировок существенно увеличивает риск известных побочных эффектов.
В настоящее время широко изучается возможность эффективного применения нового поколения кардиоселективных β-блокаторов пролонгированного действия, в частности атенолола, конкора и др. При этом существует мнение о том, что кардиоселективные β-блокаторы у больных ГКМП не имеют преимуществ перед неселективными, так как в больших дозах, к достижению которых следует стремиться, селективность практически утрачивается. Следует отметить, что рекомендуемый к применению у больных ГКМП с тяжелыми суправентрикулярными и желудочковыми аритмиями соталол сочетает в себе свойства неселективных β-блокаторов и антиаритмических средств III класса (кордароноподобный эффект).
Применение блокаторов медленных кальциевых каналов при ГКМП основано на снижении уровня свободного кальция в кардиомиоцитах и нивелировании асинхронии их сокращения, улучшении расслабления миокарда и снижении его сократимости, подавлении процессов гипертрофии миокарда. Среди блокаторов кальциевых каналов препаратом выбора, благодаря наибольшей выраженности отрицательного инотропного действия и наиболее оптимальному профилю фармакологических свойств, является верапамил (изоптин, финоптин). Он обеспечивает симптоматический эффект у 65–80% больных, включая случаи рефрактерности к лечению β-блокаторами, что обусловлено способностью препарата уменьшать ишемию миокарда, в том числе безболевую, и улучшать его диастолическое расслабление и податливость ЛЖ [41, 42, 43]. Это свойство верапамила обеспечивает повышение толерантности больных к физической нагрузке и снижение субаортального градиента давления в покое при меньшей по сравнению с β-блокаторами способности к уменьшению внутрижелудочковой обструкции в случаях физического и эмоционального напряжения и провокации изопротеренолом. Одновременно верапамил снижает периферическое сосудистое сопротивление вследствие вазодилататорного действия [44]. И хотя этот эффект чаще всего нивелируется непосредственным положительным влиянием на диастолическую функцию ЛЖ, у отдельных больных с базальной внутрижелудочковой обструкцией в сочетании с повышенным конечно-диастолическим давлением ЛЖ и склонностью к системной артериальной гипотензии при уменьшении постнагрузки внутрижелудочковый градиент давления может резко возрастать. Это способно приводить к развитию отека легких, кардиогенного шока и даже внезапной смерти [45]. Подобные грозные осложнения фармакотерапии верапамилом описаны также у больных необструктивной ГКМП с высоким давлением в левом предсердии, у которых они обусловлены отрицательным инотропным действием препарата. Очевидно, как важно соблюдать осторожность при начале лечения верапамилом этой категории больных. Прием препарата следует начинать в условиях стационара с малых доз — 20–40 мг 3 раза в день с постепенным их повышением при хорошей переносимости до снижения частоты сердечных сокращений в покое до 50–60 уд/мин. Клинический эффект наступает обычно при приеме не менее 160–240 мг препарата в сутки; более удобны в условиях длительного применения пролонгированные формы (изоптин-ретард, верогалид-ретард). С учетом благоприятного влияния верапамила на диастолическую функцию и величину субаортального градиента давления в ЛЖ, а также доказанной способности увеличивать выживаемость больных ГКМП по сравнению с плацебо [46], целесообразно его профилактическое назначение у асимптоматичных больных ГКМП высокого риска.
Место дилтиазема в лечении ГКМП окончательно не определено. Имеются данные, что в средней дозе 180 мг/сут за 3 приема он оказывает столь же выраженное, как 240 мг верапамила, благотворное влияние на диастолическое наполнение ЛЖ и одинаковый симптоматический эффект, однако в меньшей степени улучшает физическую работоспособность больных [47].
В нашей клинике продолжается проспективное наблюдение (от 1 до 5 лет) более 100 больных ГКМП. Больные были рандомизированы на 3 сопоставимые по количеству, полу, возрасту и тяжести клинических проявлений группы. Пациентам произвольно назначались атенолол или изоптин-ретард; в третьей группе преобладали лица с тяжелыми желудочковыми нарушениями ритма, и им был рекомендован прием соталола. Оценка эффективности различных вариантов медикаментозного лечения проводилась в условиях длительного (не менее 1 года) применения препаратов. Суточные дозы при двухкратном режиме приема титровались индивидуально и составили в среднем 85, 187, 273 мг для атенолола, изоптина и соталола соответственно. Длительная терапия привела к улучшению клинического состояния соответственно у 77, 72 и 83% пациентов каждой группы, что выражалось в достоверном уменьшении основных симптомов, проявлений сердечной недостаточности (СН), увеличении мощности и времени выполненной нагрузки и улучшении показателей качества жизни (на 25, 32 и 34% соответственно). При этом выявлены достоверное (p
С. А. Габрусенко, кандидат медицинских наук
Ю. В. Сафрыгина
В. Г. Наумов, доктор медицинских наук, профессор
Ю. Н. Беленков, доктор медицинских наук, профессор
НИИ кардиологии им. А. Л. Мясникова РК НПК МЗ РФ, Москва
Стандартная электрокардиография в педиатрической практике
Электрокардиография (ЭКГ) остается одним из самых распространенных методов обследования сердечно-сосудистой системы и продолжает развиваться и совершенствоваться. На основе стандартной электрокардиограммы предложены и широко используются различные модифи
Электрокардиография (ЭКГ) остается одним из самых распространенных методов обследования сердечно-сосудистой системы и продолжает развиваться и совершенствоваться. На основе стандартной электрокардиограммы предложены и широко используются различные модификации ЭКГ: холтеровское мониторирование, ЭКГ высокого разрешения, пробы с дозированной физической нагрузкой, лекарственные пробы [2, 5].
Отведения в электрокардиографии
Однополюсные грудные отведения обозначают латинской буквой V (потенциал, напряжение) с добавлением номера позиции активного положительного электрода, обозначенного арабскими цифрами:
С помощью грудных отведений можно судить о состоянии (величине) камер сердца. Если обычная программа регистрации 12 общепринятых отведений не позволяет достаточно надежно диагностировать ту или иную электрокардиографическую патологию либо требуется уточнение некоторых количественных параметров, используют дополнительные отведения. Это могут быть отведения
Техника регистрации электрокардиограммы
ЭКГ регистрируют в специальном помещении, удаленном от возможных источников электрических помех. Исследование проводится после 15-минутного отдыха натощак или не ранее чем через 2 ч после приема пищи. Пациент должен быть раздет до пояса, голени следует освободить от одежды. Необходимо использовать электродную пасту для обеспечения хорошего контакта кожи с электродами. Плохой контакт или появление мышечной дрожи в прохладном помещении может исказить электрокардиограмму. Исследование, как правило, проводится в горизонтальном положении, хотя в настоящее время стали также осуществлять обследование в вертикальном положении, так как при этом изменение вегетативного обеспечения приводит к изменению некоторых электрокардиографических параметров [7].
Нормальная электрокардиограмма
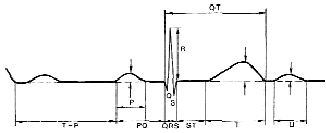 |
| Рисунок 1. Нормальная электрокардиограмма |
Анализ электрокардиограммы
Общая схема анализа ЭКГ включает несколько составляющих.
Анализ сердечного ритма и проводимости
Определение источника возбуждения производится по определению полярности зубца Р и по его положению относительно комплекса QRS. Синусовый ритм характеризуется наличием во II стандартном отведении положительных зубцов Р, предшествующих каждому комплексу QRS. При отсутствии этих признаков диагностируется несинусовый ритм: предсердный, ритм из АВ-соединения, желудочковые ритмы (идиовентрикулярные), мерцательная аритмия.
ЧСС = 60 R-R,
При неправильном ритме можно ограничиться определением минимальной и максимальной ЧСС, указав этот разброс в «Заключении».
Регулярность сердечных сокращений оценивается при сравнении продолжительности интервалов R-R между последовательно зарегистрированными сердечными циклами. Интервал R-R обычно измеряется между вершинами зубцов R (или S). Разброс полученных величин не должен превышать 10% от средней продолжительности интервала R-R. Показано, что синусовая аритмия той или иной степени выраженности наблюдается у 94% детей. Условно выделены V степеней выраженности синусовой аритмии:
Кроме физиологически наблюдаемой синусовой аритмии, неправильный (нерегулярный) ритм сердца может наблюдаться при различных вариантах аритмий: экстрасистолии, мерцательной аритмии и других.
Оценка функции проводимости требует измерения продолжительности зубца Р, которая характеризует скорость проведения электрического импульса по предсердиям, продолжительности интервала P-Q (P-R) (скорость проведения по предсердиям, АВ-узлу и системе Гиса) и общую длительность желудочкового комплекса QRS (проведение возбуждения по желудочкам). Увеличение длительности интервалов и зубцов указывает на замедление проведения в соответствующем отделе проводящей системы сердца.
Интервал P-R может быть укороченным (менее 0,10 с) в результате ускоренного проведения импульса, нарушений иннервации, из-за наличия дополнительного пути быстрого проведения между предсердиями и желудочками. На рисунке 3 представлен один из вариантов укорочения интервала P-R.
На данной электрокардиограмме (см. рис. 2) определяются признаки феномена Вольффа-Паркинсона-Уайта, включающего: укорочение интервала P-R менее 0,10 с, появление дельта-волны на восходящем колене комплекса QRS, отклонение электрической оси сердца влево. Кроме того, могут наблюдаться вторичные ST-T-изменения. Клиническое значение представленного феномена заключается в возможности формирования наджелудочковой пароксизмальной тахикардии по механизму re-entry (повторного входа импульса), так как дополнительные проводящие пути обладают укороченным рефрактерным периодом и восстанавливаются для проведения импульса быстрее, чем основной путь [8].
 |
| Рисунок 2. ЭКГ ребенка В. Г., 14 лет. Диагноз: феномен Вольффа-Паркинсона-Уайта |
Определение положения электрической оси сердца
Повороты сердца вокруг переднезадней оси. Принято различать три условные оси сердца, как органа, находящегося в трехмерном пространстве (в грудной клетке).
Поперечная ось проходит через середину основания желудочков перпендикулярно продольной оси. При повороте вокруг этой оси наблюдается смещение сердца верхушкой вперед или верхушкой назад.
Основное направление электродвижущей силы сердца представляет собой электрическую ось сердца (ЭОС). Повороты сердца вокруг условной переднезадней (сагиттальной) оси сопровождаются отклонением ЭОС и существенным изменением конфигурации комплекса QRS в стандартных и усиленных однополюсных отведениях от конечностей.
Повороты сердца вокруг поперечной или продольной осей относятся к так называемым позиционным изменениям.
Определение ЭОС проводится по таблицам. Для этого сопоставляют алгебраическую сумму зубцов R и S в I и III стандартных отведениях.
Различают следующие варианты положения электрической оси сердца:
Анализ предсердного зубца Р
Анализ зубца Р включает: изменение амплитуды зубца Р; измерение длительности зубца Р; определение полярности зубца Р; определение формы зубца Р.
При более горизонтальном положении сердца в грудной клетке, например у гиперстеников, зубец Р увеличивается в отведениях I и aVL и уменьшается в отведениях III и aVF, а в III стандартном отведении зубец Р может стать отрицательным.
Анализ желудочкового комплекса QRST
Комплекс QRST соответствует электрической систоле желудочков и рассчитывается от начала зубца Q до конца зубца Т.
Составляющие электрической систолы желудочков: собственно комплекс QRS, сегмент ST, зубец Т.
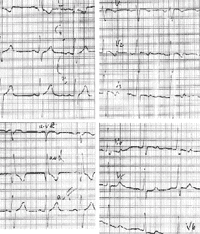 |
| Рисунок 3. ЭКГ ребенка Р. Б., 4 года. Диагноз: аномальное отхождение левой коронарной артерии от легочной артерии |
В то же время у детей грудного возраста глубокий зубец Q может быть в отведении III, aVF, а в отведении aVR весь желудочковый комплекс может иметь вид QS.
За зубцом Т следует горизонтальный интервал Т-Р, соответствующий периоду, когда сердце находится в состоянии покоя (период диастолы).
Зубец U появляется через 0,01-0,04 с после зубца Т, имеет ту же полярность и составляет от 5 до 50% высоты зубца Т. До настоящего времени четко не определено клиническое значение зубца U.
Интервал Q-T. Продолжительность электрической систолы желудочков имеет важное клиническое значение, поскольку патологическое увеличение электрической систолы желудочков может быть одним из маркеров появления угрожающих жизни аритмий.
Электро кардиограф ические признаки гипертрофии и перегрузок полостей сердца
Электрокардиографические изменения при этом обусловлены: увеличением электрической активности гипертрофированного отдела сердца; замедлением проведения по нему электрического импульса; ишемическими, дистрофическими и склеротическими изменениями в измененной мышце сердца.
Однако следует отметить, что широко используемый в литературе термин «гипертрофия» не всегда строго отражает морфологическую сущность изменений. Нередко дилатация камер сердца имеет те же электрокардиографические признаки, что и гипертрофия, при морфологической верификации изменений.
При анализе ЭКГ следует учитывать переходную зону (рис. 4) в грудных отведениях.
 |
| Рисунок 4. Состояние основных зубцов лектрокардиограммы в грудных отведениях. Переходная зона |
Признаки перегрузок предсердий
Электрокардиографические признаки перегрузки левого предсердия формируют электрокардиографический комплекс признаков, называемый в литературе Р-mitrale. Увеличение левого предсердия является следствием митральной регургитации при врожденной, приобретенной (вследствие ревмокардита или инфекционного эндокардита), относительной митральной недостаточности или митрального стеноза. Признаки перегрузки левого предсердия представлены на рисунке 5.
Увеличение левого предсердия (см. рис. 5) характеризуется:
Поскольку удлинение зубца Р может быть обусловлено не только увеличением левого предсердия, но и внутрипредсердной блокадой, то наличие выраженной отрицательной фазы зубца Р в отведении V1 более важно при оценке перегрузки (гипертрофии) левого предсердия. В то же время выраженность отрицательной фазы зубца Р в отведении V1 зависит от частоты сердечных сокращений и от общих характеристик вольтажа зубцов.
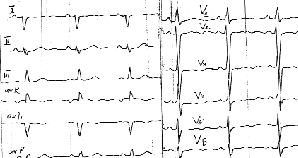 |
| Рисунок 6. ЭКГ ребенка В. С., 13 лет. Первичная легочная гипертензия |
Признаки увеличения правого предсердия представлены на рисунке 6.
Увеличение правого предсердия (см. рис. 6) характеризуется:
На рисунке 6 кроме признаков перегрузки правого предсердия отмечаются также признаки перегрузки правого желудочка.
Признаки перегрузок(гипертрофии) желудочков
Поскольку в норме ЭКГ отражает активность только левого желудочка, электрокардиографические признаки перегрузки левого желудочка подчеркивают (утрируют) норму. Там, где в норме высокий зубец R (в отведении V4, положение которого совпадает с левой границей сердца), он становится еще выше; где в норме глубокий зубец S (в отведении V2), он становится еще глубже.
Преобладающая дилатация левого желудочка имеет следующие признаки: R в V6 больше, чем R в V5, больше, чем R в V4 и больше 25 мм; внезапный переход от глубоких зубцов S к высоким зубцам R в грудных отведениях; смещение переходной зоны влево (к V4) (рис. 7).
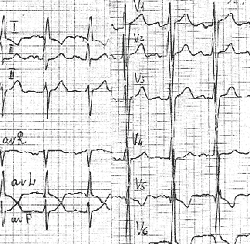 |
| Рисунок 7. ЭКГ ребенка Г. Ш., 3 года. Диагноз: врожденная недостаточность митрального клапана |
Признаками преоблающей гипертрофии миокарда левого желудочка является депрессия (смещение ниже изолинии) сегмента S-T в отведении V6, возможно, и в V5 (рис. 8) [4, 7].
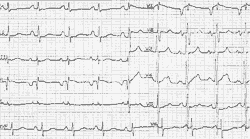 |
| Рисунок 8. ЭКГ ребенка Г. Ш., 3 года. Диагноз: врожденная недостаточность митрального клапана |
Дополнительными признаками являются вторичные изменения в виде смещения сегмента S-T и изменения зубца Т. При некоторых патологических состояниях, в частности при дефекте межпредсердной перегородки, гипертрофия правого желудочка демонстрируется также неполной блокадой правой ножки пучка Гиса в виде rsR в отведении V1 (рис. 9) [7].
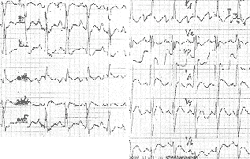 |
| Рисунок 9. ЭКГ ребенка М. К., 8 лет. Диагноз: дефект межпредсердной перегородки |
По вопросам литературы обращайтесь в редакцию.
Редакция приносит свои извинения за опечатки
В выходных данных статьи «Ящур», № 8 2004, следует читать:
А. Е. Кудрявцев, кандидат медицинских наук, доцент,
Т. Е. Лисукова, кандидат медицинских наук, доцент,
Г. К. Аликеева, кандидат медицинских наук
ЦНИИ эпидемиологии МЗ РФ, Москва
В статье И. Ю. Фофановой «Некоторые вопросы патогенеза внутриутробных инфекций», № 10.2004. На странице 33 во 2-й колонке слева направо следует читать: «Во II триместре (после уточнения диагноза) показано применение антибактериальной терапии с учетом чувствительности антибиотиков (пенициллинового ряда или макролидов). Назначение амоксиклава, аугментина, ранклава, азитрокса, сумамеда при беременности возможно, только когда предполагаемая польза для матери превышает потенциальный риск для плода или ребенка. Несмотря на то, что в экспериментальных исследованиях тератогенного действия этих препаратов выявлено не было, применения их во время беременности следует избегать».
Е. В. Мурашко, кандидат медицинских наук, доцент РГМУ, Москва
