Преквалификация лекарственных средств ВОЗ
Основные факты
Ежегодно международными закупочными организациями закупаются лекарственные средства стоимостью, исчисляемой миллиардами долларов США, для их распределения в странах с ограниченными ресурсами. Целью преквалификации является предоставление этим организациям возможности выбора среди широкого ассортимента качественных лекарств для массовых закупок.
Как ВОЗ осуществляет процесс преквалификации лекарственных средств?
Преквалификация состоит из пяти компонентов:
1. Предложение
Программа ВОЗ по преквалификации лекарственных средств, другие организации ООН (ЮНЭЙД и ЮНИСЕФ) и ЮНИТЭЙД предлагают производителям представить выражение заинтересованности в оценке продукта. Критериям преквалификации соответствуют только продукты, включенные в этот список.
Включение лекарственного средства в список основано на одном или более из трех критериев:
2. Предоставление досье
Производитель предоставляет всесторонние данные о качестве, безопасности и эффективности продукта, представленного для оценки. Эти данные включают:
3. Оценка
Все представленные данные оцениваются группой специалистов по оценке. В ее состав входят сотрудники ВОЗ и эксперты из национальных органов регулирования разных стран.
4. Инспекция
Группа инспекторов проверяет, соответствуют ли участки по производству готового фармацевтического продукта и его активного/-ых фармацевтического/-их ингредиента/-ов надлежащей практике производства ВОЗ. Они также проверяют, соответствует ли контрактно-исследовательская организация, проводящая какие-либо клинические испытания, имеющие отношение к представленному продукту, надлежащей клинической практике ВОЗ и надлежащей лабораторной практике ВОЗ.
5. Решение
Если оказывается, что продукт отвечает установленным требованиям и соответствующие участок/-ки по производству и контрактно-исследовательская/-ие организация\-и соответствуют стандартам ВОЗ, продукт вносится в перечень лекарственных препаратов, прошедших преквалификацию ВОЗ.
Процесс преквалификации лекарственных средств может длиться всего лишь три месяца, при условии что представлены полные данные, которые демонстрируют, что продукт соответствует всем необходимым стандартам. Однако, если данных недостаточно, процесс может значительно затянуться, поскольку производитель должен представить необходимые данные для повторной оценки.
Для обеспечения того, чтобы прошедшие преквалификацию продукты продолжали соответствовать спецификациям ВОЗ, в рамках программы регулярно проводятся повторные инспекции участков по производству преквалифицированных продуктов. В то же время оцениваются какие-либо изменения (известные как » вариации «) в спецификациях, процессах производства и контроле качества преквалифицированных продуктов и проводятся тесты по контролю качества на произвольно выбранных преквалифицированных продуктах.
Расширение доступа к лекарственным средствам гарантированного качества
В основе деятельности программы по преквалификации лежат международные фармацевтические стандарты качества, безопасности и эффективности лекарственных средств. Наряду с преквалифицированными лекарственными средствами, она также преквалифицирует фармацевтические лаборатории контроля качества (ЛКК) и активные фармацевтические ингредиенты и проводит большую информационно-пропагандистскую работу в защиту лекарственных средств гарантированного качества. В долгосрочной перспективе ее целью является расширение доступа к лекарственным средствам гарантированного качества путем содействия производителям в обеспечении соответствия стандартам ВОЗ и поддержки органов регулирования в области их соблюдения. Эта программа не стремится заменить национальные органы регулирования или национальные системы, разрешающие импорт лекарственных средств.
Создание потенциала и техническая помощь
Помимо деятельности по оценке и инспекции Программа по преквалификации создает национальный потенциал для устойчивого производства и мониторинга качественных лекарственных средств путем организации подготовки и передачи непосредственного опыта на уровне отдельных стран.
В рамках Программы существует трехмесячный ротационный пост в штаб-квартире ВОЗ для сотрудников национальных органов регулирования из развивающихся стран. В тесном сотрудничестве со старшими специалистами Программы по оценке лица, занимающие эту должность, расширяют свои технические знания, а также способствуют обмену информацией между их органами регулирования и ППК по возвращении в свои страны. Эта деятельность способствует обмену информацией между заинтересованными сторонами по фармацевтическим вопросам, связанным с качеством.
Программа также оказывает целевую техническую помощь производителям и лабораториям контроля качества. Такую помощь оказывают специалисты, которые не участвуют в деятельности ВОЗ по преквалификационной оценке или инспекции, но могут проводить аудиты и подготовку на уровне отдельных стран. Эта помощь направлена на решение конкретных технических проблем.
Почему ВОЗ проводит Программу по преквалификации лекарственных средств?
Программа по преквалификации является программой Организации Объединенных Наций, которая координируется ВОЗ. Это единственная глобальная программа по обеспечению качества лекарственных средств. Ни один другой глобальный орган не получает активную поддержку со стороны экспертов по регулированию как из развитых, так и из развивающихся стран.
Международное сотрудничество
Пресс-релизы
Размещен: 17.07.2014 г.
О программе преквалификации лекарственных средств ВОЗ
Ежегодно международными закупочными организациями и фондами системы ООН (ЮНИСЕФ, Глобальный фонд по борьбе с ВИЧ/СПИД, туберкулезом и малярией, ЮНИТЭЙД) закупается значительное количество лекарственных средств для их распределения в странах с ограниченными ресурсами.
Обязательным требованием для реализации лекарственных средств через данные механизмы является прохождение программы преквалификации ВОЗ.
Преквалификация лекарственных средств ВОЗ — это услуга, оказываемая ВОЗ для оценки качества, безопасности и эффективности лекарственных препаратов. Программа ВОЗ по преквалификации лекарственных средств обеспечивает соответствие лекарственных средств, поставляемых закупочными организациями, допустимым стандартам качества, безопасности и эффективности. Целью преквалификации является предоставление международным закупочным организациям возможности выбора среди широкого ассортимента качественных лекарств для массовых закупок.
Программа ВОЗ по преквалификации лекарственных средств была начата в 2001 году при поддержке Объединенной программы ООН по ВИЧ/СПИД (ЮНЭЙДС), Детского фонда ООН (ЮНИСЕФ) и Фонда ООН в области народонаселения с целью решения проблемы качества закупаемых ВОЗ лекарственных средств для вакцинопрофилактики, лечения ВИЧ/СПИД, малярии и туберкулеза. С 2006 года в программу включили препараты и медицинские изделия по репродуктивному здоровью.
В конце 2012 года в Перечень ВОЗ преквалифицированных лекарственных средств входило более 316 препаратов для основных болезней. Перечень лекарственных препаратов, прошедших преквалификацию ВОЗ, используется международными закупочными организациями и все шире странами для управления массовыми закупками лекарственных средств.
Программа преквалификации проводится на безвозмездной основе сотрудниками ВОЗ и включает оценку данных по безопасности, эффективности и качеству препаратов в форме регистрационного досье, а также аудит предприятия на соответствие правилам надлежащей производственной практики (GMP). С 2003 года аудит предприятий был расширен на производителей активных фармацевтических субстанций.
Данный процесс построен на строгих регуляторных принципах. В случае невыполнения всех требований предприятие не сможет пройти преквалификацию.
Для начала процесса преквалификации производитель должен направить всю информацию, начиная от источника активного вещества и его качества, заканчивая процессом производства готового лекарственного средства и, в большом количестве случаев, данных о результатах исследований биоэквивалентности, на рассмотрение и принятие экспертами ВОЗ по оценке досье и инспекторами ВОЗ. Необходимым условием является наличие у производителя системы качества, соответствующей требованиям надлежащей производственной практики ВОЗ.
Преквалификация состоит из пяти компонентов:
1. Предложение
Программа ВОЗ по преквалификации лекарственных средств, другие организации ООН (ЮНЭЙД и ЮНИСЕФ) и ЮНИТЭЙД предлагают производителям представить выражение заинтересованности в оценке продукта. Критериям преквалификации соответствуют только продукты, включенные в этот список.
Включение лекарственного средства в список основано на одном или более из трех критериев:
— оно включено в Примерный перечень основных лекарственных средств ВОЗ;
— заявка на его добавление в Примерный перечень представлена в соответствующий Экспертный комитет ВОЗ для оценки, и оно, по всей вероятности, соответствует критериям для включения (исходя из потребностей общественного здравоохранения, относительной эффективности, безопасности и эффективности по стоимости);
— оно рекомендовано для использования одним из нынешних руководств ВОЗ для лечения.
Список лекарственных средств, которые могут быть представлены на преквалификацию, публикуется на сайте ВОЗ http://apps.who.int/prequal/. В настоящее время в него входит ряд препаратов для лечения ВИЧ/СПИД, туберкулеза, гриппа, малярии, забытых тропических болезней и др.
2. Предоставление досье
Производитель предоставляет всесторонние данные о качестве, безопасности и эффективности продукта, представленного для оценки. Эти данные включают:
— данные о чистоте всех ингредиентов, используемых при производстве;
— данные о конечном фармацевтическом продукте (такие как информация о стабильности);
— результаты тестов на биоэквивалентность (клинических испытаний, проводимых на здоровых добровольцах), если только это требование не снято.
3. Оценка
Все представленные данные оцениваются группой специалистов по оценке. В ее состав входят сотрудники ВОЗ и эксперты из национальных органов регулирования разных стран.
4. Инспекция
Группа инспекторов проверяет, соответствуют ли участки по производству готового фармацевтического продукта и его активного/-ых фармацевтического/-их ингредиента/-ов надлежащей практике производства ВОЗ. Они также проверяют, соответствует ли контрактно-исследовательская организация, проводящая какие-либо клинические испытания, имеющие отношение к представленному продукту, надлежащей клинической практике ВОЗ и надлежащей лабораторной практике ВОЗ.
5. Решение
Если оказывается, что продукт отвечает установленным требованиям и соответствующие участок/-ки по производству и контрактно-исследовательская/-ие организация\-и соответствуют стандартам ВОЗ, продукт вносится в перечень лекарственных препаратов, прошедших преквалификацию ВОЗ.
Процесс преквалификации лекарственных средств может длиться всего лишь три месяца, при условии что представлены полные данные, которые демонстрируют, что продукт соответствует всем необходимым стандартам. Однако, если данных недостаточно, процесс может значительно затянуться, поскольку производитель должен представить необходимые данные для повторной оценки.
Для обеспечения того, чтобы прошедшие преквалификацию продукты продолжали соответствовать спецификациям ВОЗ, в рамках программы регулярно проводятся повторные инспекции участков по производству преквалифицированных продуктов. В то же время оцениваются какие-либо изменения в спецификациях, процессах производства и контроле качества преквалифицированных продуктов и проводятся тесты по контролю качества на произвольно выбранных преквалифицированных продуктах.
Информация о требованиях, предъявляемых к производству лекарственных препаратов, список необходимой документации и пошаговая инструкция прохождения программы преквалификации на английском языке размещены в свободном доступе на официальном сайте ВОЗ http://apps.who.int/prequal/.
Общая информация об основных этапах прохождения преквалификации на русском языке также в свободном доступе размещена на сайте ВОЗ http://www.who.int/mediacentre/factsheets/fs278/ru/.
22-25 сентября 2014 года в Копенгагене в очередной раз состоится совместное совещание ВОЗ/ЮНИСЕФ/Фонда ООН по народонаселению с производителями и поставщиками диагностических препаратов, готовой фармацевтической продукции, активных фармацевтических субстанций и вакцин. Совещание предоставит возможность производителям диагностических препаратов, лекарственных средств и вакцин, экспертам в области качества, безопасности и эффективности фармпродукции, представителям закупочных агентств и международным донорам совместно обсудить вопросы, связанные с производством и поставкой качественной фармацевтической продукции. На совещании также будут организованы индивидуальные консультации между производителями и специалистами в области преквалификации.
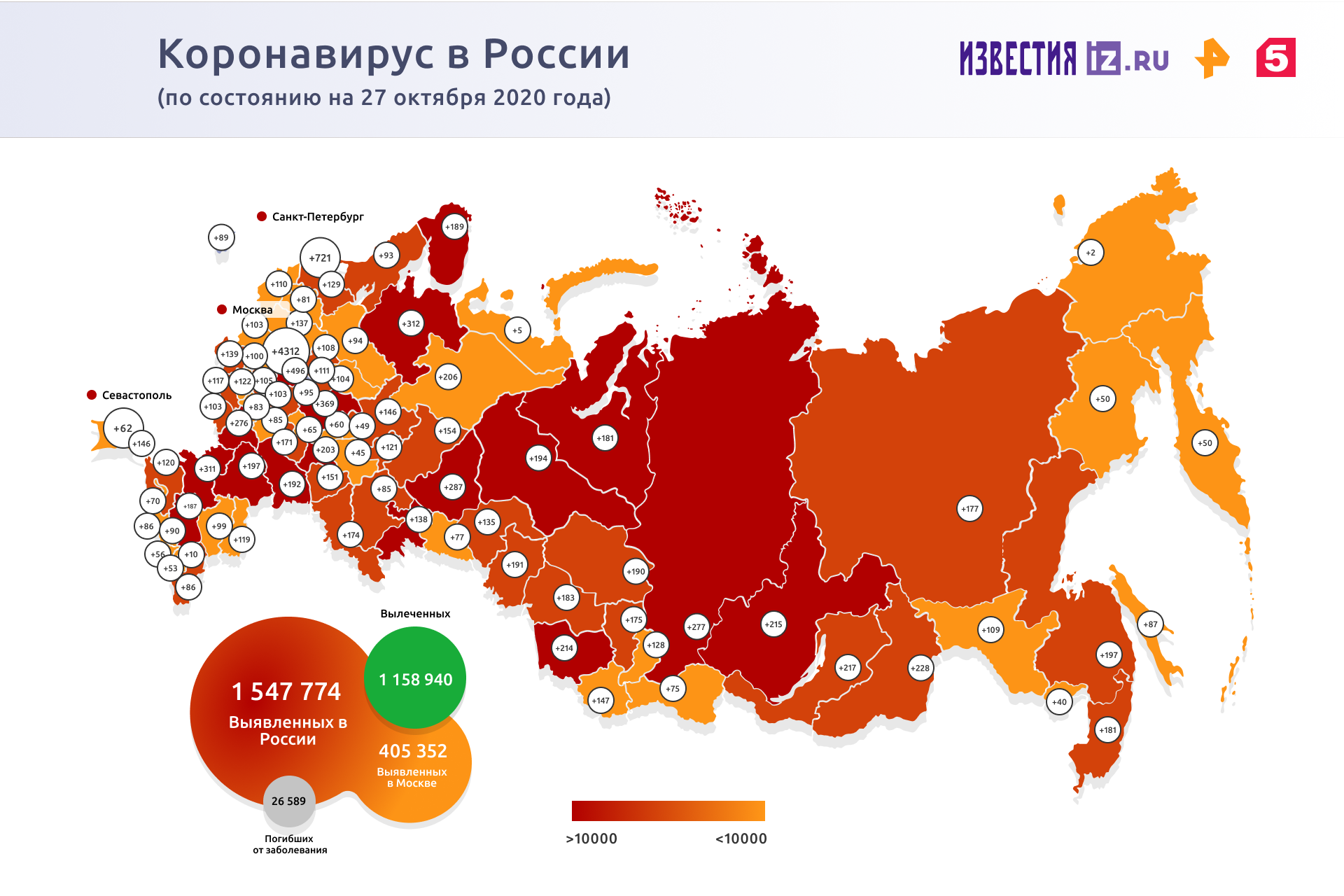
Россия одной из первых подала заявку на преквалификацию ВОЗ вакцины от COVID-19
Российская заявка на преквалификацию Всемирной организацией здравоохранения (ВОЗ) вакцины «Спутник V» стала одной из первых с начала приема заявок. Об этом сообщили «Известиям» во вторник, 27 октября, в Российском фонде прямых инвестиций (РФПИ).
В рамках процедуры преквалификации лекарственных средств оцениваются качество, безопасность и эффективность лекарственных препаратов. При условии соответствия установленным требованиям и стандартам медицинский препарат вносится в перечень лекарственных препаратов, прошедших преквалификацию.
«Мы направили заявку на ускоренную регистрацию и преквалификацию вакцины Всемирной организацией здравоохранения, что позволит включить «Спутник V» в перечень лекарственных препаратов, отвечающих ведущим стандартам качества, безопасности и эффективности. Выражаем признательность ВОЗ за активное сотрудничество и рассчитываем на успешное прохождение процесса преквалификации на всех основных этапах», — заявил генеральный директор Российского фонда прямых инвестиций Кирилл Дмитриев.
Отмечается, что в условиях пандемии ускоренная регистрация вакцины в рамках процедуры EUL позволит сделать российскую вакцину доступной для всего мира в более короткие сроки.
Кроме того, успешное прохождение переквалификации даст возможность включить «Спутник V» в перечень лекарственных препаратов, который используется международными закупочными организациями и странами для управления массовыми закупками лекарственных средств.
Ранее в этот же день представитель ВОЗ в России Мелита Вуйнович выразила надежду, что в скором времени можно будет рекомендовать к применению вакцины от коронавируса, которые разработали в России и других странах.
Накануне глава Центра имени Гамалеи Александр Гинцбург сообщил, что прививка вакциной от коронавируса «Спутник V» не влияет на уменьшение защитных свойств организма.
Штамм в паспорте

При этом в Москве, например, власти уже проявили инициативу: пожилые москвичи и студенты получают приглашения на прививку с пометкой, что после вакцинации им разблокируют социальные карты для бесплатного проезда.
Пока же в ВОЗ считают, что «требование о наличии «иммунного паспорта» при совершении международных поездок в настоящее время не считается обоснованным с научной точки зрения и поэтому не рекомендуется ВОЗ… Необходимо также учитывать аспекты, связанные с соблюдением этики, законности и прав человека, которые касаются безопасности личных данных, а также вопросы конфиденциальности медицинских сведений, возможного риска фальсификации, опасных видов поведения, стигматизации и дискриминации».
Айдар Ишмухаметов, директор ФНЦ исследований и разработки иммунобиологических препаратов имени М.П. Чумакова РАН, член-корреспондент РАН:
Внутригосударственное регулирование вопроса обязательной вакцинации применимо для каждой страны: для этого есть национальные требования к медицинским иммунобиологическим препаратам (вакцинам) и их применению у населения. Существуют также требования для въезда в страну, если данная страна признана эндемичной по какому-либо инфекционному заболеванию: въезд могут ограничить для туристов, не сделавших прививки. Это необходимо, чтобы предотвратить вспышки инфекционных заболеваний.
Станет ли необходимой вакцинация против коронавирусной инфекции для международных поездок? На данный момент ВОЗ не рекомендует применение паспортов вакцинации для ограничения межгосударственного перемещения. Насколько мне известно, ВОЗ и ООН рассматривают вопрос о введении в действие электронного сертификата иммунитета (сведений о наличии антител к коронавирусной инфекции). Такой подход не ограничивает в правах людей, переболевших COVID-19 и, кроме того, способствует получению более полной информации о напряженности иммунитета по всему миру.
Что касается международного признания вакцин, хочу отметить, что ВОЗ является международной организацией рекомендательного характера. Национальная система здравоохранения любой страны может принимать или не принимать рекомендации ВОЗ. Но в любом случае национальные требования страны, прописанные в ее законах, будут в приоритете. Вакцина может применяться в стране только если она имеет национальную регистрацию и утверждена к применению регулирующей системой страны.
Наш научный центр более 20 лет является преквалифицированным производителем и поставляет вакцину от желтой лихорадки по всему миру. Преквалификация необходима для поставки вакцины на экспорт. Досье на коронавирусную вакцину производства нашего Центра будет передано для прохождения преквалификации ВОЗ после утверждения Министерством здравоохранения России.
Вашингтон прост: США пустят привитых «Спутником V» после признания ВОЗ
США готовы открыть границы для привитых «Спутником V» после включения вакцины в список разрешенных для экстренного использования ВОЗ. Об этом «Известиям» заявили в Госдепе, информацию подтвердили в американском Центре по контролю за заболеваниями (CDC). Из ответа обоих ведомств следует, что на российскую вакцину будут распространяться те же правила, что и на индийскую и китайскую: в Штаты допускают граждан, привитых Covaxin и Sinovac — эти препараты из Индии и КНР признаны Всемирной организацией здравоохранения, но не сертифицированы национальным американским регулятором. В Российском союзе туриндустрии (РСТ) «Известиям» заявили, что даже после признания «Спутника V» ВОЗ въехать в США россиянам будет сложно из-за проблем с визами: посольство в Москве с мая этого года их не выдает, а в американских диппредставительствах в Казахстане и Турции ближайшие свободные даты собеседования — только с августа 2022 года.
Признаки признания
С 8 ноября въехать в США могут только те, кто привит вакцинами, признанными ВОЗ или американским регулятором Food and Drug Administration (FDA). Всего в списке разрешенных восемь вакцин, включая индийские и китайские.
В Госдепе США подтвердили «Известиям», что для въезда в страну достаточно быть привитым вакциной, признанной ВОЗ или FDA. Если Всемирная организация здравоохранения включит в этот список «Спутник V», то США откроют свои границы и для привитых российским препаратом, следует из ответа американского ведомства.
— Центр США по контролю за заболеваниями (CDC) определил: список разрешенных вакцин, действительных для въезда в США, будет включать препараты, одобренные или разрешенные FDA, а также вакцины, признанные Всемирной организацией здравоохранения (ВОЗ) разрешенными для экстренного использования. В настоящее время для въезда в США разрешены: Pfizer, Moderna, Johnson & Johnson; но также вакцины, такие как AstraZeneca, которые имеют лицензию ВОЗ. Мы отсылаем вас к ВОЗ по вопросу о признании организацией Sputnik V для экстренного использования», — говорится в ответе Госдепартамента на запрос «Известий».
В Центре США по контролю за заболеваниями «Известиям» уточнили, что все вакцины, признанные ВОЗ, будут приняты для въезда в Штаты.
23 октября ВОЗ возобновила ранее приостановленную процедуру преквалификации «Спутника V» для экстренного применения. Представители организации допускали, что сертификация препарата завершится до конца года.
В пресс-службе ВОЗ «Известиям» заявили, что у организации пока нет новостей о дальнейшей сертификации «Спутника V». Там также уточнили, что появление нового штамма коронавируса «Омикрон» не замедлит регистрацию российского препарата.
В конце ноября глава РФПИ Кирилл Дмитриев заявил, что Минздрав РФ продолжает диалог с ВОЗ по этому вопросу, ожидается, что повторная инспекция организации прибудет в Россию в декабре. «Мы видим определенные позитивные подвижки», — уточнил глава РФПИ. На вопросы «Известий» в Российском фонде прямых инвестиций не ответили.
Юридические препятствия в рамках процесса преквалификации «Спутника V» устранены, искусственных задержек быть не должно, и всё состоится, как только российская сторона даст отмашку, заявил «Известиям» зампостпреда РФ при международных организациях в Женеве Александр Алимов.
При этом он уточнил: подтверждение — не просто «зеленый семафор». Положительное мнение экспертов может сопровождаться комментариями и техническими вопросами, на которые нужно будет дать ответы. Поэтому экспертная работа будет продолжена и потребует определенного времени.
— Затягивать, конечно, никто не будет. ВОЗ, насколько мы можем наблюдать отсюда, вопреки расхожему мнению, искусственно процесс не блокирует и заинтересована в сертификации российской вакцины. К качеству вакцины претензий также нет. Смотрим вперед с оптимизмом, — заключил дипломат.
Ранее в Министерстве здравоохранения РФ «Известиям» заявили, что в начале октября представители России и США обсудили взаимное признание сертификатов вакцинации.
По результатам обсуждения Минздрав РФ направил в департамент здравоохранения и социальных служб США письмо «с предложением рассмотреть возможность взаимного признания сертификатов о профилактических прививках против новой коронавирусной инфекции и проработать механизм взаимного признания сертификатов вакцинации», заявили в пресс-службе ведомства.
В посольстве США в Москве, а также в российском посольстве в Вашингтоне не ответили на вопрос «Известий» о том, на каком уровне находятся переговоры РФ и США по взаимному признанию сертификатов вакцинации.
Очередь на визу до августа
В США есть политизация вопроса вакцинации, считает президент Американского университета Эдуард Лозанский. По его словам, за ней стоят и фармгиганты, поскольку для них невыгодно появление на американском рынке зарубежных конкурентов, включая «Спутник».
— С другой стороны, если ВОЗ утвердит российскую вакцину, то у США не будет возможности дальше эту вакцину не признавать, — констатировал эксперт.
По его словам, в Штатах у истеблишмента есть предвзятое отношение ко всему российскому: «Всё, что исходит от России, — от вакцины до идей — встречает в лучшем случае подозрение».
Еще одной причиной для пересмотра нынешних правил въезда иностранцев в США может стать новый штамм коронавируса «Омикрон». 1 декабря в Белом доме заявили, что Вашингтон изучает возможность ограничить авиасообщение с другими странами в свете его распространения.
Даже в том случае, если Штаты откроют границы для привитых «Спутником V», это не упростит въезд в страну для наших путешественников, считает вице-президент Российского союза туриндустрии (РСТ) Дмитрий Горин. Это связано с визовым фактором: получить запись на американскую визу сложно, в РФ это невозможно.
С 1 августа диппредставительство США в России работает в минимальном составе — 120 сотрудников. Потому в американском посольстве в Москве россиянам рекомендовали обращаться за неиммиграционными визами в представительства США в других странах.
Сокращение американской дипмиссии произошло после того, как РФ ввела ограничения на наем граждан России и третьих стран в диппредставительства Соединенных Штатов. Эти меры были вызваны апрельскими антироссийскими санкциями со стороны Вашингтона.
— Но даже в других странах, где россияне ранее получали визу в США, очередь на собеседования — год. И то не всегда эти записи подтверждаются, — пояснил Дмитрий Горин «Известиям».
Благодаря транспортной доступности наибольшей популярностью у россиян, желающих получить американскую визу, пользуется Казахстан. Однако сейчас временных слотов на собеседование практически не осталось. Как убедились «Известия», в посольстве США в Алма-Ате ближайшая дата для собеседования на неиммиграционную туристическую или деловую визу B1/B2 — 10 августа 2022 года. В диппредставительстве в Нур-Султане — 14 декабря 2022 года.
Аналогичные даты предлагают посольства США в Анкаре и Стамбуле — ноябрь следующего года и январь 2023-го.
С 12 мая посольство США в Москве прекратило обработку неиммиграционных виз для недипломатических поездок. Представительство продолжает оказывать лишь экстренные услуги для граждан США, выдает дипломатические и иммиграционные визы в случае истечения срока действия и в случае документально подтвержденных вопросов жизни и смерти.